Повзун С. Важнейшие синдромы: патогенез и патологическая анатомия
Подождите немного. Документ загружается.


щими неполноценность противомикробной защиты при уремии
(Cohen G., 2003).
Другим фактором снижения иммунитета является изменение ба
ланса Тh 1 /Th2-хел перных лимфоцитов за счет уменьшения количе
ства фракции Thl из-за ускорения апоптоза этих клеток (Alvarez-La-
ra М. A. et al., 2004). Ускоренный апоптоз лимфоцитов обусловлен как
самой уремией, так и мембранами, применяемыми для гемодиализа, и
их проницаемостью (Soriano S. et al., 2005).
При уремии ускоряется апоптоз и моноцитов крови, что не коррек
тируется методами гемодиализа. Установлена (Martin-Malo A. et al.,
2000) достоверная обратная связь (г = -0,62; р< 0,005) между интен
сивностью апоптоза моноцитов и клиренсом креатинина, а также от
рицательное влияние на апоптоз этих клеток различных типов гемо-
диализных мембран. Феномен ускоренного апоптоза моноцитов рас
сматривают как один из факторов более высокой подверженности
больных с ХПН инфекциям и злокачественным новообразованиям
(Andrikos Е. et al., 2005). С моноцитами происходят не только коли
чественные, но и качественные изменения, проявляющиеся снижени
ем содержания в крови у-интерферона: в эксперименте in vitro пока
зана существенно более низкая выработка этого вещества моноцитами
в ответ на стимуляцию их эпидермальными стафилококками (Lonne-
mann G. et al., 2003).
Частота клинически значимых инфекций у больных ХПН начина
ет превышать таковую в популяции при снижении скорости клубоч
ковой фильтрации до 5-10 мл/мин (Hoffsten P., Klahr S., 1984). Те или
иные инфекции наблюдаются у 20-30% больных, находящихся на диа
лизе, при этом у 20-30% из них они становятся непосредственной
причиной смерти. Из бактериальных возбудителей наиболее частыми
оказываются грам-положительные бактерии, в особенности стафи
лококки. Сепсис у таких больных наблюдается в 50 раз чаще, чем
в популяции, туберкулез — в 15 раз, причем последний встречается
преимущественно у лиц, прибывших из эндемичных по туберкулезу
регионов (Vanholder R., Van Biesen W., 2002), что косвенно свидетель
ствует о том, что заболевание у такого пациента связано с реактива
цией старых очагов на фоне снижения иммунитета, а не о первичном
заражении.
Содержание в крови у-глобулинов и комплемента обычно остается
нормальным, если только ХПН у пациента не связана с гломеруло-
нефритом и не сопровождается нефротическим синдромом. Есть дан-
200
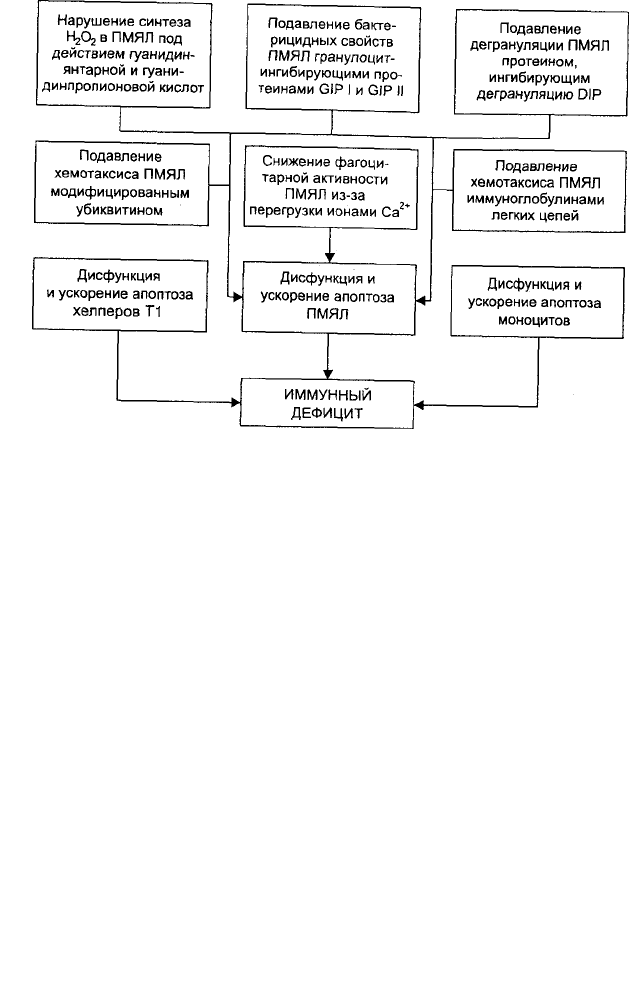
Рис. 4.5. Патогенез иммунного дефицита
при хронической почечной недостаточности
ные об угнетении функции клеток макрофагальной системы, прояв
ляющемся в замедленном выведении из крови различных частиц.
В отношении большей подверженности вирусным или грибковым
инфекциям литературные данные неоднозначны. Вместе с тем есть
основания говорить о большей частоте у уремических больных вирус
ных гепатитов В и С и более частых грибковых инфекциях при пери
тонеальном диализе.
Стоит также напомнить и о том, что иммунный дефицит у уреми
ческих больных может быть связан также как с самим заболеванием,
послужившим причиной ХПН, например, с сахарным диабетом, так и
с иммуносупрессивной терапией, применяемой, скажем, для лечения
гломерулонефритов.
Патологическая анатомия
Отеки. Внеклеточная гипергидратация приводит к увеличению
количества воды в крови и внеклеточных пространствах, что стано
201

вится заметным при скоплении в организме лишних 4-5 л жидкости.
Клинически это проявляется отеком кожи, подкожной жировой ос
новы, мышц, а также скоплением транссудата в серозных полостях.
Основной причиной таких отеков считают снижение выделения Na
+
и нарастание его концентрации в крови.
Изменения в костях. У больных с ХПН в финальной стадии раз
виваются изменения костной ткани, обозначаемые как ренальная ос
теодистрофия. Перестройка прежде всего начинается с костной ткани
стволового скелета, а кости черепа и диафиза бедер вовлекаются в зна
чительную перестройку позже всего. Хотя механизм развития ХПН
у разных больных может быть сходным, характер изменений в костной
ткани отличается существенно, варьируя от снижения интенсивности
обмена веществ в ней до его усиления.
Ренальная остеодистрофия включает в себя фиброзный остеит,
остеомаляцию, остеосклероз и остеопороз. Вторичный гиперпарати-
реоз приводит к развитию кистозного фиброзного остеита, который
при рентгенографическом исследовании определяется как поднадкос-
тичная резорбция кости. Такие изменения чаще всего обнаруживают
ся в средних фалангах пальцев рук, латеральных полюсах ключиц,
проксимальных эпифизах большеберцовых костей. Гистологически
выявляется усиленная резорбция костных балок остеокластами и
разрастания соединительной ткани, что всегда сопровождается повы
шением в крови активности щелочной фосфатазы. Именно фиброзный
остеит в первую очередь сопровождается метастатическим обызвест
влением стенок сосудов, мягких тканей, в том числе околосуставных,
конъюнктивы глаз, кожи.
При резистентности к витамину D и резком нарушении всасывания
Са
2+
в кишечнике развивается остеомаляция. При ней нарушается
обызвествление органического матрикса костных балок. Главным
симптомом остеомаляции являются боли в различных костях и мыш
цах, настолько выраженные, что требуется прием анальгетиков. Остео
маляция может возникать в результате низкого уровня кальция и
фосфора в сыворотке крови или в результате развития неких аномалий
в органическом матриксе (Hoffsten P., Klahr S., 1984).
Остеосклероз — увеличение плотности костной ткани — представ
ляет собой нечастую форму ренальной остеодистрофии. Патогенез
этого состояния, так же как и остеопороза, остается неясным.
На основании гистоморфометрического изучения костной ткани
выделяют несколько типов ренальной остеодистрофии в зависимости
202

от характера изменения обмена веществ (Ferreira А., 2006; Iwasaki Y.
et al., 2006). При умеренном типе метаболизм костной ткани макси
мально приближен к таковому у людей с сохраненной функцией почек.
При фиброзном остеите обмен веществ в костной ткани патологически
ускорен. Это состояние характеризуется высоким темпом обновления
костной ткани. Часть обызвествленной кости теряет свою ламелляр
ную структуру и имеет вид соединительнотканной кости. В этой со
единительной ткани при иммуногистохимическом исследовании
трепанобиоптатов отмечается выраженная экспрессия ИЛ-1а, ИЛ-6,
ФНО-а и TGF-J3, что указывает на роль этих цитокинов в развитии
фиброзного остеита (Duarte М.Е. et al., 2002), реализующуюся под
контролем паратгормона, поскольку паратиреоидэктомия ведет не
только к замедлению перестройки кости, но и к снижению экспрессии
этих цитокинов и ростовых факторов в остеобиоптатах (Santos F.R.
et al., 2003). В кортикальной пластинке также активизируется резорб
ция кости за счет активации остеокластов, здесь формируется костный
мозг, и ткань приобретает вид губчатой кости.
При остеомаляции поверхность кости покрыта лишенным извести
остеоидом. Это состояние связывают с накоплением в организме алю
миния или дефицитом витамина D.
При смешанном типе ренальной остеодистрофии отмечаются из
менения, характерные как для фиброзного остеита, так и для остеома
ляции. Обновление костной ткани настолько ускорено, что кость не
успевает кальцифицироваться.
При замедлении обмена веществ в кости замедляются как резорб
ция, так и неоостеогенез. В то время как масса костной ткани снижа
ется, количество остеоида в ткани оказывается небольшим.
Существование этих различных типов изменений в костях, вероят
но, связано с различной степенью нарушения функции почек, разным
уровнем паратгормона и витамина D в сыворотке крови. Эти состоя
ния осложняются патологическими компрессионными переломами
позвонков, некрозом головки бедренной кости, деформацией костей
скелета, а у детей, помимо прочего, — задержкой роста.
В связи с применением хронического гемодиализа в костях боль
ных с ХПН накапливается алюминий, который, как считается, вносит
свой отрицательный вклад в уремическую остеопатию. Как показано
на основании г истоморфометр и чес ко го изучения 73 костных биопта-
тов с окрашиванием их алюминоном (Jarava С. et al, 2001), у 22 боль
203

ных была выявлена перегрузка ткани алюминием. Она наблюдалась
при всех формах ренальной остеодистрофии, хотя оказалась более
характерной для смешанной ее формы или остеомаляции. У большин
ства пациентов с адинамической формой поражения алюминия в био-
птатах не выявлялось. Для перегрузки алюминием характерным был
замедленный темп образования кости и ее минерализации.
Уремическая кардиомиопатия. Характерным изменением в серд
це у больных с уремией являются гипертрофия левого желудочка,
гипертрофия стенок мелких артерий и артериол и мелкоочаговый
кардиосклероз. Эти изменения нельзя напрямую объяснить проявле
ниями вторичной артериальной гипертензии, наблюдающейся у этих
больных. Помимо гипертрофии кардиомиоцитов на микроскопиче
ском уровне выявляется интерстициальный фиброз, то есть разраста
ние соединительной ткани не только вокруг относительно крупных
артерий (рис. 4.6). В ряде случаев при посмертном исследовании па
томорфологами такая картина трактуется как миокардитический
кардиосклероз в результате ранее перенесенного миокардита, однако
такому заключению обычно противоречат данные постоянного меди
цинского контроля за этими больными, не подтверждающие факта
перенесения миокардита.
Рис. 4.6. Диффузный мелкоочаговый кардиосклероз
и гипертрофия кардиомиоцитов при уремии
204

В эксперименте с удалением крысам 5/6 объема почечной парен
химы уже через месяц наблюдали гипертрофию кардиомиоцитов
с увеличением их диаметра на 14% (р<0,02) и поперечной их площа
ди на 13% (р<0,03) (McMahon А.С. et al., 2006). Это свидетельствует
о первичном характере поражения кардиомиоцитов, не связанном
с гипертензией или с кардиосклерозом.
Описанный мелкоочаговый кардиосклероз сопровождается раз
режением капиллярной сети. Это обстоятельство, а также связанное
с фиброзом увеличение расстояния между кардиомиоцитами и достав
ляющими к ним кислород капиллярами должно проявляться тканевой
гипоксией кардиомиоцитов.
Изменению при уремии подвергаются и правые отделы сердца, что
проявляется расширением полости правых предсердия и желудочка,
как, впрочем, и левого предсердия, по мере увеличения массы миокар
да левого желудочка, то есть в процессе ремоделирования сердца при
ХПН участвуют все его отделы (Кускова Ю.В., 2003).
В кардиомиоцитах помимо снижения содержания гликогена в тя
желых случаях уремии обнаруживаются явления «базофильной деге
нерации», мелкие и более крупные очаги некробиотических изменений
и некроза — миолиза, в том числе с их дистрофическим обызвествле
нием (Terman D.S. et al., 1971). Характерной особенностью этих изме
нений является отсутствие вокруг них воспалительных явлений, что
характерно для апоптоза, а не некроза.
Тщательное исследование позволяет в ряде случаев выявить и
другие важные изменения. Так R.R. Henderson с соавт. (1971) наблю
дали очаги обызвествления в синоатриальном и атриовентрикулярном
узлах и пучке Гиса. Эти изменения при жизни больных проявлялись
прогрессирующими нарушениями ритма, нарастающей сердечной
недостаточностью и иногда внезапной смертью.
Ведущей непосредственной причиной смерти при ХПН являются
изменения со стороны сердечно-сосудистой системы, и значительный
процент таких случаев связан с ишемическим поражением миокарда,
в том числе с инфарктами, однако сравнительное исследование ауто-
псийных данных, проведенное немецкими исследователями (Schwarz U.
et al., 2000) с гистоморфометрией венечных артерий, показало, что
вопреки распространенному мнению о более выраженном их атеро
склеротическом поражении при ХПН размер бляшек не отличался от
такового у умерших от ишемии миокарда и не страдавших ХПН, од
нако степень обызвествления бляшек была более значительной.
205

Следует отметить, что тяжесть поражения миокарда при ХПН за
частую недооценивается патоморфологами, в том числе судебно-ме
дицинскими гистологами, основывающими свои заключения иногда
только на исследовании микропрепаратов, окрашенных гематоксили
ном и эозином. Дополнительная окраска срезов гематоксилином—ос
новным фуксином—пикриновой кислотой (Серов В.А. с соавт., 1977)
с выявлением участков фуксиноррагии в цитоплазме кардиомиоцитов
и исследование в поляризованном свете с обнаружением анизотропии
в цитоплазме поврежденных кардиомиоцитов позволяют точнее оце
нить объем повреждения миокарда и его танатологическое значение.
Следует также учитывать, что указанные изменения всегда развива
ются на фоне гипертрофии кардиомиоцитов, что отрицательно отра
жается на компенсаторно-приспособительных возможностях сердеч
ной мышцы.
Как уже упоминалось, характерным, но не обязательным проявле
нием ХПН в финальной стадии является уремический перикардит.
Клинико-морфологически следует различать острый перикардит,
хронический констриктивный и подострый перикардит, являющийся
как бы переходным вариантом между двумя упомянутыми. М. АН и
A.D. Fayemi (1982) из 56 умерших от уремии, находившихся на хро
ническом гемодиализе, отмечали перикардит у 41 человека: у 3 — гной
ный, у 3 — фибринозно-гнойный, у 27 — фиброзный неконстриктив-
ный, у 8 — фиброзно-констриктивный. У остальных 15 умерших в
полости перикарда был серозный или серозно-геморрагический выпот,
при этом неясно, носил ли он воспалительный характер.
Наиболее часто приходится сталкиваться с подострым перикарди
том, при котором отмечается фибринозный выпот и прорастание
фибрина грануляционной тканью с формированием немногочислен
ных сращений между листками сердечной сорочки (рис. 4.7). Воспа
ление, как правило, носит асептический характер. Инфекционный
перикардит при уремии — редкость, и возможно связан с пункциями
перикарда.
Надо заметить, что в асептической стадии перикардит весьма ус
ловно можно считать таковым, поскольку в случае смерти больного
при микроскопическом исследовании лишь единичные нейтрофиль-
ные лейкоциты обнаруживаются среди масс фибрина. То есть в отли
чие от классического экссудативного воспаления повышенная прони
цаемость микрососудов является не результатом воздействия на их
206
Рис. 4.7. Фибринозный перикардит при уремии.
Воспалительная инфильтрация выражена минимально
стенки биологически активных веществ с целью обеспечения доставки
к месту повреждения фагоцитов, а следствием химического поражения
сосудистой стенки мочевиной в высоких концентрациях и, возможно,
другими уротоксинами. В начальных стадиях ХПН проницаемость
сосудов для жидкости и белка повышается, а в поздних стадиях носит
парадоксальный характер: либо повышается, либо понижается (Гами
дов И.М., 1984). Вероятно, с этим связано то обстоятельство, что не
у всех умерших с явлениями уремии обнаруживаются фибринозные
отложения на серозных и слизистых оболочках. Следует иметь в виду,
что в ряде случаев перикардит в начальных его проявлениях может
остаться нераспознанным на вскрытии и устанавливается лишь при
последующем гистологическом исследовании материала.
Изменения кровеносных сосудов. Эти изменения заключаются
в утолщении и уплотнении стенки аорты, периферических артерий и
вен со снижением содержания в стенках этих сосудов эластических
волокон, в расширении внеклеточного матрикса и диффузном каль
цинозе средней оболочки (Amman К., Tyralla К., 2002), что увеличи
вает ригидность сосудистой стенки и ухудшает растяжимость аорты
во время прохождения пульсовой волны и перистальтику артерий
(рис. 4.8). В средней оболочке аорты наблюдается не только кальциноз,
но и фиброз, одной из причин которого является изменение фенотипа
207

Рис. 4.8. Обызвествление артерий при уремии:
а — пылевидные отложения извести в аорте по типу
мёнкенберговского медиокальциноза,
б — очаговые отложения извести в венечной артерии
у мужчины 23 лет, умершего от уремии
гладкомышечных клеток на фибробластический фенотип и синтез ими
коллагена под влиянием повышенных доз паратгормона, что проде
монстрировано V. Percovic с соавт. (2003) в эксперименте in vitro.
208

Кроме того, при ХПН в артериях более выражены, чем обычно, ате
росклеротические изменения, чему способствует существующая у таких
больных даже при истощении гипертриглицеридемия (Prinsen В.Н.
et al., 2003), наличие которой может быть объяснено повышенным
уровнем ФНО-а, блокирующего фермент липопротеинлипазу и, со
ответственно, усвоение триглицеридов адипоцитами. Атеросклероти
ческое поражение усугубляется и повышением проницаемости эндо
телия (Harper S.J., Bates D.O., 2003).
В мелких артериях наблюдается пролиферация интимы и проли
ферация гладкомышечных клеток медии под стимулирующим влия
нием эндотелина-1 (Amann К. et al., 2001).
Ооызвествление тканей при уремии — явление общеизвестное.
Традиционно оно объясняется гиперкальциемией, связанной с нару
шением функции паращитовидных желез, и минерализацией тканей.
Вместе с тем подмечено, что такой минерализации подвергаются глав
ным образом стенки сосудов, причем крупных артерий. Почему не всех
подряд? Объяснение этому феномену найдено в последние годы.
В стенках подвергшихся обызвествлению крупных сосудов обна
руживаются клетки с фенотипом остеобластов, остеокластов и хонд-
роцитов. Кроме того, липидные везикулы матрикса сосудистой стенки,
имеющие гистохимические и ультраструктурные «опознавательные
знаки» везикул матрикса костной ткани, обусловливают минерализа
цию сосудистой стенки не только при уремии, но также при сахарном
диабете и дизлипидемии. Вещества, обеспечивающие морфогенез кост
ной ткани, в частности, костный морфогенный белок-2 и другие, из
меняют фенотип мезангиобластов аорты, интрамуральных перицитов
(клеток, кальцифицирующих сосуды), гладкомышечных клеток со
судов или миофибробластов створок и заслонок клапанов сердца
в остеогенные клетки. Экспрессия этих паракринных стимуляторов,
запускающих кальцификацию, обнаруживается в стенках пораженных
сосудов, их концентрация в крови при уремии оказывается примерно
в 1,5 раза выше нормы (р < 0,05): 169 ±33 против 117 ±15 пг/мл
(Chen N.X. et al., 2006).
При уремии воспаление, продукты ПОЛ, гиперфосфатемия и элас-
тинолиз обеспечивают поступление стимуляторов остеогенеза в сосу
дистую стенку и перестройку матрикса, а также подавляют сосудистые
механизмы защиты, заключающиеся в ограничении отложения каль
ция и подавлении остеогенной или хондрогенной трансдифференци-
ровки упомянутых клеток сосудистой стенки (Shao J.S. et al., 2006).
209
