Коваленко В.Н. Руководство по кардиологии
Подождите немного. Документ загружается.

СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
980
_______________________________________________________
ГЛАВА 6
Q
МИОКАРДИТ
поддерживающих дозах или не назначая вовсе у
больных с минимально выраженной симптома-
тикой (I или II ФК). Даже на фоне применения
сердечных гликозидов в обычных дозах появля-
ется высокий риск гликозидной интоксикации.
СН при миокардите отличается резистентностью
к сердечным гликозидам и диуретикам. Важно
устранить гипокалиемию и ацидоз. Для лечения
рефрактерной СН оправдано применение пери-
ферических вазодилататоров. Нитраты уменьша-
ют венозный возврат крови к сердцу, давление
в сосудах малого круга кровообращения, то есть
преднагрузку ЛЖ, что проявляется клиническим
улучшением. Применение сердечных гликози-
дов на фоне периферических вазодилататоров
позволяет достичь адекватной дигитализации
при отсутствии токсического эффекта.
У пациентов с молниеносным течением мио-
кардита могут использоваться механические
устройства для поддержки функции желудочков,
в случаях когда их состояние не улучшается, не-
смотря на максимальную инотропную терапию.
У больных, размер и систолическая функция
ЛЖ которых полностью нормализовались, тера-
пия ингибиторами АПФ и блокаторами β-адрено-
рецепторов в принципе может быть прекращена
при условии тщательного контроля функции ЛЖ
и хронических заболеваний. У многих выздоро-
вевших пациентов субъективные ограничения
в функциональной способности и объективные
ограничения при нагрузочных пробах могут при-
сутствовать, возможно, благодаря более медленно-
му восстановлению диастолической функции ЛЖ.
Непрямые антикоагулянты назначают боль-
ным с тромбоэмболическими осложнениями
(в том числе и в анамнезе), наличием тромбов
в полостях сердца и фибрилляцией предсердий
на фоне кардиомегалии.
При нарушениях ритма назначают антиарит-
мические препараты или вживляют кардиовертер-
дефибрилятор, электрокардиостимулятор.
Трансплантацию сердца следует планировать
только на поздних стадиях заболевания, особен-
но с учетом высокой ранней послеоперационной
смертности в результате отторжения трасплантата
у пациентов, чья иммунная система исходно акти-
вирована против антигенов миоцитов. При оттор-
жении трансплантата, которое чаще развивается
в первые 3 мес после трансплантации сердца, на-
значают ГКС в высоких дозах (пульс-терапия).
В терминальной стадии используют двухка-
мерную стимуляцию, аппаратное поддержание
сокращения желудочков.
Прогноз
Прогноз значительно зависит от степени вос-
становления функции ЛЖ. В большинстве слу-
чаев (до 90%) миокардит протекает бессимптом-
но и в течение 1–2 мес заканчивается полным
выздоровлением, исчезают все субъективные
симптомы, нормализуется ЭКГ в покое и при
проведении ВЭМ. У 30–50% пациентов с дис-
функцией ЛЖ происходит существенное ее улуч-
шение в течение первого года после заболевания.
У многих больных сохраняются остаточные из-
менения ЭКГ, свидетельствующие о развитии
очагового миокардитического кардиосклероза
(миокардиофиброза), что подтверждается при
эхоКГ-исследовании. При наличии клиниче-
ских проявлений дисфункции ЛЖ прогноз хуже:
у 10–33% больных развивается ДКМП.
Гигантоклеточный миокардит и некротизи-
рующий эозинофильный миокардит могут иметь
молниеносное развитие симптомов с неблаго-
приятным прогнозом. При гигантоклеточном
миокардите продолжительность жизни без транс-
плантации сердца в среднем составляет 5,5 мес,
через 4 года остаются живыми только 11%, при
лимфоцитарном миокардите — 44% больных.
Неблагоприятными факторами, отягощаю-
щими прогноз миокардита, считают повышение
давления в левом предсердии, низкий сердечный
индекс, диастолическую дисфункцию ПЖ, раз-
витие застойной СН, тромбоэмболии, наруше-
ния проводимости и аритмии высоких градаций.
ЛИТЕРАТУРА
1. Амосова Е.Н. (2000) Миокардиты. Междунар. мед. журн., 1: 22–25.
2. Дерюгин М.В., Бойцов С.А. (2005) Хронические миокардиты. ЭЛБИ-СПб,
Санкт-Петербург, 288 с.
3. Коваленко В.Н., Несукай Е.Г. (2001) Некоронарогенные болезни сердца.
Практ. руководство. Морион, Киев, 480 с.
4. Коваленко В.Н., Рябенко Д.В. (2005) Современные представления о мио-
кардите. Мистецтво лікування, 9: 12–20.
5. Наказ № 436 Міністерства охорони здоров’я України від 03.07.2006 р. «Про
затвердження протоколів надання медичної допомоги за спеціальністю
«Кардіологія» (2006) Укр. кардіол. журн.,6: 89–115.
6. Badorff C., Knowlton K.U. (2004) Dystrophin disruption in enterovirus-induced
myocarditis and dilated cardiomyopathy: from bench to bedside. Med.
Microbiol. Immunol, 193: 121–126.
7. Bowles N.E., Ni J., Kearney D.L. et al. (2003) Detection of viruses in myocardial
tissues by polymerase chain reaction: evidence of adenovirus as a common
cause of myocarditis in children and adults. J. Amer. Coll. Cardiol., 42: 466–
472.
8. Chimenti C., Russo A., Pieroni M. et al. (2004) Intramyocyte detection of
Epstein-Barr virus genome by laser capture microdissection in patients with
infl ammatory cardiomyopathy. Circulation, 110: 3534–3539.
9. Cooper L.T., Baughman K.L., Feldman A.M. et al. (2007) The role of
endomyocardial biopsy in the management of cardiovascular disease. Eur.
Heart J., 28: 3076–3093.
10. Daliento L., Calabrese F., Tona F. et al. (2003) Successful treatment of
enterovirus-induced myocarditis with interferon-α. J. Heart Lung Transplant.,
22: 214–217.
11. D’Ambrosio A., Patti G., Manzoli A. et al. (2001) The fate of acute myocarditis
between spontaneous improvement and evolution to dilated cardiomyopathy:
a review. Heart, 85: 499–504.

СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
ГЛАВА 6
Q
МИОКАРДИТ
_______________________________________________________
981
12. Deonarain R., Cerullo D., Fuse K. et al. (2004) Protective role for Interferon-β
in coxsackievirus B3 infection. Circulation, 110: 3540–3543.
13. Dill T., Ekinci O., Hansel J. et al. (2005) Delayed contrast-enhanced magnetic
resonance imaging for the detection of autoimmune myocarditis and long-term
follow-up. J. Cardiovasc. Magn. Reson., 7: 521–523.
14. Elliott P., Andersson B., Arbustini E. et al. (2008) Classifi cation of the
cardiomyopathies: a position statement from the european society of
cardiology working group on myocardial and pericardial diseases. Eur. Heart
J., 29: 270–276.
15. Eckart R.E., Scoville S.L., Campbell C.L. et al. (2004) Sudden death in young
adults: a 25-year review of autopsies in military recruits. Ann. Intern. Med.,
141: 829–834.
16. Galderisi M., Mondillo S. (2007) Echocardiography in clinical practice .One
Way S.r.l., 120 p.
17. Huber S.A., Sartini D. (2005) Roles of tumor necrosis factor alpha and the
p55 receptor in CD1d induction and Coxsackievirus B3-induced myocarditis.
J. Virol., 79: 2659–2665.
18. Hufnagal G., Pankuweit S., Schonian U. et al. (2000) The European Study of
Epidemiology and Treatment of Cardiac Infl ammatory Diseases (ESETCID).
First epidemiology results. Herz, 25: 279–285.
19. Kittleson M.M., Minhas K.M., Irizarry R.A. et al.(2005) Gene expression in
giant cell myocarditis: altered expression of immune response genes. Intl. J.
Cardiol., 102: 333–340.
20. Kühl U., Pauschinger M., Schwimmbeck P.L. et al. (2003) Interferon-β
treatment eliminates cardiotropic viruses and improves left ventricular function
in patients with myocardial persistence of viral genomes and left ventricular
dysfunction. Circulation, 107: 2793–2798.
21. Liu P.P., Mason J.W. (2001) Advances in understanding of myocarditis.
Circulation, 104: 1076.
22. Liu P.P., Yan A.T. (2005) Cardiovascular magnetic resonance for the diagnosis
of acute myocarditis. J. Amer. Coll. Cardiol., 45: 1823–1825.
23. Maisch B., Portig I., Ristic A.et al. (2000) Defi nition of infl ammatory
cardiomyopathy (myocarditis): on the way to Consensus. A status report. Herz,
25(issue 3): 200–209.
24. Mason J.W., O’Connell J.B., Herskowitz A. et al. (1995) A clinical trial of
immunosuppressive therapy for myocarditis. The Myocarditis Treatment Trial
Investigators. N. Engl. J. Med., 333: 269–313.
25. McCarthy R.E., Bochmer J.P., Hruban R.H. et al.(2000) Long-term outcome
of fulminant myocarditis as compared with acute (nonfulminant) myocarditis.
New Engl. J. Med., 342: 690–694.
26. McNamara D.M., Rosenblum W.D., Janosko K.M. et al. (1997) Intravenous
immune globulin in the therapy of myocarditis and acute cardiomyopathy.
Circulation, 95: 2476–2478.
27. Pauschinger M., Chandrasekharan K., Noutsias M. et al. (2004) Viral heart
disease: molecular diagnosis, clinical prognosis, and treatment strategies.
Med. Microbiol. Immunol., 193: 65–69.
28. Smith S.C., Ladenson J.H., Mason J.W. et al. (1997) Elevations of cardiac
troponin I associated with myocarditis. Circulation, 95: 163–168.
29. Topol E.J. (Ed.) (2007) Textbook of cardiovascular medicine. 3
th
ed. Lippincott
Williams&Wilkins, 1628 p.
30. Wojnicz R., Nowalany-Kozielska E., Wojciechowska C. et al. (2001)
Randomized, placebo-controlled study for immunosuppressive treatment of
infl ammatory dilated cardiomyopathy: two-year follow-up results. Circulation,
104: 39–45.

СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
982
______________________________________________________
ГЛАВА 7
Q
ЭНДОКАРДИТ
Определение
Инфекционный эндокардит — воспалитель-
ное заболевание эндокарда инфекционной этио-
логии, обусловленное инвазией возбудителя
с его локализацией на клапанных структурах, эн-
докарде, эндотелии в зоне прилегающих к сердцу
магистральных сосудов, сопровождающееся, как
правило, бактериемией и поражением различ-
ных органов и систем организма.
Эпидемиология
В течение последних 10–15 лет отмечают по-
вышение заболеваемости инфекционным эндо-
кардитом, что может быть обусловлено несколь-
кими факторами:
• распространением операций, выполняемых
на сердце, — появлением инфекционного эндо-
кардита протезированного клапана;
• повышенной предрасположенностью к за-
болеванию при наличии:
• врожденных пороков сердца (10–20%),
в том числе двустворчатого аортального клапана
(12–30%);
• пролапса митрального клапана (22–29%);
• приобретенных пороков сердца (37–76%);
• обструктивной ГКМП;
• операции на сердце без замены клапанов;
• постинъекционными абсцессами после
введения различных лекарственных средств;
• появлением новой формы – нозокомиаль-
ного инфекционного эндокардита, связанного
с широким использованием инвазивной инстру-
ментальной техники (катетеров, искусственных
водителей ритма сердца, шунтов), вводимой
в сердце и сосуды;
• появлением инфекционного эндокардита
наркоманов.
Инфекционный эндокардит может возникать
в любом возрасте. До эпохи антибиотиков им
наиболее часто заболевали лица среднего возрас-
та, в последние десятилетия пик заболеваемости
сместился к 50-летнему возрасту, в 5 раз увели-
чилось количество заболевших в возрасте стар-
ше 60 лет. Мужчины болеют в 2 раза чаще, чем
женщины. У большинства пациентов инфекция
поражает аортальный (28–45%), митральный
(5–36%) или оба клапана (до 35%). Эндокардит
правых отделов сердца выявляют реже (пораже-
ния трехстворчатого клапана — <6%, клапана
ЛА — <1%). У мужчин преобладает поражение
аортального клапана, у женщин – митрального.
Этиология
Инфекционный эндокардит — полиэтиоло-
гическое заболе вание, потенциальными возбу-
дителями которого могут быть до 128 разновид-
ностей микроорганизмов. Основными среди них
являются стафилококки (30–50%) и стрептокок-
ки (20–30%).
Повышение этиологической роли стафило-
кокка (чаще золотистого) за последние 10–15 лет
объясняется широким внедрением в клиниче-
скую практику анти биотиков, а также распро-
странением оперативных вмешательств на серд-
це, имплантации эндокардиального электрода
искусственного водителя ритма сердца, инвазив-
ных инструментальных исследований.
Из всех штаммов стрептококка наиболее ча-
сто высевают зеленящий стрептококк, удается
выделить и другие штаммы стрептококка, пре-
жде всего энтерококк, вызывающий инфекци-
онный эндокардит в 10–15% случаев.
Пневмококковый эндокардит особенно часто
диагностируют у больных после кардиохирур-
гического вмешательства с имплантацией ис-
ГЛАВА 7
Q
ЭНДОКАРДИТ
В.Н. Коваленко, Е.Г. Несукай
Определение
Эпидемиология
Этиология
Патогенез
Патологическая анатомия
Классификация
Клиническая картина
Диагностика
Лечение
Прогноз
Профилактика
ЛИТЕРАТУРА .................................................993

СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
ГЛАВА 7
Q
ЭНДОКАРДИТ
_______________________________________________________
983
кусственных материалов, а также у пациентов,
перенесших в послеоперационный период пнев-
монию.
Наблюдения последних лет свидетельствуют
об увеличении в этиологии инфекционного эн-
докардита удельного веса грамотрицательной ми-
крофлоры: эшерихий, протея, сальмонелл, синег-
нойной палочки, клебсиелл, которые явля ются
причиной заболевания в 3–8% случаев. У инъек-
ционных наркоманов грамотрицательные бакте-
рии вызывают заболевание в 5–64% случаев.
Возросла частота эндокардита, вызванно-
го грибами (1,5–6%); среди возбудителей этой
группы преобладают дрожжеподобные грибы.
Эндокардит грибковой этиологии в 5–14% слу-
чаев возникает у инъекционных наркоманов.
В последнее время в появлении инфекцион-
ного эндокардита также повысилась этиологи-
ческая роль анаэробной флоры. Предполагают,
что повреждающая роль анаэробных бактерий
реализуется только в ассоциации с аэробными
микроорганизмами.
У больных с искусственным клапаном серд-
ца в 50% случаев раннего эндокардита высевает-
ся золотистый и эпидермальный стафилококк,
в 21% — грамотрицательная микрофлора, в
10% — грибы. Возбудителями позднего эндокар-
дита протезированного клапана являются эпи-
дермальный стафилококк и стрептококк (50%),
золотистый стафилококк (16%), энтерококк
(11%), грамотрицательная микрофлора (12%).
В настоящее время соотношение между пер-
вичным и вторичным эндокардитом, связанным
с пороками клапана ревматической или иной
этиологии, существенно изменилось в пользу
первого, частота которого составляет более 30%.
Патогенез
Вопросы патогенеза инфекционного эндо-
кардита сложны и окончательно не выяснены.
Инфекционный эндокардит возникает в ре-
зультате взаимодействия трех составляющих:
состояния организма (предрасполагающих фак-
торов), бактерие мии с учетом тропности и сте-
пени вирулентности бактерий. В большинстве
случаев в анамнезе имеются указания на порок
сердца, атеросклероз, операции на сердце, кото-
рые предрасполагают к избирательной адгезии
микроорганизмов на эндокарде. Возникновение
эндокардита, по-видимому, следует рассматри-
вать как результат микроструктурных изменений
в эндокарде под влиянием функциональных ге-
модинамических перегрузок. Эти причины в той
или иной степени объясняют появление наибо-
лее уязвимого места в эндокарде как местного
фактора, обусловливающего данную локализа-
цию инвазии возбудителя.
Возможность развития инфекционного эндо-
кардита зависит от выраженности, частоты и ви-
довой специфичности бактериемии. Под влия-
нием этиологических факторов на фоне изме-
ненной реактивности всего организма и клапан-
ного аппарата сердца возникает интерстициаль-
ный вальвулит, небактериальный эндокардит,
затем происходит присоединение инфекции,
развивается инфекционное поражение клапанов
с бактериемией и тромбоэмболическими ослож-
нениями.
Факторы, облегчающие адгезию микроорга-
низмов на эндотелиальной поверхности и спо-
собствующие развитию инфекционного эндо-
кардита, подразделяются на местные и общие.
К общим могут быть отнесены выраженные из-
менения иммунного статуса организма, отмечае-
мые у наркоманов, больных алкоголизмом, лиц
пожилого возраста, пациентов с определенными
нарушениями в HLA-системе гистосовместимо-
сти, а также у пациентов, получающих иммуно-
супрессивную терапию.
В патогенезе инфекционного эндокардита
выделяют три фазы: инфекционно-токсическую,
иммуновоспалительную (иммунной генерализа-
ции процесса) и дистрофическую (с дистрофиче-
скими изменениями внутренних органов). От со-
отношения инфекционно-токсических и имму-
новоспалительных проявлений отчасти зависит
многообразие клинической картины болезни.
Патологическая анатомия
При эндокардите сердце увеличено, обычно
преобладает гипертрофия левых отделов в связи
с недостаточностью клапана аорты. В миокарде,
помимо признаков воспаления, выявляют такие
выраженные дистрофические и некробиоти-
ческие поражения, как базофильная и парен-
химатозная дистрофия, а также микромаляции
и микроучастки глыбчатого распада мышечных
волокон.
Для всех вариантов инфекционного эндо-
кардита характерны вегетации, которые наибо-
лее часто располагаются на створках клапанов
и реже — на эндокарде желудочков или левого
предсердия, а также на легочной или других ар-
териях. Вегетации обычно выявляются через
2 нед от начала инфекционного эндокардита
при острой (стафилококковой) форме и через
6–8 нед при подострой. Свежие вегетации состо-
ят из тонких нитей фибрина, среди которых вы-

СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
984
______________________________________________________
ГЛАВА 7
Q
ЭНДОКАРДИТ
являют эритроциты и в меньшем количестве —
смешанно-клеточные лейкоциты, тромбоциты
и почти всегда колонии бактерий. Свежие веге-
тации имеют розовый, красный, желтый или зе-
леный цвет, но постепенно приобретают серую
окраску. При подостром процессе наряду со све-
жими имеются вегетации, покрытые фиброзной
капсулой, частично или полностью обызвест-
вленные, нередко на ножке, часто организо-
ванные вегетации полностью кальцинированы.
В неактивной стадии инфекционного эндокар-
дита вегетации представлены фиброзными бу-
горками или полностью кальцинированы.
При первичном эндокардите створки клапа-
нов чаще тонкие, свободный край клапана часто
утолщен, что вызвано гемодинамическими нару-
шениями или воспалительной инфильтрацией,
вегетации располагаются по свободному краю
клапанов, внутренней оболочке восходящей ча-
сти аорты. При вторичном эндокардите, когда
инфекционный процесс поражает уже изменен-
ный клапан, свежие вегетации располагаются
на фиброзно-измененных или кальцинирован-
ных створках, возможен отрыв хорд.
Классификация
В Украине используют классификацию ин-
фекционного эндокардита, принятую на VI Кон-
грессе кардиологов Украины (Киев, 2000):
I. Активность процесса: активный, неактив-
ный
II. Эндокардит нативных клапанов:
1) первичный
2) вторичный (приобретенный порок сердца,
врожденный порок сердца, травма, инородные
тела)
III. Эндокардит протезированного клапана
Локализация:
• аортальный клапан
• митральный клапан
• трехстворчатый клапан
• клапан ЛА
• эндокард предсердий или желудочков
IV. Возбудитель (грамположительные, грам-
отрицательные микроорганизмы, L-формы бакте-
рий, риккетсии, грибы)
V. Осложнения
VI. СН (0–III стадия, I–IV ФК)
По течению различают острый, подострый
или затяжной, хронический рецидивирующий и
латентный инфекционный эндокардит. К остро-
му относят случаи заболевания длительностью
до 2 мес, более 2 мес — к подострому.
Клиническая картина
При инфекционном эндокардите она отлича-
ется значительным многообразием симптомов,
что определяет и трудности диагностики. Болезнь
может манифестировать внезапно или длительно
протекать латентно, иметь быстрое или затяжное
течение. Клиническая картина заболевания, его
течение и исход в каждом конкретном случае за-
висят как от состояния защитных сил организма,
его неспецифической резистентности и реактив-
ности, так и от вида инфекционного возбудителя.
Важное значение имеет постоянная бактериемия,
местная реакция вокруг клапана, эмболизация со-
судов различных органов, циркуляция иммунных
комплексов с накоплением их в тканях.
Клинические проявления обычно развива-
ются в течение 2 нед с момента инфицирования.
Одним из основных симптомов является лихо-
радка, которая может сопровождаться ознобом,
потливостью. Температурная реакция варьирует
от высокой упорной лихорадки на протяжении
нескольких месяцев до незначительного повы-
шения температуры тела в течение нескольких
дней с последующей стойкой ее нормализацией.
Наблюдения за состоянием больных позво-
лили выявить основные типы температурных
кривых: а) транзиторный тип характеризуется
недлительным субфебрилитетом, отмечается
у 40% больных в начальной стадии эндокарди-
та; б) интермиттирующая 1–2-недельная или
1–2-дневная высокая лихорадка чередуется
с 1–2-недельными периодами нормальной или
субфебрильной температуры тела; в) стойкое
умеренное повышение температуры тела сохра-
няется длительно на фоне лечения и после лик-
видации очагов хронической инфекции; г) при
гектической температуре суточный градиент
достигает 2–3 °C, отмечают озноб и повышен-
ную потливость; д) при гипотермическом типе
температура тела ниже нормы, что характерно у
резко ослабленных больных с клинически выра-
женной недостаточностью крово обращения. По-
тоотделение не облегчает состояния пациента,
бывает профузным, иногда испариной покрыва-
ются только отдельные участки тела (голова, лоб,
верх няя половина туловища).
Клинические симптомы обусловлены появле-
нием вегетаций, части которых могут отрываться
и эмболизировать сосуды сердца, мозга, почек,
селезенки, печени, конечностей и легких (при
правостороннем эндо кардите).
СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
ГЛАВА 7
Q
ЭНДОКАРДИТ
_______________________________________________________
985
При развернутой клинической картине отме-
чают следующие симп томы:
• выраженная интоксикация: слабость, анорек-
сия, головная боль, миалгия, артралгия, похудение;
• изменения кожных покровов: бледно-
желтоватый цвет кожи, петехии (мелкоточечные
геморрагии) на коже и слизистых оболочках,
конъюнктиве нижнего века (симп том Луки-
на — Либмана), пятна Джейнуэя — красно-
фиолетовые до 5 мм в диаметре пятна на ладонях,
ступнях, туловище, узелки Ослера — болезнен-
ные, величиной с горошину, узелки красновато-
го цвета на ладонных поверхностях пальцев рук и
подошвенных поверхностях пальцев ног;
• изменения концевых фаланг («барабанные
палочки») и ногтей («часовые стекла»);
• моно- или олигоартрит крупных суставов
верхних и нижних конечностей;
• поражение аортального/митрального кла-
пана, поражение миокарда;
• тромбоэмболии селезеночной, почечных,
легочной, коронарных, мозговых артерий с раз-
витием инфарктов соответствующих органов,
сосудов сетчатки глаза;
• признаки сухого или экссудативного пери-
кардита;
• поражение сосудов: микотические аневриз-
мы артерий, генерализованный васкулит;
• гепатомегалия, спленомегалия, увеличение
лимфатических узлов;
• поражение почек (диффузный гломеруло-
нефрит, очаговый нефрит, инфаркт почки);
• поражение ЦНС: менингоэнцефалит, суб-
арахноидальное кровоизлияние, тромбоэмболия
сосудов мозга, психоз;
• прогрессирующая СН.
Изменения показателей лабораторных ис-
следований при инфекционном эндокардите не
являются специфичными, в периферической
крови часто выявляют признаки гипо- и нормох-
ромной анемии. В большинстве случаев отмеча-
ется лейкопения, но при осложнениях возможен
лейкоцитоз со сдвигом лейкоцитарной формулы
влево, моноцитоз, тромбоцитопения. Типич-
ным является повышение СОЭ, однако следует
учитывать, что вследствие диспротеинемии этот
симптом не может своевременно отражать поло-
жительную динамику при лечении заболевания.
Для оценки тяжести инфекционного эндо-
кардита предложено выделять три степени ак-
тивности процесса. Основные критерии актив-
ности процесса, дополненные данными исследо-
вания гуморального иммунитета, представлены в
табл. 7.1 (Демин А.А., 2006).
Таблица 7.1
Клинические и лабораторные критерии
активности инфекционного эндокардита
Критерий Степень активности
I (мини-
мальная)
II (уме-
ренная)
III (высо-
кая)
Лихорадка, °С Субфе-
брильная
или отсут-
ствует
37–38 39–40
Озноб — ± +
Потливость — ± +
Общее состояние Относи-
тельно
удовлетво-
рительное
Средней
тяжести
Тяжелое
Увеличение
селезенки
±++
Гломерулонефрит Очаговый Очаговый Диффуз-
ный
Формирование
порока сердца
Медлен-
ное
Медлен-
ное
Быстрое
Динамика
сердечных шумов
Медлен-
ная
Медлен-
ная
Быстрая
Динамика тонов
сердца
Медлен-
ная
Медлен-
ная
Быстрая
Миокардит Очаговый Очаговый Диффуз-
ный
СН ± ± ±
Геморрагия — ± +
Тромбоэмболия — ± +
Артралгия, артрит — ± ±
Гемокультура ± + +
СОЭ, мм/ч 20 20–40 >40
Анемия ± + +
Лейкопения ± + Иногда
лейкоци-
тоз
Тромбоцитопения ± + +
Формоловая
проба
—± +
СРБ — ± +
Фибриноген, г/л 4–5 5–6 6–10
Гемоглобин, г/л 120–150 120–110 110–90
γ-глобулинемия,
%
10–15 20–25 25–45
Примечание. «—» — отсутствие симптома; «±» —
необязательное наличие или меньшая выраженность
симптома; «+» — частое наличие или значительная
выраженность симптома.
Диагностика
В типичных случаях диагностика инфекци-
онного эндокардита несложна и основывается
на следующих признаках: лихорадка с ознобом,
наличие клапанных дефектов с появлением шу-
мов сердца при первичном эндокардите или
выраженном изменении их характера при вто-
ричном, тромбоэмболические осложнения и по-
ложительные результаты бактериологического
исследования. Значительные трудности пред-
СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
986
______________________________________________________
ГЛАВА 7
Q
ЭНДОКАРДИТ
ставляет диагностика заболевания при стертом
или атипичном течении.
На ЭКГ отмечают признаки гипертрофии ЛЖ
(при поражении аортального или митрального
клапана) или ПЖ (при поражении трехстворча-
того клапана или клапана ЛА), возможны нару-
шения AV-про водимости, предсердная и желу-
дочковая экстрасистолия. В 25% слу чаев выяв-
ляют фибрилляция или трепетание предсердий.
ЭхоКГ позволяет верифицировать диагноз, ее
рекомендуется проводить всем больным с подо-
зрением на инфекционный эндокардит. ЭхоКГ
позволяет в значительной степени объек тивно
оценить состояние клапанного аппа рата серд-
ца, своевременно выявить вегетации клапанов,
кальциноз, разрыв хорд или створки клапана, аб-
сцесс клапанного кольца и миокардиальный аб-
сцесс, уточнить характер порока сердца, а также
определять необходимость срочного оператив-
ного лечения больных с остро развившейся недо-
статочностью аортального/митрального клапана
и выраженной перегрузкой объемом ЛЖ.
При одномерном исследовании признаками
вегетаций являются неравномерное утолщение
одной из створок клапана, густо расположенные
«лохматые» мелковолновые ее осцилляции, под-
вижность створки при этом не ограничивается.
Метод позволяет визуализировать вегетации раз-
мером 2–3 мм.
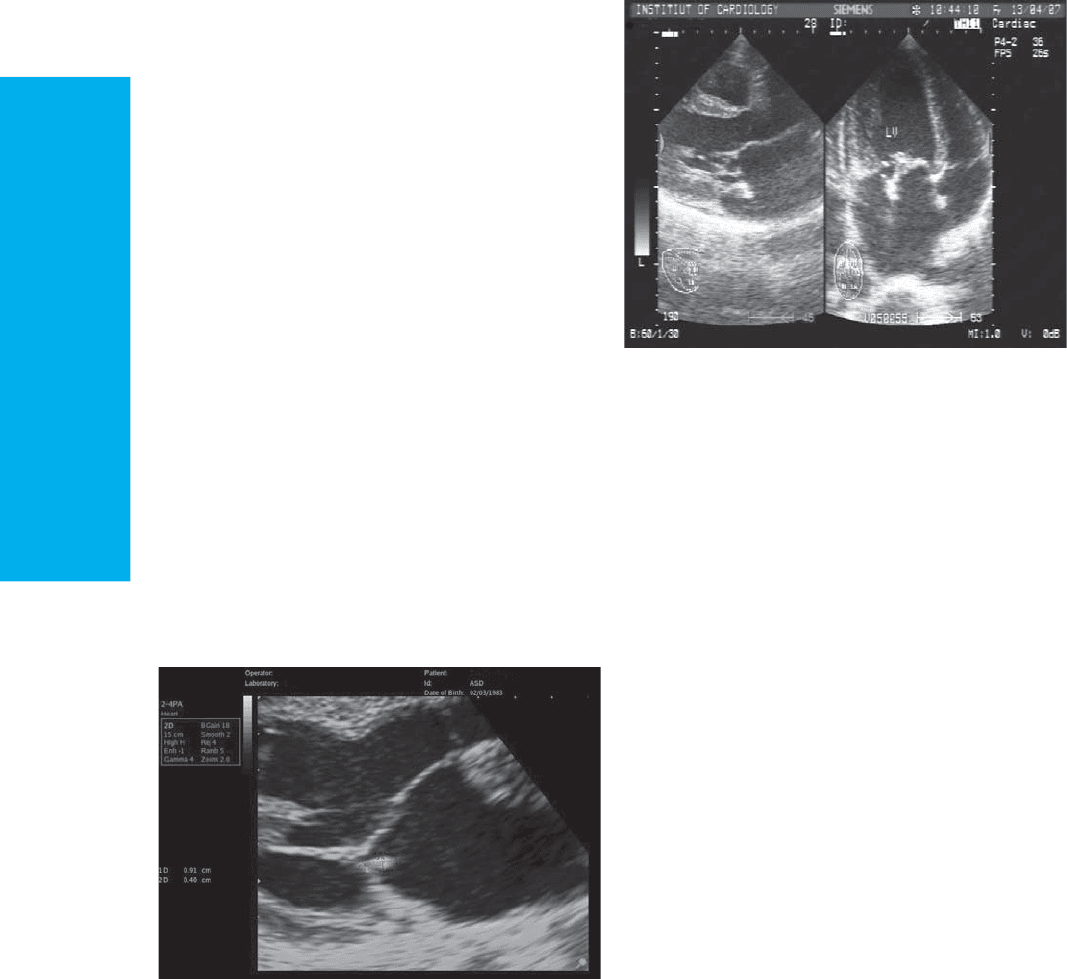
Рис. 7.1. Инфекционный эндокардит, вегетация
на задней створке митрального клапана.
В-режим, пара стернальная позиция, длин-
ная ось, ZOOM
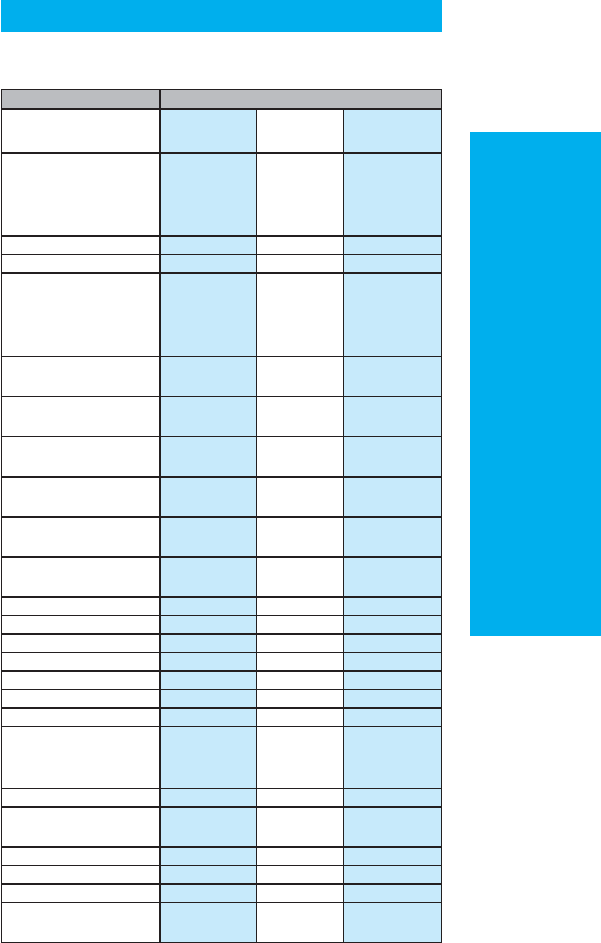
При двухмерной эхоКГ вегетации определя-
ются в виде дополнительных эхотеней, тесно свя-
занных со створками и выходящих за обычные
границы их локации (рис. 7.1). Частота выявления
вегетаций при эхоКГ-исследовании зависит от их
величины, структуры, локализации, предшеству-
ющего клапанного порока, продолжительности
заболевания. Выделяют три типа вегетаций: «си-
дячие», «на ножке», «нитчатые» (рис. 7.2).
Рис. 7.2. Инфекционный эндокардит, вегетации на
створках митрального клапана. В-режим,
апикальная четырехкамерная позиция
С помощью допплеровской эхоКГ определяют
регургитацию на аортальном и митральном кла-
панах в соответствующую фазу сердечного цикла.
Тяжесть течения инфекционного эндокар-
дита на основании данных эхоКГ-исследования
оценивается степенью разрушения створок, их
деформацией, образованием абсцессов створок,
основания аорты, разрывом хорд митрального
клапана, отрывом створки аортального клапана,
результатом чего является нарастание недоста-
точности клапанов с перегрузкой соответствую-
щих камер сердца. Сохранение или исчезновение
вегетаций на фоне лечения (по данным эхоКГ)
не является надежным критерием эффективно-
сти или неэффективности антибиотикотерапии.
Чреспищеводная эхоКГ имеет значительно
более высокую чувствительность в отношении
выявления внутрисердечных вегетаций (95–
100% по сравнению с 60–65% при проведении
трансторакальной эхоКГ).
Разработаны критерии, позволяющие более
уверенно заподозрить диагноз инфекционного
эндокардита и являющиеся показанием для не-
отложного эхоКГ-скрининга и возможной го-
спитализации (Horskotte D. et al., 2004):
• новое повреждение клапана (шум регурги-
тации);
• эмболия неизвестной этиологии (инсульт,
инфаркт почки);
• сепсис неизвестной этиологии;
• гематурия, гломерулонефрит и подозрение
на инфаркт почки;
• лихорадка в сочетании с другими фактора-
ми риска инфекционного эндокардита.

СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
ГЛАВА 7
Q
ЭНДОКАРДИТ
_______________________________________________________
987
Катетеризация сердца позволяет выявить по-
роки клапанов, врожденные дефекты, поражение
коронарных артерий, оценить степень выражен-
ности гемодинамических нарушений у больных
с инфекцион ным эндокардитом. В ряде случаев
проводить это исследование опасно, учитывая
риск отрыва вегетаций от клапана с последую-
щей эмболией сосудов большого круга крово-
обращения.
Посевы крови на стерильность — один из
основных методов верификации диагноза ин-
фекционного эндокардита. Успешное выделение
микроорганизмов из крови зависит от соблюдения
ряда условий. В 50–55% случаев в острый период
и в 80–85% случаев в подострый период посевы
крови оказываются стерильными. Причинами, за-
трудняющими идентификацию возбудителя забо-
левания, являются предшествующая забору крови
антибактериальная терапия, несовершенное бак-
териологическое оборудование для проведения по-
сева, наличие в крови бактерий, требующих при-
менения специальных сред (анаэробы, сателлиты
и штаммы стрептококка с измененными свойства-
ми (тиол- или витамин В
6
-зависимые), L-формы
бактерий, бруцеллы). Для выделения вирусов,
риккетсий, хламидий, грибов требуются специаль-
ные методы. Если посевы крови взяты у пациента,
не получавшего лечение в предшествующие 2 нед,
то возбудителя устанавливают в 96% случаев. Боль-
шие перспективы в идентификации возбудителя
инфекционного эндокардита открывает бакте-
риологическое исследование артериальной крови,
частота выявления положительной гемокультуры
при этом возрастает.
Согласно модифицированным диагностиче-
ским критериям инфекционного эндокардита
диагноз может быть достоверным, вероятным
и исключающим при наличии альтернативного
(Bayer A.S., 1996).
Диагноз «достоверный инфекционный эн-
докардит» устанавливают, если представлены
2 основных критерия или 1 основной и 3 допол-
нительных или 5 дополнительных критериев.
Диагноз «возможный инфекционный эндо-
кардит» устанавливают, если представлены 1 основ-
ной и 1 дополнительный или 3 дополнительных
критерия.
Диагноз «инфекционный эндокардит» ис-
ключается:
• при наличии альтернативного диагноза,
объясняющего имеющиеся признаки;
• при исчезновении проявлений, напоминаю-
щих эндокардит, после 4 дней антибактериаль-
ной терапии;
• при отсутствии морфологических призна-
ков инфекционного эндокардита во время опе-
рации или при аутопсии.
Основные диагностические критерии инфекци-
онного эндокардита
1. Положительная гемокультура, характерная
для инфекционного эндокардита:
- типичный микроорганизм, выделенный из
двух флаконов: Streptococcus viridans, Streptococcus
bovis, бактерии группы НАСЕК; внебольничный
штамм Staphylococcus aureus или энтерококки при
отсутствии первичного очага; однократная по-
ложительная культура крови Coxiella burneti или
IgG более 1:800;
- повторные положительные гемокультуры,
характерные для инфекционного эндокардита:
• в образцах крови, взятых с интервалом >12 ч;
• во всех 3, в 3 из 4 или в большинстве дру-
гого количества образцов крови, взятых на посев
с интервалом между первым и последним забо-
ром крови более 1 ч.
2. ЭхоКГ-признаки инфекционного эндокар-
дита:
- наличие характерных эхоКГ-признаков:
• вегетации на клапанах сердца или других
структурах;
• внутрикардиальные абсцессы;
• дисфункция протезированных клапанов;
- появление новых признаков регургитации
крови через клапаны.
Вспомогательные диагностические критерии
инфекционного эндокардита
1. Предшествующие заболевания сердца или
внутривенное употребление наркотиков.
2. Лихорадка >38 °С.
3. Сосудистые осложнения: артериальная эм-
болия, инфаркт легкого, микотические аневриз-
мы, внутричерепное кровоизлияние, симптом
Лукина, пятна Жаневье.
4. Иммунные нарушения: гломерулонефрит,
узелки Ослера, пятна Рота, ревматоидный фактор.
5. Положительная гемокультура, не соответ-
ствующая основным критериям, или серологи-
ческие признаки активной инфекции, вызван-
ной потенциальным возбудителем инфекцион-
ного эндокардита.
Диагностические критерии инфекционного
эндокардита у пациентов пожилого и старческо-
го возраста включают:
• лихорадку с необъяснимой СН;
• лихорадку с цереброваскулярными расстрой-
ствами;
• лихорадку с необъяснимой почечной недо-
статочностью;

СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
988
______________________________________________________
ГЛАВА 7
Q
ЭНДОКАРДИТ
• лихорадку и боль в области спины;
• анемию неясного происхождения и умень-
шение массы тела;
• вновь появившийся шум над областью сердца;
• внутрибольничную инфекцию с лихорад-
кой у больных с установленными внутривенны-
ми катетерами.
К сожалению, средний срок установления
диа гноза «инфекционный эндокардит» от первых
жалоб и обращений к врачу составляет не ме нее
2–3 мес, а при поражении правых отделов сердца
и того более, до 87% больных поступают в стацио-
нар с неправильным диагнозом. Диагностика ин-
фекционного эндокардита у больных пожилого
возраста особенно затруднительна, количество
диаг ностических ошибок достигает 50%.
Для установления правильного диагноза не-
обходим учет всего комплекса проявлений пато-
логического процесса.
Возможные «маски» инфекционного эндокардита
1. Общие: недомогание, анорексия, умень-
шение массы тела, бледность кожных покровов,
ночная потливость.
2. Со стороны сердца: миокардит, перикардит,
поражение клапанов, ИМ (шумы, аритмия, СН).
3. Со стороны легких — чаще отмечаются при
поражении клапанов правых отделов сердца и
обусловлены развитием повторных инфаркт-
пневмоний, инфаркта легкого (плеврит, крово-
харканье, отек легких).
4. Со стороны органа зрения: внезапная сле-
пота, петехии на веках, на глазном дне — пете-
хиальные кровоизлияния и пятна Рота (белые
округлые пятна диаметром 1–2 мм, расположен-
ные поверхностно, иногда за крывающие сосуды
сетчатки, состоящие из скоплений клеток, об-
разовавшихся вследствие инфарктов сетчатки),
отек и неврит зрительного нерва.
5. Церебральные — протекающие под видом
острого нарушения мозгового кровообращения,
реже — менингита или менингоэнцефалита (ге-
миплегия, афазия, атаксия, головная боль, пси-
хические нарушения).
6. Почечные — проявляющиеся симптомами
диффузного гломерулонефрита или инфаркта
почки (протеинурия, гематурия, гипертензивный
криз).
7. Гематологические — проявляющиеся ане-
мией.
8. Со стороны опорно-двигательного аппара-
та: артрит, остеомиелит.
9. Сосудистые — воспроизводящие клинику си-
стемного васкулита, тромбангиита (геморрагиче-
ский синдром, тромбоэмболические осложнения).
Лечение
Терапия инфекционного эндокардита бази-
руется на нескольких принципах:
1. Терапия должна быть по возможности
этио тропной, то есть направленной на эрадика-
цию конкретного возбудителя.
2. Необходимо применять комбинацию не-
скольких антибактериальных препаратов для до-
стижения высоких бактерицидных концентраций
и предупреждения развития резистентности.
3. Терапия должна быть продолжительной:
при заболевании стрептококковой этиологии —
не менее 4 нед, стафилококковой — 6 нед, при
заболевании, вызванном грамотрицательными
возбудителями, — не менее 8 нед.
4. При нарастании признаков иммунного
конфликта в форме гломерулонефрита, васку-
лита, миокардита и др., а также проявлений
инфекционно-токсического шока рассматрива-
ют вопрос о назначении ГКС.
5. При острых формах инфекционного эндо-
кардита, вызванного преимущественно стафило-
кокками и грамотрицательными микроорганиз-
мами, целесообразно проведение иммунотера-
пии (антистафилококковая плазма, антистафи-
лококковый γ-глобулин) и дезинтоксикации.
6. При отсутствии эффекта в течение 2 нед
после применения адекватной антибиотикоте-
рапии необходима консультация кардиохирур-
га. Хирургическое лечение следует проводить по
строгим показаниям и свое временно.
В соответствии с приказом МЗ Украины
№ 436 от 03.07.2006 г. «Стандарти надання допо-
моги кардіологічним хворим» программа лече-
ния инфекционного эндокардита предусматри-
вает следующий перечень медицинских услуг:
Обязательный ассортимент
• оперативное лечение;
• этиотропная терапия: антибиотикотерапия
под контролем чувствительности возбудителя,
применение ГКС и др.
• симптоматическое лечение СН и ослож-
нений.
Дополнительный ассортимент
• применение амиодарона у больных с симп-
томными или тяжелыми желудочковыми арит-
миями;
• внутривенное введение симпатомиметиче-
ских средств (допамина и/или добутамина);
• непрямые антикоагулянты у больных с по-
стоянной формой фибрилляции предсердий, на-
личием тромбов в полостях сердца, тромбоэмбо-
лий в анамнезе.

СЕКЦИЯ 12
БОЛЕЗНИ ПЕРИКАРДА, МИОКАРДА,
ЭНДОКАРДА И КЛАПАНОВ СЕРДЦА
ГЛАВА 7
Q
ЭНДОКАРДИТ
_______________________________________________________
989
При выборе антибиотика следует учитывать
результаты микробиологического исследования,
чувствительность выделенного возбудителя.
Трудности лечения прежде всего обуслов-
лены широким распро странением нетипичных
возбудителей заболевания с высокой резистент-
ностью многих микроорганизмов к существую-
щим антибиотикам. Немаловажное значение
имеет и тот факт, что антибиотики плохо про-
никают в клапаны сердца и миокард и во многих
случаях (например при наличии искусственных
клапанов сердца, шунтов, кардиостимуляторов)
течение эндокардита не всегда прогнозируемо.
При выявлении инфекционного эндокардита
антибактериальное лечение необходимо начи-
нать как можно раньше, не дожидаясь иденти-
фикации возбудителя, поскольку процесс быстро
диссеминирует. В случаях с неустановленным
возбудителем инфекционного эндокардита ре-
комендуют начинать терапию бета-лактамными
антибиотиками и аминогликозидами (схема 7.1).
Отсутствие эффекта через 3–5 дней и отрица-
тельные результаты бактериологического иссле-
дования позволяют предположить наличие ста-
филококкового эндокардита, который вероятнее
всего обусловлен пенициллино- и метициллино-
резистентными стафилококками, что требует за-
мены антибиотика.
Наиболее эффективными считаются бензил-
пенициллин, цефалоспорины и аминогликозиды.
Антибиотиком выбора для начальной терапии,
как правило, является бензилпенициллин в су-
точной дозе 12–24 млн ЕД. Выбор этого антибио-
тика (при соблюдении рекомендуемой дозы) объ-
ясняется его доступностью, выраженным бакте-
рицидным действием на многие микроорганизмы
и широким терапевтическим диапазоном.
Современная этиотропная химиотерапия ин-
фекционного эндокардита у больных с нормаль-
ной функцией почек представлена в табл. 7.2.
Для лечения инфекционного эндокардита,
вызванного стрептококком, назначают бензил-
пенициллин в течение 4 нед или бензилпеницил-
лин в комбинации с аминогликозидом (гентами-
цин, тобрамицин в течение 2 нед). Эти режимы
требуют длительной госпитализации пациен-
тов и использования внутривенных катетеров,
что часто приводит к развитию флебитов. AHA
опубликовала результаты двух исследований по
лечению цефтриаксоном пациентов со стрепто-
кокковым эндокардитом. Высокая степень из-
лечения (98%) после 4-недельной терапии пре-
паратом оправдывает применение цефтриаксона
с учетом спектра активности и фармакокинети-
ческих особенностей, позволяющих назначать
его 1 раз в сутки и использовать для амбулатор-
ного лечения неосложненного инфекционного
эндокардита . При аллергических реакциях на
пенициллины и цефалоспорины рекомендованы
гликопептидные антибиотики.
Современная антибиотикотерапия энтеро-
коккового эндокардита с учетом того, что эн-
терококки значительно менее чувствительны
к бензилпенициллину и гентамицину, включает
комбинацию антибиотиков, обладающих синер-
гическим действием: аминопенициллин (ампи-
циллин) или гликопептидный антибиотик (ван-
комицин, тейкопланин) с аминогликозидами
(гентамицин, стрептомицин). Серьезную про-
блему представляют инфекционный эндокардит,
вызванный энтерококками с высоким уровнем
резистентности к аминогликозидам. В этих слу-
чаях назначают длительную (8–12 нед) терапию
бензилпенициллином или ампициллином в вы-
соких дозах. При аллергии к бета-лактамным
антибиотикам следует назначать ванкомицин
в комбинации с амино гликозидами внутривен-
но, тейкопланин. Частота реци дивов при этом
составляет 50%. При рецидиве показано кардио-
хирургическое лечение с имплантацией клапана.
Если энтерококки резистентны к пенициллинам,
аминогликозидам и ванкомицину, эффективной
антибактериальной терапии нет. Возможно при-
менение линезолида в дозе 600 мг каждые 12 ч.
Цефалоспорины не следует применять для
лечения энтерококкового эндокардита из-за
первичной резистент ности к ним этих микроор-
ганизмов.
При стафилококковом эндокардите дока-
зано, что бактерицидный эффект, стерилиза-
ция клапанов и профилактика их тяжелых по-
вреждений обеспечиваются быстрее при ис-
пользовании комбинации пенициллинов или
цефалоспоринов, устой чивых к действию бета-
лактамаз, и аминогликозидов. При неэффек-
тивности терапии, выделении пенициллино- и
метициллинорезистент ных штаммов золотисто-
го или эпидермального стафилококка или при
аллергии к бета-лактамным антибиотикам при-
меняют гликопептиды (ванкомицин, тейкопла-
нин) в сочетании с аминогликозидами. В случаях
аллергии к бета-лактамным антибиотикам при
стафилококковом эндокардите применяют так-
же линкозамиды (линкомицин, клиндамицин).
Высокой противостафилококковой активностью
отличается цефепим.
Эндокардиты, вызванные грамотрицательны-
ми микроорганизмами, почти всегда развивают-
