Эйхгорн Г. (ред.) Неорганическая биохимия. Том 1
Подождите немного. Документ загружается.

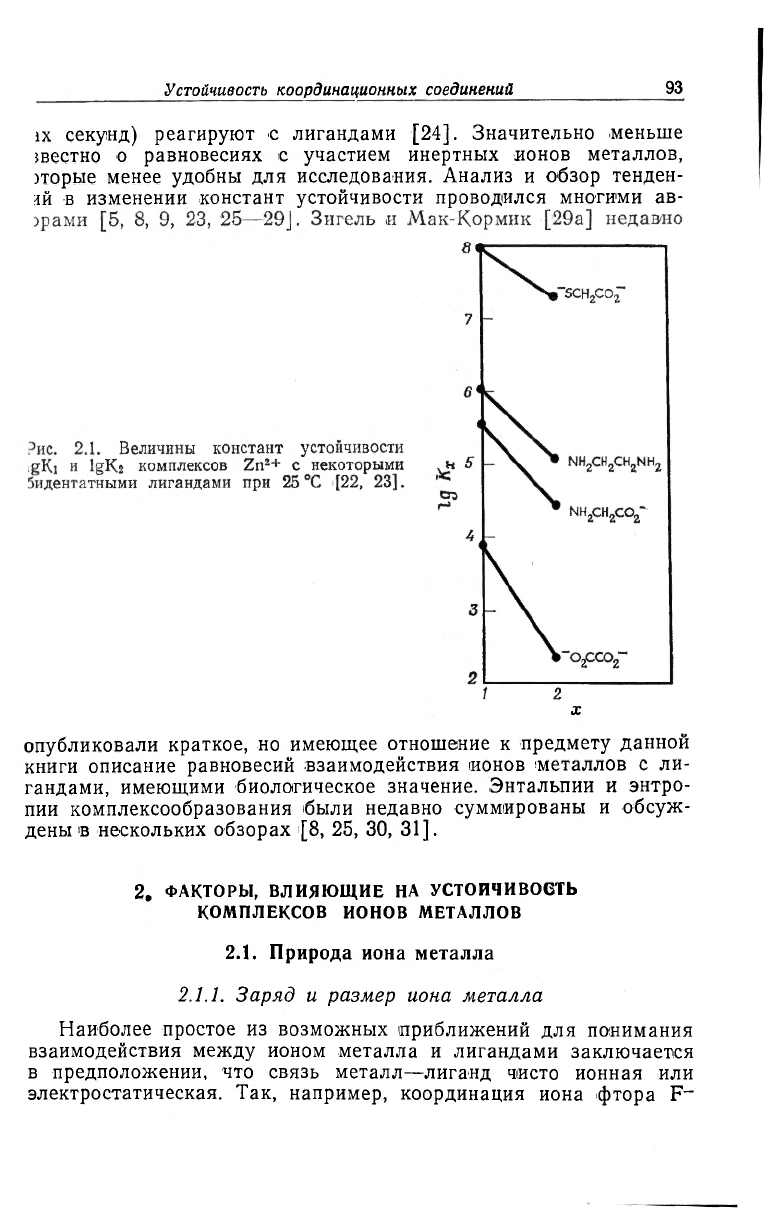
Устойчивость координационных соединений
93
IX секунд) реагируют с лигандами [24]. Значительно меньше
$вестно о равновесиях с участием инертных ионов металлов,
)торые менее удобны для исследования. Анализ и обзор тенден-
лй в изменении констант устойчивости проводился многими ав-
X
опубликовали краткое, но имеющее отношение к предмету данной
книги описание равновесий взаимодействия ионов !металлов с ли-
гандами, имеющими биологическое значение. Энтальпии и энтро-
пии комплексообразования были недавно суммированы и обсуж-
дены в нескольких обзорах [8, 25, 30, 31].
2. ФАКТОРЫ, ВЛИЯЮЩИЕ НА УСТОЙЧИВОСТЬ
КОМПЛЕКСОВ ИОНОВ МЕТАЛЛОВ
2.1. Природа иона металла
2.1.1. Заряд и размер иона металла
Наиболее простое из возможных приближений для понимания
взаимодействия между ионом металла и лигандами заключается
в предположении, что связь металл—лиганд чисто ионная или
электростатическая. Так, например, координация иона фтора F
-
94 i лава 2
ионом 'металла должна зависеть от зарядов на взаимодействуй
щих ионах и расстояния (г) между их ядрами. Предполагаете
что ионы представляют жесткие сферы
Mm+ F
-
с зарядами, локализованными на их ядрах. Вычисленная электрс
статическая энергия такой связи равна £ = E
2
Z
M
M
+Z
F
-/r, где е-
заряд электрона, a Z
M
M
+ и Z
f
- —полные заряды на ионах.
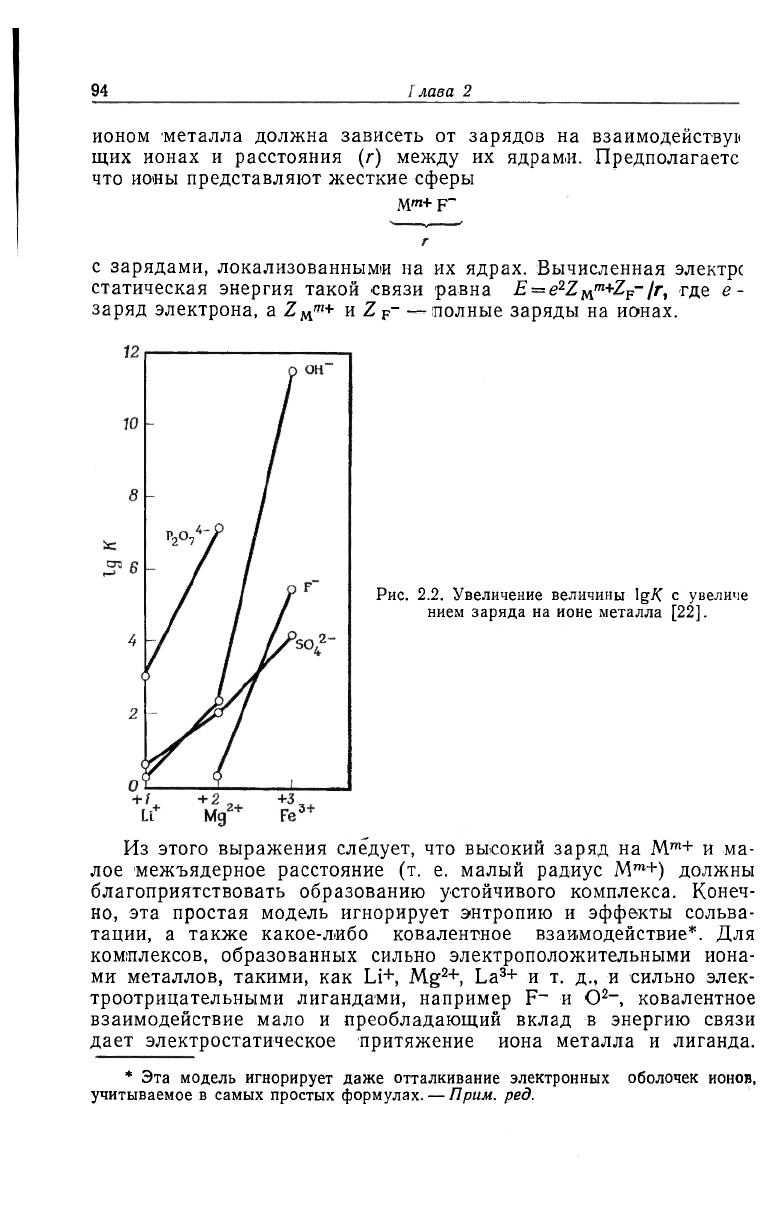
Рис. 2.2. Увеличение величины IgTC с увеличе
нием заряда на ионе металла [22].
Из этого выражения следует, что высокий заряд на M
m
+ и ма-
лое межъядерное расстояние (т. е. малый радиус M
m
+) должны
благоприятствовать образованию устойчивого комплекса. Конеч-
но, эта простая модель игнорирует энтропию и эффекты сольва-
тации, а также какое-либо ковалентное взаимодействие*. Для
комплексов, образованных сильно электроположительными иона-
ми металлов, такими, как Li+, Mg
2
+, La
3
+ и т. д., и сильно элек-
троотрицательными лигандами, например F
-
и О
2-
, ковалентное
взаимодействие мало и преобладающий вклад в энергию связи
дает электростатическое притяжение иона металла и лиганда.
* Эта модель игнорирует даже отталкивание электронных оболочек ионов,
учитываемое в самых простых формулах. — Прим. ред.

Устойчивость координационных соединений
95
эны металлов и лиганды этого типа называются жесткими [или
шнадлежагцими к классу (а)] кислотами и основаниями соот-
тственно. Эта система классификации более детально обсужда-
ся в разд. 2.1.2.
Если рассматриваются только жесткие ионы металлов и ли-
нды, то в общем верно, что наиболее устойчивые комплексы об-
1зуют ионы металлов, имеющие наиболее высокие заряды, при
УЮВИИ близости их ионных радиусов. Из рис. 2.2 видно, что IgK
1Я равновесия M
m+
+L
n
-^MU
m
-'
1
'+ увеличивается с увеличени-
\ заряда на ионе металла в следующем порядке: Li+(0,68 А) <
;Mg
2
+(0,65 A)<Fe
3
+(0,53 А), в скобках приведены ионные ра-
1усы. Следует также отметить, что соответствующее повышение
с увеличением заряда на лиганде_отсутствует. Поведение ли-
шда усложняется тем, что ион SO
4
может быть как моноден-
атным, так и бидентатным, в то время как Р2О7 , по-видимому,
ядентатен.
Величины К повышаются также при уменьшении размера иона
еталла. Так, например, при комплексообразоваяии иояов щелоч-
эземельных металлов [22] с пирофосфатным ионом P
2
Of вели-
ина К уменьшается при переходе в группе сверху вниз:
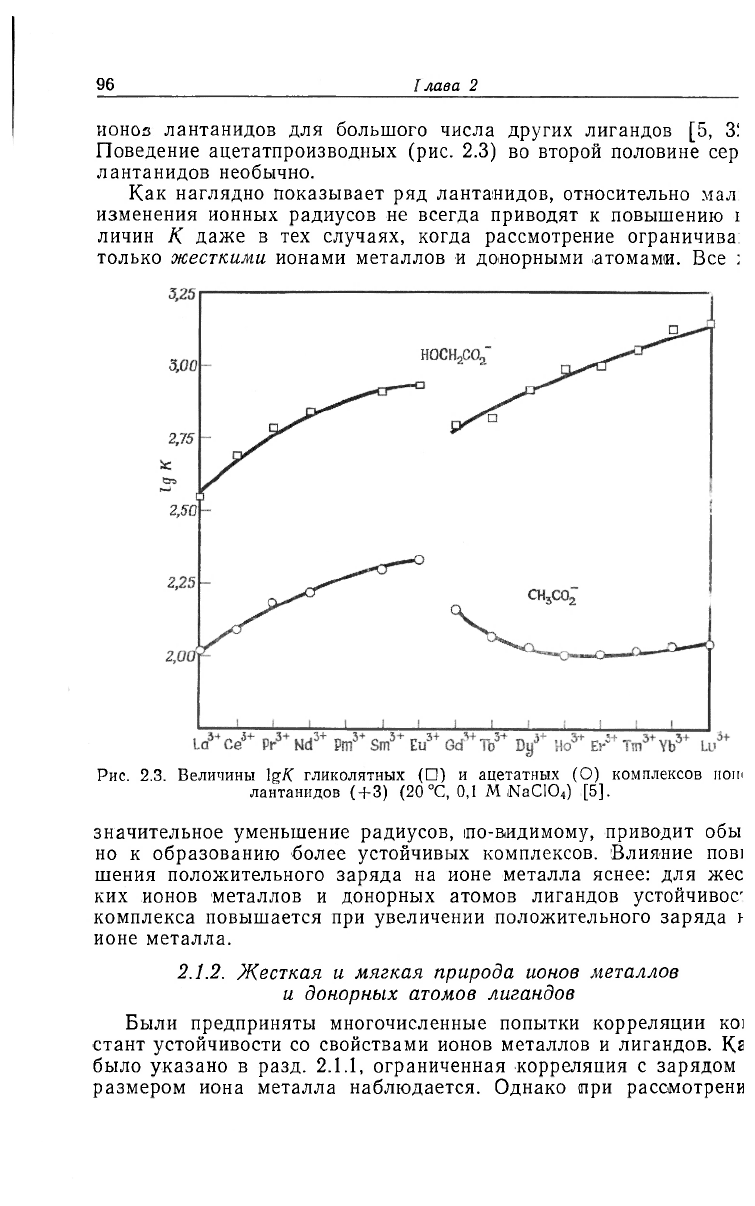
•та тенденция иллюстрируется (рис. 2.3) также ионами лантани-
ов (Ln
3
+), ионные радиусы которых равномерно уменьшаются от
,06 А для наиболее легкого элемента La
3
+ до 0,85 А для наиболее
яжелого элемента Lu
3
+. На рис. 2.3 приведены кривые, относящие-
я к константам устойчивости комплексов с анионом гликолевой
ислоты, который координируется бидентатно через атомы кисло-
ода карбоксильной и спиртовой групп, и комплексов с ацетат-
ым ионом. Простая электростатическая модель предсказывает
!авномерное повышение IgTC от La
3
+ до Lu
3
+. Точнее, зависимость
g/С от
1
/г должна представлять прямую линию. Однако в дейст-
ительности такая зависимость не является прямой, и даже каче-
твенно отсутствует равномерное повышение lg/(. Действительно,
[антаниды ведут себя так, как если бы они состояли из двух
тличающихся друг от друга групп: La
3
+—Eu
3
+ и Gd
3
+—Lu
3
+. Ta-
;ое изменение свойств при переходе к Gd
3
+ объясняли [5] различ-
[ыми причинами, такими, как энергия стабилизации кристалличе-
ким полем или стерические факторы, но полностью удовлетвори-
•ельного объяснения не найдено. Такой же тип зависимости, как
[ля гликолята, обычно наблюдается для равновесий с участием
о
Mg
2
+
Ca
2
+
Sr
2
+
Ba
2
+
Радиус, А
0,65
0,94
1,10
1,29
IgK
7,2
6,8
5,4
4.6
96
i лава 2
ионоз лантанидов для большого числа других лигандов [5, 3!
Поведение ацетатпроизводных (рис. 2.3) во второй половине сер
лантанидов необычно.
Как наглядно показывает ряд лантанидов, относительно мал
изменения ионных радиусов не всегда приводят к повышению I
личин К даже в тех случаях, когда рассмотрение ограничива:
только жесткими ионами металлов и дояорными атомами. Все :
Рис. 2.3. Величины lg/C гликолятных (•) и ацетатных (О) комплексов нош
лантанидов ( + 3) (20 °С, 0,1 MiNaClO
4
) [5].
значительное уменьшение радиусов, по-видимому, приводит обы
но к образованию более устойчивых комплексов. Влияние пов1
шения положительного заряда на ионе металла яснее: для жес
ких ионов металлов и донорных атомов лигандов устойчивое'
комплекса повышается при увеличении положительного заряда \
ионе металла.
2.1.2. Жесткая и мягкая природа ионов металлов
и донорных атомов лигандов
Были предприняты многочисленные попытки корреляции KOI
стант устойчивости со свойствами ионов металлов и лигандов. Ka
было указано в разд. 2.1.1, ограниченная корреляция с зарядом
размером иона металла наблюдается. Однако при рассмотрени

Устойчивость координационных соединений
97
шрокого диапазона ионов металлов и лигандов становится ясно,
то существует очень мало корреляций. Более того, имеется мно-
D примеров обращения тенденции. Например, константы устойчи-
ости галогенидных комплексов Fe
3
+ понижаются в ряду F
-
>
>С1
-
>Вг
_
;>1~. В противоположность этому Hg
2
+ образует более
стойчивые комплексы с более тяжелыми галогенидами, и К по-
ижаются следующим образом: I->Br->Cl
-
>F-. Из этого
многих других примеров Шварценбах [33], а затем Арланд,
[атт и Дэвис [34] пришли к заключению, что по отношению к
онам галогенидов некоторые 'металлы ведут себя подобно Fe
3
+,
другие — подобно Hg
2
+. Первые были отнесены к классу (а),
вторые — к классу (б) ионов металлов или кислот. Сравнивая
онстанты устойчивости комплексов других лигандов с различ-
ыми ионами металлов, можно дать более полную характеристи-
у двух классов ионов металлов. В табл. 2.2 приведены лоследо-
ательности констант устойчивости, которые обычно наблюдают-
я для ионов металлов классов (а) и (б) с различными донорны-
:и атомами лигандов. Для классификации ионов металлов были
акже важны термодинамические параметры [31] этих реакций.
В табл. 2.3 приведены ионы металлов, принадлежность кото-
ых к этим классам была установлена экспериментально [35].
!ледует указать, что существуют металлы, подчиняющиеся неко-
орым тенденциям класса (а) и некоторым тенденциям класса (б)
онов металлов; они располагаются в пограничной области этой
лассификации. Можно заметить, что многие из ионов металлов,
аходящихся в пограничной области, — это двухзарядные ( + 2)
оны переходных металлов.
Таблица 2.2
Определение жестких [класс (а)] и мягких [класс (б)]
ионов металлов (в соответствии с порядком изменения
устойчивости комплексов с различными донорными
атомами лигандов)
Изменение устойчивости
комплексов жестких, или
класса (а), ионов металлов
Изменение устойчивости
комплексов мягких,
или класса (6),
ионов металлов
F > Cl > Br > I
F<Cl<Br<I
0»S>Se>Te О « S ~ Se ~ Те
N»P>As>Sb N С P > As > Sb
При рассмотрении ионов металлов класса (а) обнаруживает-
я, что их свойства во многом сходны. Они имеют малые радиусы
: высокие положительные заряды, но обычно не имеют неподелен-
ых электронных пар в их валентной оболочке (а многие из них
-2451

98
i лава 2
Таблица 2.
Классификация ионов металлов
Жесткие, или класс (а)
Пограничная область
Мягкие, или класс (б)
H+, Li+, Na+, к+
Fe
2
+, Со
2
+, Ni
2
+
Cu+, Ag+, Au+, Tl+
Be
2
+, Mg
2
+, Ca
2
+, Sr
2
+
Cu
2
+, Zn
2
+, Pb
2
+
Hgl+, Hg
2
+, Pd
2
+, Pl
2
+
Mn
2
+, Al
3
+, Sc
3
+, Ga
3
+
Sn
2
+, Sb
3
+, Bi
3
+
Р{4+ JJ3+
In
3
+, La
3
+, Gd
3
+, Lu
3
+
Cr
3
+, Со
3
+, Fe
3
+, Si
4
+
Ti
4
+, Sn
4
+, WO
4
+, VO
2
+
обладают электронной конфигурацией благородного газа). Вслед
ствие малых размеров и высоких положительных зарядов и
поляризуемость низка; по этой причине они были названы [35
«жесткими». Наиболее прочные комплексы эти ионы металло
образуют с очень электроотрицательными атомами, такими, как С
N и F (табл. 2.2). Связь в этих комплексах преимущественно ион
пая.
Ионы металлов класса (б) значительно больше; они имеют бо
лее низкие положительные заряды я неспаренные валентные р
или d-электроны. Благодаря этим свойствам ионы металлов клас
са (б) в большей степени поляризуемы, вследствие этого они бы
ли названы «мягкими». Наиболее устойчивые комплексы эти иош
металлов образуют с донорными атомами лигандов (Р, S и I)
имеющими низкие электроотрицательности и высокую поляризус
мость. Связи в этих комплексах содержат значительный коваленг
ный вклад.
Как было указано выше, жесткие ионы металлов образую
наиболее прочные комплексы с донорными атомами (N, О и F)
которые обладают высокими электроотрицательностями, низко
поляризуемостью, малыми радиусами и трудно окисляются. Бла
годаря этим свойствам они были обозначены как жесткое основа
ние Льюиса или жесткие донорные атомы. С другой стороны, т
атомы лигандов (р, sHi), которые образуют наиболее устойчл
вые комплексы с мягкими ионами металлов, имеют большие pas
меры, низкие электроотрицательности, высокие поляризуемости i
относительно легко окисляются; они были названы мягкими лу.
гандами. Наиболее типичные жесткие, мягкие и промежуточны
ляганды приведены [35] в табл. 2.4.
В терминах нашей новой номенклатуры тенденции табл. 2.
можно суммировать следующим образом [40]: жесткие ионы Mt
таллов предпочитают координировать жесткие лиганды, а мягки

Устойчивость координационных соединений
99
Таблица 2.4
Классификация лигандов
Жесткие, или класс (а)
Промежуточные
Мягкие, или класс (б)
,0, ОН-, F-, Cl-
C
6
H
5
NH
2
, C
5
H
5
N R
2
S, RS, I-
I
3
COJ, РОЦ-, SOl"
N
3
, Br-, NOJ SCN-, S
2
0§-
}§-, СЮГ, NOJ
SO
2
3
-, N
2
R
3
P, (RO)
3
P, R
3
As
ЭН, R
2
O, NH
3
CN-, RNC, СО
MH
2
, N
2
H
4
H
-
, R-, C
2
H
4
оны металлов предпочитают координировать мягкие лиганды.
!отя были предприняты многочисленные попытки [35—38] теоре-
ического обоснования этого правила, его следует рассматривать
ак эмпирическое. Путем полуэмпирической обработки [39] с ис-
ользованием ионных радиусов, зарядов, потенциалов ионизации
: электроотрицательностей ионов металлов был получен количе-
твенный параметр мягкости иона металла. Наряду с другими
[араметрами иона металла и лиганда он коррелируется с доволь-
ю большим числом констант устойчивости комплексов металла.
3 коррелировании свойств мягкости и жесткости 'было довольно
/спешным и более теоретическое приближение [40]*.
Это правило полезно для качественного описания взаимодейст-
вий в биологических системах. Пирсон [41] указал, что биоло-
гические комплексы состоят преимущественно из жестких ионов
металлов и лигандов. Преобладающие донорные атомы лиган-
дов — кислород и азот, а жесткие ионы щелочных и щелочнозе-
мельных металлов присутствуют в изобилии. Конечно, имеются
также относительно мягкие ионы металлов (например, Cu
2
+)**
и лиганды (например, лиганды с донорными атомами серы), но
они относительно неподвижны и концентрация их низка. Пирсон
также заметил, что соединения, представляющие яды для живых
организмов, часто относятся к классу мягких, например такие ли-
ганды, как СО, CN
-
и H
2
S, и такие ионы металлов, как Hg
2
+. Ес-
ли эти мягкие ядовитые частицы присутствуют в относительно
высоких концентрациях, то они взаимодействуют с мягкими иона-
ми металлов и лигандами, препятствуя таким образом выполне-
нию их функций. Хотя несомненно, что эти обобщения не могут
быть применены ко всем аспектам рассмотрения живых организ-
* См. также Яцимирский К. БЖ. анал. хим., 6, 211 (1951); ЖФХ, 25, 221
(1951); Теор. эксп. хим., 6, 462 (1970). — Прим. ред.
** И в особенности Cu
+
Cd
2
+, а также токсичные ионы Hg
2
+ и Pb
2
+. —
Прим. ред.
7*

100
i лава 2
мов, они представляют еще одну исходную точку для исследов
ния этих исключительно сложных систем.
Принцип жесткости и мягкости можно применить к координ
ции ионов переходных металлов >к нуклеотидди- и нуклеотидтр
фосфатам [42]. Жесткие ионы металлов, такие, как щелочноз
мельные и Mn
2
+, координируются главным образом через атом
кислорода фосфатных групп, в то время как более мягкий ис
Cu
2
+ координируется как к мягкому атому азота ароматичеоко!
пуринового или пиримидинового основания, так и к_ фосфатнс
группе. Подобным образом лиганд CH
3
CH
2
SCH
2
CO коордиш
руется к относительно жестким ионам металлов Mn
2
+и Zn
2
+толы*
через атом кислорода, в то время как ион Cu
2
+ образует хела'
координируясь как через атом кислорода, так и через мягкий ато
серы [43].
Наше рассмотрение предполагает, что молекулы воды занимг
ют координационные места, не занятые другими лигандами. Ka
было указано [35], природа лигандов, присоединенных к ион
металла, влияет на его жесткость и мягкость. По-видимому, жест
кие лиганды делают лиганд еще более жестким, а мягкие —боле
мягким по отношению -к дополнительным лигандам. Так, напри
мер, ионы металлов, связанные с серусодержащими лигандам,:
или относительно мягкими порфириновыми кольцами, будут про
являть большую тенденцию к образованию комплексов с допол
нительными мягкими лигандами по сравнению с гидратированньм
ионом металла [M(H
2
O)
6
]
2
+, связанным с молекулами воды, ко
торые относятся к жестким лигандам. Именно влиянием лигандо]
можно объяснить тот факт, что железо ,в геме столь прочно коор
динирует такие мягкие лиганды, как СО и CN
-
, даже в присутст
вии большого количества жесткого лиганда воды. Этим адожнс
объяснить такое высокое сродство Fe
2
+ (и, по-видимому, даже
Fe
3
+) к сере в негеминовых железо-серусодержащих белка>
[44, 45].
2.1.3. Последовательность Ирвинга—У альянса устойчивостей
комплексов ионов металлов первого переходного ряда
Как было отмечено в предыдущем разделе, ионы металлов пер-
вого переходного ряда по их жесткости и мягкости занимают про-
межуточное положение. По этой причине часто трудно предска-
зать устойчивости их комплексов. Однако в течение многих лет
было известно [46—48], что константы устойчивости двухзаряд-
ных ионов этих элементов с данным лигандом изменяются в соот-
ветствии с последовательностью Mn
2
+<Fe
2
+<;Co
2
+<Ni
2
+<Cu
2
+>
>Zn
2
+. Эта последовательность часто называется порядком устой-
чивостей Ирвинга—Уильявдса. Для нескольких лигандов она по-
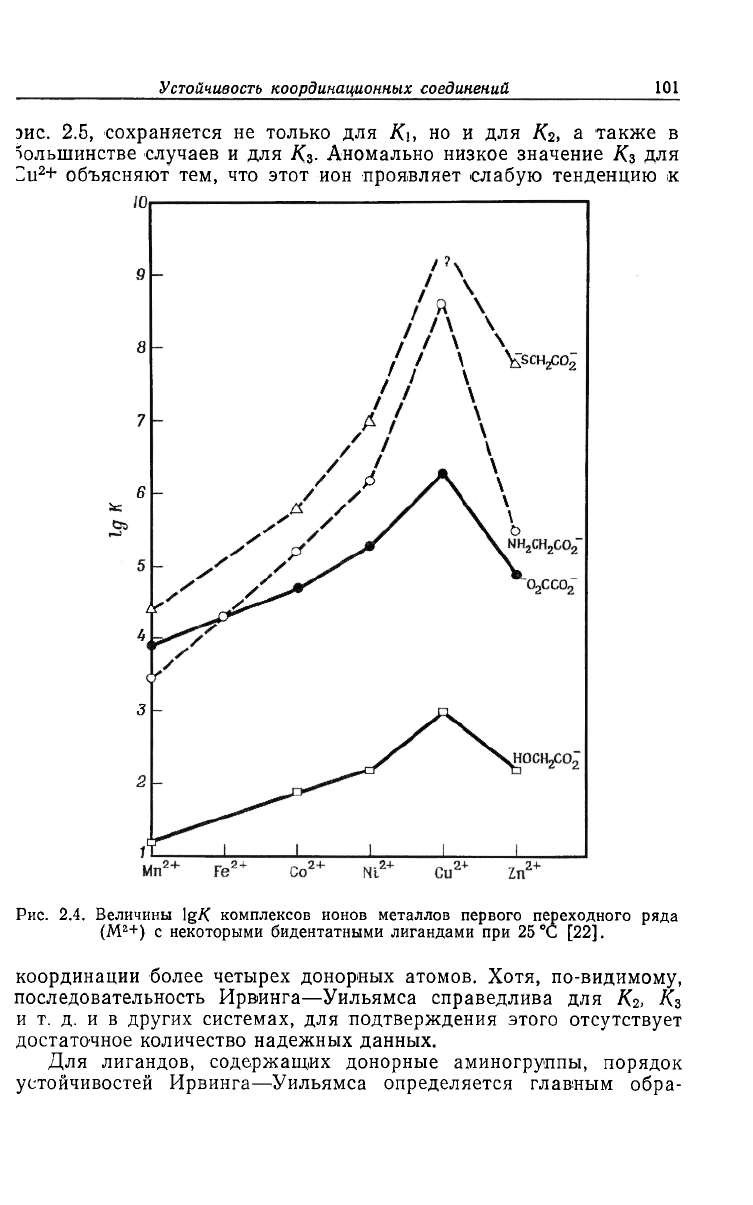
казана на рис. 2.4. Эта последовательность, как можно видеть из
Устойчивость координационных соединений
101
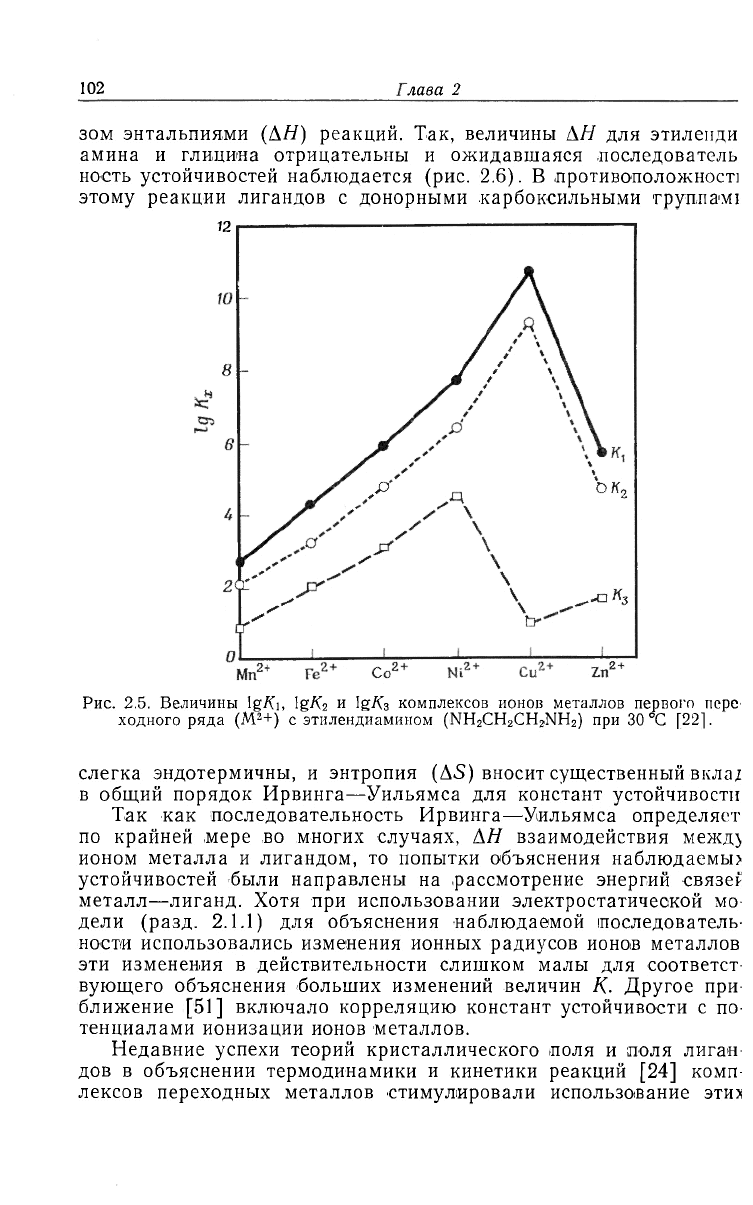
эис. 2.5, сохраняется не только для Ku но и для Къ, а также в
большинстве случаев и для Kz- Аномально низкое значение Kz для
Zu
2+
объясняют тем, что этот ион проявляет слабую тенденцию к
Рис. 2.4. Величины lg/f комплексов ионов металлов первого переходного ряда
(M
2+
) с некоторыми бидентатными лигандами при 25
0
C [22].
координации более четырех доноряых атомов. Хотя, по-видимому,
последовательность Ирвинга—Уильямса справедлива для K
2
, Kz
и т. д. и в других системах, для подтверждения этого отсутствует
достаточное количество надежных данных.
Для лигандов, содержащих донорные аминогруппы, порядок
устойчивостей Ирвинга—Уильямса определяется главным обра-
102
i лава 2
зом энтальпиями (АН) реакций. Так, величины А Я для этиленди
амина и глицина отрицательны и ожидавшаяся последователь
ность устойчивостей наблюдается (рис. 2.6). В противоположное^
этому реакции лигандов с донорными карбоксильными труппам!
Рис. 2.5. Величины lg/Ci, Ig/C
2
и IgZC
3
комплексов нонов металлов первого пере
ходного ряда (M
2+
) с этилендиамином (NH
2
CH
2
CH
2
NH
2
) при 30 °С [22].
слегка эндотермичны, и энтропия (AS) вносит существенный вклад
в общий порядок Ирвинга—Уильямса для констант устойчивости
Так как последовательность Ирвинга—-Уильямса определяет
по крайней мере во многих случаях, АН взаимодействия межд}
ионом металла и лигандом, то попытки объяснения наблюдаемы?
устойчивостей были направлены на рассмотрение энергий связей
металл—лиганд. Хотя при использовании электростатической мо-
дели (разд. 2.1.1) для объяснения наблюдаемой последователь-
ности использовались изменения ионных радиусов ионо.в металлов
эти изменения в действительности слишком малы для соответст-
вующего объяснения больших изменений величин К. Другое при-
ближение [51] включало корреляцию констант устойчивости с по-
тенциалами ионизации ионов металлов.
Недавние успехи теорий кристаллического поля и поля лиган-
дов в объяснении термодинамики и кинетики реакций [24] комп-
лексов переходных металлов стимулировали использование этих
12
