Чемерис М.М., Люкшова Н.В., Мозуленко Л.М. Органическая химия.Часть 1
Подождите немного. Документ загружается.

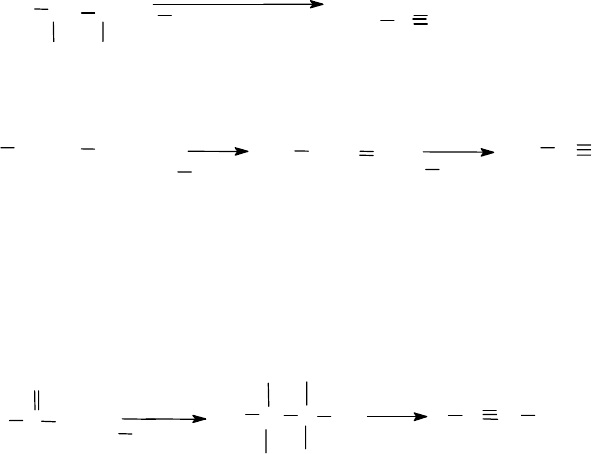
111
а) вицинальных, содержащих атомы галогена у соседних атомов
углерода, обработкой спиртовым раствором КОН или амидом натрия
(NaNH
2
):
C
H
3
C
H
C
H
2
B
r
B
r
K
O
H
C
2
H
5
O
H
H
B
r
2
C
H
3
C
C
H
Отщепление может протекать в две стадии:
HBr
CH
3
CHBr CH
2
Br
C
H
3
CB
r
CH
2
H
Br
CH
3
CCH
Отщепление водорода идет по правилу Зайцева: от наименее гид-
рогенизированного атома углерода.
б) геминальных, содержащих оба галогена у одного атома углеро-
да. Такие галогенопроизводные получают при действии
PCl
5
на оксо-
соединения:
2
R C C H
2
R
O
P O C l
3
R C C R
C l
C l
H
H
K O H
спирт
R C C R
+
H C l
3.3.4. Спектральные характеристики алкинов
Ацетиленовые углеводороды имеют в ИК-спектре характеристиче-
ские полосы поглощения валентных колебаний тройной связи
С
≡
С
при 2100-2300 см
-1
, С
SP
-Н при 3100-3300 см
-1
. УФ-излучение они по-
глощают в области ниже 200 нм, т.е. не дают спектров на обычных
УФ-спектрометрах, которые работают выше 200 нм. В спектрах ЯМР
проявляются сигналы протона при тройной связи
С
≡
С -Н в области 2-
3 м.д. (
δ
).
3.3.5. Химические свойства
Химические реакции ацетиленовых углеводородов можно разде-
лить на 4 группы:
1) реакции присоединения по С
≡
С-связи;
п
р
опин
112
2) реакции замещения водорода либо металла в ацетиленидах (этини-
лирование);
3) реакции окисления;
4) реакции полимеризации.
3.3.5.1. Реакции присоединения к алкинам
обычно протекают в
две стадии:
Первая
-
приводит
к производным этилена;
Вторая
-
приводит к производным предельных углеводородов (ал-
канов).
Вы помните, что тройная связь является суммой одной
σ
- и двух
π
-связей, следовательно, она осуществляется шестью электронами и
максимальная электронная плотность молекулы сосредоточена в об-
ласти между ядрами атомов С. Таким образом, область повышенной
электронной плотности будет подтвержена атаке электрофильными
положительными частицами (Н
,
Вr
и др
.)
или
положительным кон-
цом диполей
(
Cl
δ+
OH
δ−
, Br
δ+
Br
δ−
и др.)
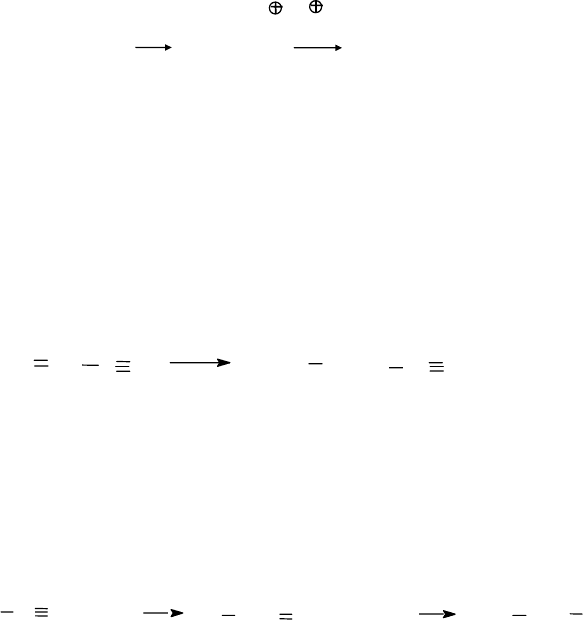
Для алкинов характерны те же реакции электрофильного присое-
динения, что и для алкенов, Однако ацетилены в эти реакции вступа-
ют труднее, чем алкены. Это можно объяснить тем, что тройная связь
(0,120 нм) короче, чем двойная (0,134 нм) и, следовательно, электроны
сильнее удерживаются ядрами. Электроны
π
-связей имеют меньшую
поляризуемость, а, в следствии этого, меньшую реакционную способ-
ность в реакциях электрофильного присоединения к алкинам. Приме-
ром меньшей реакционной способности тройной связи в реакциях
электрофильного присоединения является бромирование винилацети-
лена, при котором происходит присоединение брома к двойной связи.
CH
2
CH C CH
Br
2
BrCH
2
CHBr C CH
В отличие от алкенов, для алкинов характерны некоторые реакции
нуклеофильного присоединения (например, присоединение аминов,
алкоголятов, меркаптидов).
Рассмотрим примеры реакций электрофильного присоединения.
Механизм этих реакций аналогичен механизму в алкенах.
3.3.5.1.1. Галогенирование ацетиленовых углеводородов
CH
3
CCH
+
Br
2
V
1
CH
3
CBr CHBr
V
2
CH
3
Вr
2
+
CBr
2
CHBr
2
Кинетические измерения показали, что скорость первой стадии ре-
акции V
1
, значительно меньше скорости второй стадииV
2
, что
сви-
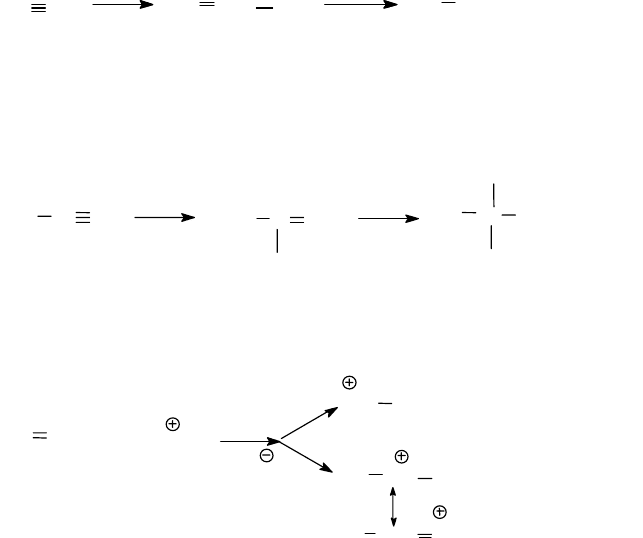
113
детельствует о меньшей реакционной способности тройной связи по
сравнению с двойной.
3.3.5.1.2. Присоединение галогеноводородов
CH CH
H
Cl
CH
2
CH
C
l
H
Cl
C
H
3
CHCl
2
CH CH CH
2
CH
C
l
H
Cl
CHCl
2
Присоединение
галогеноводородов к несимметричным ацетиле-
нам идет по правилу Марковникова: водород присоединяется к наи-
более гидрогенизированному атому углерода.
HBr
CH
3
C
C
H
CH
3
CCH
2
+
CH
3
CCH
3
Br
Br
Br
HBr
+
При присоединении второй молекулы галогеноводорода возможно
образование двух карбокатионов (1) и (2):
H
B
r
+
-B
r
2
C
H
2
C
H
B
r
C
H
2
C
H
2
B
r
C
H
3
C
H
B
r
C
H
3
C
H
B
r
(
)
(
)
1
Однако карбокатион (2) обладает большей стабильностью вслед-
ствие резонансной стабилизации. Поэтому региоселективно образует-
ся дибромид, содержащий оба галогена у одного и того же атома уг-
лерода.
3.3.5.1.3. Присоединение воды (реакция Кучерова)
Осуществляется пропусканием ацетилена или его гомологов через
разбавленный раствор H
2
SO
4
в присутствии HgSO
4
.
При этом получа-
ется уксусный альдегид (в случае ацетилена) или кетоны (в случае го-
мологов ацетилена):
3
C H C l
2
дихло
р
этан
хлористый винил 1,1-дихлорэтан
пропин 2,2-дибромпропан
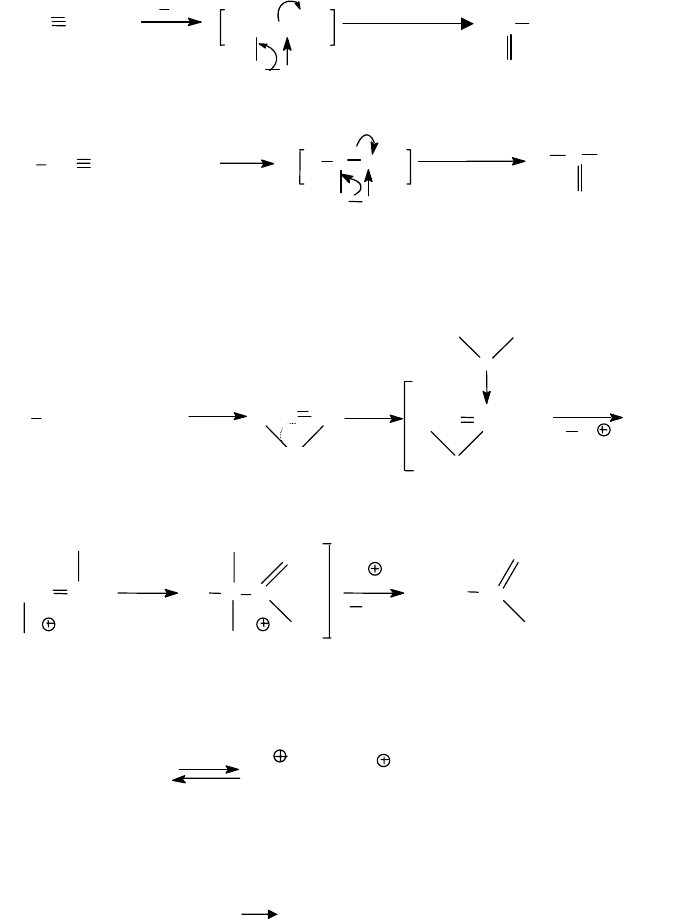
114
гомологи ацетилена
ацетилен енол (неустойчив) уксусный альдегид
HgSO
4
H
2
SO
4
+
C
H
C H
H O H
Н-С -
..
СH
2
H
H C C H
3
O
O
изомеризация
+
C
H
..
H
2
SO
4
C H
H
HgSO
4
O
H
R
C
C H
2
H
C C H
3
O
O
изомериз.
R
R
Присоединение воды идет по правилу Марковникова.
Предполагается, что механизм гидратации ацетилена следующий:
2+
C
≡
2+
C H
H
O
H g C H C H
H
2
O
H
H
.
.
C H C
H
H
+
H g
Hg
2+
O
H g
C
H
C H
C C
H
Hg
H
+
+
2
H
O H
H
H g
C H
3
C
O
H
Роль кислоты, добавляемой вместе с HgSO
4
, заключается в предот-
вращении гидролиза солей двухвалентной ртути.
H
g
H
2
O
+
2
O
H
H
g
H
+ +
3.3.5.1.4. Присоединение синильной кислоты HCN,
катализатор (CuCl
2
+ NH
3
)
CH
≡
CH + H-C
≡
N CH
2
= CH – CN
акрилонитрил
Продукт реакции используют как исходное сырье для получения
полиакрилонитрильных волокон - нитронов.
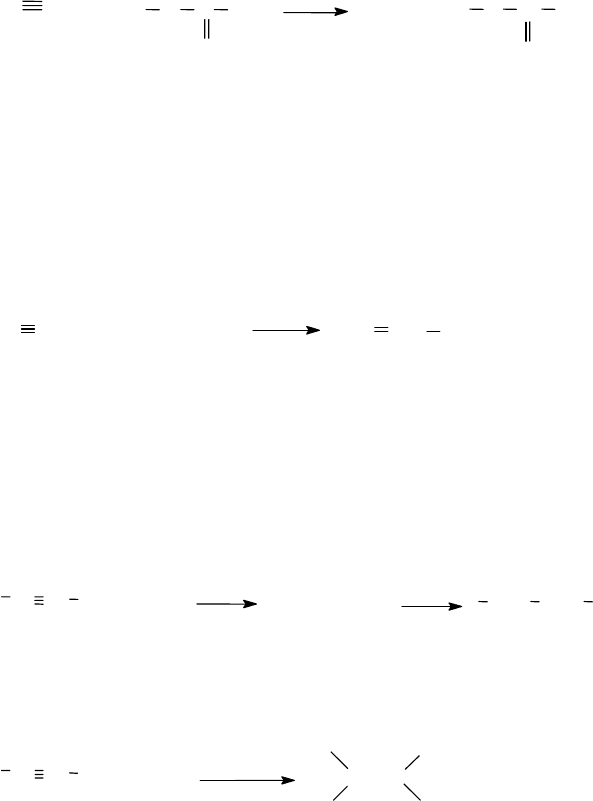
3.3.5.1.5. Присоединение карбоновых кислот
C H C l
2
ихло
р
этан
115
винилэтиловый эфир
Реакция приводит к получению сложных эфиров винилового спир-
та, которые являются мономерами для синтеза полимеров. Так, при-
соединением уксусной кислоты к ацетилену синтезируют винилаце-
тат, полимеризацией которого получают широко используемый поли-
винилацетат:
CH CH
+
HOCC
H
3
O
H
3
PO
4
CH
2
=CHO C CH
3
O
винилацетат
3.3.5.1.6. Присоединение спиртов (реакция Фаворского)
В отличие от вышеизложенных реакций, присоединение спиртов в
щелочной среде протекает по механизму нуклеофильного присоеди-
нения при температуре 150
о
С и давлении 2
.
10
6
Па.
CH CH
+
C
2
H
5
OH
KOH
CH
2
CH OC
2
H
5
Продукт реакции используют как исходное сырье для получения
полиалкилвиниловых эфиров.
3.3.5.2. Каталитическое гидрирование алкинов
Обычно осуществляется водородом на Ni, Pd, Pt - катализаторах.
Реакция идет в две стадии:
RC C R
+
RCH = CH
R
+
H
2
H
2
Ni
Ni
RCH
2
CH
2
R
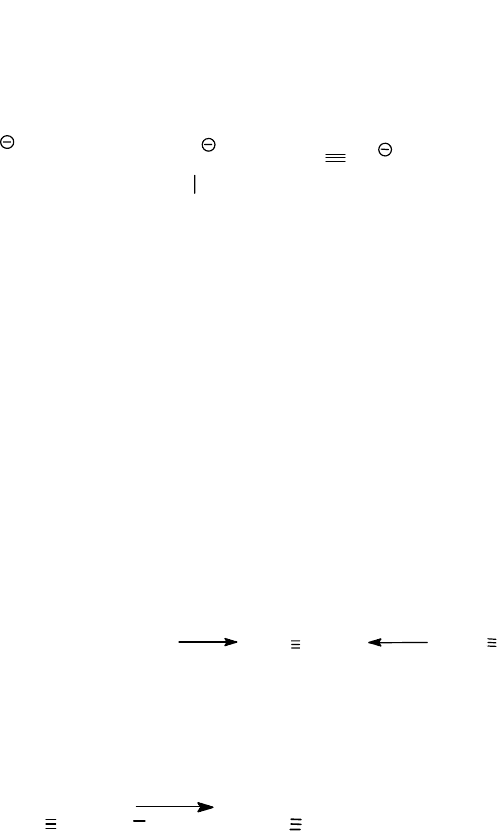
Если в качестве катализатора использовать Pd, отравленный соля-
ми свинца, то реакцию можно остановить на стадии образования ал-
кена. При этом образуется цис-изомер.
RC C R
+
H
2
Pd
PbCO
3
C=C
R
R
H
H
Механизм каталитического гидрирования алкинов аналогичен та-
ковому для алкенов.
116
3.3.5.3. Реакция замещения и этинилирования
Известно, что электроотрицательность углерода растет в ряду:
<
S
P
3
C
S
P
2
C
S
P
C
<
2,50 2,62 2,75
Наиболее электроотрицательный
sp
-гибридизованый атом углеро-
да более, чем другие, способен к стабилизации карбаниона, образую-
щегося при диссоциации связи С-Н
по
кислотному типу:
:CH
3
CH
2
=C:
H
CH C:
Вследствие этого ацетилен и его гомологи являются кислотами,
хотя и более слабыми, чем вода.
Константы диссоциации некоторых кислот
СН
3
СООН Н
2
О С
2
Н
5
ОН НС
≡
СН
К
а
= 1,75
.
10
-5
10
-16
10
-18
10
-22
3.3.5.3.1. Взаимодействие алкинов с металлами I и II групп
При пропускании ацетилена над поверхностью металлического
натрия при 150
о
С образуется ацетинилид натрия, который может быть
получен также при взаимодействии ацетилена с NaNH
2
в жидком NH
3
(t
кип
=-33
о
С).
Н
C
≡
-
CН
+
H
2
N
a
НC
C
N
a
150
o
C
1
/
2
НC
CН
N
H
3
(
ж
)
+
N
a
N
H
2
При нагревании мононатриевого ацетиленида с натрием до
∼
220
о
С
получается динатриевый ацетиленид.
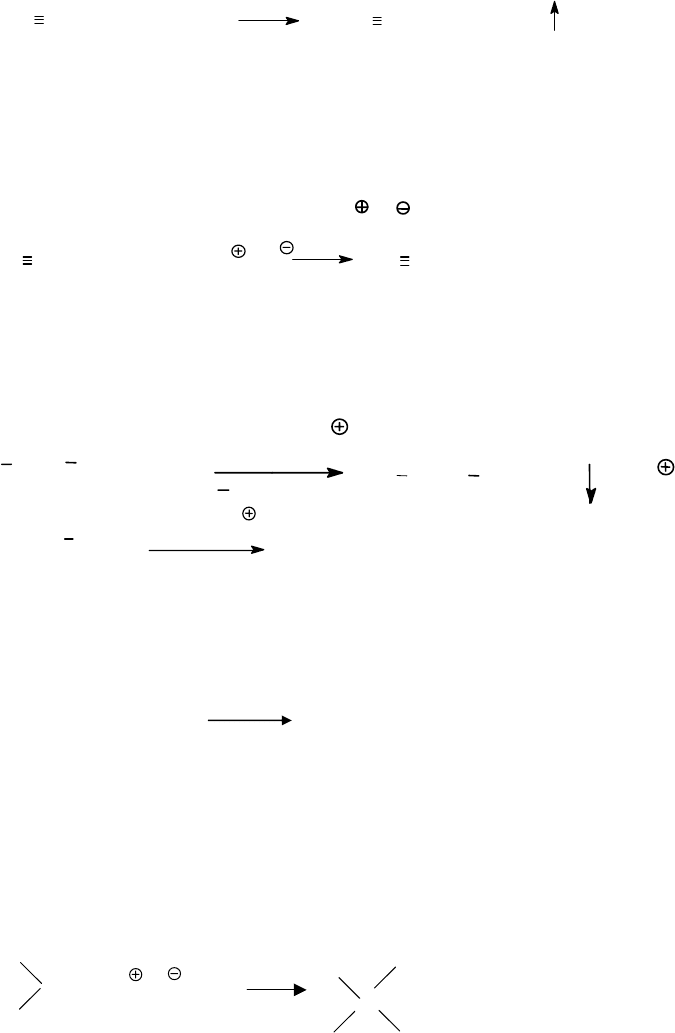
Карбид кальция
(
СаС
2
) является по существу ацетиленидом каль-
ция.
ацетиленид Na
N a
C C
N
a
+
H
2
N
a
НC
C N
a
1
/
2
117
Димагниевое производное ацетилена можно получить, пропуская
ацетилен в раствор магнийорганического соединения. CH
3
MgI
явля-
ется реагентом на подвижный водород, о наличии которого судят по
выделению метана (реакция Церевитинова):
+ 2
2
НC
H
C
C
H
3
M
g
I
I
M
g
C
C
M
g
I
+
C
H
4
3.3.5.3.2. Соединение алкинов с тяжелыми металлами
Практическое значение для идентификации алкинов имеют ацети-
лениды меди (I) или серебра. Они выпадают в виде осадков при про-
пускании ацетилена через аммиачные растворы соответственно хло-
рида меди (I) и нитрата серебра
[
M(NH
3
)
2
] OH, где
M= Ag, Cu (I).
+
2
НC H C
M C C M
+
[ M ( N H
3
)
2
] O H
2
H
2
O
Ацетилениды Cu
и Ag
устойчивы к действию воды, однако при
нагревании в сухом состоянии или при ударе они взрываются.
Эта реакция является качественной на концевую тройную связь.
Например, необходимо различить изомерные 1- и 2- бутины.
CH
3
-
C
≡
C
C
H
3
[
C
u
(
N
H
3
)
]
2
3.3.5.3.3. Реакции ацетиленидов
а) ацетилениды натрия с галогеналкилами образуют
гомологи
ацетилена.
HC
≡
CNa + CH
3
I HC
≡
C –CH
3
+ NaI
Только первичные алкилгалогениды ( R-CH
2
– Hal ) дают хорошие
выходы продукта замещения алкина; вторичные и третичные алкилга-
логениды при действии ацетиленид - иона подвергаются дигалогени-
рованию с образованием алкенов.
б) ацетилениды натрия и магния реагируют с альдегидами и ке-
тонами, образуя непредельные спирты (реакция Фаворского).
реакция не идет
Na
C
≡
CH
3
CH
CH
3
CH
3
C=O
+
H
2
O
+NaOH
CH
3
C
C
≡
CH
OH
δ
+
δ−
H
2
C H
3
C H
2
C
≡
CН
[
C
u
(
N
H
3
)
2
]
( N H
3
)
C
H
3
C
H
2
C
≡
C
Cu
+
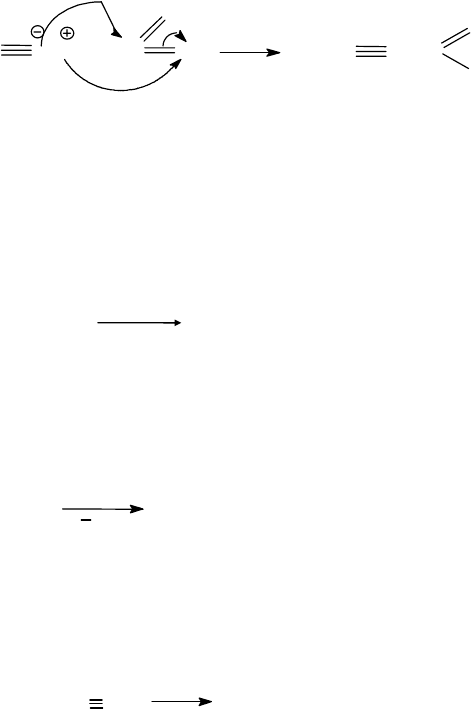
118
ххромовая
ккислота
в) при взаимодействии ацетиленидов с диоксидом углерода обра-
зуются соли карбоновых кислот, содержащих тройную связь:
3
CH -C CNa + C
O
O
δ
δ
-
+
CH -C C - C
3
O
ONa
3.3.5.3.4. Реакции окисления
По продуктам окисления можно установить положение тройной
связи в молекуле алкина. Окислители: хромовая кислота, перманганат
калия в кислой среде, озон. Продукты окисления – карбоновые кисло-
ты.
R - C
≡
C - R
1
R - СООН
+ R
1
- СООН
3.3.5.3.5. Реакции полимеризации
а) димеризация ацетилена протекает в присутствии хлорида меди (1)
в солянокислом растворе.
2НС
≡
СН
C
u
2
C
l
2
p
p
H
C
l
СН
2
= СН-
C
≡
C
H
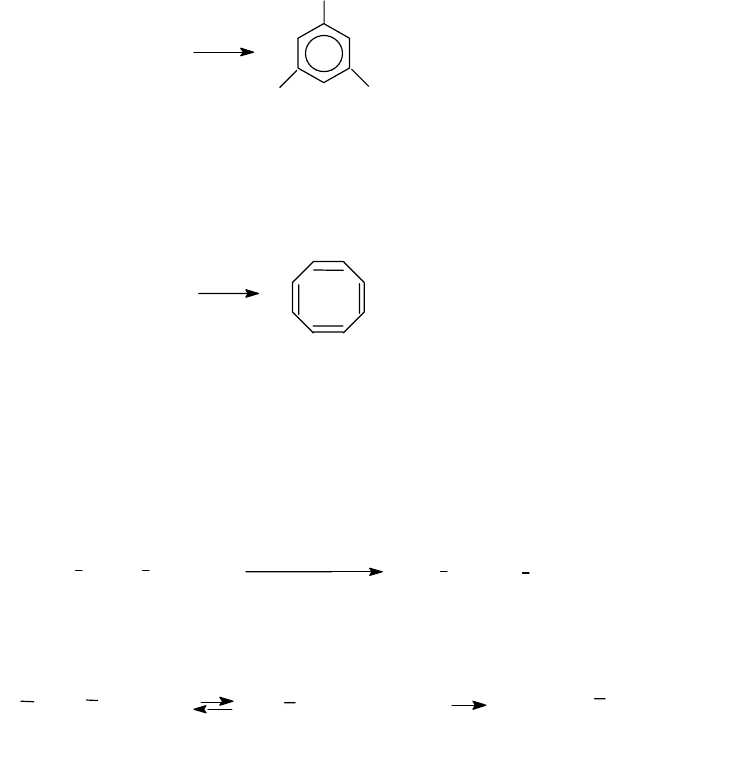
в) тримеризация ацетилена при 600-800
0
С осуществлена Бертло в
1861 г., выход бензола составил 30%. Н.Д.Зелинский предложил в ка-
честве катализатора активированный уголь:
3
C H CН
500
о
С
C
6
H
6
Использование катализатора Ni(CO)
2
[(C
6
H
5
)
3
P]
2
(В.Реппе) повы-
шает выход бензола до 80%, снижает температуру реакции до 60
о
С.
Гомологи ацетилена полимеризуются в более мягких условиях,
например, при действии серной кислоты:
винилацетилен
119
3 СH
3
– С
≡
СН
H
2
S
O
4
C
H
3
C
H
3
C
H
3
в) четыре молекулы ацетилена в присутствии Ni(CN)
2
при Р=20
МПа. и Т = 60
0
С образуют циклооктатетраен (Реппе, 1945):
3.3.5.3.6. Изомеризация алкинов
Ацетиленовые углеводороды
способны к изомеризации
с переме-
щением тройной связи или превращением в диеновые углеводороды.
а) перемещение тройной связи (А.Е.Фаворский, 1885г.):
C
H
3
C
H
2
C
≡
C
H
C
H
3
C
≡
C
C
H
3
C
2
H
5
O
N
а,170
0
С
N
a
б) превращение в диены (Я.М.Слободин):
3.4. Диеновые углеводороды (алкадиены)
3.4.1. Классификация диенов
Алкадиенами
называют углеводороды, содержащие две двой-
ные связи. Все диены по строению и химическим свойствам делят на 3
группы:
1) с кумулированными двойными связями (аллены):
R - CH = C = CH-R,
например СН
2
=СН=СН
2
-
аллен;
2) с изолированными двойными связями:
метилацетилен мезитилен
циклооктатетраен
C
H
3
C
H
2
C
≡
C
H
C
H
3
C
H
=
C
=
C
H
2
к
а
т
C
H
2
=
C
H
C
H=
C
H
2
алкин аллен
д
иен
4 HС
≡
СН

120
аллен п
р
опин
бутадиен-1,3 2-метилбутадиен-1,3 2-хлорбутадиен-1,3
(дивинил) (изопрен) (хлоропрен)
R - CH = CН - (CH
2
)
n
-CH = СН - R, n
≥
1;
3) с сопряженными двойными связями:
R - CH = CН – CH = СН-R
Аллены являются малоизученными соединениями. Известна спо-
собность алленов перегруппироваться в гомологи ацетилена при на-
гревании с металлическим натрием:
H
2
C=C=CH
2
CH
3
C
≡
CH
Диены с изолированными связями
по химическим свойствам ана-
логичны алкенам, т.к. двойные связями в них не оказывают друг на
друга существенного влияния.
Сопряженные диены представляют наибольший интерес в силу
особенностей строения и свойств, а также вследствие большой прак-
тической значимости. Остановимся на этой группе соединений под-
робнее.
3.4.2. Способы получения сопряженных диенов
Для получения сопряженных диенов можно использовать те же
методы, что и для синтеза алкенов. Мы рассмотрим лишь промыш-
ленные способы получения диенов, используемых в настоящее время
в качестве сырья для получения синтетических каучуков.
C H
2
= C H C H = C H
2
C H
2
= C C H = C H
2
СH
2
= С -СН = СН
2
C H
3
Сl
3.4.2.1. Синтез бутадиена-1,3 (дивинила)
Дивинил
получают в промышленности дегидрированием бутан-
бутеновой фракции, крекинг-газов (газы, выделяющиеся в процессе
крекинга нефти) при пропускании их при 650
о
С над катализатором из
оксида хрома (VI) и оксида алюминия.
C
4
H
10
C
4
H
8
CrO
3
/Al
2
O
3
650
o
C
CH
2
=CHCH=CH
2
б
у
тан
изомерные бутены
