Брунауер С. Адсорбция газов и паров
Подождите немного. Документ загружается.


СТРУКТУРА ПГ,р АДСОРБЕНТА '.'М
температуре
И
давлении неодинаковы. Следует отметить,
что адсорбируемость этих газов на других адсорбен-
тах различается не так сильно. Например, в случае
активного угля мы имеем отношение величин адсорб-
ции около 4:1. На шабазите это отношение возра-
стает в 15 раз.
Лэмб и Вудхауз предполагают, что расхождение
между отношениями 60 : 1 для частично обезво-
женного шабазита и 4 : 1 для активного угля имеет
место вследствие того, что размеры пор этих двух ад-
сорбентов неодинаковы. Если допустить, что в шаба-
зите газы могут проникать во все поры, в то время
как в активном угле наиболее тонкие поры достзшны
лишь малым молекулам, то эти последние, вообш,е
говоря, менее адсорбируемые молекулы будут отно-
сительно лучше адсорбироваться именно активным
углем. Но эти соображения могут лишь частично объ-
яснить отмеченное выше расхождение отношений вели-
чин адсорбции; главной же причиной являются, по-
видимому, не различные размеры доступной поверх-
ности, а неодинаковые теплоты адсорбции. Как будет
показано ниже, теплоты адсорбции газов на шаба-
зите приблизительно в два раза больше, чем на актив-
ном угле. Благодаря этому отношение адсорбируемо-
стей на шабазите составляет е^, или приблизительно
в семь раз больше, чем на угле. Остающееся еш,е рас-
хождение в два раза можно объяснить различной до-
ступностью пор по Лэмбу и Вудхаузу.
Другой интересной особенностью рис. 122 являет-
ся расположение максимумов кривых для трех га-
зов. Максимум адсорбции водорода соответствует де-
гидратации шабазита на 97,8%; соответственно для
кривой кислорода — на 96,9% и для кривой углекис-
лого газа — на 92,9%. Положение максимумов зави-
сит от двух взаимно противоположных эффектов де-
гидратации: удаление воды сопряжено с увеличением
внутренней поверхности, разрушение же структуры
сокращает поверхность. Если, как можно ожидать, в
первую очередь разрушаются стенки более грубых
пор, то раньше всего достигает максимума кривая

502 ГЛЛВЛ XI
адсорбции углекислого газа. При дегидратации свы-
ше чем на 92,9% продолжают открываться тонкие
поры, хотя более широкие поры начинают исчезать.
При дегидратации свыше чем на 96,9% начинают ис-
чезать поры, достаточно широкие для адсорбции кис-
лорода, но недоступные для углекислого газа; вме-
сте с тем продолжается образование более тонких пор.
Наконец, при дегидратации свыше чем на 97,8% на-
чинается разрушение наиболее тонких пор*.
Следует отметить, что вода, входящая в состав
частично дегидратированного шабазита, удерживается
несколько прочнее, так что водород, кислород и угле-
кислый газ не увлекают ее с собой при десорбции. В слу-
чае органических веществ дело обстоит иначе. Лэмб
и Оль[^®] нашли, что пары органических веществ при ад-
сорбции увлекают с собой некоторое количество воды.
Баррер[^^] определил изостерические дифферен-
циальные теплоты адсорбции азота, аргона и водорода
на шабазите по изотермам для интервала температур
от 104 до 237° К. Найденные им теплоты адсорбции
очень велики; вероятно, это самые высокие из изве-
стных теплот физической адсорбции. Совершенно так
же, 1^ак и в случае графита (гл. У1П), сначала диф-
ференциальные теплоты уменьшаются, по мере возра-
стания количества адсорбированного газа, а затем их
значения делаются постоянными, т. е. достигается не-
который предел. Однако в случае шабазита и началь-
ные и предельные величины тепловых эффектов в два
раза больше, чем для графита. Начальные теплоты
адсорбции азота, аргона и водорода составляют соот-
ветственно 8800, 6000 и 4000 кал/лшъ. По расчетам
де Бура и Кюстерса [1^] дисперсионная энергия ван-
дер-ваальсового взаимодействия в длинных цилинд-
рических каналах может быть в шесть раз больше, чем
*Ломб п Вест;»] исследовал!! эффект дегидратации М§'(0Н)2,
Са(0Н)2 и 2п(ОН)2По адсорбции закиси азота. Хотя пористость
этих веществ значительно меньше, чем шабазита, однако
полученные кривые очень похожи на изотермы рис. 122. Эти
кривые обладают максимумом, вероятно, по той же причине,
что и в случае шабазита.

СТРУКТУРА ПОР ЛДСОРБЕПТА 503
на плоской поверхности. И действительно, экспери-
ментально определенная начальная теплота адсорб-
ции азота на шабазите приблизительно в четыре раза
больше величины, вычисленной по уравнению Лон-
дона [уравнение (65), гл. VII]. Теплоты адсорбции
азота и аргона на графите незначительно отличаются
друг от друга (соответственно 4600 и 4100 кал!молъ)\
на шабазите они отличаются очень сильно. Веро-
ятно, что это тоже находится в связи с размерами
пор. Если ширина пор как раз достаточна для проник-
новения молекул азота, диаметр которых составляет
4,08 А, то атомы аргона с диаметром 3,83 А в резуль-
тате адсорбции располагаются ближе к одной стенке
и несколько удалены от противоположной. Это может
объяснить заметное снижение теплоты адсорбции ар-
гона, так как дисперсионная энергия падает пропор-
ционально кубу расстояния от стенки.
Лэмб и определяли интегральные теплоты
адсорбции многих паров на шабазите и тоже получили
значительно большие значения, чем при адсорбции
тех же паров на угле. Интегральные теплоты* адсорб-
ции углекислого газа, окиси азота, хлористого метила
и метил-эвого спирта составляют соответственно 12,41,
12,83, 13,47 и 23,32 ккал/люлъ, в то время как на угле
получено 7,7, 7,76, 7,18 и 14,3 ккал/молъ. Пары пере-
численных веществ адсорбируются в больших коли-
чествах, так как их молекулы достаточно малы*, чтобы
проникнуть в поры шабазита. Наоборот, этиловый
спирт и хлористый этил адсорбируются очень слабо;
их молекулы слишком велики и не могут проникнуть
в поры, и теплоты их адсорбции меньше, чем на
угле. Интегральные теплоты адсорбции этилового
спирта и хлористого этила на шабазите равны
9,27 и 11,06ккал/моль, а на угле—соответственно 16,4 и
13,49 ккал/молъ. Лэмб и Оль полагают, что адсорбция
этих двух паров протекает лишь на внешней поверх-
ности кристаллов шабазита.
* Эти величины представляют собой интегральную теплоту
адсорбции 1 моля газа на 500 а адсорбента.

54(5 ГЛАВА XI
Другие цеолиты не обладают такой замечательной
адсорбционной способностью, как шабазит. Имеется
три типа цеолитов: с трехмерной решеткой (шабазит,
анальцит), со слоистой структуре!"! (хеуландит) и с
волокнистым строе!шем (натролит, сколе!<ит). Бар-
рер[1^] изучал адсорбцию азота, аргона и водорода
на этих пяти цеолитах. Анальцит, дегидратированный
в вакууме при 330° в течение трех дней, адсорбирует
при температуре жидкого воздуха в пять раз меньше
азота, чем шабазит. Это означает, или что его поры
тоньше, чем в шабазите, или что кристаллическая
решетка анальцита пр!! 330° сильно разрушается. Теп-
лоты адсорбции на редкость постоянны для различных
количеств адсорбированного газа. Начальные и ко-
нечные дифференциальные теплоты для азота, аргона и
водорода соответственно равны 5500 и 5000, 3700 и
3300 и 1500 и 1400 кал]моль.
В слоистом кристалле хеуландита молекулы кри-
сталлизационно!! воды расположены между слоями.
Дегидратация происходит очень легко и сопровож-
дается сильным сокра1цением кристаллов в направ-
лении, перпендикулярном к плоскости слоев. Благо-
даря этому сокра1цению пространство между слоями
оказывается !!едоступным для адсорбируемых молекул
газа. Хеуландит, дегидратированный как полностью,
так и частично, адсорбирует ничтожные количества
азота и аргона. При дегидратации двух образцов цео-
литов волокнистого строения вода удаляется через
каналы, недоступные для молекул газов.
Вероятно, для всех адсорбентов в известной сте-
пени имеет место персорбция. Это обнаруживается при
определении величины поверхности по адсорбции мо-
лекул различных размеров. Так, Брунауер и Эммет[1®]
нашли, что поверхность силикагеля, определенная по
адсорбцпи бутана, на 22,5% меньше средней величины,
полученной по изотермам адсорбции пяти газов с
меньшими молекулами (аргон, азот, кислород, окись
углерода и углекислый газ). Для исследованного об-
разца угля получилось е1це большее различие, которое
составляло 34%. Хотя площадь, занимаемая бутаном

СТРУКТУРА ПГ,р АДСОРБЕНТА '.'М
на поверхности адсорбента, представляет собой вели-
чину несколько неопределенную, однако можно с уве-
ренностью утверждать, что как в угле, так и в оили-
кагеле имеется значительное количество пор слишком
тонких для того, чтобы в них могли проникнуть моле-
кулы бутана. Если определять поверхность адсорбен-
та, пользуясь рядом молекул различных размеров, то
можно оценить, какая часть поверхности соответ-
ствует порам с диаметром меньшим размеров каждого
рода применяемых молекул.
Объем пор адсорбента
Если адсорбент находится в сосуде, то сосуд со-
держит твердое вещество и пространство, заполнен-
ное воздухом. Манегольд[1^] делит это пространство
на три части: пустое пространство, капиллярное про-
странство и силовое пространство. Если объем про-
странства настолько велик, что силы, создаваемые
адсорбентом, действуют только на ничтожно малую
часть заполняющей его материи, то оно называется
пустым пространством. Слово «пустое» следует по-
нимать не в смысле отсутствия в нем вещества, а в
том смысле, что пространство свободно от действую-
щих сил. Такое пространство можно без затруднений
и заполнять и количественно эвакуировать. Если объем
пространства так мал, что силовое поле адсорбента
действует на большую часть вещества, находящегося
в этом пространстве, то оно называется капиллярным
пространством. Такое пространство может быть эва-
куировано только с трудом. И наконец, пространство
между атомами адсорбента и внутри атомов образует
«силовое пространство». Чтобы найти объем пор ад-
сорбента, надо уметь определять пустое пространство
и капиллярное пространство. Для силового простран-
ства это обычно не представляет затруднений.
Простой способ определения объема пор состоит
в погружении адсорбента в какую-либо жидкость, вы-
сушивании его зерен после отделения от жидкости и
взвешивании в тот момент, когда их поверхность
гоа
ГЛАВА XI
становится сухой. Если разделить увеличение веса ад-
сорбента на удельный вес жидкости, то получается
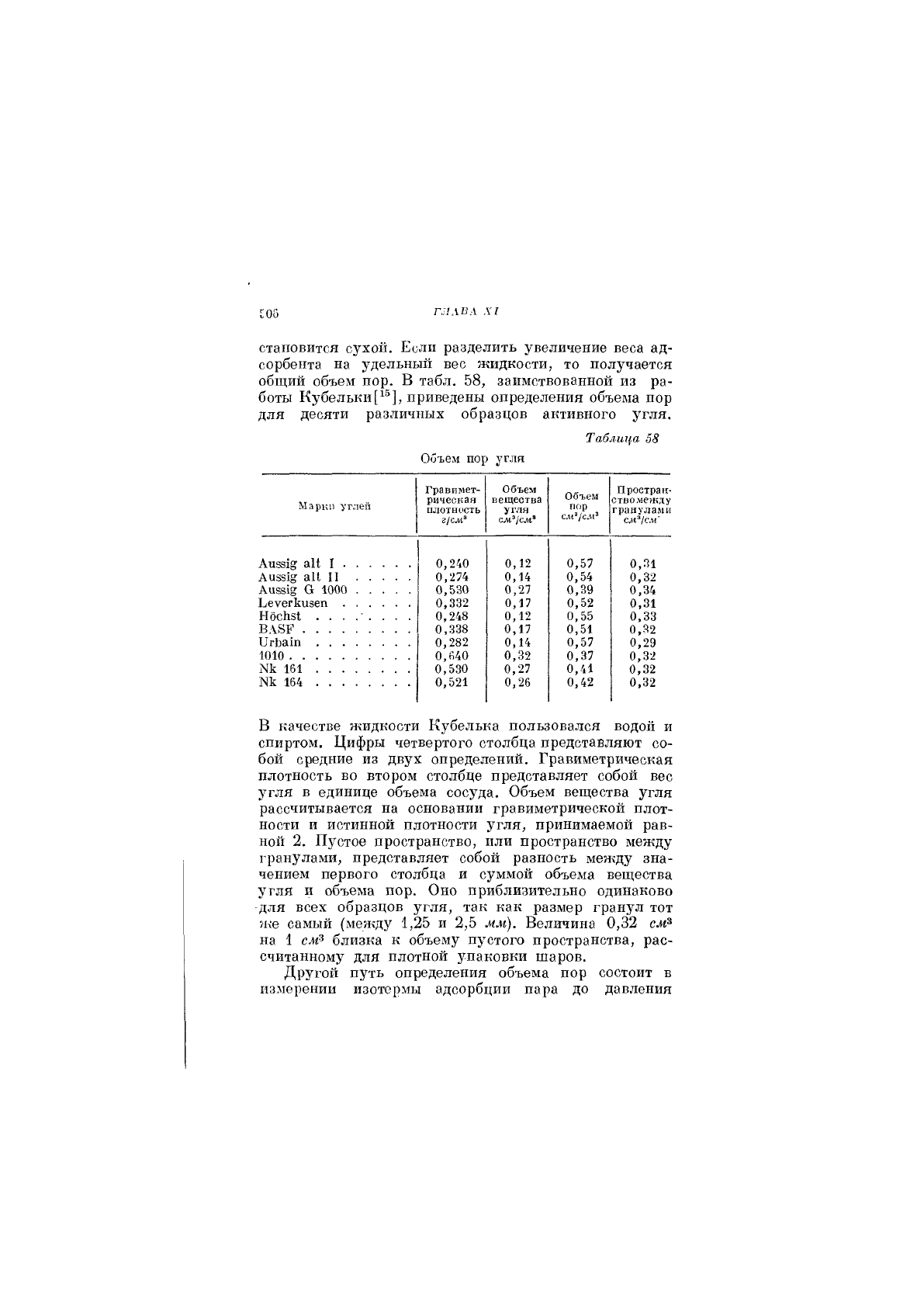
общий объем пор. В табл. 58, заимствованной из ра-
боты Кубельки[^®], приведены определения объема пор
для десяти различных образцов активного угля.
Таблица 58
Объем пор угля
Марки углей
Гравимет-
рическая
плотность
г/см"
Объем
вещества
угля
Аизз1§г аИ I .
Аизз!^ аИ II
Аиз818 О 1000
Ьеуегкизеп .
НбсЬз! . . .
ВЛ8Р ....
ПгЬаш . . .
1010
N15; 161 ...
Мк 164 ...
,240
,274
,530
,332
,248
,338
,282
,Й40
,530
,521
0,12
0,14
0,27
0,17
0,12
0,17
0,14
0,32
0,27
0,26
0,57
0,54
0,39
0,52
0,55
0,51
0,57
0,37
0,41
0,42
0,31
0,32
0,34
0,31
0,33
0,32
0,29
0,32
0,32
0,32
В качестве жидкости Кубелька пользовался водой и
спиртом. Циф1)ы четвертого столбца представляют со-
бой средние из двух определений. Гравиметрическая
плотность во втором столбце представляет собой вес
угля в единице объема сосуда. Объем вещества угля
рассчитывается на основании гравиметрической плот-
ности и истинной плотности уг.пя, принимаемой рав-
ной 2. Пустое пространство, или пространство между
гранулами, представляет собой разность между зна-
чением первого столбца и суммой объема вещества
угля и объема пор. Оно приблизительно одинаково
для всех образцов угля, так как размер гранул тот
же самый (между 1,25 и 2,5 мм). Величина 0,32 см^
на 1 см^ близка к объему пустого пространства, рас-
считанному для плотной упаковки шаров.
Другой путь определения объема пор состоит в
измерении изотермы адсорбции пара до давления

СТРУКТУРА ПГ,р АДСОРБЕНТА '.'М
насыщения. При давлении насыщения все поры адсор-
бента должны быть заполнены сжиженным паром, и
таким образом можно проверить величины объема
пор, найденные описанным выше методом погружения
углей в жидкость. Само собой разумеется, величины,
на11денные двумя разными методами, обычно не сов-
падают между собой. Для первых трех углей табл. 58
Кубелька получил на основании изотерм адсорб-
ции бензола объемы пор 0,196, 0,236 и 0,248 см^ на
1 ел® вместо соответствующих величин 0,57, 0,54 и
0,39. Это расхождение может быть объяснено, если
допустить, что объем пор распадается на две части —
капилляры и грубые некапиллярные поры и что ад-
сорбция происходит преимущественно в первых.
В первых трех образцах угля объем капилляров состав-
ляет соответственно 34, 44 и 64% от общего объема
пор. При точно 100-процентном насыщении заполняются
и наиболее широкие поры, но только если предоставить
достаточно времени для достижения равновесия. Со-
гласно уравнению Кельвина (гл. V), капилляры с
радиусами больше 0,15 ц заполняются бензолом лишь
при р1рд большем 0,99. Этот участок изотермы иссле-
довать очень трудно, и поэтому адсорбция при насы-
щении обычно находится экстраполяцией на основании
точек, полученных при немного меньших относитель-
ных давлениях.
Объем пор адсорбента принято разделять на ма-
кропоры и микропоры, что в буквальном переводе
означает большие поры и малые поры. Если эти две ч
группы пор резко различаются между собой, то полу-
чаются изотермы адсорбции, которые указывают, что
адсорбент почти нацело заполнен при давлениях пара'
значительно меньших, чем давление насыщения (ти-
пы I, IV и V), Если же провести границу между ма-
кропорами и микропорами трудно, то адсорбция вблизи '
точки насыщения неопределенно растет, и получаются
изотермы типов II и III.
В табл. 59 приведены объемы пор для двух углей и
двух силикагелей, определенные Вике[1®]. Общий объем
пор был определен погружением в бензол; объем

54(5
ГЛАВА XI
микропор — на основании изотермы адсорбции бензола.
Поскольку силикагель дает изотерму типа II, провести
границу между макро- и микропорами невозможно.
Таблица 59
Величины объема пор угля и силикагеля
Вещество
м
а а
и ая
ео «5
с;
КЗв
Я8-.
5 а
й>
Ш
„
«5
?
2 а
У
§э|
а
о
о о
а"
к
Ч
о
со
"
О
3
&
О
а»
X
^
10 Н ^^
О 8
Уголь КА . . . .
0,36 0,55 1,81
0,55
1,27
0,60
0,67
Уголь КВ . . . . 0,53 0,89
2,08 0,48
0,65 0,41
0,24
Силикагель Е . . 0,85
1,10
2,38 0,42
0,49 0,35
0,14
Силикагель . .
0,47
0,76 2,28
0,44
0,87
—.
На основании изотерм адсорбции, полз'ченных для
трех других адсорбентов, Вике рассчитал по уравне-
нию Кельвина, что все их микропоры обладают ра-
диусами менее 30 к, причем средний радиус прибли-
зительно равен 10 А, Радиус наименьших микропор
составляет около 0,1 ц, а средний радиус, по его оцен-
ке, — около 1 ц. Исходя из этих данных, можно рас-
считать внутреннюю поверхность микропор и макро-
пор. Поверхность шара равна ЗУ/г, а боковая поверх-
ность цилиндра равна 2У/г. Вике принимает, что внут-
реннюю поверхность пор можно выразить формулой
(1)
где V — объем пор, а г — их средний радиус. Если
значения V взять из двух последних столбцов табл. 59,
то для г=10~'' в случае микропор и для г:=10~*
в случае макропор получается поверхность микропор от
900 до 1500 м^/г и поверхность макропор от 0,35 до
1,7 ж^/г. Этот приближенный расчет порядка неличин
показывает, что адсорбция на поверхности макро-
пор ничтожна по сравнению с адсорбцие!! в микро-
порах. Однако это не значит, что макропоры не иг-
рают никакой роли при адсорбции. Значение их очень
велико, так как они определяют скорость адсорбции.

СТРУКТУРА ПГ,р АДСОРБЕНТА
'.'М
В гл. XIII будет показано, что в длинных и очень
тонких порах адсорбция проте1?ает медленно. Если
поры с большим диаметром чередуются с тонкими по-
рами, то путь, проходимый молекулами в микропорах,
сокращается, и скорость адсорбции возрастает.
В случае изотерм типов II и III размер пор 5'ве-
личивается непрерывно, и по мере приближения к
насыщению заполняются все более и более широкие
поры. Таким образом, в данном случае макро- и микро-
поры не образуют двух резко разделенных систем, а
постепенно переходят одни в другие. Именно этим,
конечно, можно объяснить тот факт, что Бахман[1']
получил одинаковые объемы пор нескольких образ-
цов силикагеля как погружением в жидкость, так и
измерением адсорбции паров в точке насыщения. Из
табл. 60 видно, как хорошо совпадают результаты
Таблица 60
Общий объем пор силикагелей
Гель
номер
Применяемая
жидкость
Метод опре-
деления
Общий объем
пор {смЧсм"}
СНС1з
СНС1з
П1р
пар
пар
0,374
0,377
0,374
5 н,о
СеНе
пар
пар
0,426
0,4-20
2
Н^О
н,о
С2Н,ВГ4
Н^о'
?кидкость
пар
пар
жидкость
пар
0,564
0,561
0,562
0,5С0
0,560
анализов по этим двум методам и как точно сходятся
объемы пор, определенные с помощью различных жид-
костей и паров для одного и того же образца силикагеля.
Вместе с тем все три образца заметно отличаются друг
от друга по общим объемам пор.
54(5
ГЛАВА XI
В обсуждавшихся работах Кубелькп['®], В11ке[1''1
и Бахмана["] размеры микро- и макропор были опре-
делены неточно. В настоящее время микропорамп
называются поры с радиусами меньше 100 А. Раби-
нович и Фортунатов
[1®]
определяли изотермы адсорб-
ции паров воды на многих веш,ествах и рассчитывали
по уравнению Кельвина количество паров, адсорби-
рованных в капиллярах с радиусами, меньшими 10~®сл.
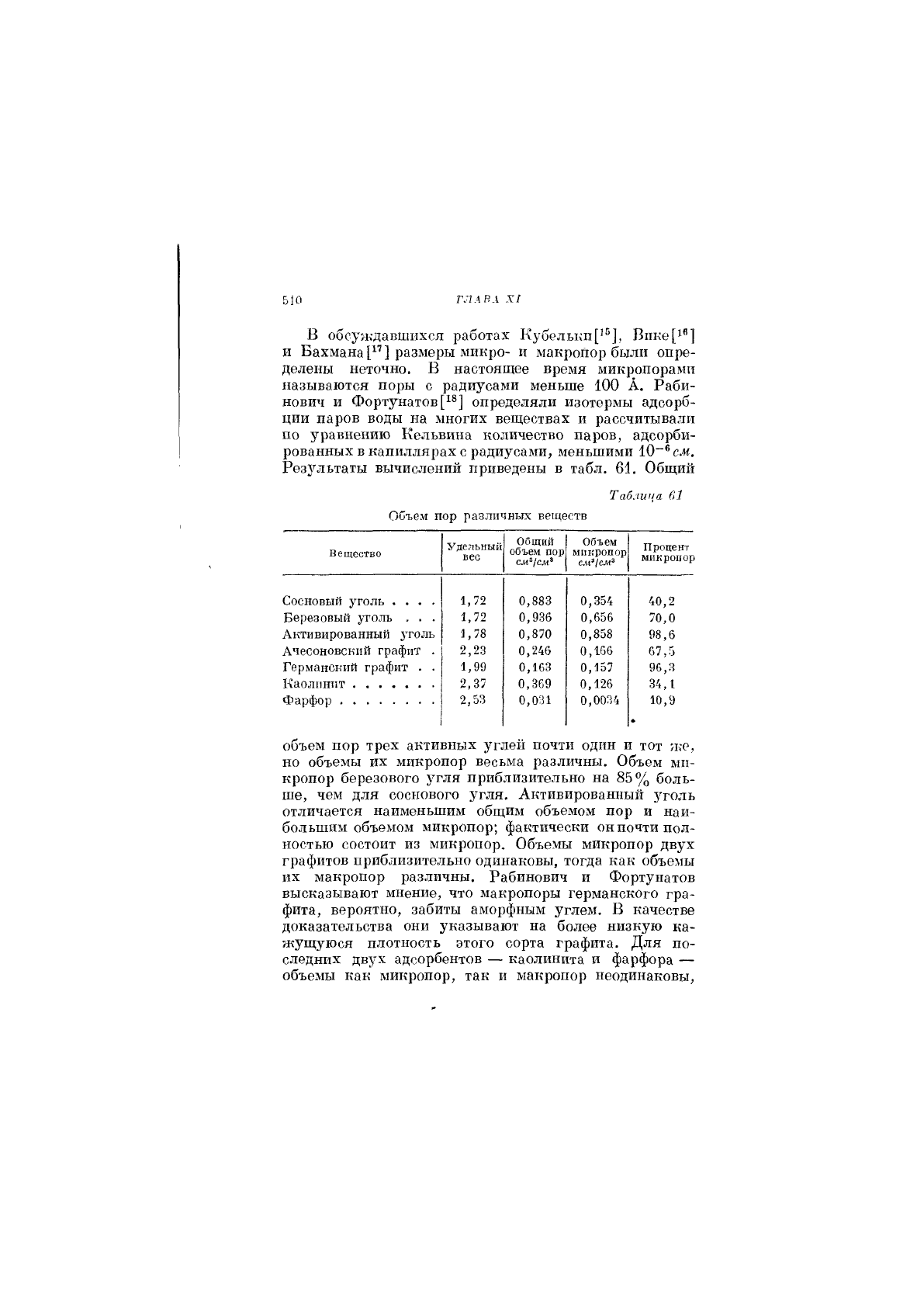
Результаты вычислений приведены в табл. 61. Общий
Таблица 61
Объем пор различных веществ
Вещество
Удельный
вес
Общий
объем пор
см^/см^
Объем
микропор
смЧсм'
Процент
микропор
Сосновый уголь ....
1,72
0,883
0,354 40,2
Березовый уголь . . .
1,72
0,936 0,656
70,0
Активированный уголь
1,78
0,870
0,858
98,6
Ачесоновский графит . 2,23
0,246 0,166
67,5
Германский графит . . 1,99 0,163
0,157
96,3
Каолинит 2,37
0,369 0,126 34,1
Фарфор
2,53
0,031 0,0034
10,9
•
объем пор трех активных углей почти один и тот же,
но объемы их микропор весьма различны. Объем мп-
кропор березового угля приблизительно на 85% боль-
ше, чем для соснового угля. Активированный уголь
отличается наименьшим обш,им объемом пор и наи-
большим объемом микропор; фактически он почти пол-
ностью состоит из микропор. Объемы микропор двух
графитов приблизительно одинаковы, тогда как объемы
их макропор различны. Рабинович и Фортунатов
высказывают мнение, что макропоры германского гра-
фита, вероятно, забиты аморфным углем. В качестве
доказательства они указывают на более низкую ка-
жущуюся плотность этого сорта графита. Для по-
следних двух адсорбентов — каолинита и фарфора —
объемы как микропор, так и макропор неодинаковы,
