Брунауер С. Адсорбция газов и паров
Подождите немного. Документ загружается.

ИЗОТЕРМА АДСОРБЦИИ II
1
есть 5
плотность вещества в газовой фазе,
аV — ^, где Ж—молекулярньШ вес адсорбируемого
вещества. Для вычисления этого интеграла нужно вы-
разить молярный объем V пли плотность 5 как функ-
цию давления в газовой и адсорбционной фазах. Хотя
Газовая фаза
Лдсорбциттп^
простри/,-ст^о
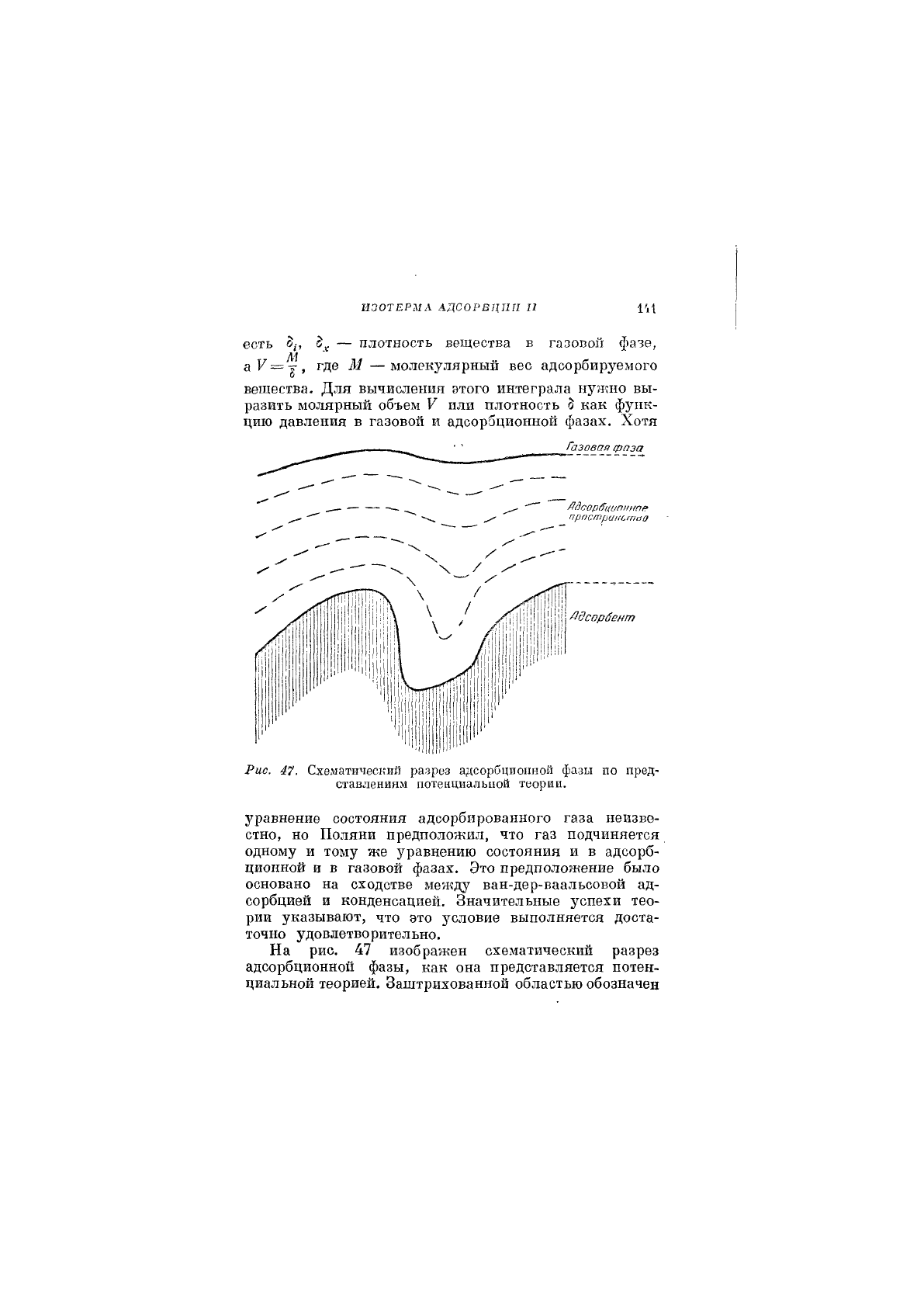
Рис. 47. Схематический разрез адсорбционной фазы по пред-
ставлениям потенциальной теории.
уравнение состояния адсорбированного газа неизве-
стно, но Поляни предположил, что газ подчиняется
одному и тому же уравнению состояния и в адсорб-
ционной и в газовой фазах. Это предположение было
основано на сходстве между ван-дер-ваальсовой ад-
сорбцией и конденсацией. Значительные успехи тео-
рии указывают, что это условие выполняется доста-
точно удовлетворительно.
На рис. 47 изображен схематический разрез
адсорбционной фазы, как она представляется потен-
циальной теорией. Заштрихованной областью обозначен

142 ГЛАВА III
адсорбент; сплошная линия является поверхностью
раздела между газовой фазой и адсорбционной фазой,
а пунктирными линиями обозначены эквипотен-
циальные поверхности. Потенциал на поверхности
адсорбента можно обозначить через 30, а потенциалы на
последовательных эквипотенциальных поверхностях-—
через г,, г^,..., г^-,... и т. д. Предполагается, что ад-
сорбционный потенциал, подобно гравитационному по-
тенциалу, на 1-й поверхности всегда равен г,-, незави-
симо от числа и вида молекул, находящихся между
1-й поверхностью и адсорбентом или газовой фазой.
Это предположение, позднее получившее полное под-
тверждение в квантово-механической теории ван-
дер-ваальсовых сил Лондона["], будет рассмотрено в
в гл. VII.
Между каждой из эквипотенциальных поверхностей
и поверхностью адсорбента заключен некоторый объем.
Обозначим эти объемы через ср^, ср^,..., ср,-,... и т. д.
Объем, заключенный между поверхностью адсорбента
и поверхностью раздела газовой и адсорбционной фаз,
равен (Смаке, и является объемом всего адсорбционного
пространства. Потенциал на наружной поверхности
этого объема равен нулю. На поверхности адсорбента,
где
ср
= 0, потенциал достигает своего максимального
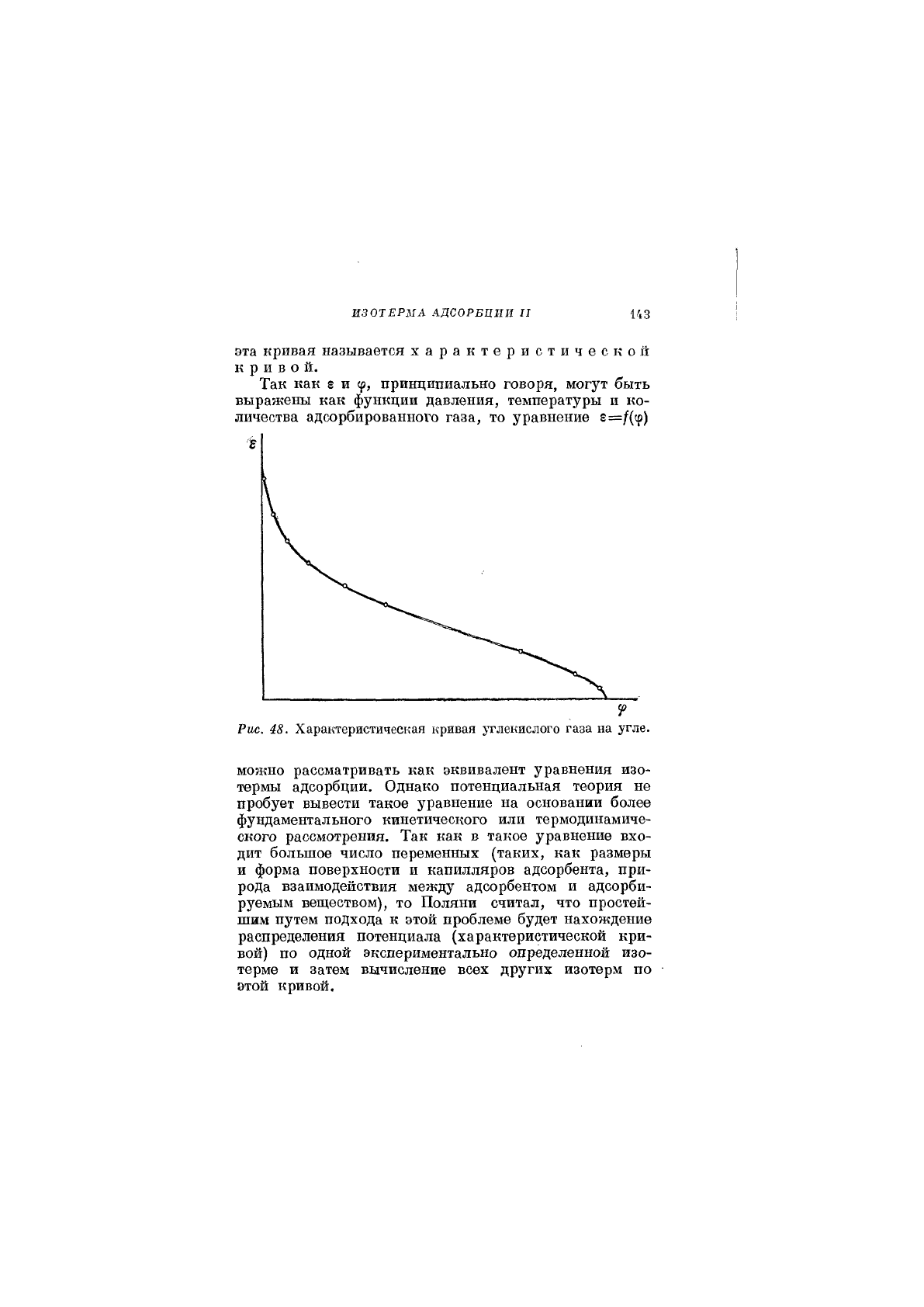
значения гц. Характер кривой 5=/(ср) между этими
крайними значениями показан на рис. 48. Кривая рас-
считана Поляни[1] по данным Титова для адсорб-
ции углекислого газа на угле.
Потенциальная теория предполагает, что адсорб-
ционный потенциал не изменяется с температурой:
Л,.
= (2)
откуда следует, что
2 = 0. (3,
Это означает, что кривая, представляющая распре-
деление потенциала в адсорбционном пространстве,
т. е. г =/(?), одинакова для всех температур. Поэтому
ИЗОТЕРМА АДСОРБЦИИ II 143
эта кривая называется характеристической
кривой.
Так как г и ф, принципиально говоря, могут быть
выражены как функции давления, температуры и ко-
личества адсорбированного газа, то уравнение г—/((р)
Рис. 48. Характеристическая кривая углекислого газа на угле.
можно рассматривать как эквивалент уравнения изо-
термы адсорбции. Однако потенциальная теория не
пробует вывести такое уравнение на основании более
фундаментального кинетического или термодинамиче-
ского рассмотрения. Так как в такое уравнение вхо-
дит большое число переменных (таких, как размеры
и форма поверхности и капилляров адсорбента, при-
рода взаимодействия между адсорбентом и адсорби-
руемым веществом), то Поляни считал, что простей-
шим путем подхода к этой проблеме будет нахождение
распределения потенциала (характеристической кри-
вой) по одной экспериментально определенной изо-
терме и затем вычисление всех других изотерм по
этой кривой.
144
ГЛАВА III
В гл. IV было показано, что уравпс-пие Лэнг-
мюра может быть проверено по трем критериям: 1) удо-
влетворяют ли уравнению экспериментальные данные,
2) имеют ли константы уравнения, представляющие
собой независимо измеряемые физические величины,
подходящие значения, 3) хорошо ли воспроизводит
Кривая 1
4
^^ривой 3
(ириааи 2)
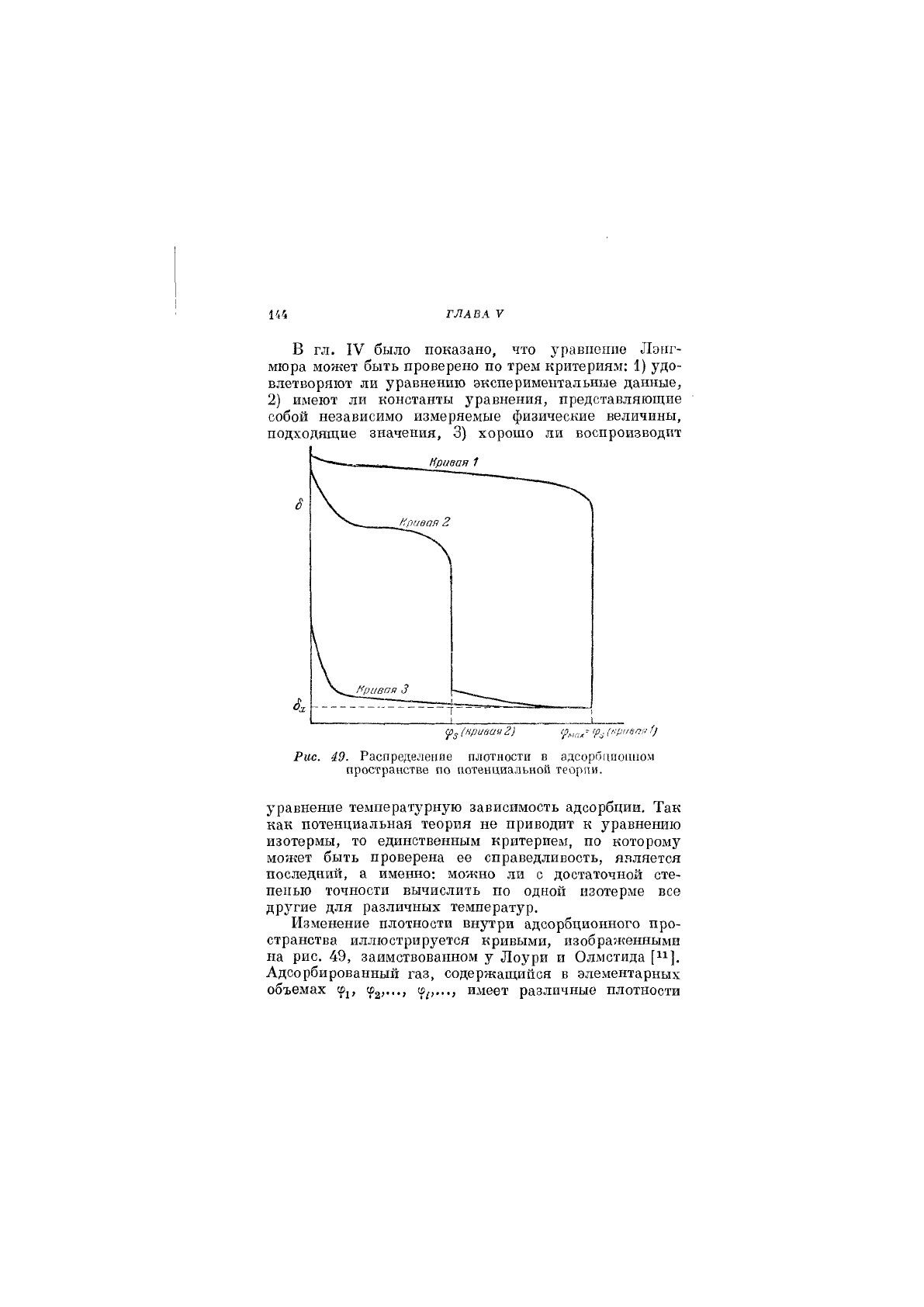
Рис. 49. Распределение плотности в адсорбцпошюм
пространстве по потенциальной теории.
уравнение температурную зависимость адсорбции. Так
как потенциальная теория не приводит к уравнению
изотермы, то единственным критерием, по которому
может быть проверена ее справедливость, является
последний, а именно: можно ли с достаточной сте-
пенью точности вычислить по одной изотерме все
другие для различных температур.
Изменение плотности внутри адсорбционного про-
странства иллюстрируется кривыми, изображенными
на рис. 49, заимствованном у Лоури и Олмстида [11].
Адсорбированный газ, содержащийся в элементарных
объемах (р^..., имеет различные плотности

ИЗОТЕРМА АДСОРБЦИИ II 145
др Ь^,..., Ьр... Максимальной плотностью он обладает
на поверхности адсорбента, минимальной — в непо-
средственной близости от газовой фазы. Последняя,
дд., равна плотности газа. При температуре ниже кри-
тической в части адсорбционного пространства плот-
ность равна или больше плотности жидкости; объем
этой части адсорбционной области обозначим (р^. Фор-
ма кривой резко зависит от температуры и дав-
ления. Кривая 1, изображенная на рис. 49, характе-
ризует состояние при температуре намного ниже кри-
тическо11 и при давлении, близком к насыщенному.
В этом случае практически весь адсорбционный объем
заполнен жидкостью, так что !р^=(рмако. Другой крайний
случай дается кривой 3, представляющей распреде-
ление плотности газа при температуре намного выше
критической. Здесь плотность адсорбционного слоя
нигде не достигает плотности жидкости. Кривая 2
показывает промежуточное состояние, при котором
часть адсорбированного вещества находится в жидком
состоянии, а часть — в газообразном. Здесь, даже
если ср^ меньше половины (рмако.. большая часть адсорби-
рованного вещества сосредоточена в так как плот-
ность вещества в этом объеме много выше, чем в
остальном.
Масса адсорбированного газа может быть получена
путем интегрирования (5—в пределах от
О
до (рмакс.:
"Гмакс.
Ж— ^ — З^Шмакс.. (4)
О
Поправочным членом §^(рмано. обычно можно прене-
бречь, исключая случаи очень высоких давлений (ког-
да становится большим) и высоких температур (когда
д становится малым). Для того чтобы произвести
интегрирование, надо знать зависимость д от Как
будет показано далее, эта зависимость может быть
получена с помощью характеристической кривой и
уравнения состояния газа.
10 с. Брунауер

146 ГЛАВА III
Приложения потеицнальиой теории
Проверка теории состоит из двух стадий: вычисле-
ние характеристической кривой из эксперилюнтальной
изотермы и вычисление других изотерм по характери-
стической кривой. Изотерма, применяемая для опре-
деления характеристической кривой, должна покры-
вать распределение потенциала во всем адсорбцион-
нолр пространстве. Так как участки с низкими зна-
чениями потенциала заполняются только при низких
температурах, то для вычисления следует пользоваться
изотермой для температуры ниже критической.
С другой стороны, температура, при которой изме-
рена изотерма, не должна быть слишком низкой, так
как в этом случае большая часть адсорбционного про-
странства заполняется при очень низких давлениях
и область высоких потенциалов не может быть оце-
нена с достаточной степенью точности. Если подобная
идеальная изотерлш не может быть получена практи-
чески, то характеристическая кривая должна быть
вычислена из двух или более изотерм.
Первые вычисления произвел Поляни[1], но Бе-
рени[1^. 1®] значительно усовершенствовал метод рас-
чета. Оба автора различают три различных метода
расчета: 1) для изотерм при температурах значитель-
но ниже критической, у которых практически весь
адсорбированный газ находится в жидком состоянии;
2) для изотерм при температурах хотя и ниже, но
приближающихся к критической. В этом случае в
адсорбционном пространстве, кроме жидкости, имеется
также и сжатый пар в количествах, которыми нельзя
пренебречь; 3) для изотерд! при температурах выше
критической, для которых в адсорбционном простран-
стве имеется только сжатый газ. Три кривых на рис. 49
соответствуют этим трем различным распределе-
ниям плотности вещества в адсорбционном простран-
стве.
Вычисление характеристической кривой по изо-
терме для температуры значительно ниже критической
является простейшим. В первом приближении потен-

ИЗОТЕРМА АДСОРБЦИИ II 147
цпал вычисляется на основании двух предположений:
1) пар в газовой фазе подчиняется законам идеальных
газов; 2) жидкость в адсорбционной фазе несжимаема.
При этом г,, является просто работой изотермического
сжатия идеального газа от давления р^ в газовой фазе
до—давления насыщенного пара над жидкостью.
В этом сл5^чае уравнение (1) принимает вид:
(5)
Рх
Следует отметить, что в этом выражении мы пре-
небрегли работой образования поверхности жидкости.
Если даже эта работа не исчезающе мала по сравне-
нию с г^, то ошибка, вводимая этим допущением в
вычисления, все же не очень велика.
Так как по допущению жидкость несжимаема, то
значение соответствующее г^, выражается просто
уравнением
где
X
— масса адсорбированного пара, а — плотность
жидкости при температуре Т. Каждой паре значе-
ний X и р^, т. е, каждо11 точке изотермы адсорбции,
соответствует пара значений и г^, т. е. точка харак-
теристической кривой.
Второе приближение заключается во внесении по-
правок в величину ср^ — на сжимаемость адсорбиро-
ванной жидкости, и в величину — на отклонения
пара от законов идеальных газов. Берени внес
эти поправки простым эмпирическим путем. Если бы
жидкость была несжимаема и не расширялась с тем-
пературо!!, то мы имели бы
= (7)
где Ьв — плотность нормальной жидкости в точке
кипения. Чтобы получить изменение 5 с давлением и
с температурой, необходимо ввести две поправки.
10^

148
ГЛАВА III
Поправка на сжимаемость более трудна, так как для
этого надо из всех возможных распределений потен-
циала в адсорбционном пространстве избрать какое-
нибудь одно, а также принять определенное значение
для 5„ — адсорбционного потенциала на поверхности
адсорбента. Приняв значение 5о=6000 кал и допу-
ская линейное уменьшение г с ростом ср, Берени вы-
числил, по измерениям Амага, для эфира поправки
на сжимаемость /ц, приведенные в табл. 5 (а). В пер-
вом столбце ЭТ011 таблицы даны отношения температур,
соответствующих изотермам, к температуре кипения
в последующих столбцах приведены коэффициен-
ты /д, на которые нужно умножать й^» чтобы получить
среднюю плотность адсорбционного слоя, когда дав-
ление в газовой фазе равно р^.
Таблица 5
Поправки для Ед
а) Поправка на ссисимаемость
Т/Т^
1 10
100
1000 мм
Нё
0,6
1,01
1,02
1,03
0,8
1,01 1,02 1,03
1,04
—
1,0
1,01
1,03 1,05 1,07 1,09
1,2
1,01 1,04 1,07 1,10 1,12
1,4
1,01
1,05 1,09 1,13
1,15
Ь) Поправка на температурное расширение /
Т/Т^
0,й
1,16
0,8
1,10
1,0 1,00
1,2 0,89
1,4
0,74

ИЗОТЕРМА АДСОРБЦИИ. II
с) Общая поправка /
149
г/г^.
1 10
100
1000 мм
нз
0,6
0,8
1,0
1,2
1,4
1,17
1,11
1,01
0,90
0,75
1,18
1,12
1,03
0,93
0,79
1,19
1,13
1,05
0,96
0,83
1,14
1,07
0,99
0,87
1,09
1,01
0,90
Если значение недоступно и известно только
то из табл. 5 (Ь) могут быть получены поправки
/у на температурное расширение адсорбционного слоя-
Эти поправки Беренп вычислил, усредняя температур-
ное расширение двенадцати различных жидкостей. Он
нашел, что ни у одной из жидкостей расширение не
отклоняется от приведенных данных более, чем на
2—3%. Чтобы получить надо умножить на /у.
Наконец, полный поправочный множитель / приве-
ден в табл. 5 (с). Таким образом, исправленное зна-
чение (р^ выражается так:
(8)
X X
Благодаря тому, что при соответственных темпе-
ратурах сжимаемости и тепловые расширения различ-
ных жидкостей весьма схожи, поправочные множи-
тели применимы для всех жидкостей с ошибками, не
превышающими нескольких процентов.
Поправки к вносимые на отклонения пара от
законов идеальных газов, совершенно незначительны
вплоть до температур, близких к критической. Бе-
рени выражает их в следующей форме:
(9)
И при !Г/Гд==1,4 значение едва превышает 100 кал.
Это составляет лишь несколько процентов от г^. Для
значений Т/Тд=1,0; 1,2 и 1,4 Берени дает для зна-
чения 0; 46 и 137 кал соответствен^Юс
150
ГЛАВА III
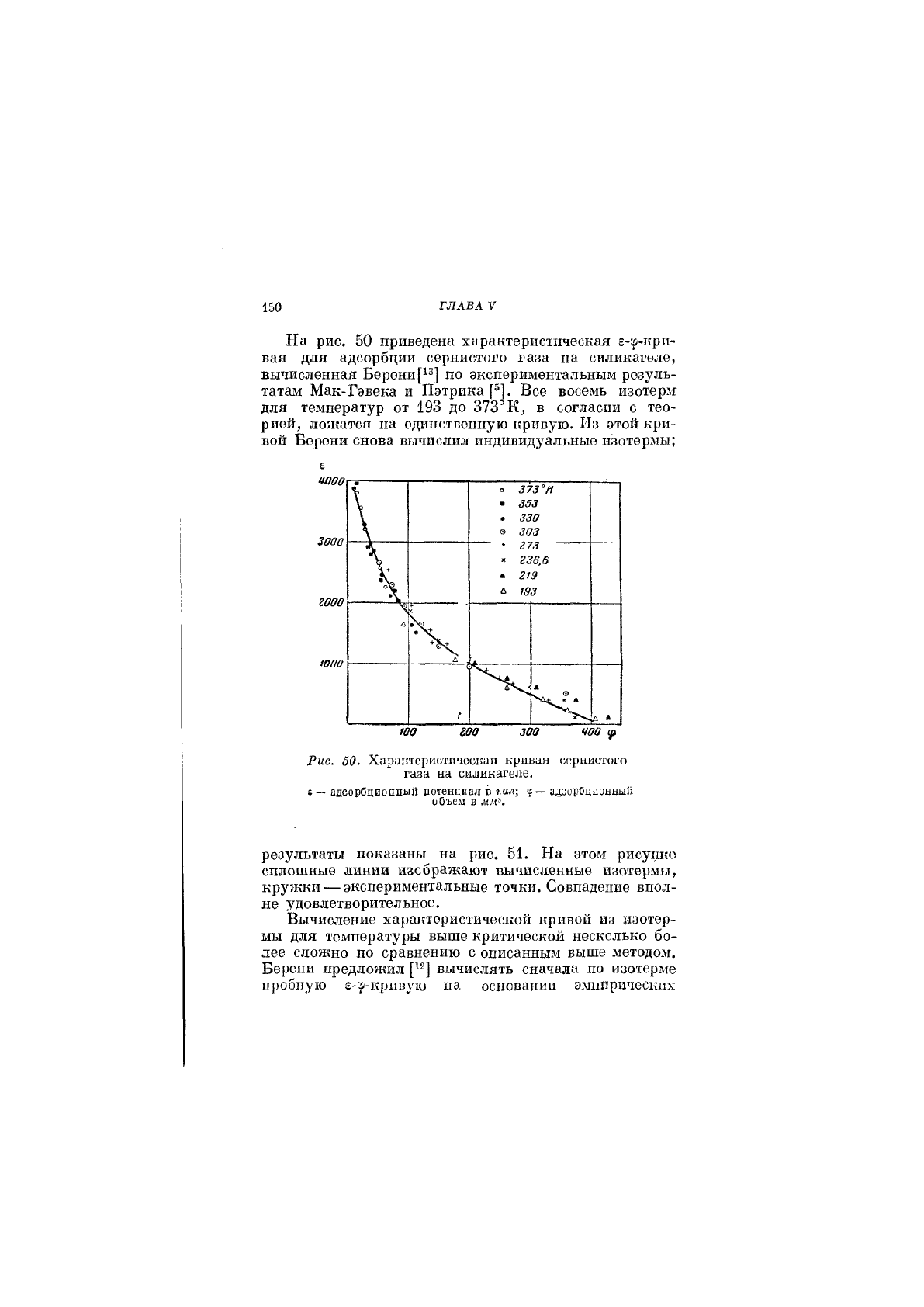
На рис, 50 приведена характеристическая г-:р-кри-
вая для адсорбции сернистого газа на силикагеле,
вычисленная Берени[1®] по экспериментальным резуль-
татам Мак-Гэвека и Пэтрика Все восемь изотерм
для температур от 193 до 373° К, в согласии с тео-
рией, ложатся на единственную кривую. Из этой кри-
вой Берени снова вычислил индивидуальные изотермы;
гооо
таи
400
Рис. 60. Характеристическая кривая сернистого
газа на силикагеле.
6 — адсорбционный потенциал в га-ц
1}
— азсорОцпонный
о Оъеы Б
результаты показаны на рис. 51. На этом рисунке
сплошные линии изображают вычисленные изотермы,
кружки — экспериментальные точки. Совпадение впол-
не удовлетворительное.
Вычисление характеристической кривой из изотер-
мы для температуры выше критической несколько бо-
лее сложно по сравнению с описанным выше методом.
Берени предложил вычислять сначала по изотерме
пробную 5-^-крпвую на основании эмпирических
