Вафин Д.Б. Задания по физике
Подождите немного. Документ загружается.

Решение:
F
тр
=
l
М
2
2
=
50
2
173000
2
= 8670 H.
Знак «» показывает, что сила направлена противоположно ско-
рости движения.
Проверяем условие
g
l2
2
0,29,8 = 1,96
502
17
2
= 2,89.
Отсюда видно, что
g <
l2
2
.
Поэтому груз будет скользить по днищу кузова.
W
к
=
4
3
2
m
=
4
17503
2
= 10837 Дж.
N =
R
l
2
=
34,02
50
= 23,4.
Ответ:
Результирующая сила торможения, действующая на автомобиль
во время торможения : F
тр
= 8670 Н.
Сила трения, действующая на груз со стороны днища кузова ав-
томобиля, меньше, чем сила, необходимая для обеспечения одинако-
вого с автомобилем ускорения торможения. Поэтому груз, находя-
щийся в кузове автомобиля во время торможения будет скользить по
днищу, пока не упрется о передний борт.
Кинетическая энергия одного колеса автомобиля до начала тор-
можения: W
к
= 10837 Дж.
До полной остановки колеса автомобиля сделают N = 23,4 оборо-
та.
1.3. Задания для самостоятельной работы по механике
Задание 1.
Координата материальной точки массы m, движущейся по оси
x изменяется по закону: x=a + bt + ct
2
+ dt
3
. Определить путь, прой-
денный в промежутке времени от t
1
до t
2
, среднюю скорость и среднее
ускорение на этом промежутке, силу, действующую на частицу в дан-
ные моменты времени. Постройте графики изменения координаты
частицы, скорости и ускорения в зависимости от времени в промежут-
ке от t = 0 до t = t
2
.
20

Таблица с исходными данными для задания 1
№ вар.
m, г a, м b, м/с c, м/с
2
d, м/с
3
t
1
, с t
2
, с
1 1 1 2 -3 1 2 6
2 2 -2 1 2 -0,5 3 7
3 3 3 3 1 -0,9 4 8
4 4 4 4,2 -1 0,4 4 7
5 5 -5 2,5 2 -0,8 3 5
6 6 6 1,6 -3 -0,6 3 6
7 7 7 1,7 -2 1,7 2 7
8 8 8 -0,8 -1 1,8 4 8
9 9 9 1,9 -0,9 -0,3 4 9
10 10 10 5 -2 -0,5 5 10
11 11 -11 1,1 -3 0,5 2 6
12 12 12 1,2 -2 -0,4 3 8
13 13 13 1,3 -1 2 3 7
14 14 -14 4 -2 1,4 4 9
15 15 1,5 5 1,5 -0,9 5 9
16 16 1,6 0,6 -1,6 0,6 2 6
17 17 1,7 1,7 7 -1,7 3 7
18 18 1,8 -1,8 1,8 0,8 4 8
19 19 1,9 0,9 1,9 -1,9 3 9
20 20 2,0 2 -2 1 2 7
21 21 2,1 2,1 -1,2 -0,1 1 5
22 22 2,2 2 -2,2 1,2 2 6
23 23 2,3 3 -1,3 -0,3 3 9
24 24 2,4 4 -2,4 1,4 4 8
25 25 2,5 2,5 -2,5 1 5 9
26 26 2,6 6 3 -2,6 2 6
27 27 2,,7 0,7 7 -3 3 7
28 28 2,8 2,8 2 -2,8 2 8
29 29 2,9 0,9 1,9 -0,9 4 9
30 30 3,0 3 -1,3 -0,3 3 7
31 31 3,1 1,3 -3,1 -0,6 2 6
32 32 3,2 2 -1,5 -0,7 3 8
21
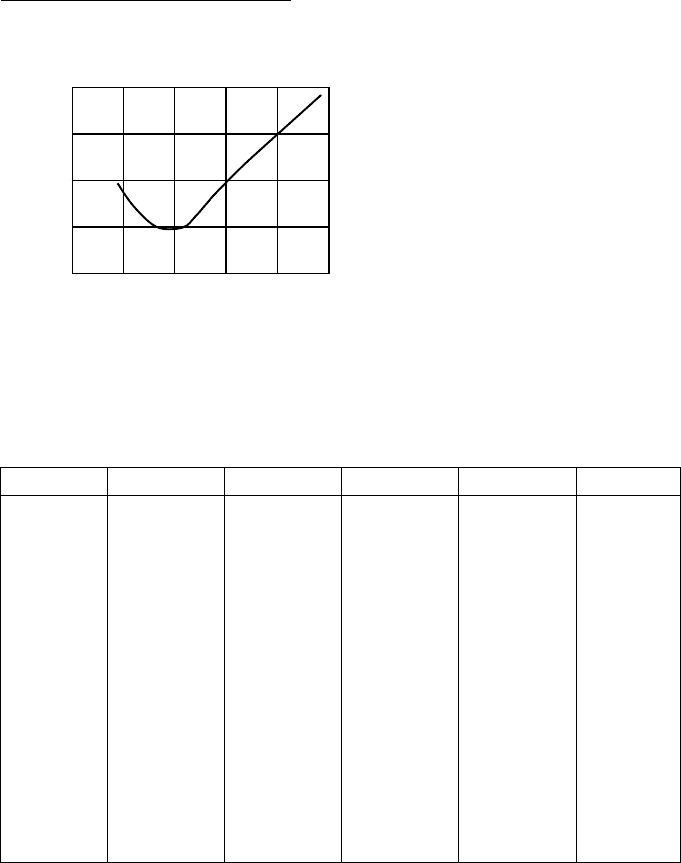
Задание 2. Нечетные варианты
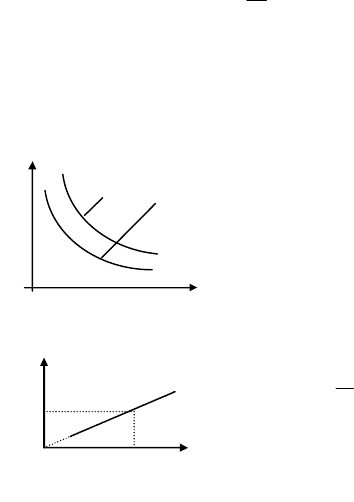
Расстояние от города, где находится база, до магазина в другом
населенном пункте S. Поло-
вину времени автомобиль
движется со скоростью
1
, дру-
гую половину со скоростью
2
. Определить стоимость бен-
зина, необходимого для пере-
возки груза, общее время дви-
жения и среднюю скорость
движения. Считать, что авто-
мобиль использует бензин
марки АИ 80. График измене-
ния расхода бензина на 100 км
пути
в зависимости от ско-
рости движения приводится на рисунке. Как изменятся искомые вели-
чины, если автомобиль движется с указанными скоростями разные
половины пути? Какую среднюю мощность развивает двигатель авто-
мобиля на каждом участке, если масса автомобиля М, коэффициент
сопротивления движению
?
№ вар. S, км
1
, км/ч
2
, км/ч
М, т
1
3
5
7
9
11
13
15
17
19
21
23
25
27
29
31
33
1000
300
500
700
900
1100
330
550
670
900
600
800
250
700
660
310
330
45
50
35
70
40
100
30
80
40
90
70
50
60
60
90
40
50
75
80
60
40
80
60
80
50
70
50
50
80
30
80
40
75
75
3,5
3
4,5
3,7
2,9
3,1
3,3
3,5
2,7
2,9
3,1
3,3
3,5
2,7
2,9
3,1
3,3
0,021
0,023
0,025
0,027
0,029
0,031
0,03
0,035
0,027
0,019
0,021
0,023
0,035
0,017
0,019
0,032
0,033
22
,
л/100км
20
18
16
14
20 40 60 , км/ч
Задание 2. Четные варианты
Катер движется против течения от одного населенного пункта до
другого, расстояние между которыми S. Скорость катера относитель-
но воды
, скорость течения
т
. Определить стоимость дизельного то-
плива, необходимого для преодоления данного расстояния, если на
спокойной воде катер расходует на каждый км пути топливо, в коли-
честве
. Какую мощность развивает двигатель катера, если сила со-
противления движению пропорциональна скорости F
тр
=
r
? Найти
время преодоления пути.
№ вар. S, км
, км/ч
т
, км/ч
, л/км r, кНс/м
2
4
6
8
10
12
14
16
18
20
22
24
26
28
30
32
34
200
240
260
180
100
120
140
160
180
200
220
240
260
280
300
320
340
20
24
26
28
21
22
24
26
18
19
32
34
26
28
30
32
34
2,5
2,4
2,6
2,8
2,1
2,2
2,4
2,6
2,8
2,9
3,2
3,4
2,6
2,8
3
3,2
4,4
1,2
1,4
1,6
1,8
1,1
1,2
1,3
1,5
1,8
1,9
1,15
1,14
1,16
1,18
1,3
1,22
1,24
143
139
147
154
125
130
129
199
226
142
81
81
107
101
104
92
87
Задание 3. Варианты: 1, 4, 7, 10, 13, 16, 19, 22, 25, 28, 31
Сколько времени потребуется автомобилю для увеличения скоро-
сти движения от υ
1
до υ
2
, если он движется с постоянным ускорением
а? Какой путь пройдет автомобиль за это время? Какая результирую-
щая сила действует на автомобиль, если его масса М? Определить на-
чальные и конечные значения кинетической энергии одного колеса
массой m и радиусом R, предполагая, что колесо имеет вид сплошно-
го диска.
23

Какую полезную работу совершает двигатель автомобиля за это
время? Сколько оборотов сделает колесо за время разгона?
№ вар. υ
1
, км/ч υ
2
, км/ч а, м/с
2
М, т m, кг R, см
1
4
7
10
13
16
19
22
25
28
31
36
54
25,2
18
10,8
18
32,4
9
18
43,2
36
75,6
90
50,4
36
46,8
54
90
36
72
90
82,8
2,1
2,5
1,7
1,1
1,3
1,6
1,9
2,2
2,5
1,8
2,1
1
1,5
1,7
1,1
1,6
1,5
1,9
2,2
2,5
2,8
3,1
21
24
27
20
26
25
29
32
35
38
41
21
24
27
22
26
25
29
32
35
38
41
Задание 3. Варианты: 2, 5, 8, 11, 14, 17, 20, 23, 26, 29, 32
При быстром торможении трамвай, массой М, имевший скорость
, начал двигаться «юзом» (заторможенные колеса, не вращаясь, на-
чали скользить по рельсам). Коэффициент трения колес о рельсы
.
Какой участок пути пройдет вагон с момента начала торможения до
полной остановки? Какая средняя сила трения действует на вагон во
время торможения? С какой силой должен держаться пассажир мас-
сой m
1
, чтобы не удариться от резкого торможения? Определить кине-
тическую энергию одного колеса вагона до начала торможения, если
масса колеса m
2
. Сколько оборотов сделало бы колесо до полной оста-
новки при торможении без «юза», если радиус колеса R.
№ вар. М, т
, км/ч
m
1
, кг m
2
, кг R, см
2
5
8
11
14
17
20
23
26
29
32
20
25
18
21
24
17
22
23
16
19
22
22
25
28
31
24
27
20
23
26
29
32
0,2
0,15
0,18
0,21
0,14
0,17
0,12
0,13
0,16
0,19
0,12
52
50
58
61
64
77
80
63
66
69
72
82
85
88
81
84
87
80
83
86
89
92
32
35
38
31
34
37
30
33
36
29
32
24

Задание 3. Варианты: 3, 6, 9, 12, 15, 18, 21, 24, 27, 30, 33
Автомобиль массой М движется с постоянной скоростью υ.
Из-за наличия препятствия на пути водитель решает сделать экстрен-
ное торможение. Время реакции водителя τ. Колеса на сухой дороге
обеспечивают ускорение торможения а. Какой путь пройдет автомо-
биль до полной остановки? Какая средняя сила трения действует на
автомобиль во время торможения, и какая работа при этом совершает-
ся? Если колесо автомобиля приближенно можно представить в виде
сплошного диска диаметра d и массы m, то насколько изменяется его
кинетическая энергия при торможении? Сколько оборотов сделают
колеса до полной остановки?
№ вар. М, т υ, км/ч τ, с а, м/с
2
d, см m, кг
3
6
9
12
15
18
21
24
27
30
33
34
3
1,6
1,9
1,2
1,5
1,8
2,1
2,4
2,7
3,0
3,3
3,4
72
57,6
68,4
79,2
86,4
90
79,2
86,4
93,6
100,8
108
79,2
0,82
0,6
0,8
0,92
0,95
0,88
0,82
0,74
0,66
0,9
0,93
0,94
7,2
6,0
6,8
5,2
6,5
7,8
6,2
6,4
6,7
5
5,3
5,4
73
66
69
62
65
68
71
74
77
70
73
74
30
26
29
32
35
28
31
34
37
40
43
44
25

2. ТЕРМОДИНАМИКА И МОЛЕКУЛЯРНАЯ ФИЗИКА
2.1. Основные законы и формулы
Все окружающие нас тела состоят из атомов. Связанные состоя-
ния небольшого числа атомов называются молекулами. Размеры (диа-
метры) атомов и молекул имеют в среднем порядок d
10
–10
–10
–9
м.
Все непосредственно наблюдаемые нами тела являются макро-
скопическими, т.е. состоят из громадного числа частиц – структурных
элементов.
Молекулы, образующие тело, находятся в состоянии непрерывно-
го теплового движения. Между молекулами действуют силы притяже-
ния и отталкивания, которые в сильной степени зависят от расстояния
между ними. На расстояниях более 10
–9
м межмолекулярным взаимо-
действием можно пренебречь.
В различных газах молекулы удалены друг от друга настолько
( 10
–8
м), что силы взаимодействия между ними практически отсутст-
вуют. Молекулы непрерывно сталкиваются между собой и со стенка-
ми сосуда, производя на них давление.
В твердых телах и жидкостях расстояние между соседними час-
тицами составляет величину порядка 10
–10
м и сравнимо с размерами
молекул и атомов. В твердых телах молекулы, атомы или ионы со-
вершают колебания около некоторых средних положений, называе-
мых узлами кристаллической решетки.
В жидкостях наблюдаются черты, присущие тепловому движе-
нию частиц как в газах, так и в твердых телах. Молекулы внутри жид-
кости колеблются и медленно перемещаются.
Единицей количества вещества является моль.
Моль – это такое количества вещества, в котором содержится
столько структурных элементов, сколько имеется атомов в 0,012 кг
изотопа углерода С
12
.
Число структурных элементов (атомов, молекул, ионов) в одном
моле называется числом Авогадро: N
А
= 6,0225210
23
1/моль.
Масса одного моля вещества называется молярной массой:
=
ν
m
m
o
N
А
,
где
количество молей, m – масса вещества, m
о
– масса одного
структурного элемента.
26
Молекулы, образующие тело, находятся в состоянии непрерывно-
го беспорядочного теплового движения. Поэтому, каким бы ни было
внутреннее состояние тела до его помещения в данные условия, при
постоянстве внешних условий вещество перейдет в новое состояние,
которое со временем меняться не будет. Это состояние называется
состоянием теплового или термодинамического равновесия.
Равновесное состояние характеризуется постоянством небольшо-
го числа параметров, называемых макроскопическими или термоди-
намическими параметрами.
Важнейшими термодинамическими параметрами являются объем,
плотность, давление, температура и др.
Объем V – это часть пространства, которую занимает данное тело.
Единица измерения объема [V] = м
3
.(1л = 10
–3
м
3
– литр).
Плотностью называется масса вещества, приходящаяся на еди-
ницу объема тела:
=
3
м
кг
,
V
m
.
Давлением называется среднее значение силы, действующей по
нормали на единицу площади поверхности емкости со стороны моле-
кул газа или жидкости:
р =
S
F
.
Единица измерения давления: [p] =
2
м1
Н1
][
]
[
S
F
= 1 Па(паскаль).
Внесистемные единицы измерения давления: 1ат = кгс/см
2
=
=0,98110
5
Па – техническая атмосфера; 1 атм = 1,01310
5
Па – физиче-
ская атмосфера.
Температура это мера интенсивности теплового движения час-
тиц тела. Для классических частиц средняя кинетическая энергия по-
ступательного движения одной частицы тела пропорциональна темпе-
ратуре:
2
v
2
o
к
m
W = kT
2
3
,
где m
o
– масса одной частицы, v – ее скорость.
Температура, определяемая с помощью данной формулы, называ-
ется абсолютной температурой. Коэффициент пропорциональности
k называется постоянной Больцмана: k = 1,3810
–23
Дж/К.
Абсолютная температура измеряется в кельвинах: [T] = K. Значе-
ние Т = 0 К называется абсолютным нулем температуры.
27
Между абсолютной температурой и часто используемой на прак-
тике температурой t по шкале Цельсия существует линейная зависи-
мость: T = t + 273,15.
Различные макроскопические параметры не являются независи-
мыми. Закон, выражающий зависимость между термодинамическими
параметрами называется уравнением состояния: F(p,V,T) = 0.
Аналитический вид уравнения состояния установлен только для
идеального газа. Газ называется идеальным, если: а) соударения моле-
кул такого газа происходят как соударения упругих шаров, б) размеры
молекул пренебрежимо малы, в) между молекулами не проявляются
силы взаимного притяжения.
Таким условиям удовлетворяют реальные газы при сильных раз-
режениях и не очень низких температурах.
Уравнением состояния идеального газа является уравнение Кла-
пейрона – Менделеева, полученное обобщением экспериментальных
газовых законов:
pV =
m
RT
или p = nkT
где R = 8,31 Дж/(моль
.
К) универсальная газовая постоянная; n
концентрация молекул (количество молекул в единице объема);
k=R/N
A
= 1,38
.
10
–23
Дж
.
К
–1
постоянная Больцмана(N
A
число Аво-
гадро).
Частные случаи уравнения состояния:
1) Изотермический процесс: Т =const.
pV = const (закон Бойля-Мариотта)
или p
1
V
1
= p
2
V
2
.
Графики зависимостей давления от
температуры для изотермического про-
цесса представлены на рис. 12.
2) Изобарический процесс: p = const.
T
V
= const (закон Гей–Люссака)
или V = V
o
(1 +
t),
где V
o
= объем при температуре t = 0
о
С,
= 1/273,16 К
–1
– термический коэффи-
циент объемного расширения.
График изобарического процесса показан на рис.13.
28
V
V
o
0 T
273
Рис. 13. График V = f(T)
р
Т
1
Т
2
0 V
Рис. 12. График р = f(V)

3) Изохорический процесс: V = const.
T
p
= const (закон Шарля)
или р = р
o
(1 +
t),
где р
o
= давление при температуре t = 0
о
С.
Зависимость давления от температуры
при изохорическом процессе представлена
на рис. 14.
Для смеси не реагирующих газов общее количество вещества оп-
ределяется как сумма количества вещества отдельных компонент:
v =
m
m
см
i
i
i
n
1
= v
i
i
n
1
.
Из последнего соотношения можно определить эффективную мо-
лярную массу смеси:
см
= m v
i
i
n
1
.
Если учитывать собственный объем молекул и силы притяжения
между ними, из уравнения состояния идеального газа получается
уравнение Ван-дер-Ваальса:
(p + v
2
a
V
2
)(V
vb) = vRT ,
где a, b
постоянные Ван-дер-Ваальса. Они связаны с критическими
термодинамическими параметрами:
V
= 3b, p
к
= a/ (27b
2
), T
к
= 8a/(27Rb) .
Уравнение Ван-дер-Ваальса более точно описывает состояние ре-
ального газа, чем уравнение Клапейрона.
Внутреннее давление реального газа: p = a/V
,
где V
молярный объем.
Основное уравнение молекулярно - кинетической теории газов:
p =
2
υ
3
1
o
nm ,
где m
о
масса одной молекулы, υ среднеквадратичная скорость
молекул.
Средняя кинетическая энергия поступательного движения моле-
кулы одноатомного, идеального газа:
2
υ
2
o
m
W
к
=
3
2
kT .
29
р
р
o
0 T
273
Рис. 14. График р = f(T)
