Петров А.А., Бальян X.В., Трощенко А.Т. Органическая химия: Учебник для вузов
Подождите немного. Документ загружается.

Отдельные
представители.
Применение
ИЗ
Щ1ОмаТИ'lеских
яльдсгид()в
наибольшее
зна'lение
имеет
бенаальде
гид
-
жидкость
с
зяпахом
горького
миндялSl.
Т.
кип.
179
ос.
На
воздухе
бысТРО
окисляется
в
6ензойную
кислоту
и
поэтому
хранится
в
доверху
lIа
nOJ1lICHHbIX
и
плотно
закрытых
склянках.
БеllЗЯJlьдегид
встречается
в
виде
гликозидя
амигдалина
в
масле
горьких
миндалеи,
в
косточках
вишни,
1'16-
рикоса,
персика
и
т.
д.
Амигдалин
под
влиянием
энзимов
дает
бевза.'lbде
гид,
синильную
кислоту
и
генцио6иозу
(дисахарид
-
6-ГJlIОКОЗИДО
глюкозу):
CliH:.CH(CN)-О-СllНlIОIIl
+
HlO
----+
C1iH,,:-СНО
+ HCN + CIlH2l011'
Бензальдегид
широко
применяется
в
производстве
красителей,
души
стых
веществ.
В
парфюмерной
ПРОМЫШJlенности
применяется
коричный
альдегид
С
6
Н
5
-СН=СН-СНО.
2.
ЗАМЕЩЕННЫЕ
АРОМАТИЧЕСКИЕ
АЛЬДЕГИДЫ.
ГИДРОКСИАЛЬДЕГИДЫ
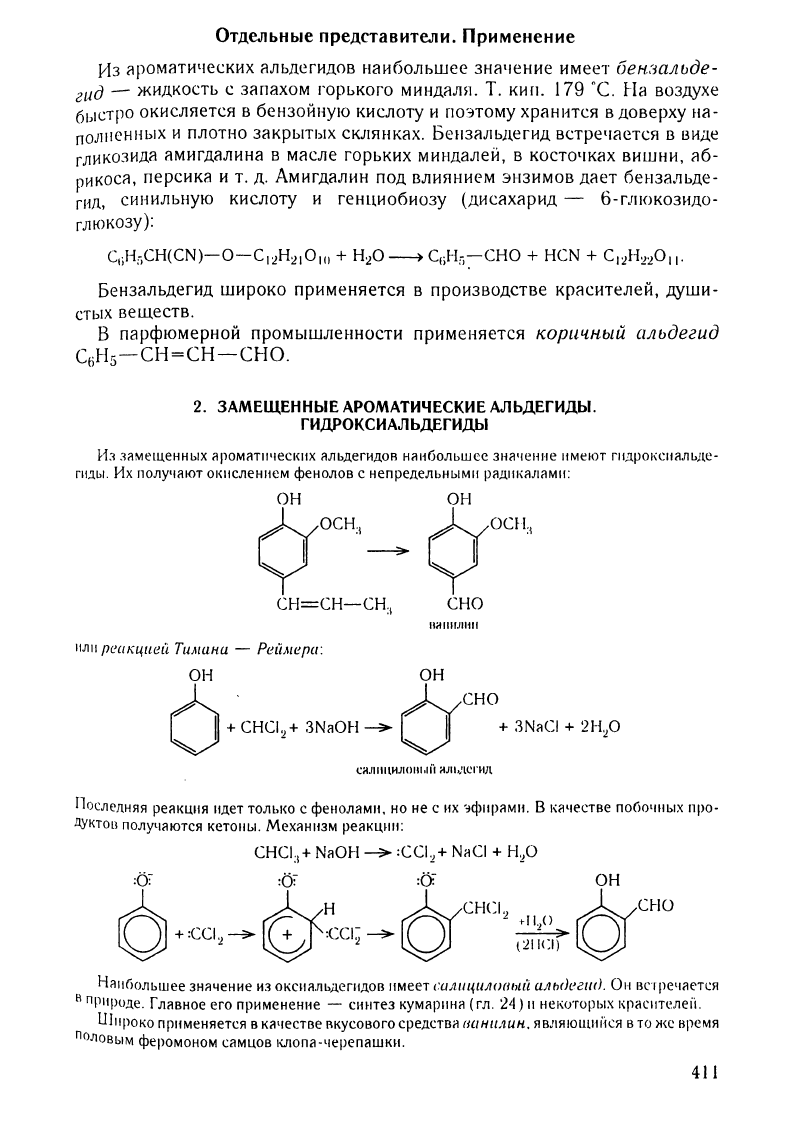
Из
зямещенных
ЯРОМЯТl1чеСЮIХ
яльдеГИДОR
Н~llбольшес
зн~ченне
IIMelOT
Г1tд1JOI\СII~льде·
Гlt.lbI.
Их
IlОЛУ'I~IOТ
ОЮlслеН11ем
фенолов
с
непредеЛЬНЫМlt
Р~Дltl(~JШМI1:
ОН
<:т
ОСНа
I
~
~
СН=СН-СН:
1
IIИIIIIJlIШ
I1ЛI1
реакцией
ТШlUна
-
РеLiJlшра:
6
01-1
.
~CHO
: I + CHCI
2
+ 3NaOH
~
(J
+ 3NaCI +
2Нр
С;.lJII11LНJIOШ.li",
tlJll.JLСГИJL
Последняя
реаlЩltя
идет
толы<о
с
фенолаМ11.
но не
с
их
,Фl1раМ11.
В
I\ачестве
поБОЧIIЫХ
про·
ЦУКТОLl
получаются
кеТОIIЫ.
Мехинltзм
peaKЦlII1:
CHCl
a
+
NиОН
~
:CCI
2
+
NиСI
+ HP
6 +
<:С',
--'>-
dt
ш
;
--'>-
Ь
СНС
',
;:,':::,r
6
рю
НЯllfiольшее
знячение
из
оксиильдепlДОВ
I1меет
саЛIЩIIЛ()(lы!i
алы)егl/().
ОН
8С·I
речиется
8
ПРllроде.
Главное
его
применеНllе
-
синтез
KYMapl1Ha
(гл.
24)
11
иеl\UТОРЫХ
I\раСl1телеii.
ШIlРОКО
Прltменяется
в
Ka'IeCTBe
вкусового
средства
(/l/НI1ЛIIН.
ЯВJIЯIOIШIЙСЯ
В
ТО
же
время
половым
феромоном
самцов
КJlопа·черепаШЮI.
411

3.
АРОМАТИЧЕСКИЕ
КЕТОНЫ
Способы
получения
Для
получения
ароматических
кетонов
могут
быть
использованы
мно
гие
методы
получения
кетонов
жирного
ряда,
например
окисление
вто-
ричных
ароматических
спиртов:
.
С
6
Н
5
-СНОН
.JQ4
Н
2
О
+
C
6
H
5
-СО-СН
з
·
I
СНз
Кроме
того,
имеются
и
специфические
методы
получения
кетонов
Этого
ряда.
1.
Основным
методом
получения
ароматических
кетонов
служит
реак
ция
Фриделя
-
Крафтса:
С
6
Н
6
+
CI-СО-СН
з
~lQз
)
C
G
H
5
-СО-СН
з
+ HCI.
хлорнстыА
ацетил
Предполагается,
что
хлорид
алюминия
образует
с
хлорангидридом
ком
плекс,
который
становится
активным
началом
в
реакции
под
влиянием
из
бытка
хлорида
алюминия:
СНз-СОCl
+
АlCl
з
~[СНз-СО)+
AICI4'
СНз
[сн,-со]
"a;+c,н.~~~O
]
AlCI.~
+311.0
~
C
6
Hr.-СО-СН
з
·
АlCl
з
~
C
6
Hr.-СО-СН
з
+
AI(ОН)з
"
-31-ICI"
В
качестве
исходных
веществ
ДJJЯ
этой
реакции
могут
применяться
уг
леводороды,
эфиры
фенолов.
2.
Непредельные
ароматические
кетоны
получают
конденсацией
аро
матических
альдегидов
с
жирными
кетонами:
-Н
о
CljH'i-СНО
+
HaC-СО-СН
з
-~
CGHG-СН=СН-СО-СН
з
·
• .
(НО-I
З.
Ароматические
оксикетоны
получают
реакцией
Фриса
(гл.
20):
0-
'
о_с(О
нэомернэация~
'~C~OH
_
СНз СНз
~_
фСIIИJI3IIL'Т"dТ
n-ГIlдpОКСИ3
1
lетоФенои
4.
Для
ПОЛ)'Чl!ния
ароматических
фенолокетонов
применяется
также
метод
Геша.
ис
ходными
веществами
являются
многоатомные
фенолы,
особенно
с
ГIIДРОКСИЛЬНЫМИ
группа
ми
B,I!-положеИIlИ:
НОуОН
Н~НVЗ
С
N~~HCI
I
+С~з-СN;Н.CI
~
~
I
+H20~
'-
(ZnCI
2
1;
О
С
'-
-NH
4
C1
ОН ОН
412
O=C-СН
з
Hoh
OH
У
ОН
Физические
и
химические
свойства
Ароматические
кетоны
-
жидкости
или твердые
вещества
с
приятным
цветочным
запахом.
Нерастворимы
в
воде.
Ароматические
кетоны
менее
реакционноспособны,
чем кетоны
жир
ноГО
ряда;
они,
например,
не
реагируют
с
гидросульфитом
натрия.
1.
Большинство
кетонов
реагирует
с
гидроксиламином
и
производны
МИ
гидразина
по
обычной
схеме
(механизм
см.
гл.
5.1):
АГ2С=О
+ H
2
NOH
---+
Н
2
О
+ Ar2C=NOH;
кетоксимы
АГ2С=О
+
Н
2
О
+ H
2
N-NH-C
6
H
5
---+
Н
2
О
+
АГ2С=N-NН-С6Н5'
фенилгидраЗОIIЫ
ИЗ
всех
этих
азотистых
производных
кетонов
наибольший
интерес
представляют
оксимы.
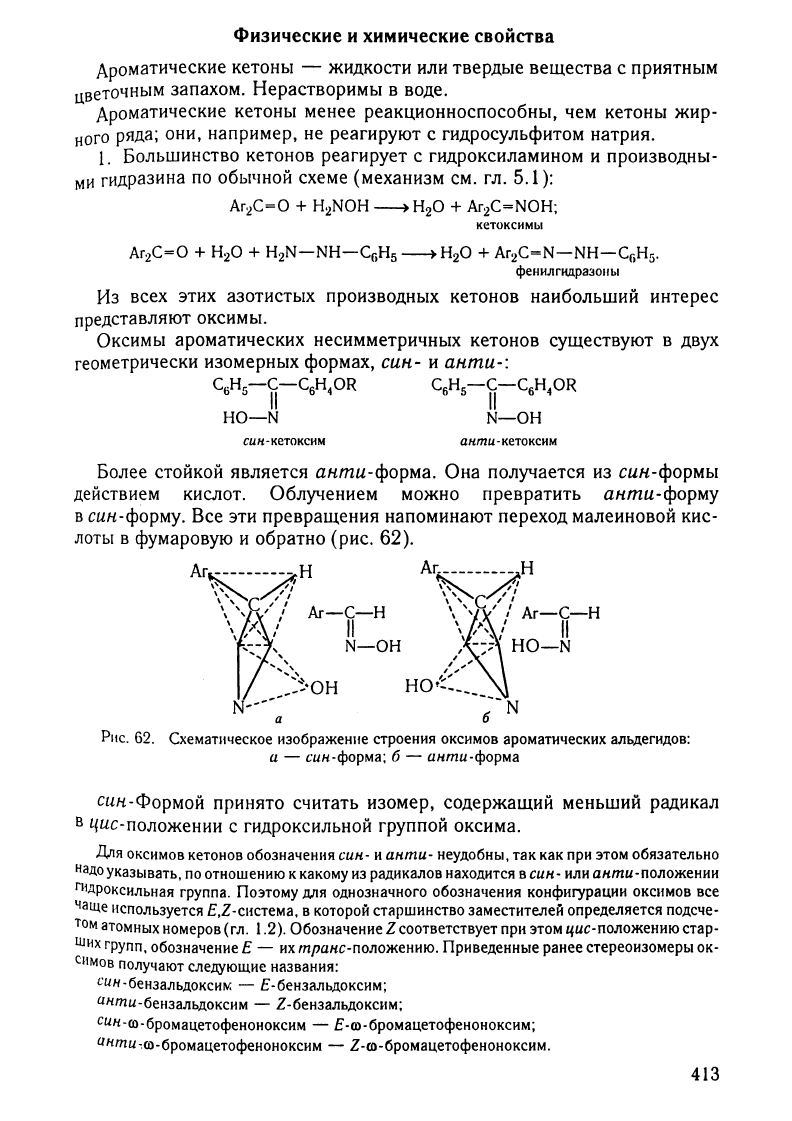
Оксимы
ароматических
несимметричных
кетонов
существуют
в
двух
геометрически
изомерных
формах,
син-
и
анmи-:
C6Hs-n-С6Н40R
СБНS-n-С6Н40R
HO-N
N-OH
сuн-кетоксим
анmи-кетокснм
Более
стойкой является
анmи-форма.
Она
получается
из
син-формы
действием
кислот.
Облучением
можно
превратить
анmи-форму
в
син-фОрму.
Все
эти
превращения
напоминают
переход
малеиновой
кис
лоты
в
фумаровую
и
обратно
(рис.
62).
AГ~--AH
\\:~"'7:/'?
Аг-С-Н
\
)(,
/
11
'::
"
N-OH
......
"
':~'OH
N~-~~~~
а
Aг.~
____
-A--
н
\...
, I
\ " , I
\
...
, I
'.',
':
Аг-С-Н
'\
/", /
11
,
-;,
HO-N
" "
HOt~"
••••
~
••
N
PIIC.
62.
СхемаТllческое
изображеИllе
строения
оксимов
ароматических
альдегидов:
а
-
син-форма;
6 -
анти-форма
син-Формой
принято
считать
изомер,
содержащий
меньший
радикал
в
ЦиС-положении
с
гидроксильной
группой
оксима.
Дnя
оксимов
кетонов
обозначеиия
син-
и
анти-
неудобны,
так как
при
этом
обязательно
надо
указывать,
по
отношению
к
какому
из
радикалов
находится
в
син-
или
анти-положении
ГИдроксильная
группа.
Поэтому
д.nя
однозначного
обозначения
конфигурации
оксимов
все
чаще
используется
E,Z-Сlfстема,
в
которой
старшинство
заместителей
определяется
подсче
том
атомных номеров
(гл.
1.2).
Обозначение
Z
соответствует
при
этом
цuс-положению
стар
ШИХ
групп,
обозначение
Е
-
их
транс-положению.
Приведенные
ранее
стереоизомеры
ок
симов
получают
следующие
названия:
СUН-бензальдоксиw.
-
Е-бензальдоксим;
антU-бензальдоксим
-
Z-бензальдоксим;
Сuн-т-бромацетофеноноксим
-
Е-т-бромацетофеноноксим;
а
нтu
,т-
бромацетофеноноксим
- Z
-т-бромацетофеноноксим.
413

OI\CllMbI
ЖllрноаромаТllllеСКlIХ
l<eToHoB
обычно
(НО
не
всегда)
существуют
в
одной
БОJ\е
cToill<oil
форме.
Возможно.
это
связано
со
способность
IIX
1<
таутомерИII.
I\оторая
ведет
к
пе~
реходу
одного
ОКСI1МЯ
в
другой.
более
СТОlll\иii:
C(.H,-C-CH
1
?
С(.Н.--С=СН,
?С(.Н,-С-СН,
,..
11
.
•.•
1 "
..,
11
.
HO-N
N(OH)
N-OH
аНftШ-II:ЮМЩ'
cuh.-lt:ЮМСI)
J-IЯЛllчне
:lяместителеii
в
бензоЛl.ном
ядре
повышает
стабильность
стереОl1зомерных
ОК
шмов;
т3(,.
например.
2-бром-5-НIпроацетоФеНОНОI<СIIМ
существует
в
Вl1де
устоilЧI1ВЫХСUН_
11
ahml/-фОРМ
с
т.
пл.
171
11
132·С
соответственно.
Большое
зн(\чение
имеет
бекм(\новск(\я
перегруппировка
оксимов,
происходящая
под
влиянием
концентрироваННblХ
минер(\льных
КИслот,
хлорангидридов
и
ангидридов
кислот.
Два
изомеРНblХ
оксида
дают
при
этом
два
изомерных
амида:
С(.Н,-С-С(.НДСН.,
~HO-C-C(.H.oCH,?O=C-C(.H
IOCH,
,..
11
.,.
11""
1'"
N-OH
N-C(;H"
NH-Сt;Н"
UHII1Il-Ф~II"JI-f/-МСТОК
С~lф~IIIIJ1К~Т()КСI1М
аШIJШJL
fl-МСТОКСlt
()t'II:ШЙlюi",
КИСJIOТI.,
C,.H,-C-C(.H'IOCH,~
С(.Н,-С-ОН
?
С,.Н.--СО
•.•
11
• .
•.•
11
•.•
1
HO-N
CH:,OC1;H.1-N
NH-Сt;НрСН:,
CUH-ф~IIIIJI-f/-М~ТОКСII
фl'lIlIJIКСТОКСIIМ
ЮlfШIД
(iСII:шiIllОЙ
KIICJlOTI~1
Предполагаемый
мехаНI1ЗМ
-~Toii
переГРУПГJIIРОВЮI
следующий:
2.
Присоединение
водорода
к
ароматическим
кетонам
в
раЗЛИLIНЫХ
условиях
приводит
к
раЗЛИЧНblМ
проДУктам_
При
каталитическом
восста
новлении
кетонов
с
а-положением
карбонильной группы
по
отношениЮ
к
бензольному
ядру
образуются
углеводороды:
Восстановление
по
Клименсену
-
нагреванием
альдегидов
или
кетона
с
амальгамой
цинка
в
водной
HCI -
также
приводит
к
углеводородам.
При
восстановлении
щеЛОЧНblМИ
метаJIлами
в
апротонных
растворите
JIЯХ
кстоны
изучаемого
ряда
дают
пинаконы:
(С('Н')2
С
-
ОН
2(C(;H,,)~CO
~
•.•
1
(C
1
;H)2
C
-
OH
414

здесЬ
имеет
место
перенос
электрона
от
металла
к
карбонилу:
R'
R
I I
R-C-C-R'
I I
0- 0-
3.
Магнийорганические
соединения
нормально
присоединяются
к
БОЛЬШИНСТВУ
кетонов
(гл.
3.1).
4.
Присоединение
щелочных
металлов
к
чисто
ароматическим
кетонам
дает
металлкети
лЫ.
Это
I,нтенсивно
окрашенные
вещества,
которым
приписывается
радикальная
структура:
5.
Жирноароматические
кетоны
легко
окисляются.
При
окислении
Se02
они
дают
аль
дегидокетоны
или
а-дикетоны:
+
SC
02
)
СпН,,-СО-СНО:
+
SC
02
)
снн,,-СО-СО-СН:\.
При
действии
более
сильных
окислителей
образуются
аромаТII'lеские
кислоты.
б.
ЖltрноаромаТИ'lеские
кетоны
благодаря
ПОДВllжностlt
водородных
атомов
у
а-угле
родного
атома
весьма
склонны
к
реакциям
замещения
водородных
атомов.
Так,
они
легко
га
логеНltруются,
причем
даже
в
присутствии
таких
катализаторов,
как
железо,
замещение
идет
в
боковой
цепи:
+
ВГ
2
C(jH:"I-СО-СН:i--~)
ChH
5
-СО-СН
2
Вг
БРОММСТИJlФСllИJlКСТOII
+
ВГ
2
~
C'iH:j-СО-СНВГ2
)
C'iHii-СО-СВг:\.
диБРОММСТIIJI-
тр"(jРОММСТИJI-
ФСIIИJIКСТ()II
феШIJlКСТ()II
Моногалогенозамещенные
ацетофенона
называют
фенuцuлгuлогенur}UАШ.
Они
приме
Няютея
для
идентификаЦИII
кислот
(в
виде
фенациловых
эфиров).
Лакриматоры.
7.
По
той
же
причине
жирноароматические
кетоны
способны
к
раз
ЛИчным
реакциям
конденсации
за
счет
а.-водородных
атомов
по
отноше
нию
к
карбонильной
группе:
а)
конденсация
Кляйзена:
C1iH,j-СО-СН:
i
+
CHO-С'iН"
~
ChH,,-СО-СН=СН-СнН,,:
l.'uh-(jСII:ЮНJIФСllliJI'-:tТИJIСII
C1iH,,-СО-СН
а
+
CH:i-СО-СfiН"
~
CtiH,,-С(СН;i)=СН-СО-С1iН,,:
ДlIIIII()1I
б)
реакция
Манниха:
C1iH,,-СО-СН:
i
+ CHlO + (NH(C
fi
H
ii
)2]'
НСI
~
~(С(jН,,-СО-СН2-СН2N(С(iН,,)2]'НСI
+
Н
2
О.
415

Возможный
механизм:
9.
Чисто
ароматические
кетоны
расщепляются
амидом
натрия
по
СХе
ме:
ОNи
_ _ +NaN
112
_ l
_.
+IICI.
_
(C
1
;Hr.)2
CO
~
Ct;H,;-т-сг.Нr.
-CHII:~
ChHr.-П-ОNа
~
C
1
;H
5
-CONH
2
NH
2
NH
Эта
реакция
позволяет
устанавливать
строение
кетонов.
Отдельные
представители.
Применение
Ацеmофенон
-
т.
пл.
20
"С,
т.
кип.
202
"с.
Имеет
запах
цветов
чере
мухи.
Встречается
в
каменноугольной
смоле.
Ацетофенон
в
настоящее
время
производит
в
промышленных
масштабах
каталитическим
окислени
ем
этил
бензола
кислородом
воздуха:
+
Sc
02
_
CtiH5-СН2-СН:1
+
02
)
CtiH'j-СО-СН'
1
+
Н
2
О.
130
·С;
3,5
зтм'
,
Применяется
в
паРфlOмерии.
Бензофенон
существует
в
двух
модификациях
с
т.
пл.
27
и
49
"с.
Устой
чивой
является
последняя.
Применяется
в
парфюмерной
промышлен
ности.
Галогенозамещенные
о-аминобензофеноны
применяются
в
синтезе
большой
группы
успокаивающих
лекарственных
препаратов
(транквили
заторов)
производных
бензазепина,
например
mазеnама
(7
-хлор-2,З-ДИ
гидро-З-окси-5-фенил-l
Н-l,4-диазепин-2-0Н):
1 2
.
NH-CH
CX
~
I
:lCН
7~
5
__
4/
('
C--N
'6
(:(
.
NH-CH~
I
"(НОН
CI
~
C=N/
6
ТИ:tСllам
416
4.
ХИНОНЫ
ХинОНЫ
-
специфический
класс
циклических
карбонильных
соедине
ний.
Они
не
являются
в
CTporOM
смысле
ароматическими
соединениями.
Ядро
хинона
не
проявляет
ароматического
характера.
Однако
хиноны
так
легко
получаются
из
ароматических
соединений
и
так
легко
в
них
перехо
дят.
что
оказывается
наиболее
целесообразным
рассматривать
их
при
изучении
соединений
ароматического
ряда.
Первый
представитель
ряда
хинонов
-
n-бензохинон
-
был
получен
А.
А.
Воскресенским
в
1838 r.
окислением
хинной
кислоты,
откуда
и
получил
название
весь
класс
соеди
нениЙ.
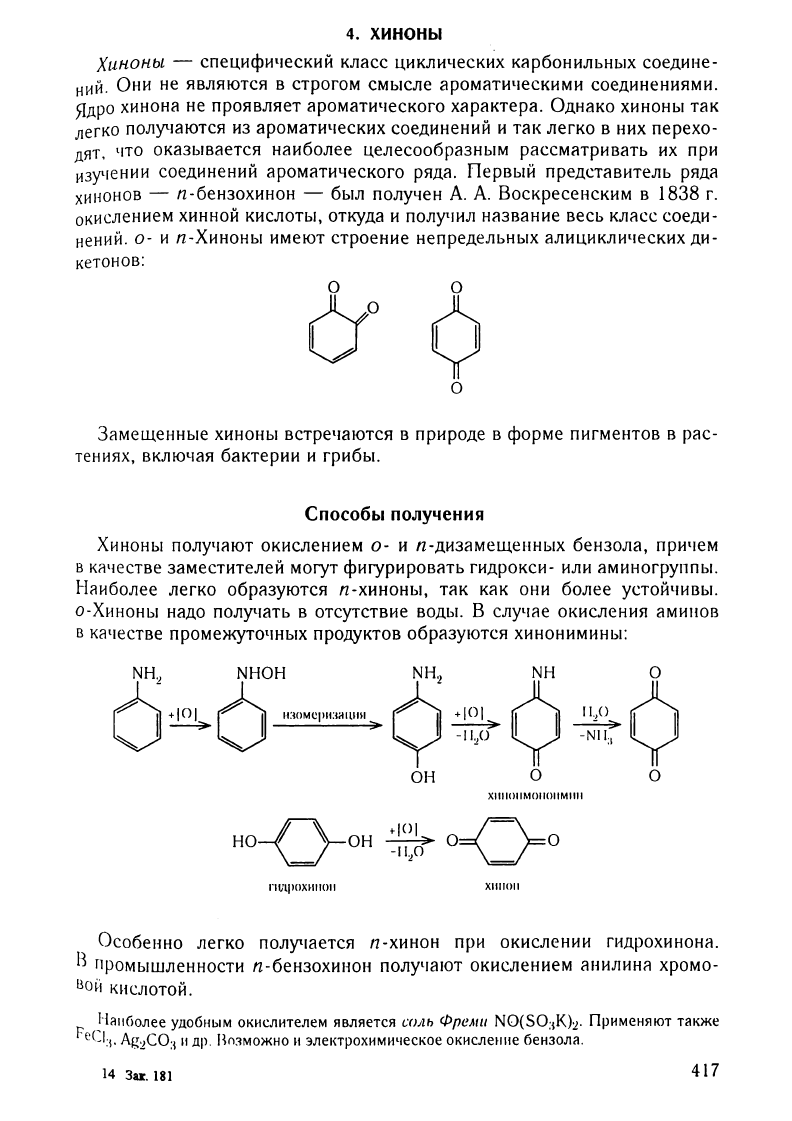
0-
и
n-Хиноны
имеют
строение
непредельных
аЛИЦИКЛИ'lеских
ди
кетоНОВ:
6
о
Замещенные
хиноны
встречаются
в
природе
в
форме
пигментов
в
рас
тениях,
включая
бактерии
и
грибы.
Способы
получения
Хиноны
получают окислением
0-
и
n-дизамещенных
бензола,
причем
в
К<lчестве
заместителей
MOryT
фигурировать
гидрокси-
или
аминогруппы.
Н<lиболее
легко
образуются
n-хиноны,
так
как
они
более
устойчивы.
о-Хиноны
надо
получать
в
отсутствие
воды.
В
СЛУ'lае
окисления
аминов
в
качестве
промежуточных
продуктов
образуются
хинонимины:
NH
2
NHOH
6
~
6
'~.'''".'''".
N~
NH
О
~~rr~n
у
-11,0
У
-NII'I
У
ОН
о О
ХIIIЮIIМОIIOIIМIIII
но-О-'
он
~
O~O
-11/1
""=г"
l'IVIIIOХШЮII
XItlIOII
Особенно
легко
получается
n-хинон
при
окислении
гидрохинона.
В
Промышленности
n-бензохинон
получают
окислением анилина
хромо
вой
КИСJlОТОЙ.
Наllболее
удобным
окислителем
является соль
ФреАIlI
NO(SO:IK)2'
Применяют
также
FeCI:
1
.
Ag
2
CO:
1
"
др.
В()JМОЖНО
It
электрохимическое
окислеllllе
бензола.
14
З
•.
181
417
Физические
свойства
Хиноны
-
вещества
кристаллические
и
обычно
имеют
интеНСИВНУIQ
окраску:
n-хиноны
-
желтую,
о-хиноны
-
оранжевую
или
красную.
Ле
тучи
с
водяным
паром.
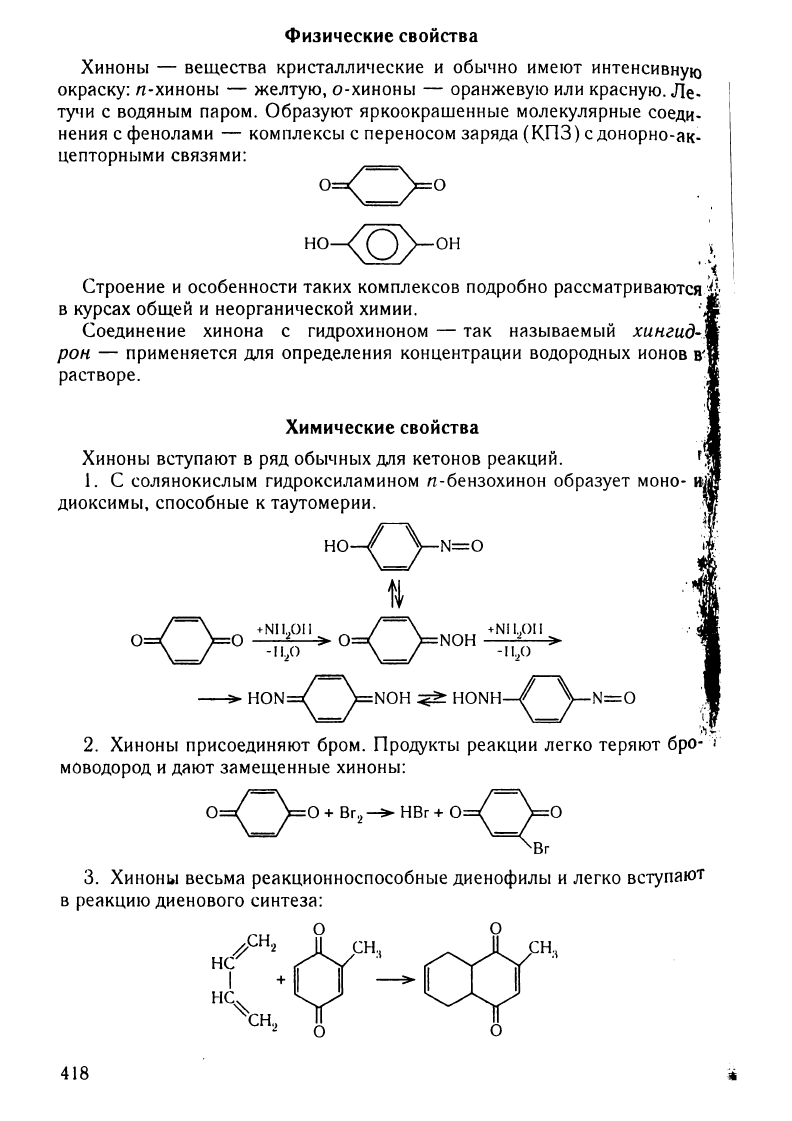
Образуют
яркоокрашенные
молекулярные
соеди
нения
с
фенолами
-
комплексы
с
переносом
заряда
(КПЗ)
СДОНОрНо-ак_
цепторными
связями:
О=<
)=0
но---@-он
.!'
С
~
троение
и
особенности
таких
комплексов
подробно
рассматриваются';·'.
в
курсах
общей
и
неорганической
химии.
'
Соединение
хинона
с
гидрохиноном
-
так
называемый
хингuд~,
рон
-
применяется
д/lя
определения
концентрации
водородных
ионов
8~
растворе.
Химические
свойства
Хиноны
вступают
в
ряд
обычных
д/lЯ
кетонов
реакций.
'"
1.
С
солянокислым
гидроксиламином
n-бензохинон
образует
моно-
и!'
диоксимы,
способные
к
таутомерии.
H0-o-N=O
t~
0=0=0
+NllpII
~
O~NOH
+NIIpII
~
_
-IIP
~_
-IIP
---;о.
HONONOH
?
HONH-o-N=O
;.'.
I
'.>j~,
2.
Хиноны
присоединяют
бром.
Продукты
реакции
легко
теряют
бро-
'!
моводород
И
дают
замещенные
хиноны:
oOO+Bг2....."..HBг+0~0
"=<вг
3.
ХИНОНIoI
весьма
реакционноспособные
диенофилы
и
легко
вступаюТ
в
реакцию
диенового
синтеза:
418
СН
О О
нС'
2+
(11
CH~
WI
СНа
не
~
СН
2
О О
Эта
реакция
применяется
в
синтезе
красителей
и
лекарственных
ве
lllесТВ,
например
М,еmuн.он.а
(с.
420).
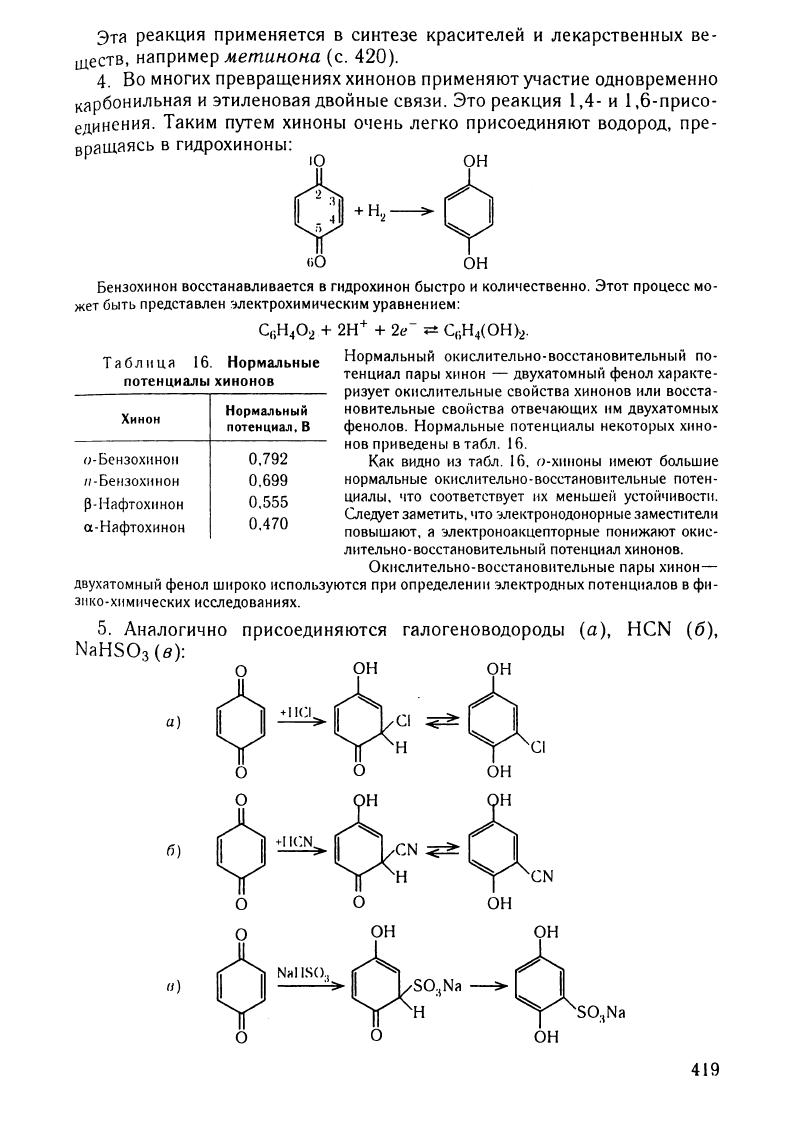
4.
Во
многих
превращениях
хинонов
применяют
участие
одновременно
карбонильная
и
этиленовая
двойные
связи.
Это
реакция
1,4-
и
1,6-присо
единения.
Таким
путем
хиноны
очень
легко
присоединяют
водород, пре
вращаясь
в
гидрохиноны:
ф+~~~
Ю
ОН
Бензохинон
восстанавливается
в
гидрохинон
быстро
и
количественно.
Этот
процесс
мо
жет
быть
представлен
электрохимическим
уравнением:
СНН
4
О
2
+
2Н+
+
2е-
+=t
C
1i
H
4
(OH)2'
Таблиц!!
16.
Нормальные
потенциалыхинонов
ХИНОН
()·БеНЗОХИНОII
II-Бензохttнон
~-НафТОХItНОН
а-Н!!фтохинон
Нормальный
потенциал.
В
0.792
0.699
0.555
0,470
Нормальный
окислительно-восстановительный
по·
тенциал
пары
XI!HOH
-
двухатомный
фенол
характе
ризует
окttСЛllТельные
свойства
хинонов
или
восста
новительные
свойства
отвечающих
11М
двухатомных
фенолов.
Нормальные
потенциалы
некоторых
хино
нов
приведены
в
табл.
16.
Как
видно
из табл.
16,
()-ХИIIОНЫ
имеют
большие
нормальные
ОКИСЛllТельно,восстановttтельные
потен,
циалы.
'ITO
соответствует
11Х
меньшей
УСТОЙ'lIiВОСТИ.
Следует
заметить.
что
элеlпронодонорные
заместltтели
повышают,
а
электроноаlщепторные
ПОНИЖ!!ЮТ
окис-
Лllтельно-восстановительный
потенциал
хинонов.
Окt!слительно-восст!!новttтельные
пары
хинон
двухатомный
фенол
широко
используются
при
определении
электродных
потеНЦlt!!ЛОВ
в
фи-
31t1{Q·хltмнческих
исследованиях.
5.
Аналогично
присоединяются
галогеноводороды
(а),
HCN (6),
NаНSО
з
(8):
а)
б)
(1)
о
ОН ОН
rr~~CI'~~
у
VH
~CI
О О
ОН
(r
+IICN~
I
~
CN
Е"
;-
I
о
Q
<i
У
Н'
CN
О О
ОН
419
6.
НарядУ
с
реакциями
присоединення
д.nя
хннонов
характерны
и
некоторые
реакции
замещення.
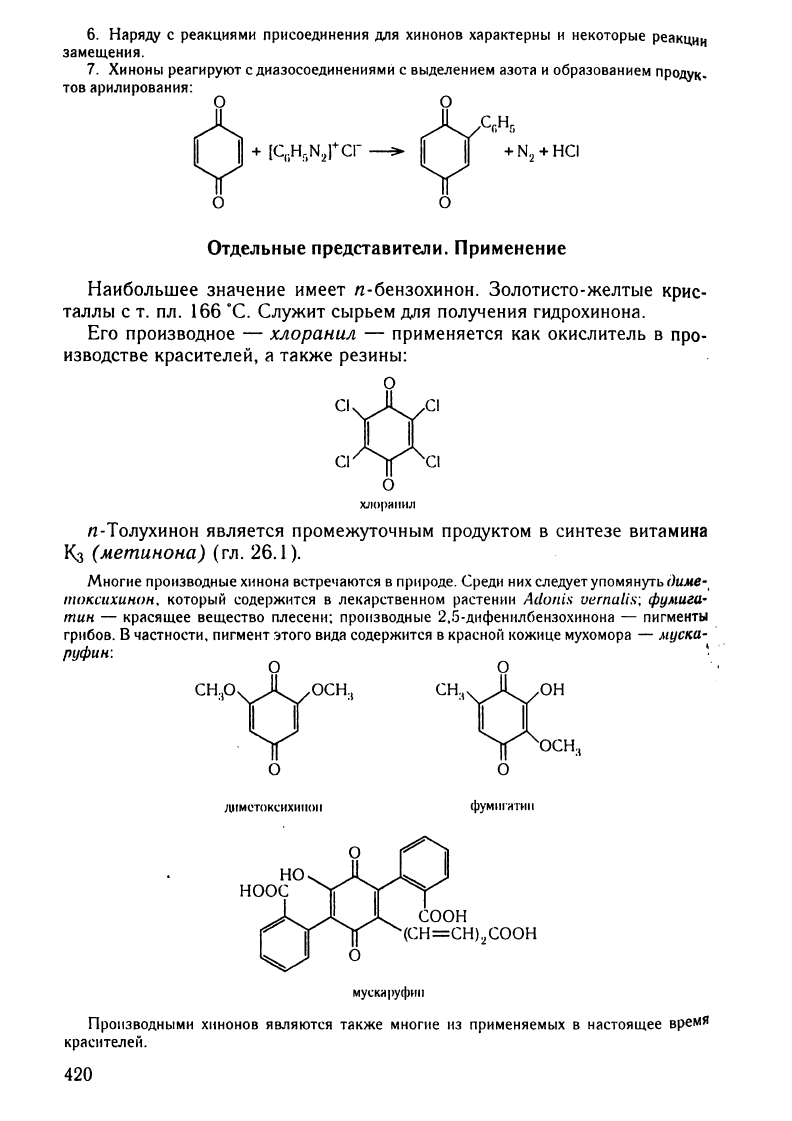
7.
Хиноны
реагируют
сдиазосоединениями
с
выделением
азота
н
образованием
ПРОдУк.
тов
арилирования:
~CГoH
..
V .
:N,+HCI
О
ОтдеЛЬНblе
представители.
Применение
Наибольшее
значение
имеет
n-бензохинон.
Золотисто-желтые
крис
таллы
с
т.
пл.
166
ос.
Служит
сырьем
для
получения
гидрохинона.
Его
производное
-
хлоранил
-
применяется
как
окислитель
в
про
изводстве
красителей,
а
также
резины:
О
ClyyCI
CIYCI
О
XJЮРИIIИJI
n-
Толухинон
является
промежуточным
продуктом
в
синтезе
витамина
кз
(метинона)
(гл.
26.1).
Многие
ПРОllзводные
хинона
встречаются
в
пр"роде.
Среди
них
СЛедУет
упомянуть
iJue-.
mшссихинон.
который
содержится
в
лекарственном
растении
Atlonis
!Jl!гnalis;
Фумига
тин
-
красящее
вещество
плесени;
ПРОlIзводные
2.5·дIIФенилбензохинона
-
пигмеиты
грибов.
В
частности,
пигмент
этого
вида
содержится
в
красной
I<ОЖlще
мухомора
-
",ус"а-
о
руфин:
~
00
О О
о
СНРnО<Ж.
CH,yyo~
.у
VOCH:
1
О О
JUIМСТОКСИХIШОII
ФУМШ'ИТlIII
мусКltРУфlll1
ПРОll3ВОДНЫМИ
ХIIНОНОВ
являются
также
многие
И3
при
меняемых
в
настоящее
времЯ
краСllтenеЙ.
420
