Петров А.А., Бальян X.В., Трощенко А.Т. Органическая химия: Учебник для вузов
Подождите немного. Документ загружается.


3.
Отщепление
галогеноводородов
от
галогенкарбонильных
соедине
•
Наиболее
легко
этим
путем
получаются
соединения
с
трехчленными
нии.
.
цикламИ.
Однако
метод
приемлем
и
для
получения
других
циклов:
_ _ _
-lIl1г
_ _ _
CH:,-CO-?H-?H~
~
CH:j-СО-С~
/СН
2
Н
ВГСН
2
СН
2
5·бром·2-пентанон
аЦИТНЛЦllклопропан
(метнлциклопропнлкетон)
4.
Декарбоксилирование
солей
двухосновных
кислот,
начиняя
с
шести
атомов
углерода
в
цепи,
например
адипиновой
и
пимелиновой
кислот.
Этот
метод
применим
для
получения
соединений
с
5, 6
и
более
членами
в
цикле:
CH.)-CH~-CO-O"
CH~-C~2
I -
/Ва
~
I
/СО+ВаСО.,
СН
2
-СН
2
-СО-О
СН
2
-СН
2
.
аднпинат
бария
циклопентанон
5.
Сложноэфирные
конденсации
с
У'lастием
эфиров
двухосновных
кис
JIOT.
Конденсация
сложных
эфиров
под
влиянием
алкоголятов
часто
идет
с
образованием
пяти-
и
шестичленных
циклических
систем
(Дж.
Дикман).
Например:
а)
межмолекулярная
конденсация:
HCH-СООС
2
Н
r.
соос..Н.
I
INиос..II-1
I
•..
+
СН
•
")0
СООС
Н.
I
~
_
-2С
2
1
1,,01
1
-~
"
нсн-СООС2Н"
со-сн-соос.
Н,
1
"
~
.,
/СН
2
СО-СН-СООС
2
Н,.
б)
внутримолекулярная
конденсация:
СН
2
-СН
2
-СООС
2
Н;,
I
INиОС..Н"1
~
,1;;.
-C}I}JII
CH
2
-СН
2
-СООС
2
Н
r.
с
п
е
Ц
и
а
л
ь
н
ы
е с
п о
с
о
б
ы
получения
али
циклических
соединений,
Применимые
только для
получения
соединений
с
определенной
величиной
ЦИкла.
.
1.
Соединения
с
т р
е
х ч
л
е
н н
ы
м
циклом
наиболее
часто
получают
ся
Присоединением
карбенов
(с.
123)
к
непредельным
соединениям:
а)
CH
2
N
2
~
:CH
2
+N
2
JUfit:ЮМСТ311
СН:,-СН=СН
2
+
:CH~
~
CH:I-C~
/СН
2
СН
2
301
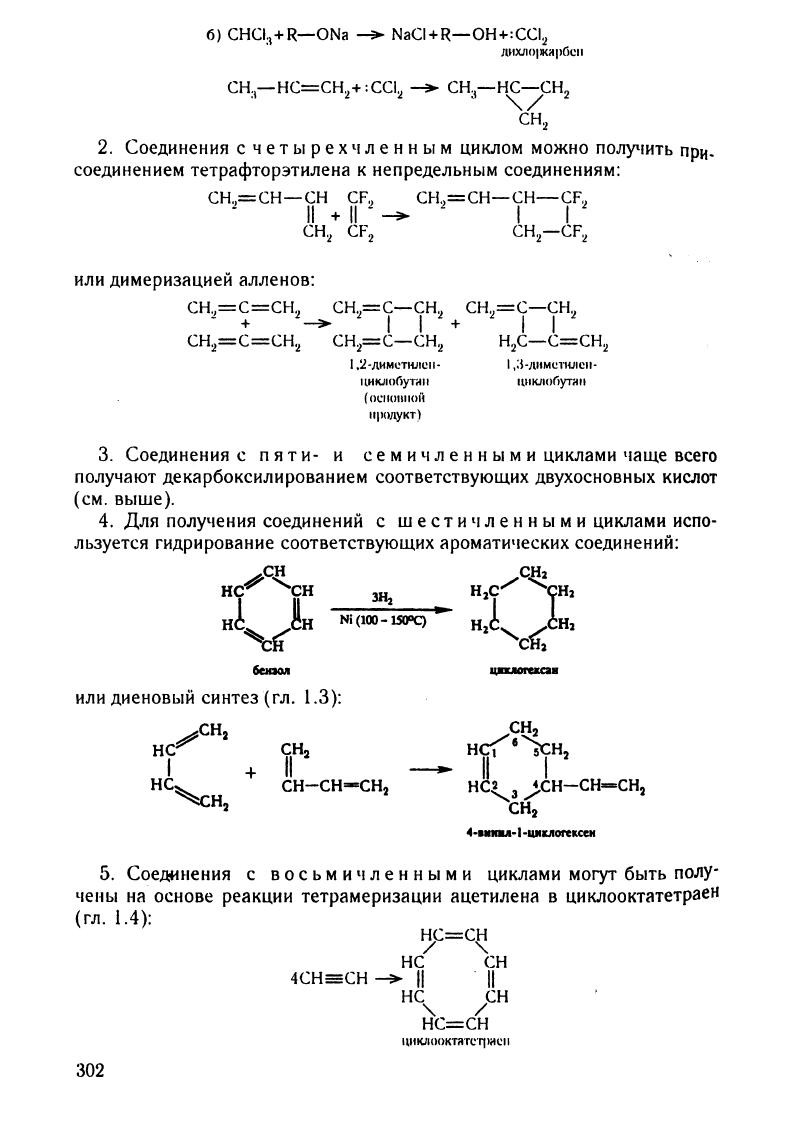
б)
CHCla+R-ОNа
--+-
NaCI+R-ОН+:ССI
2
ДИXJI()I'КIIl'БСII
CH
a
-НС=СН
2
+:ССI
2
--+-
CH
a
-
Н
Z/СН
2
СН
2
2.
Соединения
с ч
е
т
ы ре
х
ч
л
е
н
н
ы
м
циклом
можно
получить
при.
соединением
тетрафторэтилена
к
непредельным
соединениям:
СН
2
=СН-СН
CF
2
CH
2
=CH-CH-CF
2
11
+
11
--+- 1 1
СН
2
CF
2
CH
2
-CF
2
или
димеризацией
алле
нов:
СН
2
=С=СН
2
СН
2
=С-СН
2
СН
2
=С-СН
2
+ --+- 1 1 + 1 1
СН
2
=С=СН
2
СН
2
=С-СН
2
Н
2
С-С=СН
2
1.2·ДНМСТИJIСII·
II,НКJю(iУТЮI
(ОСIЮlllюА
IIJЮДУКТ)
1.:!·/lItМСТИJlСII·
III\КJlO(iYТ~1I
3.
Соединения
с
n
я
т
и-
и
с е
м
и ч
л
е н н
ы
м
и
циклами
чаще
всего
получают
декарбоксилированием
соответствующих
двухосновных
кислот
(см.
выше).
4.
Для
получения
соединений
с
ш
е
с т
и
'1
Л
е
н н
ы
м
и
циклами
испо·
льзуется
гидрирование
соответствующих
аромаТИ'lеских
соединений:
.АСИ
СН2
НС....
.........си
3нz
Н
2
С
......
"""~H2
и~'с(gН
Н;
(100-
JSOOC).
нJ.,с(~И2
liCIIIOII
или
диеновый
синтез
(гл.
1.3):
,СН
2
НС
I
HC~_
~H,
+
СН
2
11
СН-СН-СН,
СН,
Hc(''icH
2
нМ,
4JH-CH
....
CH,
.........
3/
СН
2
4-
......
-1-1UI1UIOre1<CCll
5.
Соединения
с
в
о
с ь
М
И Ч
л
е
н н
ы
м
и
циклами
могут
быть
полу
чены
на
основе
реакции
тетрамеризации
ацетилена
в
циклооктатетраен
(гл.
1.4):
302
НС=СН
/ "
НС
СН
4СН=СН
--+-
11
.
11
НС
СН
" /
НС=СН
III\КJIШIКТИТС..,IIIСII

а
основе
реакции
димеризации
1
,3-алкадиенов
на
специальных
ката
или
н
лизаторах
(гл.
1.3):
Hc/H2C-C~H
~II
11
НС
СН
" /
Н
2
С-СН
2
1,5-циклооктадиен
б.
Для
получения
в
ы
с
ш
и х
циклов
с
числом
углеродных
атомов
30
и
более
Л.
Ружичка
использовал
сухую
nерегон.к.у
ториевых
солей
дикар
бонОВЫХ
кислот.
Все
перечисленные
общие
и
специальные
способы
получения
алицик
лических
соединений
могут
быть
использованы
для
синтеза
не
только
сое
динений,
указанных
в
приведенных
выше
уравнениях.
Путем
обычных
пе
реходов
между
классами
из
них
можно
получить
и
соединения
других
клас
сов
с
тем
же
циклом.
Однако
при
этом
всегда
следует
учитывать
возможность
изомеризации
цикла
(подробнее
см.
ниже).
Физические
свойства
Циклические
соединения
обычно
имеют
более
высокую
температуру
кипения
и
плавления
и
большую
плотность
по
сравнению
с
аналогично
построенными
соединениями
жирного
ряда
с
тем
же
'IИСЛОМ
углеродных
атомов.
Температура
кипения
тем
выше,
чем
БОJlьше
цикл
(при
том
же
со
ставе).
Главнейшие
константы
HeKoTopblX
циклопарафинов
приведены
в
табл.
12.
т
а
б л
и
ц
а
12.
Физические
свойства
aJlканов
и
ЦИКЛОaJIканов
Соединение
Пропан
Циклопропан
Бутан
Ц11К,106vтаll
МеТIIЛ~;II(лопропан
Пентаl1
ЦIII(лопеНТiiН
МеТlIЛЦIIl(ло6утан
ЭТII."IЩГiJlопропан
Гексан
Цl1к.10гексан
МеТIIЛЦIII<ЛОllентан
ЭТI1.ЩIII(ЛО6утан
ПРОlllIлциклопропан
Т.
пл.,·С
-187.1
-126.9
-136
-80
-177,2
-129,7
-94.4
-149.3
-149,1
-94.0
6.5
-142.2
-142.9
Т.
кип
..
·С
-42.2
-33
-0.5
13
0.7
36.1
49.3
36.8
34.5
68.8
80.7
71.9
71.5
68.5
79.5
~1.0)гeKcaH
I
llри
температуре
Iшпения.
:.1
При
-20.0
ос.
з
При
16.7
ос.
0.58241
0.6881
0.57881
0.7038
0.69122
0.6263
0.7460
0.6931
0.677
0.6594
0,7781
0,7488
0,7450
0.7120:\
0.8144

Химические
свойства
Важнейшей
особенностью,
отличающей
алициклические
соединения
от
соединений
жирного
ряда,
является
наЛИ'lИе
цикла.
Поэтому
мы
преж_
де
всего
рассмотрим
на
примере
циклоалканов
особенности
разли'!Ных
по
величине
циклов.
Циклопарафины
сильно
отличаются
между
собой
по
устойчивости
ЦИК
ла.
Из
малых
и
средних
циклов
наименее
устойчивы
трехчленные
и
наИбо_
лее
устойчивы
пяти-
и
шестичленные
циклы.
Последние
не
разрываются
при
действии
на
холоду
перманаганата
калия,
озона,
брома,
бромистого
водорода.
Эта
закономерность
связана
с
величиной
напряжения
в
указан
ных
циклах.
Особая
неустойчивость
трехчленного
цикла
связана
со
спе
цифической
гибридизацией
орбиталей
углеродных
атомов,
приближаю
щейся
по
характеру
к
sр2_
ги
бридизации
алкенов.
Ниже
рассмотрены
направления
химических
превращений
циклоалка
нов
в
зависимости
от
величины
цикла.
1.
Гидрирование.
При
каталитическом
гидрировании
трех-,
четырех
и
пятичленные
циклы
разрываются
с
образованием
парафИlЮВЫХ
углево
дородов.
Особенно
легко
идет
эта
реакция
в
случае
циклопропана
и
его
гомологов.
Пятичленный
цикл
разрывается
только
при
высоких
темпе
ратурах:
H~C-CH~
1'1
I
I
+
н.,
~
сн.,-СН.,-сн.,-сн.,-сн.,
- - -
:ЮО·С
. - • • .
н
2
с
СН
2
,,/
СН
2
Соединения
с
шестичленными
циклами
при
нагревании
с
катализато
рами
гидрирования
дегидрируются
и
превращаются
в
ароматические:
/~2
OC~
Н.,С
CH~
1',1
не:?"
ен
- 1 1
Е
Э
1
11
+
3Н
2
н.
е
сн.
:ЮО"С
не
ен
2,,/
2
~/
еН
2
ен
2.
Галогенирование.
Реакция
циклопарафинов
с
галогенами
идет
в
различных
напраВJlениях
в
зависимости
от
величины
цикла.
Трехчлен
ный
цикл
при'действии
raJloreHOB
разрывается:
ен.
/,,~
+CI2~
енр-ен
2
-енр
Н
2
С-СН
2
ХJlорирование
с
разрывом
связи
С-С
сопровождается
заместителЬ
ным
хлорированием.
Бром
действует
на
циклопропан
при
освещении
или
в
присутствии
катализаторов
с
образованием
смеси
1,3-, 1,2-
и
1,
l-ди-
304

б
омпропанов.
Образование
двух
последних
связывают
с
миграцией
бра
р
в
промежуточном
карбениевом
ионе.
ма
uиклопарафИНЫ
с
пяти-
и
шестичленными
циклами
вступают
в
обыч-
ДЛ
Я
парафинов
реакции
замещения
(циклобутаны
реагируют
в
обоих
ные
направлениях):
з.
Действие
галогеноводородов.
Циклопропан
и
его
гомологи
реагиру
ют
с
галогеноводородами
с
разрывом
цикла:
сн;
/"-
+
НВг
~
CH
j
-СН
2
-СНВг-R
R-HC-CH
2
.
Реякция
проходит
в
соответствии
справилом
Марковникова.
Циклопа
РЯфНIIЫ
с
ббльшим
числом
углеродных
атомов
в
цикле
с
галогеноводоро
адми
не
реагируют.
4.
Циклопропановый
цикл
расщепляется
и
при
действии
сильных
кис
лородных
кислот
с
образованием
спиртов
и
сложных
эфиров
также
в
со
ответствии
справилом
Марковникова:
_
/СН
2
_ _
R-CH,
I +
CF.j-СООН
~
CH.,-CH,-CH-R
'СН
2
.
.,.
I
ОСОСЕ
!
Циклы
с
ббльшим
числом
углеродных
атомов кислотами
не
рясщепляются.
Все
реакции
циклопропанов
с
электрофильными
реагентами
рассмат
риваются
как
реакции
электрофильного
присоединения
с
промежуточным
образованием
различных
видов
карбениевых
ионов.
5.
Окисление.
При
действии
сильных
окислителей
циклопарафины
(с
разрывом
цикла)
образуют
двухосновные
кислоты
с
тем
же
числом
уг
леродных
атомов.
Этим
они
отличаются
от
изомерных
олефинов,
окисля
IOЩихся
с
образованием
кислот
или
карбонильных
соединений
с
меньшим
числом
углеродных
атомов
(гл.
1.2):
Y~2
H~C
СН
2
I()I
_.
_ _ _ _
I I
~
НООС-СН.,-СН,-СН,-СН,-СООН
Н
С
СН
• - • -
~
"-/
2
СН
2
Особенности
непредельных
a.JIициклических
соединений.
Двойную
СВ
связь
можно
ввести
в
любое
кольцо,
начиная
с
трехчленного.
Две
двойные
язи
МОжно
ввести
только
в
пятичленное
кольцо
в
сопряженном
305
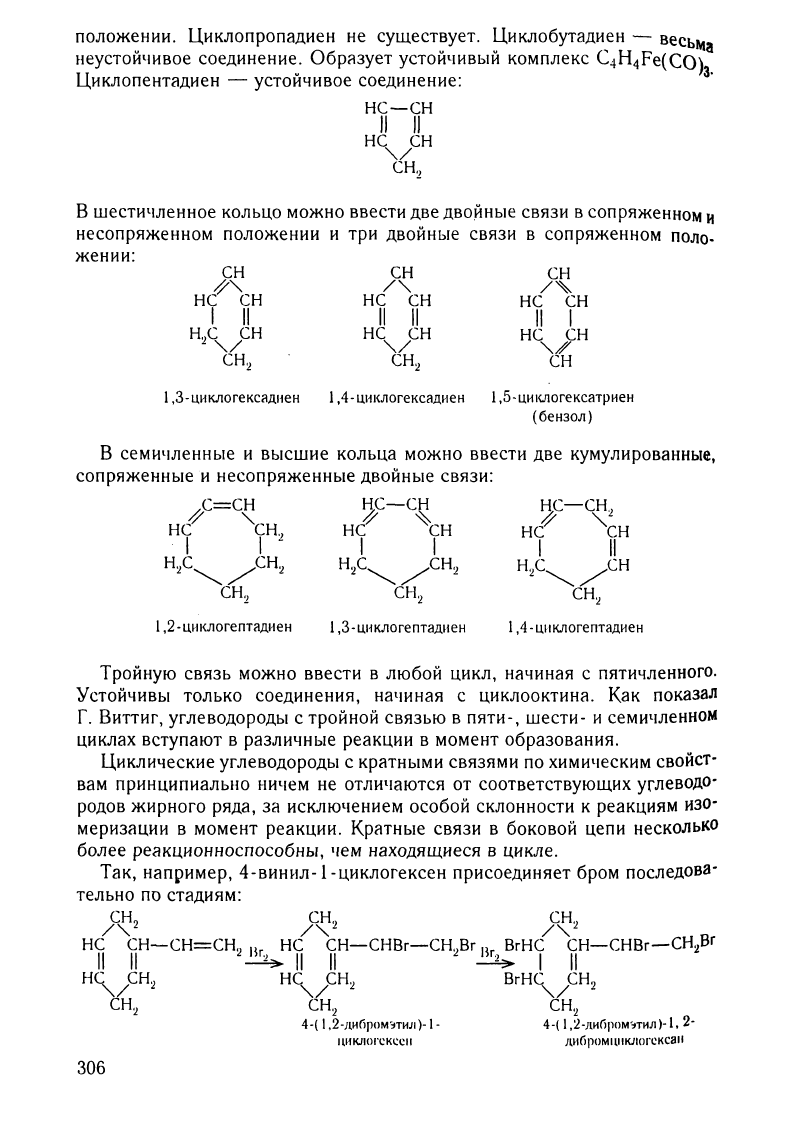
положении.
Циклопропадиен
не
существует.
Циклобутадиен
-
BeCbt.la
неустойчивое
соединение.
Образует
УСТОЙ'IИВЫЙ
комплекс
C
4
H
4
Fe(
СО)
Циклопентадиен
-
устойчивое
соединение:
3·
не-ен
11 11
не ен
"../
еН
2
в
шестичленное
кольцо
можно
ввести
две
двойные
связи
в
сопряженном
и
несопряженном
положении
и
три
двойные
связи
в
сопряженном
ПОло-
жении:
ен
-f"..
не
ен
1
11
не
ен
2"../
еН
2
1,3-циклогексаДllен
ен
/"..
не ен
11
11
не ен
"../
еН
2
1,4-ЦИl<логексадиен
ен
/'-
не ен
11
1
не ен
"../
ен
1,5-ЦИl(JlOгексатриен
(бензол)
В
сеМИ'Iленные
и
высшие
кольца
можно
ввести
две
кумулированные,
1,2
-
ЦШ<Jюгептадllен
1,3-Цl1клогеnтадиен
1,4-ц"клогеПТадl1ен
Тройную
связь
можно
ввести
в
любой
цикл,
начиная
с
пятичленногО.
Устойчивы
только
соединения,
начиная
с
циклооктина.
Как
показал
Г.
Виттиг,
углеводороды
с
тройной
связью
в
ПЯТИ-,
шести-
и
семичленноМ
циклах
вступают
в
различные
реакции
в
момент
образования.
Циклические
углеводороды
с
кратными
связями
по
ХИМИ'Iеским
свойСТ
вам
принципиалыю
ничем
не
отличаются
от
соответствующих
углеводо
родов
жирного
ряда,
за
исключением
особой
склонности
к
реакциям
изо
меризации
в
момент
реакции.
Кратные
связи
в
боковой
цепи
несколЬКО
более
реакционнослособны,
чем
находящиеся
в
цикле.
Так,
наПLJимер,
4-винил-l-циклогексен
присоединяет
бром
последова
тельно
по
стадиям:
Y-t'2
y-t'2 y-t'2
не
eh-ен=еН
2
Вг
не
ен-енвг-ен
2
вг
Вг
вгне
ен-снвг-ен
2
вг
11
11
---4-
11 11
---4- 1
11
H~/eH2
H~/eH2
вгне"../еН
2
еН
2
еН
2
еН
2
4-(
1,2-диб[!ОМЭТИJI)-I-
4-(
I,:l-дибромэтил)-l,
2-
IIИКJIOI-СКССII
Дllб[!ОМIIIIКJlOгсксаll
З06
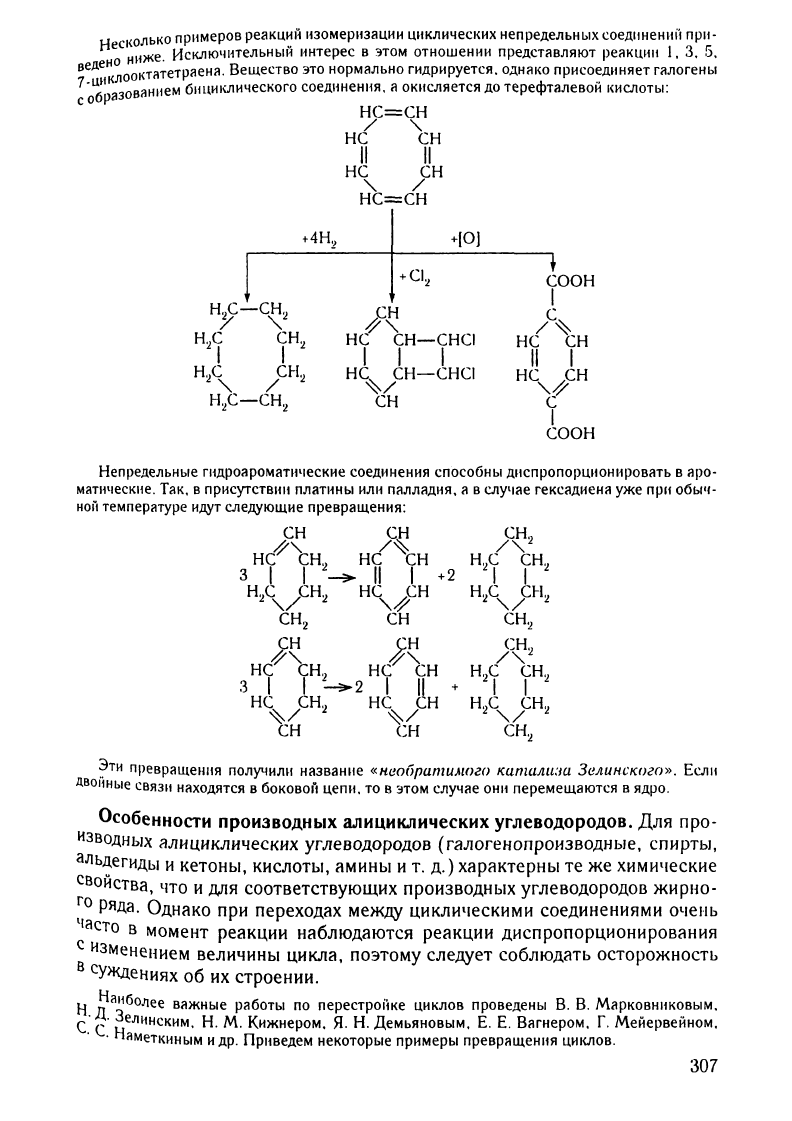
НеСI(ОЛ
ЬКО
примеров
реакц~й
изомеризации
циклических
иепредельных
соеДllнений
ПРIf-
о
ниже.
ИСКJlючительныи
IJИTepec
в
этом
отношении
представляют
реаКЦИIf
1.
З.
5.
веден
oOKTilTeTpaeHa.
Вещество
это
нормально
гидрируется.
однако
присоединяет
галогены
7
-ЦбIIКJIЗОВiIНllем
61ЩИКJIического
соеДl1Нения.
а
окисляется
до
терефталевои
IШСЛОТЫ:
С
о ра
нс=сн
/ "
нс сн
11 11
нс
сн
" /
нс=сн
j .(01
сн
~"
нс
СН-СНСI
I I I
нс
СН-СНСI
-~/
сн
+
соон
1
с
/~
нс сн
11
1
нс сн
,,~
С
I
соон
Непредельные
ГlщроаромаТII'lеские
соединения
способны
ДИСПРОПОРЦIЮНllровать
в
аро
маТllческие.
Так.
в
присутствии
платины
или
палладия.
а
в
СЛУ'lае
гексадиена
уже
при
обы',
ной
температуре
идут
следующие
превращения:
СН ен
и"
/~
не"
ен.
не
ен
3 I 1
2~
11
1 +2
Н
2
С
/СН
2
НС
/.сн
"
,,~
еН
2
СН
JH JH
H<;:~'cH2
Hc~'cH
3 I 1
~2
1
1I
нс
ен.
не
СН
~/
2
~/
СН
сн
~ти
превращеllllЯ
получили
назваНllе
«неоfiраmUАЮZО
каmалlt:1U
3елuн.скоz()).
Если
ДВОllНые
Связи
находятся
в
боковоrt
цепи.
то
в
этом
случае
OHII
перемещаются
в
ядро.
Особенности
производных
алИЦИКJIических
углеводородов.
Для
про
ИЗВодных
али
циклических
углеводородов
(галогенопроизводные,
спирты,
~ль~егиды
и
кетоны,
кислоты,
амины
и
т.
д.)
характерны
те
же
химические
воиства,
что
и
д,ля
соответствующих
производных
углеводородов
жирно
го
ряда.
Однако
при
переходах
между
циклическими
соединениями
очень
'lacl'O
в
момент
реакции
наблюдаются
реакции
диспропорционирования
С
ИЗменением
величины
цикла,
поэтому
следует
соблюдать
осторожность
в
СУЖДеНИЯХ
об
их
строении.
1-1.
Nа~более
важные
работы
по
nepecTpoiiKe
циклов
проведены
В. В.
Марк~виик~вым.
С.
с'
нелинским.
н.
М.
Кижнером.
Я.
Н.
Демьяновым.
Е. Е.
Вагнером,
Г.
Меиервеином.
.
аметкиным
и
др.
При
ведем
некоторые
при
меры
превращеНlIЯ
ЦИКJIов.
307
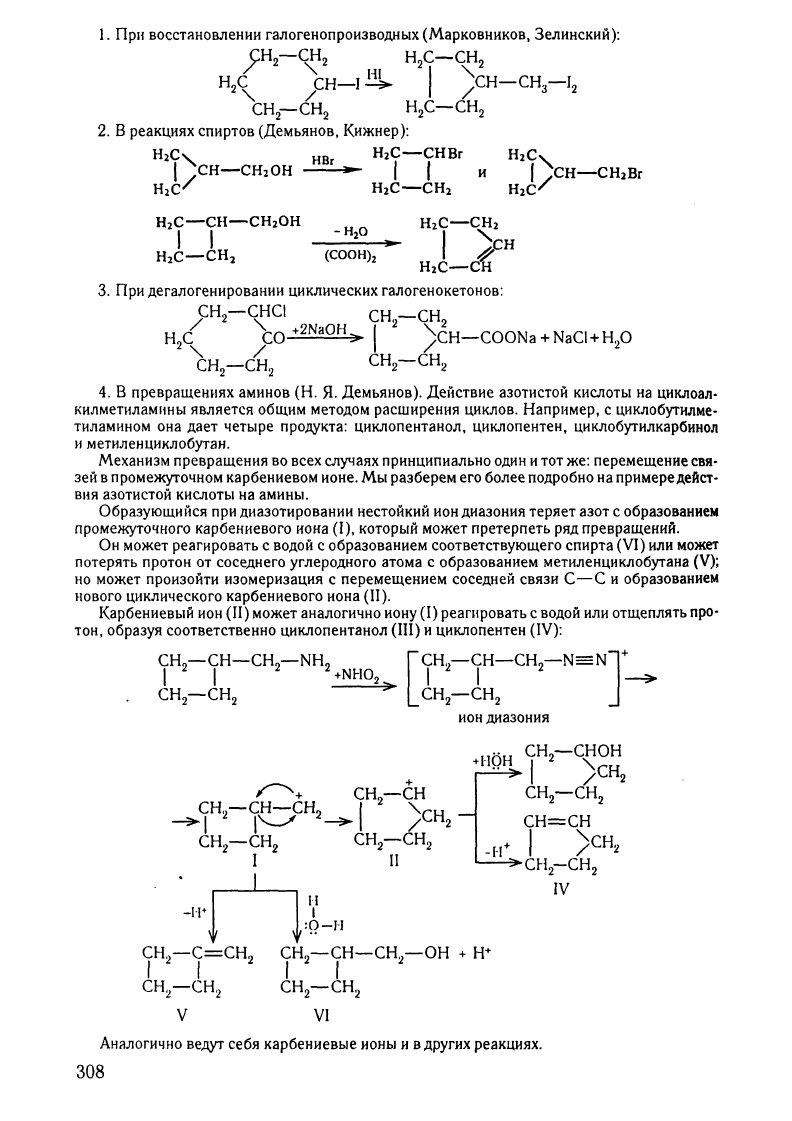
1.
При
восстановлении
галогенопроизводных
(Марковников,
Зелинский):
СН
2
-СН
2
Н
2
С-СН
2
/ "
1-11
1"
H2~
iH-I
~
/CH-СН
з
-I
2
СН
2
-СН
2
Н
2
С-СН
2
2.
В
реакциях
спиртов
(Демьянов,
Кижиер):
Н2С,
ив,
H
2
C-СНВr
'/СН-СН20Н
- I I
и
H1C
Н
2
С-СН2
(СООИ)2
3.
При
дегалогенировании
циклических
галогенокетонов:
СН
2
-СНCI
СН
-СН
Н
2
<
;0
+2NаОНэ-
I 2
)CH-СООNа+NаСI+Нр
СН
-СН
СН
2
-СН
2
2 2
4.
В
превращениях
аминов
(Н.
Я.
Демьянов).
Действие
азотистой
кислоты
на циклоал
килметилаМI\НЫ
является
общим
методом
расширения
циклов.
Например,
с
циклобyrнлме
тиламином
она
дает
четыре
продукта:
циклопентанол,
циклопентен,
циклобyrилкарбиноn
и
метилен
циклобутан.
Механизм
превращения
во
всех
случаях
прннципиально
один
и
тот
же:
перемещение
свя
зей
в
промежуточном
карбениевом
ионе.
Мы
разберем
его
более
подробно
на
примередеАст
ВIIЯ
азотистой
кислоты
на
амины.
Образующийся
при
диазотировании
нестойкий
ион
дназония
теряет
азот
с
образоваиием
промежуточного
карбениевого
иона
(1),
который
может
претерпеть
рядпревращениЙ.
Он
может
реагировать
с
водой
с
образованием
соответствующего
спирта
(VI)
или
может
потерять
протон
от
соседнего
углеродного
атома
с
образованием
метиленциклобyrана
(V);
но
может
произойти
изомеризация
с
перемещением
соседней связи
с-с
и
образованием
нового
циклического
карбениевого
иона
(11).
Карбениевый
нон
(П)
может
аналогично
иону
(1)
реагировать
с
водой
или
отщеплять
про
тон,
образуя
соответственно
циклопентанол
(111)
и
циклопентен
(IV):
СН
-СН-СН
-NH
[CIH2-CIH-CH2-N=NJ~
I 2 I 2 2 +NH0
2
---....-
>
СН
2
-СН
2
СН
2
-СН
2
ион
дназония
Аналогично
ведут
себя
карбениевые
ионы
и в
других
реакциях.
308

Отдельные
представители.
Применение
Простейший
циклопарафин
-
цuклоnроnан
-
газообразное
веще
во
с
т.
кип.
-34
ос.
Его
получ~ют
В
промышленном
масштабе
обработ
ст
1'-,
1
з_дихлорпропана
цинковои
пылью
в
этаноле
и
используют
в
качест
ко
..
, .
ве
ингаляциОННОГО
анестезирующего
средства.
1
3_Дихлорпропан
получают
хлорированием
пропана
при
400
ос
газо
обр~ЗНblМ
хлором.
Образу~тся
смесь
дихлоридов,
содержащая
19,3%
1
з_дихлорпропана,
которыи
довольно
легко отделяется
от
других
изоме
~B
вследствие
большой
разницы
в
температурах
кипения.
р
Недавно
синтезированный
циклобутадиен
устойчив
только
при
темпе
ратурах
ниже
-35
ос.
Выше
этой
температуры
он
димеризуется:
D~IIIIII
Неустой'lИВОСТЬ
циклобутадиена
обусловлена
не
только
стерическим
напряжением,
но
главныIM
образом
антиароматичностью
(гл.
16):
он
на
76
кДж/моль
менее
устойчив,
чем
1,3-бутадиен.
При
обычных
условиях
он
может
существовать
в
виде
комплексов.
Как
уже
отме'lалось,
гомологи
циклопентана
содержатся
в
кавказских
нефтях.
Циклопентановое
или
циклопентеновое
кольца
входят
в
состав
ПРИРОДНblХ
веществ
-
nросmагландuнов.
Впервые
простагландины
были
обнаружены
в
предстательной
железе
млекопитающих.
Теперь
из
вестио,
что
оии
содержатся
в
небольших
количествах
почти
во
всех
тканях
и
оргаиах
живых
организмов.
Неожиданным
явилось
их
высокое
содержа
Hиe
в
мягком
коралле.
Один
из
простагландинов
обнаружен
в
тканях
лука.
Простагландины
являются
регуляторами
функций
клетки
и
обладают
гор
мональной
активностью.
В
отличие
от
гормонов
они
синтезируются
в
ор
ганизмах
не
в
специальных
железах,
а
непосредственно
в
клетках.
Раз
ЛИчные
'представители
этих
веществ
(вьщелено
около
20
простагланди
нов)
стимулируют
сокращение
гладких
мышц,
понижают
кровяное
давление
и
проявляют
иные
виды
терапевтического
действия,
причем
в
НИЧтожных
концентрациях.
Простагландины
являются
производиыми
простановой
кислоты:
~OOH
простаиовая
КИСЛОта
в
Метках
они,
по-видимому,
образуется
из
полиненасыщенных
кислот
в
реЗультате
замыкания
циклопентанового
или
циклопентенового
цикла.
Простагландины
получили
широкое
применение
в
медицине,
ветерина
Рии,
растениеводстве.
Так,
например,
простагландин
Еl
применяется
при
лечении
бронхиальной
астмы.
б
Цuк.логексан
-
жидкость
с
т.
кип.
81
ос.
Получается
гидрированием
еНзола.
Применяется
как
растворитель
и
д,ля
получения
адипиновой
кис
лотыI и
капролактама.
309
Гексахлорцuклогексан
(гексахлоран),
получаемый
оБЫ'IНО
ПРИСоеДlt.
нением
хлора
к
бензолу
на
свету,
применяется
как
инсектицид.
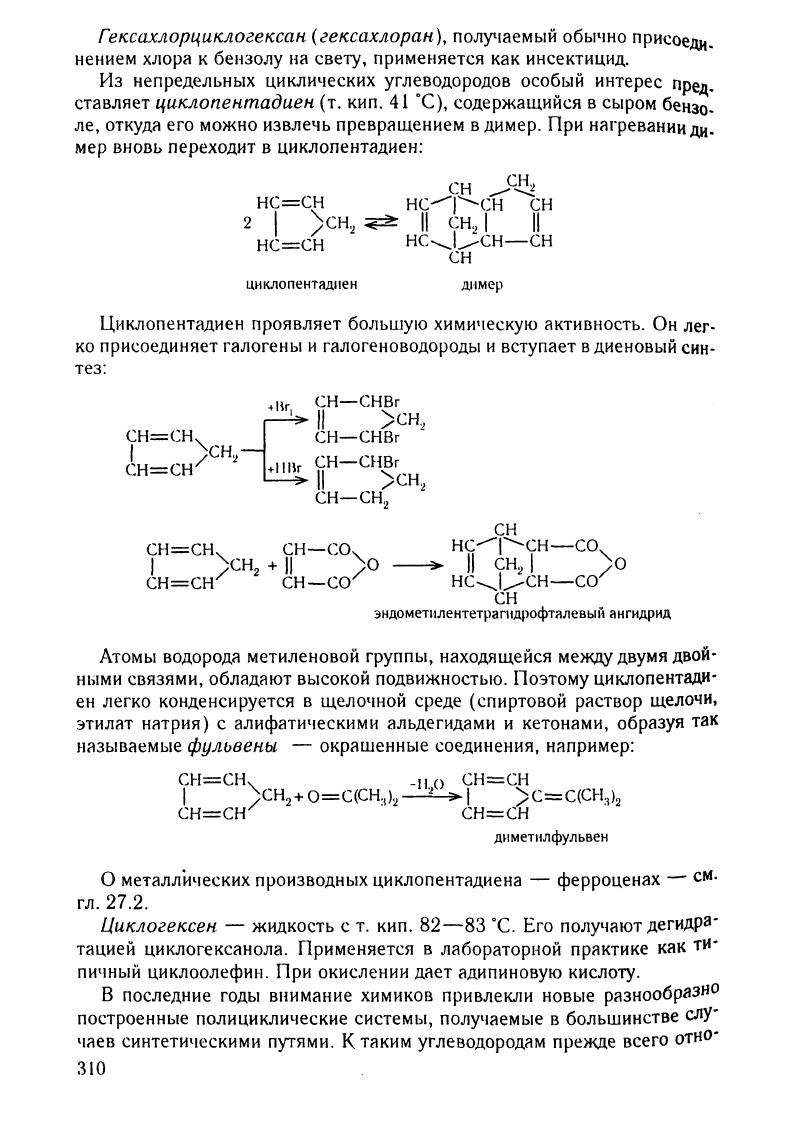
Из
непредельных
циклических
углеводородов
особый
интерес
Пред.
ставляет
цuклоnенmадuен
(т.
кип.
41
·С),
содержащийся
в
сыром
бензо.
ле,
откуда
его
можно
извлечь
превращением
в
димер.
При
нагревании
дн_
мер
вновь
переходит
в
циклопентадиен:
(
'Н
СН2
.
...-~
НС=СН
HC...-г
....
СН СН
2 I
)СН
2
Е"
11
СН
2
1
11
НС=СН
НС
........
'...-СН-СН
СН
циклопеНТ3дllен
Дllмер
Циклопентадиен
проявляет
БОJIЬШУЮ
химическую
активность.
Он
лег
ко
присоединяет
галогены
и
галогеноводороды
и
вступает
в
диеновый
син
тез:
СН
СН=СН, СН-СО,
НС...-'
........
СН-СО,
I
'СН
+
11
)0
----+
11
сн
2
1
)0
СН=СН/
2
СН-СО
Hc
........
I...-СН-Со
СН
эндометнлентетрагltдрофталевый
ангидрид
Атомы
водорода
метиленовой
группы,
находящейся
между
двумя
двой
ными
связями,
обладают
высокой
подвижностью.
Поэтому
циклопентВДИ
ен
легко
конденсируется
в
щелочной
среде
(спиртовой
раствор щелочИ,
этилат
натрия)
с
алифатическими
альдегидами
и
кетонами,
образуя
так
называемые
ФУЛ/Jвены
-
окрашенные
соединения,
например:
СН=СН"
-11
о
СН=СН
I
/CH2+0=C(CH:I)2~1
)С=С(
С1
Ч2
СН=СН
СН=СН
димеТlIлфульвен
о
металлических
производных
циклопентадиена
-
ферроценах
-
СМ.
гл.
27.2.
Цuклогексен
-
жидкость
с
т.
кип.
82-83
ос.
Его
полу'!ают
дегидра
тацией
циклогексанола.
При
меняется
в
лабораторной
практике
как
ти
пичный
циклоолефин.
При
окислении
дает
адипиновую
кислоту.
В
последние
годы
внимание
химиков
привлеКJIИ
новые
разнообразнО
построенные
полициклические
системы,
ПОЛУ'lаемые
в
большинстве
слу
чаев
синтетическими
путями.
К
таким
углеводородам
прежде
всего
OTtl
O
-
310
