Михеева Е.В., Пикула Н.П. Физическая и коллоидная химия
Подождите немного. Документ загружается.


161
Дж
TT
k
k
TRT
E
a
107680
393413
1002,4
1083,19
ln413393314,8
ln
4
4
12
1
2
21
.
2. Для расчета предэкспоненциального множителя в уравнении Ар-
рениуса воспользуемся уравнением (6.32):
14,25
393314,8
107680
1002,4lnlnln
4
RT
E
kA
a
.
11014,25
1032,8 ceA
.
Теории химической кинетики
Основной задачей химической кинетики является создание теории,
позволяющей вычислить скорость реакции, исходя из молекулярных
параметров реагирующих веществ и внешних условий протекания про-
цесса.
Теория активных столкновений
Первой теорией, позволяющей теоретически рассчитать константу
скорости химической реакции, была теория активных столкновений
(соударений). Эта теория не потеряла своего значения и сегодня благо-
даря наглядности и простоте использования математического аппарата.
Теория активных столкновений, предложенная Аррениусом, осно-
вана на том, что химическое взаимодействие осуществляется только при
столкновении активных частиц, которые обладают достаточной энерги-
ей для преодоления потенциального барьера. То есть, для того чтобы
произошла реакция, реагирующие молекулы в момент столкновения
должны обладать некоторым минимальным избытком энергии, который
называется энергией активации реакции. В теории активных столкнове-
ний считается, что акт превращения начальных веществ в конечные
продукты совершается в момент столкновения активных молекул и про-
текает мгновенно.
Основное уравнение теории активных столкновений, выведенное
для газов, имеет вид:
RTE
a
ePzk
0
, (6.34)
где k – константа скорости реакции; Р – стерический фактор, учи-
тывающий пространственную ориентацию молекул в момент столкно-
вения; z
0
– общее число столкновений молекул газа в единице объема за
единицу времени; Е
а
– энергия активации.
162
Теория активных столкновений с ее сравнительно простой трактов-
кой проблем химического взаимодействия оказалось довольно плодо-
творной, и объяснила много разнообразных факторов. Но вместе с тем
из-за своей схематичности она привела к противоречиям с опытом. Мо-
дель активных столкновений не объясняет влияния растворителя, дав-
ления и других факторов на скорость реакции.
Теория активированного комплекса
Теория активированного комплекса или переходного состояния
основана на том, что элементарный акт взаимодействия молекул состо-
ит в постепенной перестройке химических связей, при котором началь-
ная конфигурация атомов в исходных молекулах переходит в конечную
у продуктов реакции при непрерывном изменении межатомных рас-
стояний.
Количественную теорию, основанную на этих представлениях, с
использованием математического аппарата статистической термодина-
мики, так называемую теорию абсолютных скоростей реакций, пред-
ложили Г. Эйринг и М. Поляни (1935).
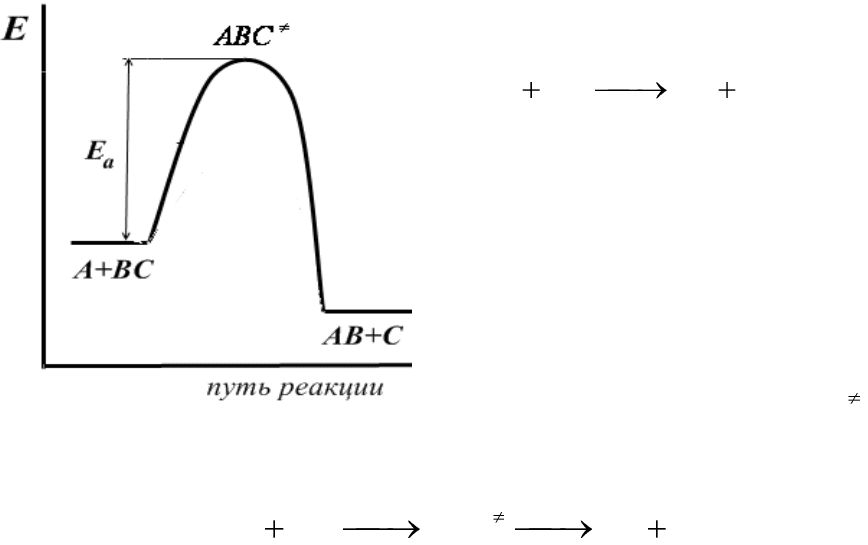
Рис.6.7. Изменение потенциальной
энергии системы во время элемен-
тарного акта химической реакции
Рассмотрим механизм бимоле-
кулярной реакции:
CABBCA
.
Согласно теории активирован-
ного комплекса при сближении
атома А с молекулой ВС ослабляет-
ся связь В—С и возникает связь
А—В. Процесс завершается образо-
ванием молекулы АВ и атома С.
Предполагается, что на вершине по-
тенциального барьера образуется
активированный комплекс
ABC
,
когда атом В в одинаковой степени
принадлежит молекулам ВС и АВ:
CABABCBCA
Качественные представления об элементарном акте как о сложном
процессе перестройки химических связей при сближении молекул, а
также представления о поверхности потенциальной энергии и коорди-
нате реакции называют теорией активированного комплекса или пере-
ходного состояния. Согласно рассматриваемой теории, скорость реак-
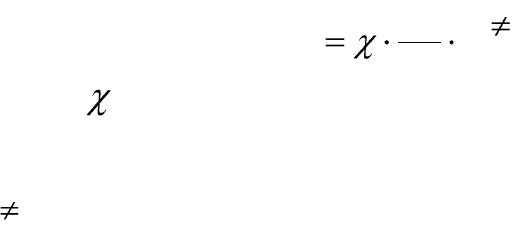
163
ции равна скорости перехода активированного комплекса через энерге-
тический барьер.
Основным уравнением теории абсолютных скоростей реакции яв-
ляется уравнение, связывающее константу скорости реакции со свойст-
вами активированного комплекса:
k
T
h
K
, (6.35)
где – трансмиссионный коэффициент, учитывающий долю ак-
тивированных комплексов, распадающихся на продукты реакции;
– постоянная Больцмана; Т – температура; h – постоянная Планка;
K
– константа равновесия между исходными веществами и активиро-
ванным комплексом.
Вопросы для самоконтроля
1. В чем заключается отличие в определениях скорости химической
реакции и скорости химической реакции по компоненту?
2. В чем отличие порядка и молекулярности химической реакции?
3. Что такое константа скорости химической реакции и где она ис-
пользуется?
4. Физический смысл энергии активации.
5. Укажите констант скоростей химических реакций различных по-
рядков.
6. Какова суть теорий химической кинетики?
7. Каким образом можно рассчитать энергию активации химиче-
ской реакции?
164
7. КАТАЛИЗ
Основные понятия. Основные свойства катализатора
Для управления химической реакцией особенно ценной является
возможность изменения ее скорости, что имеет большое значение в
промышленности. В одних случаях реакцию требуется ускорить, со-
кращая таким образом время выпуска продукции; в других – замедлить
(коррозия, цепные реакции). Все это достигается при помощи катализа.
Катализ является практически основным средством осуществления
химических превращений в природе и в практической деятельности че-
ловека. Например, в области нефтепереработки каталитические процес-
сы за последние 50 лет привели к техническому перевороту, существен-
но повысили выход моторного топлива и других ценных продуктов из
нефти и резко улучшили их качество; мощность основных каталитиче-
ских процессов нефтепереработки (крекинга, гидроочистки, риформин-
га, гидрокрекинга, изомеризации) достигает сотен миллионов тонн; на
применении катализаторов основаны все процессы нефтехимии.
Катализ – возбуждение химических реакций или изменение их
скорости под влиянием катализаторов, веществ, многократно вступаю-
щих в промежуточное химическое взаимодействие с участниками реак-
ции и восстанавливающих после каждого цикла промежуточного взаи-
модействия свой химический состав.
Катализатор – вещество, изменяющее скорость химической реак-
ции участием в образовании активированного комплекса одной или не-
скольких стадий химического превращения и не входящие в состав ко-
нечных продуктов. Если катализатором служит твердое вещество, то
обычно наблюдается постепенное изменение структуры катализатора, а
иногда и его состава в результате взаимодействия с примесями или даже
с основными компонентами реакционной смеси (спекание, механиче-
ский износ, отравление каталитическими ядами).
Катализ может быть положительным и отрицательным: в первом
случае скорость реакции под действие катализатора увеличивается, во
втором – уменьшается. Под увеличением скорости понимается также
возможность протекания реакции, осуществление которой без катализа-
тора практически не возможно. В настоящее время отрицательный ката-
лиз принято называть ингибированием, а вещества, его вызывающие –
ингибиторами. На практике ингибирование используется для подавле-
ния или снижения скорости нежелательных реакций.
Под действием катализатора или ингибитора скорость реакции мо-
жет изменяться в миллионы раз, а некоторые реакции вообще осущест-
165
вимы только в присутствии катализатора. Это совсем не означает, что
катализатор может вызвать термодинамически невозможный процесс.
Причина действия катализатора заключается в проведении реакций по
новому пути с меньшим энергетическим барьером. При этом термоди-
намические свойства реакции (ΔН, ΔS, ΔG, ΔA) остаются неизменны-
ми. Инициирование реакций, практически не идущих без катализаторов,
состоит лишь в многократном увеличении их скорости. Восстанавлива-
ясь к концу реакции, катализаторы способны участвовать в них много-
кратно, вызывая небольшим количеством превращение значительных
масс вещества.
Различают гомогенный и гетерогенный катализ.
При гомогенном катализе реагирующие вещества и катализатор
находятся в одной фазе (в растворе или смеси газов). Например, реакция
окисления оксида серы (IV) может осуществляться в присутствии ката-
лизатора NO
2
по реакции:
)()()(
3
)(
2
2
1
2
2
гSOгOгSO
гNO
.
При гетерогенном катализе реагирующие вещества и катализатор
находятся в разных фазах и химическая реакция протекает на границе
раздела фаз. Например, эта же реакция окисления оксида серы (IV) мо-
жет осуществляться на поверхности платинового катализатора:
)()()(
3
)(
2
2
1
2
гSOгOгSO
твPt
.
Наибольшее практическое значение имеют каталитические реак-
ции, когда катализатор находится в твердой фазе, а реагенты в жидкой
или газообразной фазах.
Одно и то же вещество может быть хорошим катализатором по от-
ношению к одной реакции (или нескольким однотипным реакциям) и
плохим катализатором, и даже ингибитором, по отношению к другой.
Способность катализатора ускорять химическую реакцию характеризу-
ется его каталитической активностью (А), под которой понимается
изменение скорости реакции в результате введения катализатора. Ак-
тивность катализатора зависит от его природы и условий проведения
реакции: температуры, давления, концентрации реагентов, растворителя
и т.д.
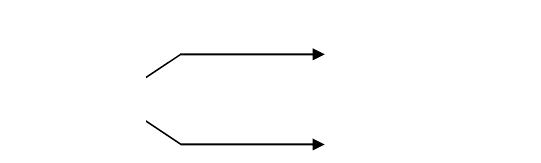
Эффективность катализатора оценивают также по его селективно-
сти (избирательности) – способности ускорять химическое превра-
щение лишь в одном из нескольких возможных направлений, например:
166
В отсутствие катализатора обе реакции идут параллельно. Однако
под действием различных катализаторов и при разных температурах
идет преимущественно одна из них. Зависит селективность главным об-
разом от природы катализатора, а количественно определяется отноше-
нием скорости получения основного продукта к сумме скоростей пре-
вращения исходных веществ. Обычно гомогенные катализаторы обла-
дают большей селективностью (до 95%), чем гетерогенные (около 70%).
Одним из общих свойств гомогенных и гетерогенных катализато-
ров является их специфичность, состоящая в том, что каждый катали-
затор способен ускорять лишь одну реакцию или группу реакций. Так
Ni ускоряет реакции гидрирования, но не влияет на реакции окисления,
а V
2
O
5
– хороший катализатор для реакций окисления, но не гидриро-
вания. Существуют и малоспецифичные катализаторы (Pt, Pd, AlCl
3
),
способные ускорять многие виды реакций. Специфичность катализатора
обусловлена видом химических связей, которые возникают между реа-
гентом и катализатором. В образовании такой связи участвуют не все
молекулы (атомы) катализатора, а лишь определенные их группы – ак-
тивные центры.
При добавлении к катализатору некоторых веществ его активность
и селективность могут измениться. Вещества, увеличивающие актив-
ность катализаторов, называют промоторами, а само явление – про-
мотированием. Понижение каталитической активности называется
отравлением катализатора, а вещества, вызывающие такое отравле-
ние – каталитическими ядами. Как для гомогенных, так и для гетеро-
генных катализаторов каталитическими ядами являются: CO, HCN,
PH
3
, соединения серы, мышьяка, ртути и т.д. Сами по себе промоторы и
каталитические яды на скорость реакции не влияют, но, будучи добав-
ленными даже в ничтожных количествах в реакционную систему, где
находится катализатор, способны значительно (иногда и в сотни раз)
увеличить (в случае промоторов) или уменьшить, а иногда и полностью
подавить (в случае ядов), каталитическое действие катализатора. Счита-
ется, что действие промоторов заключается в их способности разрых-
лять поверхность твердого катализатора, препятствовать его спеканию
при высоких температурах, а также вступать в химическое действие с
активными центрами катализатора, образуя новые структуры с повы-
C
2
H
5
OH
CH
3
COH +Н
2
H
2
C
2
H
4
+ H
2
O
Cu, 200-250°C
Al
2
O
3
, 350-360°C

167
шенной каталитической активностью. Каталитические яды, напротив,
адсорбируясь на активных центрах катализатора, уменьшают их число
или образуют с ними устойчивые инертные соединения, что приводит к
частичному или полному отравлению катализатора.
Гомогенный катализ
Гомогенный катализ широко используется в химической, нефтепе-
рерабатывающей, пищевой, фармацевтической и других отраслях про-
мышленности. В случае гомогенных каталитических процессов катали-
затор образует с реагентами промежуточные реакционноспособные со-
единения. Например, для некоторой реакции:
DBA
в присутствии катализатора протекают две реакции: на первой стадии
образуются частицы промежуточного соединения исходных веществ с
катализатором АВК (через образование активированного комплекса
АВК
#
), на второй стадии происходит распад промежуточного соедине-
ния с образованием продуктов реакции и регенерацией катализатора:
ABKBA
K
KDABK
Примером такого процесса может служить реакция разложения
ацетальдегида, энергия активации которой равна 190 кДж/моль:
COCHCHOCH
43
В присутствии паров йода этот процесс протекает в две стадии:
COHJJCHCHOCH
J
33
2
243
JCHHJJCH
Уменьшение энергии активации этой реакции в присутствии ката-
лизатора составляет 54 к Дж/моль, константа скорости при этом увели-
чивается примерно в 105 раз.
Наиболее распространенным видом гомогенного катализа является
кислотно – основной катализ, при котором в роли катализатора вы-
ступают ионы водорода или гидроксид-ионы.
Между гомогенным и другими видами катализа нет принципиаль-
ной разницы. Во всех случаях ускоряющее действие катализатора сво-
дится к тому, что из нескольких возможных путей реакции с энергети-
ческими барьерами разной высоты он ведет реакцию по пути с наи-
меньшей высотой потенциального барьера и минимальной энергией ак-
тивации. Катализатор, взаимодействуя с реагентами и участвуя в обра-
168
зовании активированного комплекса, уменьшает энергию активации и
таким образом повышает скорость химической реакции.
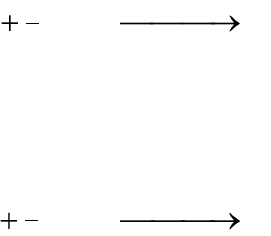
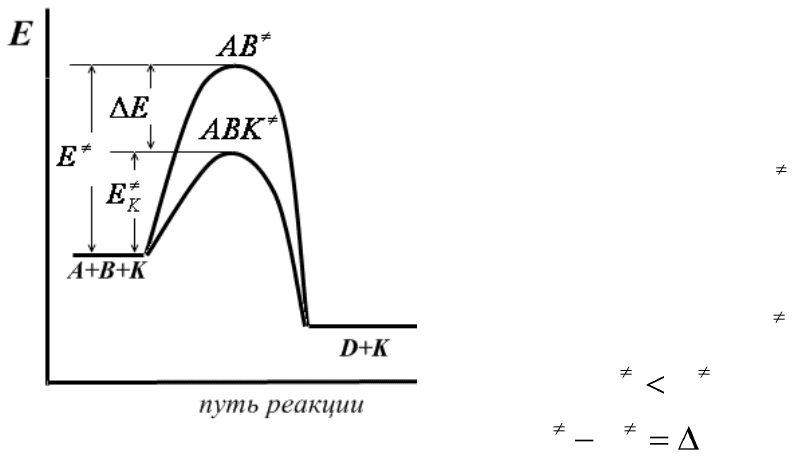
Рис.7.1. Влияние катализатора на
энергию активации
В присутствии катализатора
реакция идет с преодолением
потенциального барьера, высота
которого и соответствующая
ему энергия активации
K
E
зна-
чительно меньше по сравнению
с высотой потенциального барь-
ера и энергией активации нека-
талитической реакцией
E
:
.
;
EEE
EE
K
K
Гетерогенный катализ
При гетерогенном катализе реагирующие вещества и катализатор
находятся в разных фазах, а химическая реакция протекает на границе
раздела этих фаз. Наибольшее распространение получил катализ с твер-
дым катализатором, когда реагирующие вещества находятся в жидкой
или газообразной фазе.
Каталитическое действие твердого катализатора связано с наличи-
ем на его поверхности активных центров, представляющих собой от-
дельные атомы или группу атомов, обладающих повышенной энергией
по сравнению с остальными атомами поверхности. Существование ак-
тивных центров объясняется неоднородностью твердой поверхности,
возникающей в результате различных дефектов кристаллической ре-
шетки. Так как дефекты кристаллической решетки могут быть самыми
различными, активные центры энергетически неравноценны между со-
бой. Поэтому в гетерогенном катализе исключительно большое значе-
ние имеют химический состав, строение и состояние поверхностного
слоя твердого катализатора. Обычно активные центры составляют лишь
небольшую долю твердой поверхности (иногда всего 4–5%) и лишь в
исключительно редких случаях каждая молекула поверхности является
активным центром. В связи с этим важной характеристикой гетероген-
ных катализаторов является удельная поверхность – отношение пло-
169
щади поверхности катализатора к его объему или массе. Чем больше
удельная поверхность и число активных центров на единице поверхно-
сти, тем эффективнее катализатор.
Наиболее высокая удельная поверхность характерна для пористых
катализаторов, у которых стенки пор, уходящих от внешней поверхно-
сти вглубь твердого тела, образуют внутреннюю поверхность, намного
превышающую поверхность внешнюю и способную также участвовать
в каталитической реакции. Если удельная внешняя поверхность зерни-
стого катализатора не превышает 0,01 – 1,0 м
2
/г, то его внутренняя
удельная поверхность может составить от 5 до 500 м
2
/г.
Для увеличения доли поверхностных атомов катализатора его из-
мельчают или наносят на поверхность пористых веществ – носителей, в
качестве которых используют: древесный уголь, пемзу, асбест, силика-
гель, алюмогель, стекло, фарфор и т.д. В таких системах катализатор
располагается на стенках пор носителя в виде частиц размером 2 – 20
нм. Таким образом повышается эффективность использования единицы
массы катализатора и его экономия, что имеет большое значение при
использовании таких дорогостоящих катализаторов, как платина, пал-
ладий, осмий, иридий, рений, золото и серебро.
По своей сути гетерогенный катализ аналогичен гомогенному: ка-
тализатор, вступая во временное химической взаимодействие с реаги-
рующими веществами с образованием активированного комплекса или
неустойчивого промежуточного соединения, ведет реакцию по новому
пути с минимальным энергетическим барьером. Обычно снижение
энергии активации в гетерогенном катализе приводит к росту скорости
реакций в 10
6
– 10
16
раз.
На эффективность твердых катализаторов большое влияние оказы-
вают промоторы и каталитические яды. Промоторы способствуют со-
хранению активных центов, их устойчивости к изменению внешних ус-
ловий, препятствуют сокращению удельной поверхности, а также по-
вышают активность и селективность катализатора путем изменения
строения и химического состава активных центров. Каталитические
яды, напротив, дезактивируют поверхность катализатора за счет осаж-
дения на активных центрах и выключения их из каталитического про-
цесса, а также за счет изменения их химического состава и строения,
что может привести даже к изменению направления реакции.
Гетерогенная каталитическая реакция представляет собой сложный
процесс, протекающий через несколько основных стадий:
1) доставка исходных веществ к поверхности катализатора;
2) адсорбция исходных веществ на поверхности катализатора;
170
3) химическая реакция с образованием продуктов, адсорбирован-
ных на поверхности катализатора;
4) десорбция продуктов реакции с поверхности катализатора;
5) удаление продуктов реакции от поверхности катализатора.
Общая скорость такого многостадийного процесса определяется
самой медленной (лимитирующей) стадией и может подчиняться зако-
номерностям диффузии, адсорбции или химической кинетики.
Уменьшение энергии активации – основная, но не единственная
причина ускорения гетерогенной каталитической реакции. Катализатор
не только снижает энергетический барьер, а создает новые, энергетиче-
ски более выгодные пути протекания реакции. При этом эффективность
гетерогенного катализатора определяется структурой и химическим со-
ставом его поверхностного слоя, а также соответствием между химиче-
скими свойствами катализатора и реагирующих веществ.
Причины, вызывающее каталитическое действие, многообразны и
не поддаются точному расчету. Этим обстоятельством объясняется от-
сутствие единой современной теории гетерогенного катализа. Сущест-
вующие теоретические положения могут дать лишь некоторые общие
указания при выборе катализатора для той или иной реакции:
1. Катализатором может быть вещество, способное образовывать
промежуточное поверхностное соединение с реагирующими вещества-
ми.
2. Промежуточное поверхностное соединение должно быть менее
прочным, чем конечные продукты реакции.
3. Катализатор должен быть активным (то есть значительно сни-
жать энергию активации), селективным, стабильным и способным к ре-
генерации.
4. Катализатор должен иметь максимально развитую поверхность,
наибольшее число активных центров на поверхности, оптимальную
энергию связи с молекулами реагирующих веществ, достаточную меха-
ническую прочность и т.д.
Многие современные промышленные катализаторы представляют
собой многокомпонентные и многофазные системы, в которых поверх-
ность катализатора состоит из кристаллов нескольких различных ве-
ществ, что позволяет ускорять различные стадии сложного каталитиче-
ского процесса на различных участках поверхности.
Особое место среди гетерогенных катализаторов занимают природ-
ные и синтетические цеолиты (алюмосиликаты), обладающие настолько
большими параметрами кристаллической решетки, что молекулы реа-
гентов могут проникать внутрь кристалла, каталитическая реакция в
этом случае осуществляется при участии практически всех внешних и
