Куликов И.С. Термодинамика карбидов и нитридов
Подождите немного. Документ загружается.

|
\Р,э€,
как
с.,|едует
п7
та6л.9.6,
воэможно
лишь
при
температурах
>3000к.
ч4н1ко
эти
данныР
следует
считать
приблил<енными
и.
требующими
уточ-
нения- |
|лава
10
-
кАРБидь|
элвмвнтов
гРуппь|
у||А
|. систвмА
|!|п_€
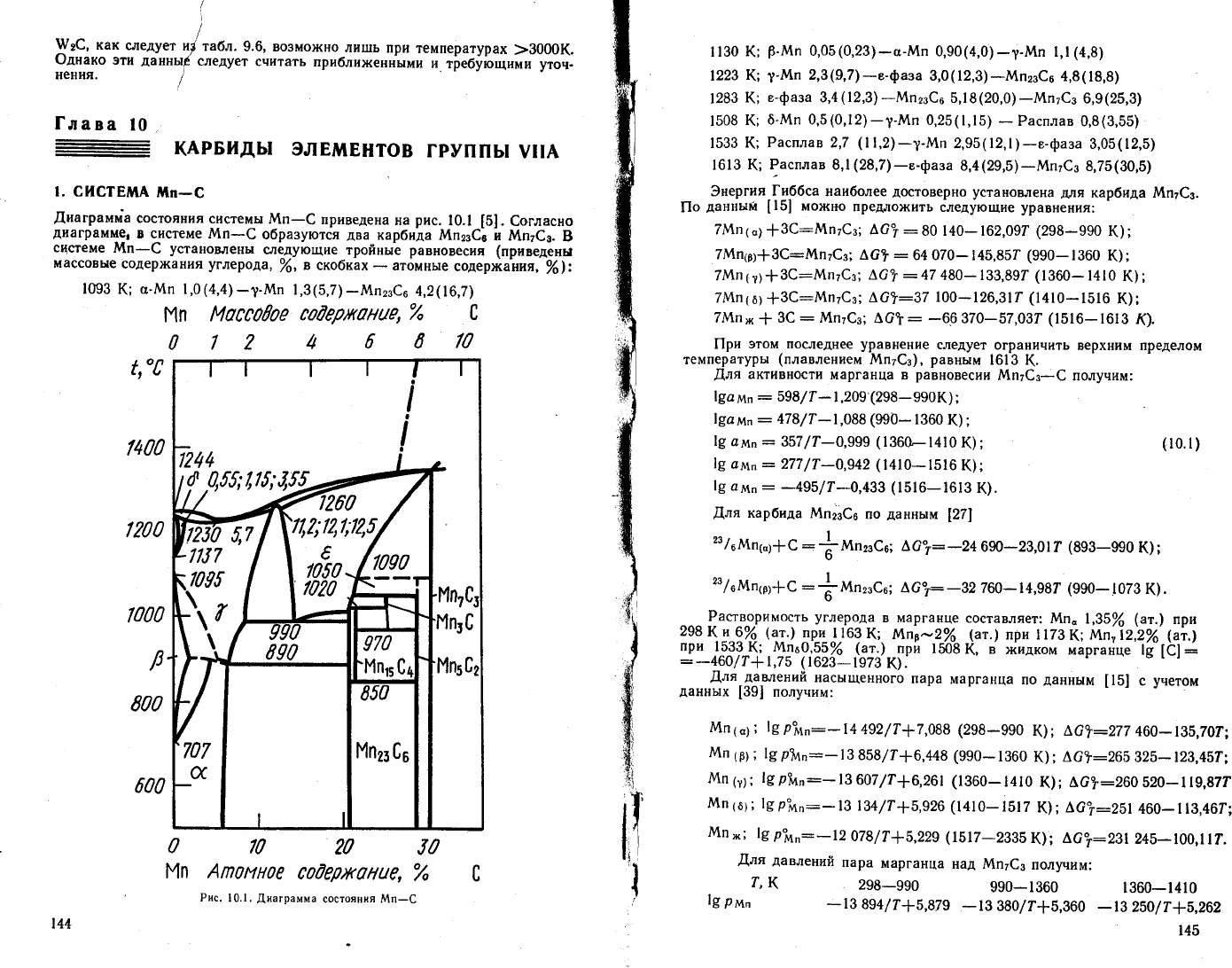
.|!,иаграмйа
состояния
системы
/у1п-€
пРиведена
на
рис.
10.!
!5]
.
€огласно
диаграмме,
в с*|стеме йп_€
образуются
два
карбида ]{п:з€о
й мпасз.
8
сцстеме
.!!1п_€
установлены
слфующие
тройны}
равновесия
(приведенн
массовые
содер)кания
углерода' /9,
в
ско6ках
_
атомные
содер:кавия'
/9):
|Ф3
(;
о.йп 1'0(4'4)_т-мп
|,3(5,7)_&1пэз€о
4,2(16,7\
14п
/"/ассп8ое
со0ер//0нце, %
с
46670
!|30 к;
$.йп
0'05(0'23)-с_йп
0'90(4'0)_т_мп
1,!
(4,8)
1223
\\;
1_|*1п
2'3(9'7)_е_фаза
3'0(12'3)*!т1п23с6
4'8(18,8)
!283
(;
е-фаза
3'4(!2'3)-}1пэз€о
5'|8(20'0)-мп:€з
6'9(25'3)
|508
(;
6-}1п 0'5(0'|2)_т-/у1п
0'25(|'|5)
_
Расплав
0'8(3'55)
!533
к;
Расплав
2'7
(!\'2)-у-|т1п
2,95(|2,|)-в-фаза
3'05(12,5)
|613
(;
Расплав 8'1
(28'7)-е_фаза
8,4(29,5)-]!1па€з
8,75(30,5)
3нергия
_[иббса
наиболее
достоверно
установ]|ена
!,ля
кар6п\а .]\,!пт€з.
!|о
данным
[!5]
можно
преш[о)!(ить
следующие
уравнения:
7!{п
1о;
*3€:]!1па€з;
А6?
:
80 [40_ 162,097
(298_990
();
7|!1п1р1}3€:/т1пт€з;
А6}
:
64 070_ |45,85г
(990_
|360
к);
71!1п111}3€::}1пт€з;
^с}:47
480_ 133,89г (!3ф_|4|0
();
7|![п1о1
{3€:/м1пт(1:
^6?:37
100_126'31г
(1410_1516
();
7йп*
{
3€
:
,&1пт€з;
^61:
_66
370_57,03г
(|516_16|3
к).
||ри
этом.последнее
уравнение
следует
ограничить
верхним пределом
температуры
(плавлением
мп7сз),
равным
|6!3
к.
.(ля
активности
марганца
в
равновесии
}1пт€з_€
получим:
|3с
ц,
:
598
/
т
-
''2о9
(298_990()
;
|9'м.
-
47в/т-!'о8в (990_
1360
к);
19сд6:357/г-0'999
(1360-1410();
(10.1)
1д
сц'
:
277
/
т-о,942
(
1410* |516
к)
;
|9 см'
-
_495/т_о'433
(1516_!6|3
к).
.(ля
карбида
йпэз€о
по
данным
[27]
237о
|,1п1.1{
€
=
{
м,''с';
[6"':
_246ю_23,0
|
г
(в93-Ф0
к)
;
237о,|{п1р14с
:{мпязсо;
\6'':_32760_|4,98г (990_|073
к).
^^^
Раст_в_оримость
углерода
в марганце
составляет:
!'гтп"
|,35/6
(ат.)
при
298
1<'.и^67э
(ат)
1р-и^|163
\\;
г{тпр-э/.
(ат.)
при |173к;
мп'\э'эц'с,а:г.7
при
1533_(;
.{з'9,!9%
_(9].)--,р"
|508к,
в
жидком
маргаг|ше !ы[с]
:
:_46о/т+
|'75 (1623-!973
к):
.(ля давлений
нась|ще|{ного
пара
марганца
по
данным
[15]
с
унетом
даннь|х
[39]
полуним:
]!1п1с1!
|9рй':_14
492/т+7,}вв (29в*990
&\;
ББ0|:эт7
460_|35,707;
}1п
1р1
!
|9
р!т.:-!3
в5в/г+6,44в
(990-1360
()
;
^6}:265
325_123,45[:
:!1п
1'1
;
|8
Рйп:_|3
607
/т+6,261
(1360_!410
();
^6}:260
520_1
|9,87[;
]!1'со);
|врй':_|3
\34/т+5,926 (|4|0_|5|7
к)
;
ьс.т:25|
460-113,46[;
}и1п
д
;
|3
Р"м,:
_
12
о7в
/
т
+5'229
(
15
17-2335
к)
;
^с?:231
245_
100, 1 1
г.
.(ля
давлений
пара
марганца
над /{пт€з
полу{им:
г,
к
298_990
990_1360
|360_1410
|в
рм,
_13
894/г+5,879
_13
3в0/т+5,360
_\325о/т+5'262
145
!'"[
/400
0 72
07020
10
[4п Апопное
с0аер/онце,
%
Рис.
10.1.
.[|.награмма
состояния |у1п_€
7000
800
р
|т
'!
{ !,[5;/,т$;,$!
|230
а7
144
т,к
|8
рм,
!410-1516
1516-16|7
_|2
857
/т +4'984
-12
573/т
+4'796
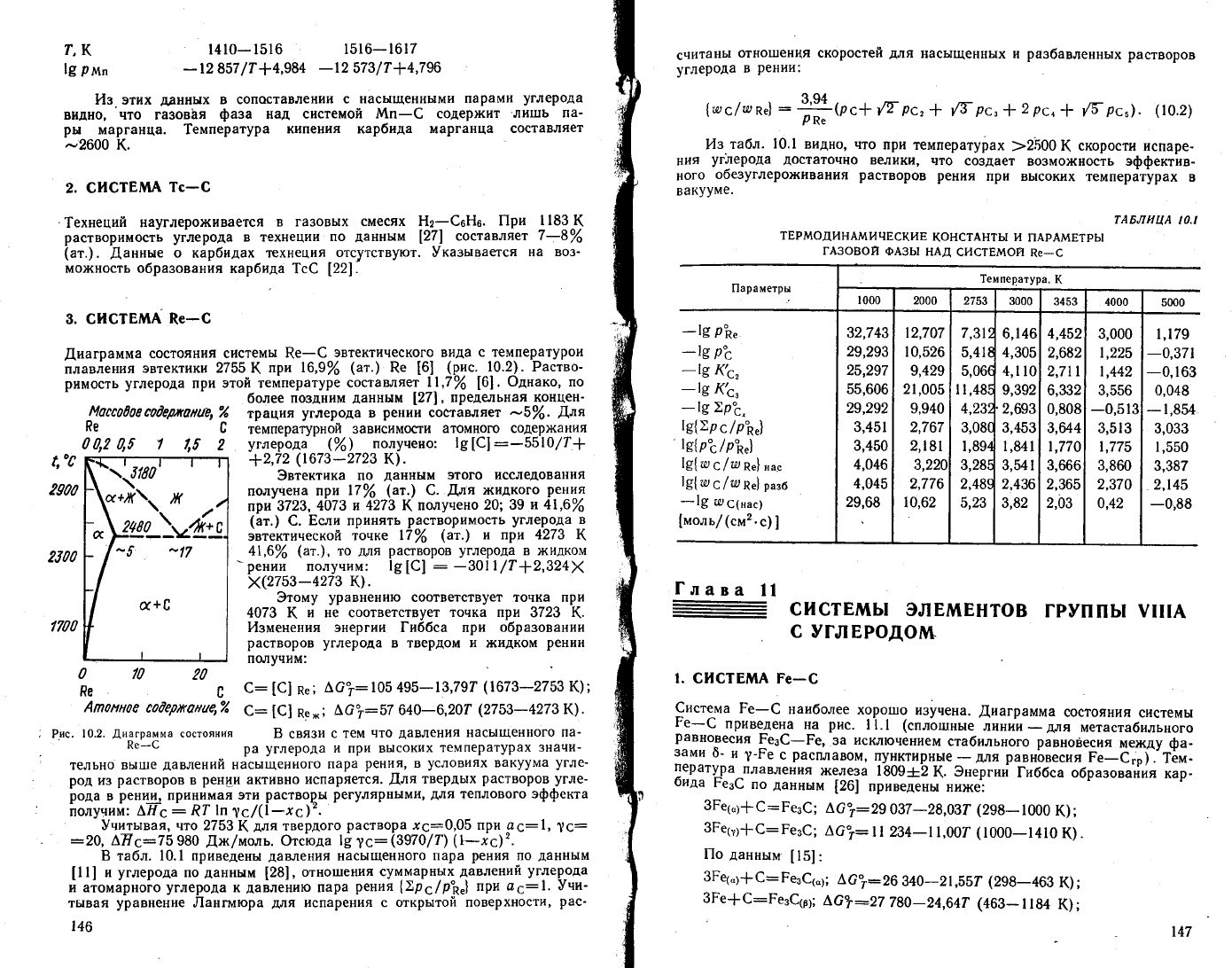
.[|,иаграмма
состояния
системы
Ре-6
эвтектического вида
с температурои
плавйения
эвтектики 2755( при
|6'9%
(ат.)
&е
[6]
(рис.
10.2). Раство_
римость
углерода
при
этой тейпературе
составляет
\!'7%
|61.
Фднако, по
[7ассоФесо0ерхансе,%жн?*Ёх#]Ё"|,'?;.}3"?#}т5йтж;
пе
6
темперацрной зависимости
атомного содержания
0 0.2 п' 1 |5 2 углеоола
(о/"\
получено:
|д
]€,!:_5510/1-Ё
0
ц2
ц'
1 1,'
2
углерода
(%\
получено:
|9
[с]
:_5510/г{
''
оа
п\и1_т1
*''1'"{]!]1;'?''
}],,""
этого исследования
:заа
[\\.
х
,)
;;*ч#;'
\81'''{,у;',|Р"3;#,]"
}#'^;;т #Ёи
|"|ес\4*.]]:;;].*;"'.11}"Р"1,}Ё"'Р#'?:1:/т'"";#!%"й
отлл[ !-5
-17
|
4|'6%
(ат.),
то
для
растворов
углерода
в )кидком
*-'1
| |_рении
получим:
!в[с]
:_30'\/т+2'324х
Аз.этих
данных
в сопоставлении
с
насыщенными
парами
углерода
видно, что газов[ая
фаза
вад системой
;!1п-€ содер'(ит
'ли|!]ь
па_
ры
марганца. 1емпература
кипения карбида марганца
составляет
-2600
к.
2. €}!€тР1|1А
1с_€
1ехнеций
[{ауглероживается
в газовых
смесях Ё:-€оЁо.
|1ри
!
18?^к
растворимость
углерода
в технеци!!
по
данным
[27]
составляет
7-8/6
(ат.).
Аанные
о
карбидах
технеция
отсутствуют. }казывается
на воз_
мо)кность образования
карбида
1с€
[22].
3. систвмА пе-с
рении
получим: |в
[с]
:
_30'1
/т +2'324х
х(2753_4273
к)
'
9тому
уравнению
соответствует точка при
4073
к
и не соответствует
точка при
3723
(.
1700
!| |
йзменения энергии [иббса при
образовавии
растворов
углерода
в твердом и )!(идком
рении
по;|учим:
01020
Ре
6
€:
[€]
ке;
А6'т:105 495-13'79г
(1673_2753
к);
Апонное
с0аерйа/!це'%
с:
[€]
п:*;
Б6..:57 640-6,20т
(2753-4273к,.
Ряс.
|0.2.
.[1иаграмма
состояния
Б связи
с тем
что
давления
насыщенного па-
Ре_€
ра углерода
и
при
высоких
температурах
3начи-
тельно выше
давлений
насыщенного
пара
рения,
в
условиях
вакуума
угле_
род
из
растворов
в
рени_и
активно
испаряется.
[ля
твердых
растворов угле-
рода
в
рениц
принимая
эти
раствоРы
Регулярными,
для
теплового эффекта
получим:
ьн
с:
Р[
\п
11/(_х9)'.
}чить:вая, что 27531(
для
твердого
раствора
хс:0'05 при сс:1,
тс:
:2|,
[Ёс:75 980
.||я</моль.
Фтсюда
19
тс:
(397о/т) (1_хс)'.
8
табл.
10.1
привелены
давления
насыщенного
пара
рения
по
данным
[1!]
и
углерода
по
данным
[28],
отно:шения
суммарнь!х
давлений
углерода
и атомарного
углерода
к
давлению
пара
рения
{>рс/р1а.}
при сс:1.
учи_
тывая
уравнение
/1ангмюра
д|я
испарения с
открытой поверхности,
рас_
146
1(
>а|
-17
считаны
отно1ценця скоростей
для
насыщенных
и
разбавленных
растворов
углерода
в
рении:
{шс/шп"\:
}},'.*
{|
рс,* {'{
рс,*
2
рс'*
{'!!рс,).
(|0.2)
Аз
табл.
|0.!
видно, что
при
температурах
>2500
к
скорости испаре_
ния
углерода
достаточно
велики'
что создает
возможнос1ь эффект!-:в-
ного
обезуглеРо).(ивания
растворов
рения
при вь[соких
температурах
в
вакууме'
тАБл||цА
!0.|
твРмодинАмичвскив
констАнть|
и
пАРАмвтРь|
гАзовои
ФАзь|
нАд
€й€1ЁйФй
Ре_€
|'лава
|!
-
систвмь|
элвмвнтов
гРуппь| у!|!А
с углвРодо}1
!. €||€1Ё'1}1А Ре_€
€истема
Ре-€
наиболее
хорошо
изучена.
[иаграмма
состояния
системь|
Ре-€
привелена
на
рис.
|!.1
(сплошньпе'линии
_дпя
метастабильного
р_авновесия
Рез€-Ре,
за
исключением
стабильного
равноЁесия
мея<ду
фа-
11ми
о-
и
1_Ре
с
расгиавом'
пунктирные
-
для
равновесия
Ре-€19).'тё"-
пература^плавления
желе3а
1809*2
(.
3нергий
[иббса образоваЁйя
кар-
оида
ге3с
по
данным
[26]
привелены
ниже:
3Ре16}
(
:
|9з€
;
А6):29
о37
_28,о3т
(29в_
1
000
к)
;
3Ре1'1{(:р9з€;
А6!:
|1 234-|1,00г
(!000-1410
к).
||о
данным
[15]:
3Ре1.1{
€: Рез€1.1;
А
6):
!
6 34о-2\,55т
(
29в-463
к)
;
3Ре*
€: Без€
<ру:
Б6?
:27
78о
_24,64т
(463_
| | в4
к)
;
[араметры
1емпература,
[(
1000
2000
2753
3000
3453
4000
5Ф0
-|в
р1а"
-|в
рё
-|9
|(с,
-|в
('с,
-|в
>рё'
|в{>р
с
/р"п.}
:в{р"с
/р"п")
|8{
ш
с
/о пе}
на.с
]8(шс/опе}
разо
-19
<о
с(""с)
[моль/
(см2.
с)
]
32,743
29,293
25,297
55,606
29,292
3,451
3,450
4,046
4'о45
29,68
12'7о7
10,526
9,429
21,005
9,940
2,767
2,1
81
3,22с
2,776
10,62
7,}\,
5,41{
5,06(
1 1,481
4,23,
3,08(
!,894
3,28{
2,48{
5,23
6,146
4,305
4,1
10
9,392
2'ф3
3,453
!
,841
3,54 |
2,436
3,82
4, 452
2,682
2,711
6,332
0,808
3,644
|
'77о
3,666
2,365
2,о3
3,000
1,225
\,442
3,556
-0,513
3,5!3
1,775
3'8Ф
2,370
0,42
1,179
-0,371
-0,163
0,048
-1'8и
3,033
1,550
3,387
2,145
-0,88
\47
3Рч11{€:
Реа€1р1
;
А6!:
|2
070-
1 1'39г
(
1 1
84-
1665
()
;
3Ре1о1$ €:
Ре
з€
р11
['
6"7:
/ 6| о
-8'7
2т
(
1 665_ 1
809
()
;
3Ре
ж*'€:
Рез€1р;
;
А6"1:
_39
800+ 1 7'52г
(
1 809_2ф0
к)
.
}1з приведенннх
уравнений
епедует'
нто карбид
0_Рез€
сгабилен
в
ин_
тервале
[тэт_уооо
1(,-по
данным
[15]
_
выше 1080
к'
поданяым
[26|
-
вь|ше
1020
|(.9читывая
ска3анное
о стабильности
кар6ида
Рез€
при
темпе_
.[|ля
линии
солидус
растворимость
углерода
в
1-Ре [21]
состаы1яет:
[€]
**:
:8.59_5'62
.
10_'г.
Растворимость
углерода
в жидком
я{ф|е3е
[76]
характеризуется
^выражени-
ем
[€]
**:1'34+2'53
'
|0_' т
(|473-
_1973
к).
1!реде'|
растворимости
углерода
в
о-ге
при
равновесии
с
Рез€
[77]
составляет;
18
[с]
**:0'31
-2645
/
т
(573-993
к).
8сли выделяющийся
цементит
суще-
072.1
45
ге масс000е со0ерханое,
% Ё
||релот
растворимости углерода
в
о-Ре
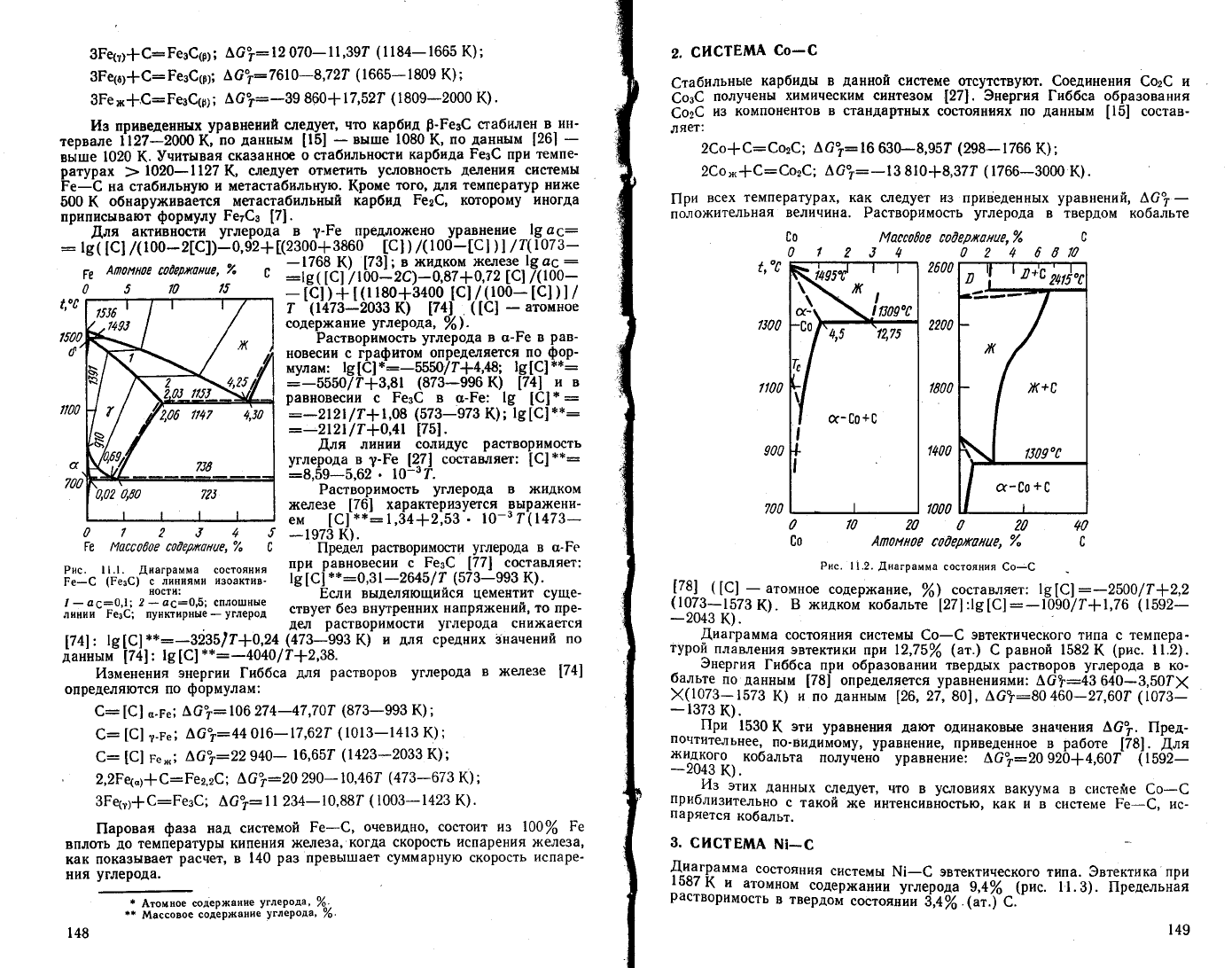
Рис. !|.|.
Аиаграмма
состояния
}ру
Ре_€
(Реа€)
с
линиям! изоактив'
ности:
1
_
о6:0];
2
_
а6:Ф$1 сплошные
;;;"т;;ё!'"_'"1!"]]Ё;]'}!#ЁЁй
ствует
без
внутренних
напрях<ений, то пре-
]7{ ]
: [
в [6 ]
* *
:
_3,3ь
/
т+0,%
Ё%]#?у?т#
.}:Ё'""Ё"-"
н:#;ч;
данным
[7{]
:
|9
[с]
**:_4040/|
*2,38.
}1зменения
энергии
|иббса
для
растворов
углерода
в х<олезе
[74]
определяются
по
формулам:
€:
[€]
о.ге]
А6?:
106 274-47'7от
(873-993
к)
;
€:
[€]
т_Ре}
А6"1.:{4016_17'62т
(1013-1413
();
с:
1с]
Реу1
Б6"7:|! 940-
16'65г
(1423*2033
к);
'
2,2Рчо*€:Ре:,э€;
Б6"':29296-10,46|
(473-673();
3Рч'1-|€:Рез€; А6'': 1 1 234-10'88г
(
1003-1423
к).
||аровая
фаза
над системой
Ре_€,
очевидно, состоит из 100/'
Ре
вплоть
до
температуры
кипения
желе3а'
когда скорость
испарения
)келе3а'
как
показывает
расчет,
в 140
раз
превы1шает
суммарную скорость
испаре_
ния
углерода.
ратурах
>
|02о_\\27 |(, следует
отметить
условность
дФ|ения
системы
Ре-€ на
стабильную
и метастабильщю.
кроме
того,
д'|я
температур них(е
500
(
о6наРух<ивается мегастабильный
карбид
Реэ€,
которому
иногда
приписывают
формулу
ге7с3
[7].
-
!,ля
актиБносйи_углерода
в
1-Ре
предлоя(ено
уравнение
|9а6:
:
|9(
[€] /(
100_2[с])_0,92+
к2300+3860
|с]
) /(
100_гс]
) ]
/т(
1 073_
_1768
к)
[73];
в жидком
же,,|езе
19с6:
содер'(ание
углерода'
7о'.
Растворимость
углеРода
в с-Ре
в
рав_
новесии с графптом
опреде'|яется
по
фор-
мулам:
|3[€]*:-55ы/т+4'8;
!9[€]**:
:-55бо/т+3'81 (873-996
к)
|74|
п
ъ
равновесии
с Рез€
в
о-Ре:
[9
[€]
*
:
:_2!2\
/
т+1'08
(573-973
()
;
|в
[€]
**:
:-2|2\
/т+0'41 [75]
.
148
*
Атомвое
содерханпе
углерола,
7о.-
**
массовое
сод?рхание
углерода'
%.
149
а.
€}!€1Ё]}1А
€о-€
€табильнь:е
карбиды в
даняой
системе
отсутствуют. €оединения
€о:€ и
€о3€
полуяены
химическим синтезом
|27|.
9нергпя [иббса образования
(оэ(
пцз компонентов
в
стандартных
состояниях
по
данным
[1б]
состав-
ляет:
2€о*6:€оэ€;
^с?:16
630_8'95т
(298_|766
();
!(9*$€:€оэ€;
А6!:_13
810+8'37г
(
1766-3000
к).
|1ри
всех
темперацрах, как следует из
приведеннь:х
уравнений,
66'т_
положительная
величина.
Растворимость
углерода
в твердом кобальте
с0
["1ассо8ое со0ерасанше,%
с
0
|
2 3 4 0 2 4 6 870
2600
7300
п00
900
1000
{''€
700
0702002040
[о Ап0мн0е
со0ерханше,
7"
с
Рис. 11.2.
диаграмма
состояния
€о:€
{78]
(
гс]
-
атомное
содержание'
/9)
составляет:
|9[€]
:_2500/т+2,2
(|073_1573
|().
Б х<идком
кобальте
[27|:|9[€]
:-|090/г+1,76
(1592-
_2043
к).
.(иаграмма состояния системы 6о-€
эвтектического
типа с темпера-
туроц
плавления
эвтектики
прп \2,75/1
(ат.)
6
равной
1582(
(рис.
11.2).
-
3нергия
[иббса
при образовании'твердых
растворов
углерода
в ко-
бальте
по
данным
[78]
опрелеляется
уравнениями:
А6}:43
640_3,50гх
х(!{_3
|573
к)
и
по
даннь|м
|2в'
27' в0],
А6}:60 46о-27,60т
(|073_
_
1373
к).
|1ри
1530
!( эти
уравнения
дарт
одинаковые
3начения
А6!.
||рел-
почтительнее'
по_видимому'
уравнение'
приведенное в
работе [78].
Аля
жидкого
кобальта
получено
уравнение:
Б6"':2992о+4,60г
(1592-
_2043
к).
-14з
этих
даннь[х следует' что
в
условиях
вакуума
в систейе
€о-€
приблизительно
с такой
х(е
интенсивностью'
как й""
сис'"'*
Ре-€,
ис_
паряется
кобальт.
3.
систвмА
ш|_с
$,11гр3мма
состояния
системы
!.{|-€
эвтектического типа. эвтектика
при
]19'к
,
атомном
содер)кании
углерода
9,4/,
@*лс.
11.3).
||релельн1я
растворимость
в
тверАой
состоя::-ии
5'+%
'<6т.[с.
\
о(-,
ж
с-с0+о
|
!
1100ос
12,75
4,5
ж+с
1309
"с

Фаза }.,[!з€ существует ли!шь в
метаста6ильном
виде.
9нергия [иббса
образования
этой
фазы,
по
данным
[!5],
составляет:
Ас?*33 890-7'03г
(э98-
1726
();
А6!:-1ц 225+2о'92т
(1726-ю00
к).
||о
данным
[26]'
^с?:39
760_17'16т
(298-773
к).
3кспериментально при
цементации
в токе
€Ф при
523_673
1(
полупен
карбид
\!з€.
||ри
температурах
>
673
к
карбил не образуется.
||релелы
растворимости углерода
в твердом
и
жидком
никеле
[27,80]
составляот
(
1с]
-
атомное со!ержание
углерода,
/9):
'7
[7ассо0ое со0ерханае,
%
,
0/
2 4 6 /0
[''€
1700
/500
/300
//00
010201040
.ш'
1
А',"',,
со0ерханае,
%
с
Рис. | |.3.
.[1иаграмма
состояния
ш!_с
|9
{(]:-260о/т+2'2
(773-1573
();
19
[€]:_696/т+|,55
(1673-!973
к).
.[!ля
энергий |'иббса при образовании
Растворов
углерода
в твердом
и
жидком
никеле получим:
с:
1с]
ш;;
А6?:49 780-3,83т
(773_|573
к);
с:
]с]
ш:*;
А6}:|7 150+8'62г
(1673-1973
к).
||оведение системы
ш!-с
в вакшме
аналогично поведению систем
Ре-€
и
€о_€.
4. систвмь|
&ш_€,
пь_с,
Ра_с
€истемы &ц_€, кь-с,
Р6-€
имеют эвтектические
диаграммы
состояния
[7].
по
данным
[5],
в
рутении
при
температуре кипения
растворяется
4'8% с,
в жидком
ролии
(23Ф-3900
к)
растворимость
от 1,42
до
7
'38/1
(;
в жидком
палладии
-
2'45% €.
9втектические
температуры
составляют
для
рутения
|
э:22|5
(,
7,,:2523 1(;
для
родия'[":1967(
1,,:2236
(;
для
палладия
[
":1777
|(, 1пл:
1825
к.
150
Атомные
концентрации
углерода
в эвтектиках
(нислитель)
и пределы
растворимости
в тве$лом с6стойнии
(знаменатель)
приведены
нн>ке,
/,:
|", |(
|€|'%
(ат)
Рц_€
22|5
эвт
/
т.
кп_с
1967
15'5
/
3'75
Рс_с
|777
/
-5
!,ля растворов'углерода
[27]
(атомное
содер)кание'
!/р)
ь
рутенпп
!ц
1€1:-443в/т+3'о2
(1073_1523
();
^о'т:84
970_
19'53г'
в
родии
1[
!6!
:-+613/т+3,05 (1073-1523
();
^с1:вв
32о_20'\от'
в палла'
д"ий*
!3
1с|:_3022/т+2,42
{1о73_1673
к);
^о"т:|;7
860_8'04г.
1емпературы
кипения
рутения'
родия
и палладия
соответственно
со'
ставляют
]39]:
4423' 3970
п 3237 }(.
|1оскольку
температура
сублимации
графита
3990
к
то возмо}кности-
разго!|ки
в нейтральном'вакууме
ограни_
нёнйо
сушествуют
для
рутения
(преимушественное испарение
углерода)
и
палладйя-(прёимушественное
испарение
палладия),
подобно,
например'
системе
\|_€.
Фднако наиболее
эффективным процессом
обезуглеро>ки'
вания
палладия
является окисление
углерода.
Рутений,
родий
и
палладий
образуют
газообразные
соединения
с
углеродом:
Рц€'
Р[€
и Р6€' энергии
диссоциации
которых со0тветственно
!авны
[25]
: 632*|7,582+13
и 531 кАх</моль.
3нергия
диссоциации.Р^6€
6ценена
по
экстрапо][яции.
|1ри сверхнизких
температурах
(1'28-1'9
к
и менее)
карбидй
родия
и
рутения
&}:€
и
&ц6
являются сверхпроводни_
ками
[25].
|16
уравнению
(1.35)
дгя
констант
атомизации газообразных
моле-
кул
получим:
19
('р"6:_
(33
663*870)
/т*6'270*0'038;
!9
('д66:-
(31
040-1650)
/г*6'1
58*0'028;
|8
къас:_28
4\8/
т
+6'045'
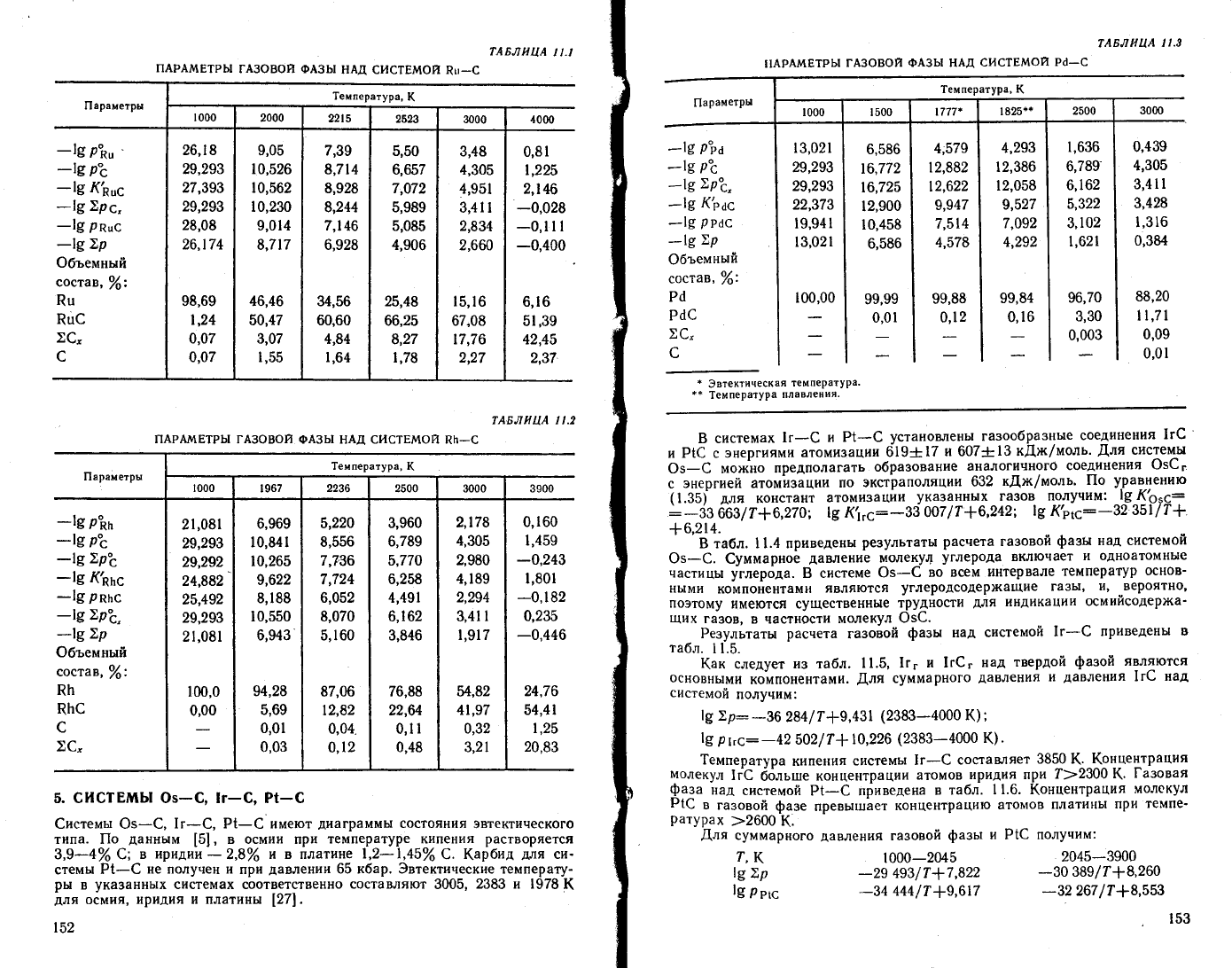
Б табл. 11.1
приведено
сопоставление
давлений
насышенного
пара
Рш,
(, ("
и
Рц€.
|1о
данным
тай.
11.1 полувим:
18
рк,с:-36
020/т+9,|16
(2215_4000
();
19
)р:-3о 373/т+9'493
(22|5-4000
к).
'
1емпература
кипения
системы
&ц-€
3830 1(
ниже температуры
субли_
мации
графита
в свя3и
с тем'
что при высоких
температурах
в газовую
фазу
переходит
главным
образом
&ш€.
Б
табл. 11.2 приведено
сопоставле_
ние
давлений
пара
родия,
углерода
и
&}:€.
,0,ля
пара
&1т€
по
данным
табл.
11.2
полуним:
|8
р
кьс:-33
2\7
/т +8'699
(
1э67_39Ф
();
!9
)р:_29
324/т+7,965
(1967_3900
к)'
йз
э'д,:х
даннь!х
следует,
что температура
кипения
системы
составит
3680
к'
т.
е.
существенно
ни)ке температур
кипения
родия
и
углерода'
и
потери
родия
в
газовую
фазу
в виде мо'|ецл
&[п€
больще,
чем атомарного
родия.
8 табл.
|1.3 приведены
аналогичные
данные
для
палладия.
. _ 4'"
с}мм6рного
давления
газовой
фазы
полувим:
|9 )р:-13
28о|т+
*5,71.
1емпер6тура
кипения системы
равпа
32ф|(
и лишь немного
ниже
температуры
кипения
палладия 3237
к.
+
в
ра6оте
[27!
для
палладия
пр{{ пересчетах
допущена
ошибка.
151
пАРАмвтРь|
гА3овои фА3ь[
нАд €и€1БйФй
Рш_€
['|араметрн
1емпература,
(
1000
2000
2215 262з
3000 1000
-|8
р'п"
'
-|в
р?
_|8
('п,с
*|8
}рс,
-|8
рп'с
_|9
)р
Фбъемный
состав'
/6:
Рц
Рц€
'с,
с
26,1 8
29,293
27,393
29,293
28,08
26,174
98,69
|,24
0,07
о'о7
9,05
10,526
10,562
10,230
9,014
8'7\т
46,46
5о'47
3'о7
|,55
7,39
8,714
8,928
8,244
7,146
6,928
34,56
60,60
4,84
1,64
5,50
6,657
7
'о72
5,989
5,085
4,906
25,48
66,25
8,27
|,78
3,48
4,305
4,951
3д1 |
2,834
2'6ф
|5,|6
67,08
!7,76
2,27
0,81
|'22ь
2,14$
-0,028
-0,1
1 !
-0,400
6,|6
5!,39
42,45
2,37
тАБлнцА
! !.1
тАБл||цА 11.2
5. систвмь| Фэ_€, !г_€' Р|_€
€истемь: Фз-€,
|г_€, Р1-€ имеют
диаграммы
состояния
эвтектического
типа. ||о
данным
[5],
в осмии при
температуре кипения
растворяется
3,9_4% €;
в
иридии
-2'8%
и в платине
12_|'45%
€.
(арбид
дпя
си-
стемы
Р1_(
не получен и
при
давлении
65 кбар. 3втектические темперац-
ры
в
указаннь!х
системах соответствевно
составляют
3ш5'
2383 и 1978
(
для
осмия'
\\р|1дпя и платины
[27].
132
пАРАмвтРь|
гА3овои ФА3ь| нАд систвмои
пь_с
[1араметры
1емпература,
(
1000 1967 22з6 2500 ю00 3900
_|в
р'пь
_|в
рё
_1в
>р'с
_|в
('пьс
_|в
рпьс
-|в
>р?,
_|в
2р
Фбъем::ый
состав,
/9:
&ь
кьс
с
>с,
21,081
29,293
29,292
24,882
25,492
29,293
2 1,081
1ш'0
у
6,969
10,841
10,265
9,622
8,188
10,550
6'и3
94,28
5,69
0,01
0,03
5'22о
8,556
7,7в6
7,724
6,052
8,070
5,1 60
87,06
12,82
0,04
0.12
3,960
6,789
5,770
6,258
4,49!
6,162
3,846
76,88
22'Ф
0,|
|
0.48
2,178
4,305
2,980
4, 189
2,294
3,4!
1
1,917
ь4'82
41,97
0,32
3,21
0,|60
1,459
-0,243
1,801
-0,182
0,235
-0,446
24,76
54,41
1,26
20,83
тАБл|1цА
11.3
1|АРАмвтРь[
гА3овои ФА3ь! нАд
систвмои
Ра_с
1емпература,
|(
|[араметры
-|€
р'ра
_|в
р"с
-.1в
>рё,
_|в
(!,ас
_\у
реас
_|в
2р
Фбъемный
состав,
$:
Ра
Рас
!с,
с
13,021
29,293
29,293
22,373
19,941
13,021
'ч'
6,586
16,772
\в'725
12,900
10,458
6,586
99,99
у'
4;579
12,882
12,622
9,947
7,514
4,578
99,88
у'
4,293
12,386
12,058
9,527
7
'о92
4,292
99,84
0,16
1,636
6,789
6,162
6,322
3,102
1,62!
96,70
3,30
0,003
0,439
4,305
3,411
3,428
1,3
16
0,384
88,20
|
1,71
0,09
0,01
*
3втектическая
температура.
**
1емперлура
плавления.
Б системах
!г_€
и Р1*6
установлены
газообразные
соединения
1г0
и Р{€ с энергиями
атомизации
619*17
и
607:!13
кАж/моль.
Аля
системы
Фэ-€ мож1о
предполагать
образование
аналогичного
соединения
Фз€"
с
энергией атом1.:зации
по
экстраполяции
632
к,[,ж/моль.
|1о
урав-нению
(
1.35[
для
констант
атомизации
указанных
газов_
п_о-лучим:
_!^в^{1ояс:
_-5з
ооз/г+о,это;
19
(!,.:*3]
007/|
*6'2ц2:
19
('р,.:-32
35!/т+
+6,214.
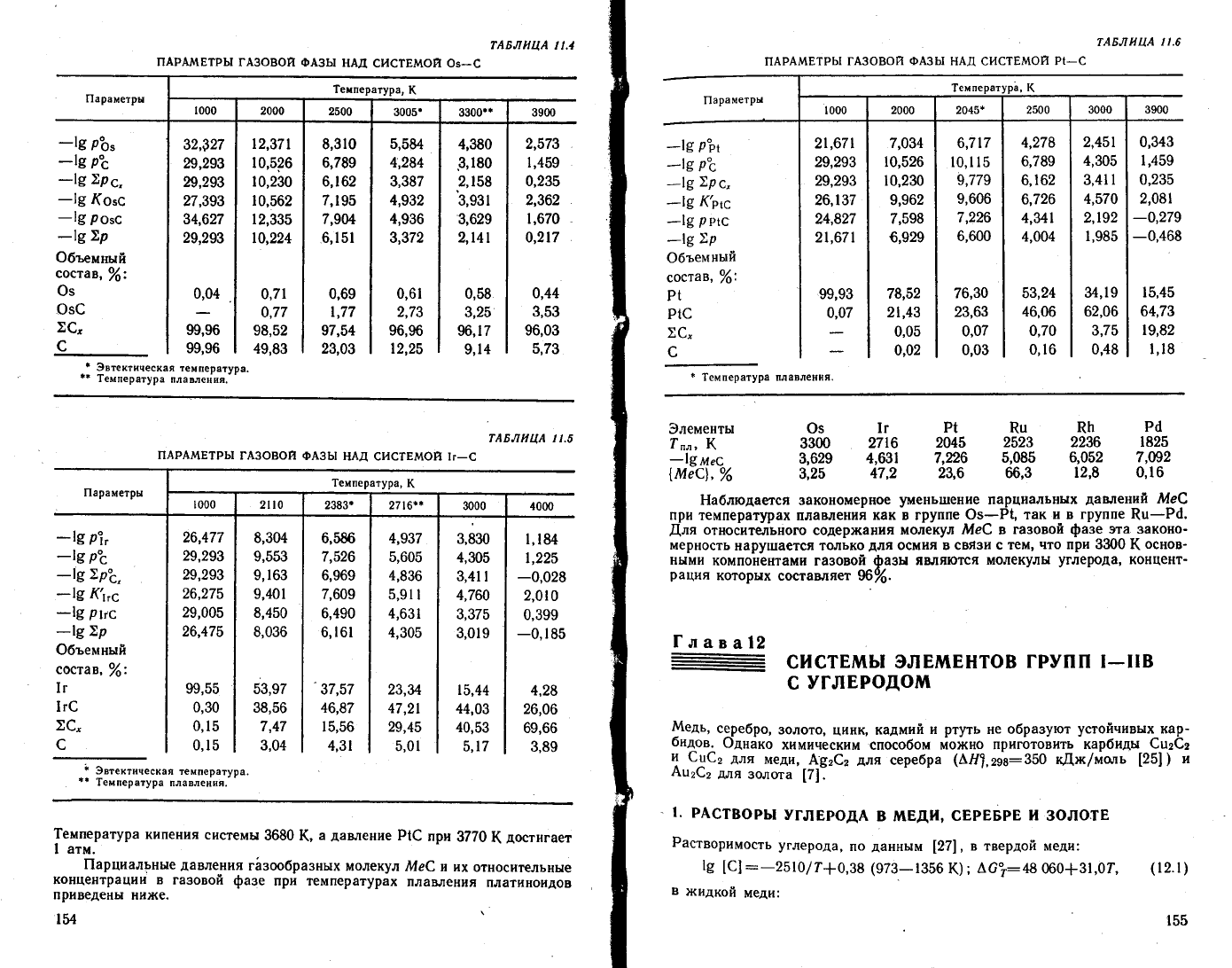
' 'Б
табл. 1 1.4 приведены
результаты
расчета
газовой
фазы
над системой
Фз-(.
€уммарное
давление
молеку,'!
углерода
вк]1ючает
и одноатомные
частицы
углерода.
Б системе
Фз-€
во
всем
интервале
темперацр
основ_
иь!ми
компонентами
являются
углеродсодер)кащие
га3ы'
и,
-вероятно'
поэтому
имеются существенные
трудности
для
индикации
осмиисодержа'
щих
га3ов'
в частности
молекул
Фз(.
Результаты
расчета
газойой
фазы
над системой
|г_€
приведег:ы
в
табл.
1 1.5.
|(ак
следует
из табл.
11.5, |гг
и |г€'
над
твердой
фазой
являются
основнь|ми
компонентами.
.[1,ля
суммарного
давления
и
давления
|гь
над
системой
получим:
!9
:р:
_}$
284
/
т
+9'43|
(2383_4000
к)
;
|€
рг,с:-42502/[
+
10,226
(2383-40ф
к).
?емпература
кипения
системь1
!г-(
составпяет
3850
\'(оншентрашия
молекул
]Ё(
б6льше концентрации
атомов
[1рпдпя при
[>2300
1(.
[азовая
фаза
над
системой
Р1-€ привелена
в табл.
1
1.6. 1(онцентрация
молокул
Р1€
в
газовой
фазе
превь:шает
концентрацию
атомов
платинь|
при
темпе'
ратурах
>2600
к.
.[|.ля
суммарного
давления
газовой
фазь:
и Р1€ полуним:
7,
к
1000-2045
2045_3900
|9
:р
-29
493/т+7,822
_30
389/г+8'260
|врр:с
-34444/т+9'617
-32267/т+8'653
153
тАБлпцА 11.1
параметРш
_|8
р6.
_|в
рЁ
_18
}Рс,
-|9
/(овс
-|в
ро.с
_1в
}р
Фбъемный
состав,
)(з
Фэ
_Фз€
'с,
с
32'э27
ж'293
29,293
27,393
34,627
29,293
0,04
99,96
99,96
\2,37\
10,526
|0'2ю
10,562
12,335
|о'224
0,71
о'77
98,52
49,83
8,310
6,789
6,|62
7,!95
7'9м
6,1 51
0,69
1,77
97,54
23,03
5,584
4,284
3,387
4,932
4,936
3,372
0,61
2,73
96,96
12,26
4,380
3,180
2,158
3,931
3,629
2,\4\
0,58
3,25
96,1 7
9,
14
2,573
1,459
0'23б
2,362
1,670
о'2\7
о,44
3,53
96,03
5.73
*
3втектическая
темпеоатуоа.
**
1емпература
плавлег]ия."
тАБл[4цА 11.5
1емпература,
(
параметРн
_|е
р1.
_|в
р.с
-|в
>рё,
_18
(]'с
_|в
рггс
_|в
)р
Фбъемный
состав,
/.:
|г
1г€
:с,
с
26,477
29,293
29,293
26,275
29,005
26,475
99'5б
0,30
0,15
0, |5
8,304
9,553
9,163
9,401
8,450
8,036
53,97
38,56
7
'4т
3,04
6,586
7,526
6,969
7,609
6,490
6,
|6|
37,57
46,87
15,56
4,31
4,937
5,605
4,836
5,91!
4,631
4,305
23,34
47,21
29,45
5,01
3'8ш
4'ю5
3,41|
4,760
3,375
3,019
15,44
44,03
40,53
5,17
1,184
1,225
-0,028
2,010
0,399
-0,
|
85
4,28
26,06
69,66
3,89
*
3втектическая
температура.
'|
1емпература
плавления'
1емпература
кипения
системы
3680
к'
а
давление
Р1€
при
3770
|(
достигает
1
атм.
||аршиальные
давления
г1зообразных
молекул
!у\е€
п +лх
относит€льные
конце||трации в
газовой
фазе
при температурах
плавлен|{я
платиноидов
приведены
ниже.
|и
пАРАмвтРь[
гАзовои ФАзь!
нАд €!4€!Р]!1Ф! Фз_€
пАРАмвтРь|
гАзовои
ФА3ь|
нАд систвмои |г_с
тАБлицА
11.6
пАРАмвтРь!
гА3овои
ФАзь|
нАд систвмои
Р1-с
параметрн
_|в
р'р:
-|в
р"с
-|в2рс'
_|9
('р*с
-[8
рР1с
-|е
2р
Фбъемный
состав,
/6:
Р1
Р1с
:с,
с
2\,671
29,293
29'29з
26,137
24,827
2\,671
7,о34
10,526
10'2ю
9,962
7'б98
6,929
78,52
21,43
0,05
0'о2
6,717
10,1 15
9,779
9,606
7,22$
6,600
76,30
23,63
о'о7
0,03
4,278
6,789
6,162
6,726
4'м\
4,004
63,24
46,06
о'70
0,16
2,451
4,305
3,411
4,570
2,192
1,985
и'19
62,06
3,76
0,48
0,343
1,459
0,235
2,081
-0,279
-0,468
15,45
64'7з
19,82
1, !8
*
температура плавле1!ня.
3лементы
|,,, }(
-|в
м"с
|мес\' /.
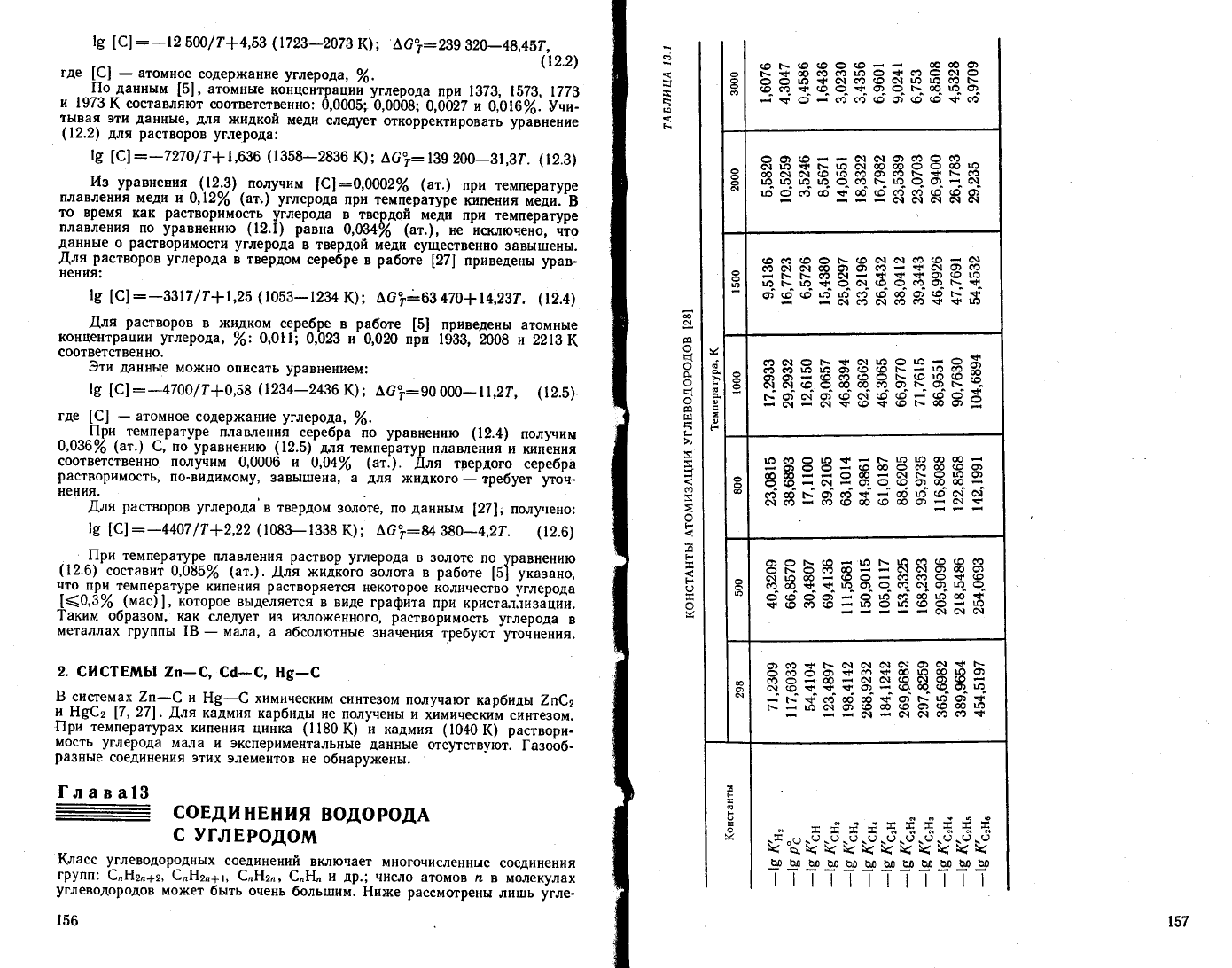
Ёаблюдается закономерное
уменьшение
парциальных
давлени{г
!т1е(
при
температшах плавлений
как в группе
Фэ_Р1' так
и
в
группе
Рш_Р6.
.[1,ля
относитопьйогю
содерх<ания
молекул йе€ в
газовой
фазе
?та законо'
мерность
нарушается только
для
осмия в связи
с тем'
что при 3300 |(
основ'
ными
компонентами газовой
фазы
яш|яются
молекулы
углерда'
ко!{цент-
рация
которых
составляет 96/6.
|лава12
:
систвмь|
элвмвнтов
гРупп [_|!в
с
углвРодом
йель,
серебро,
золото,
цинк,
кадмий
и
ртуть
не образуют
устойнивых
кар-
бндов.
Фднако
химическим
способом
йойпо прийтовить
карбиды
€ш:€:
и
€д€:
для меди'
А9э€э
лля
серебра
(^|4'й:350
кАх</йшпь
[25]
)
и
Ац2с2
д'|я
золота
[7].
!.
РАствоРы
углвРодА
в мвди,
свРвБРв
и
3олотв
Растворимость
углерода,
по
данным
[27],
в тверлой меди:
1в
[€]:-:ьп0/т+0'3в
(973-|356();
А6"1:ш060+3!,0г,
(12.|)
в
жидкой
меди:
Фз
|г
Р{
Рц
3300
2716
2045
2623
3'629 4'631
7'у26
5'085
3,25
47,2 23,6 66,3
пь
Р6
2236
1825
6'052
7'Ф2
12,8
0,16
!55
|9
[с]:-12
6Ф/т+4'53
(1723_2о73
к);
^с?:239
320_48,45г,
гле
[_€]
_
атомное_
содержание
углерода, 96.
('2'2'
.^||^о_данным
[5],
атомные
концейтрации
углеРода
прп 1373, 1573,
1773
и
1973
(
составляют
соответственно:
0,ош5}
0,0оф;
о,о0эт
п
о,охв/..
хни-
тывая
эти
данные'
для
жидкой
меди
следует
откорректировать
уравнение
(\2.2|
для
растворов
углерода:
1в
|с1
:
_72707г+
|'636
(
1
358_2836
()
;
Ас7:
|39
200-31'37.
(
1 2.3)
}1з
уравнения^('^2.9).получим
1с|:о'о0о2%
(ат.)
при температуре
плавления
меди и
0'\2/,
@т.)
углерода
при температуре
кипения
меди.'8
то время
как
растворимостъ^
уллерола
ч 1вердо{
меди
пРи темперацРе
плавления
по
уравнению
(12.1)
равна
о'о34%
(ат.),
не исключено,
ч}о
данные
о
растворимости
углерода
в тверлой
меди существенно
завышены.
для
растворов углерода
в твердом
серебре
в
работе [27]
приведены
урав-
нения:
|в
[с]:-3317/т+\,25
(1053_1234
к);
Ас?:ф
47о+14,23т.
(,2.4)
.(ля
растворов
в )кидком
серебр
в
ра6оте [5]
приведены
атомные
концентрации
углерода' /.:
0,0\|;
0'023 и
0'0ф при
1933, 2008
и 2213
(
соответственно.
3ти
данные
можно
описать
уравнением:
|9
[€]:_д7607т+0'58
(|234-2436();
А6?:900ф_!1,2г'
(12.5)
где
[с]
_
атомное
содерх(ание
углерода, уо.
^ ^^^т]Р"-
темп_ературе
плав.,1ения
серебра
по
уравнению
(12.4)
полщим
о'о36%
(ат.)
€' по
уравнению
(12.5)
шд]:
темпе-ратур
плаы1ения
и
кипения
соответственно
получим
0'0006 и
0'04}
(ат.).
,(ля
твердого
серебра
растворимость'
по-видимому'
завышена' а
для
жидкого
-
требует
утоп-
нения.
,[1ля
растворов
углерода
в твердом
зФ|оте' по
дан}|ым
[27];
полунено:
|9
[с]:_4407 /т+2'22
(!083-1338
();
^с?:вц
38о_4,2т. (12.6)
.-^
^!р"
температуре^плавления
раствор углерода
в золоте
по
уравнению
(12.6)
составит
0'085/6
(ат.).
[ля
жидко1о
з6лота
в
работе [5)'ука3ано'
:т9 _п!|-
темпер_атуре
кипения
растворяется
некоторое количество
углерода
к0'3%
-(мас)]'
которое
вьлделяется
в виде
графйта
при
кристал1"з'ции.
1аким образом'
как
следует
и3 изложенного,
растворимость
углерода
в
металлах
группь|
|Б-мала,
а абсолютные
значения-требуют
уто;нения.
2.
систвмь1 2п_|,
€(*€, }!9_€
Б
9учем.ц ?:_9
"
Ё9_€ химинеским
синте3ом
получают
кар6иды 2п(,э
и
Ё9€:
17'27|..[[ля
кадмия карбидь[
не
получень|
и
химическим
синтезом.
[ри температурах
кипения
шийка
(|1в0к)
;
кадмця
(1040к)
раствори_
мость
углерода
мала
и экспериментальные
данные
отсутствуют.
[азооб-
разные
соединения
этих
элементов
не
обнару>кепы.
|лава13
:
совдинвния
водоРодА
с углвРодом
|(,л:асс
углеводородных
соединений
вкпючает
многочисленные
соединения
групп:
€'Ё2,4э, €'Ёэ'+:,
('}!э,,
€,Ё,
и
др.;
число
атомов
п
в молекулах
углеводородов
может
быть
очень
большим.
Ёиже
рассмогрены
лишь
угле_
|56
/
н
:
н
о
в
6ь(о(оо(о__
сосоо)
ь<ф(т)со!оо+соос\о
6 о ]о <
^!
со
(о
6|
!о !о со
г-
(эф+(оо+о)ог-ф!оо,
]<.6.]с'с,6о'6,6-Ёс.'
ы
о6|'(о_-с-!6|о)соо({)
бй+г![ос\|ффооф!о
ф ы 6!
(о
1о
со о)
со
г_ <1
г-
со
!о
|о
!о !о о
со
г-
!о
о о)
_
б|
6оо1Ф<оо(ососо(о(оо,
Ф
66(ооь(о61 6.|со(о_6-!
йыыф6'о'со-тб!о)сэ,
;ЁЁс6ф-++чЁФ(о!о
!о^
ч
[о_
ч
о^
ч
(о-
ч
со-
е.-- ч
Ф9.о9к3к3вч\в
о
со^|ог-ч'.о!!оо!о-о*
6 ф !о !|э 6)
(о (о
ь.
-
!л
ф
;(
66)-(осо(оог-(о!о(о;(
^|ы(оофф(оо)г-о)г--.
5к1к€в€вЁввё
о
Ф
|6о1о]о!Ё_г-!о|офф_
-о'бо;Ффософ(9о)
ф6==оф-6!ьо!оо)
6с6-6|:о)о(оо)фф-
с]Фьо)с6!#_ф!о(оФ.
6|
фф;фФф(офФ=э=
8Рь8;з!ккввв
-ьй;Фо-с']с')Ф*(о
ф^
ф^
ч ч
й^ Ф- о-
с)-
ч ч'о-
ч
€ввв=в8в389Б
6| о.! 6.|
Ф
Ф
66+ьыы6!б!о'о!!+ь
Ёв9в=кх3кв39
фб_ччче1ччФ-чч
-г-+софсо{+о'г-фФч
ь_йы6ФфФФ(оф|о
-*;ф_о'!с'|сф(о<
Ё
1
о
у
.[
^о
.0 .0
-о
-о -9 -0 -о.о
\0
.о
ч
о-чччччччччч
Фффо0ьоь!ь!ь!00ь0ьоФ
!!!!
в-9дор9дР|
с
числом
атомо-в
у{л_е_ро4а_Р
молещлах
{2'
т.е. газы
€Ё,
€Ёэ,
€Ёз'
€Ёа' €аЁ,
€яЁэ,
€эЁз,
€эЁ+'
(эЁь
и
€эЁо;
для}оторых
в
раб_й
г'ат
приведень|
константы
атоми3ации
в |широком
интервале
темпеРатур.
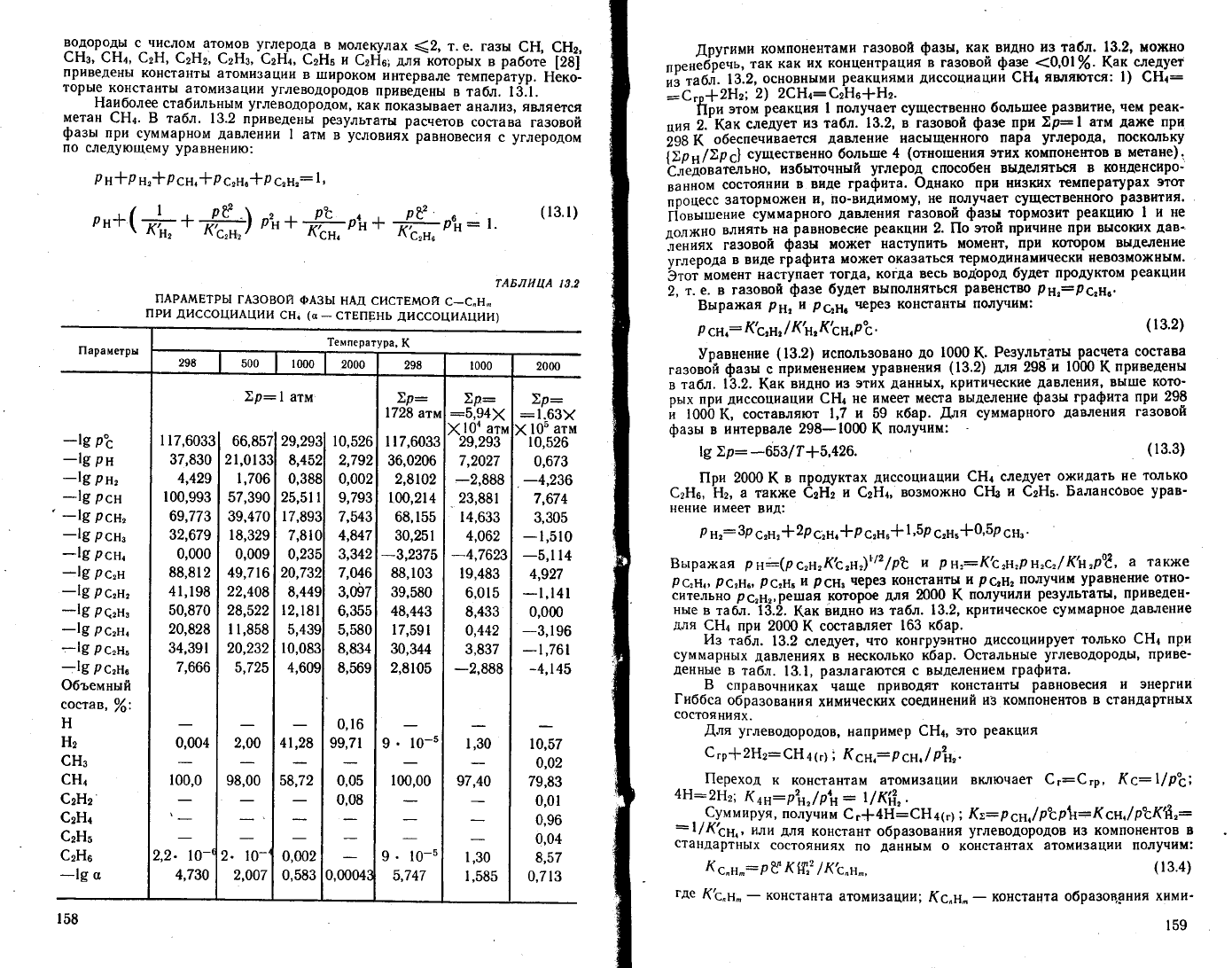
нёко_
торы-е-константы
атомизации
углеводородов
приведены
в
табл. 13.1.
Ёаи более
стабильным
углеводородьм,
ка к
;оказывает
а нал из' является
метан
€Ёс. 8 табл.
13.2
приведен*
результаты
расчетов
состава
газовой
фазьп
при
суммарном
давлении
| атй
в-условиях
равновесия
с
углеродом
по следующему
уравнению:
р
н*
р
н"*
р
сн,*Р
с'н'*р с,н,:
1,
,"+(+
**)
Ё"+фг,+
$о'н:
г.
(13.1)
тАБл14цА
13.2
пАРАмвтРь|
гА3овои
ФАзь!
нАд
систвмои
с_с"н.
пРи
диссоциАции сн.
(о
_
€1Ё||БЁБ
диссоциАции)
|[ ара
метрш
1емпература,
1(
500
298
:ооо
|
2000
298
1000
20Ф
_|в
рё
-|в
рн
-|в
рн,
_1в
рсн
_|8
рсн,
-|в
рсн,
_|8
рсн,
-|в
рс,н
_|в
рс"н,
_|8
рс'н,
_|е
рс'н,
-|8
рс'н,
---:|8
рс'н'
Фбъемный
состав,
/9:
н
}!а
€Ёз
€}|с
€эЁэ'
€яЁа
€эЁь
€эЁо
_|в
о
2р:
117,60ш!
66,в57
37,ш0
|21,0|33
4,42э
1
1,706
|00,993
!
ьт,зоо
60,773
!
39.470
32,679
!
1в,329
0,000
!
0,000
вв.в12 ! 40.7161
д:':эв
!
ээ'цов1
50,в70
!
2в.5221
20,в2в
!
|1,в6в!
34,39!
|
2о'%2|
7,666
!
5.7251
[_!
т*|т!
'1'|'ч
!
!_!
!_!
я'э.
:о_4:. :о-1
4,730|
:'шт|
2э,203! 10,526
в,4521
2.7э2
0,3вв!
0,002
25,51 1
!
0,703
17,вэ3|
7.543
7'ы01 4'в47
0,2351 3,342
2о'732| 7,046
8,4491 3.097
|2,|в|!
6,355
5,4391
5,580
[0'0ш!
в.в34
4,6о0!
в,56э
_
[
','
'':* !''{'
5в,72
!
о,о5
-
!
о.ов
_!_
0,0021
0,бш
|0'00043
2р:
1728 атм
! 17,6033
36,0206
2,8102
1ф,214
68,155
30,251
-3'237б
88,103
39,580
48,443
17,591
30,344
2,8105
9.-
-5
100,00
9
.ъ_'
5,747
2р:
:5'94х
!
|0{
атм
29,293
7'2о27
-2,888
23,881
14,633
4'о62
-4,7623
19,483
6,015
8,433
о'442
3,837
-2,888
1,30
9й
_
1,30
1
|,585
1
2р:
:1.63)(
(
105
атм
10,526
0,673
-4236
7,674
3,305
-
1,510
-5,114
4,927
-1,141
0,000
-3,196
-
1,761
-4,145
10'б7
0,02
79,83
0,0|
0,96
0,04
8,57
0,713
|58
.|1ругими
компонентами
газовой
фазы,
как. видно
из табл. 13.2, мохсно
',"небреч,,
так как
их
концентрация
в газовой
фазе
<0'0|$.
|(ак следует
"5
'а6}л.
13.2,
основными
реакциями
диссоциации
€Ё+
яш:яются: |)
€Ё,о:
_
6",|2Бэ}
2)
2€Ёа:€яЁо*Ёэ.
!ри
этом
реакция
1 полупает
существенно большее
развитие'
чем
реак'
ция2.'\ак
слёдует
из
та6л.
13.2, в газовой
фазе
при
2р:!
атм
даже
при
298
к
обеспечивается
даы!ение
насыщенного
пара
углерода'
поскФ!ьку
ц5р"/2рс\
существенно боль:це
4
(отношения
этих компонентов
в метане).
ёйе!оватйьно,
избыточный
углерод
способен
выделяться
в конденсиро_
ванном
состоянии
в виде графита.
Фднако при низких темпеРацрах
этот
процесс
затормохен
!|' по-видимому'
не получает
чщественного Ра3вития.
Ёовы:шение
суммаРного
дав.,1ения
газовой
фазы
тормозит
реакцию
1
и не
пполжно
влиять
на
равновесие
реакции
2. ||о
этой причине
п!и высоких
[ав'
лениях
газовой
фазы
моя<ет
насцпить
момент,
при котором
выделение
углер9да
в виАе
графита моя(ет
ока3аться теРмодинамически
невозможным.
это|
момент
наступает
тогда'
ко!да весь
водород булет
пролуктом
реакции
2,
т.
е. в газовой
фазе
6удет
выполняться
равенство
Р||':Рсз\1в,
Бырах<ая
Рн,
14
Рстно
[!ерез
константы
получим:
Р
сн,:
|(с"н,
/
('н, (|н.Р?.
(
13.2)
(
13.3)
}равнение
(
13.2)
исполь3овано
до
1000
к.
Резул_ьтаты
_р_асяета
состава
газовой
фазы
с
применен!|ем
уРавнен[{я
(13.2)
для
298
я 10Ф !( приведены
в
табл.
13.2. |(ак
видно
из этих
данных,
критические
давления'
выше
кото'
рь!х
при
диссоциации
€}|+
не
имеет места выделевие
фазы
графита
при
298
й
пооб 1(, составляют
\,7
п
59
кбар.
.[1дя
суммарного
давления
газовой
|1ри 20ф 1( в продуктах
диссоциац|{и
€Ёц слеА}ет
ожидать
не
только
€эЁо, Ё:, а также ё:Ёэ
и €:}1ц,
возмФжно
(}!з
и
€яЁв.
Балансовое
урав'
нение имеет
вид:
Р
н,:3Р
с,н,*2р
6;1'*Р с,н.{
1,5р
6,ч'*0,5р
сн..
Бьтражая
р
6:(р 1,н'!{'с"н')|/2
/р|
н
р
н,:&'с'н"Р
н"с,/
!(\,роё'
а
так)ке
Р(о\1ц,
Р(-лАв,
Р€'н"А рсн3
чере3 константы
\1
|€в\{.э
получим
уРавнение
отно_
сительво
рс1н2,решая
которое
для
2000
(
получили
результаты'
приведен'
ные
в
тай. 13.2.
(ак
йидно
из
табл.
|3.2' критическое
суммарное
давление
для
€Ё+
при 20Ф |(
составляет
163
кбар.
14з
та6л.
13.2 слелует,
что конгруэнтно
диссоциирует
только €Ё+
п!и
суммарнь!х
давлениях
в
несколько
кбар.
Фстальные
углеводороды,
приве'
денные в
табл.
13.|,
разлагаются
с выделением
графита'
Б
справонниках
чаще
приводят
константы
равновесия
и энергии
[иббса
образования
химически}
соединений
из
компонентов
в
стандартных
состояниях.
.(ля
углеводородов'
например
€Ёс,
это
реакция
€др}2}|2:€Ё+(г1
!
/(6ч,:Р
сн,/
р"н'.
||ереход
к
константам
атомизации
включает €г:€'р,
|(с:|/р"с1
4}!:2Ё:;
|(
цн:р2н,/
Р|н
:
\
/
к!#,'
_
€ум
м иру!,
по!уй
й с
.+
цй: сн
ц
в|',
!(>:
Р
сн,/
р"с
р|:
|(
сн}
Р"с|('А,:
:\/]{'сн,,
или
для
констант
образования
углеводородов
из компонентов
в
стандартнь!х
состояниях
по
данным
о константах
атомизации получим:
|(
с
"н-:
р
{
|(
[{,'
/
къ
^н-.
(
13.4)
где
:('с"н.
-
ко|{станта
атомизации;
д(с'н.
-
константа
образов.3ния
хими-
159
ческого
соединения
€,Ё'
из
компонентов
в стандартннх состояниях.
.(ля
энергии
|иббса
(.0,ж/моль)
имеем:
А6"':-19,1ц67 16:(с'н'.
(13'5)
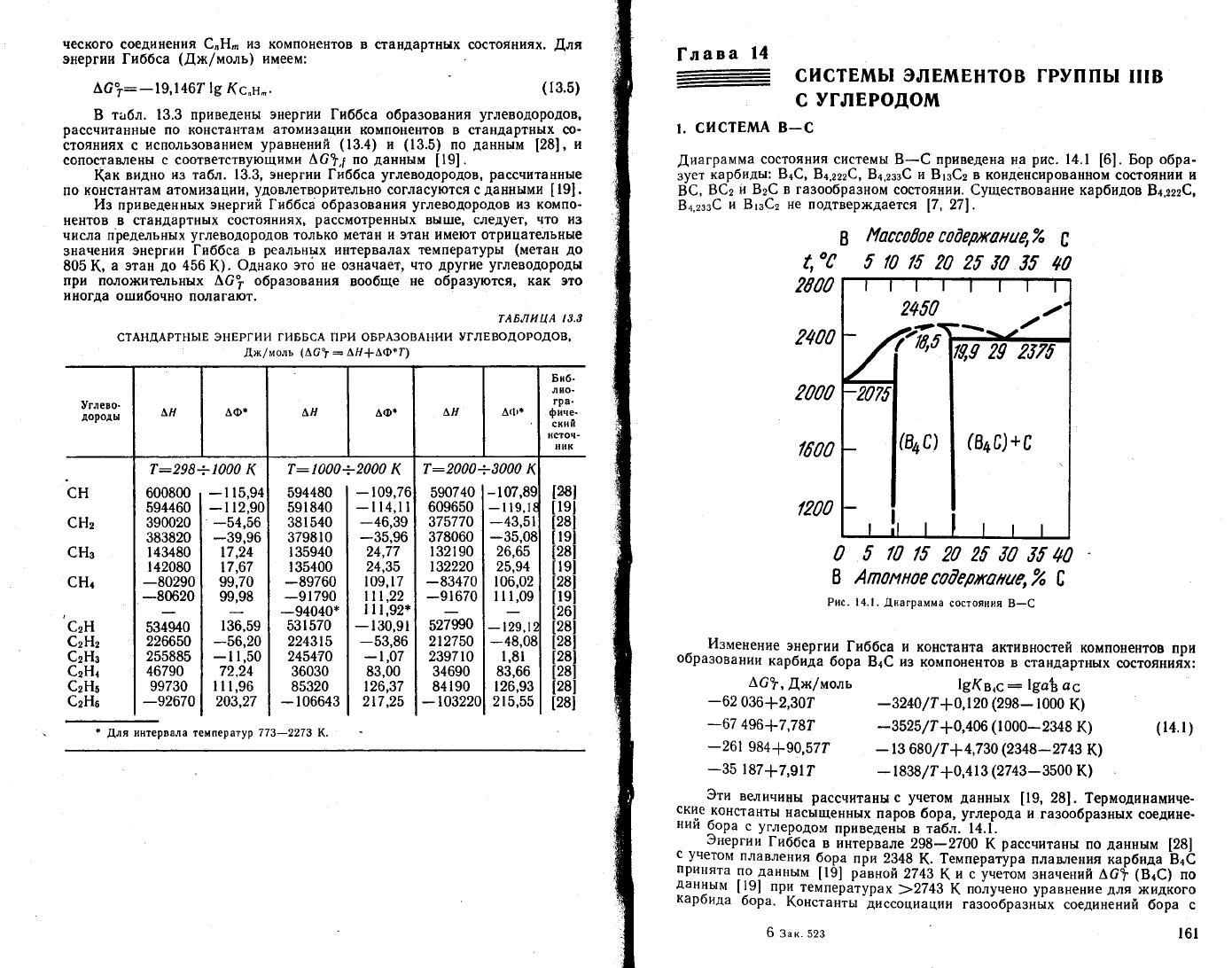
8 табл.
13.3 приведены
энергии [иббса
образования
углеводородов,
рассчитаннь|е
по константам
атомизации
компонентов
в
стандаРтных сю-
стояниях с
исполь3ованием
уравнений
(13'4)
и
(13.5)
по
данным
[28]'
и
сопоставлень|
с соответствующими
А6};
по
данным
[10].
(ак
видно
нз табл. !3.3,
энергии
|'иббса
углеводородов, рассч|{танные
по
константам
атомизации'
удовлетворительно
согласуются с
данвыми
[
19].
|4з приведенньпх
энергий
|иббса
образования
углеводородов
и3
компо-
нентов
-в
етандартных
состояниях'
рассмотренных
выше' следует'
что из
числа предельнь!х
углеводородов
только метан
и этан имеют
отрицательные
значения
энергии
|иббса
в
реальных
интервалах температуры
(метан
до
805
('
а этан
до
456
к).
Фднако
это не означает,
что
другие
углеводороды
при полох(ит€,'!ьных А6}. обра3ования
воо6ще
не образуются, как это
иногда
ошибочно
полагают.
тАБл||цА
13.3
стАндАРтнь!в
энвРгии
гиББсА
пРи оБРАзовАнии
углвводоРодов'
Аж/моль
(^с}
:
^,'+^Ф*г)
[глево-
дороды
^н
дФ} ьн
^Ф*
^н
^()
*
Биб-
ляо-
гр а-
ф!че.
ски
й
исто{-
ник
сн
€Ёя
€Ёз
€Ё+
€эЁ
(у|1э
€эЁз
€э[!+
(эЁо
€эЁо
т:298
600800
594460
390020
383820
143480
142080
-80290
-80620
534и0
22ф50
255885
46790
99730
-92670
.1000
к
-
1 15,94
-
1 12,90
-54,56
-39,96
17,24
17,67
99,70
99,98
136.59
-56,20
-
1
1,50
72.24
! 1
1,96
203.27
|:1000
594480
591840
381540
379810
135940
!35400
-89760
-91790
-94040*
53!570
224315
24547о
36030
85320
-
! 06643
2000
к
-
109,76
-114,11
-46,39
-35,96
24,77
24,35
109,17
\\\,22
| |
1,92*
-
130,91
-53,86
-
1,07
83,00
126,37
217,25
[:2000-
590740 |
600650 !
зт577о 1
373060 !
132|э0 !
в222о !
-$4701
-э!670!
!
527Ф0 !
21275о !
23э7|0 !
34690 !
в4190 !
-
1о322о!
-3000 |<
-
107,8!
-1!9,1{
-43,51
_35'0€
26,65
2ь'94
106,02
1|ш9
-
1 29,1:
-48,0{
1,81
83,66
126,93
215,55
{!8!
шэ|
[28]
{
10]
[281
[10|
128!
шэ]
[26]
[281
[28!
[28]
[28]
[28]
[28]
}
для
интеРвала температур 773-2273
к'
|'лава
14
:
систвмь| элвмвнтов гРуппь|
|||в
с
углвРодом
!.
систвмА
в_с
[иаграмма
состояния
системы 8_€ приведена
на
рис.
14.1
[6].
Бор
обра-
зует
карбиды:
Б+€,
Б+.:э:€' 8а,:зз€ и
8:з€э в конденсированном
состоянии
и
8€,
Б€э
и
Бэ€ в газообразном
состоянии'
€ушествование карбидов
Бц,эээ(,
Бц,,:зз(
н
Б:з€:
не
подтвер)кдается
|7'
2711.
3
/'/ассо0ое
с00ерханце'%
8
'/0/5202'1015ц0
0
5
/0
/5
20 26 10
3,40
8 Апопное
со0ерханце,%
Ё
Рис. 14.!.
.[иаграмма
состояния
8-€
^.__Р1зменение
энергии
|иббса и
константа активностей
компонентов
при
ооразовании
карбида
бора
Бо€
и3
компояентов
в
стандартных
состояниях:
А6},
Аж7моль
_62
036+2,30т
-67
496+7'78т
|3(в'с
:
\ца|
ас
_324о/т+0'120
(298_
1000
к)
_3525
/
т
+0'406
(
| 000_2348
к)
(14.|)
_261
984+90,57г
_
13 6в0/г+4
'730
(234в-2743
к'
-35187+7'91г
-1в3в/г+0'413(2743_3500к)
3ти
величиньп
рассчитаныс
учетом
даннь|х
119,
2в]. 1ермодинамине_
с-к_и€{онстанты
нась[щенных
паров бора,
углерода
и
га3ообРа3ных
соеди[|е-
пии
оора
с
углеродом
приведены
в табл. 14.1.
3нергии
[иббса
в и!ттервале
298_27оо 1(
расснитаны
по
данным
[28]
с
учетом
плавления
!ора
при 2348
к.
1емпература
плавления
карбида в4с
принята
по^даннь[м
[19]
равной
2743
к
и
с
унет6м
значений
^6$
(в1с)
по
даннь|м
[19|
при
тейпер6турах
>2743
к
по1унено
уравнение
для
жидкого
карбида
бора.
[(онстанты'диссоциации
га3оьбразн**
соеди"ений бора с
(цс)
1
(8цф+6
6 3ак. 523
|61

:
н
о
о
о
1!!!!!|!!!!
ь
ф
в9 г-с!(о(оь(о<+в
ф_ц
\чччфчччч
+со
с)!Ё6|оооо6|о|
ь*
ь
ф
ь\ о б! со
(ь
6!
_
6-{ с.|
о_ Ф_
ч
о_
6|
ч
6!
1€о_
6.с\6.!оооо6.с{
ФЁ
зо)
61 6)
о-
(о-
|о
(о
ф
!о !о
|о6!
]ЁФФо|ос)тф!Ё
оьЁ
о)'о(ооо6!о!ЁФ
ч1
{с:'665666с,
г!
!о
о,
Ф
!о |о
ог-о(о(о
!оооог-
'оооо(о
(о
оь.6)
ччч
Фоо
о)
о)
ч..
ф!о
оь.
о
за
&5_:пгё:!к
{{ 8о
о
'й
о
о
эк
$
'
!
! ! ! ! !
!
Ф
53 Ё'
, ! ! ! ! [ 1
з
:
с
д!
сб
н
о
о
0
.х
з^ э
\^;
з-Ф
э п.1
о
ттр.': с)ч*
^0
|
|9о\фФФФФо(.)оэ
.ф
ч
\о
ь
Ф
Ё
Ф
!*
ч
.о
о
Ф-
ч
163
6*
162
!!!!!!
(оь<сосо(о
:'!б|с\
(о+(оо(о-
==}х(ооЁ
;пкь3ББё-+й-квР
ы;6ы663т-со6ы6
|
кь9вь3вЁвЁББ*
ь+^!<6.!оч.{-!оо)-':
€"'-'€66=т.':ы9*
6) о,
_
сф,^
:Ё
6 ф
(о
о) ф
(о
:Ё
б66о=ьЁз(о$ьо'со
6| г- со 6! х 6| ;\ ф о
со з о
г-
о6Ё+Ё=6Ф6Ёг'{{'6
пп
в$8Рв3$€;€Ёэ>
ф ь о' с6 о)
]Ё
ч
_"-
г-
!о
-:
* 6)
€9:3'63*:я9кх
ьс6<оо]
-
(ог-Ф-6.!оо
оо)с{Ф_:'96|о'ооф6.|
(ъ
ы ь
-
-
1_- 9) г- 6! Ф
со.!о
о)
ыы:6с.':8о'г'666ы
:
6|6]-
6|ф_[о.ф
*Ё.эа$ЁяЁчэн$€
€!;аэ"'Ёчах${Ё
(оьсоФ(о(о
6|ф_ыф]о
ффсоь.г-о
|о
!Ё
({) (о
!о
<.
(!
о.|
|о
(о
<Ё
6!
ььФг_(оФ
ооЁо)о6ч
(о|осо(о(о<
БЁэк$ха€.Ё8цяя
о)!осоФоАь:!о_(оог-
--!
ыф!ос\|(ог-
|о6!со6!_ц]
:Ё$-!*{||э
Фг-!оо)со(о
(о
({)
ь-
<Ё
с) ь
с\г-[о6|-б
ч
ч ч
г--
(о-
й5_
_ог-о|_о,
(о(ог!,о3БцФФ1оФ6!_
!6 ы
-
о)
(о
+ 9ьо) 6! о г-
-
!о
6'[оо!ос€со9Ф<#ос!фф
ы6г]'6]6в-:ы:,6о6'{
ф- со
-
б!
(')Ф_г-_6
6оф6)-ф*
ч\ччоо-!Ф^
фь.6!оф@
фя-
о
!
ф
ч
Ф
к
о
о
!
о
Ф
Ф
о
Ф
Ф
о
{
Ф
в
ц
э
о и.,
