Грасси Н. Химия процессов деструкции полимеров
Подождите немного. Документ загружается.


Окисление олефинчвых модельных соединений
131
температуры наблюдается тенденция к увеличению скорости разложения
гидроперекисей. Однако скорость образования гидроперекисей повышается
при облучении системы ультрафиолетовым светом или применении соедине-
ний, образующих свободные радикалы, например перекиси бензоила. Чем
выше степень ненасыщенностн соединения, тем больше скорость поглощения:
кислорода; диены, например, автокаталитнчески окисляются самопроиз-
вольно на рассеянном дневном свету . Хотя веществами, моделирующими
каучук, являются
1,5-диены.
тем не менее целесообразно рассмотреть также
и особенности окисления 1,3- и 1,4-диолефинов. Ненасыщенные группы
1,6-, 1,7- и т. д. соединений ведут себя как изолированные моноолефнновые
группы.
Продуктами автокаталитического окисления 1,4-днолефинов также
являются только а-гидроперекиси. Скорость этой реакции, как и следовало
ожидать, учитывая уникальное положение а-метиленовой группы относи-
тельно двух двойних связей, каждая из которых повышает реакционную спо-
собность этой группы, значительно выше скорости окисления моноолефинов.
Это имеет место при окислении эфиров линолевой кислоты
ОН,- (СН.,), -СН = СН-СН.;-СН = СН-(СН.,)
;
-СООСН
;!
.
*
линоденовоп кислоты
СН
3
—
СИ.,
—
СН = СН
—
СН
2
—
СН = СН —СН„
—
СН = СН
—
(СН.,)
;
—
сооса,
и весьма реакционноспособных кислот рыбьего жира, таких, как докоза-
гексаенкарбоновая. Указанная особенность согласуется с предположением
¡10—12] о том, что первичная реакция происходит почти исключительно
в этих точках и что другие продукты образуются в результате вторичных
реакций, которые, как правило, могут быть устранены или по крайней мере
сведены к минимуму соответствующим выбором условий опыта.
Реакционная способность
1,5-диенов
по отношению к кислороду
является средней между реакционными способностями моноолефинов и
1.4-диенов. К исследованным простым соединениям этого типа относятся
дигидромирцен (11). дигидрофарнезен (III) и сквален (IV) [13]
СН
3
I
Н-(СН,—
С
= СН
—
СН.,).,-Н (II)
сн
а
I
Н
—
(СН
2
-С = СН-СН.).,-Н (111)
СН. СН.
I I
Н-(СН, -С = СН
—
СН.,)з-(СН.,-СН = С-СН.
2
)
:)
-Н (IV)
Первые работы по исследованию этих соединений показали, что при
окислении образуются гидроперекиси, но их выход всегда был меньше
величины, рассчитанной из данных о поглощении кислорода. Сначала это
1
объясняли разложением перекисных соединений. Однако в дальнейшем
сквален был исследован более подробно и было показано, что строение про-
дукта окисления не изменяется при поглощении кислорода по крайней мере
доЗ°1)
от стехиометрического количества [14, 15]. Молекула этого продукта
содержит одну гидроперекисную группу, но четыре атома кислорода. Кроме
того,
было показано, что все другие возможные кислородсодержащие струк-
туры отсутствуют, за исключением простых эфирных или циклических пере-
кисных групп, аналитическое определение которых представляет значитель-
ные трудности. При гидрировании на никеле Ренея образуются три гидро-
ксильные группы, одна из которых образуется из гндроперекнсной группы.

132
4. Окисление
Две гидроксильные группы присоединены к соседним атомам углерода. Хотя
этих данных и недостаточно для решения вопроса о строении этой группиров-
ки,
сочетание их с результатами кинетических измерений позволяет с боль-
шой степенью достоверности считать, что она имеет следующую струк-
туру :
ООН
сн.-с-сн-сн-сн,—
с—сн-сн,—-
СН
3
| СН,| (V)
О
-О
Конъюгированные диены и полиены отличаются от моноолефинов и не-
конъюгированных полиенов тем, что они обычно не образуют гидропереки-
сей даже в тех случаях, когда метиленовая группа находится, на первый
взгляд, в выгодном положении, как, например, в эфире элеостеариновой
кислоты [IG]
СН
3
-(СНг),-(СН = СН|
:1
-(СН,)
т
-СООСНз.
Вместо этого наблюдается тенденция к присоединению кислорода к концам
диенового участка с образованием кислородного мостика, аналогичного
имеющемуся в трансаннулярных перекисях [17]
CHj—^
Ч—СН
CHj-^-O—о->—сн
\
/ N
CH, \ /
х
сн
3
ее -
Терпи
нен
или с образованием полимерных перекисей 118, 19]
"<z>
a
[-<z>-°-°-]-
Циклсгексаднон
Последние редко имеют длину цепи больше 8 звеньев, но обычно они очень
стабильны и поэтому анализ их представляет значительные трудности.
Присоединение кислорода к концам ненасыщенной молекулы наблю-
дается не только в случае конъюгированных диенов. Это, по-видимому,
является общим свойством олефинов, так как среди продуктов окисления
рассмотренных выше олефинов, образующих при окислении главным обра-
зом гидроперекиси, обычно находят небольшие количества полимерных пере-
кисей [20]. Схему образования этих полимерных перекисей можно предста-
вить следующим образом:
R-CH = CH-R' -О. —»•
R
—СИ —CH-R'
ос-
R—CH-CH-R'
R-CH=CH-R' О O-i
О
I
R—СН-СН-R'
сн
-сн-
•
R'
\
о
О
1
1
•СН
-сн-
R'
1
о
1
I
0
Однако неомыляемость кислородных связей дает
основание
считать,
что эти
связи могут быть
и
эфирными.
Такое присоединение
к
двойной
связи было
Окисление олефиновых модельных соединений
133
1 г-
предложено для объяснения инициирования реакции образования гидро-
перекисей при полном отсутствии гидроперекисей или соединений, образую-
щих радикалы, и будет рассмотрено ниже.
Механизм и кинетика образования гидроперекисей
в олефиновых модельных соединениях
с неконъюгированными двойными связями
1,4-Диолефин—этиллинолеат был выбран Болландом и его сотрудниками
121—261 для подробного изучения по ряду причин. Среди них наиболее важ-
ными были высокая реакционная способность этого соединения по отноше-
нию к кислороду при температурах немного выше комнатной и количествен-
ное образование гидроперекисей, не осложненное их распадом в этих усло-
виях. Измерения могут быть
проведены в жидкой фазе при
температуре 35—55^ и давле-
нии кислорода порядка 100-и.и
рт. ст., т. е. в условиях, близ-
ких к реальным условиям
эксплуатации материалов это-
го типа.
О возможности ингиби-
рования и катализирования
этих реакций говорилось вы-
ше.
Эти свойства, а также не-
обходимость тщательной очи-
стки реагентов для получе-
ния воспроизводимых значе-
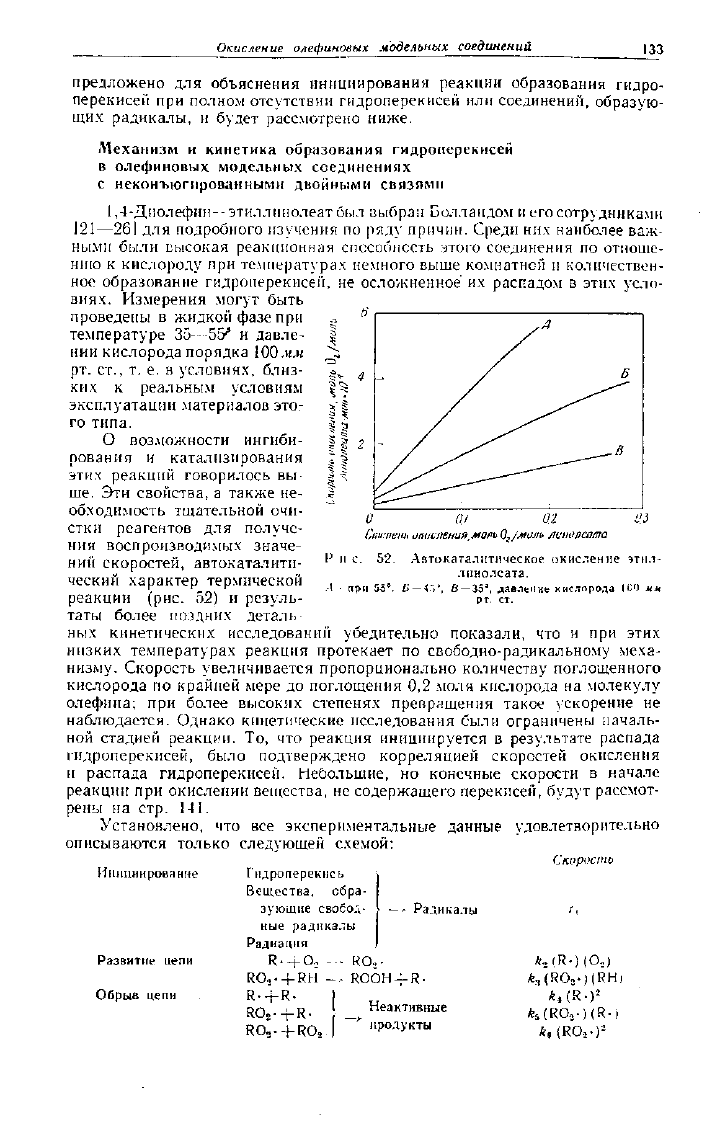
ний скоростей, автокаталити-
ческий характер термической
реакции (рис. 52) и резуль-
таты более поздних деталь-
ных кинетических исследований убедительно показали, что и при этих
низких температурах реакция протекает по свободно-радикальному меха-
низму. Скорость увеличивается пропорционально количеству поглощенного
кислорода по крайней мере до поглощения 0,2 моля кислорода на молекулу
олефина; при более высоких степенях превращения такое ускорение не
наблюдается. Однако кинетические исследования были ограничены началь-
ной стадией реакции. То, что реакция инициируется в результате распада
гидроперекисей, было подтверждено корреляцией скоростей окисления
и распада гидроперекисей. Небольшие, но конечные скорости в начале
реакции при окислении вещества, не содержащего перекисей, будут рассмот-
рены на стр. 141.
Установлено, что все экспериментальные данные удовлетворительно
описываются только следующей схемой:
8
*
О 0,1 0.2
Стспет, аписления.мопь 0
г
/моль линолеата
Р и с. 52. Автокаталитическое окисление этил-
линолеата.
Л—при 55°. Б — 45
3
. В
—35
3
,
давление кислорода 100 мм
рт.
ст.
Инициирование
Развитие цепи
Обрыв цепи
Гидроперекись
Вещества, обра-
зующие свобод-
ные радикалы
Радиация
!?•
+ О,
1*.
+[?.
1Ю,-
+
1Ю
5
—- Радикалы
ЧО,-
ШЭН + И-
Неактивные
продукты
Скорость
*2
(К') (О-;)
А,(!Ю.,-)(£Н)
А, (НО,-)(!*•)
*. (Ш,-)
г

134
4. Окисление
где R—радикал этиллинолеата, образующийся при отрыве атома Н
от метиленовой группы, активированной двумя смежными с ней группами,
a ROO—радикал, образующийся при присоединении к радикалу R- мо-
лекулы кислорода.
В стационарном состоянии скорости образования и гибели радикалов
равны, поэтому
г, = k, (R
•
г -г -¿k, (R-) (RO,-) -i- k
t
(RO,
•
f.
Если длина кинетической цепи достаточно велика, то можно принять, что
k.,(R.)(0,) = k
3
(RO,.) (RH).
Комбинируя эти два уравнения, найдем
(RO,
•)- =
kik¡¡ (RH)a |
2k
h
k,jRH) ~~
•
Полная скорость реакции г равна
r = ft,(RO,-)(RH).
Подставляя в последнее уравнение найденное выше значение для (RO„-),
получим [27—30]
Г
г
= 'Г' \К% (0,Г + 2k;%%
(RH)"
1
(О.)"' f fe-
2
/í
6
(RH)~-]. (49)
Если принять, что fe./e
6
=/¡j, то уравнение (49) переходит в
_i i i
г-' = г.
-
5
Lfeí'Éf
(О.)"
1
+ Aí^^RH)-
1
]. (50)
При очень высоких давлениях кислорода, когда (RO., •) >(R •) и обрыв происхо-
дит исключительно при взаимодействии пар радикалов RO„-, уравнение (50)
переходит в
r
=rf k
:¡
k~Hm-. (5i)
при низких давлениях кислорода, когда (R-)>(RO„-),
i _ i
r = rí
i
k.Ji~'
i
{0„). (52)
Во всех этих уравнениях (0
2
)—концентрация кислорода в жидкой фазе.
Применение этих уравнений к процессам окисления, сопровождающимся
образованием гидроперекисей, рассмотрено в следующем разделе этой
главы.
Важной особенностью реакций, описываемых приведенной выше схемой,
является то, что полная скорость реакции пропорциональна квадратному
корню из скорости инициирования. Если для инициирования реакции
используется инициатор типа перекиси бензоила или ультрафиолетовая
радиация, то и в этом случае соблюдается линейная зависимость между
начальной скоростью и квадратным корнем из концентрации инициатора
[26] или интенсивности света [31]. Если же используется гидроперекись,
то ее концентрация входит в выражение для скорости реакции в первой сте-
пени. Независимым путем было доказано, что в широком интервале условий
кинетика распада гидроперекисей соответствует бимолекулярной реакции.
Несмотря на то, что наиболее тщательно было исследовано только
окисление этиллинолеата, теоретические выводы, сделанные на основе при-
веденного выше механизма, применимы к большому числу моноолефинов
Окисление олефиновых модельных соединений
135
и
1,4-диенов
[19, 29, 32—36] и поэтому должны быть приняты как общие
для этого класса соединений. Однако мнения о применимости этого меха-
низма к окислению тетралина расходятся [37, 38]. Если не рассматривать
предположение Джорджа и Робертсона 137] о том, что термическое окисление
тетралина представляет собой цепную реакцию с энергетическими цепями,
которое в свете более поздних данных кажется крайне маловероятным,
то в настоящее время общепринятым является представление о цепном ради-
кальном механизме этой реакции и о протекании реакции роста цепи по
приведенной выше схеме. Главные расхождения между различными иссле-
дователями относятся к природе процессов инициирования и обрыва цепей
[39—411.
Робертсон и Уотерс [40] предположили, что обрыв цепи происхо-
дит при взаимодействии радикалов Г^- с гидрокснльными радикалами, обра-
зующимися при распаде инициатора, а Бэмфорд и Дьюар [41] считают, что
приведенная выше схема точно описывает реакцию, в связи с чем они
пересмотрели результаты Робертсона и Уотерса.
Несмотря на то, что продукты окисления 1,5-диолефннов (V) значи-
тельно сложнее, чем продукты окисления моно- и 1,4-диолефинов, завися
мость скорости реакции от различных переменных в обоих случаях одина-
кова. Поэтому и механизм реакций должен описываться приведенной выше
схемой (стр. 133). Константы скоростей £
3
и £„ для сквалена имеют тот же
порядок величин, что и соответствующие константы для моноолефинов ана-
логичного строения [15]. Поэтому можно предполагать, что в обоих случаях
активные центры, участвующие в развитии цепи, имеют сходное строение.
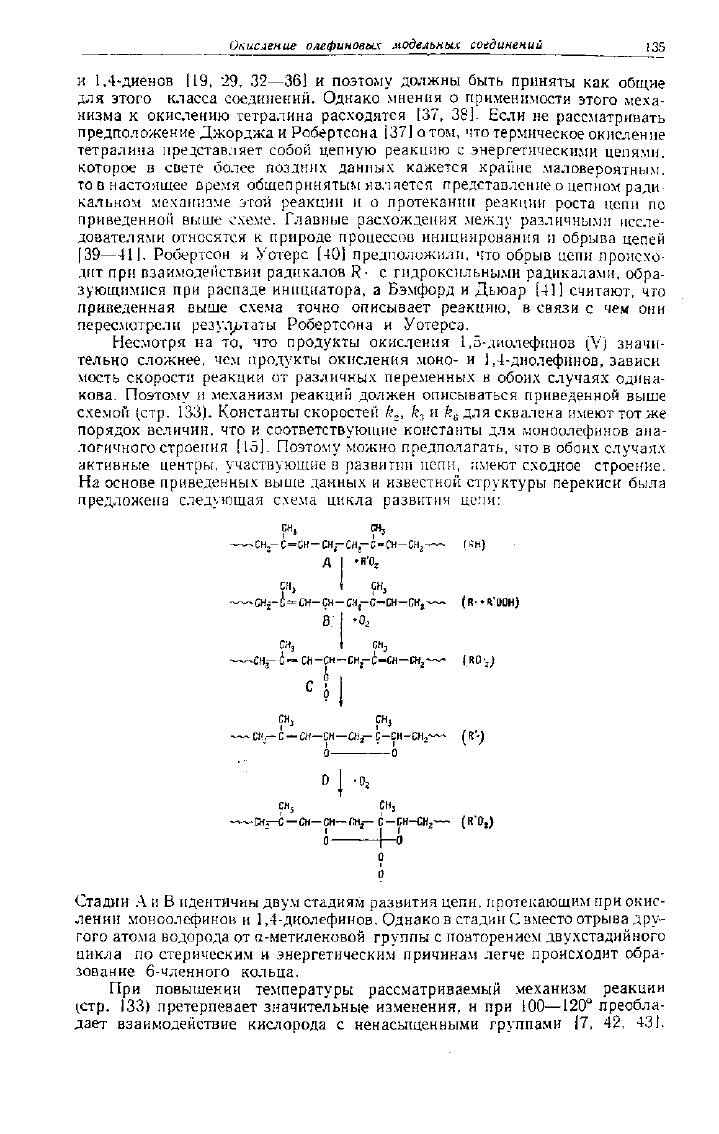
На основе приведенных выше данных и известной структуры перекиси была
предложена следующая схема цикла развития цепи:
сн,
сн
3
-—•сн.-с=сн-сн,-сн
г
-с«гн-сн
2
(НИ)
А
| 'КО,
СН,
» СИ,
•*СН,-
С,=
сн-сн-
ьч
г
-с-сн—сн
г
.
(И-
•
и'оон)
СН,
~~СН,-4—
СН-СН—СН
г
-С-СН—0)
г
-— (КО;)
о
о
сн
3
сн
)
С
—
СН—СН—Сн,—
С-СН-СН
г
о о
о | -о
г
сн
3
сн,
>~«-Си—С=СН—
СН—
пн
г
—
с-сн-сн
2
— (я'0
г
)
а —|—о
о
о
Стадии А и В идентичны двум стадиям развития цепи, протекающим при окис-
лении моноолефинов и 1,4-диолефинов. Однако в стадии С вместо отрыва дру-
гого атома водорода от а-метиленовой группы с повторением двухстадийного
цикла по стерически.м и энергетическим причинам легче происходит обра-
зование 6-членного кольца.
При повышении температуры рассматриваемый механизм реакции
(стр.
133) претерпевает значительные изменения, и при 100—120° преобла-
дает взаимодействие кислорода с ненасыщенными группами [7, 42, 431.
136
4. Окисление
Как было показано выше (стр. 132), образование полимера указывает на
присоединение некоторого количества кислорода к двойным связям даже
при низких температурах. Далее (стр. 141) будет показано, что присоедине-
ние кислорода к этиленовой связи является энергетически наиболее вероят-
ным процессом инициирования реакции окисления (с образованием гидро-
перекиси) в системе, не содержащей перекисей.
Такое высокотемпературное окисление удовлетворительно описывается
следующей схемой:
о-
СН = СН —СН, СН-СН-СН.. *
\
О-СГ
* СН-СН = СН
ООН
Сдвиг двойных связей
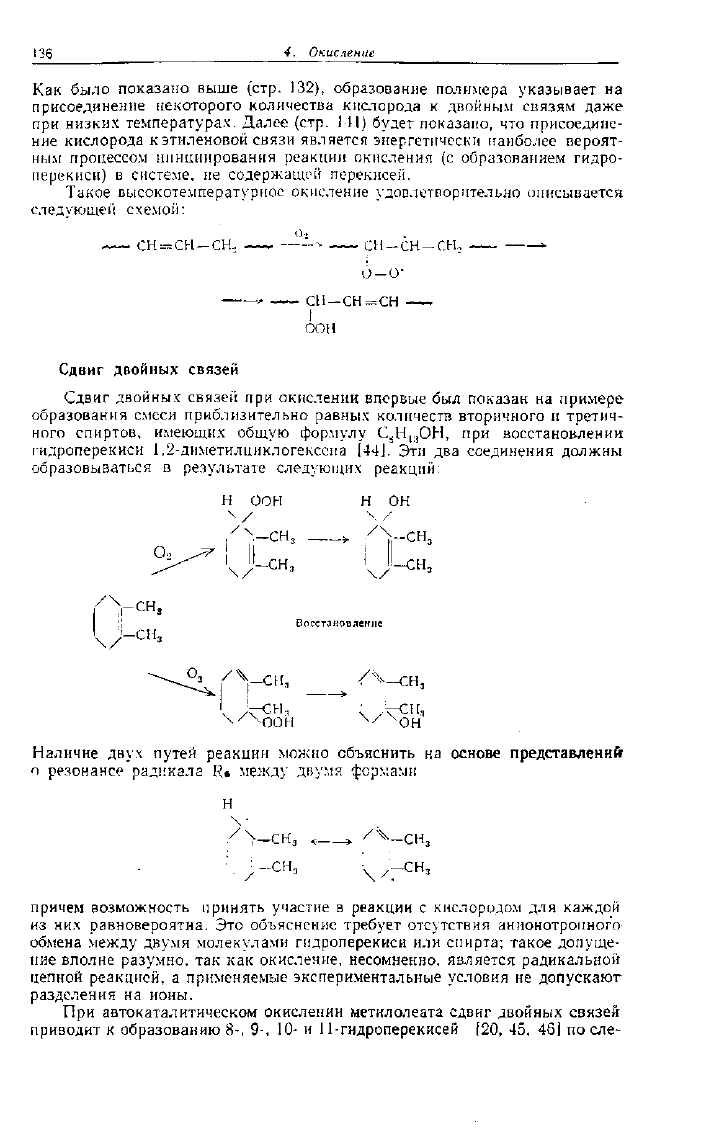
Сдвиг двойных связей при окислении впервые был показан на примере
образования смеси приблизительно равных количеств вторичного и третич-
ного спиртов, имеющих общую формулу С
а
Н1
3
ОН, при восстановлении
гидроперекиси 1,2-диметилциклогексена [44]. Эти два соединения должны
образовываться в результате следующих реакций:
\
/Х
00Н
Наличие двух путей реакции можно объяснить на основе представлений
о резонансе радикала Г?» между двумя фермами
Н
\-
/>-СН
3
<
>
/Ч—сНз
причем возможность принять участие в реакции с кислородом для каждой
из них равновероятна. Это объяснение требует отсутствия анионотропного-
обмена между двумя молекулами гидроперекиси или спирта; такое допуще-
ние вполне разумно, так как окисление, несомненно, является радикальной
цепной реакцией, а применяемые экспериментальные условия не допускают
разделения на ионы.
При автокаталитическом окислении метилолеата сдвиг двойных связей
приводит к образованию 8-, 9-, 10- и 11-гидроперекисей [20, 45, 46] после-
Окисление олефиновых модельных соединений
137
дующей схеме:
СН
3
-(СН-.),-СН-СН=СН-(СН;)в-СООСНз
СМ
3
-(СН
2
)в-СН=СН-СН-(СН»)
7
-СООСН:,
ООН
\
ООН
Сдвиг
двойных
свезен
СНз-<СИ-.)1-СН=СН-(СН-)7 .
Непосродсзвенное
образование
'
СООСНз
СН
3
-(СН2)7-СН=СН-СН-(СН
2
)в-СООСНз
СНз-(СН
2
)о-СН-СН!=СН~(СН.2|7-СООС[[:,
ООН ООН
Сдвиг двойных связей характерен для реакции при высокой температуре
(стр.
136). В этом сл-учае не происходит образования гидроперекисей с двой-
ными связями в исходном положении.
Можно ожидать, что сдвиг двойных свя-
зей при окислении 1,4-диенов, например лин-
олеатов, будет приводить к образованию
трех гидроперекисей '
ООН
СН = СН-
оон
-сн-сн = сн
сн—сн
=
сн- сн=сн —
сон
I
СН = СН —СН = СН-СН
из которых вторая и третья имеют конъюги-
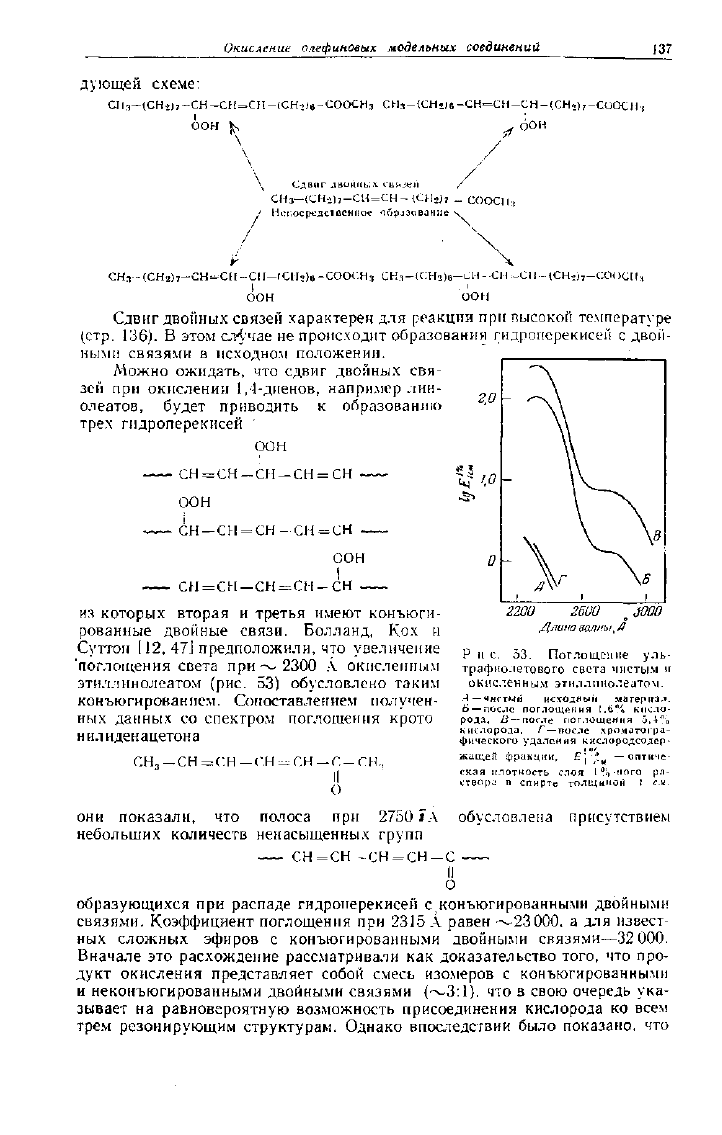
рованные двойные связи. Болланд, Кох и
Суттон [12, 471 предположили, что увеличение
'поглощения света при ~ 2300 А окисленным
этиллинолеатом (рис. 53) обусловлено таким
конъюгированием. Сопоставлением получен-
ных данных со спектром поглощения крото
нилиденацетона
СН, —СН=СН
—
С.Н = СН —Г.-ГН-
II
о
они показали, что полоса при 2750 *А
небольших количеств ненасыщенных групп
СН=СН-СН = СН-(
2200 2600
т
то
Длина
волны,/!
Р и с. 53. Поглощение уль-
трафиолетового света чистым и
окисленным этиллинолеатом.
.-1—чистый исходный материал.
Ь
— после
поглощения
1.6%
кисло-
рода,
В—
после
поглощения
3,4%
кислорода,
Г
— после хроматогра-
фического удаления кислородсодер-
жащей фракции, £] ^
м
—оптиче-
ская плотность слоя
1
%-него ра-
створа в спирте толщиной ! см.
обусловлена присутствием
ооразующихся при распаде гидроперекисей с конъюгированными двойными
связями. Коэффициент поглощения при 2315 А равен ^-23 000, а для извест-
ных сложных эфиров с конъюгированными двойными связями—32 000.
Вначале это расхождение рассматривали как доказательство того, что про-
дукт окисления представляет собой смесь изомеров с конъюгированными
и неконъюгированными двойными связями (~3:1), что в свою очередь ука-
зывает на равновероятную возможность присоединения кислорода ко всем
трем резонирующим структурам. Однако впоследствии было показано, что
138
4. Окисление
правильное объяснение значительно более сложно. Оказалось, что вомногих
случаях образующиеся продукты почти полностью состоят из соединений
с конъюгированными двойными связями и что расхождение в значениях ко-
эффициентов поглощения связано с различиями в конфигурации заместите-
лей V двойных связей [361.
При автокаталитическом окислении соединений с одной двойной связью
также наблюдается увеличение поглощения в ультрафиолетовой области,
имеющее, однако, совершенно иной характер. Этот эффект объясняли при-
сутствием в системе продуктов распада, в частности кетонов, так как спектр
поглощения изменяется при ее обработке щелочами, что. по-видимому,
связано с енолизацией.
Элементарные реакции при окислении
Инициирование
Стадия инициирования реакции автокаталитического окисления сво-
дится к образованию радикалов в системе. Распад перекисей и азосоедине-
ний, например перекиси бензоила и динитрила азодиизомасляной кислоты,
достаточно полно изучен в связи с их
способностью инициировать реакции по-
лимеризации; установлено, что эти соеди-
нения распадаются на радикалы по мо-
номолекулярной реакции. Если иниции-
рующие вещества такого типа исполь-
зуются для инициирования реакции
образования гидроперекиси, то эти пер-
вичные радикалы с наибольшей вероят-
ностью реагируют с а-метиленовой груп-
пой олефиновой молекулы с образова-
нием радикала К-, ведущего цепь. Ско-
рость распада азосоединения в различ-
ных окисляющихся соединениях почти
не зависит от характера среды точно так'
же,
как это имеет место и при полиме-
ризации; поэтому соединения этого типа
очень ценны при кинетических исследо-
ваниях. С другой стороны, перекись
бензоила малопригодна для этих це-
чей
[Л-9],
'Т'ак как скорость ее распада
заметно зависит от окружающей среды.
Фотоинициированне веществ, содержа-
щих хотя бы следы перекисей, почти
несомненно происходит в результате рас-
пада катализатора на радикалы
точно так же, как это имеет место при
термическом инициировании в при-
сутствии того же катализатора.
Однако механизм инициирования реакционных цепей гидроперекисями
при термическом автокаталитическом окислении гораздо сложнее, чем рас-
смотренный выше, на что указывает пропорциональность скорости реакции
первой степени концентрации гидроперекиси. Раньше считали, что неболь-
шие,
но конечные скорости окисления, которые, по-видимому, имеют место
при отсутствии гидроперекиси (см. рис. 52), связаны с процессами иницииро-
вания, в которых не принимают участия перекиси. Однако подробное иссле-
г з
количество
поглощенного
пислороёа,
моль/л* !О
г
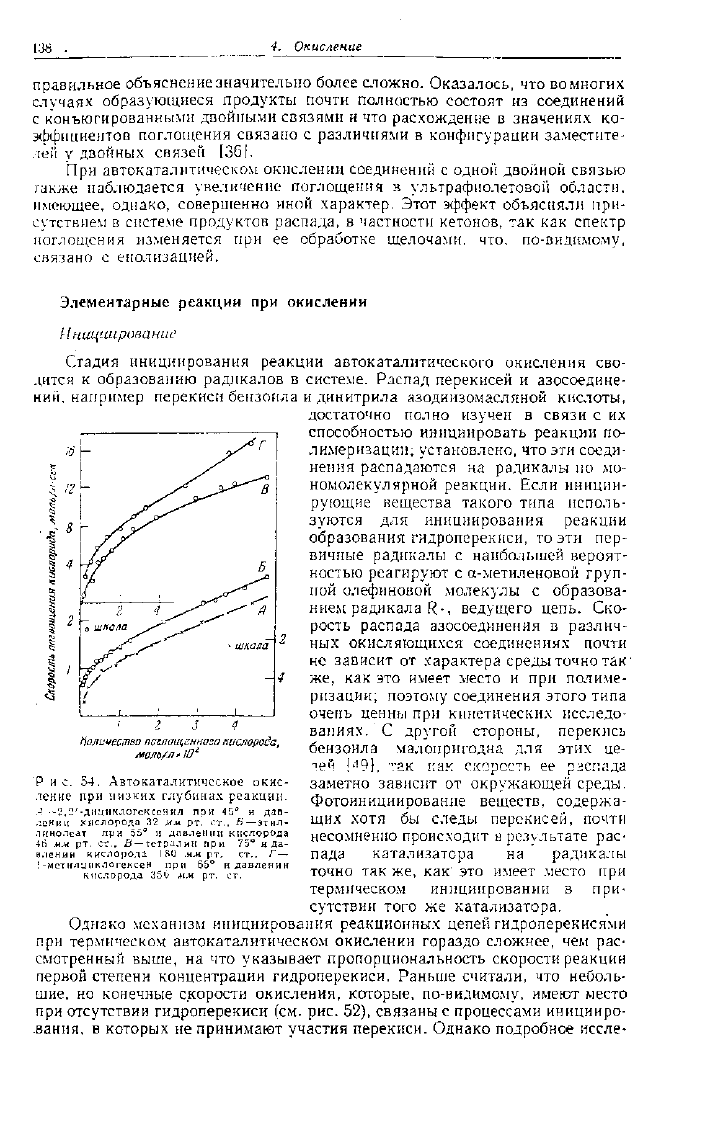
Р н с. 54. Автокаталитическое окис-
ление при низких глубинах реакции.
А
-2,2'-дицикдогексенил при 45
э
и
дав-
лении
кислорода 32 ям рт. ст.,
Б—этил-
лннолеат
при 55° и давлении кислорода
46
мм рт. ст.. В— тетралин при 75° н да-
влении
кислорода 180 мм рт. ст., Г —
!-метилцнклогексен
при 65° и давлении
кислорода
350 мм рт. ст.

Окисление олефиновых модельных соединений
139
дование начальной части этих кривых показало, что они имеют значительную
кривизну при низких степенях превращения, проходят через начало коор-
динат (см. рис. 54 [35]) и описываются соотношением
1
скорость = согЫ
•
(ГДООН)
2
,
которое показывает, что при этих условиях распад гидроперекиси протекает
по реакции первого порядка. Таким образом, кривые, приведенные на рис.54,
полностью описываются уравнением
скорость = .4 \В (ьЮОН) 4- С ЩООН)
2
]^
где Л, В и С—константы.
Можно предположить, что соотношение первого порядка между ско-
ростью и концентрацией гидроперекиси получается в результате протека-
ния и инициирования и обрыва по реакциям первого порядка. Однако это
маловероятно, так как при замене гидроперекиси на перекись бензоила или
при инициировании реакции светом скорость реакции становится пропор-
циональной квадратному корню из концентрации инициатора или интенсив-
ности освещения. С другой стороны, зависимость от квадратного корня при
низких концентрациях гидроперекиси может иметь место при инициирова-
нии в результате бимолекулярной реакции между гидроперекисью и олефи-
ном, хотя это весьма маловероятно. Прямые данные о природе инициирова-
ния были получены опытами по распаду гидроперекиси циклогексенила
в растворе циклогексена в отсутствие кислорода [50]. Главным продуктом
реакции является циклогексенол; эти результаты вместе с кинетическими
данными позволили предложить следующую схему реакций:
Инициирование
Развитие
Обрыв цепи
р--!-к:-
Р--г1Ю-
РП.
во.
2Р,ООН
ш-~ ко, -+-Н
2
0
(1Ю«.+Р.Н Р.ООН + Р.-)
НО-
+ ЯН ^> ГЮН-
к>
•
-г
РООН
1?ОН-
ЕЮ-
Неактивные продукты
Скорость
*
а
(ГЮОН)
г
ЫКО-)(кН)
*
с
(Р-)
(КООН)
^(Я-1-
*с(Я-)(КО-)
Из этой схемы следует, что если к
ь
> к,, и обрыв происходит
только в результате взаимодействия двух радикалов И •, то
1
_ \_
скорость = (¿,1-
к
,?Кк,1
2
~)(ьЮОН)-. (53)
в то время как если к„<йк
с
и обрыв происходит только в результате взаимо-
действия двух радикалов Г<0-, то
1
_
1
скорость = к^(ЯООН)--к
а
Ч
ь
к, ЦНН) (РЮОН). (54)
Если к
ь
и к
г
сравнимы по своей величине, то, даже если допустить, что
к\=к^к
р
получается значительно более сложное выражение, которое, как
и уравнение (54), приводит к дробному порядку реакции относительно

140
4. Окисление
(ROOH). Для гидроперекиси циклогексенила в циклогексене при 80° поря-
док реакции оказался равным 1,77. Когда в качестве растворителя приме-
няется бензол, порядок реакции повышается до 2. Однако это последнее
значение нельзя рассматривать как указание на протекание реакции в
соответствии с уравнением (53), поскольку продукты реакции содержат
цнклогексенон и циклогексенол, а не фенол или дифепил. Скорее всего эта
величина обусловлена тем. что бензол, имеющий значительно менее подвижные
водородные атомы, не может реагировать по первой реакции развития цепи,
вследствие чего цепная реакция полностью подавляется и уравнение для
процесса инициирования, протекающего по реакции второго порядка,
описывает полную реакцию.
Ключом к пониманию причин изменения порядка реакции распада
гидроперекисей от второго к первому при переходе от высоких концентра-
ций к низким явились изменения, происходящие в инфракрасных спектрах
гидроперекиси при ее разбавлении. Установлено, что в чистой гидроперекиси
и в ее концентрированных растворах все гидроксильные группы входят
в образованные водородными связями комплексы, которые диссоциируют при
разбавлении. Поэтому поведение гидроперекисей как инициаторов можно
представить следующей схемой:
2ROOH —Z! ROOH - OOR
\ *~ i I
H
! !
RO-
—-ОН RO.,- — H.O-RO-
.Мономолекулярный распад аналогичен распаду перекиси бензоила. Имеются
достаточные доказательства, что насыщенные гидроперекиси, такие, как
гидроперекись mpem-бутила, претерпевают аналогичный распад 151].
Показано, что некоторые соединения металлов оказывают сильное ката-
литическое действие на реакцию окисления олефинов. Эти соединения исполь-
зуются для промотирования отверждения, или «высыхания» ненасыщенных
эфиров в лаках и красках. В то же время их присутствие в каучуках и рези-
нах крайне нежелательно. Металлы, обладающие этим свойством, например
марганец, медь, железо, кобальт и никель, могут существовать по крайней
мере в двух валентных состояниях. Это является серьезным доказательством
того,
что в их присутствии протекают окислительно-восстановительные
процессы. По результатам опытов по окислению в присутствии ацетата
кобальта (II) в уксусной кислоте Баун, Пеннингтон и Типпер [52] устано-
вили, что стадией, определяющей скорость инициирования, является реак-
ция
ROOH
-j-
M
5
* —» RO,
•
— М
;
* —
H -.
где M
3
" и M-'—комплексный ион трехвалентного кобальта и соответствую-
щий ион двухвалентного кобальта. Ион трехвалентного кобальта регене-
рируется в результате реакции
ROOH-f-М-- RO--f-M»--r-OH-.
В сумме эти реакции идентичны в стехиометрнческом отношении рассмот-
ренному выше бимолекулярному распаду гидроперекиси.
Если во время реакции автокаталитического окисления концентрация
олефина остается практически постоянной, то в конце концов должно быть
достигнуто стационарное состояние [531, при котором концентрация гидро-
перекиси и скорость реакции, измеряемая по поглощению кислорода, не
изменяются. Такое стационарное состояние было достигнуто при окислении
тетралина [37, 38, 54] и бензальдегида [55], окисление которого, как и окис-
