Фрумкин А.Н., Багоцкий В.С., Иофа З.А., Кабанов Б.Н. Кинетика электродных процессов
Подождите немного. Документ загружается.

снятием
аноднь]х
кривь1х
зарях(ения.
Рсли
производить
это
измерение
в
сравнительно
концентрированном
растворе
щелочи,
то
ока3ь]вается
не_
о6ходимьтм
3атратить
относительно
больтпое
количество
электричества.
1ак.
например,
при анодной
поляри3ации
активного
'<елезного
электрода
в2
н.
!']абЁ
(ём.
йривая 1рис.
111)),
пассивация
наступила
только
после
прохождения
чере3
элек6род
0,26
кцл
на
см2,
вместо
приблизительно
0,ь. :о-'
кцл,
нео6ходимь1х
для
образоваъ{ияодного
монослоя
кислорода'
9казанная
величина'0,26
кул|см2
йе является'
однако,
мерой
количества
пассивирующих
окислов
на
поверхности'
|1рй
-анолной
поляризации
}келеза
в
щелочи
протекают
параллельн.о
д*"
рЁ',ц'й.-
п"р"'"
йз
-них
приводит
к
образоЁани1о
осадка
Ре(ФЁ),
через
проме)куточное
образование
ферроат-йона
ЁРеФБ
в
растворе
и
не
"-у-
,]йй йй'''а.
Б{орая
реакция
3аклю_
0'2
чаетс
я в
обр азова
н
|4и
ласс|1вирующих
поверхностнь1х
окислов.
Фтнотпение
скоростей
первогои
второго
процессов
0'1
убьтвает
по мере
умень1пения
концен-
трации
ионов
ФЁ-
в
растворе
и
увели_
чения
плотности
тока.
3следствие
это-
го
общее
количество
электричества'
не-
|.0
!,5
а
малла
кулоньт|см2
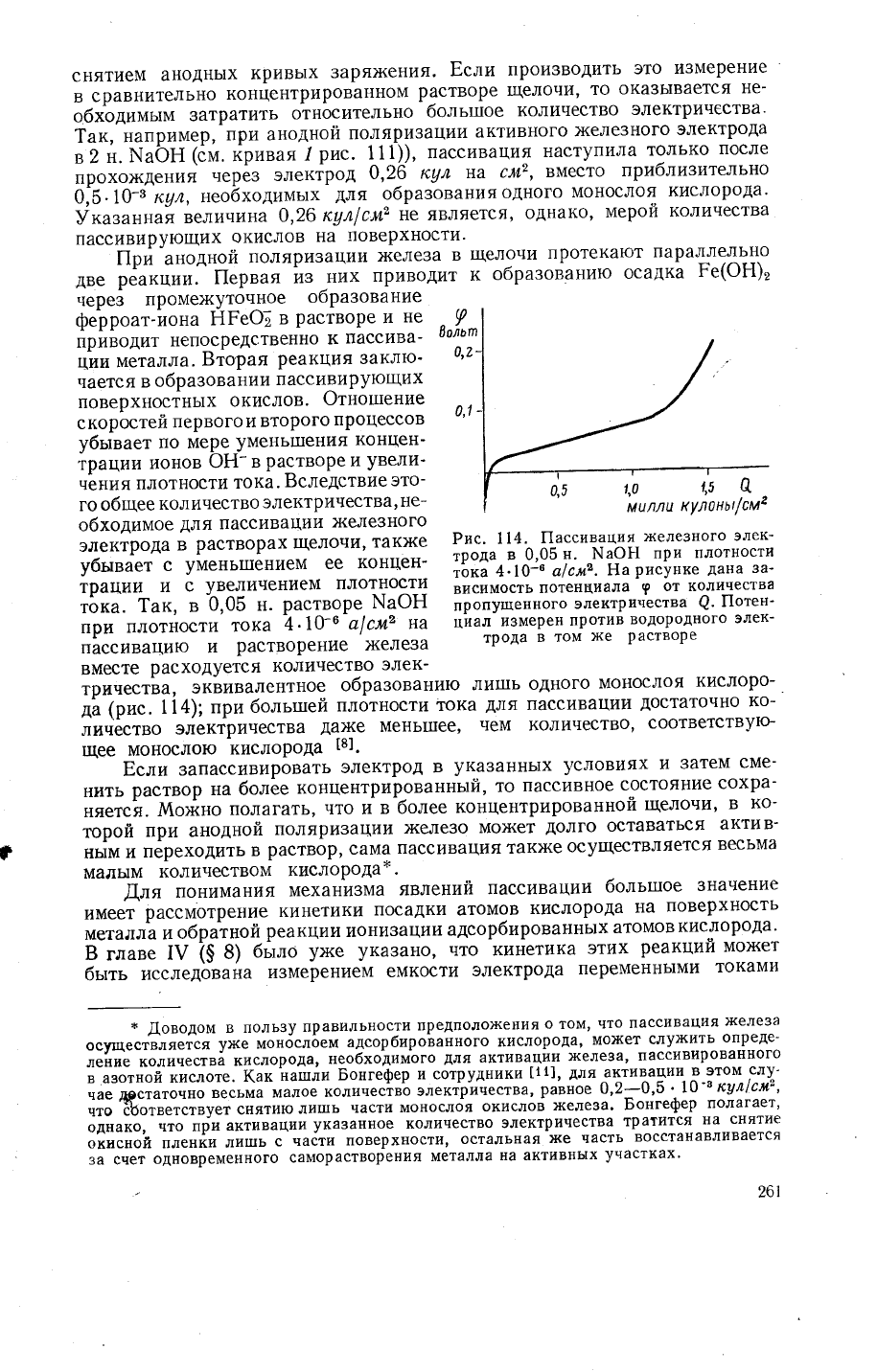
Рис. 114.
|[ассивация
)келезного
элек_
трода
в 0,05
н' }',1аФ!1
при
плотности
т6ка
4.10-6
а|см2.
Ба
рисунке
дана
за'
висимость
потенциала
9
от количества
пропущенного
электричества
@.
|1отен_
цйал
измерет{
против
водородного
элек-
трода
в том
же
растворе
вместе
расходуется
количество
элек_
тричества'
эк|ивалентное
образованию
ли1шь
одного
монослоя
кислоро-
д1
1р'с.
114);
при
больтшей
плотности
тока
для
пассивации
достаточно
ко-
личество
электричества даже
мень1пее'
чем количество,
соответству1о'
щее
монослою
кислорода
|8].
8сли
3апассивировать
электрод
в
ука3аннь1х
условиях
и
затем
сме-
нить
раствор
на болёе
концентрированнь1й,
то
пассивное
состояние
сохра_
й""'"!'.
}4о>кно
полагать,
что 1,гв-более
концентрированной
щелочи'
в
ко_
торой
при анодной
поляризации
'(елезо
мох<ет
долго
оставаться
актив_
Ё
нЁм
и
переходить
в
раствор,
сама
пассивация такх{е
осуществляется
весьма
мадым
количеством
кислорода*.
Аля
понимания
механи3ма
явлений
пассивации
боль:лое
3начение
имеет
рассмотрение
кинетики
посадки атомов
кислорода
на
поверхность
металл
а и
об
р
а1
но
й
р
еа
кци и ио
низаци|1
адсо
рби ров
а
ннь|
х атомов
к]'1сл
о
рода
.
3
главе
|у
($
в)
было
у>ке
ука3ано,
что кинетика
этих
реакции
мох<ет
бьтть
исслед6вана
и3мерением
емкости
электрода
переменнь1ми
токами
обходимое
для
пассивации
;{еле3ного
электрода
в
растворах
щелочи'
так)ке
убывает
с
умень1пением
ее
концен_
то^!1ии
и
сувеличением
плотности
т6ка.
1ак, в
0,05 н.
растворе
}'{аФЁ
при
плотпости
тока
4'10_6
а|см2
на
пассивацию
и
растворение
)келе3а
*
.[1оводом
в пользу
правильности
предполо)кения
о том'
что
л^сс|1ва\|11я
)келеза
осуществляется
у)ке
мон6сл6ем
адсорбированного
кислорода'
может
слу'(ить
опреде_
ление
количества
кислорода,
необходимого
для
активации
)келеза'
пассивированного
Б
.азот"оя
кислоте.
1(ак
на:пли
Бонгефер
и сотрудники
[111,
для
?ктивации
в этом
слу'
чае достаточно
весьма
малое
количест"о
э,екф!'чества'
равное
0,2-0,5
'-1'|'в
кул|см2,
;;;
ъ;;;ъ;;;"ф
с","''литпь
части
монослоя
окислов
)келеза.
Бонгефер
полагает,
однако'
что при
активации
указанное
количество
электричества
тратится
на
снятие
'кисно?
пленйи
ли1[|ь
с
васти
поверхности'
остадьная
11<е часть
восстанавливается
за счет
одновременного
саморастворения
металла
на активнь|х
участках'
261

различной
частоть].
Б
слунае платинового
электрода
при
этом
обнарух<и_
вается'
что
указаннь|е
реакции
протекают
медленно.
Ёаличие
вь|сокого
перена
пр
я}кения'
хара
ктеризующего
3амедленность
реакции
посадки
и снятия
адсорбированнь!х
атомов
кислорода'
хоро1по
иллюстрируется
осциллографинескими
записями
кривь]х
3аря}кения
глад_
кого
п"цатиг{ового
э.пектрода
в
интерва"тте потенциалов
существования
окис-
ной
пленки,
приведеннь1|у1и
на
рис.
115
|12].
Анодная
кривая
3аря}кения
во
всех
случаях
Р2!]1{Ё3а']3€Б
при потенциале
0,5
в, лри
котороп{
поверхность
||а'131!1}{Б!
относительно
свободна
от
адсорби_
рованнь|х
слоев.
|1ри налох{ении
анодного
поляризующего
тока
наблюдается
резкий
сдвиг потенциала,
тем
больтпий'
.тем
больтше
плотность
тока
(кривьте
/
и
2
рис.
115).
Беличина
этого
сдвига
потенциала
опреде_
ляется перенапрях{ением
при
посадке
атомов
кислорода.
|[р, обращении
направления
поляри3ующего
тока происходит
сдвиг по-
тенциала
в
обратную
сторону'
в
ре3ультате
анодная
и
катодная
кривь]е
зарях<ения
о6ра-
зуют
петлю'
ве,цичина которой
характери3ует
ттеобратимость
процессов
образования
и сня-
тия окисной
пленки.
|{еренапрях{е}{ие
катод-
ного процесса
восстановления
окисной
п,:ен.
ки
во3растает
с
увеличением
времени'
про.
Рис.
1]5.
Фсциллографическая
тек1пего
после
посадки
кислорода,
что
ука_
3апись
процесса
окисления
зьтвает
на постепенное
увеличение
прочноста
;;;ъ''}";жъд+:;ъъ?.['"?:?|:
связи
''''',
^'.''р'д'"
с металлоп{.
сной_пленки
(ни;г;ние
кривьте)
в
0,01 н.
н95о.'+1н.
1.{а,5Ф,:
!
|!ассив
ность'
вь13ва
нная
адсорбциот{нь|ма
в
0,01 н.
н25о{+1н.1.{аа5Ф';
и
1'-!:4,2.10_2
а|'см2:
2
г]редстав.|1я1от
3ависимость
по_
нась]щения
свободнь]х
ва"центностей
метал.па
'Ё"ц1,,л^
ф 1''й"р."-!".;';;;
посторонними
атомами.
йзменение
это
мол{ет
тив
водородного
электрода
в
влиять
на кинетику
электрохимических
про-
то],1
)ке
растворе)
."^:::.1::-
цессов
различнь1ми
путями'
например'
через
ства
пропу1ценного,,1'-]|]]-.";
изптенеЁие
строения
двой:того
слоя
или
через
ства@(в
микрокулонахт:асм2)
;;;;;;;;;
ве",1ичин
эгтергий
адсорбции
реа.
€пецифичес
ка
я х
и
ми
ч""
;ъ,
;у#;#;:
''^"орбирова
н нь1х на
поверх-
ности
метал:'та,
в осФб€нности
четко
вь|ступает
при
рассмотрении
влиян|1я
этих
атомов т{а кинетику
анодньтх
процессов'
протекающих
на поверхно-
сти п{еталла'
когда последняя
находится
в активном
состоянии.
1е
>ке ато-
ш1ь1
-или
групг{ьт
атомов'
адсорбция
которь1х
в и|{ьтх
условиях
приводит
к образова_нию
пассивирующих
слоев' могут
ускорять
течение
анодного
пРо1{есса.
(ак
увидим
ни)ке'
адсорбция
маль1х
количеств
кислорода
на
поверхности
х{елеза
из газовой
фазьт
не
умень1пает'
а
уве''1ичивает
реак-
цион-}!уто способность
)келеза
при
анодном
процессе.
}(
аналогичному
ре3ультату
приводит
сопостав'.|ение
скоростей
анод_
ного
растворения
)келе3а
в
растворах
\аФБ
и Б6|.
!,ля
такого
сопостав-
ления
необходимо
определить
3акономерность'
связь]вающую
скорость
растворения
х{еле3а
в кислоте
с потенциалом'
и
проэкстраполировать
ее
на
те 3начения
потенциала,
лр|1
которь1х происходит
растворение
йёлеза
в
щелочи
(рис. 116).
Фказьгвается'
нто прй
одинаковом
з}|ачении потен-
циала
с-ко^рость
растворения
)келеза
в
щелочи
(кривая
б)
гора3до вь]1ше'
чем
в
Ё€1 (кривая
а); скорость
эта приблизительно
йропоршиональна
у
6ольгп

1{о}{центрации
он- в степени
0,7. в обоих
растворах
процессь| анодного
растворения
)келе3а
являются
необратимь]ми
и скорость-
их
определяется
ёамой электрохимической
реакцией,
а
не
диффу3ией.
Баблюдаемое
ра3_
ли|1ие
скоростей
нельзя
объяснить иначе'
как предполагая,
что в
щелоч_
ном
р:ртворе
первой стадией
анодного
процесса
растворения
}келе3а
является
образование адсорбированнь1х
групп'
содерх(ащих
гидроксил.
!,альнейтпее
в3аимодействие
этих
групп
с
раствФром
приводит
к иониза-
ции
и
переходу
в
раствор
поверхностнь1х
атомов
>келеза
|8].
1аким
обра3ом,
в
это1!{
случае адсорбция
кислорода
приводит
к
ускорению
анодной
реа
кции.
€
интереснь!м
слу1|аем
ускоряютцего
действия
окисной
пленки
на
кинетику
электродного
процесса мь1
встречаемся
при
рассмотрении
дей-
ствия света
на
величину
перенапрях(ения
вь|деления
кислорода и
анодного
окисления
металла.
Фсвещение
металлов
с окисленной
поверхность}о
по-
ни)кает' напри1!1ер'
кислородное
пере-
напря'{ение
на
платине
и серебре,
и
перенапря}{<ение.
окисления
серебра,
инь1ми
словами'
ускоряетанодную
элек-
.
трохйминескую
реакцию.
(ак
пока3ал
Б. и. Беселовский
[13],
окисная
пленка
-',2'
слу)кит в это\4
случае
приемником'
улав,цива1ощ'*
.,"''!ой
квайт и
переда-
-0'50
.
у!
6ольп|
г,)
ющи\,1 его
энергию
частицам'
участвую-
щим
в
электрохимическом
акте.
|!ассивация
металла мох{ет
вь1зь1-
ваться адсорбцией
не только кислорода,
-0,?5
-6
-5
-4
но и
других
атомов.
Ёапример,
анало_
Рис.
1 16.
(равнение
скоростей
анод-
гично
кислородной
пассивации
>келеза
"'''
р'.',6рения
)келеза в
раство-
в
щелочах,
в
кисль]х
растворах
проис-
рах
}1€1
(а)
и $аФЁ
(6).
|1отеншиал
ходит пассивация
)келеза
при
адсорбции 9
и3мерен
против
нормалького
водо_
галоидов. Ёаиболее
сильнь1м
пассиви_
'
родного
электрода
рующим
действием
обладает иод,
затем
бром
и
3начительно
более
слабьлм
хлор
г14]'
€
увелинением
концентрации
кислоть]'
например'
серной,
эффект
пассивируюшего
действия
соедине-
ний иода или-
брома заметно
во3растает.
3то
действие
вьтра>кается в
ре3ком
замедлении
катодной
реакции-вь]де-
ления водорода
и анодной-ионизации
)келеза.
1(ак и
вслучае
пассивации
}{елеза кислородом в
щелочах,
здесь,
повидимому' происходит
обра_зо-
вание адсорбционного
химического
соединения
х{елеза
с
галоидом.
1(ак
показь1вают непосредственнь1е
определения,
адсорбированное
количество
галоида при
этом
остается
мень1пе
количества'
необходимого
для
за'
по.}]нения
монослоя.
|,1нтересно
обратить
внимание
на
тот
факт,
нто галоидь]'
как и кисло-
род,
обусловливая
пассиваци}о
металлов в
одних
условиях'
активируют
[.1х в
других.
1ак,
в
присутствии адсор6ирующихся
анионов
возрастает
величина тока
обмена п{ех{ду
амальгамой
цинка
и
раствором
его
соли
(гл.
9|,
$
2). 14оньт хлора
в
щелочнь]х
растворах
депассивируют
х{еле3о
(см.
них<е
$
4).
[
алоидь1
оказь1вают а
ктиви
рующее
действие,
адсорбируясь
в
виде ионов, сохраняющих'
очевидно'
хотя
бьт
в
деформированном
виде'
гид_
ратную
оболонку. 3ти эфекть1 могут
бьтть
истолковань1
на основании
теории
двойного
слоя
при
унете
ф'-потенциала'
как это
бьтло
показано
в главе о водородном
перенапря)кении.
|!ассивирующее
действие
связано,
вероятно'
с
более
глубоким
взаимодействием
ме}кду
галоидом
и
металлом'
приводящим
к образованию
поверхностнь]х соединений.
Б настоящее
вре'

п1я еще нет
такой }ке простой
теории, которая
6ьт
о6ъясняла
полность}о
наблюдающиеся
в этом
случае кинетическиё
эффектьт.
Бозмо>кно'
что
в некоторь1х
случаях
образование
адсорбционнь]х
соединений
с галоидами
так)ке
приводит
не
к
замедленито'
а к
ускорени}о
анодного
процесса
на
металле. 1'\нане,
наприп{ер'
трудно
бьтло
бьт объяснить
тот
факт,
что ско-
рость
анодного
растворения
платинь]
при
постоянном
потенциале
оказь].
вается пропорциональной
концентрации
ионов хлора
в электролц16
|91.
|1ерейдем
теперь к
рассмотрени1о
пассивации'
связанной'с
образо-
ва
нием
относительно
толстого
слоя'
экранирующего
поверхность
электро-
да.
1акого
рода
'пассивацию
мох{но
на3вать
(механической)*,
в отличие
от <химической>,
т.
е. связанной
с химической
адсорбцией,
о
которой
рень
1пла^вь]чте. Бопроса
м меха
нической
пассива
тции
6ьт7и посвящень1^
ра6о'ьт
л.ю.
(уртца,
А.
[.
€амарцева,
Б.
н.
(абанова,
а
так}ке
ряда
иностран-
ньтх
авторов.
1акие
электроднь!е
системь1' как
серебро в
растворах
галогени_
дов
и
свинец
в
растворах
сульфатов' при
анодг:ой
поляризации
покрь]вают_
ся
и3олирующим слоем
соответствующей
соли. Б
качестве
характерного
примера
вьтберем практически
вах<нь;й
и
детально
изунеЁньтй
слунай
пас-
сивации
свинца в
растворах
серной
кислоть1
!:5].
|1рактическое
значение
этого
случая
3аключается
в том' что пассивация
свинца
ограничивает
!Рошесс
ра3ряда
свинцового
электрода
сернокислотного
аккумулятора.
3тот
электрод состоит
из
губтатого свинца' порь1
которого
3аполнень1
электролитом-раствором
серной
кислоть].
[[ри
разряде
происходит
ре-
акция
Рь
+
5о4--:
Рб5Фц
*
2е
(А)
и-образуется нерастворимьтй
сернокисль]й
свинец. 3 ходе
реакц[ц.1
ионь|
5Ф,- потребляются,
а ионь1 Ё*
уАаляются
переносом'
вследствие
чего
кон'1ентрация
серной кислотьт
у
отрицательного
электрода
падает.
Реакция
(А)
в
аккумуляторе
никогда не
идет
до
конца:
и3
наличного
количества
свинца
используется
только
некоторая
часть'
величина
кото-
рой
определяет
емкость электрода**. ||ри
увеличении
плотности
тока
и
по_
них(ении температурь1'величина
емкости свинцового
электрода
падает.
Фбьтчно
это
явление свя3ьтвали с
умень1пением
концентрации
сер-
ной кислоть1
в
порах' которое' как полагали'
долх<но
сильнее
сказь1ваться
при
ни3ких температурах вследствие
3амедления
диффузии.
Фднако
и3у_
чение
поведения
гладкого свинцового электрода
показало'
что
ва}кнь1м
фактором,
ограничивающим возмо}кность
использования
металлического
сви нца' являетс
я
пассивация'
проис ходяща
я
Ёследствие
за
к
рь1ти
я
бол ьтпей
части
поверхности
свинца
непроводящим
слоем кристаллов
Рь5о4,
поля-
ри3ация
)ке такого электрода
определяется перенапря)кением
анодного
процесса.
3ависимость
потенциала свинцового
электрода
в
растворе
н25о1
от
пропущенного
количества электричества
изобрах<ена на
рис.
!|7'
Ёачальная точка оси ординат соответствует
обратимому потенциалу
свинца
в
растворе
серной
кислотьт'
нась1щенном
сернокисль1м
свинцом.
*
Ёеобходимо
отметить' что некоторь|е
авторь| вкладывают
в термин
(механиче_
ская) пассивация несколько иное
содер)кание.
**
1ермин
<емкость>
используется
здесь не в
том смь1сле' в
котором мы неодно-
кратно
употребляли
его в предыдущих главах
(т.
е. емкости
двойного
слоя'
аналогич_
ной
емкости конденсатора), а
в том, в
котором
он применяется
в
литературе по химиче_
ским источникам
тока.
йнапе говоря)
емкость о3начает
здесь количество
электричества'
отдаваемое электродом при
разряде.
1ермин
(емкость))
в
этом смысле
мо)кет быть так>ке
заменен
вь|рах(ением
(выход
электрохимического процесса>.
264
|!ри
анодной
поляризации
потенциал сдвигается в
полох{ительну1о сторо_
ну. 3лектрохимическая
поляризация
при
реакции
ионизации
свинца
при
маль1х
плотг1остях тока
мала' и
этот
сдвиг
потенциала
вь]3ван в
основном
увеличением
концентрации ионов
РБ**
в6лизи
поверхности
электрода.
|1ри
дости)кении
определенного
пересь]щения
раствора
сернокисль]м
свинцом
на
поверхности электрода
начинают
вь|деляться
кристалль{ сернокислого
свинца'
что
приводит к
умень1пени1о
пересь1щения
||
лоявлению на
кривои
некоторого
сдвига
потенциала
в
обратном направлении
(унасток
А на
кривой
рис.
1|7). Аа кривой
потентт,иал-количество
элек1'ричества
(при
постоянной
плотности
тока поляризашии)
в
ее
начальной
стадии наблю_
дается,
таким
образом,
некоторьтй
перескок значения
потенциала
3а
ве-
личину'
которая соответствует
установив1пемуся
процессу
образования
кристаллов
Рь5о4,
изобрах<аемому
горизонтальнь|м
участком
кривой.
Б
отличие
от
аналогичного
явления'
которое наблюдается
при
снятии
окиснь]х
слоев с
поверхности
платинь]
и
родия
(рис. 35
и
36),
перескок этот
3ависит
от
труднос1у|
начала
пРоцесса
кристаллизации
растворенного
веще-
ства' в
то время
как
в
ранее
описанном
случае
мь1'имели
дело
с чисто
поверх-
ностной
реакцией.
|[ри
появлении
пер-
вь]х
кристаллов
Рб5Ф4
на
поверхности
электрода
потенциал не во3вращается'
однако'
к
равновесному
3начен\4ю'
и
раствор
остается
пересь1щеннь]м'
хотя
и в
несколько
мень1пей
степени,
чем
до
начала образования
слоя
Рь5о4.
Беличина пересь1щения 3ав\4сит,
.[
ФА-
ной
сторонь]'
от плотности
поляри3ую-
щего
тока
и
с
другой-от
скорости
кристалли3ашии
Рб5Ф'.
|1осле пропускания
определенно-
го
количества
электричества
ч
(рис.
|\7\,
при
дальнейгпем
пропускании
тока
потенциал
электрода сперва
по_
немногу
возрастает'
а 3атем
ре3ко
сдвигается в
положительную сторону_
наступает
пассивация. 9то возрастание
поте1{циала' которое
ках<ется вне-
запнь|м' вь]зь]вается
возрастанием
плотности тока в
порах и3олирующего
слоя соли в
конце
пРоцесса 3акрытия
поверхности.
1'1змерения
\1оказал\4,
что при анодной
пассивации свинца
током
постоянной силь1 емкссть
Авой-
ного слоя
умень1|]ается
во
времени
приблизительно линейно
(рис.
118),
и'
следовательно'
поверхность свинца 3акрь|вается
слоем
сернокислого
свинца
равномерно.
[_|р"
равномерном
во времени
закрь1тии
поверхности
потенциал'
в
соответствии
с логарифмической
зависимостью
потенциала
от плотности тока'
долх{ен
возрастать
так'
как это
наблтодается
на
опь1те
(рис.
117).
(оличество
электричества,
которое гтеобходимо
для
полной
пассивации свинца в этих
условиях'
соответствует
образованию
на боль-
ш:ей части
поверхности металла
слоя соли
толщиной
порядка одного
микрона[151.
Ёаличие
кристаллических
слоев нерастворимьтх
солей на
поверхности
эдектрода при такой
<механической>
пассивации обнару>кивается
так)ке
по
появлению
двойного
лучепреломления
в
отра'<енном
свете.
Фписанная вь|1ше
пассивация
}келе3а
в
щелочг{ь|х
растворах
такх{е
со-
прово},(дается
появлением
слоя нерастворимого
соединения
Ре(ФЁ!)9"
ц
мв
60
40
20
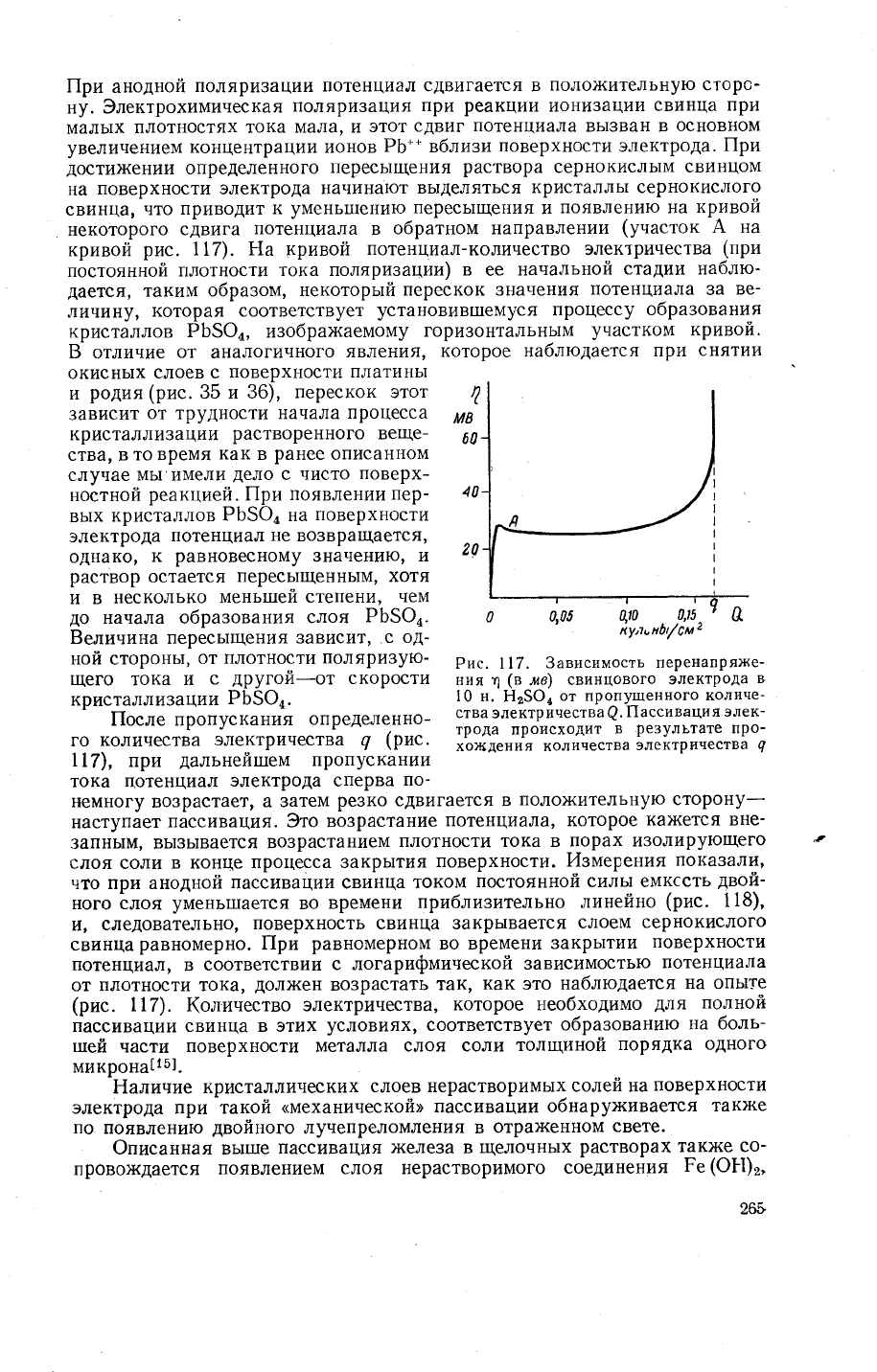
Рис' \|7.
3ависимость
перенапря)ке-
ния
1
(в
лв)
свинцового
электрода
в
10 н.
!12$@,
от пропущенного
количе-
ства
электринества
@.
|!ассивация
элек-
трода
происходит
в
результате
про-
хождения количества
электричества
{
265
обволакивабщего
электрод.
||ассивация
свинца
отличается'
однако, от
пассивации
>келеза
тем, что
рь1хль!й
слой
Ре(ФЁ),
не
преграх{дает
доступа
электролита
к
электроду.
||оявление такого
слоя
прямо
не влияет
на элек-
трохимические
свойства металла'
которь]е 3ависят
в
основном
от возник-
новения
гора3до
более
тонкого
слоя
пассивирующего
окисла.
|1оявление
слоя
Рь5о4, г1лотно
прилегающего
к электроду,
нао6орот,
резко
сокра!'!,ает
его активную
поверхность и
приводит
тем
самь1м
к
умень1шению
его
элек_
трохими!{еской
активности.
Ёаряду
с этими
кореннь]ми
различиями
ме}кду
протеканием
процесса
пассив[ций в
обоих
случаях
существуют
и некоторь1е
черть1
сходства.
в
обоих
случаях
количество
электричества
ц,
необходимое
для
пассивации
электрода'
уп{ень1пается
при
пони}кении температурь]
и
увеличении
плот_
0
|
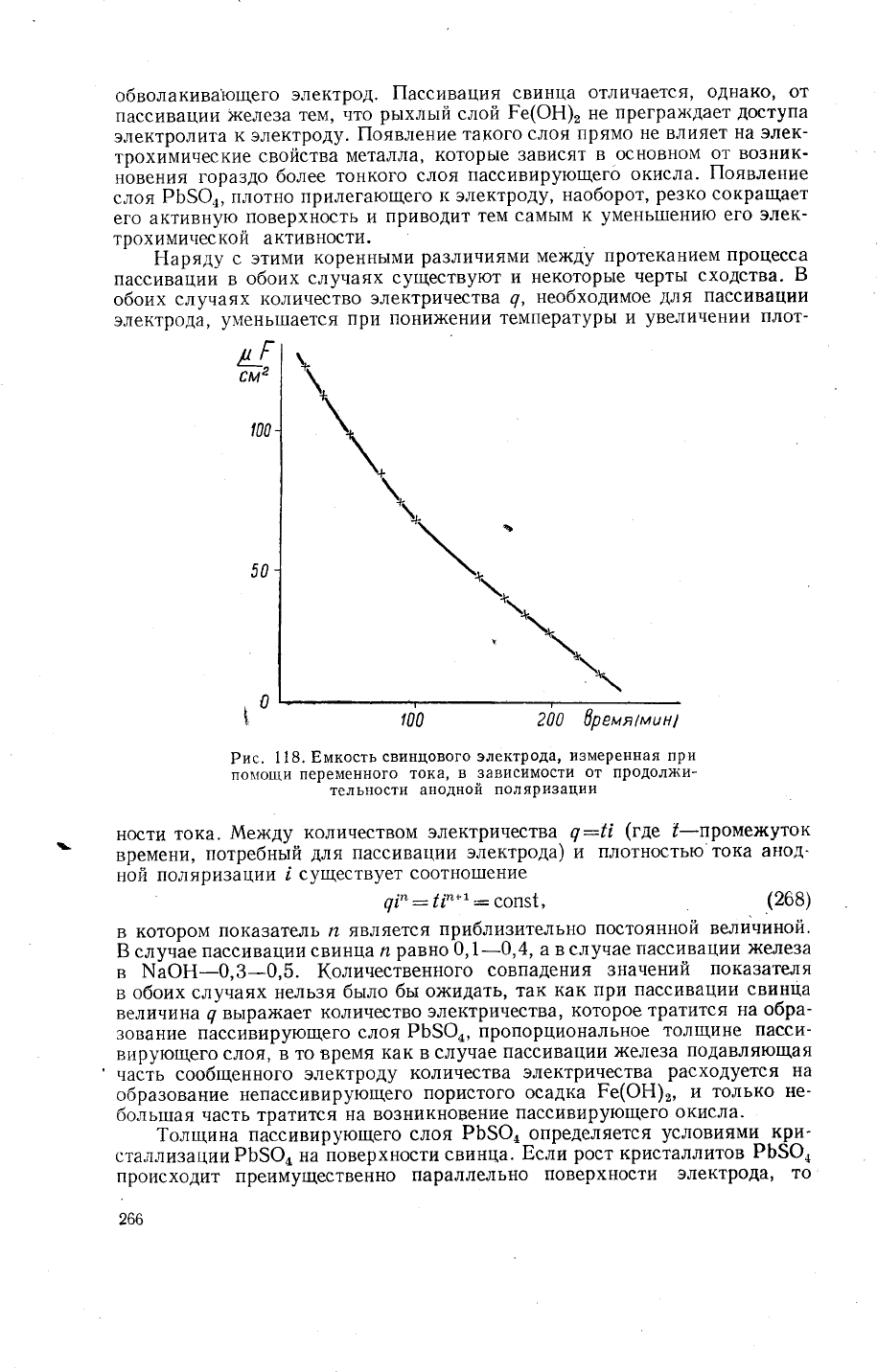
Рис.
1 18.
Бмкость
свинцового
электрода'
измеренная при
п
о 1|ощ
и
"'
,
"'ъ:1}:1?"
"?|3;#"
#' 1:;}ш1.#
пр
одол х{
и
-
ности
тока.
}1ех<ду количеством
электричества
ч:[1
(где
|-промех<уток
времени,
потребный
для
пассивации
электрода)
и
плотностью'тока
анод_
ной
поляризац|4и
!
сушествует
соотно1пение
ц!":!Р'1:
€Ф|51,
(26в)
/1
г
};а
200
100
в
котором
показатель п
является
пр_ибли3ительно
постоянной
величиной.
Б слунае
пассивации свинца
п
рав|то
0,
1
-0,
4,
а
в случае
пассивации
}}(еле3а
в
шаон-0,3_0,5.
(оличественного
совпадения
3начений
пока3ателя
в
обоих случаях нельзя
бьтло
6ы ох{идать,
так
как при
пассивации
свинца
величина
9
вь]ра}кает
количеств-о
электричества,
которое
тратится
на обра-
зование
пассивирующего
слоя
Рь5о4,
пропорциональное
толщине
пасси-
вирующего
слоя, в то
время
как
в
случае
пассивации
'(елеза
подавляю|т\ая
часть сообщенного
электроду
количества
электричес1ва
расходуется
на
обра3ование непассивиру}ощего
пористого
осадка
Ре(ФЁ)',
и
только
не-
больтшая часть тратится
на
возникновение
пассивирующего
окисла'
1олщина
пассивирующего
слоя
Рб5Ф' определяется
условиями
.кр]'|_
сталли3ации
Рь5о4 на
поверхности
свинца.
Рсли
рост
кристаллитов
Рь5о4
происходит преимущественно
параллельно
поверхности
электрода'
то
266
0ремя
/"шн1
:::9"т::::-1ступает
рань1пе'
и во3никает
более
тонкий
пассивирующий
с'|0и'
г1апротив'
относительное
увеличение.
скорости
роста
перпендику-
лярно
к поверхности
приводит
к
утолщению
пассив"рующего
ёлоя.'
БЁ_
лич|1[1а
отно1шения
скоростей
роста
в направлении
парал"тельном
и
перпен-
дикулярном
поверхности'
повидимому'
_связана
с
растворимостью
рБзб.
и со
степенью
-пересь]щенця
раствора
Рь5о4,
образуюфгося
у
поверх_
ности
свинца.
}словия,
благойриятствующие
вь1соким
,ере",'щей
""*
1"Б",
например'
повь]1пение
плотности
тока
или
при
заданной
Ёлотности-сни}ке_
ние
растворимости
Рь5о4
вследствие'
и3менения
концентрации
серной
кислоть1
или пони)кения
температурьт),
приводят
к
образованию
б?лее
тонких
пасс.ивирующих
слоев
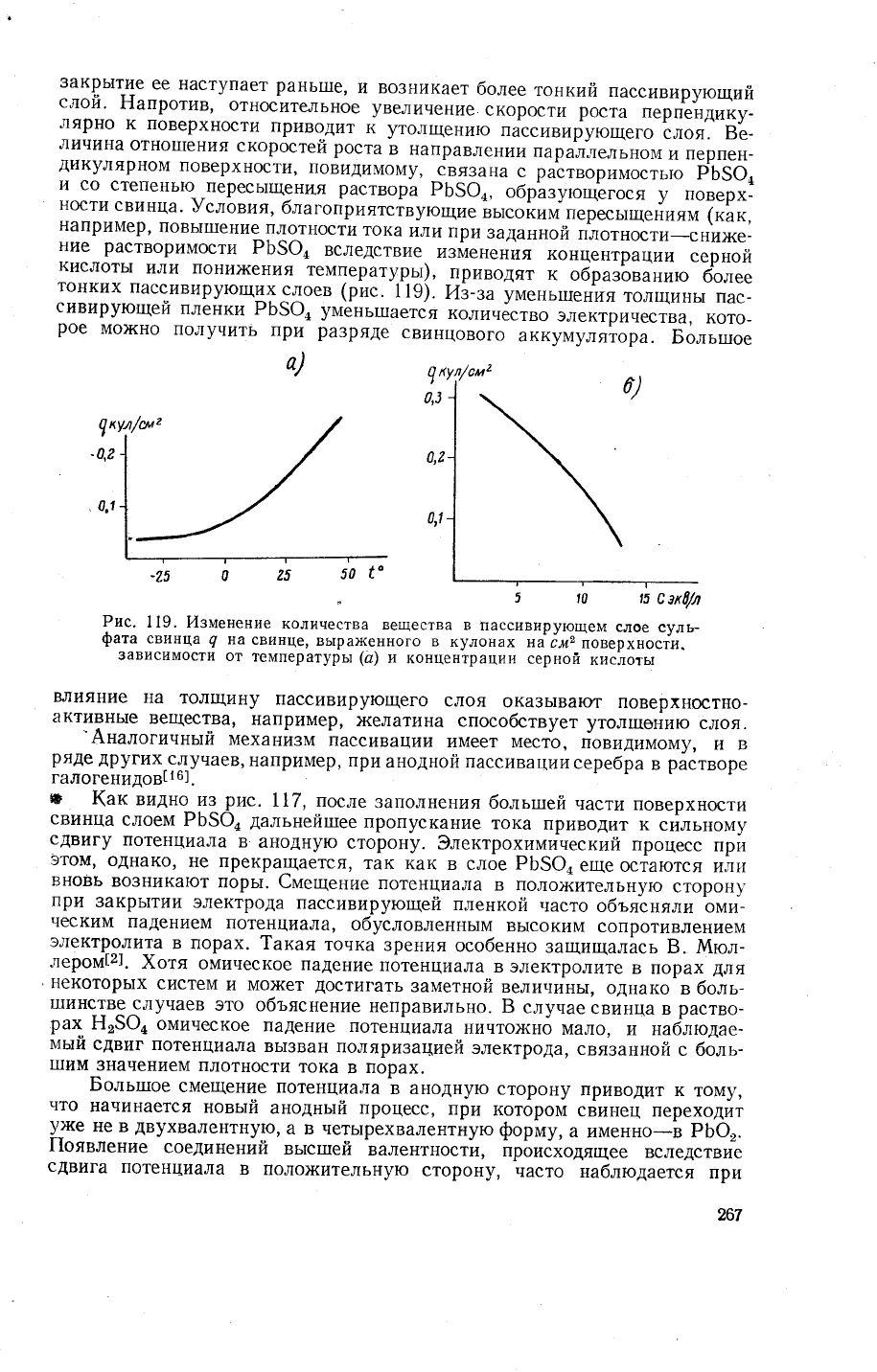
(рис.
119).
Аз-за
умен,ш-тения
толщинь!
пас-
сивирующей
плёйки
Рь5о|
умЁньтпается
количество
электричества'
кото-
рое
мо)*(но
получить
при
разряде
свиццового
аккумуля\ора.
Больтпое
Ф
5о
{'
Рис.
119.
|4зменение
.,'",".'"'
вещества
,
,'".1"',,
.:;"-
"'::'"{::
фата
свинца
4
на
свинце'
вь|рая{енного
в
кулонах
на'Ёл2
Ёоверхности.
зависимости
от
температурьл
(а)
и
концентрации
серной
кислоть!
влияние
на
толщину
пассивирующего
слоя
ока3ь1ва[от
поверхностно-
активные
вещества'
например'
)келатина
способствует
утолщонию
слоя.
-Аналогичньтй
механизм
пассивации
имеет
место'
повидимому'
и в
ряде
других_сл_учаев' например'
при
анодной пассивациисеребра
в
растворе
галогенидов[
1 6).
*
(ак
видно-у3^!ис.
117, после
3аполнения
больтпей
части поверхности
свинца
слоем Рь5о4
дальнейгпее
пропускание
тока
приводит
к
сильному
сдвигу
потенциала
в
анодную
сторону.
3лектрохимический
процесс
при
этом,
однако'
не прекращается'
так
как
в слое Рб5Фц
ёп{€
Фста1Фтся
|1,л\1
вновь
возникают
порь1.
6мещение
потенциала
в поло'{ительнуто
сторону
при
закрь1тии
электрода
пассивирутощей
пленкой
часто
объясняли
оми-
ческим
падением
потенциала,
обусловленнь1м
вь1соким
сопротивлением
электроли1а
в порах.
1акая
точка
зрения
особенно
защищалась
Б. }1юл_
лером|2!.
{,отя
омическое
падение
потенциала
в электролите
в порах
для
.некоторь]х
систем
и
мо)кет
достигать
заметной
величиньт'
однако
в боль_
1пинс-тве
9лучаев
это
объяснение
неправильно.
Б
слунае
свинца
в
раство-
рах.
Ё{'5Ф*
омическое
падение
потенциала
ничтох<но
мало'
и наблюдае_
мый
сдвиг потенциала
вьт3ван
поляризацией
электрода'
свя3анной
с боль_
[пим
значением
плотности
тока
в
порах.
Больтпое
смещение
потенциала
в анодную
сторону
приводит
к
тому,
что
начинается
новь:й
анодньтй процесс,
при
котором
свинец переходит
у}ке
не в
двухвалентну|о'
а в четь|рехвалентную
форму,
а
именно-в
РБФ'.
||оявление
соединений
вьтсш:ей
}алентности,
происходящее
вследствие
сдвига
потенциала
в
поло)кительную
сторону'
часто
наблюдается
при
267

явленииях
пассивации,
незавиоимо
от
характера
пассивирующей
пленки'
[ак.
при
пассивации
хрома
нормальнь1й
прошесс
перехода
хрома
в ионь!
д"у*,.'"*'ного
(и
частично
трехвалентного)
хром,
,р:1Р1^щ'ется'
но
при
достаточно
вь]соких
полох{ительнь1х
потейцйалах
наблюдается
о6разо-
вание
ионов
хромата'
в
которь]х
хром
1пестивалентен.
)(елезо
в
кон_
центрированнь1хщелочнь1храстворах'приведенноевпассивноесостояние
по отно[пению
к
пр0цессу
образования
соединений
двухвалентного
}келеза'
в зависимости
от
условий
опБ1та
мо)кет'
как
ска3ано
вь11ше'
переходить
в
раствор
с
образованием
ферритов'
в
которь1х
)келезо
"р'1_"_1'::]}_9:-]*1;
йр'й
"й"'о''""
,','''"тельных
потенциалах,
с образованием
соединений
_
стивалентного
>келеза-ферратов'
Фазовь:е
пассивирующйе_слои,
отделяя
больп:ую
или
мень1пую
часть
поверхности
электро!а
от
раствора'
могут
и3мен_ять^
усл^о-вия
протекания
электрохимических
|?!.ш"};
",
'Ё,'л,"ой,
не
закрь1то*
пов19111'':
Ё:::
слой'обладает
значйтельной
металлической
электропроводностьто
(как'
й',р''"р
слой
Ре'Ф'
на
>келезе),
то
и на
закрьттой
поверхности
лр|1
подхо_
дящих
условиях
может
протекать
электрохймический
процесс.
1ак,
если
растворсодер)киткислород,онмо)кетвосстанавливатьсянетолькона
незакрь1том
металле,
но
й
на
поверхности
окисного
слоя
(см.
следующую
главу).
1\ас"и"ация
анодно
растворяющегося
металла
в
некоторь1х
случаях
существенно
зависит
от
йристаллической
формьт
появляющегося
осадка'
Ёапример,
при
анодном
растворении
цинка
в
щелочах
при
небольтших
плотностяхтока'какиеприменяютсявгальваническихэлементах'пас.
сивацияцинкапроисходитли1пьвтомслучае'к9гдаизнась]ще!1ногоцин.
катного
раствора
вь]деляется
ромбинеская
модифик111:
:"др'окиси
цин-
6д11?1.
3{о
имеет
место
в
ко9центрированнь]х
растворах
щелочи
при ни3_
ких
температурах
ил\4
в
растворах
щелочи
средних
концентраций_1!"
_1'.у_
натной
'емпературе.
||ассивация
электрода
связана
с
тем'
что
эта
моди-
фикация
гидроокиси цинка
покрь1вает
электрод
спло1шнь1м
плотно
-пРиле-
|д.|;;;';;;ы.
'оара3ование
х?е
негидратированной
окиси
цинка
(в
кон_
центрированнь]х
растворах
едкого
кали
1ри
комнатной
температуре)
или
призматической
модйфикашии
гидроокиси
цинка
(в сравнительно
раз_
бавлейньтх
растворах
прй низких
температурах)
не
приводи'
1 :3:::_::;
ции
цинкового
электрода,
так
как
кристаллизация
'""*
_*-"ц:::11'
и
рост
их
кристаллоЁ
не
приводит
к
появлению
плотно
прилегающеи
сплотпной
пассивирующей
пленки
на
электроде'
Ёесмотря
на
^йирокую
распространенность
явлений
<механическои>
лассивации.
нух{но
пом нить,'
что
-бол
ьтпое
число
наблюдаемьтх
-:Р:_
:::::'
].ц"],
"',",
п
не могут
бь:ть
истолковань]
на
основе
,р'_д"3^"]"*].}]':
учить1вающих
ли1шь
экранирующее действие
пассивирующего
слоя'
\ак
это
ух(е
подчеркивалосБ,
разнообразньте
эффектьт,
которь1е
наблтодаются
в
присутствии
постороннйх
атомов
на
поверхности_
электрода'
свидетель-
-',уй'"'
глубоких
хймических
и3менениях
^ее
свойств
и
н-е
могут
бьтть
сведень1
к
механическому
закрь1тию
поверхности.
Бьтло
бьт
однако,
со_
вер1пенно
неправильно
сделать
отсюда
вывод
о
том'
-'"-^?:|::1Р_"':',}::
поверхности
не играет
существенной
роли
в
явлениях
пассивности'
\-0-
стояние
поверхноётного
слоя
зависит
от
плотности
п_роход:1т2^::-
рез
него
тока.
|[оследняя'
)ке'
очевидно'
во3растает
во
много]-11:€"]1]]'1'^"'{
йая часть
поверхности
электрода
экранирована
непроводящеи
пленк0и
,
окислов
или
нерастворимь]х-солей,
а
электрохимические
процессь1
сосре_
доточень1
только
в
порах.
1(роме
того'
переме1пивание
раствора
в
порах
3атруднено'
что
о6леЁчает
изменение
его
состава.
|!оэтому
при
построе-
"йй
Ё''"'а
теории
пассивности
обя3ательно дол}кна
бьтть
унтена
}1е
толь_
268

ко химическая
природа
адсорбционнь1х
или
других
пассивирующих
слоев,
6лизких
по
своей
толщине
к молекулярнь1п{'
но и
ра3нообразньте
структур-
ные свойства
более
толсть]х
пленок'
находящихся
на
поверхности
элек-
',',?|"'',"ческая
3аслуга
1пирокой
по_становки
этой
части
проблемь1
пас'_
сивности
принадле)кит
акад.
'в.
А.
(истяковскФму[51,
которь]й
в
своей
фильмовой
теории
пассивности
и
коррозии
охватил
цель1и
ряд
процессов'
происходящих
в
окиснь!х
пленках
и
влияющих
на
их
'3ащитнь1е
свойства'
в.
А.
(истяковский
подчеркивает,
что
защитнь1е
пленки
дол)кнь1
иметь
коллоидное
строение
и считает'
что
ра3ру1пение
пленки
идет
3а
счет
обра-
зования
корро3ионнь1х центров'
напоминатощего
кристалли3ацию;
с
поло-
х{ением
об_йсчезновении
защитнь]х
свойств
при
кристалли3а|\и'1
пленки
в
настоящее
время
согласиться
нельзя.
-
йр'
рассйотрении
пассивности
нер)каве|ощих
сталей
|.
Б'
Акимов|:8]
пр!11пел
к вь1воду'
что
боль1пая
часть
поверхности.3акрь]та
тонкой,
плот-
н6й
(фазовой) пленкой,
под которой
(и
в
ее
порах)
находятся
атомь|
или
ионь!
кислорода'
прочно адсорб;рованньте
на
поверхности.
€очетание
тонкой'
эластичной,
прочной
пленки
и адсо'рбированного
кислородного
слоя
определяет
вь1соку}о
корро3ионную
стойкость
нер>кавеющих
сталей
в средах'
содерх{ащих
окислители.
'Аля
даль;ейшего
ра3вития
на1пих
представлений
о
явлении
пассив-
ности
6ольтлое
3начение
имеет
исследование
кристаллической
структурь|
поверхностнь1х
пленок[!9],
их
пористости'
распределения
в них
дефект_
нь1х мест
|4
т.
д.|201,
с
применением
методов
элек'тронографии,
электрон-
ной микроскопии
и
элекърохимических
и3мерений.
$ .3. оБРА3овАнив
пАссивиРующих
словв
нА гРАницв
мвжду
йЁтдллом
и элвктРо,,|итом
и
окислвнив
мвтАллов
гА3о-
оБРА3нь1м кислоРодом
'
6опоставление
явлений'
происходящих
при образовании
окиснь1х
пле-
нок на
границе
ме}кду
металлами
и
электролитами'
с однои
сторонь1'
и
при
в3аимодействии
мета;лов
с га3ообразньтм
кислородом-с
другой,
предста_
вляет
значительнь1й
интерес.
Фстановимся
вначале
вкратце
на
основнь|х
кинетических 3акономер-
ностях'
которь1м
подчиняются
последние.
Аля
киЁетики
взаимодействия
металлов
с газообра3нь1м
кислородом
существенное
значение
имеет
соотно1пение
ме>кду
атомнь1м
объемом
ме-
талла
и
молекулярнь1м
объемом
обра3ующегося
и3
него
окисла.
в
том
случае'
когда
последний
больтше
первого'
как это имеет
место'
например'
пр;
окислении
>келеза или
алюминия'
в
результате
окисления
часто
обра-
зуется
спло1пнои
слой
окисла,
в той
или
другой
мере
о6лада1ощий
3ащит-
ными
свойствами.
Бследствие
умень1пения
объема,
связанногос
переходом
от.атома
металла
к содер}кащемуся
в
окиси
иону,
увеличение
объема
при
,окислении
металла
происходит
не
всегда;
например'
оно
не
происходит
при окислении
щелочнь!х
металлов.
в
этом
случае
не
получается
спло1п-
нь1х
слоев
0кис./|а' и
окисление
идет
беспрепятственно
до
ко}1ца,
по
край-
ней
мере
при не сли1пком
ни3ких
температурах.
|[ри
налинии
спло1шнь]х
окиснь]х
пленок
скорость
окисления
у}1ень_
т'|'ается
во времени
по характернь1м
законаш1.
наиболее
простое
соотно1шение
получается в
том
случае'
когда
толщина
образовавшейся
пленки
превь]-
1шает
молекулярнь1е
ра3мерь|,'и
скорость
процесса в
целом
определяется
диффузией
!"аЁ'ру'шего
вещества
через
пленку'
причем
коэффициенту
269

диффузии
!
мо>кно приписать
постоянное
3начение'' не
и3меняющееся
при
увеличении
толщинЁ пленки х' 1ак
как скорость
диффузии
обратно
про-
порциональна
толщине
с"цоя' через которь:й
происходит
диффузия,
то
в этом случае очевидно'
4х
ко
а[ х'
(26э)
где 1(-некоторь;й
фецтрр
пропорциональности'
|-время.
||ри
интегри-
ровании уравнения
(269) получается
соотно1пение
х2:2(|!,
р7о)
вь1ра)кающее
параболический
закон
роста
пленки. 9равнение
(270)
пра-
вильно только
при
не сли1пком
маль{х
значениях
п, так как
вь11пеизло}кен-
нь:е
-с-ообра)кения
неприменимь1
к пленкам
молеку./1ярнь]х
размеров|2:).
Аз-за медленности
Аиффузионнь1х
процессов
в
твердь1х
телах
диффу_
зик) в спло11]нь1х окиснь|х
пленках'
покрь1вающих
металл'
практически
мо)кно наблюдать только
при
повь!1пенных
температурах.
Ёекоторь!е
сорта
сталей
(например, хромисть]е
стали'
содерх<ащие
добавки
кремнйя'
моли6-
дена
|1ли
других
элементов)
сохраня}от
устойтивость
по
отно1пению к кис-
лороду
при
вь1соких температурах'
достигающих
1000"
с.
Фсобьтй
интерес представляет
вьтяснение
вопроса о
том'
какие
именно
частиць]
диффундируют
через пленку.
(ак
показь1вает
от]ь]т' во многих
случаях
при
росте
пленок под
действием
кислорода
(и
других
агрессивнь|х
агентов'
например'
серьт' галоидов)
происходит
дифузия
металла
от гра-
ниць1 металл/пленка к
ее вне1шней поверхнрсти'
причем
металл
лифф}н_
дирует
не
в виде
атомов'
а
в
виде
ионов с'одновременнь|п{
перемещением
электронов. 3лектронь! присоединяются
у
внетпней поверхности
пленки
к кислороду
с
образованием
ионов кислорода..
1аким
образом,
в
пленку,
с одной сторонь|' поступают
ионь{ металла'
с
другой
>ке-ионьт
кислорода'
и
пленка
растет
в
ре3ультате
электрохимического
пРоцесса. причем
замь|-
кание этой своебразной
электрической
цепи
происходит
благодаря
дви_
*
"
"
1?,
;{
:;#"""1'";
#"'*', #
{,?Ё]'
1,];
н
к
у
в о 3
м
о}к н о то
л
ь ко'
."
', "
'",
, ,
" "
отличается от стехиоп{етрического'
причем
отклонения
эти бьтвают
ра3ного
рода.
1ак,
в
случае окисления
цинка
окисная
пленка
вблизи поверхности
металла содер)кит
избь]ток ионов
цинка
по
сра'внению с
составом' которь}й
бы точно
отвечал
формуле
7пФ,
и
эквивалентное
количество
электронов:
14збьтточньте
ионь1
7п**
распределень]
мФкду
у3лами ре1петки.
} внегпней
поверхности концег{трация
этих
избь;точньтх
ионов
падает
почти
до
нуля.
|1ри процессе
окисления происхолит
диффузия
иог1ов
цинка
и
э"цектро_
нов от
внутренней к нарух{ной поверхности
п.']енки.
Аругая
картина
наблюдается
в случае окисления
меди с образованиепт
закиси меди. €остав
образующегося
окисла
и
в
этом случае
отличается от
стехиометрического
состава
€ш'Ф, однако
у)ке
не
в сторону
избьттка
шце_
талла'
а
в сторону
избьттка
кислорода.
Б
ретпетке
€ш'Ф насть мест' которь]е
дол)кнь1
бьтли
бь:ть
3анять| ионами
€ш*, свободнь:,
а
недостаток
в
поло-
}кительнь|х
3арядах по сравнению
с зарядами
анионов
Ф-- компенсируется
заменой
части
ионов €ш* на
ионь] €ш**.
|1оследние
мо}{но
рассматривать,
как места
недостатка
электронов
или электроннь1е
(дь1рки>.
Ё1едостана
ионов €ш* и
концентрация
(дь1рок)'
очевидг1о'
больтше
у
втлетпней границь{
слоя'
1]е\{
у
внутренней.
!-|ри
окислении
происходит
дифузия
ионов 6ц"
от
внутренней к
вттетшней
поверхности'
осуществляемая
благодаря
ряду
последовательнь|х
переходов
ионов €ц*
с
занять]х
мест
на свободнь:е, и
обмен
электронами
мех{ду
ионами €ш*
и €ш**,
которь;т] мо>кно
рассматри-
27о
