Фрумкин А.Н., Багоцкий В.С., Иофа З.А., Кабанов Б.Н. Кинетика электродных процессов
Подождите немного. Документ загружается.

11ри
изунен|4|4
|1
сопоставлении
кинетических
закономерностей
в
рас-
творах
с
различнь1ми
3начениями
рн
целесообразно
сравнивать
величинь|
потенциала
поляри3ованного электрода'
а
не
величинь[
перенапрях{ения.
!,ело
в
том'
что если
рн раствора
меняется'
то изменение
перенапря)кения
обусловлено
не только
сдвигом
потенциала
полярчзованного
электрода'
но
и
сдвигом потенциала
равновесного
электрода.
14зменение
перенапря-
){{ения
при
переходе к
раствору
с
другим
3начением
рБ
поэтому
у)ке
не
мо)кет
слух{ить
характеристу1кой
и3менения
потенциала
поляри3ован-
ного
электрода.
Бьтшле
бь:ло
отмечено'
что в
разбавленнь1х
растворах
чисть1х
сильнь|х
кислот
перенапря)кение
не
зависит от
концентра\\'|и
кислоть1'
3то
озна'
.0'1
мнс7
-1,0
п от
\3,0
я
и
-,,0.
"
-70""
-10,0
-
.
-12,5
-
|о
-г
!ц| а|слт2
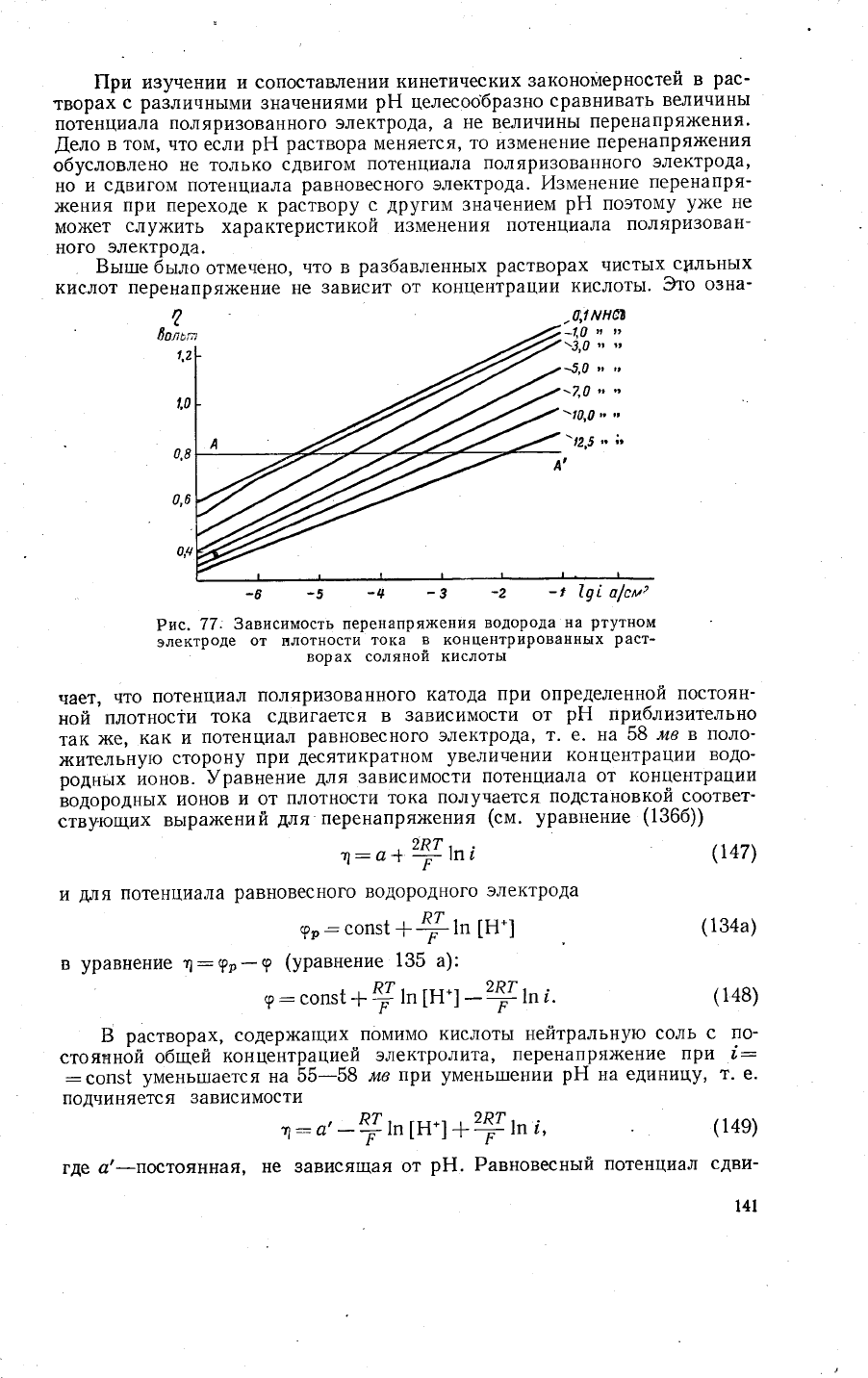
Рис.77:
3ависимость перенапря)кения
водорода
на
ртутном
электроде
от плотности
тока
в
концентрированных
раст_
ворах
соляной кислоть1
чает'
что
потег{циал
поляризованного
катода
при опре_деленной
постоян-
ной
плотносфи
тока
сдвигается
в
3ависимости
от
рн
прибли3ительно
так
х(е'
как п
потенциал
равновесного
электроА2,
1.е.
на 5в мв
в
лоло-
}{ительную
сторону
при
десятикратном
увеличении
концентрации
воАо-
роднь|х
ионов.
9равнение
Аля
зависимости
потенциала
от
концентраци|4
Ёодороднь:х
ионов
и от
плотности
тока
получается
подстановкой соответ-
ству-ющих
вь|ра)кений
для
перенапря}кения
(см.
уравнение
(136б))
(\47)
( 1
3{а)
(148)
Б
растворах'
содерх{ащих-.помип{о
кислоть] нейтральную
соль с
|о-
стоянной
общей
концентрацией
электролита'
перенапря)кение
при
'_
:€Ф||51
умень1пается
на
55_5в
мв
лри
умень].1]ении
рн
на
единицу,
т. е.
подчиняется
3ависимости
[н-]
+
21'
1,
с,
(140)
где
с'_постоянная,
не зависящая от
рЁ.
Равновесньтй
потенциал
сдви-
141
2
8ольп
-3-5
и
м\я
потенциала
равновесного
водородного
электрода
9р:сопз1
++1п
[Ё-]
в
уравнение
т]_
9р-9
(уравнение
135
а):
9:
соп5{
+
$:п
1н'1_$:п;.
1:-
а'
_#'"

гается
при
этом на
такую >ке
величину
в поло}{(ительную сторону. 3то
озна-
чает,
что
при
десятикратном
увеличении
концентрации водороднь|х
ионов
потенциал
электрода
лри
!:сопз1
становится
на
2х0,058:0, 116
с более
полох(ительнь1м:
9:
соп51
++1п
[Ё-]
-$т"
;. (
150)
Б последнем
уравнении
коэфишиенть1 перед
логарифмом концентра-
ции
водородн!1]х
ионов и
перед
логарифмом
плотности
тока
равнь1
по
величине и отличаются
знаком.3то обстоятельство по3воляет
сделать ва)к-
ньтй вЁтвод о
порядке
реакции
катсд'{ого вь]деления
водорода;
действи-
тельно,
уравнение
(150)
мо>кет
бь:ть
переписано
в виде
|Р
!:Ё[А-1е_*3,
(151)
откуда
вь1текает'
что при
постоянном
потенциале электрода
скорость
реакции
(плотность
тока)
прямо
пропорциональна концентра
ции
водород-
нь!х ионов в
растворе,
1. €.' что
реакция
разряда
водороднь|х
ионов
является
реакцией
первого порядка.
ЁетруАно видеть'
что закономерность
(143)
соответствует
порядку
реакции, равному
половине;
даль1|]е
будет,
однако,
показано' что
та-
кой
дробный
порядок
реакции
является ли1пь ка)кущимся
и что и в этом
случае
реакция
такх(е
является
реакшией
первого порядка.
.
в
щелочнь|х
растворах
с
постоянной концентрашцей
электролита
перенапря)кение
на
ртутном
электроде
умень1'пается
лри6лизительно на
5&
мв
при
увеличении
рЁ
на единицу;
равновесньтй
потенциал при
этом
сдвигается
на
такую х(е величину в отрицательную сторону. Фтсюда вы-
текает' что
в
щелочнь|х
растворах
при
постоянной
плотности
тока потен-
циал
электрода остается
постояннь1м и
от
рЁ
не
зависит
Р:сопз1
_2$т"
с.
Б
этом
случае концентрация водороднь1х ионов
не влияет на скорость
вь1деления водорода' и
реакция
имеет нулевой
поРядок
по
отно]пени}о
к
водороднь]м
ионам.
||/равнение
(150),
вьтра)кающее
зависимость
катодного потенциала
от
концентрации ионов водорода при
постоянной
общей
концентрации
электролита,
по3воляет
нам вь|вести
уравнение
концентрационной поля-
р||зации
при
вь|делении водорода |13
растворов
кислот' содер)кащих и3-
бь:ток индиферентной
соли.
(онцентрационная
поляризация вь|3вана
умень11]ением
концентрации ионов водорода вблизи
поверхности
элек_
трода при прохо)кдении
тока. €огласно
уравненито
(56)
концентрация
у
поверхности
*
[Ё*]'
свя3ана с
объемной
концентрацией
ионов водо-
рода
[Ё-]0'
плотностьто тока ! и
предельной плотностью тока
|6
€оотно-
1пением
(153)
'|1одставляя
(153)
в
уравнение
(150),
в
которое при
концентрацион-
ной поляризации'
естественно, входит значение
концентрации ионов
Р*
у
поверхности,
а
не
в
объеме'
получаем
*
|(онцентрацию
ионов
у
поверхности
[н']",
измененную благодаря прохождению
тока' как
у>ке
было
указано
в
$
1
главы |, не следует сме1пивать
с
концентрацией
ионоь
водорода'
адсорбированных
в
двойном
слое'
которую
мы
булем
обознанать
[!1'|".
\42
(152)
[Ё-]': |н-].(1_;)
9
:
соп51
++'"
*#
+'$
\,'';' .
(154)
|{оскольку
предельная
плотность
тока
!6
пропорциональна
объемной
концентрации
Ё*,
отно1пение
ч+
является
вели.тиной
постоянной,
1а
и
уравцение
(15{)
принимает вид
9:соп51
+'#м'#
(155)
.
}равнение
(155)
формально
напоминает
уравнение
концентрационной
лоляри3ации
лри
вь1делении
металла
с
обра_зованием
амальгамь|
(урав-
:ф
.&
?!;р
-р
,'
-'$
}'
'.,.'
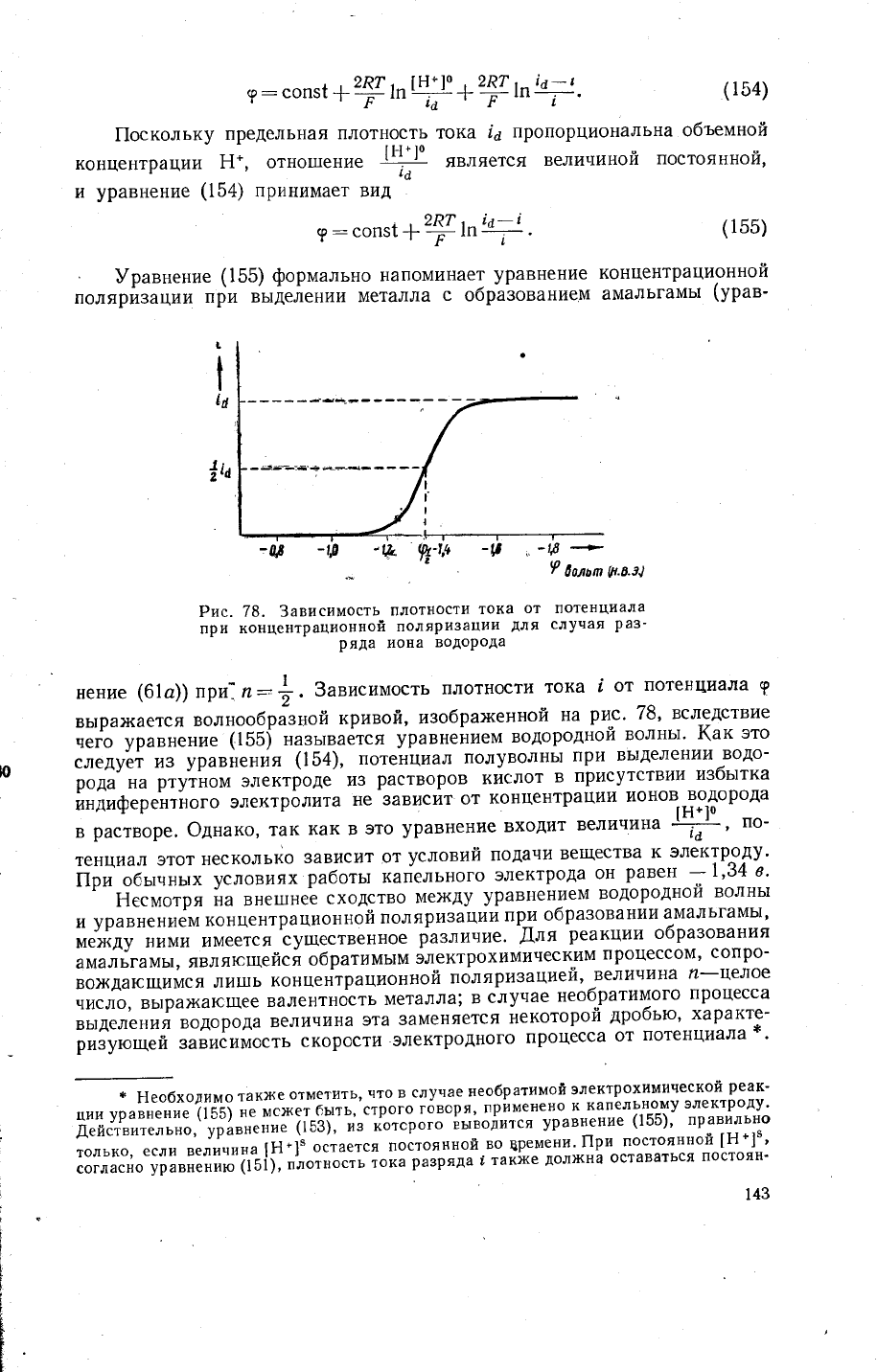
Рис.
78. 3ависимость
плотности
тока
от потенциала
при
концентра:{ионной
поляризации
для
случая
раз-
ряда
|1она
водорода
нение
(61с))
лри п:
|.
3',"симость
плотности
тока
|
от
потенциала
9
вь1рах{ается
волнообрйной
кривой,
изобра>кенной
на
рис'
78'
вследствие
;;;;'й;;;ъ"""'
(1
8ь!
"'',"'""""
уравнением
водородной
волнь1.
1(ак
это
следует
из
уравненйя
(|54), потенциал
полуволнь1
при
выделении
водо-
рода
на
ртутном
электроде
из
растворов
кислот
в
присутствии
из6ьттка
йндиферентного
электролита
не
зависит
от
концентрации
ионов
водорода
в
растворе.
Фднако,
так
как в
это
уравнение
входит
величина
щ:ц
'
по-
тенциал
этот
нескол,*о
за"исит
от
условий
подачи
вещества
к
электроду.
|1ри
обьтнн,'*
у.'',й"х
работьт
к'Ёе',"о''
электрода
',
РР^"].;':!1'::
'
Ёесмотря
на вне:шнее
сходство
ме}кду
уравнением
водороднои
волнь1
и
ура
внен11ем
концентра
т{ионной
пол яриза ции
п
р:а
образ
овании
амальгамь|'
ме}кду
ними
имеется
существенное
ра3личие'
.[ля
реакшии
образования
амальгамь|,
являющейсй
обратимь|м
электРохимическим
процессом'
сопро-
во}{даю
щимс
я л и1шь
концентрацион1]ои
пол
я
ризацие
й,
тел
инина'?-целое
число,
вь!рах{ающее
валентность
металла;
в
случае
|"_чтт''ого
процесса
вь]деления
водорода
величина
эта
3аменяется
йекоторой дробью,
характе-
ризующей
3ависимость
скорости
электродцого
процесса
от
потенциала*'
!
!4
*
Ёеобходимо
также
отметить'
что в
случае
необратимой
электрохиминеской
реак-
ш""
ур'""."1"
(;ьь:
не
мсжет
быть,
строго
говоря,
прйменено
1|3_1т.'^',,'"у
электроду'
.0,ействительно,
уравнеййе
(153),
йз
которого
!ь'водитс"
уравнение
(155),
правильно
только,
если величина
[н']'остается
постоянной
во
цремени'|!ри^лостоянной
[[{*]$'
;;;;;ъ;"';;;"!!!йй
(:ь]),
,}'""'.",
тока
разряда
!
так:ке
дол)кна
оставаться
постоян'
143
14меется
ряд
веществ,
добавление
которь1х
в
раствор
существенно
ме-
няет
величину
перенапряжения водорода' хотя сами эти
вещества
не при-
нимают непосредственного
участия
в
электродной
реакции.
Ёаиболее
прост
и очевиден слунай,
когда
введение
добавки
изменяет
состав и.гли
свойства поверхности металлического электрода. Рсли
взять,'
например' свинцовьтй электрод
и
лри6авить
в
электролит некоторое коли-
чество
хлорной
платинь1,
то
платина
оса)кдается на
свинце;
после
этого
вь]деление
водорода булет происходить
преимущественно
на
кристалли-
тах вь{сах(енной
платинь1 и' следовательно' перенапря>кение
на таком
электроде
значительно
снизится.
Ао6авки
органических
кислот и спиртов могут привести
к
оченЁ
3аметному
повь11пению перенапря)кения'
достигающему
0,|-0,2
в, что
отвечает
умень1пению
скорости вь1деления
водорода
(при
постоянном
пе-
в],.'
\';}
ной.
}1ех<ду
тем'
как это бьтло
показано
в главе 11,
плотность
тока
диффузии
к
поверх'
ности
капли
убь:вает
пропорционально
'-'72,
где
'_время'
протек1шее
с момента
начала
ее
роста.
1аким образом,
условие
постоянства
концентрации
н'
у
поверхности
капли
не
может
бьпть
вьлполнено в случае
необратимого
электродного
процесса,
если
рост
капли
происходит
пРи
постоянном потенциале'
в то
время
как
оно автоматически
вь|полняет-
ся' если поляризация имеет чисто концентрационный
характер.
}1ожно'
однако' пока'
зать'
что оптйбка,
которая получается
при применении
уравнения
(155)
к процессу
выделения
водорода
на
капельном электроде,
не
очень велика, если под
, и
'/
понимать
усредненные
значения плотностей тока
й
предедьного тока
[28].
144
ц9
0,8
0,7
0,6
0,5
|у[
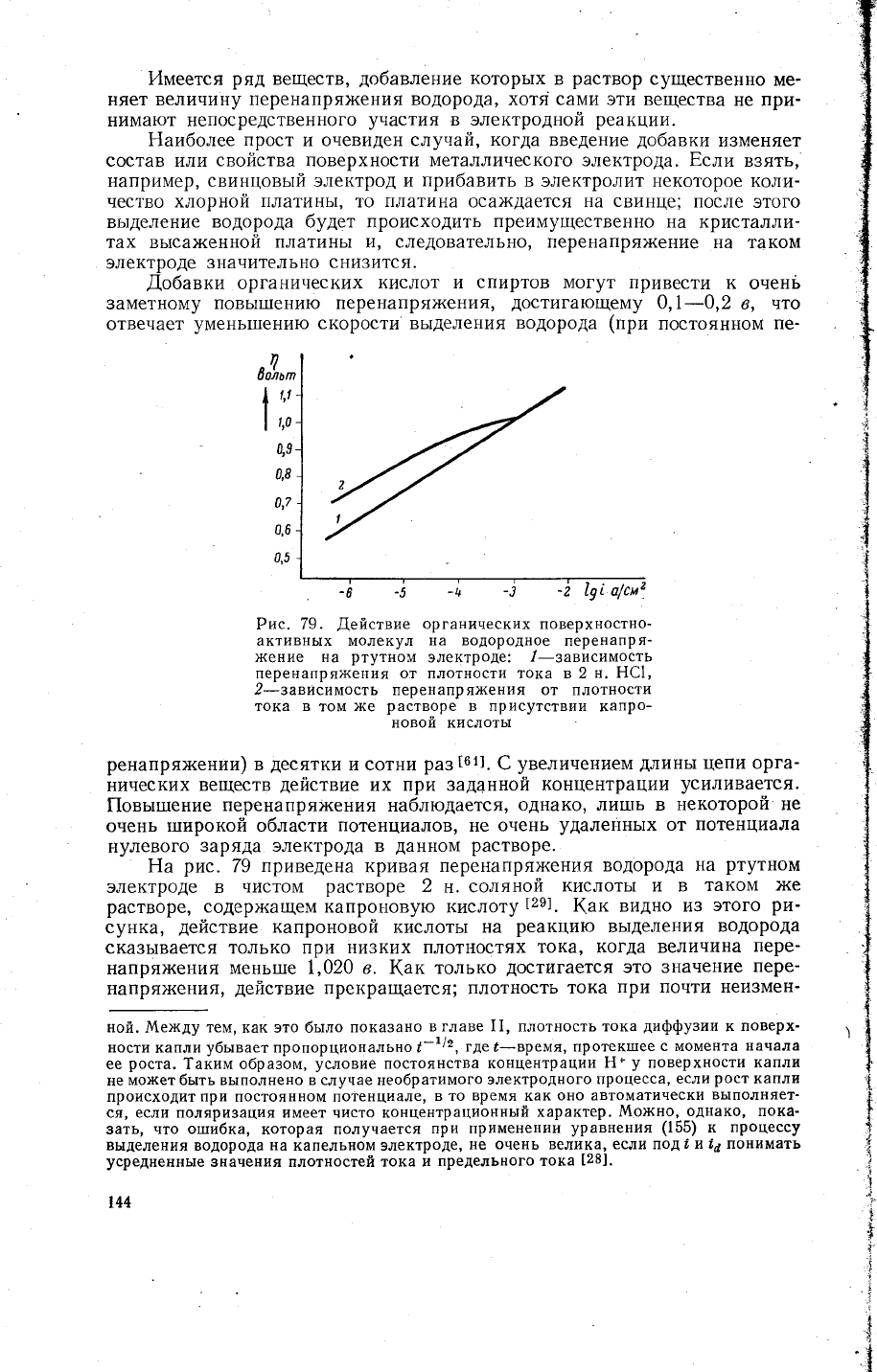
Рис. 79.
Аействие
органических поверхностно-
активных молекул
на водородное
перенапря-
)кение на
ртутном
электроде:
/-зависимость
перенапря)кения
от плотности тока в 2
н. Ё61'
2-зависимость
перенапРя)кения от плотности
тока в
том
)ке
,"ъ";?,;'&;усутствии
капро-
ренапря)кении)
в
десятки
и сотни
раз
|61].
€
увелинением
длинь]
цепи
орга-
нических
веществ
действие
их
при заданной
концентрации
усиливается'
|1овьтш:ение
перенапрях<ения
наблюдается'
однако'
ли1пь в
некоторой не
очень
тширокой
области
потенциалов'
не очень
удаленнь1х
от
потенциала
нулевого
заряда электрода в
данном
растворе.
Ёа
рис.
79
приведена
кривая
перенапря)кения
водорода
на
ртутном
электроде в
чистом
растворе
2
н.
еоляной
кислоть1 и в
таком
>ке
растворе,
содерх{ащем капроновую кислоту
|29].
как
видно
из
этого
ри-
сунка'
действие
капроновой
кислотьт
на
реакцию
вь]деления
водорода
сказь]вается только при
ни3ких
плотностях
тока' когда величина
пере-
!{апря)кения
мень1пе |'020 в.
(ак
только
достигается
это значение
пере-
напря}{ения,
действие
прекращается; плотность
тока
при почти неизмен_
*
'{
,{
'|
{
:
*
,$
{
.о
ном перенапря'(ении повь-][|]ается
до
3начения'
характерного
для
чистого
раствора
соляной
кислоть|.
|[ри больтпих
значениях
'плотности
тока
кри_
вые
перенапрях(ения
для
чистого
раствора
соляной
кислоть1
|1
для
рас-
твора'
содер}кащего
капроновую
кислоту'
полность}о
совпадатот.
8стественно
связать прекращение
действия
капроновой
кислоть1
на
реакци1о^вь!деления
водорода
при
потенциалах
более отрицательнь]х'
чем
-1,00
6*, с
десорбшией
молекул
кислоть1
с поверхности
электрода.
Ё{а это
ука3ь1вают
даннь|е
электрокапиллярнь|х
измерёний
в этих
раство-
рах
и измерений емкости
двойного
слоя'
и3
которь|х
следует'
что
капро_
новая
.кислота
адсорбируется
на
поверхности
ртутного
электрода
в об_
-4
1!
!.
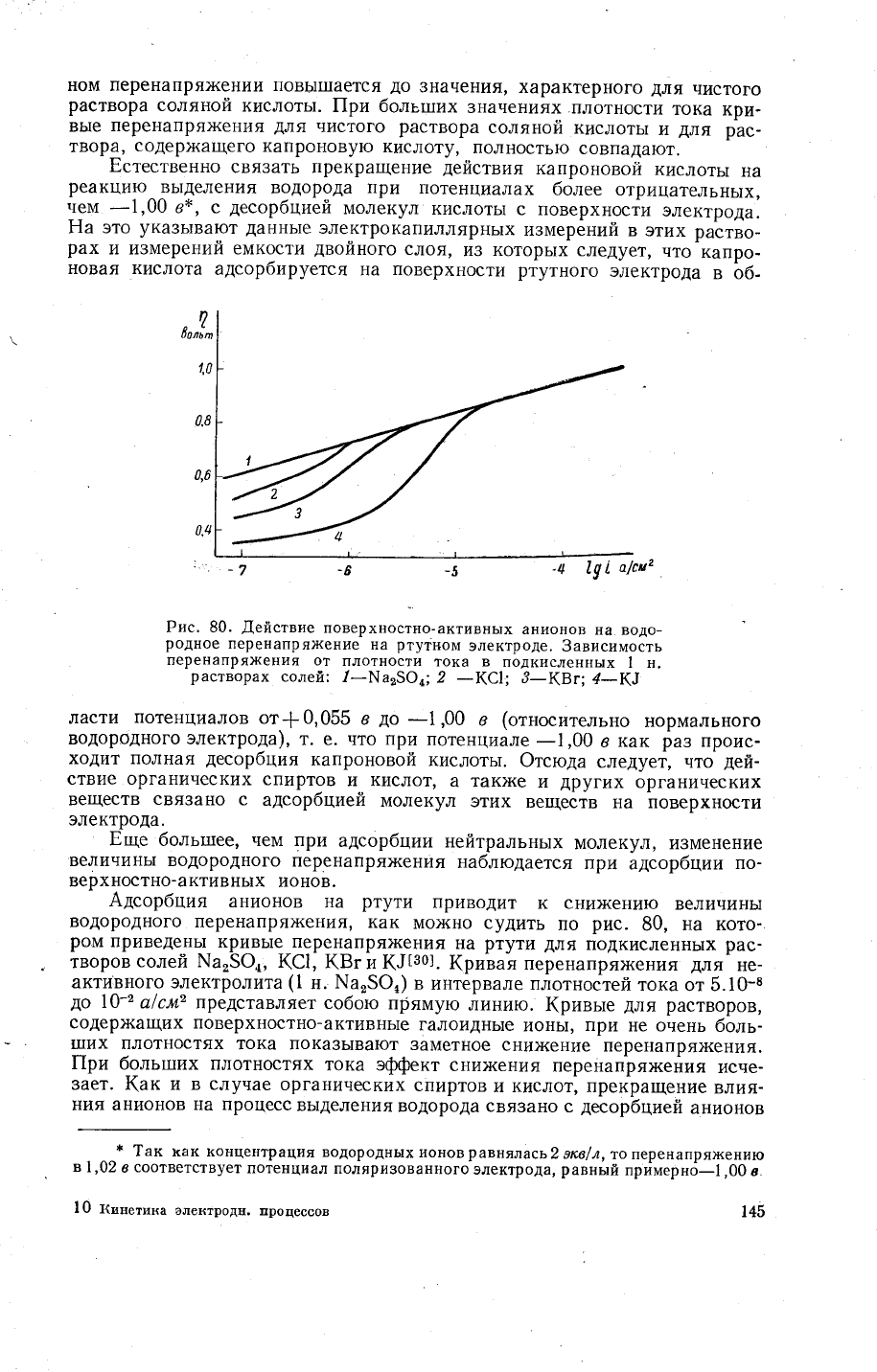
Рис. 80.
[ействие
поверхностно-активнь|х
анионов
на
водо_
родное
перенапря)кение
на
ртутном
электроде.
3ависимость
перенапряжения
от
плотности
тока в
подкисленных
1 н.
растворах
солей:
.[_!.,]а230,;2
-(€|;
3-(Бг;
4_(]
ласти
потенциалов
от.{0,055
в
до
-1
,00
в
(относительно
нормального
водородного электрода),
т.
".
что
при
потенциале
_1,00
в
как
раз
проис_
ходит полная
десорбция
капроновой
кислотьт.
Фтсюда
следует, что
дей-
ствие органических
спиртов
и
кислот'
а так)ке
и
других
органических
веществ
связано
с
адсорбцией
молекул
этих
веществ
на поверхности
электрода.
Бще
больплее, чем при
адсорбции
нейтральньтх
молекул' и3менение
величинь! водородного
перенапряжения
наблюдается
лр|1
адсорбции
по-
верхностно-активнь|х
ионов.
Адсорбция
анионов
на
ртути
приводит
к сни}кению
величины
водородного перенапря)кения'
как
мо'{но судить
по
рис.
30,
на кото_
ром
приведе1ь_1-
кРщь19-ц9р9]'зпря'ц-9ния
на
ртути
для
подкисленнь1х
рас_
творов
солей \а'5Ф.,
(€1,
1(Бг
и
к.}!30].
(ривая
перенапря)кения
для
не-
активного электролита
(1
н.
!х{а'5Ф')
в
интервале плотностейтока
от 5.10-в
до
10-2
а|см2 представляет
собою
прямую
линию.
1(ривьте
для
растворов'
содер>кащих поверхностно_активнь1е
галоиднь]е
ионь1'
при
не очень
боль-
1пих плотностях
тока показь|вают
заметное
сни'{ение
перенапрях{ения.
|[ри
б-ольтпих плотностях
тока эффект
сних{ения
перенапря)кения
исче-
зает.
(ак
и в случае
органических
спиртов
и кислот' прекращение
влия-
ния анионов
на процесс
вь]деления
водорода свя3ано
с
десорбцией
анионов
*
1ак как концентрация
водородных
ионов
равнялась
2 экв/л,
то перенапря)кению
в
\,02
в
соответствует
потенциал
поляризованного
9лектрода,
равный
прймерн6-1
,00
о.
.2
6о льп
1,0
10
кинетика
але1{тродт|.
процеосов
145
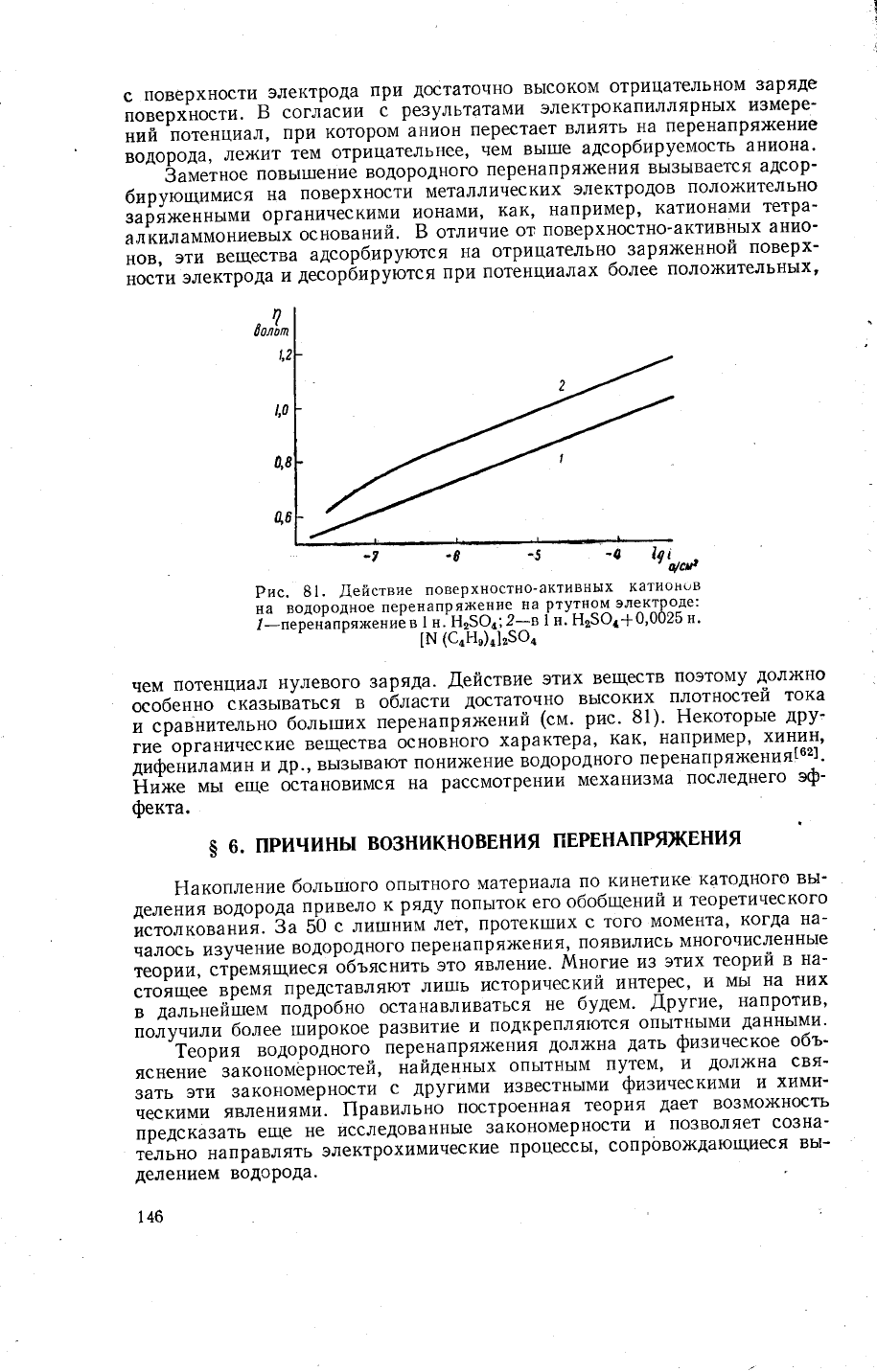
!
1
|
!
с
поверхности
электрода
при
достаточно
вь1соком
отрицатель11ом
3аряде
й'Б"р*'*'.'и.
Б
согласии
ё
результатами
электрокапиллярнь|х
измере-
ний'потенциал,
при
котором
анион
перестает
влиять
на
перенапрях<ение
водорода'
ле)кит
тем
отрицательнее'
чём
в,тп:е
адсорбируемость
аниона'
''
3айет,ое
повьттление
водородного
перенапря}кения
вь]зь!вается
адсор-
6ирующимися
на
поверх}1ости
металлических
электродов
полох{ительно
за!й>кеннь'ми
органическими
ионами'
как'
например,
катионами
тетра-
алкиламмониевых
оснований.
Б отличие
от
поверхностно-активнь1х
анио_
нов,
эти
вещества
а!сороирутотся
ца
отрицательно
зарях(енной
поверх_
ности
электрода
и
десор6ируются
при
потенциалах
более
поло)кительнь|х'
Рис.
81.
Аействие
поверхностно_активных
катион!
на
водородное
перенапряжение
на
ртутном
электроде:
:_,.р.й"'й|!й.ййё
й
й]н"з,3;;,:':
[ н'
н,5о.+0'0025
н'
чем
потенциал
нулевого
3аряда.
.[1ействие
этих
веществ
поэтому
дол)кно
особенно
ска3ь1ваться
в
о6ласти
достаточно
вь1соких
плотностей
тока
;;;;;й..;';;'
б'','"'
перенапря)кений
(см.
рис.
31).
Ёекоторьте
дру-
гие
органические
вещества
основного
характера'
как'
напри}!Р:^-}.]].?#'
1йф","','ин
и
др.'
вь1.ь1вают
поних{ение
водородного
перенапрях{ения|"','
Ё{и>ке
мь1
еще
остановимся
на
рассмотрений
механизма
последнего
эф-
фекта.
$
6.
пРичинь!
во3никноввния
пвРвнАпРяжвния
Ёакопление
больш:ого
опь|тного
материала
по-кинет.ике
катодного
вы_
деления
водорода
привело
к
ряду
попь]ток
его
обобщений
и
теоретического
}ЁБ''*'".Ё"А.
ё'
50
с литпним
лет,
протек1пих
с
того
момента,
когда
на-
чалосьи3учениеводородногоперенапря)кения'появилисьмногочисленнь1е
теории,
стремящие."
Бб'"с"ить
это
явление.
}1ногие
и3
этих
теорий
в
на-
стоящее
время
представля1от
ли|пь
исторический
интерес'
и
мь|
на
них
в
дальнейтпем
подробно
останавливат,ся
не
буАем'
[ругие'
напротив'
",1у"","
более',йр'.'е
развитие
и
подкрепля'о-г:
я-
:]'_ь11нь1ми
да
ннь1ми'
1еория
водородного
перенапрях<е,ий дол)кна
дать
физинеское
объ-
яснение
3акономерностей,
найденньтх
опь1тнь1м
путем'
и
дол}кна
свя-
3ать
эти
закономерности
с
другими
известнь!ми
физинескими
и
х|1ми'
ческими
"'ле*'"*й.
|1равильйо
построенная
теория
дает
возмох{ность
йЁ"д"*а"''ь
еще
не
исёледованнь1е
закономерности
и
позволяет
созна-
тельно
направлять
электрохимические
процессь1'
сопровох(дающиеся
вь]-
делением
водорода.
146

3лектродная
реакция
при
ра3ряде
водороднь1х
ионов протекает
в
две
последовательнь]е
стадии'
которь1е
могут
бь:ть представлень]
следующим
образом
*:
2н-
+
эе
\ун3 н'.
Бследствие
нал\4чия
отталкивательнь|х
сил мех(ду
одноименно
3аря)кен-
нь1ми
частицами'
на одном
и том х{е
участке
поверхности
электрода
одно-
временно
не
могут
разрях{аться
два
иона
водорода;
поэтому при
вь!де-
лении
водорода первично
образуются
атомь1'
а
не
молекуль|
водорода.
||олунающиеся
в
пРоцессе
разряда
атомь|
в
дальнейтпем
путем
вторйяной
химической
реакции
превращаются
в
молекулярньтй
водород. 1олько
пер-
вая
из
этих
двух
стадий
является
собственно
электрохиминеской,
т. е,
свя3ана
с
изменением
заряда
реагирующих
частиц. Бторая
стадия пред-
ставляет
собой
обь;нную
химическую
реакцию'
протека!ощую
на поверх-
ности
электрода.
Баиболее
распространеннь1е
теории
водородного
перенапря>ке[1ия
можно
объединитц
в
две
группь] в
3ависимости
от того' с
какой_
из
этих
двух
стадий
они связь|вают
причину
во3никновения
перенапрях{ения.
Рассмотрим
равновеснь]е
состояния
мех<ду
ионами и атомами
и мех(ду
атомами
и
молекулами
водорода
велит{инь]
|1
и !1, определяющие
для
первой
стад||и
(токи
разряда
скорость
катодной
и анодной
реакций
и
ион|1зации)
и аналогичнь]е
величинь!
(А)
(А')
(А')
нару1пается;
на
направо. Бведем
атомов
н
на поверхности
при
этом
услови|1
плотность
токов
катодной
и анодной
стади|4|
2н-
+
2е!2|1,
2н
=
н?.
3ти
равновесия
носят
динамический
характер
и связань1
с протека-
нием процессов
обмена.
Фбозначим
величинь1 скоростей
обмена
для
_первой
и
для
второй
стаАии
(в
электринеских
единицах)
нерез
!! и |!.
Белининь:
эти
играют
для
ках{дой
стадпи
в отдельности
ту
роль'
которую
величина
тока
обмена
|0, определенная
в
предь1дущей
глайе,
играет
для
процесса
в
целом.
||ри прохо)кдении
тока чере3
электрод
равновесие
катоде'
например'
реакции
(А')
и
(А,,)
протекают
слева
1,
и
12
для
второй стади|1
(токи
рекомбинации
и
диссоциашии).
|1о опре-
делению
при
равновесии
.
; .{!
11----
'\-
|7
3
стационарном
состоянии
количество
электрода
сохраняет постоя|]ное
значе]{ие;
вне11]него
тока
равна
ра3нос-ти
плотностей
реакции
как
для
первой,
так
и
для
второй
(156)
считая поло)кительнь1м
катодное
направление
тока
во внетшней
цепи
(см.
примечание
на стр.
137)'
(инетические
3акономерности
реакции
определяются
соотно1шением
ме)кду
величинами
!, !!
и |!.
|{усть,
например'
ток обмена
второй
стадш\4
нам}1ого
превь]1]]ает
ток обмена первой
и
пусть
плотность
вне1пнего
тока
обладает проме}куточнь1м
значением
(!!
<
,
<
!|).1ак как плотность
вне1ш_
!0* 1
'т:

него
тока мала
по
сравнению с !!,
то
равновесие
второй
стадии 3аметно
+*-
пе
нару1шится;
токи
!, и
!,
попрежнему
почти компенсируются.
в про-
тивополох{ность
этом!
для
первой стадии
|
".',''"'",
значительно
больш:иш:
!!, а7'
умень1пается'
что
приводит к
резкому
наруш1ени}о
рав-
новесия.
|!ри
достаточном
различии
мех{ду скоростями
обмена
пер-
вой
и второй
стаА:гг*1
в
11]ироком
вь11пеука3анном интервале
плотностей
+
тока
величиной
|, мо>кно
будет
пренебрень ло сравнению с |',
т. е.
скорость
всего
процесса определится |''
и
первая стад|1я
сделается
не-
обратимой,
в
то время
как
вторую
стадию
мох(но
попре}кнему
рассма-
тривать
как
равновесную.
Баоборот,
если !9
намного мегтьтпе !!, а
| имеет
промех{уточное
значение'
то скорость
общей
'реакции
опреде-
ляется
величиной !',
и вторая
стад|1я
сделается
необратимой,
в то вре_
мя
как
для
первой сохранятся
условия'
6лизкие
к
равновеснь|м.
Б
общем
случае
мо)кно
ска3ать' что скорость
всей
реакции
определяется
кинетическими
3акономерностями
той из ее
промех{уточных
стадий,
кото'
рая
обладает
самь1м
маль1м
током
обмена и
которую
мъ] в
дальнейтпем
условно
назовем
самой медленной
стадией
реакции
*.
|1ри
достаточном
разл||ч|\ут
токов
обмена
остальнь1е стадии
(бьтстрьте
стадии) мо)кно
попрех(-
нему
рассматривать
как
равновеснь1е.
Бозникновение
перенапрях{ения при
катодном вьтделении
водорода
является
при3наком
нару1пения
равновесия
и мо>кет
быть
связано с 3амед_
ленностью
одной
из стадий процесса.
3
историнеской
последовательности
первь1ми
бьтли
развить1
теории'
сводящие
причиньт
пере11апря)кения
к
замедленности
второй-химической
стадп|4.
3ти
представления
в
той
или
иной
форме
сохранились
до
настоящего
времени
и
удовлетворите.,1ьно
объясняют
часть
опь1тнь]х
даннь1х.
|[редполох<ение
о том' что
прининой
поляризации электрода
является
кинетическая
задерх(ка
первой_электрохимической
стадии,
долгое
время
относительно
мало
использовалось.
Б
последние
годьт, благодаря
ра6о-
там советских
электрохимиков' эти
пр.едставления
6ьули в значительной
степени
переработань| и
усовер1пенствовань1
и
получили прочное
экспери-
ментальное
обоснование.
3тп группь1
теорий мь|
рассмотрим
в их
исторической
последователь_
ности' т. е. сначала
теории' связаннь1е
с представлением
о
3амедленности
процесса
удаления
адсорбированного
атомарного
водорода'
а затем
теории'
связаннь]е с
представлением о замедленности
процесса
разряда.
$
7. РвкомБинАционнь|в
твоРии водоРодного
пвРвнАпРяжЁния
1еории, в
которь1х возникновение
перенапря)кения
свя3ь]вается
с
на_
коплением
избьтточного
по сравнению
с
равновеснь1м
количества адсор-
бированного
атомарного
водорода
на поверхности
электрода'
происходя-_
щего
вследствие
медленности
его
удаления'
мь] булем
назь1вать
десорб-
ционнь|ми.
Бсли
в
этих
теориях к тому
)ке
предполагается'
как это изло-
}1{ено вь11ше'
что
процесс
удалени
я п
роисходит
благодаря
соеди
нению атомов
водорода
в
мол9куль1'
то
такиетеории
мьт
будем
назь]вать
реком6инашион_
ньтмй
(иногда
говорят такх{е
о
(каталитическом
механизме>
удаления).
*
Б
самом
деле'
при протекании
реак!|{и
в
последовательных
стадий,
устанавливающиеся
в
148
одну сторону
скорости
всех отдельньп
стационарных
условиях'
оди}{аковы'

||ри
катодном вь]делении
водорода
на
поверхности электрода
уста-
навливается
некоторая
стационарная концентрация
адсорбированнь1х
атомов'
3ависящая
от соотно1пения
скоростей их образования и
удаления
с
поверхности.
€огласно основному
допущени1о десорбционных
теорий,
разряд
ионов
водорода и ионизация адсорбированных
атомов
происхо'
дят
свободно
и
с
достаточной
скоростью;
при
любь;х 3начениях
плотности
вне1шнего
поляри3ующего тока мо'{но
с
достаточным
приблих<ением
счи-
тать,
что
равновесие
ме'(ду ионами и
адсорбированными
атомами
не
нару!шается,
(тадия
ра3ряда
поэтому
не
долх(на
ска3ываться
на общей
кинетике
реакции.
Аальнейц:ее
превращение атомов водорода в молекулы
протекает
уже
не свободно'
а с
некоторой
ограниченной скоростью' зависящей
от
по'
верхностной
концентрации адсорбированпого водорода. ||ри
прохо>кде-
нии тока
поверхностная концентрация
водорода
принимает такое 3наче'
ние'
при котором
скорость
удаления
атомов
становится
равной
ско-
рости
их.
образования, т. е. соответствует
плотности поляризующего
тока"
9ем
боль:::е
плотность катодного тока' тем боль|пе стационарная
поверх-
ностная
концёнтрация
атомов водорода.
!1 а
копление
адсорбирова
нного
водорода
в кол ичествах'
-превь1]'цающих
равновесную
концентрацию' сдвигает
потенциал электрода в отрицате.]1ь-
ную сторону. 1акая
картина несколько
напоминает явление
концентра-
ционной
поляри3ации' где прохо'{дение тока так}ке и3меняет
стационар_
ную концентрацию
потенциал-определяющего
вещества
в6лизи
поверх-
ности
электрода
и вследствие
этого сдвигает
электроднь1й
потенциал.
ймеется,
однако' принципиальное
ра3личие
ме)кду этими
двумя
явления_
ми.
Б
рассматриваемом
здесь случае
речь
идет
о
поверхностной коншентра-
ции
атомов водорода'
находящихся
непосредственно па электроде'
причем
эта
концентрация меняется не
вследствие
замедленного
отвода
реагирую-
щего
вещества
с
поверхности
электрода
путем
диффузии
или
миграции'
а вследствие
замедленности одной из
стадий самой электрохимической
реакции.
|!оэтому
применение
термина
<концентрационная
поляри3ация)}
в
данном
случае
нецелесообразно.
Ёаличие из6ьттка адсорбированного
водорода
на
поверхности
неко-
торь1х электродов
при
их
катодной
поляризации мох{ет бьтть
доказано
прямь]м опытнь1м путем.
Аля
этой
цели
мо>*{ет
бьтть,
например, исполь3о-
ва!{о
известное свойство отдельных металлов
(например,
)|(елеза'
лалла-
дия
и
др.)
не
только адсорбировать'
но
и
растворять
атомарный
водород
в
объеме металла.
||ри катодной
поляри3ацп|1
х{елеза
в
кислом
растворе
концентрация
растворенного
водорода' проникающего
в глубь
металла'
достигает
3на-
чений во много
ра3
превы1шающих
концентрацию,
соответствующу1о
рас-
творимости
газообразного
водорода
при
атмосферном
давлении.
3то
следует'
в
частности,
из
того, что при наличии в
металле включений'
катали3ирую_
щих
рекомбинацию
атомов
водорода в молекулы'
давление
выделяющегося
.и3
металла водорода мо)кет
достигнуть
сотен
атмосфр, вы3ь1вая
механи-
ческое'
ра3ду1пение
металла.
9вление
это
указь!вает
на то'
что вследствие
увелинёний
концентрации
адсорбированного
водорода
на
поверхности
металла атомь|
его
начинают
дифундировать
в
ре1!1етку
металла иди
по
мех(кристаллитнь|м
плоскостям*.
*
Аля
появления
растворенного
атомарного водорода в
хеле3е
нет необходимости
поляРи3овать ]|(елезо в||е[шним источ}{иком тока.
Аля
этого
достаточен
тот
отрицатель-
цый потенциал, который
самопрои3вольно
устанавливается
при
действип
кислот
на'
'(еле3о
(см.
главу
!1|1).
Раство!енный
водород:вляется
причиной хорошло
извест:дой
}|з
техники
<водородной
хрупкости> металйа.
|1роникновение
водорода
наблюдается
149
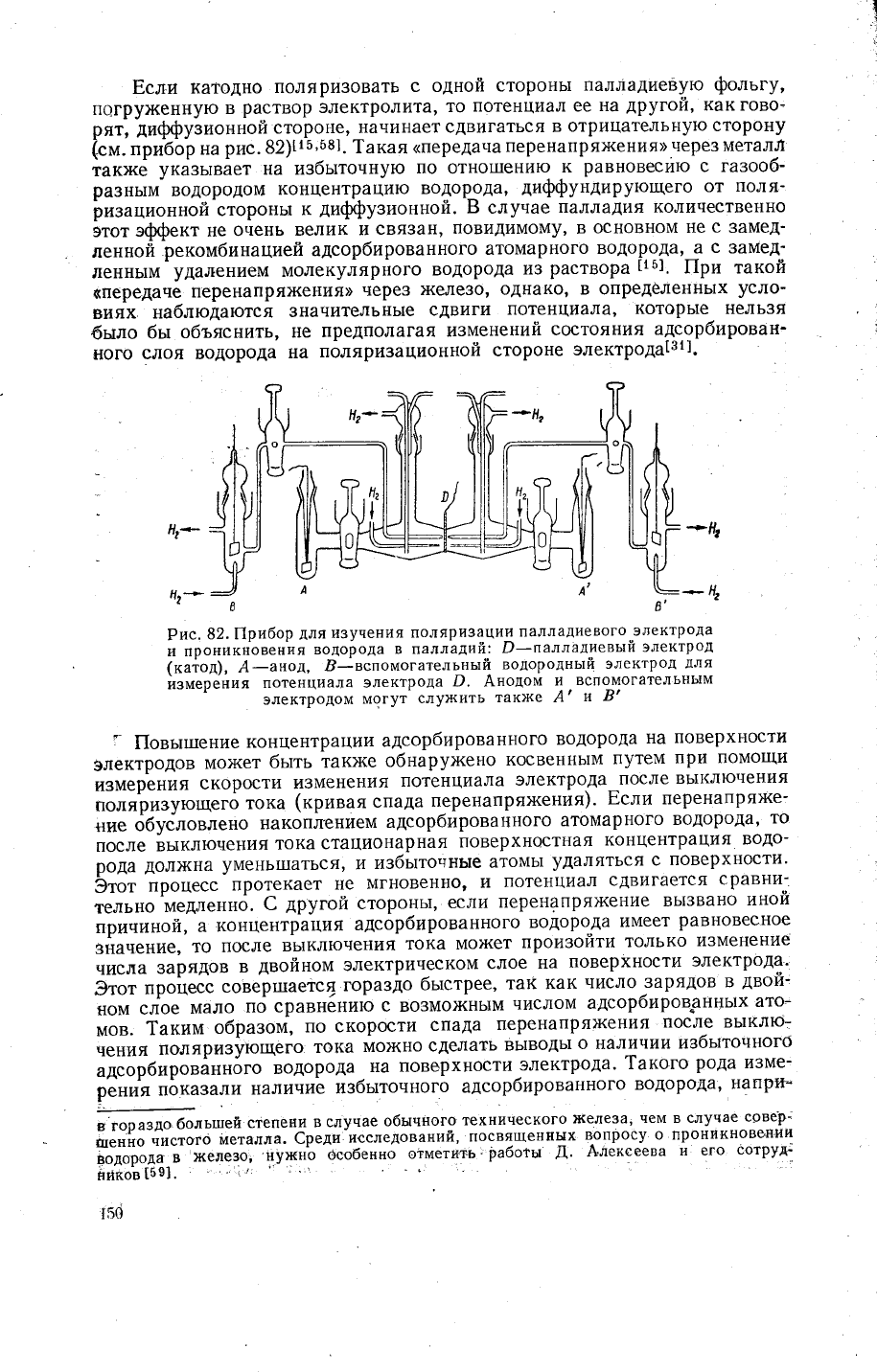
1
,1
]
Бсл-и
катодно
поляризовать
с одной
сторонь1
палладиевую
фольгу,
погру}кенную
в
раствор
электролита'
то
потенциал ее
на
другой,
как гово-
рят,
дифузионной
стороне'
начинает
сдвигаться
в
отрицательнуто
сторону
(см.
прибор
на
рис.
в2)!15'581.
|акая
(передача
перенапря)кения>через
металл
так>!(е
ука3ь1вает
на избьтточную
по
отно1пению
к
равновесйю
с газооб-
разным
водородом
концентрацию
водорода,
диффундирующего
от
поля-
}изационной
-сторонь:
к
дифузионной.
Б случае
т1алладАя количественно
этот эфект
не
очень
велик
и
свя3ан,
повидимому' в
основном
не
с
замед-
ленной
.рекомбинацией
адсорбированного
атомарного
водорода'
а
с
замед_
леннь1м
удалением
молекулярного
водородаиз
раствора
|15].
при такой
(передаче
перенапря)ке!{ия>
через
х(елезо' однако'
в опредёленнь|х
усло-
виях.
наблюдаются
3начительнь!е
сдвиги
потенциала'
которь1е нельзя
было
бьт
объяснить,
не
предполагая
изменений
состояния
адс9рбирован'
!{ого
слоя водорода
на
поляризацио!!ной
стороне
электрода|31!.
8а*
|а*
*!з
..
11а
Рис.
82. ||рибор
для
изуче!{ия
поляризации
палладиевого
электрода
и проникновения
водорода
в палладий'.
Р-палладиевьхй
электрод
(ка{од), А-анод,
3_вспомогательнь:й
водородньтй
электрод
для
йз
мер е
н и я
**;;3;Ё;
;Ё$;'
:#}#й
"';;А?ъ
1,
"
;,
у."
''ел
ьн ь1
м
г
|1овьттпение
концентрации
адсорбированного
водорода
на
поверхности
электродов
мо)кет
бьтть
такх<е
обнарух<ено
косвеннь|м
путем
при
помощи
измерения
скорости
изменения
потенциала
электрода*после
вь[!(лючения
поляри3у1ощего
тока
(кривая
спада
перенапря)кения).
Бсли
перенапря)ке-
,""
6бу"''влено
накоплением
адсорбированного
атомарного
водорода,
то
после
вь1кл1очения
тока
стационарная
поверхностная
концентрация
водо-
рода
дол)кна
умень1патъся,
и
избь:точные
атомь1
удаляться
с
поверхности'
5тот
процесс
протекает
не
мгновенно'
и
потенциал
сдвигает€я
€!авни-.
тельно'медленно.
6
другой
сторонь]'
если
перенапря)кение
вь1звано
инои
причиной,
а
концентрация
адсорбированного
водорода
имеет
равновесное
значение'
то
после
вь1ключения
тока мох{ет
произойти
только
и3менение
числа
зарядов
в
двойном
электрическом
слое
на
поверхности
электрода.
5;;;ъй;{;;ё
"'""р*."тся
гораз,[о
бьтстрее,
так
11-': 11:{:..'р"Аов
в
АвФй.
ном
слое
мало
.по
сравнени}о
с возмох(нь!м
числом
адсорбиров4анць1х
ато-
мов.
1аким
образой
по скорости
ст1ада
перенапряжения
после ББ1(.'1б:
йЁйй"_й''"ризуюшего'
тока
мо}кно
сделать
вь1водь1
о наличии
избь|точного
|й.'ро"р'"Ан"'го
водорода
-
на поворхности
электрода.
такого
рода
изме-
рения
показали
наличиъ
избь1точного
адсорбированного
водорода'
напр1г'
" ''р',л'
больц:ей
степени
в случае
обычного
технического
я<еле3а,
чем в случае
совер;
шенно
чистого
металла.
€реди-исследований,
посвященных
вопросу о проникновелии
;"-;ьъ;';_;-;ъ'.'',
]йуж'Б'6собенно
отметкгь;
ра6о1ы
А.
А.лексеева
и его
сотрул:
йй?'Б[6э;.
150
