Фёршт Э. Структура и механизм действия ферментов
Подождите немного. Документ загружается.

ХИМИЧЕСКИЙ
КАТАЛИЗ
81
в соответствии либо
со
схемой (2.58),
где
лимитирующей
ста-
дией является образование тетраэдрического промежуточного
соединения, либо
со
схемой (2.59),
где
лимитирующей стадией
является разрыв связи.
R—С
О
OR'
R—С
s-
О
•7
\
OR'
ПС
(2.58)
R—С
\
О
OR'
R-/
R—С
s-
О
в-
OR'
(2.59)
ПС
а.
Линейные
зависимости
свободной
энергии,
уравнения
Брёнстеда
и
Гам
мета
Количественно оценить чувствительность реакции
к
измене-
нию электронной плотности атакующего нуклеофила можно
пу-
тем измерения констант скорости второго порядка
для
реакций,
где определенный эфир атакуется рядом нуклеофилов. Анало-
гично
тому,
как это
делалось
для
общего основного катализа,
строят график зависимости логарифма константы скорости
от
рКа нуклеофила. Обычно
в тех
случаях,
когда используются
лишь нуклеофилы сходной химической природы
и
когда диапа-
зон
значений
р/(
а
невелик, получается линейная зависимость.
Наклон
прямой обозначается буквой
р, как и в
случае
общего
основного катализа.
Эти линейные зависимости
между
логарифмом константы
скорости
и рК
а
известны
под
названием
линейных
зависимостей
свободной энергии,
поскольку логарифм константы скорости
пропорционален энергии активации Гиббса
для
данной реакции,
а логарифм константы равновесия
—
изменению энергии Гиббса
реакции
(раньше энергия Гиббса называлась свободной
энер-
гией).
Наличие корреляции
между
нуклеофильностью нуклео-
фила
и его
основностью указывает
на то, что
энергия активации
Гиббса
для
образования связи
с
углеродом карбонильной груп-
пы
пропорциональна энергии Гиббса
для
переноса протона
к
нуклеофилу.
Аналогичная корреляция (соотношение Брёнстеда) суще-
ствует
между
константой скорости
и р/С
а
уходящей группы
в том

82
ГЛАВА
2
случае, когда определенный нуклеофил взаимодействует
с ря-
дом эфиров, имеющих разные уходящие группы. Другой способ
графического представления данных, который используется
для
ароматических соединений, основан
на
применении уравнения
Гаммета
и
констант Гаммета
для
заместителей.
Эти
константы,
характеризующие способность заместителей
в
бензольном коль-
це отдавать
или
принимать электроны, связаны
с рКа
замещен-
ных бензойных кислот следующей эмпирической зависимостью:
(Р^аК
=
(
р/С
а)
0
~
а
Х>
(2.60)
где
X —
заместитель
в
бензойной кислоте
в
мета-
или
пара-
положении,
(рКа)х — это р/Ca
замещенной кислоты,
Таблица
2.5
Константы,
характеризующие различные заместители
а)
Заместитель
—NH
2
—NHj
—NHAc
—ОН
—ОАс
—N(Me)
3
+
-со;
—СО
2
Н
—СОСНз
р
—С1
—Вг
—I
—NO
2
—CN
—СНз
—ОСНз
Алифатическое
соединение ")
°1
0,10
0,60
0,28
0,25
0,39
0,73
—0,17
0,34
0,29
0,52
0,47
0,45
0,39
0,63
0,58
—0,05
0,25
°т
—0,16
0,63
0,21
0,121
0,39
0,88
-0,10
0,37
0,38
0,337
0,373
0,391
0,352
0,710
0,56
—0,069
0,115
Ароматическое
соединение
в
'
°Р
—0,66 (-0.17)
г)
0,00
-0,37 (—0,11)
г)
0,31
0,82
0,00
0,45
0,50 (0,87)
д)
0,062
0,227
0,232
0,18
0,778
(1,24)
А)
0,66
(0,90)
д)
-0,17
-0,268 (-0,11)
г)
а
> Из Charton M., J. org. Chem., 29, 1222 (1964); Ritchie С. О.,
Sager
W. F.,
Progress
in
Physical
Organic Chemistry, 2, 323 (1964).
б
> Рассчитано из уравнения (о,) х=[(РКа)СНзСО
2
Н-(РКа)Х-СН
2
СО
2
н]/з,95.
в
> Рассчитано из уравнения o=(pK
a
)phCO
2
H-(P^a)x-PhCO
2
H.
г
) Для соединений, отличных от бензойной кислоты и карбонильных соединений.
д
) Для фенолов, анилинов и тиофеиолов.

ХИМИЧЕСКИЙ
КАТАЛИЗ 83
(рК
а
)о
— рКа незамещенной кислоты, ох — константа, характе-
ризующая заместитель X (разная для заместителей в
пара-
и
жега-положениях). Обнаружено, что уравнение Гаммета выпол-
няется и для реакций с
участием
производных бензойной кисло-
ты (при определении скорости гидролиза эфиров бензойной
кислоты, а также при изучении равновесий
других
реакций, в
которых
участвует
соединение с бензольным кольцом, например
при
ионизации фенолов), но, оценивая чувствительность реакции
к
изменению а, используют коэффициент пропорциональности р,
постоянный
для данной реакции. Например, при ионизации фе-
нолов
=
(Р*а)
0
-Р
СТ
Х.
(2.61)
где р = 2,1. Для щелочного гидролиза фенилацетатов
T
x-
(2.62)
где р = 0,8.
Соотношения Брёнстеда и Гаммета эквивалентны. Например,
согласно уравнению Гаммета, для щелочного гидролиза фенил-
ацетатов логарифм константы скорости, как и р/С
а
исходных
фенолов, пропорционален а. Следовательно, логарифмы кон-
стант скорости гидролиза пропорциональны р/Са, что непосред-
ственно
следует
из графика Брёнстеда для зависимости лога-
рифма константы скорости от р/Са.
Соотношения Брёнстеда и Гаммета выполняются также в
случае
атаки определенным нуклеофилом эфира с конкретной
уходящей
группой, в которой варьируется ацильный фрагмент.
б. Смысл коэффициента р в уравнении Брёнстеда
Важным параметром, который можно определить из графи-
ков
Брёнстеда, является коэффициент р.
Знак
и величина этого
коэффициента
указывает на знак и величину заряда переходно-
го состояния. Рассмотрим, например, атаку эфиров нуклеофила-
ми.
Для констант равновесия при переносе ацильных групп
между
оксианионами, а также третичными аминами р равно
1,6—1,7.
Эта величина больше 1,0, поскольку ацетильная группа
сильнее оттягивает электроны, чем протон (для которого р =
=
1,0 по определению), и более чувствительна к изменению р/С
а
спирта или амина. Установлено, что для атаки третичными ами-
нами
эфиров, образованных сильно основными спиртами, значе-
ние
р при замене нуклеофила составляет
i+l,5,
а при замене
спирта —1,5 [43]. Это показывает, что переходное состояние
реакции по своей
структуре
очень близко к продуктам, т. е.
84
ГЛАВА2
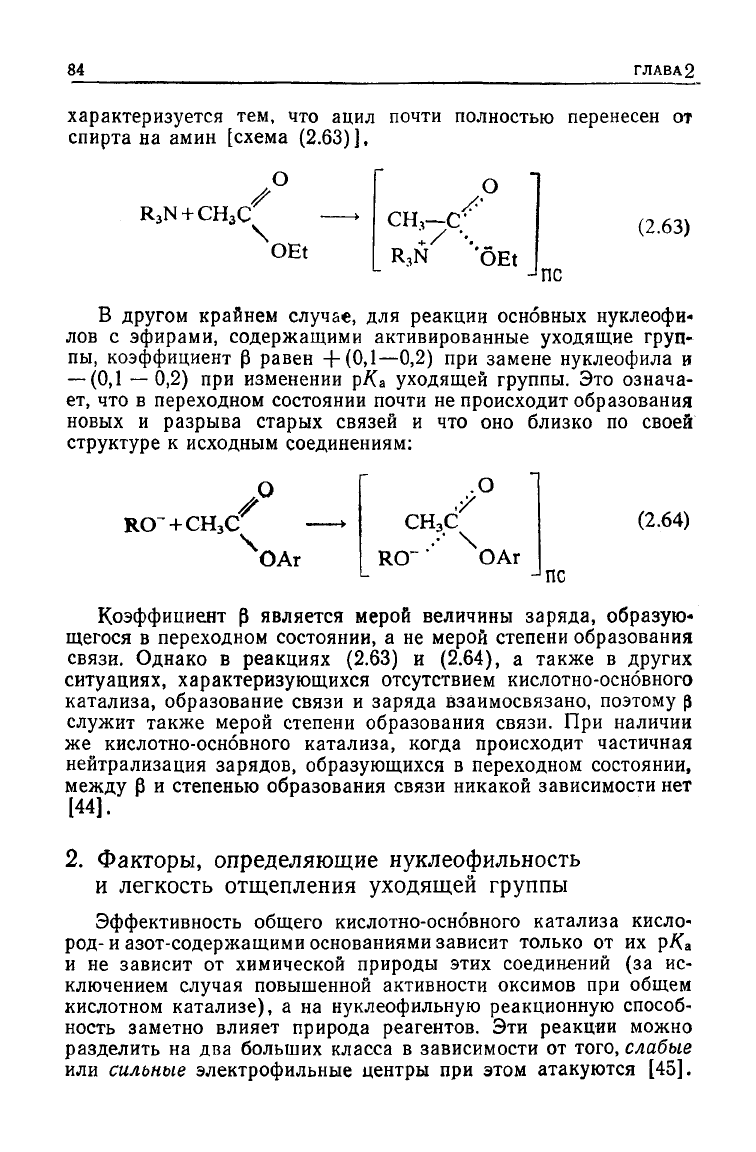
характеризуется
тем, что
ацил почти полностью перенесен
от
спирта
на
амин [схема (2.63)],
у
О
OEt
О
сн.,—cf
'OEt
(2.63)
ПС
В
другом
крайнем случае,
для
реакции основных нуклеофи-
лов
с
эфирами, содержащими активированные уходящие груп-
пы,
коэффициент
р
равен +(0,1—0,2)
при
замене нуклеофила
и
— (0,1
—0,2) при
изменении
р/Са
уходящей группы.
Это
означа-
ет,
что в
переходном состоянии почти
не
происходит образования
новых
и
разрыва старых связей
и что оно
близко
по
своей
структуре
к
исходным соединениям:
,0
RCT
+
СНзС
\
ОАг
.О
СНэ.С
RCT
' ОАг
(2.64)
ПС
Коэффициент
р
является мерой величины заряда, образую-
щегося
в
переходном состоянии,
а не
мерой степени образования
связи.
Однако
в
реакциях
(2.63)
и
(2.64),
а
также
в
других
ситуациях, характеризующихся отсутствием кислотно-основного
катализа, образование связи
и
заряда взаимосвязано, поэтому
р
служит также мерой степени образования связи.
При
наличии
же кислотно-основного катализа, когда происходит частичная
нейтрализация зарядов, образующихся
в
переходном состоянии,
между
р и
степенью образования связи никакой зависимости
нет
[44].
2. Факторы, определяющие нуклеофильность
и
легкость отщепления уходящей группы
Эффективность общего кислотно-основного катализа кисло-
род-и азот-содержащими основаниями зависит ТОЛЬКО
ОТ ИХ р/Са
и
не
зависит
от
химической природы этих соединений
(за ис-
ключением случая повышенной активности оксимов
при
общем
кислотном катализе),
а на
нуклеофильную реакционную способ-
ность заметно влияет природа реагентов.
Эти
реакции можно
разделить
на два
больших класса
в
зависимости
от
того,
слабые
или
сильные
электрофильные центры
при
этом атакуются
[45].

ХИМИЧЕСКИЙ
КАТАЛИЗ
85
а. Реакции
нуклеофилов
с
карбонильной,
фосфорильной,
сульфгидрильной
и
другими
сильными
электрофильными
группами
Атака
нуклеофилом амидного, эфирного
или
карбонильного
углерода
сопровождается образованием «реально существую-
щего»
промежуточного соединения,
и
валентность углеродного
атома
не
превышает
при
этом обычного значения,
т. е. 4. Ана-
логичным образом атакуется эфир фосфорной кислоты, при этом
образуется промежуточное соединение
с
пятивалентным атомом
фосфора.
Переходное состояние
для
этой реакции включает
об-
разование обычной ковалентной связи. Такая ситуация харак-
терна
для
сильных электрофильных центров. Основным факто-
ром,
определяющим нуклеофильность
в
этих реакциях, является
основность нуклеофила
—
чем
она
выше,
тем
сильнее нуклео-
фильность.
Однако реакционные способности разных классов
нуклеофилов различаются: амины
и
тиолят-анионы,
как
прави-
ло,
более сильные нуклеофилы, чем окси-анионы [46,47]. Кроме
того,
ряд
нуклеофилов,
у
которых
два
электроотрицательных
атома расположены рядом (например,
NH
2
OH,
NH
2
NH
2
,
NH
2
CONHNH
2
,
НОО-
и
МеОО~), обладают большей реакцион*
ной
способностью, чем можно было
бы
ожидать, исходя
из
значе-
ний
их р/Са. Это
явление известно
под
названием
а-эффекта.
Относительные реакционные способности разных классов
нук-
леофилов часто коррелируют
с
константами равновесия реак-
ций
присоединения этих веществ
к
альдегидам
и
кетонам
[48].
Легкость
отщепления
группы
зависит
как от ее
р/С
а
,
так и от
состояния
протонирования.
По
существу
«хорошая уходящая
группа»— это группа, устойчивая
в
растворе. Например, м-нит-
рофенолят-ион
является хорошей уходящей группой, поскольку
представляет собой слабое основание (р/Са л-нитрофенола равен
7,0).
В
основе
его
стабильности лежит делокализация отрица-
тельного заряда
на
ароматическом кольце
и
нитрогруппе [схема
(2.65)
NO
2
(2.66)
86
ГЛАВА
2
ч
г
0
-1
-2
-3
-4
-
-
-
-
SC
• о/
/\ i
•
H
2
N0H
о
У
/
•NH
2
Nrl
2
R^
/
У
1
1 I I
7
8
PKa
W
11
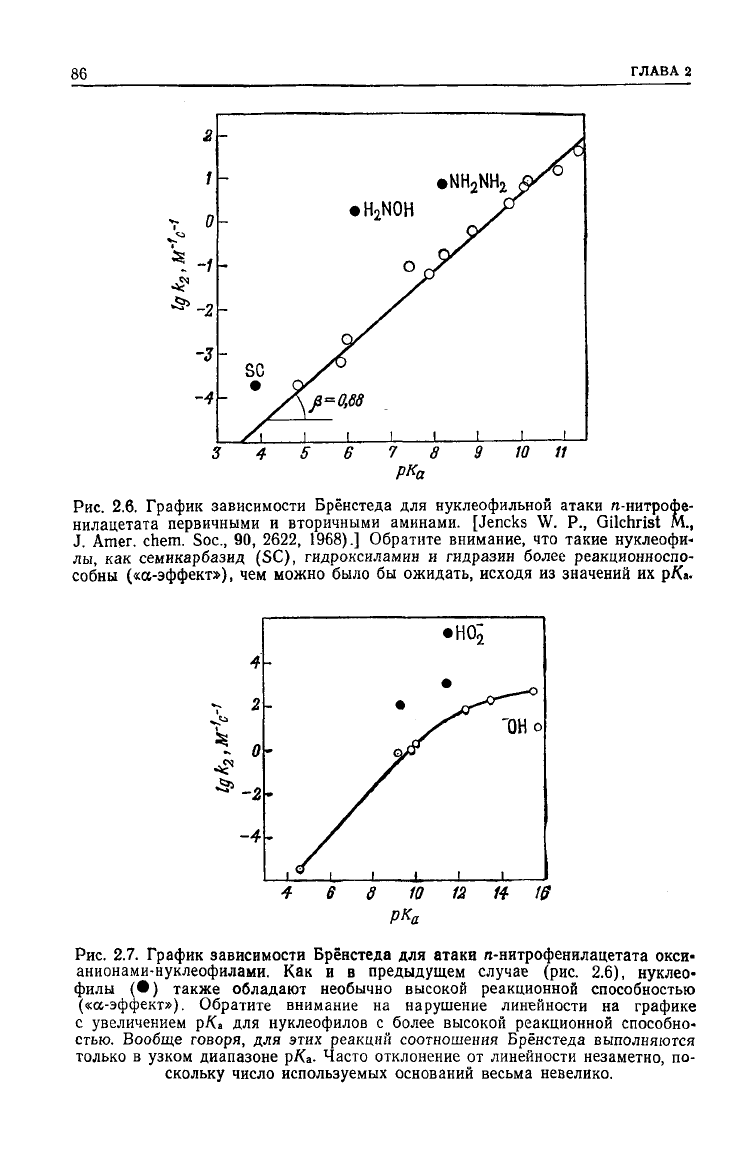
Рис.
2.6. График зависимости Брёнстеда для нуклеофильнои атаки л-нитрофе-
нилацетата первичными и вторичными аминами. [Jencks W. P., Gilchrist М.,
J.
Amer.
chem. Soc, 90,
2622,
1968).]
Обратите внимание, что такие нуклеофи-
лы,
как семикарбазид (SC), гидроксиламин и гидразин более реакционноспо-
собны («а-эффект»), чем можно было бы ожидать, исходя из значений их
рК>-
- 0-
6 8 10 12 Н IS
Рис.
2.7. График
зависимости
Брёнстеда
для атаки л-нитрофенилацетата окси-
анионами-нуклеофилами.
Как и в предыдущем
случае
(рис. 2.6), нуклео-
филы
(••) также обладают необычно высокой реакционной способностью
(«а-эффект»). Обратите внимание на нарушение линейности на графике
с увеличением р/(
а
для нуклеофилов с более высокой реакционной способно-
стью. Вообще говоря, для этих реакций соотношения Брёнстеда выполняются
только в узком диапазоне р/Са- Часто отклонение от линейности незаметно, по-
скольку число используемых оснований весьма невелико.

ХИМИЧЕСКИЙ
КАТАЛИЗ
87
(2.65)]. Этот ион легко высвобождается непосредственно из
тетраэдрического промежуточного соединения [схема (2.66)].
Для данного класса уходящих групп уменьшение основности
приводит к облегчению отщепления уходящей группы.
Ацетат
(р/Са уксусной кислоты равен 4,76) — более хорошая уходящая
группа, чем n-нитрофенол и фосфат (р/С
а
около 7), которые в
свою очередь являются более хорошими уходящими группами,
чем ОН-
(р/Са=
15,8).
Отщепление алкоголят-ионов затруднено, поскольку это
сильные основания (р/С
а
низших спиртов равен примерно 16).
Отщепление спиртов ускоряется при общем кислотном катализе
[схема (2.67)].
СН
^ ^
СНз
~/х
~*
СН
К
+HOEt
(267
>
по
C
OEt
он
H ВН
+
В.
Нитрофениловые эфиры часто используются в качестве ухо-
дящих групп в синтетических
субстратах
по
двум
причинам:
а) нитрофенолят-ион имеет характерный максимум поглощения
при
400 нм и, следовательно, легко идентифицируется спектро-
фотометрически; б) этот ион является очень хорошей уходящей
группой, в
результате
чего образуется реакционноспособный
субстрат.
Оба эти фактора обусловлены делокализацией заря-
дов [схема (2.65)].
Чтобы амин отщепился от молекулы, он должен присоеди-
нить протон, поскольку амид-ионы
(RNH-)
слишком нестабиль-
ны,
чтобы непосредственно высвобождаться в раствор. (Исклю-
чение составляют сильно активированные производные, напри-
мер, 2,4-динитроанилин.)
б.
Атака
нуклеофилом у насыщенного атома
углерода
Атака
нуклеофилом у насыщенного атома
углерода
(напри-
мер, бимолекулярная реакция, в
ходе
которой тиол атакует
углерод
метильной группы в S-аденозилметионине) сопровож-
дается образованием переходного состояния, в котором к обычно
четырехвалентному
углероду
присоединено пять групп (2.68).
<T%.s*
L
>
Л
Я
/\
c
(2.68)
ДО

88
ГЛАВА
2
Такое число связей
не
является нормальным
для
углерода
и
свойственно лишь переходному состоянию. Это типичный пример
«слабого»
центра. Тяжелые, способные поляризоваться атомы,
например атомы серы
и
иода
(т. е.
«слабые»
лиганды), более
реакционноспособны,
чем
слабо поляризующиеся атомы
—
кис-
лород
или
азот
(т. е.
«сильные» лиганды). Способность
к
поля-
ризации
является главным фактором, определяющим нуклео-
фильность
по
отношению
к
алкильным группам
и
другим
сла-
бым центрам.
В
пределах любого данного класса соединений
увеличение основности увеличивает нуклеофильность, однако
при
переходе
от
класса
к
классу более важным фактором
ста-
новится способность
к
поляризации (табл.
2.6).
Таблица
2.6
Относительная реакционная способность
различных нуклеофилов
а
*
Нуклеофил
Н
2
О
N0"
F-
СН
3
СО
2
"
С1"
C
6
H
6
N
НРО*-
Вг-
ОН"
C
6
H
5
NH
2
Г
CN"
SH"
—
1,74
-1,3
3,17
4,76
-7,0
5,17
7,21
-9,0
15,74
4,62
—
10,0
9,40
7,00
Реакционная
способность
по
отношению
к
реак-
ционной
способности
СНзВг
1,00
11
100
525
1,1
•
10
3
4,0 •
10
3
6,3-10
3
7,8
•
10
3
1,6-10*
3,1
•
10
4
1,1-10
5
1,3- 10
s
1,3-10
5
а
'
Swain
С. О.,
Scott
С. В., J. Am.
chem.
Soc. 75,
141 (1953).
Как
и в
случае
реакций
с
карбонильной группой, слабоос-
новные уходящие группы замещаются легче,
чем
группы
с
высо-
кой
основностью.
в.
Активация
уходящей
группы
Как
ясно
из
предыдущего раздела, замещение сильнооснов-
ных групп
в
карбонильных соединениях
и
групп, связанных
с
насыщенным атомом
углерода,
затруднено. Крайним примером
ХИМИЧЕСКИЙ
КАТАЛИЗ
89
такого рода является этерификация спирта карбоксилат-ионом.
Для ее осуществления потребовалось бы образование тетраэд-
рического промежуточного соединения с двумя отрицательно
заряженными атомами кислорода и последующим высвобожде-
нием О
2
-.
R—С—СГ
OR'
RCO
2
R'
2-
(2.69)
При
катализируемой аминоацил-тРНК-синтетазой этерифика-
ции
тРНК аминокислотами аминокислота активируется путем
образования связанного с ферментом смешанного ангидрида с
AMP [схема
(2.70)]
точно таким же образом, как это
делает
химик-органик, когда он активирует карбоновую кислоту с по-
мощью образования ацилхлорида или смешанного ангидрида.
.• W
г
г-
г
Р—О—Р—О—СН
2
id •
ОН
ОН
RHC
7
NH
3
О о~
Mg
2+
p
2
or+RHC—с—о—Р—осн
(2.70)
ОН
ОН
[Заметьте,
что в схеме (2.70) субстратом является комплекс АТР
с
магнием, причем ион Mg
2+
является электрофильным катали-
затором].
Карбонильная группа аминокислоты активируется со-
гласно
схеме (2.70), связываясь с хорошей уходящей группой —
фосфатным
остатком AMP, имеющим р/С
а
около 6 или 7. Он
легко
атакуется одной из гидроксильных групп рибозного коль-
ца
концевого аденозина
тРНК.
90
ГЛАВА
2
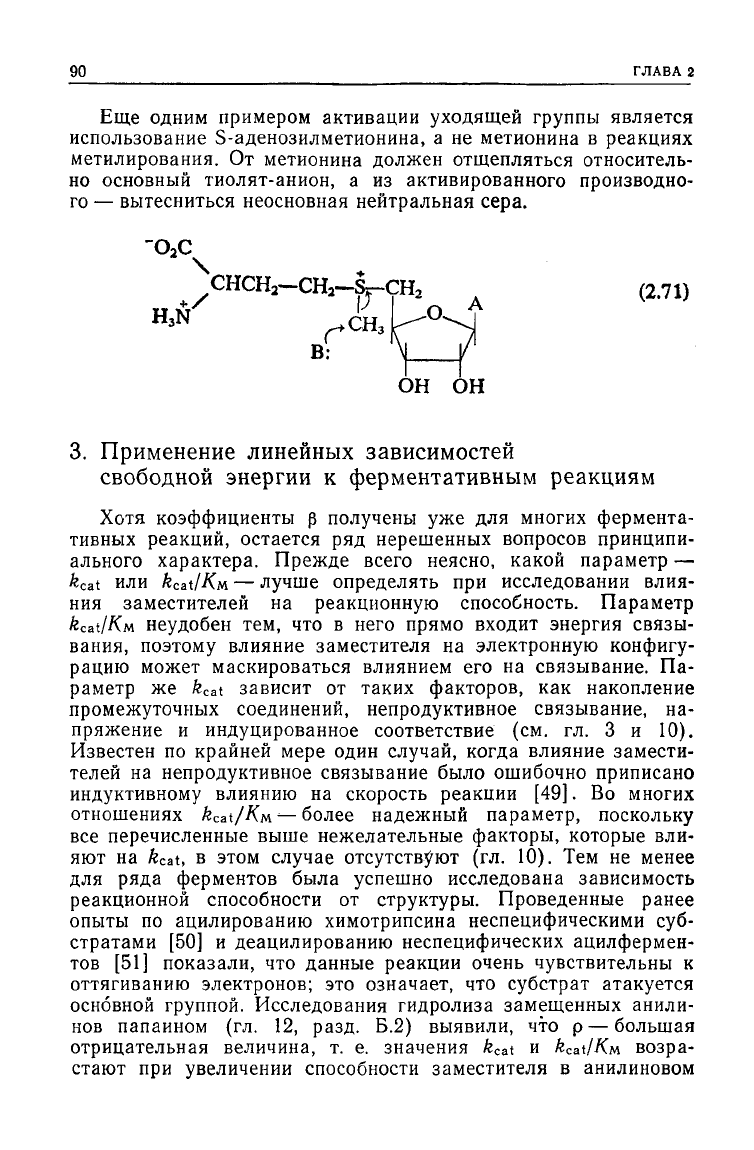
Еще одним примером активации
уходящей
группы является
использование S-аденозилметионина, а не метионина в реакциях
метилирования. От метионина должен отщепляться относитель-
но
основный тиолят-анион, а из активированного производно-
го — вытесниться неосновная нейтральная сера.
"О
2
С
CHCH
2
-CH
a
~S
r
CH
2
(2.71)
он он
3. Применение линейных зависимостей
свободной энергии к ферментативным реакциям
Хотя
коэффициенты р получены уже для многих фермента-
тивных реакций, остается ряд нерешенных вопросов принципи-
ального характера. Прежде всего неясно, какой параметр —
fecat
или
fecat/^См
—
лучше
определять при исследовании влия-
ния
заместителей на реакционную способность. Параметр
kcat/Кгл
неудобен тем, что в него прямо
входит
энергия связы-
вания,
поэтому влияние заместителя на электронную конфигу-
рацию может маскироваться влиянием его на связывание. Па-
раметр же
fecat
зависит от таких факторов, как накопление
промежуточных соединений, непродуктивное связывание, на-
пряжение и индуцированное соответствие (см. гл. 3 и 10).
Известен по крайней мере один случай, когда влияние замести-
телей на непродуктивное связывание было ошибочно приписано
индуктивному влиянию на скорость реакции [49]. Во многих
отношениях
kcat/K/л
^- более надежный параметр, поскольку
все перечисленные выше нежелательные факторы, которые вли-
яют на &cat, в этом
случае
отсутствуют
(гл. 10). Тем не менее
для ряда ферментов была успешно исследована зависимость
реакционной
способности от
структуры.
Проведенные ранее
опыты по ацилированию химотрипсина неспецифическими суб-
стратами [50] и деацилированию неспецифических ацилфермен-
тов [51] показали, что данные реакции очень чувствительны к
оттягиванию электронов; это означает, что
субстрат
атакуется
основной группой. Исследования гидролиза замещенных анили-
нов
папаином (гл. 12, разд. Б.2) выявили, что р — большая
отрицательная величина, т. е. значения
fe
C
at
и
kcat/Км
возра-
стают
при увеличении способности заместителя в анилиновом
