Фёршт Э. Структура и механизм действия ферментов
Подождите немного. Документ загружается.


ИЗМЕРЕНИЕ
КОНСТАНТ СКОРОСТИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ 131
ды, в то время как число оборотов большинства ферментов
составляет
—1000
с
-1
. Второй — метод
релаксационной
кине-
тики.
Проблема мертвого времени, связанного со смешиванием
реагентов, здесь
отсутствует
благодаря использованию предва-
рительно смешанных растворов.
А. Методы
быстрого
смешивания
реагентов
и
быстрого
«замораживания»
реакции
1. Метод непрерывной струи
В 1923 г. Хартридж и Роутон при исследовании присоедине-
ния
лигандов к дезоксигемоглобину применили метод непре-
рывной
струи [1]. Принцип этого метода иллюстрирует рис. 4.1.
Два шприца соединены через сместитель с реакционной трубкой.
Смеситель
t=l/x
Скорость
струн
— л;лс"'
^Субстрат
Рис.
4.1. Схема устройства, используемого в методе непрерывной струи.
Один шприц заполняется раствором фермента, другой — рас-
твором субстрата; оба раствора продавливаются с постоянной
скоростью и тщательно перемешиваются в смесителе, а затем
поступают в трубку и «старятся». При постоянной скорости
струи
«возраст»
раствора прямо пропорционален пути, пройден-
ному им в трубке, и скорости струи. Например, если скорость
струи равна 10 м-с-
1
, то на расстоянии 1 см от смесителя «воз-
раст»
раствора
будет
равен 1 мс, на расстоянии 10 см — 10 мс и
т. д. Скорость протекания струи
следует
поддерживать выше
критической,
чтобы гарантировать турбулентность потока. Ниже
этого критического значения, равного для трубки диаметром
1
мм приблизительно 2 м-с~', поток может стать ламинарным и
жидкость в центре трубки
будет
течь быстрее, чем у стенки. Тем
самым устанавливается верхний временной предел для трубки
данной
длины.
2. Метод остановленной струи
Этот метод был разработан в 1934 г. Роутоном [2] и значи-
тельно усовершенствован шестью годами позже Чансом [3].
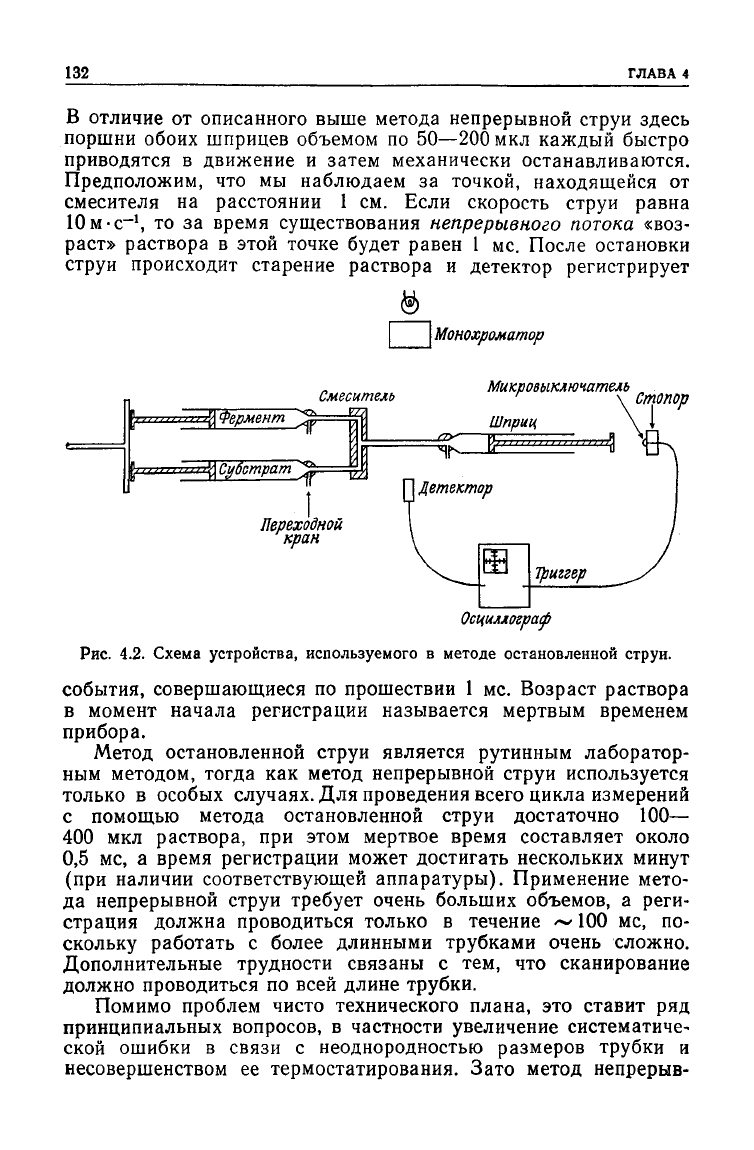
Лежащий в его основе принцип иллюстрирует рис. 4.2 [4].
132
ГЛАВА
4
В отличие
от
описанного выше метода непрерывной струи здесь
поршни
обоих шприцев объемом
по
50—200
мкл каждый быстро
приводятся
в
движение
и
затем механически останавливаются.
Предположим,
что мы
наблюдаем
за
точкой, находящейся
от
смесителя
на
расстоянии
1 см.
Если скорость струи равна
10м-с"
1
,
то за
время существования
непрерывного
потока «воз-
раст»
раствора
в
этой точке
будет
равен
1 мс.
После остановки
струи происходит старение раствора
и
детектор регистрирует
Монохроматор
Смеситель
Микровыключатель
Осциллограф
Рис.
4.2.
Схема устройства, используемого
в
методе остановленной струи.
события,
совершающиеся
по
прошествии
1 мс.
Возраст раствора
в
момент начала регистрации называется мертвым временем
прибора.
Метод остановленной струи является рутинным лаборатор-
ным
методом,
тогда
как
метод непрерывной струи используется
только
в
особых
случаях.
Для
проведения всего цикла измерений
с помощью метода остановленной струи достаточно
100—
400
мкл
раствора,
при
этом мертвое время составляет около
0,5
мс, а
время регистрации может достигать нескольких минут
(при
наличии соответствующей аппаратуры). Применение мето-
да непрерывной струи
требует
очень больших объемов,
а
реги-
страция
должна проводиться только
в
течение
~ 100 мс, по-
скольку работать
с
более длинными трубками очень сложно.
Дополнительные трудности связаны
с тем, что
сканирование
должно проводиться
по
всей длине трубки.
Помимо
проблем чисто технического плана,
это
ставит
ряд
принципиальных
вопросов,
в
частности увеличение систематиче-
ской
ошибки
в
связи
с
неоднородностью размеров трубки
и
несовершенством
ее
термостатирования. Зато метод непрерыв-
ИЗМЕРЕНИЕ
КОНСТАНТ СКОРОСТИ ФЕРМЕНТАТИВНЫХ РЕАКЦИИ
133
ной
струи имеет меньшее мертвое время — всего
100—200
мкс,
поскольку
отсутствуют
трудности, связанные с механической
остановкой
струи; остановка происходит за доли миллисекунды
и
может привести к возникновению ударных волн, если осуще-
ствляется слишком резко. Второе преимущество данного метода
состоит в том, что можно использовать инерционные детекторы,
так
как в каждой данной точке трубки возраст раствора посто-
янен.
Этот фактор играл особенно большую роль в эксперимен-
тах Хартриджа и Роутона, которые использовали в качестве
детектора ручной спектроскоп!
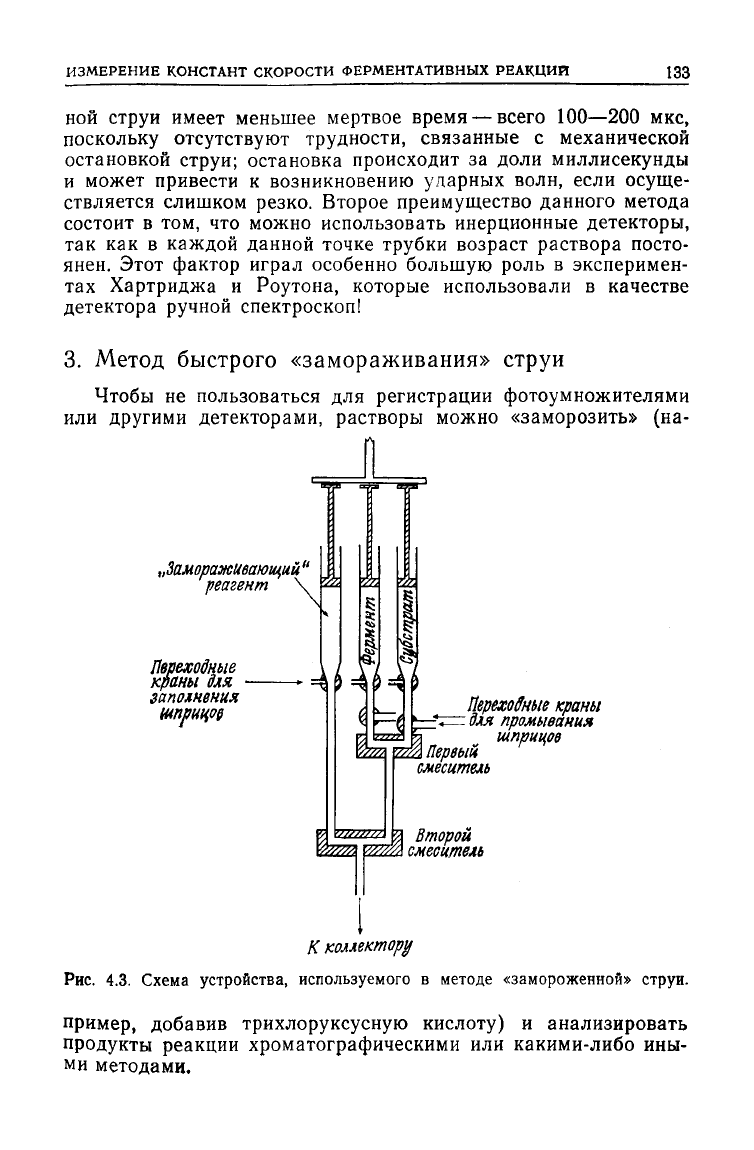
3. Метод быстрого «замораживания» струи
Чтобы не пользоваться для регистрации фотоумножителями
или
другими детекторами, растворы можно «заморозить» (на-
„Замораживающий
"
реагент
ч
Переходные
краны
для
заполнения
Переходные
краны
L
-
J
i^r
для промывания
шприцов
Первый
смеситель
Второй
смеситель
К
коллектору
Рис.
4.3. Схема устройства, используемого в методе «замороженной» струи.
пример,
добавив трихлоруксусную кислоту) и анализировать
продукты реакции хроматографическими или какими-либо ины-
ми
методами.
134
ГЛАВА
4
а.
«Замороженная»
струя
В простейшем варианте этот метод состоит
в том, что
конец
реакционной
трубки, используемой
в
методе непрерывной струи,
погружают
в
сосуд
с
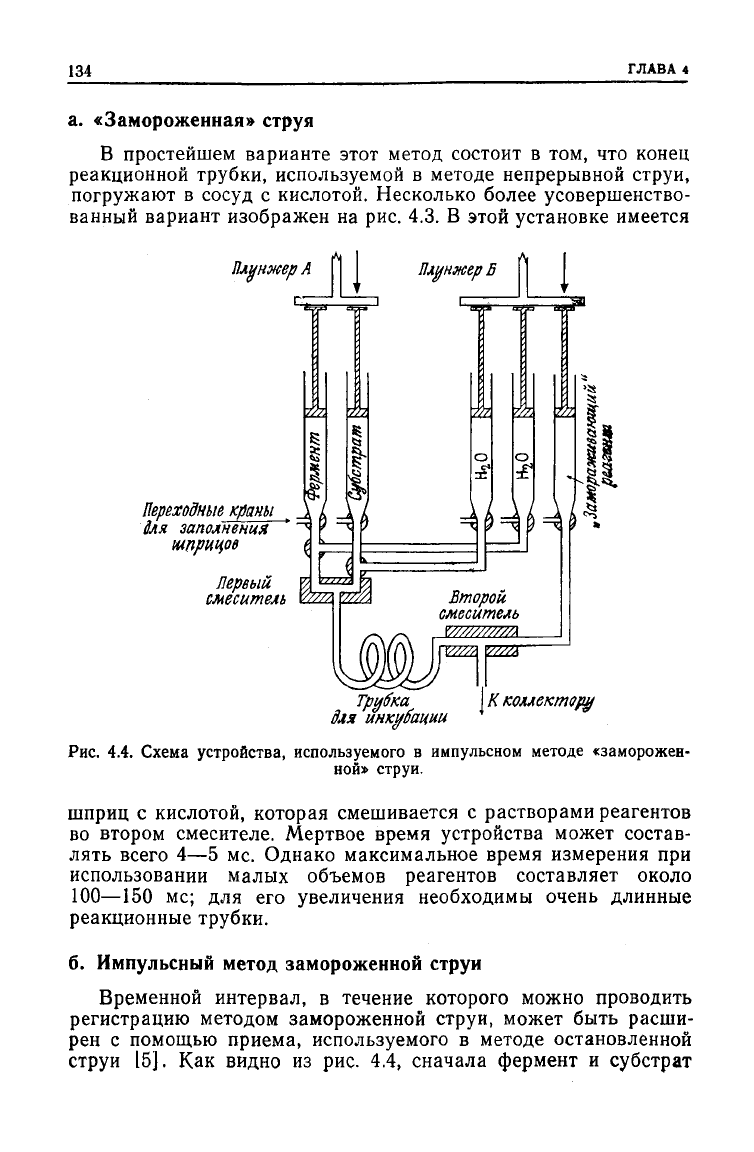
кислотой. Несколько более усовершенство-
ванный
вариант изображен
на рис. 4.3. В
этой установке имеется
Плунжер
А
Переходные
краны
для заполнения
шприцов
Первый
смеситель
г
Трибка
\К
коллектору
для инкубации
Рис.
4.4.
Схема устройства, используемого
в
импульсном методе «заморожен-
ной» струи.
шприц
с
кислотой, которая смешивается
с
растворами реагентов
во втором смесителе. Мертвое время устройства может состав-
лять всего
4—5 мс.
Однако максимальное время измерения
при
использовании
малых объемов реагентов составляет около
100—150
мс; для его
увеличения необходимы очень длинные
реакционные
трубки.
б.
Импульсный
метод
замороженной
струи
Временной интервал,
в
течение которого можно проводить
регистрацию методом замороженной струи, может быть расши-
рен
с
помощью приема, используемого
в
методе остановленной
струи
15]. Как
видно
из рис. 4.4,
сначала фермент
и
субстрат
ИЗМЕРЕНИЕ
КОНСТАНТ СКОРОСТИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
135
смешивают
и
переводят
в
инкубационную
трубку
плунжером,
приводимым
в
движение сжатым воздухом,
а
затем
по
проше-
ствии некоторого времени
(150 мс или
больше) инкубируемую
смесь вместе
с
порцией дистиллированной воды переводят
вто-
рым плунжером
во
второй смеситель,
где и
«замораживают».
Б.
Релаксационные методы
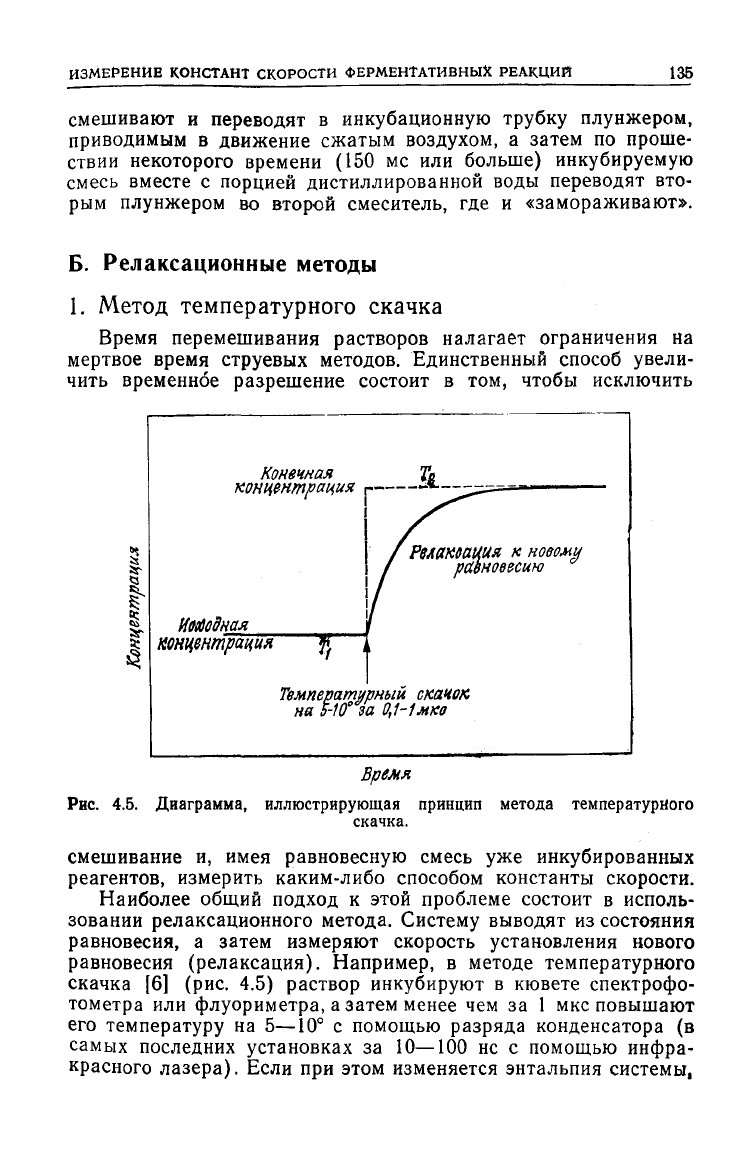
1. Метод температурного скачка
Время перемешивания растворов налагает ограничения
на
мертвое время
струевых
методов. Единственный способ увели-
чить временное разрешение состоит
в том,
чтобы исключить
Конечная
концентрация
ИШдная
концентрация
j» j
/Релаксация
к
новому
I
равновесию
•
1
Температурный
скачок
на
5-Ю
за
0,1-1мкв
Время
Рис.
4.5.
Диаграмма, иллюстрирующая принцип метода температурного
скачка.
смешивание
и,
имея равновесную смесь
уже
инкубированных
реагентов, измерить каким-либо способом константы скорости.
Наиболее общий
подход
к
этой проблеме состоит
в
исполь-
зовании
релаксационного метода. Систему выводят
из
состояния
равновесия,
а
затем измеряют скорость установления нового
равновесия (релаксация). Например,
в
методе температурного
скачка
[6] (рис. 4.5)
раствор инкубируют
в
кювете спектрофо-
тометра
или
флуориметра,
а
затем менее
чем за 1 мкс
повышают
его температуру
на 5—10° с
помощью разряда конденсатора
(в
самых последних установках
за
10—100
не с
помощью инфра-
красного лазера). Если
при
этом изменяется энтальпия системы,

136
ГЛАВА
4
то смещается и положение равновесия. Переход системы к но-
вому равновесию характеризуется в общем
случае
набором вре-
мен
релаксации т.
Ясно,
что к системам, в которых протекают необратимые
химические процессы, этот метод не применим. Наиболее ценен
он
для исследования простого связывания лигандов (например,
связывания
NAD+ с дегидрогеназой, связывания ингибиторов)
или
для исследования конформационных изменений в белке.
Предпринимались
попытки объединить метод температурного
скачка
с методом остановленной струи.
2. Ядерный магнитный резонанс [7—10]
Иногда
с помощью ЯМР можно измерить константы скоро-
сти
диссоциации
комплексов
между
ферментом и ингибитором.
В сочетании с константами связывания для данной реакции
это
позволяет получить константы скорости ассоциации.
В.
Анализ
предстационарной
кинетики
и
кинетики
релаксационных
процессов
В простых случаях дифференциальные уравнения для меня-
ющихся со временем переходных процессов решаются относи-
тельно просто. Однако важно понимать,
почему
данному
случаю
соответствует именно данная форма решения. В настоящем раз-
деле
мы сосредоточим наше внимание на интуитивном
подходе
к
решению этой проблемы. Понимание сути вещей поможет нам
избежать ошибок в алгебраических выкладках, а кроме того, мы
сможем находить решение для некоторых сложных кинетиче-
ских
схем
просто по виду этих схем.
1. Простые
экспоненциальные
функции
а.
Необратимые
реакции
Предположим, что соединение А превращается в В с кон-
стантой скорости первого порядка k\ и эта реакция идет до
конца:
А -^ В. (4.1)
В таком
случае
-^--*,[А]
(4.2)

ИЗМЕРЕНИЕ
КОНСТАНТ СКОРОСТИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
137
Интегрирование
уравнения (4.2)
дает
[A]
o
exp(-V).
где [А]
о
— начальная концентрация А. Поскольку
то
(4.3)
(4.4)
(4.5)
Как
[А], так и [В] являются простыми экспоненциальными
функциями.
Заметим,
что время полупревращения ti/, для реакции, в
которой
[А] = [В] = [А]
0
/2, задается уравнением
ехр (— kit) — -z-,
т. е.
М/2
!
0,6931
=
0,6931т.
(4.6)
(4.7)
б. Метод начальных скоростей
Рассматривая более сложные примеры, мы воспользуемся
методом
начальных
скоростей,
чтобы проиллюстрировать физи-
ческий
смысл некоторых выражений. Этот метод часто применя-
ется при изучении процессов, слишком медленных, чтобы ис-
пользовать полное время реакции, а также в том случае, когда в
системе протекают побочные реакции.
Начальная
скорость v
0
реакции (4.1) равна
»о
=
М
А
]
о
-
(4.8)
Константа
k\ определяется путем деления v
0
на ожидаемое
изменение'
концентрации реагента, следовательно,
f
=
t>
0
/A
[А]
о
.
(4.9)
в.
Обратимые реакции
В этом
случае
А превращается в В не полностью, а концент-
рация
А достигает равновесного значения.
А 4^ в.
(4.10)
1
При полном завершении реакции. —
Прим.
ред.

138
ГЛАВА
4
Для данной реакции
Л,
[А]
(4.11)
(4.12)
Подставляя выражение для [В] из уравнения (4.4), получаем
d[A]
dt
ft
r
([A]
0
-[AJ)
(4.13)
Это уравнение можно проинтегрировать, разделив переменные и
умножив каждую его часть на экспоненциальный множитель.
d [A]
—"п~—I"
fA] (ft,
•+•
к'Л = ft
r
[А]д, (4.14)
d
[A]
Отсюда
±
{[A] exp (ft, + ft
r
) t} = ft
r
[A]
o
exp (ft, + A
r
) t.
После
интегрирования получаем
К
[A] exp (ft, + ft
r
) t =
fe +
r
fe
[A] exp (ft, + ft
r
) / +
const.
(4.16)
Используя начальные условия, состоящие в том, что при / = О
LA] = [А] о, а при t = оо равновесная концентрация A, (A]
eq
,
есть
[A]
eq
= [A]
o
ft
r
/(ft
f
+ ft
r
), (4.17)
из
уравнений (4.4) и
(4.11)
получаем решение
[А]»
exp
t"
(4.18)
Выражение (4.18) для изменения во времени концентрации реа-
гента А можно разделить на различные множители. Первый из
них — экспоненциальный член, который содержит константу
скорости, или — в терминах релаксационной кинетики — вели-
чину, обратную времени релаксации 1/т, равную
1/т - ft, + k
r
,
(4.19)
а второй —
амплитудный
фактор
(4.20)

ИЗМЕРЕНИЕ
КОНСТАНТ СКОРОСТИ ФЕРМЕНТАТИВНЫХ РЕАКЦИИ 139
Для обратной реакции, т. е. для реакции, в которой исход-
ным
веществом является В, а не А, можно записать
^
ехр
<~
(*'
+
*Л
*>
+ k
&
(
4
-
21
)
Время релаксации для этого выражения такое же, как и для
уравнения (4.18), но амплитудный множитель
иной.
Первый важный момент, который необходимо отметить, со-
стоит в том, что константа скорости для процесса приближения к
равновесию больше каждой из индивидуальных констант ско-
рости, kf и k
T
, и равна их сумме. Это легко понять, если проана-
лизировать выражение для начальных скоростей. Начальная
скорость в
случае
обратимой реакции
(4.10)
такая же, как и в
случае
необратимой (4.1), однако глубина последней реакции не
столь велика, как первой. Например, до заметного накопления
продукта В в системе
будет
присутствовать только реагент А,
следовательно, уравнение
v
o = *f tA]
0
останется в силе.
Однако суммарное изменение [А] определяется теперь урав-
нением
A[A]
0
=
[A]
0
-[A]
eq
.
(4.22)
Подстановка выражения
(4.17)
дает
Л [А]
0
= [А]
0
*,/(*,+
*
г
),
(4.23)
откуда
1/т-
0о
/Д[А]
0
-*,
+ *,.
(4.24)
Второй момент состоит в том, что константы k\ и k
T
нельзя
определить, не зная амплитудный множитель.
Симметричность выражения для времени релаксации отно-
сительно констант скорости прямой и обратной реакций встре-
чается во многих
случаях,
и, как правило, константы скорости
мономолекулярных реакций нельзя рассчитать, не определив
предварительно равновесные концентрации А и В. Позже мы
увидим, что если реакция вследствие присутствия второго реа-
гента является не мономолекулярной, а псевдомономолекуляр-
ной,
то время релаксации
будет
зависеть от концентрации, что
позволит устранить указанную выше трудность.
2. Связывание
субстрата
с ферментом
E+S
3=* ES.
(4.25)
Если [S] ^?> [Е], то имеет место реакция первого порядка,
поскольку [S] меняется лишь незначительно. Если константу
скорости второго порядка для связывания фермента с субстра-
140
ГЛАВА 4
том обозначить через
k
on
, а
константу скорости
для
диссоциа-
ции
образующегося комплекса
—
через
&
O
ff,
то
уравнение
(4.25)
можно записать
в
более компактной форме:
(4.26)
Исходя
из
уравнения
(4.19),
получаем время релаксации
для
этой реакции:
(4.27)
Следует
отметить
два
момента:
а)
когда константы скорости
являются лсевдо'мономолекулярными, время релаксации зави-
сит
от
концентрации,
так что к
оп
и k
o
u
можно определить,
не
to
[Тирозин], мкМ
15
20
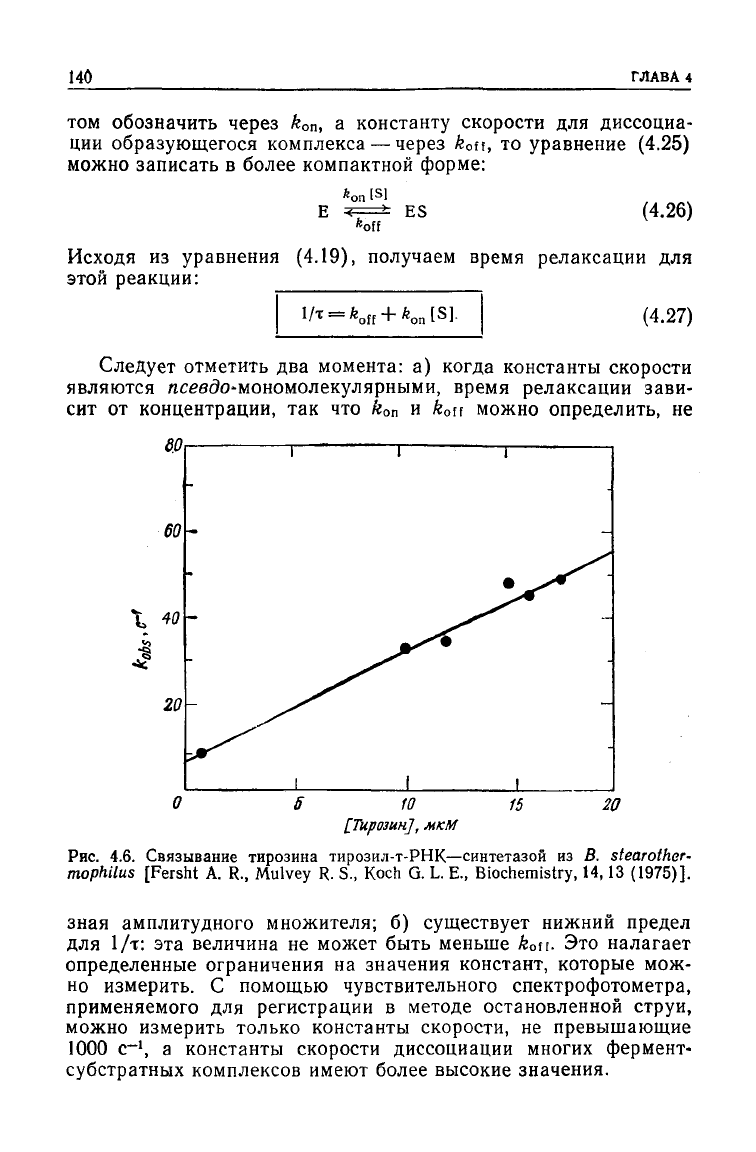
Рис.
4.6.
Связывание тирозина тирозил-т-РНК—синтетазой
из В. stearother-
mophilus
[Fersht
A. R.,
Mulvey
R. S.,
Koch
G. L. E.,
Biochemistry,
14,13
(1975)].
зная
амплитудного множителя;
б)
существует
нижний предел
для
1/т: эта
величина
не
может быть меньше
&
O
ft. Это
налагает
определенные ограничения
на
значения констант, которые
мож-
но
измерить.
С
помощью чувствительного спектрофотометра,
применяемого
для
регистрации
в
методе
остановленной струи,
можно измерить только константы скорости,
не
превышающие
1000
с~', а
константы скорости диссоциации многих фермент-
субстратных
комплексов имеют более высокие значения.
