Жариков В.А. Основы физической геохимии
Подождите немного. Документ загружается.

Рассмотрим теперь изотермические p-x диаграммы системы летучий - соль. На рис.3.166
T-p проекции системы проведено семь изотермических сечений, причем T
1
< T
2
< T
3
< T
4
< T
5
. Построение p-x сечений производится точно так же, как и изобарических. Проводим
на T-x диаграмме линии, отвечающие выбранным T
1
, T
2
, T
3
, T
4
и T
5
. Снимаем с T-р
диаграммы координаты p, отвечающие каждому из пересечений моновариантных линий и
переносим их на p-x диаграммы.
Рассмотрим последовательно изотермические сечения диаграммы. Они проведены на
рис.3.168 и 3.169. При наименьшей температуре (T
1
, рис.3.168) существуют только
равновесия твердых фаз A и C с газом. Кривые сублимации фаз C и A сходятся в
"эвтектоидной" точке (Y) сублимации смеси фаз. Повышение давления вызывает,
естественно, конденсацию твердых фаз из газа. Соответствующая зависимость
термодинамически обосновывается обычным способом. Например, для фазы C: μ
C
= μ
c
G
,
dμ
C
= dμ
c
G
. Для изотермических условий подставляем значения dμ:

Поскольку объем компонента c в газовой фазе (V
c
G
) всегда больше объема твердой фазы C
(V
c
), увеличение давления вызывает конденсацию компонента c. Форма кривой
конденсации (см. все сечения) зависит от относительных значений объемов при данных T
и p.
Изотермическое сечение T
2
имеет более сложное строение. Оно пересекает по мере
увеличения давления кривую сублимации компонента c: G → G+С, трехфазовую кривую
L → G+C, кривую сублимации легколетучего компонента a: G → G+A, кривую
конденсации бинарной системы G → L+A, и пересечение эвтектической линии L → A+C.
Перенесем нонвариантные точки (в простых системах) и нонвариантные трехфазовые
конноды (в бинарных системах) GLC, GLA и LAC. На трехфазовых коннодах важно
правильно расставить точки составов G и L. Очевидно, что состав газа всегда будет
расположен ближе к вершине A, т.е. более обогащен летучим a по сравнению с
жидкостью, но сопоставлять точки в различных изотермических сечениях следует,
опираясь на T-x и p-x проекции (см. рис.3.166) и физический смысл изменения составов в
зависимости от Т и р, по возможности отразив эти изменения составов (заметим, что
вертикальный масштаб на сечении Т
2
для ясности схемы на отрезке р
R
-p
Y
несколько
увеличен по сравнению с T-p проекцией). Сообразуясь также с T-p зависимостями
растворимости a и c в газе и жидкости проводим моновариантные линии. Соединим p
v
C
с
p
R
G
и p
R
G
с Y (точкой эвтектоидной сублимации), p
v
A
с Y, и наконец, треугольник p
R
L
- p
Y
L
-E ограничит нам дивариантное поле жидкости. Остальные поля - двухфазовые, кроме
гомогенного поля G, расположенного при малых p и расширяющегося в области составов,
обогащенных летучим a.
Термодинамическое описание равновесий A-G и C-G мы уже разобрали. На равновесии G-
L остановимся несколько ниже. Равновесия A+L и C+L описываются уравнениями,
сходными уравнениями Шредера, но только в зависимости от p. Так же, как и для
равновесий G-C, но уже для сосуществующих L
c
-C будем иметь μ
C
= μ
c
L
, dμ
C
= dμ
c
L
, и
подставляя dμ для изотермических условий:
Поскольку объем компонента в расплаве (V
c
L
) больше, чем твердой фазы V
c
, то
увеличение давления уменьшает содержание компонента c в расплаве.
Рассмотрим теперь изменение фазовых соотношений при кристаллизации вследствие
увеличения давления на примере фигуративного состава, заданного точкой 1. От точки 1
до точки 2 - однофазовое поле газа. Согласно правилу фаз n = k + 1 - r = 2 система
дивариантна (один экстенсивный параметр, например f
ex
=x
c
, два интенсивных: f
in
- p и x
a
).
От точки 2 до точки 3 - двухфазовое состояние: два экстенсивных параметра - x
c
,
определяющих количество фазы C, и x
a
, определяющей количество газа G, один
интенсивный - p. Система моновариантна: увеличение давления вызывает перемещение
общего состава из точки 2 в точку 3, состав газа при этом изменяется по кривой 2-p
R
G
. В
точке 3 система оказывается в нонвариантном состоянии (пересечение T
2
трехфазовой
кривой GLC, рис. 3.168). Для состава 3 нонвариантная (при постоянном давлении)
реакция G+C → L протекает до полного растворения фазы C в возникающем расплаве
(очевидно, что если бы точка исходного состава проектировалась на нонвариантную
конноду между точками p
R
L
и p
R
(x
c
=1), то реакция заканчивалась бы исчезновением газа
в системе). Нонвариантное состояние описывается тремя экстенсивными параметрами f
ex
:
x
a
, x
c
и V. Термодинамические соотношения ΔG = 0, ΔG = ΔF - (-pΔV) = 0, .ΔF = -p
R
ΔV = -
p
R
[x
L
V
L
- (x
G
V
G
+ x
C
V
C
)].
После полного растворения C система становится моновариантной G+L, и при увеличении
давления общий состав перемещается из точки 3 в точку 4, состав газа изменяется по
кривой p
R
G
-4
G
, состав жидкости - по кривой p
R
L
→ 4. Выше по давлению точки 4 система
находится в состоянии гомогенного расплава, состав которого может быть задан мольным
количеством любого из компонентов. В точке 5 из расплава начнет кристаллизоваться
фаза A. Состав системы изменяется от точки 5 до точки 6. Состав расплава - по кривой 5-
E, уравнения которой выражают зависимость ликвидуса от давления и приведены выше
(3.61 - 3.63). Кристаллизация в системе закончится в точке 6, представляющей эвтектику
при данном давлении (p
E
). В этой точке происходит обычная эвтектическая
кристаллизация L → A+C при данных постоянных p (p
E
) и T (выбранное изотермическое
сечение T
2
).
Изотермическое сечение T
3
, расположенное чуть выше по температуре сечения T
2
,
отличается только тем, что в рассмотренном диапазоне давлений линии ликвидусов фаз A
и C не образуют эвтектическую точку: эвтектика при T
3
расположена при более высоких
давлениях.
Еще четыре изотермических сечения T
4
, T
5
, T
6
и T
7
(см. рис.3.169) характеризуют более
высокотемпературную часть T-p диаграммы летучий (a) - соль (c). Общим для всех
сечений являются значительные области двухфазовых равновесий газ - расплав.
Поведение моновариантных линий конденсации (состав газа) и кипения (состав жидкости)
в зависимости от давления определяется аналогично тому, как выводилось уравнение Ван-
Лаара, но только теперь для зависимости x от p. При постоянной температуре из равенства
химических потенциалов μ
c
G
= μ
c
L
и их дифференциалов dμ
c
G
= dμ
c
L
следует V
c
G
dp + RT ln
a
c
G
= V
c
L
dp + RT ln a
c
L
. Oткуда:

Поскольку объем компонента c в газовой фазе ( V
c
G
) всегда больше, чем в расплаве ( V
c
L
),
то из (3.72-3.74) следует, что содержание компонента c в газовой фазе всегда меньше, чем
в расплаве, и по мере увеличения давления содержание компонента "c "в газовой фазе и
расплаве уменьшается. Для более полной характеристики фазовых соотношений в более
сложных системах (где V=f(x)) используют уравнения Ван-дер-Ваальса: из (3.25) при
T=const следует:
однако отмеченные принципиальные зависимости достаточно наглядно выступают и в
приведенных выше уравнениях (3.72-3.74). В соответствии с этими зависимостями на p-x
сечениях T
4
-T
7
проведены моновариантные линии конденсации (состав газа) и кипения
(состав расплава).
Подставив в уравнения (3.72-3.74) x
c
=1-x
a
получим обратные соотношения для
компонента a: газовая фаза всегда более богата летучим и легкоплавким компонентом,
который обладает большей упругостью пара (что наглядно видно на изотермических
сечениях T
2
, T
3
, рис.3.168, и T
4
, рис. 3.169, где p
v
A
всегда больше p
v
C
. Отметим, что
именно через упругость пара принято во многих учебниках по физической химии
выражать первый закон Коновалова.
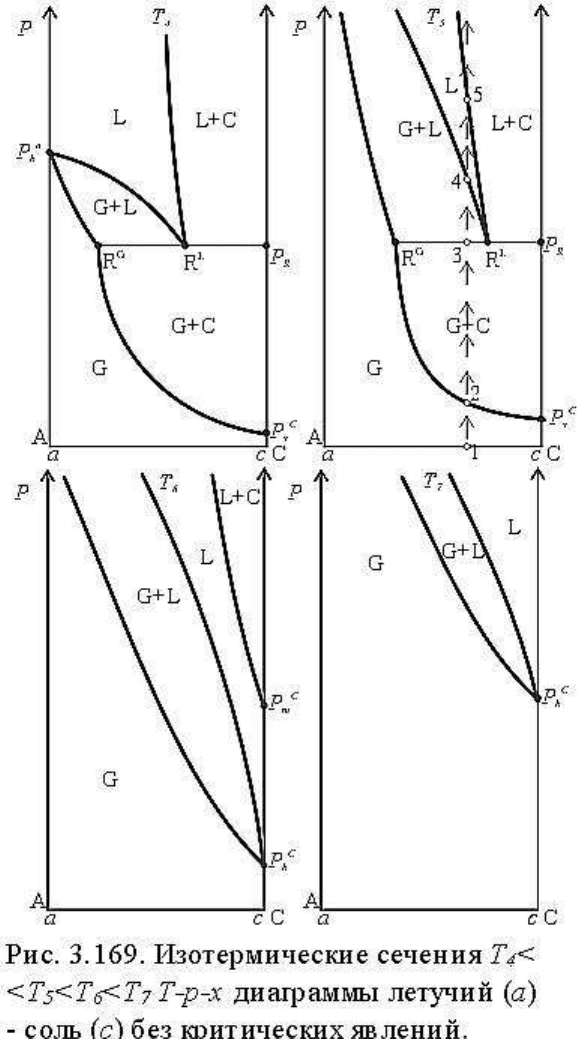
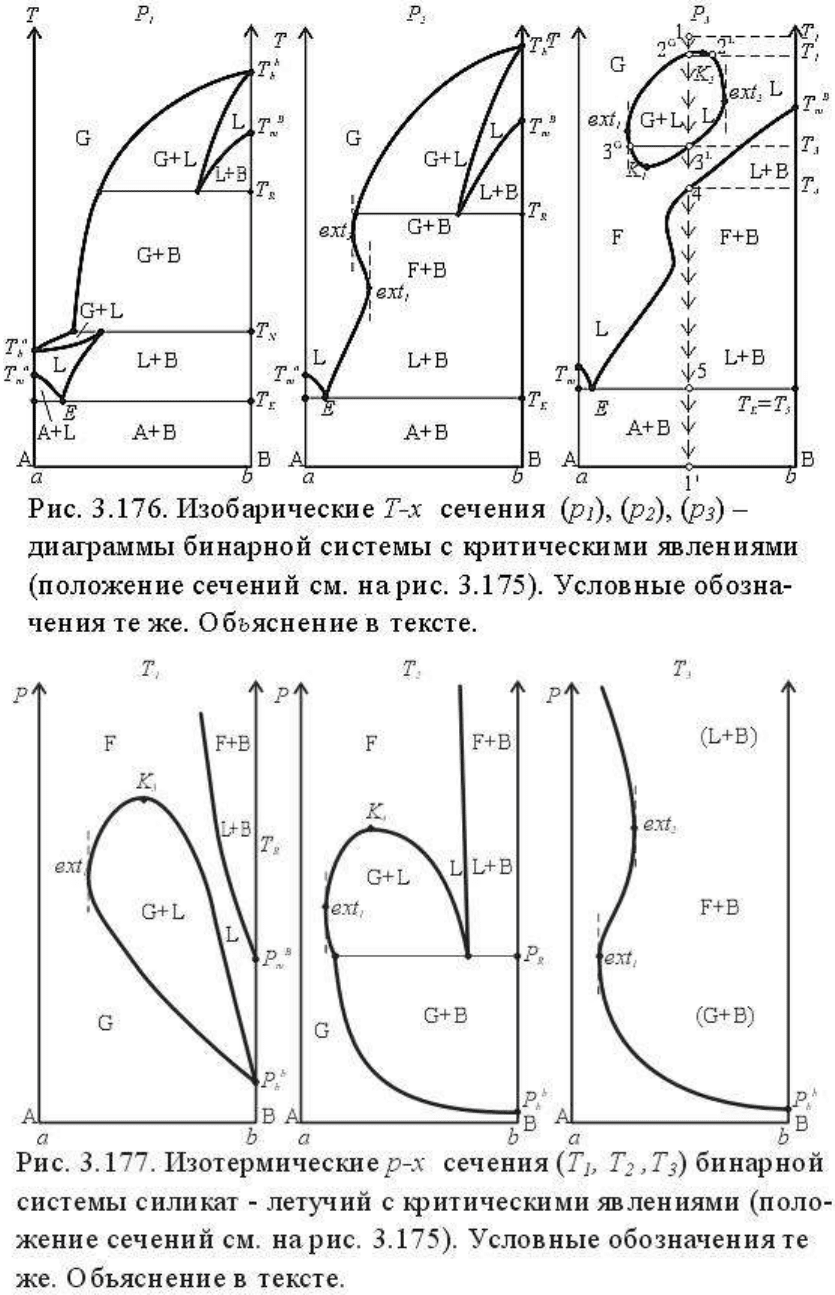
Приведенные на рис.3.169 четыре изотермических p-x сечения сравнительно просты
топологически и не требуют детального рассмотрения. Сечение T
4
и T
5
объясняет то, что
они проходят через трехфазовую кривую GLC. Различие между ними состоит в том, что
при T
4
достигается точка кипения легколетучего компонента (p
b
a
) и поле газовой фазы
ограничено по давлению этой точкой. При температуре T
5
давление летучего компонента
столь велико, что поле газа не ограничено в принятом диапазоне давлений. Ниже, в виде
схемы показана последовательность кристаллизации при увеличении давления в сечении
T
5
для фигуративного состава 1, охватывающего наибольшее число фазовых переходов:
Изотермические p-x сечения T
6
и T
7
(см. рис.3.169) расположены выше (по температуре)
трехфазовой кривой и характеризуют при T
6
зависимость от давления ликвидуса фазы C и
двухфазовое равновесие кипения (L) - конденсации (G). При самой высокой температуре
(сечение T
7
) в системе существуют только газ, жидкость и область двухфазового
равновесия (G+L) между ними. Твердые фазы отсутствуют при этих T и p во всем
диапазоне составов. Рассмотренные выше диаграммы (T-p-x, T-x и p-x) используются в
качестве модельных для системы летучий (обычно вода) - соль. К этому типу относятся
многие экспериментально изученные системы вода - хлориды ( Na, K, Ca, Mg, Li и др.),
вода - гидроокиси (K, Na, Rb, Cs и др.), вода - фториды (K, NH
3
) и другие. Однако
экспериментальные данные даже по хорошо изученным системам (H
2
O-NaCl, H
2
O-KCl)
ограничены наиболее показательными равновесиями. Обычно это T-p-x координаты
трехфазовых кривых (GLC) и координаты LC кривых растворимости в водной части
системы (равновесия EN
L
сечения Tx - p
3
, p
4
, низкотемпературная часть p
5
, см. рис.3.167),
иногда данные T-x равновесия газ - водный раствор также в низкотемпературной части
систем.
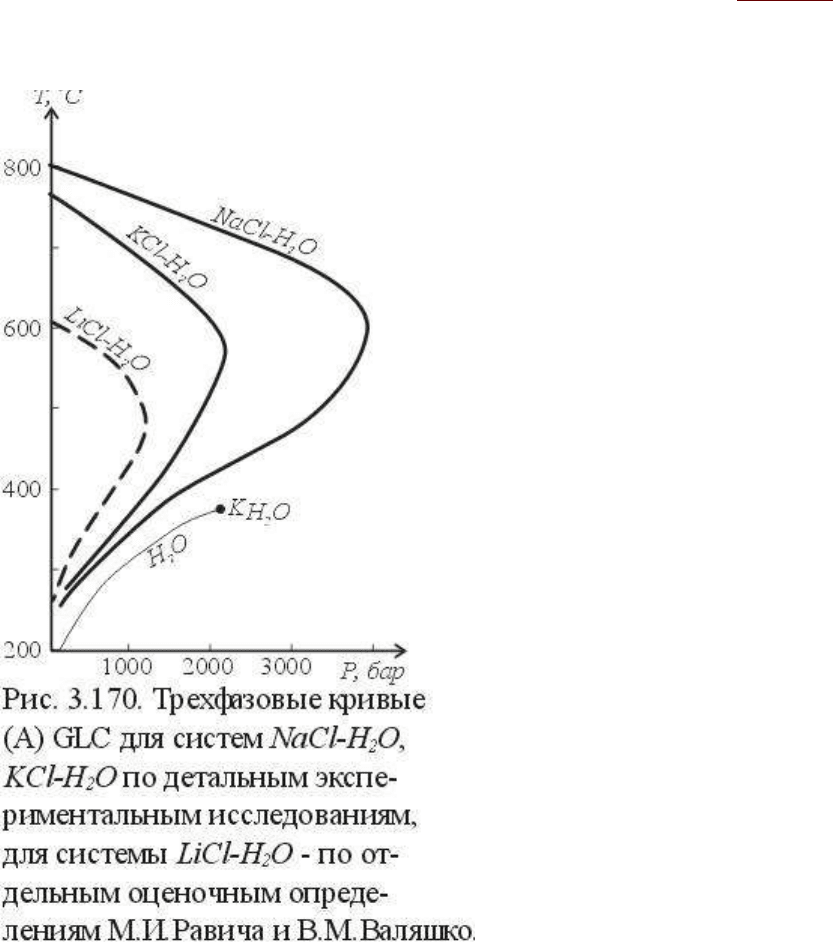
В качестве примера реальных диаграмм на рис.3.170 показано положение трехфазовых
кривых GLC (проекция на T-p плоскость) для систем H
2
O-NaCl, H
2
O-KCl, H
2
O-LiCl, по
данным М.И.Равича и В.М.Валяшко. Для наиболее интересных применительно к
геологическим процессам систем H
2
O-NaCl и H
2
O-KCl имеются достаточно полные
данные по составам газа и жидкости при различных значениях T-p трехфазовой кривой.
Эти данные, а также обширные сведения по растворимости можно найти в справочной
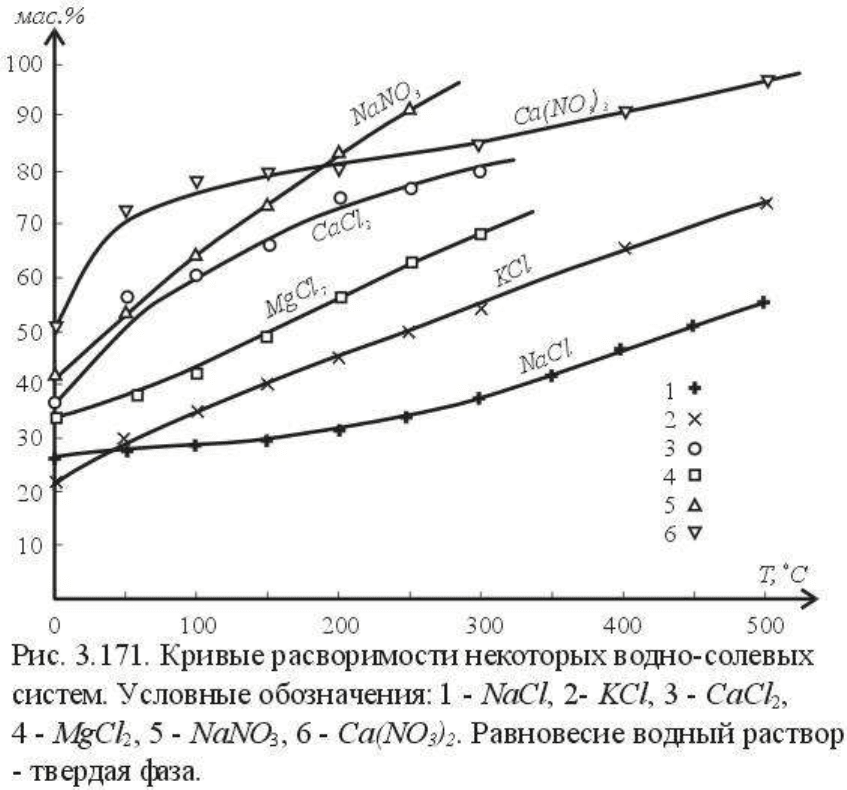
литературе (см. справочники по растворимости солевых систем). На рис.3.171 в качестве
примера (и для сравнения с системами II типа) приведены данные по растворимости
некоторых солевых систем.
Рассмотренные в этом разделе диаграммы представляют простейший тип бинарных
систем. Главные усложнения, с которыми приходится считаться при анализе природных
систем, состоят в следующем. Существование бинарных соединений, представленных
краевыми компонентами системы, например, NaPO
3
-Na
2
H
2
PO
4
-H
2
O (A) или K
2
Si
2
O
5
-
H
2
K
2
Si
2
O
6
-H
2
O (B). В первой системе соединение плавится конгруэнтно, соответственно
система имеет две эвтектические точки и на T-p проекции кроме них три
однокомпонентные нонвариантные точки с соответствующими моновариантными
кривыми (G-L, L-S и G-S), две трехфазовые кривые с максимумом давления и другие
кривые, присущие диаграммам с летучими (в зависимости от T, p координат точек
фазовых переходов однокомпонентных систем строениеT-p проекций и T-x иp-x сечений
может быть достаточно сложным).
Еще более сложную топологию имеют диаграммы системы B, где бинарное соединение
(H
2
K
2
Si
2
O
6
) плавится (или растворяется) инконгруэнтно. Как отмечалось выше, для
систем с летучий-соль обычно имеется ограниченное число экспериментальных данных.
Еще меньше их для систем с соединениями. Поэтому построение диаграмм состояния
таких систем требует существенных усилий, выходящих за рамки даже повышенных
учебных программ. Общая сводка возможных топологических схем пока еще отсутствует
в литературе и заинтересованный читатель может попробовать свои силы в этом
направлении.
T-p-x диаграмма бинарной системы с критическими явлениями
Большинство систем силикат - летучий (H
2
O) относится ко второй группе водносолевых
систем, в которых при повышении температуры обязательно наступают критические
явления. Они обусловлены тем, что силикаты представляют труднорастворимые соли, и
хотя присутствие их в растворе повышает критическую температуру раствора,
растворимость оказывается недостаточной, чтобы воспрепятствовать вскипанию раствора
и обеспечить непрерывный переход раствора в расплав (как это наблюдается в водно-
солевых системах I типа). Признаком систем второй группы является уменьшение
растворимости в каком-то интервале возрастающих температур. Аномальное поведение
растворимости фиксирует надкритические и "околокритические" состояния в системе.
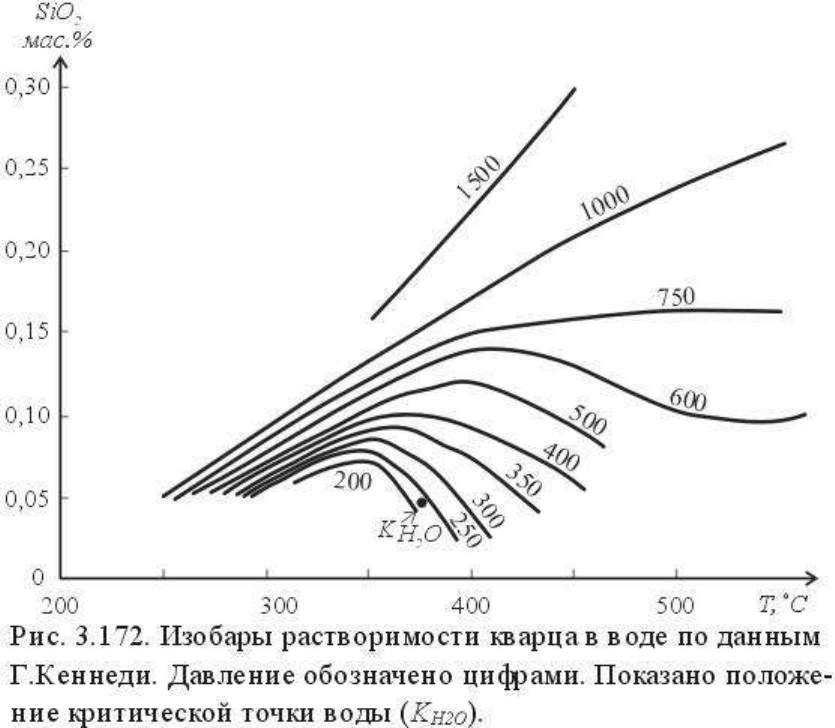
Для иллюстрации этих соотношений на рис. 3.172 приведена диаграмма растворимости
кварца в воде при различных температуре и давлении. Давление обозначено цифрами на
соответствующих изобарах растворимости. Анализируя диаграмму растворимости SiO
2
(рис. 3.172) и сравнивая ее с кривыми растворимости в водно-хлоридных системах
(рис.3.171), отметим следующее, главное. Для легкорастворимых солей (3.171)
повышение температуры вызывает увеличение концентрации солей в растворе вплоть до
чистого расплава соли. В системах с трудно растворимыми соединениями, каким является
SiO
2
, положительная зависимость растворимости от температуры во всем интервале
температур наблюдается только при достаточно высоких давлениях - 1000 бар и более, т.е.
в условиях, при которых вода сохраняет свойства жидкости и при высоких температурах.
При более низких давлениях кривая растворимости (см. на рис.3.172 изобару 600 бар)
приобретает характерный S-образный вид: при низких температурах она имеет
положительный наклон, при околокритических значениях - имеет максимум и затем
растворимость падает тем существенней, чем ближе изобара растворимости к
критической. При дальнейшем повышении температуры изобары растворимости проходят
через минимум и снова приобретают положительный наклон. На экспериментальной
диаграмме Г.Кеннеди это хорошо видно лишь для изобары 600 бар, для меньших
давлений исследованы только область максимума и отрицательный наклон изобар,
фиксирующих переход к надкритическому состоянию.
Рассмотрим топологию и физико-химические особенности диаграмм летучий (A) -
труднорастворимая твердая фаза (B) подробнее, используя T-p-x проекции,
изотермические и изобарические сечения, подобно тому, как это было сделано для систем
I типа. Системы II типа - с критическими явлениями - в геохимической и петрологической
литературе нередко называют силикат (B) - летучий (A), подразумевая в качестве летучего
H
2
O), хотя конечно критические явления наблюдаются и в других водно-солевых
системах, в системах с другими летучими. Просто для понимания процессов магматизма
первостепенное значения имеет модельная система силикат или алюмосиликат - вода.
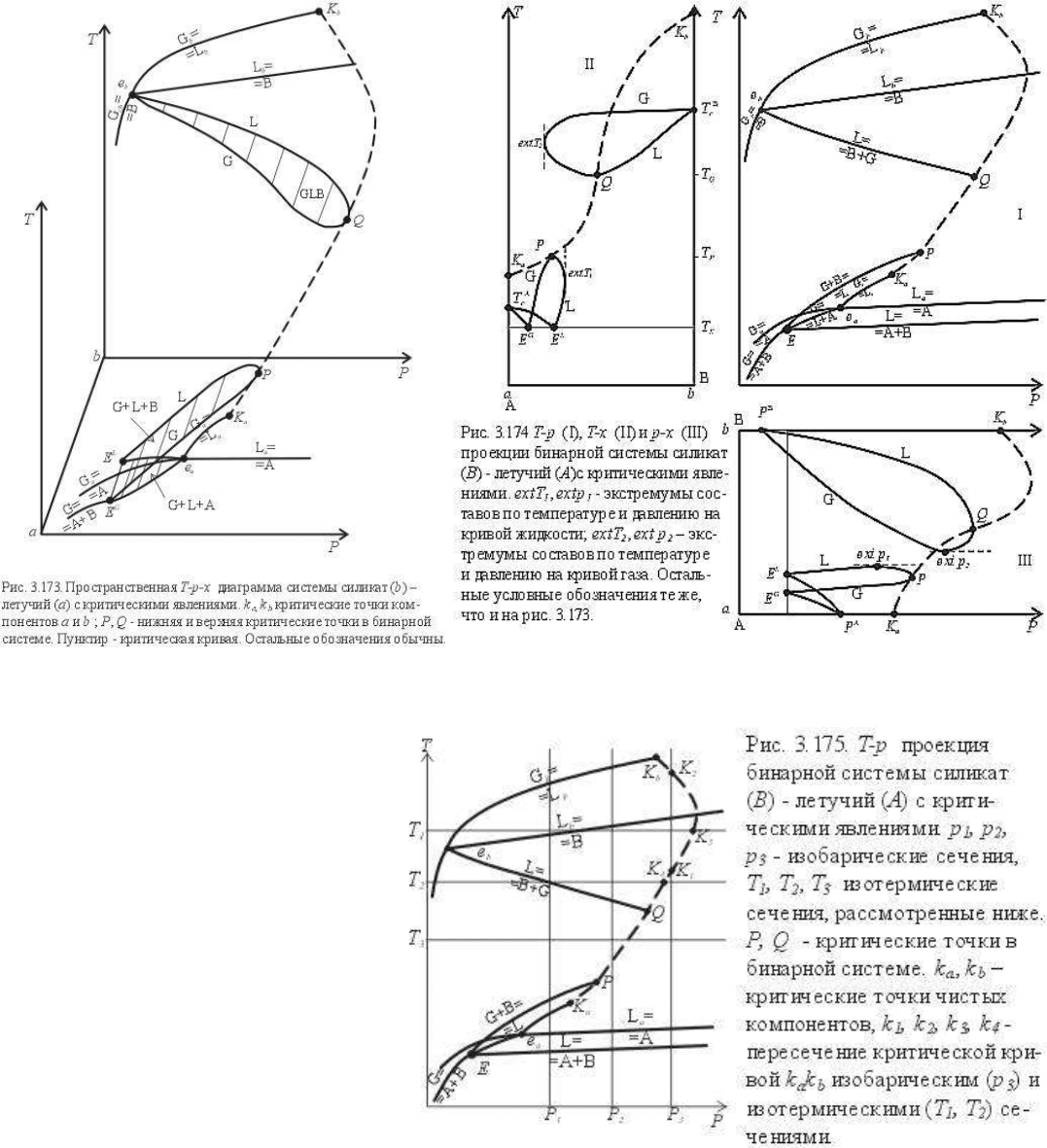
На рис.3.173 приведена пространственная T-p-x диаграмма бинарной системы силикат (b)-
летучий (a). На рис.3.174 показаны три проекции этой пространственной диаграммы на
плоскости T-p (I), T-x (II) и p-x (III). Приведенные на рис.3.173, 3.174 (и ниже, на
рис.3.175, 3.176 и 3.177) диаграммы представляют схемы диаграмм силикат-летучий. Для
наглядности изображения положение эвтектических точек E
G
и E
L
, кривых составов газа и
