Шендрик А.Н. Химия белка. Структура, свойства, методы исследования
Подождите немного. Документ загружается.

222
Для получения более надежных значений величины s и D измеряют в рас-
творах с различной концентрацией белка и экстраполируют на бесконечное
разбавление. Определенные так коэффициенты седиментации называются кон-
стантами седиментации - s
0
.
Метод измерения скорости седиментации приводит к ошибочным резуль-
татам, если форма частиц сильно отклоняется от сферической. Особенно, если
это длинные, тонкие, палочковидные молекулы. Кроме того, при вычислении
молекулярной массы по уравнению Сведберга возникают довольно значитель-
ные погрешности из-за неточностей в определении величин v. Точное измере-
ние v на небольших образцах белков почти невозможно.
4.4.7.3 Метод седиментационного равновесия
В методе седиментиационного равновесия подбирается такая скорость
вращения ротора центрифуги, при которой противодействующие друг другу
силы седиметации и диффузии уравновешены. В состоянии устоявшегося рав-
новесия в зоне мениска отсутствует зона чистого растворителя. Вдоль центри-
фужной пробирки устанавливается градиент концентрации белка. В нижнем
слое концентрация белка может быть примерно в 2 раза больше, чем в верхнем.
Измеряя концентрацию белка на различных расстояниях от оси вращения мож-
но рассчитать его ММ по уравнению:
М = 2RTln(с
2
/с
1
)/ω
2
(1 - vρ)(r
2
2
- r
1
2
)
где с
2
и с
1
- концентрации белка в пробирке на расстояниях r
2
и r
1
соответст-
венно от оси вращения.
В данном случае расчет ММ не требует знания величины коэффициента диф-
фузии. Кроме того, в методе седиментационного равновесия не вводятся ника-
кие поправки на форму частиц. Все это обеспечивает рассмотренному методу
наиболее высокую точность среди седиментационных. Основной недостаток -
это очень большие затраты времени. Иногда для установления равновесия рас
223
твор приходится непрерывно центрифугировать на протяжении нескольких су-
ток. Этот процесс можно ускорить, используя кюветы с очень небольшой высо-
той столба жидкости. Кроме того, метод седиментационного равновесия очень
критичен к чистоте белка и его гомогенности.
4.4.7.4 Метод приближения к седиментационному равновесию
Этот метод - есть компромисс между двумя вышерассмотренными мето-
дами. В нем нет присущей методу седиментационного равновесия точности, но
достигнут существенный выигрыш во времени проведения измерений. В мето-
де седиментационного равновесия требуются прецизионные измерение и под-
держание скорости вращения ротора. В методе приближения к седиментацион-
ному равновесию скорость вращения ротора доводится до равновесной на про-
тяжении 1 - 2 часов путем ряда последовательных подгонок (приближений).
Каждый раз при этом измеряют концентрацию белка у дна кюветы. Из этих
данных экстраполяцией определят ММ белка.
Метод центрифугирования в градиенте плотности. Этот метод полу-
чил широкое распространение не только для определения констант седимента-
ции, но и для разделения смесей макромолекул, органелл и вирусов. Есть два
варианта центрифугирования в градиенте плотности. В одном из них в центри-
фужной пробирке создается градиент плотности сахарозы. Достигают этого
смешением автоматическими насосами концентрированного раствора сахарозы
с водой в постепенно уменьшающихся соотношениях. Поверх раствора с гради-
ентом наслаивают смесь макромолекул, растворенных в легком растворителе.
При центрифугировании в качающемся горизонтальном роторе («бакет-
роторе») макромолекулы каждого типа осаждаются вдоль градиента плотности
с характерной для них скоростью. Она определяется в основном массой частиц.
В результате осаждения образуются полосы или зоны. Хорошее разделение
достигается быстро. Константу седиментации белка определяют исходя из по
224
ложения его полосы в градиенте по отношению к положениям полос «белков-
маркеров», константы седиментации для которых известны.
Вторая модификация метода для определения молекулярной массы не
применяется. Однако она весьма эффективна как способ разделения макромо-
лекул с различными плотностями. В этом случае градиент концентрации зара-
нее не создают. В качестве среды используют 6М раствор CsCl. Он обладает
большой растворимостью, а его высококонцентрированные растворы малой
вязкостью. В мощном гравитационном поле CsCl сам подвержен слабой седи-
ментации, что и приводит к появлению градиента концентрации CsCl. Для ус-
тановления этого градиента требуется обычно довольно продолжительное вре-
мя: от нескольких часов до нескольких суток. Распределение плотности вдоль
пробирки можно определить с высокой точностью. После центрифугирования
со смесью белков они распределяются вдоль градиента плотности на полосы.
При этом, каждая из полос оказывается в той части пробирки, в которой плот-
ность раствора CsCl совпадает с плотностью белка. Такое центрифугирование
обладает очень высокой разрешающей способностью и особенно успешно при-
меняется при разделении смесей нуклеиновых кислот.
4.4.7.5 Диффузия и коэффициент диффузии
При смешении двух газов или жидкостей их молекулы стремятся распре-
делиться по всему объему сосуда. Если разделить сосуд на две части непрони-
цаемой перегородкой и одну половину сосуда заполнить одним веществом, а
вторую другим, то после удаления перегородки молекулы обоих веществ нач-
нут распространяться по всему сосуду. Процесс это носит названия диффузии.
Направление диффузии всегда одно и то же: со стороны с большей концентра-
цией компонента в сторону с его меньшей концентрацией, т.е. вдоль градиента
концентрации. В простейшем случае скорость линейной диффузии описывается
первым законом Фика:
225
ds/dt = -Da(dc/dx)
Этот закон гласит, что количество растворенного вещества (ds), диффунди-
рующего за время dt через площадку А, расположенную перпендикулярно на-
правлению диффузии, пропорциональна градиенту концентрации (dc/dx) в этом
направлении. Коэффициент пропорциональности - D, называется коэффициен-
том диффузии. Он определяется как количество вещества, диффундирующего
через поверхность площадью [1 ед.длины]
2
при градиенте концентрации рав-
ном единице. Поскольку диффузия протекает в направлении меньшей концен-
трации в уравнении закона Фика стоит знак минус.
Коэффициенты диффузии белков определяют в диффузионных кюветах,
путем измерения скорости перемещения границы раздела белок-растворитель.
Такая граница создается в диффузионной кювете посредством осторожного на-
слоения растворителя на раствор белка. За движением границы следят оптиче-
ски. В случае очень больших белковых молекул имеется некоторая зависимость
скорости диффузии от ММ. Однако эта зависимость выражена слабо. Так, на-
пример, ММ сывороточного альбумина в 2 раза больше ММ β-лактоглобулина.
В то же время различие в их коэффициентах диффузии составляет всего 16%.
По этой причине непосредственное определение D, строго говоря, не позволяет
определять ММ с достаточной точностью. Но знание его необходимо для опре-
деления ММ по скорости седиментации (см.выше).
4.5 Методы разделения белков
4.5.1 Электрофорез
В 1809 г. проф. Московского университета О.Ю.Рейс впервые описал за-
кономерности движения заряженных частиц коллоидных растворов в электри-
ческом поле, заложив тем самым основы современного электрофореза (ЭФ). В
настоящее время электрофорез (более раннее название катафорез) широко при-
меняют для изучения коллоидных систем и белковых растворов. Перемещение
226
ионов низкомолекулярных электролитов в электрическом поле называют ионо-
форезом.
Электрофорез подразделяют на преперативный и аналитический. Препа-
ративный ЭФ используют для выделения относительно больших количеств ма-
териала. Аналитический - в исследовательских целях: контроль чистоты; анализ
состава смесей и т.д.
Кроме того ЭФ подразделяют на макроэлектрофорез (разделение более
100 мг вещества); микроэлектрофорез (разделение менее 1мг вещества); полу-
микроэлектрофорез (разделение 1-10мг вещества); низковольтный (до 1000В);
высоковольтный (более 1000В).
Методом ЭФ можно разделять белки, нуклеиновые кислоты, полисахари-
ды, ферменты, токсины, фосфорные эфиры, бактериальные антигены, вирусы,
витамины, антибиотики, алкалоиды и ряд других веществ.
В современных практических методах анализа, основанных на электро-
форезе, движение вещества происходит в жидкой буферной среде, которая
удерживается инертным твердым носителем. В качестве таковых используют-
бумагу или гели. Жидкая среда выполняет роль проводника в наложенном на
нее из вне электрическом поле.
4.5.2 Физические основы электрофореза белков
Электрические заряда на молекулах белков в растворе возникают либо в
результате диссоциации ионогенных групп, либо при адсорбции ионов из рас-
твора на поверхности больших молекул. В результате этого образуется двойной
электрический слой. Этот слой состоит из заряженной поверхности коллоидной
или белковой частицы и тонкой ионной пленки (ионной атмосферы), образо-
ванной средой вокруг частицы. Заряды на поверхности частицы и в ионной ат-
мосфере имеют различную полярность. Смотри рис. ниже.
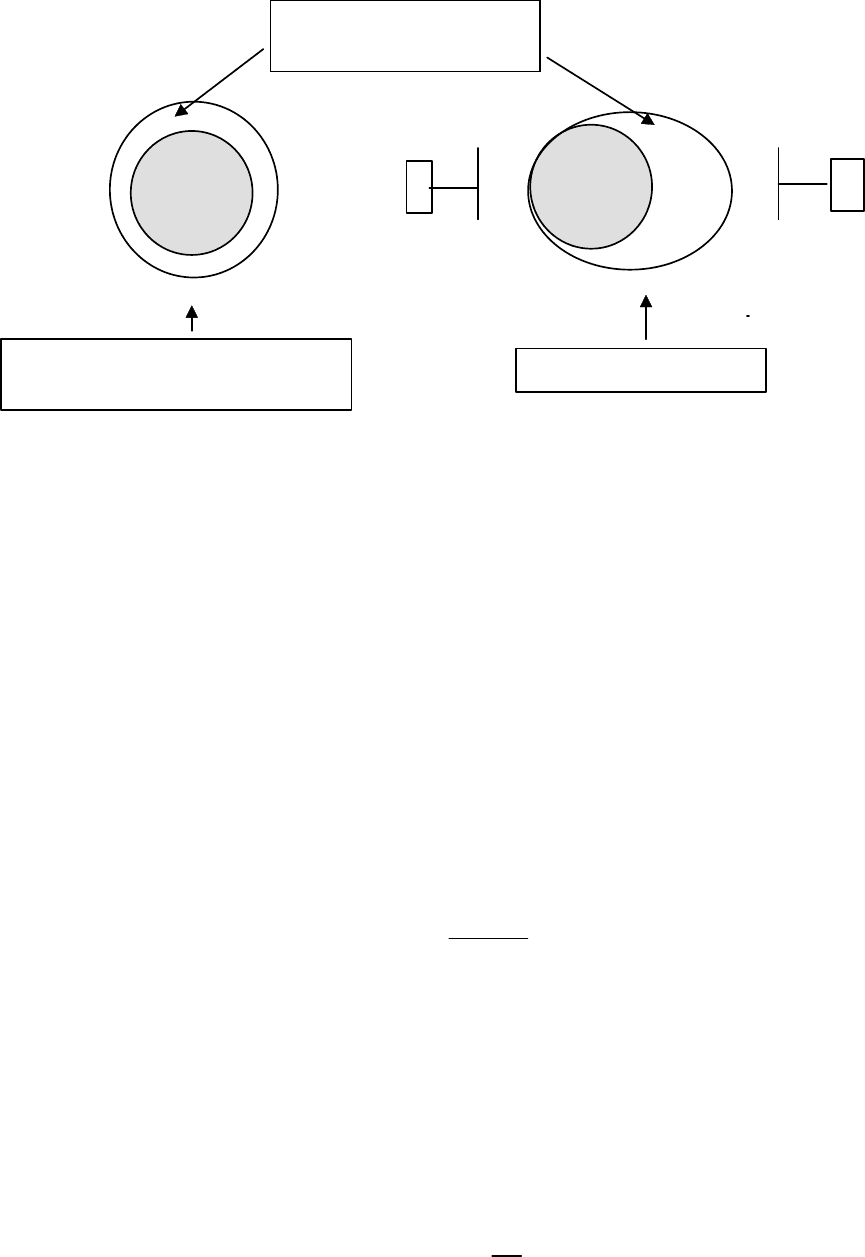
227
+
+
-
-
-
-
-
-
-
-
-
-
Двойной электрический
слой
+
-
В отсутствии электрического
поля
В электрическом поле
+
+
+
+
+
+
+
+
Во внешнем электрическом поле частица и окружающая ее ионная атмо-
сфера движутся в противоположных направлениях, поскольку имеют разные
заряды. Это создает электрофоретическое трение, которое тормозит движение
частицы.
Подвижность заряженной частицы (иона) в электрическом поле называется
электрофоретической подвижностью. Для сферической частицы в предельно
разбавленном растворе (идеальный случай, отсутствие межмолекулярных
электростатических взаимодействий между ионами) электрофоретическая
подвижность (µ) выражается формулой:
µ
πη
=
Q
r
U
6
где Q - суммарный заряд частицы, r - радиус частицы, η - вязкость среды, в ко-
торой движется ион, U - разность потенциалов (приложенное напряжение).
Из уравнения видно, что в одной и той же среде (η=const) при одинако-
вом напряжении (U=const) подвижности ионов пропорциональны отношению
заряда к их радиусу:
µ∝
Q
r
Это соотношение лежит в основе метода электрофоретического разделе-
ния смесей заряженных частиц, имеющих различные подвижности.
228
4.5.3 Экспериментальные методы электрофореза
Существует три основных разновидности ЭФ:
¾ фронтальный;
¾ зональный ;
¾ стационарный.
При фронтальном ЭФ электрическое поле прикладывается к системе, ко-
гда в ней имеется сформировавшаяся отчетливая граница между раствором за-
ряженных частиц и средой (растворитель, буферная смесь). В процессе ЭФ гра-
ница перемещается.
Зональный ЭФ основан на применении пористой стабилизированной сре-
ды (бумага, гель, блоки гранулированного материала). При электрофорезе мо-
лекулы одного типа группируются по зонам.
Стационарный (или вытесняющий) ЭФ характеризуется тем, что через
некоторое время после начала разделения устанавливается состояние равнове-
сия.
Рассмотрим детальнее перечисленные выше типы электрофоретического
разделения на примерах белковых смесей.
В 20-30 годах прошлого столетия были выполнены интенсивные иссле-
дования электрохимических свойств белков. Они позволили установить, что
молекулы белка представляют собой амфотерные полиэлектролиты, т.е. они не-
сут на себе одновременно положительный и отрицательный заряд. В приложе-
нии к белкам термин «амфотерный» означает, что они титруются как кислота-
ми, так и щелочами. Иными словами, молекула белка в довольно больших ин-
тервалах рН несет на себе одновременно положительные и отрицательные за-
ряды. А в очень кислых средах (рН ≅ 1) практически все белки имеют макси-
мальный положительный заряд. В сильно щелочных (рН ≅ 13) - максимальный
отрицательный. Есть, правда, исключения. Гистоны, например, имеют положи-
тельный заряд даже при рН = 11.
229
Различие в зарядах белковых молекул впервые было использовано для
разделения их смесей шведским исследователем Арне Тизелиусом в 1937г. Он
сконструировал первый прибор для проведения электрофореза. За достижения в
области электрофореза Тизелиус в 1948г был награжден Нобелевской премией.
Долгое время электрофорез оставался практически единственным коли-
чественным методом анализа белков. Он и сейчас весьма широко используется,
хотя и уступает современным физико-химическим методам. В частности, хро-
матографии, гель-фильтрации, ультрацентрифугированию, центрифугированию
в градиенте плотности.
В молекулах белков содержатся как основные, так и кислотные ионизи-
рующиеся группы: карбоксильные, спиртовые, аминогруппы, гуанидиновые,
фенольные, имидазольные, тиольные. Это ионогенные группы. Для каждого
белка существует совершенно определенное значение рН среды, при котором
суммарный заряд белковой молекулы равен нулю. Это изоэлектрическая точка
(ИЭТ). В этой точке в молекуле белка содержится равное количество положи-
тельных и отрицательных зарядов. Это важно четко понимать. Нулевой заряд
означает в данном случае не отсутствие зарядов, а равенство положительно и
отрицательно заряженных групп в одной и той же молекуле. При значениях рН
выше ИЭТ белок несет суммарный отрицательный заряд, а ниже ИЭТ - сум-
марный положительный. Белки сыворотки крови, в большинстве своем, имеют
ИЭТ в области рН = 4-6. В электрическом поле положительно заряженные час-
тицы движутся к катоду, а отрицательные к аноду.
4.5.3.1 Фронтальный электрофорез
Метод фронтального ЭФ (его называют еще методом движущейся грани-
цы) создал Тизелиус, разработав специальную кювету. Суть метода в следую-
щем. В U-образную прозрачную ячейку помещают раствор белка. Поверх рас-
твора осторожно наслаивают чистый буфер. Затем при постоянной температуре

230
и в условиях, исключающих вибрацию, на систему накладывают электрическое
поле.
При перемещении белка под действием поля из раствора в зону чистого
буфера создается граница, которая движется в направлении одного из электро-
дов (в зависимости от заряда белковой молекулы). На этой границе наблюдает-
ся резкое изменение показателя преломления. Оно обусловлено тем, что пока-
затели преломления чистого буфера и раствора белка в буфере различны. На
основании данных измерений градиента показателя преломления вдоль ячейки
при помощи специального оптического метода, называемого шлирен-методом
строят электрофореграмму (см. рис.)
+
-
2
1
Восходящая
граница
Нисходящая
граница
Растворенный в быфере
белок
1 - Чистый буфер
2 - Первоначальная
граница
Электрофореграмма
смеси трех белков

231
Каждый пик на электрофореграмме соответствует положению движущейся
границы определенного белка. С максимумом концентрации белка он не
совпадает.
В последнее время вариант электрофореза по Тизелиусу практически не
используется. Его заменили более совершенные и более удобные методики.
4.5.3.2 Электрофорез на бумаге
Аминокислоты, пептиды и белки можно анализировать методом электро-
фореза на бумаге. Наилучшие результаты получаются при использовании на-
пряжений до 1 кВ.
Методика электрофореза проста. Полоску или лист хроматографической
бумаги равномерно увлажняют токопроводящим буферным раствором. Закреп-
ляют в специальной ванночке между двумя электродными отделениями, кото-
рые заполнены токопроводящим раствором (см. рис.4.4).
А
Рис. 4.4
Принципиальная схема установки для низковольтного (А) и высоковольтного (Б) электро-
фореза на бумаге.
1 - крышка; 2- полоска бумаги; 3 - вода для поддержания постоянной величины насыщенных
паров; 4,5 - кюветы с буферным раствором; 6 - токопроводящий фитиль; 7 - охлаждающие
пластины; 8 - заполненный воздухом мешок.
