Платэ Н.А., Сливинский Е.В. Основы химии и технологии мономеров
Подождите немного. Документ загружается.

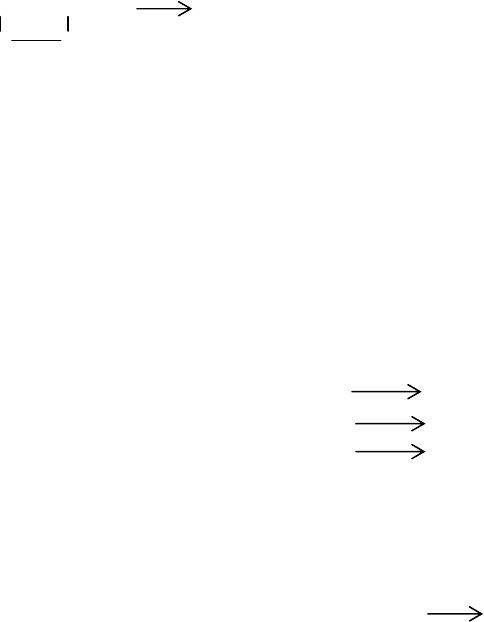
261
Далее
-пропиолактон гидролизуют водой сначала при 373-423 К, а затем
при 533 К:
H
2
O
CH
2
—CH
2
CH
2
=CH-COOH.
O CO
Фирма "Селаниз" осуществляет гидролиз лактона через промежуточную
стадию его полимеризации при 323 К под вакуумом в присутствии фосфорной
кислоты.
7.3.6. Окислительное карбонилирование этилена
Процесс, разработанный фирмой "Юнион Ойл", осуществляется в жидкой
фазе при 408-423 К и давлении 7,5 МПа в присутствии каталитической системы
хлоридов палладия и меди. При этом протекают
следующие реакции:
CH
2
=CH
2
+ PdCl
2
+ H
2
O + CO CH
2
=CH—COOH + Pd + 2HCl,
Pd + 2CuCl
2
2CuCl + PdCl
2
,
2CuCl + 2HCl + 0,5O
2
H
2
O + 2CuCl
2
Каталитическая система содержит в качестве добавок хлориды лития, на-
трия, рения и др. В качестве побочного продукта образуется 2-
ацетоксипропионовая кислота, использующаяся как растворитель:
CH
2
=CH
2
+ CO + 0,5O
2
+ CH
3
COOH CH
3
COOCH
2
CH
2
COOH.
Эту кислоту можно термически разложить на уксусную, винилацетат, ацеталь-
дегид, акриловую и пропионовую кислоты, диоксид углерода.
7.4. МЕТАКРИЛОВАЯ КИСЛОТА
Метакриловая кислота (2-метилпропеновая кислота) СН
2
=С(СН
3
)-СООН
– бесцветная жидкость с резким запахом; т. пл. 289 К, т. кип. 435-436 К. Рас-
творима в воде, спиртах, эфирах, углеводородах. При хранении она полимери-
зуется, ингибитор полимеризации – метиловый эфир гидрохинона.
Метакриловые мономеры известны в промышленности уже около 70 лет,
но расширение их производства тормозилось высокой стоимостью и трудоем-
костью применяемых методов получения
. Однако в связи с необходимостью
утилизации дешевой синильной кислоты, образующейся в значительных коли-
чествах в качестве побочного продукта в производстве акрилонитрила окисли-
тельным аммонолизом пропилена, мощности по производству метакриловых
мономеров значительно увеличились.
В настоящее время метакриловую кислоту и метилметакрилат получают
в промышленности через промежуточное образование ацетонциангидрина.
Этот метод был разработан
английской фирмой "АйСиАй" еще в 1937 г. и в те-
чение всего периода эксплуатации непрерывно усовершенствовался.

262
Недостатки ацетонциангидринного способа стимулируют постоянный
поиск новых промышленных способов получения метакриловой кислоты и ме-
такрилатов с использованием других видов сырья, например изобутилена.
Синтез метакриловой кислоты газофазным окислением изобутилена осу-
ществляют в две стадии: сначала изобутилен окисляют до метакролеина, кото-
рый затем окисляют непосредственно в метакриловую кислоту.
7.4.1. Газофазное окисление
изобутилена
Газофазное окисление изобутилена до метакролеина осуществляют над
смешанными оксидными катализаторами при 573-723 К:
CH
2
=C—CH
3
CH
2
=C—CHO CH
2
=C—COOH
CH
3
CH
3
CH
3
Метакролеин
Как правило, катализаторы промотируют щелочными или щелочнозе-
мельными металлами, а также соединениями сурьмы и олова. Например, в про-
цессе фирмы "Сумитомо" на катализаторе состава
Mo
12
Co
4
Bi
1
Ni
4,5
Fe
1
Te
0,6
P
0,1
O
48,6
при 435 К и мольном соотношении изобути-
лен:кислород:азот, равном 1:3:27, выход метакролеина составил 88% при се-
лективности 79% и степени конверсии 99%. Практически все катализаторы
окисления изобутилена в метакролеин являются оксидными полиметалличе-
скими системами и содержат, как правило, в своем составе оксид молибдена.
Из других элементов, входящих в большинство запатентованных катализаторов
окисления изобутилена,
следует отметить ванадий, сурьму, теллур, висмут, же-
лезо, кобальт, таллий, никель и др. Эти катализаторы обеспечивают конверсию
изобутилена на уровне 90-98% и селективность окисления-75-90%.
7.4.2. Окисление метакролеина
Синтез метакриловой кислоты окислением метакролеина может быть
осуществлен в газовой или жидкой фазе в присутствии катализатора:
CH
2
=C—CH
3
CH
2
=C—COOH
CH
3
CH
3
Основной проблемой при разработке этого процесса является поиск ак-
тивного, селективного и стабильного катализатора. Эта задача может быть ре-
шена двумя способами: использованием на стадии окисления метакролеина ак-
тивных катализаторов окисления акролеина и применением новых катализато-
ров окисления метакролеина.
Более высокая реакционная способность изобутилена по сравнению с
пропиленом создает
значительные сложности при проведении высокоселектив-
O
2
O
2
-H
2
O
O
2

263
ного процесса окисления. Метакролеин также легко подвергается окислению,
но селективное его окисление в метакриловую кислоту представляет достаточ-
но сложную задачу.
7.4.3. Газофазное окисление метакролеина
Для окисления метакролеина используют преимущественно катализаторы
на основе фосфорномолибденовой кислоты с добавкой соединений щелочных
или щелочноземельных металлов, таллия, сурьмы, и др. Эти катализаторы
обеспечивают конверсию метакролеина на уровне 80-90% и селективность
окисления в метакриловую кислоту 75-90%. Процесс реализован фирмой "Аса-
хи рапаси" (Япония). Окисление осуществляют в трубчатых реакторах специ-
альной конструкции во избежание смешения метакролеина с кислородом до зо-
ны катализатора, поскольку при температуре выше 593 К происходит автоокис-
ление в отсутствие катализатора. Процесс проводят при 623-673
К. В качестве
катализаторов окисления метакролеина могут быть использованы соединения
на основе молибдена и фосфора, молибдена и теллура, молибдена и никеля.
Степень конверсии метакролеина составляет 95% при селективности по метак-
риловой кислоте 95-97%.
7.5. АКРИЛАТЫ
Эфиры акриловой кислоты – акрилаты – получают в основном следую-
щими способами:
- этерификация акриловой кислоты;
- переэтерификация;
- получение
из этиленциангидрина;
- реакция Реппе на основе ацетилена, оксида углерода и спирта;
- конденсация кетена с формальдегидом;
- гидролиз акрилонитрила и этерификация полученного продукта.
7.5.1. Получение акрилатов
этерификацией акриловой метакриловой кислот
Этерификация спиртами в присутствии серной кислоты
Одним из основных методов получения эфиров акриловой и метакрило-
вой кислот является
прямая этерификация кислот спиртами, например:
CH
2
=CH—COOH + CH
3
CH
2
OH CH
2
=CH-COO-CH
2
СH
3
+ H
2
O
H
298
= 35 кДж/моль
В отсутствие катализатора этерификация обычно протекает очень мед-
ленно, поэтому в большинстве случаев процесс осуществляют каталитически. В
качестве катализаторов применяют кислоты, ионообменные смолы, соли, окси-
264
ды и др. Реакцию можно проводить в жидкой или паровой фазе при повышен-
ных температуре и давлении.
Роль кислого катализатора заключается в активации карбонильной груп-
пы кислоты. При взаимодействии протона катализатора с карбонильным кисло-
родом кислоты полярность ее карбонильной группы возрастает.Углерод с по-
ниженной электронной плотностью притягивает электроны
атома кислорода из
ОН-группы, из-за чего атом водорода кислоты легче отщепляется.Поэтому мо-
лекула карбоновой кислоты становится более реакционноспособной. Поскольку
взаимодействие кислот со спиртами каталитически ускоряется ионами водоро-
да, то каждая карбоновая кислота является катализатором собственной этери-
фикации, т.е. эта реакция является автокаталитической.
Этерификацию акриловых кислот спиртами проводят
в жидкой фазе, под
вакуумом (остаточное давление 20-100 кПа) при 343-373 К.
Использование серной кислоты в качестве катализатора этерификации
имеет ряд недостатков с точки зрения как технологии, так и гигиены труда. На-
пример, серная кислота вызывает дегидратацию спиртов до олефинов, способ-
ствует образованию простых эфиров из спиртов, сульфирует ненасыщенные со-
единения, приводит
к осмолению и обугливанию органических соединений. В
результате достижение количественного выхода сложных эфиров в присутст-
вии серной кислоты сильно затруднено.
Для снижения побочных реакций вместе с серной кислоты предложено
вводить антиоксиданты, например, 2,4-димел-6-трет-бутилфенол, 2,5-ди-
трет-бутилгидрохинон или пероксиды, которые одновременно сокращают и
продолжительность реакции.
Этерификация спиртами в присутствии
ионообменных смол
Эффективными гетерогенными катализаторами этерификации акриловой
и метакриловой кислот являются ионообменные смолы. Скорость реакции в
присутствии катионных ионообменных смол - сложная функция многих пара-
метров, влияние которых иногда не симбатно. Например, с повышением темпе-
ратуры уменьшается сорбционная емкость смол, от которой зависит концен-
трация реагирующих веществ внутри частицы смолы. Для
этерификации кар-
боновых кислот используют, например, отечественные катиониты КУ-1, КУ-2,
КУ-2/8 и другие сульфокатиониты. Реакцию осуществляют в реакторе трубча-
того типа при 373-408 К.
В связи с ограниченной термостойкостью катионитов (423-453 К) в орга-
нических средах процесс проводят под давлением около 0,78-1,18 кПа, что спо-
собствует повышению выхода эфира до 90%.
Преимущества ионообменных смол по
сравнению с гомогенными катали-
заторами заключаются в легкости отделения реакционной массы от катализато-
ра, селективности действия ионитов, т.е. в образовании эфиров с высоким вы-

265
ходом и хорошим качеством. Кроме того, при применении ионитов не требует-
ся отмывки продукта и исключается или уменьшается коррозия аппаратуры.
Этерификация олефинами
По этому методу в промышленности эфиры акриловой и метакриловой
кислот получают в результате взаимодействия свободной кислоты с олефинами
согласно схеме:
CH
2
=CH—COOH + CH
2
=CHR CH
2
=CH—COO-CH
2
CH
2
R
Этерификация кислот олефинами имеет преимущества по сравнению с
этерификацией кислот спиртами: исключается стадия получения спиртов из
олефинов; катализаторы процесса этерификации являются более эффективны-
ми; отсутствует необходимость отделения воды; при большом избытке олефина
получается эфир высокой степени чистоты.
7.5.2. Получение акрилатов переэтерификацией
Переэтерификация является одним из основных методов синтеза одних
эфиров
с помощью других в присутствии катализатора, в качестве которого
применяются кислые и основные катализаторы, алкоголяты и феноляты щелоч-
ных или щелочноземельных металлов, соединения титана, галлия и ионнооб-
менные смолы.
Реакция переэтерификация протекает согласно уравнению
CH
2
=CH-COOR + ROH CH
2
=CH-COOR + ROH.
Переэтерификация в присутствии кислотных катализаторов
Поскольку кислотные катализаторы в реакции переэтерификации не-
сколько более эффективны, чем щелочные, то обычно для этой цели применяют
серную кислоту. Именно таким образом реализованы реакции переэтерифика-
ции метилметакрилата гексиловым, н-цетиловым, н-дециловым и другими
спиртами.
На процесс переэтерификации влияют такие факторы, как
мольное соот-
ношение исходных реагентов, продолжительность реакции, природа и количе-
ство катализатора и ингибитора, температура реакции. Процесс проводят при
избытке исходного эфира. По мере проведения реакции удаляют азеотропную
смесь выделившегося спирта и исходного эфира, а оставшийся исходный эфир
удаляют под вакуумом. В качестве ингибитора полимеризации используют
преимущественно гидрохинон, а также фенол
, серу, -нафтол, п-
гидроксидифениламин, N,N–ди-2-(1,4-нафтохинонил)-п-фенилендиамин. Полу-
ченные эфиры необходимо отмыть от катализатора и ингибитора, что затрудня-
ется образованием стойких эмульсий, препятствующих разделению фаз.

266
Переэтерификация в присутствии ионообменных смол
При использовании кислотных катализаторов переэтерификации приме-
няется кислотостойкая аппаратура. Для удаления катализаторов из продуктов
реакции смесь нейтрализуют и промывают, что приводит к усложнению про-
цесса и образованию большого количества сточных вод. Применение ионооб-
менных смол в качестве катализаторов устраняет эти недостатки.
В промышленности реализованы
процессы переэтерификации метилак-
рилата бутанолом с получением бутилакрилата, выход которого достигает 93%
(в расчете на спирт), метилметакрилата гептиловым и нониловым спиртами. В
качестве катализатора используют отечественный катионит КУ-2/8 или другие
аналогичные сульфокатиониты.
Переэтерификация в присутствии других катализаторов
Фирма "Калифорния Рисерч Ко"(США) запатентовала процесс получения
алкиловых эфиров метакриловой кислоты переэтерификацией
метилметакрила-
та спиртом в присутствии метилата натрия.
Однако алкоголяты щелочных металлов с высокой реакционной способ-
ностью катализируют в условиях переэтерификации и ряд побочных реакций:
присоединение спирта по двойной связи, осмоление реагентов, омыление ме-
такрилового спирта с образованием метакрилата натрия, полимеризацию ис-
ходных и конечных продуктов. Работа с алкоголятами щелочных металлов
в
связи с их огне- и взрывоопасностью требует особых мер предосторожности,
что осложняет их применение в промышленности.
Предлагается также использовать в качестве катализаторов алкоголяты
щелочноземельных металлов. По своей активности они не уступают алкоголя-
там щелочных металлов и в то же время вследствие меньшей реакционной спо-
собности не вызывают осмоления и окрашивания
реакционной смеси.
7.5.3. Получение акрилатов из этиленциангидрина
Процесс получения акрилатов из этиленциангидрина осуществляют в две
стадии.
На первой стадии получают этиленциангидрин из этиленоксида и си-
нильной кислоты:
CH
2
—CH
2
+ HCN HOCH
2
CH
2
CN.
O

267
На второй стадии циангидрин подвергают гидролизу и переэтерификации
в присутствии серной кислоты и спирта:
HOCH
2
CH
2
CN CH
2
=CHCONH
2
H
2
SO
4
CH
2
=CHCOOR + NH
4
HSO
4.
Реакции протекают в жидкой фазе одновременно при атмосферном дав-
лении, температуре ~ 423 К и мольном соотношении циангидрин:спирт: кисло-
та, равном 1:2:2. Выход акрилата достигает 80% в пересчете на циангидрин.
7.5.4. Получение акрилатов из ацетилена по реакции Реппе
Ацетилен, оксид углерода и спирты взаимодействуют по реакции Реппе, в
которой карбонил никеля, используемый в
стехиометрических количествах,
"поставляет" необходимый оксид углерода:
Ni(CO)
4
+ 4C
2
H
2
+ 4ROH + 2HCl 4CH
2
=CH—COOR + NiCl
2
+ H
2
.
При этом карбонил никеля вступает в реакцию в полукаталитических ко-
личествах (процесс фирмы "Ром и Хаас") или каталитических (процесс фирмы
БАСФ). Если карбонил никеля вступает в реакцию в стехиометрических коли-
чествах, то процесс происходит по радикально-цепному механизму. Он являет-
ся автокаталитическим, протекает с высокой скоростью и обычно осуществля-
ется
при 298-343 К и атмосферном давлении.
Реакция сильно экзотермична: тепловой эффект получения этилакрилата
составляет Н
295
= -250 кДж/моль.
Процесс фирмы БАСФ
В процессе фирмы БАСФ карбонил никеля используют в каталитических
количествах, поэтому реакция осуществляется в жидкой фазе в относительно
жестких условиях (температура 423-573 К, давление 3-20 МПа):
HCCH + CO + ROH CH
2
=CHCOOR H
238
=240 кДж/моль
Процесс осуществляют в две стадии: на первой стадии получают акрило-
вую кислоту, а на второй - ее этерифицируют в эфир на отдельной установке.
Процесс фирмы "Ром и Хаас"
В этом процессе стехиометрические и каталитические реакции протекают
параллельно.Источником оксида углерода является вводимый в реакцию газо-
образный оксид углерода
, и оксид углерода, "поставляемый" из карбонила ни-
келя. Реакция протекает по схеме:
ROH H
2
SO
4
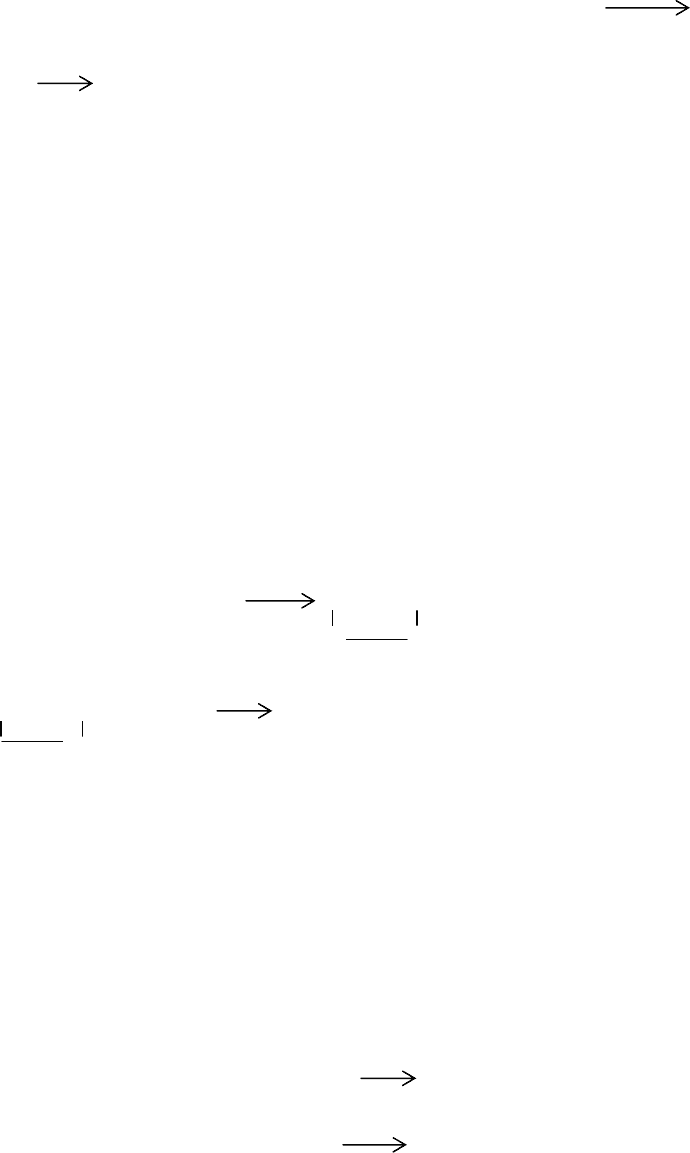
268
4C
2
H
2
+ 3,2CO + 0,2Ni(CO)
4
+ 4ROH + 0,4HCl
4CH
2
=CH—COOR + 0,2NiCl
2
+ 0,2H
2.
Процесс протекает в стационарном режиме при 303-323 К, атмосферном
давлении и мольном соотношении ацетилена и СО, равном 1:1, в реакторе с
мешалкой и циркуляцией теплоносителя для отвода тепла реакции. Для умень-
шения вязкости реакционной массы используют избыток спирта.
Выходящая из реактора жидкость охлаждается, подвергается экстракции
непрореагировавшим спиртом. Рафинат нейтрализуют карбонатом натрия для
удаления образовавшихся кислот, затем разгоняют на трех колоннах, работаю-
щих под вакуумом в присутствии ингибитора полимеризации.
7.5.5. Получение акрилатов из кетена и формальдегида
Этот способ был предложен фирмами "Селаниз" и "Гудрич" (США). В
основе способа лежат следующие реакции:
CH
2
=C=O + HCHO CH
2
—CH
2
H
238
= -190 кДж/моль,
O CO
CH
2
—CH
2
+ ROH CH
2
=CHCOOR + H
2
O H
238
= -45 кДж/моль
O CO
В настоящее время этот процесс не получил пока промышленного разви-
тия.
7.5.6. Получение акрилатов из акрилонитрила
Этот метод основан на кислотном гидролизе акрилонитрила в акриламид-
сульфат с последующей этерификацией в акрилат в присутствии спирта:
CH
2
CHCN + H
2
O + H
2
SO
4
CH
2
=CH-CONH
2
H
2
SO
4
CH
2
=CH-CONH
2
H
2
SO
4
+ ROH CH
2
=CH—COOR + NH
4
HSO
4.
Реакция протекает при атмосферном давлении при температуре около 423
К в присутствии серной кислоты в аппарате с мешалкой. Степень конверсии
акрилонитрила превышает 95-97%. Полученный на выходе продукт этерифи-
цируется при 433-453 К и атмосферном давлении в колонне с насадкой.
Общий выход акрилатов в расчете на акрилонитрил составляет 85-90%.
269
7.6 . МЕТАКРИЛАТЫ
Метилметакрилат СН
2
=С(СН
3
)-СООСН
3
является мономером для получения
важнейшего полимера – полиметилметакрилата, который используется для
производства изделий бытового и технического назначения. Термопластичный
гомополимер (органическое стекло) применяется как конструкционный мате-
риал в машиностроении (фонари, шкалы, световые отражатели, авиационные
стекла и др.), приборостроении (линзы, призмы, шкалы), в лазерной технике,
для изготовления изделий народного потребления (посуда, канцелярские при-
надлежности, пуговицы и др.), светотехнических изделий (светильники, вывес-
ки и т.д.). Суспензии полиметилметакрилата используют в производстве само-
отверждающихся пластмасс ( зубные протезы, штампы, литейные модели, абра-
зивный инструмент и прочие изделия). Дисперсии полиметилметакрилата при-
меняют как лаки для изготовления кузовов автомобилей, для отделки тканей,
волокон, бумаги, кож. Растворы полиметилметакрилата используют в
качестве
клеевых композиций. Мировое производство метилметакрилата составляет
более 1,7 млн. т/год.
Метилметакрилат и другие метакрилаты производят в промышленности
более 60 лет. Расширение производства и потребления метакриловых мономе-
ров тормозилось высокой стоимостью ацетонциангидрина и ограниченностью
ресурсов синильной кислоты.
В последние годы технология производства метакриловых мономеров
значительно обновилась. Помимо ацетонциангидринного процесса разработаны
еще
четыре способа, базирующихся на этилене, пропилене, изобутилене и изо-
бутане.
В настоящее время наибольшее распространение получили два промыш-
ленных способа синтеза метилметакрилата:
- ацетонциангидринный, основанный на реакции ацетона и циангидрина;
- процесс, основанный на получении трет-бутилового спирта и затем ме-
такролеина.
7.6.1. Получение метилметакрилата из ацетона и циангидрина
Этот метод был
разработан английской фирмой "АйСиАй" в 1937 г. Про-
цесс получения метилметакрилата осуществляют в четыре стадии: получение
циангидрина; конденсация ацетона и циангидрина до ацетонциангидрина; по-
лучение сульфата метакриламида в среде кислоты; гидролиз или этерификация
сульфата метакриламида до кислоты или эфира.
Синтез циангидрина (синильная кислота)
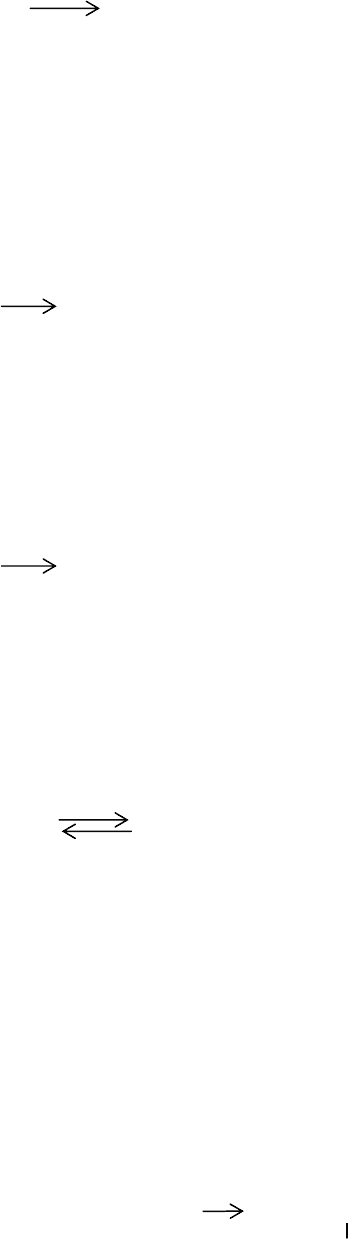
Как уже отмечалось, циангидрин образуется в качестве
побочного про-
дукта в производстве акрилонитрила. Однако циангидрин может быть получен
и прямым синтезом из метана или пропана.
270
Процесс Андрусова. Процесс заключается в окислительном аммонолизе
метана в присутствии воздуха:
CH
4
+ NH
3
+1,5O
2
HCN + 3H
2
O H
238
= -480 кДж/моль
Реакция протекает при 1373-1473 К и соотношении воздух: метан:аммиак,
равном 5:1:1, на платинорениевом катализаторе. В результате реакции получа-
ется газовый поток, содержащий ~ 6-8% (об.) НСN. Поток быстро охлаждают
до 673 К, чтобы избежать протекания вторичных процессов. Синильная кислота
образуется с выходом 80%.
Процесс фирмы "БМА – Блаузойре Метан Аммиак". Циангидрин
можно получать также
и в отсутствие кислорода:
CH
4
+ NH
3
HCN + 3H
2
H
238
= 250 кДж/моль.
Эта эндотермическая реакция протекает на платиновом катализаторе, на-
несенном на оксид алюминия, при 1473-1573 К. Концентрация синильной ки-
слоты в потоке достигает 20%, что облегчает ее выделение из газа. Выход си-
нильной кислоты составляет 85%.
Процесс фирмы "Флуомик де Дегусса". В качестве сырья в этом про-
цессе используется пропан:
C
3
H
8
+ 3NH
3
3HCN + 7H
2
H
238
= -45 кДж/моль
Реакция протекает в отсутствие катализатора при 1773 К над "кипящим
слоем" нефтяного кокса. Выход синильной кислоты на пропан и аммиак со-
ставляет 85-90%.
Конденсация ацетона и циангидрина
Реакция конденсации ацетона и циангидрина
CH
3
COCH
3
+ HCN (CH
3
)
2
C(OH)—CN H
238
= -45 кДж/моль
протекает с небольшим экзотермическим эффектом. В качестве катализатора
используют щелочные соединения (едкий натр, гидроксид бария, фосфат каль-
ция и др.) на силикагеле. Процесс осуществляют в жидкой фазе при 298-313 К,
атмосферном давлении и мольном соотношении НСN:ацетон, равном 0,7-1,1.
Конверсия синильной кислоты достигается практически полная. Выход целево-
го продукта в
расчете на исходные реагенты составляет 90%.
Синтез сульфата метакриламида
Получение сульфата метакриламида осуществляется двухстадийным гид-
ролизом ацетонциангидрина в присутствии серной кислоты как катализатора:
(CH
3
)
2
C(OH)CN + H
2
SO
4
(CH
3
)
2
C—CN + H
2
O
OSO
3
H
