Михеева Е.В., Пикула Н.П. Физическая и коллоидная химия
Подождите немного. Документ загружается.

231
Ионы одинаковой валентности адсорбируются тем лучше, чем
больше их ионный радиус, так как с увеличением радиуса уменьшается
степень гидратации ионов, наличие гидратной оболочки ослабляет
электростатическое взаимодействие ионов, препятствуя адсорбции.
Ионы, расположенные в порядке возрастания адсорбционной спо-
собности образуют лиотропные ряды (ряды Гофмейстера).
испособностнойадсорбциооевозрастани
CsRbKNaLi
3. С увеличением поляризуемости иона его адсорбционная способ-
ность увеличивается. Поляризуемость анионов всегда больше поляри-
зуемости катионов, поэтому на твердой поверхности преимущественно
будут адсорбироваться анионы.
Это имеет большое значение для стабилизации и коагуляции кол-
лоидных систем электролитами. В природе часто наблюдается избира-
тельная адсорбция калия, бария, никеля, радиоактивных элементов и др.
Ионообменная адсорбция. Ионный обмен
Ионообменная адсорбция является наиболее распространенным ви-
дом ионной адсорбции.
Ионообменная адсорбция - процесс обмена ионов между раство-
ром и ионообменником (сорбентом).
Ионообменники (иониты) – высокомолекулярные полиэлектроли-
ты, состоящие из синтетического нерастворимого каркаса с привитыми
функциональными группами кислотного ( -SO
3
, -COO, -PO
3
и др.) и
основного ( =NH, -NH
2
и др.) характера.
Особенности ионообменная адсорбции:
1. Адсорбция специфична, каждый адсорбент (ионит, ионообмен-
ник) обменивается определенными типами ионов.
2. Ионообменная адсорбция не всегда обратима.
3. Протекает более медленно, чем молекулярная адсорбция.
4. При обменной адсорбции может измениться рН среды.
Применение ионного обмена
1. Обессоливание (деминерализация) воды – удаление СаCl
2
,
МgCl
2
и т.д. Процесс обессоливание состоит в пропускании засоленной
воды через колонки, заполненные катионитом в Н
+
– форме и аниони-
том в ОН
-
- форме. На катионите происходит поглощение из воды ио-
нов Са
2+
и Мg
2+
– ионов и замена их на ионы Н
+
по схеме:
232
HClCaKatCaClHKat 22
2
22
При поступлении воды, содержащей НСl во вторую колонку на
анионите происходит замена ОН
-
группы ионита эквивалентным чис-
лом анионов Сl
-
кислоты по схеме:
OHClAnHClOHAn
2
На выходе из колонки с анионитом получают полностью деминера-
лизованную воду, не уступающую по степени очистки дистиллирован-
ной воде.
2. Опреснение воды на морских судах и космических кораблях:
HClNaKatNaClНKat
OHClAnHClOHAn
2
3. Очистка сточных вод – удаление ионов тяжелых металлов (Zn
2+
,
Cd
2+
, Pb
2+
, Cu
2+
).
NaPbKatPbNaKat 22
2
2
2
Вопросы для самоконтроля
1. В чем заключается отличие молекулярной и ионной адсорбции?
2. Какие адсорбенты используют для адсорбции органических ве-
ществ из водных растворов? Почему?
3. Какие адсорбенты используют для обезвоживания нефтепродук-
тов? Почему?
4. Какие ионы будут преимущественно адсорбироваться на поверх-
ности ионных кристаллов?
5. Каким образом можно опреснить морскую воду?
6. Каким образом проводится очистка природных вод от примесей?
233
11. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА
ДИСПЕРСНЫХ СИСТЕМ
Электрокинетические явления
Электрокинетические явления были открыты профессором Мос-
ковского университета Ф.Ф.Рейсом в 1808 г. Рейс исследовал явление
электролиза воды (недавно открытое Фарадеем).
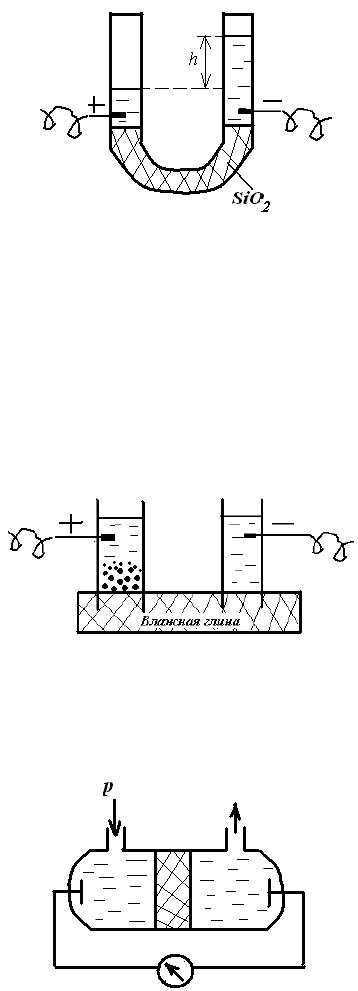
Рис.11.1 Схема опыта Рейса по
электроосмосу.
Он заполнил нижнюю часть U-
образной трубки толченым кварцем с
целью разделения продуктов электро-
лиза и заметил, что приложение внеш-
него напряжения к электродам (100 В)
приводит к перемещению воды в сто-
рону отрицательного электрода, это яв-
ление было названо электроосмосом.
Электроосмос – явление перемещения жидкой дисперсионной
среды относительно неподвижной дисперсной фазы под действием
электрического поля.
Во второй серии опытов Рейс погрузил во влажную глину две стек-
лянные трубки, наполненные водой, в трубки были введены электроды.
Рис.11.2 Схема опыта Рейса по
электрофорезу.
После включения электрического
тока наблюдалось движение отрываю-
щихся частичек глины к положитель-
ному электроду. Это явление было на-
звано электрофорезом.
Электрофорез – явление переме-
щения дисперсной фазы относительно
жидкой дисперсионной среды под дей-
ствием электрического поля.
Рис.11.3. Схема возникновения
потенциала течения
Несколько позже были обнаруже-
ны явления, обратные по характеру.
В 1859 году Квинке обнаружил,
что при фильтрации воды через порис-
тую диафрагму возникает разность по-
тенциалов, пропорциональная давле-
нию, под которым протекает жидкость.
Это явление, обратное электроосмосу,
было названо потенциалом течения.

234
Потенциал течения – возникновение разности потенциалов при
движении дисперсионной среды относительно неподвижной дисперс-
ной фазы.
Рис.11.4. Схема возникновения
потенциала седиментации
В 1879 г Дорном было открыто яв-
ление, обратное электрофорезу. При
оседании частиц кварца в воде возника-
ла разность потенциалов, возникающая
между двумя электродами, располо-
женными на разной высоте. Это явле-
ние, обратное электрофорезу было на-
звано потенциалом оседания (седимен-
тации).
Потенциал оседания (седимен-
тации) – возникновение разности по-
тенциалов при движении дисперсной
фазы относительно дисперсионной сре-
ды.
Открытые явления были названы электрокинетическими, так как
в них обнаруживалась связь между скоростью протекания (кинетикой) и
электрическим полем.
Причиной электрокинетических явлений является наличие на
границе раздела фаз двойного электрического слоя (ДЭС).
Механизмы образования двойного электрического слоя
При погружении твердой фазы в раствор электролита происходят
следующие явления: между твердой фазой и раствором возникает двой-
ной электрический слой, появляется вполне определенная разность по-
тенциалов между поверхностью дисперсной фазы и дисперсионной сре-
дой. Образование двойного электрического слоя можно объяснить ря-
дом причин.
1. Неравенство электрохимических потенциалов ионов в кри-
сталлической решетке твердого тела и ионов в растворе.
С термодинамической точки зрения возникновение ДЭС на границе
твердое тело – раствор может быть связано с неравенством электрохи-
мических потенциалов ионов в кристаллической решетке твердого тела
и ионов в растворе:
рртв
~~
235
Электрохимический потенциал – химический потенциал плюс
электрохимическая составляющая
zF
ii
~
.
Если электрохимические потенциалы одного и того же иона в твер-
дой и жидкой фазе не одинаковы, то происходит перенос иона от боль-
шего электрохимического потенциала к меньшему до полного их вы-
равнивания:
рррртвтв
zFzF
.
В рамках выравнивая электрохимических потенциалов возможно
два механизма образования ДЭС: адсорбционный и механизм поверхно-
стной диссоциации.
Адсорбционный механизм образования ДЭС
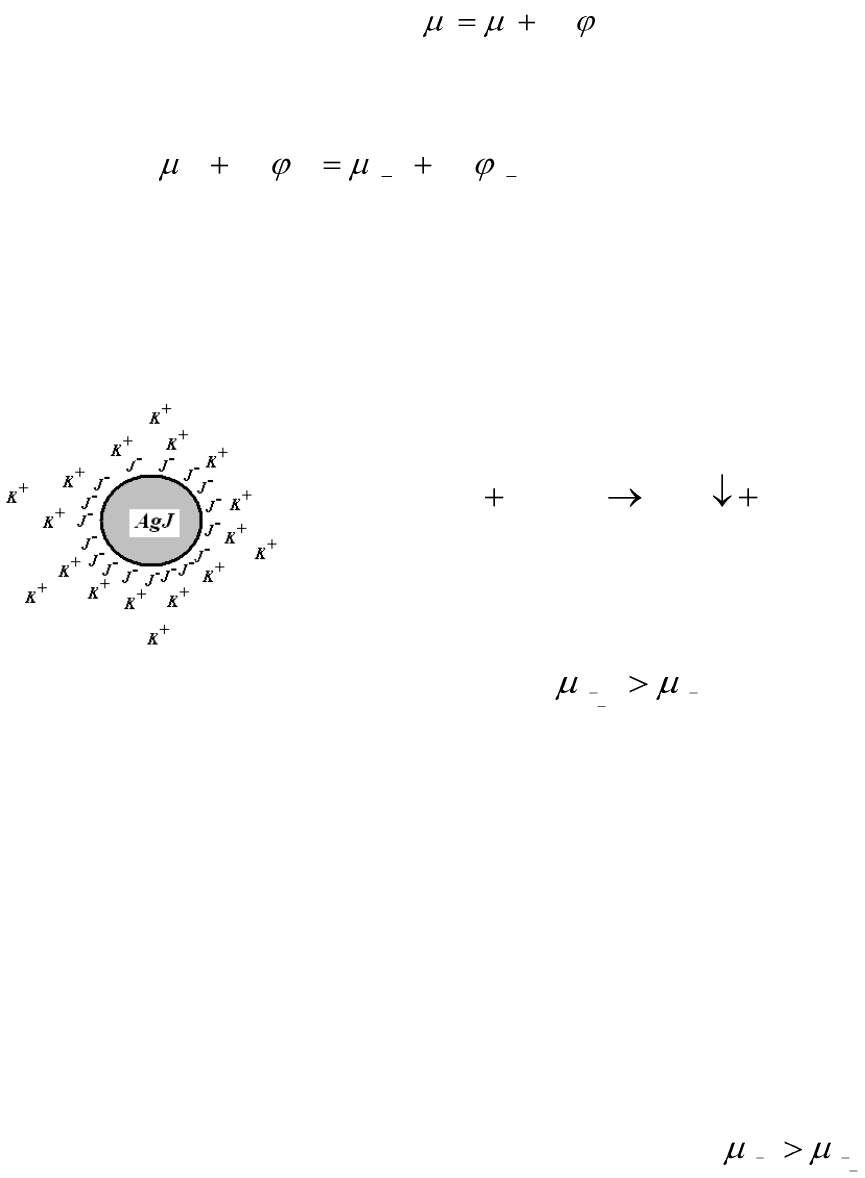
Рассмотрим адсорбционный механизм
образования ДЭС на примере золя иодида
серебра, полученного при избытке иодида
калия по реакции:
3.)(3
KNOAgJKJAgNO
изб
При избытке KJ электрохимический
потенциал иодид–ионов в растворе больше
электрохимического потенциала иодид – ио-
нов на поверхности твердой фазы:
тврр
JJ
~~
Иодид–ионы будут терять свою сольватную оболочку, и адсорби-
роваться на поверхности твердой фазы, заряжая частицу отрицательно.
К отрицательно заряженной частице из раствора за счет электростати-
ческого притяжения будут притягиваться ионы противоположного зна-
ка (ионы калия), образуется двойной электрический слой. По аналогии
со строением конденсатора вводится понятие внутренней и внешней об-
кладки ДЭС. Ионы, образующие внутреннюю обкладку и вызывающие
возникновение потенциала – потенциалопределяющие ионы (ПОИ) –
иодид–ионы; ионы, составляющие внешнюю обкладку – противоионы
(ПИ) – ионы калия.
Механизм поверхностной диссоциации
Если электрохимический потенциал иодид ионов в кристалличе-
ской решетке твердой фазы больше, чем в объеме раствора
рртв
JJ
(концентрация иодид-ионов в растворе мала), то иодид–ионы с поверх-
ности будут переходить в раствор за счет поверхностной диссоциации
ионов кристаллической решетки и образовывать у поверхности внеш-
236
нюю обкладку ДЭС. Поверхность твердой фазы в этом случае зарядится
положительно и будет служить внутренней обкладкой ДЭС.
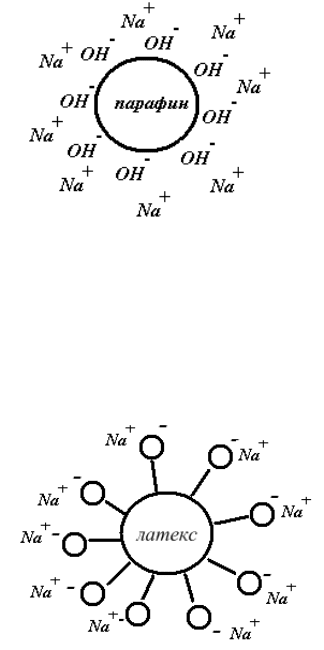
2. Специфическая адсорбции ионов на поверхности твердой фазы
Возникновение ДЭС может быть результатом специфической ад-
сорбции ионов на поверхности твердой фазы. Под специфической ад-
сорбцией понимают накопление на поверхности твердой фазы ионов
под действием адсорбционных сил.
ПОИ – OH
-
,
ПИ – Na
+
.
Так как адсорбционная способность анио-
нов выше, чем у катионов, то на поверхности
твердой частицы в результате специфической
адсорбции может появиться адсорбционный
слой анионов, которые притянут к себе ка-
тионы из раствора. Примером такой специ-
фической адсорбции может являться адсорб-
ция гидроксид-ионов на поверхности пара-
фина (золь парафина в растворе щелочи).
3. Ориентированная адсорбция поверхностно-активных веществ
Двойной электрический слой может возникнуть также в результате
адсорбции поверхностно-активных веществ.
В этом случае дифильные молекулы
ПАВ будут ориентироваться на поверхно-
сти определенным образом и образовывать
адсорбционный двойной электрический
слой. Примером может служить адсорбция
поверхностно-активного аниона стеарата
натрия на поверхности латекса.
Также двойной электрический слой может образовываться за счет
адсорбции дипольных молекул растворителя на поверхности твердых
частиц, за счет приложенной внешней разности потенциалов. Как пра-
вило, разные механизмы образования ДЭС могут реализовываться од-
новременно.
Движущей силой возникновения ДЭС является стремление систе-
мы уменьшить свою избыточную поверхностную энергию. В случае
возникновения ДЭС происходит уменьшение поверхностного натяже-
ния (поверхностной энергии) на границе раздела фаз из-за электроста-
тического расталкивания одноименно заряженных ионов на поверхно-
сти.
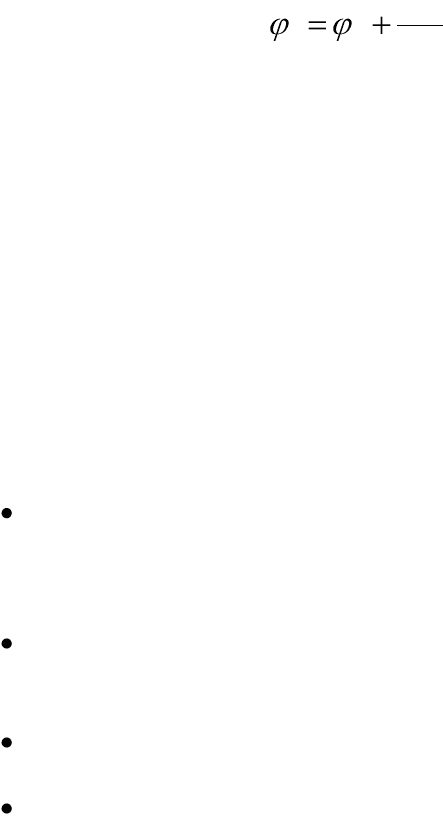
237
Теории строения двойного электрического слоя
Экспериментальные факты, послужившие осно-
вой для создания теорий строения ДЭС
1. Существует электрический (термодинамический) потенциал по-
верхности относительно жидкой дисперсионной среды φ
0
, зависящий от
концентрации потенциалопределяющих ионов по уравнению Нернста:
ПОИ
C
zF
RT
ln
0
00
.
2. Существует электрокинетический потенциал (дзета – потенциал)
ζ – потенциал, возникающий на границе скольжения при относительном
перемещении фаз в электрическом поле
3. Обнаружено, что по абсолютной величине электрический потен-
циал поверхности всегда больше электрокинетического потенциала:
φ
0
>0, ζ >0; φ
0
<0, ζ <0.
4. Оказалось, что φ
0
и ζ могут иметь разные знаки, например,
φ
0
>0, ζ <0.
5. Электролиты могут по-разному влиять на величину и знак заряда
φ
0
и ζ.
Для всех теорий двойного электрического слоя общими являются
следующие положения:
двойной электрический слой (ДЭС) состоит из потенциалопре-
деляющих ионов (ПОИ), прочно связанных с дисперсной фазой, и эк-
вивалентного количества противоионов (ПИ), расположенных в дис-
персионной среде;
поверхностный заряд, обусловленный наличием на твердой ней-
тральной поверхности потенциалопределяющих ионов, равномерно
распределен по всей поверхности дисперсной фазы;
между противоионами двойного электрического слоя и ионами
того же знака раствора существует динамическое равновесие;
дисперсионная среда влияет на строение двойного электрического
слоя через величину диэлектрической проницаемости.
Целью всех теорий являлось получение зависимости между по-
верхностным зарядом и потенциалом на границе раздела фаз.
238
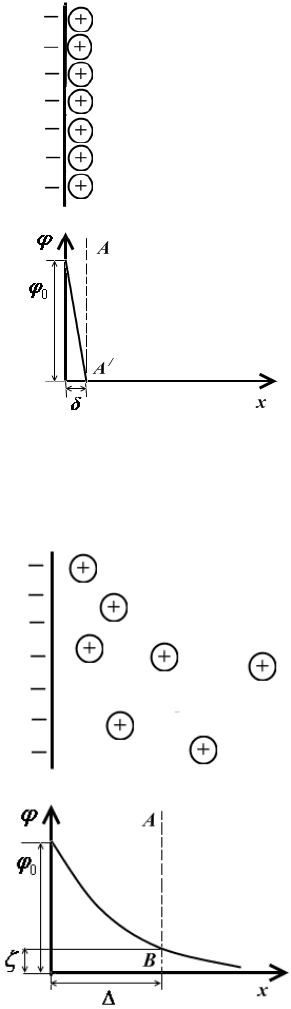
Теория строения ДЭС Гельмгольца – Перрена
В теории Гельмгольца – Перрена (1879 г.) двойной электрический
слой рассматривается как плоский конденсатор: внутренняя обкладка
которого состоит из потенциалопределяющих ионов, непосредственно
связана с поверхностью твердой фазы, а внешняя обкладка, состоящая
из противоионов, расположена в жидкости параллельно поверхности на
расстоянии межмолекулярного порядка от нее.
Рис.11.5. Модель строения
ДЭС Гельмгольца.
Поверхностный заряд (потенциал)
уменьшается линейно с расстоянием от
поверхности в соответствии с теорией
плоского конденсатора (рис.11.5). По-
добное строение ДЭС вполне возможно
при отсутствии теплового движения
ионов.
Эта теория оказалась применима
лишь для очень концентрированных
растворов. Основным недостатком тео-
рии было то, что она учитывала только
электростатическое взаимодействие
ионов с поверхностью и полностью иг-
норировала их тепловое движение.
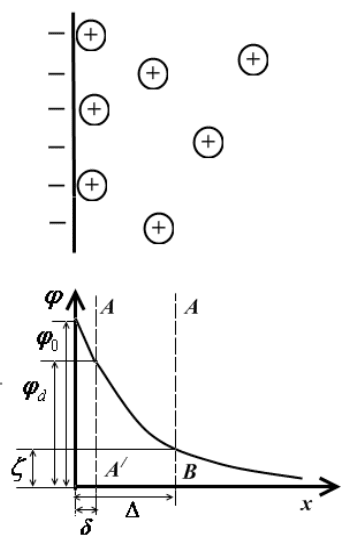
Теория строения ДЭС Гуи – Чэпмена (1910-1913 г.)
Рис.11.6. Модель строения
ДЭС Гуи-Чепмена.
Двойной электрический слой имеет
диффузионное (размытое) строение и все
противоионы находятся в его диффузи-
онной части (рис.11.6). Такое строение
определяется соотношением сил элек-
тростатического притяжения ионов, за-
висящего от электрического потенциала,
и тепловым движением ионов, стремя-
щихся равномерно распределиться во
всем объеме жидкой фазы.
Противоионы рассматриваются как
точечные заряды, не имеющие собствен-
ных размеров, а потенциал φ экспонен-
циально снижается по мере удаления от
поверхности.
239
На некотором расстоянии (Δ) от межфазной границы проходит
плоскость скольжения АВ. Плоскость скольжения – плоскость, по кото-
рой происходит разрыв ДЭС при наложении электрического поля. Тол-
щина слоя Δ не известна, но примерно составляет около 100 нм. Пере-
сечение кривой падения потенциала с плоскостью скольжения дает ве-
личину электрокинетического (дзета-потенциала). Следовательно, элек-
трокинетический потенциал ζ, измеряемый при электрокинетических
явлениях, является частью общего скачка потенциала φ
0
(φ
0
> ζ).
Теория строения ДЭС Штерна (1924 г.)
Современная теория строения двойного электрического слоя
Штерна объединяет две предыдущие теории. Согласно этой теории,
слой противоионов состоит из двух частей (рис.11.7).
Рис.11.7. Модель строения
ДЭС Штерна.
Одна часть противоионов нахо-
дится в непосредственной близости от
межфазной поверхности и образует
слой Гельмгольца (адсорбционный
слой), толщиной не более диаметра со-
ставляющих его гидратированных ио-
нов. Адсорбционный слой формируется
в результате электростатического взаи-
модействия с потенциалопределяющи-
ми ионами и специфической адсорб-
ции. В адсорбционном слое наблюдает-
ся резкое падение электрического по-
тенциала φ
0
по прямой, согласно тео-
рии Гельмгольца-Перрена.
Другая часть противоионов нахо-
дится в диффузной части ДЭС (диф-
фузный слой Гуи), толщина которого
может быть значительной и зависит от
состава системы. В диффузной части
ДЭС потенциал уменьшается по экспо-
ненте, согласно теории Гуи-Чепмена.
Таким образом, общее падение электрического потенциала φ
0
скла-
дывается из падения адсорбционного потенциала (φ
0
- φ
d
) в плотной
части ДЭС (линия АА´) и падения потенциала диффузного слоя φ
d
– в
его диффузионной части.
240
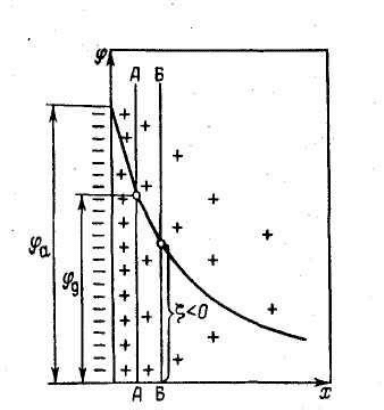
Электрокинетический потенциал
Согласно современным представлениям о строении ДЭС, полное
падение общего поверхностного потенциала φ слагается из падения ад-
сорбционного потенциала φ
а
в плотной части ДЭС и падения потенциа-
ла диффузного слоя φ
d
в его диффузионной части.
Потенциал φ снижается по ме-
ре удаления от поверхности, причем
в адсорбционном слое наблюдается
линейное уменьшение φ. Наруше-
ние линейной зависимости проис-
ходит на границе между адсорбци-
онным и диффузным слоями проти-
воионов (линия АА).
В диффузном слое снижение φ
потенциала происходит по экспо-
ненциальному закону.
Рис.11.8. Современная модель
строения ДЭС.
Теория двойного электрического слоя, широко используемая для
интерпретации поверхностных явлений, нуждается в эксперименталь-
ной проверке. Однако, не существует прямых методов измерения по-
тенциалов на границе адсорбционного слоя. Таким образом, адсорбци-
онный потенциал φ
а
принадлежит к разряду практически неизмеримых
величин.
Можно измерить другую близкую величину – электрокинетиче-
ский потенциал ζ (дзета-потенциал). Величина электрокинетического
потенциала является менее определенной, но измеряемой эксперимен-
тально.
Дзета-потенциал определяют как потенциал границы скольжения
фаз (линия ВВ) при их относительном передвижении в электрическом
поле. Положение границы скольжения в ДЭС не известно. Полагают,
что граница скольжения проходит либо на расстоянии толщины плот-
ной части ДЭС, и в этом случае ζ = φ
d
; либо смещена в жидкую фазу,
тогда ζ < φ
d
, где φ
d
– потенциал на границе плотная часть ДЭС – диф-
фузная часть ДЭС.
