Креативная хирургия и онкология №1 (5) - 2011
Подождите немного. Документ загружается.

Креативная хирургия и онкология
21
ОРИГИНАЛЬНЫЕ СТАТЬИ
1–2 степеней встречались в обеих группах больных,
но в группе Х+И их было в 2 раза меньше.
В задачу исследования входило изучение ди-
намики иммунологических показателей в процессе
химиотерапии в зависимости от применения иму-
нофана. Иммунологическое тестирование включа-
ло оценку клеточного звена иммунитета. Состояние
клеточного иммунитета оценивали по экспрессии
поверхностных антигенов лимфоцитов к дифферен-
цировочным антигенам лейкоцитов человека: СD3,
СD5, СD7 (маркеры Т-лимфоцитов), СD4 (маркер
хелперов/индукторов), СD8 (маркер супрессор-
ных/цитотоксических Т-лимфоцитов), СD16 (мар-
кер естественных киллеров). Иммунорегуляторный
индекс высчитывали по соотношению СD4+ и СD8+
клеток. Выявлена определенная связь между пока-
зателем иммунорегуляторного индекса и эффек-
тивностью химиотерапии.
При проведении только химиотерапевтическо-
го лечения эффективность лечения сильно зависит
от уровня иммунорегуляторного индекса (разница
в эффективности химиотерапии при низком уровне
иммунорегуляторного индекса составляет 15%).
При проведении сочетанной химиотерапии уро-
вень иммунорегуляторного индекса не оказывает
существенного влияния на эффективность лечения.
Отмечено, что при низком уровне иммуноре-
гуляторного индекса лечение более эффективно
у больных, получающих сочетанную терапию. При
нормальных показателях иммунорегуляторного ин-
декса эффективность в обеих группах больных (Х
и Х+И) почти одинакова. Можно сделать вывод о
том, что при исходно низком уровне иммунорегуля-
торного индекса в целях повышения эффективности
химиотерапии целесообразно включение в лечение
препаратов иммуномодулирующего действия (в
частности, имунофана).
При хороших показателях иммунорегулятор-
ного индекса применение иммуномодуляторов не
обязательно (рис. 3).
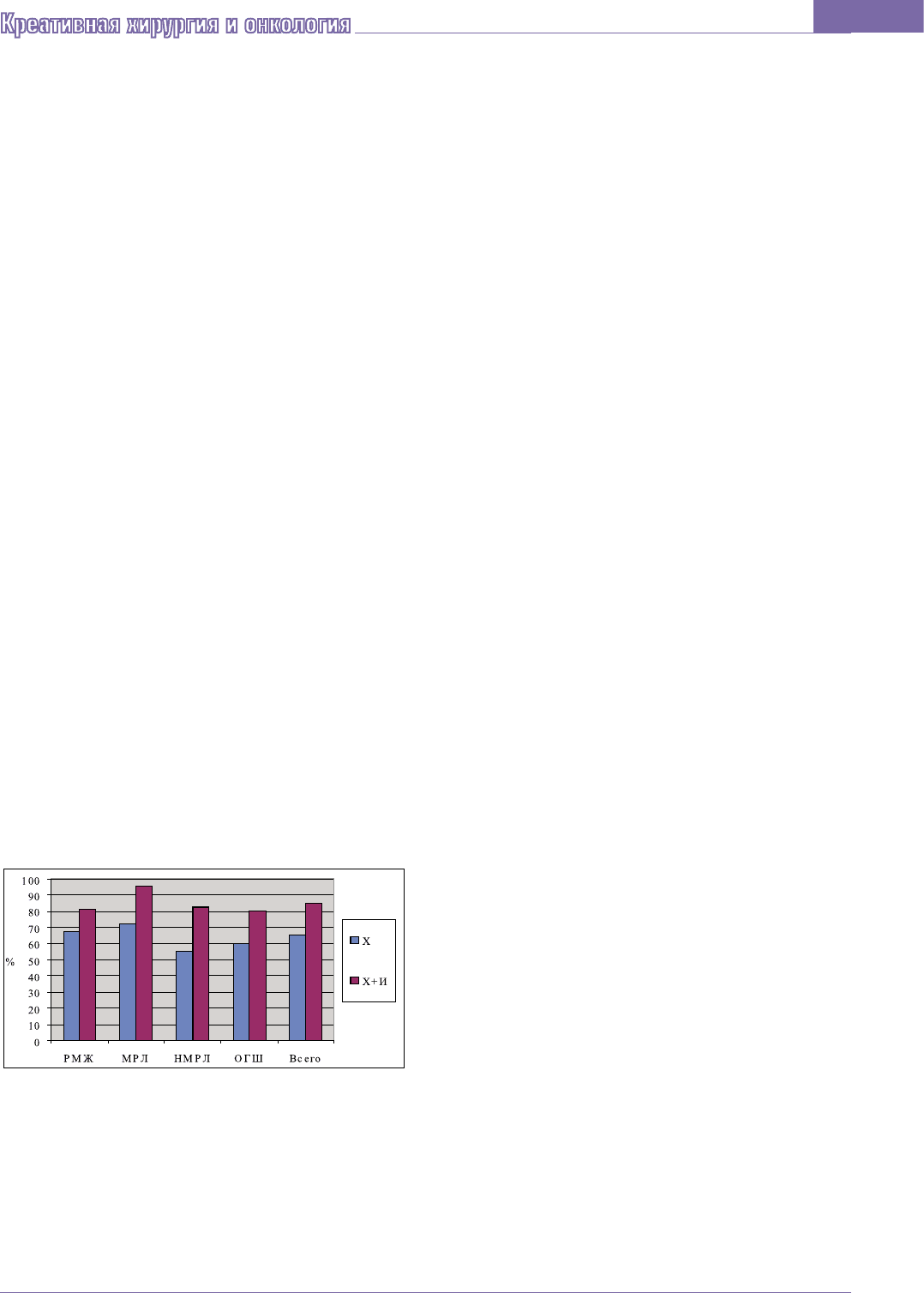
Рис. 3. Роль иммуномодулирующего
препарата – имунофан в эффективности
химиотерапии при различных уровнях
иммунорегуляторного индекса (ИИ)
Проанализированы случаи заболевания боль-
ных вирусными инфекциями. Всего вирусными
заболеваниями переболело 73% пациентов, полу-
чивших только химиотерапию, и 53% больных, по-
лучивших химиотерапию в сочетании с имунофа-
ном. Среди них отмечены случаи заболевания ОРВИ,
герпесом, которые послужили причиной прекраще-
ния или отсрочки курса химиотерапии. Так, ОРВИ
чаще болели пациенты из группы, получающей
только химиотерапию (в группе Х - 62% больных,
Х+И - 45% больных). Проявления инфекции, вы-
званной вирусом простого герпеса, отмечено в 1,5
раза чаще у больных, получающих химиотерапию
без имунофана. Таким образом, сопутствующие ви-
русные заболевания при использовании имунофа-
на возникают в 1,4 раза реже.
Биогенные амины исследовались в плазме,
лимфоцитах, лейкоцитах и эритроцитах люминес-
центно-гистохимическими методами. У здоровых
людей эти структуры периферической крови содер-
жат катехоламины, серотонин и гистамин. Именно в
таком порядке по нарастанию интенсивности люми-
несценции располагаются биогенные амины во всех
изученных структурах. Кровь у пациентов из группы
контроля исследовали дважды. Во временном про-
межутке (7 дней) отмечались лишь незначительные
колебания значений биогенных аминов (разница
не достоверна).
Исходный уровень биогенных аминов (серо-
тонина, гистамина, катехоламинов) в структурах
периферической крови здоровых людей и онко-
логических больных различен. Также он отличает-
ся среди больных обеих исследуемых групп (Х и
Х+И). Наибольшие различия среди исследуемых
групп отмечены при измерении уровня серотонина
(так, в группе Х первоначальные значения серото-
нина были выше нормы в лимфоцитах на 28-42%
и лейкоцитах - на 23-27% в зависимости от нозо-
логической группы, а в группе Х+И приближались
к нормальным значениям). Исходно уровни гиста-
мина в структурах периферической крови у здоро-
вых людей и онкологических пациентов до лече-
ния сопоставимы и мало отличаются друг от друга.
Первоначальный уровень катехоламинов в группе
Х был выше нормы (максимально в лейкоцитах на
16-28%). Исходный уровень катехоламинов в груп-
пе Х+И ниже нормы в плазме (на 18, 31, 36, 40%
у больных РМЖ, ОГШ, НМРЛ, МРЛ соответствен-
но), лимфоцитах (на 8, 11, 14, 16% у больных ОГШ,
НМРЛ, МРЛ, РМЖ соответственно), эритроцитах
(на 23-31%) и в лейкоцитах выше нормы (в среднем
на 3-8%).
Кровь у пациентов из группы контроля исследо-
вали дважды. Во временном промежутке (7 дней)
отмечались лишь незначительные колебания значе-
ний биогенных аминов (разница не достоверна). У
больных обеих исследуемых групп отмечаются бо-
лее существенные изменения в уровне биогенных
аминов, что дает основание предполагать влияние
химиотерапии на биоаминную обеспеченность
структур периферической крови. При всех изучен-
ных нозологиях изменения уровня биогенных ами-
нов до и после лечения были идентичны. Значения
отдельных биоаминов, а также их соотношения
между собой различны в группах, получавших хи-
миотерапию на фоне имунофана и без него. После
химиотерапии нарастание уровня серотонина от-

Креативная хирургия и онкология
22
ОРИГИНАЛЬНЫЕ СТАТЬИ
мечается во всех структурах периферической крови
обеих исследуемых групп (в группе, получающей
только химиотерапию: в плазме - на 60-67%, в лим-
фоцитах - на 71-80%, в лейкоцитах - на 50-57%, в
эритроцитах - на 40-51%, а в группе, получающей
химиотерапию на фоне имунофана: в плазме - на
19-27%, в лимфоцитах - на 77-104%, в лейкоцитах -
на 32-34%, в эритроцитах - на 36-49% в зависимос-
ти от нозологической группы). Оно статистически
достоверно и наиболее выражено в иммунокомпе-
тентных клетках (лимфоцитах и лейкоцитах). Зная
иммунодепрессивное действие химиотерапии на
организм в целом, наблюдая явное увеличение се-
ротонина на ее фоне, учитывая данные литературы,
можно предположить участие серотонина в моду-
ляции иммуносупрессирующего действия химиоте-
рапии. Наше предположение совпадает с мнением
многих авторов, изучавших действие серотонина
[8,13]. Небольшое снижение уровня гистамина на
фоне изолированной химиотерапии обусловлено,
вероятно, проведением стандартной премедикации
перед каждым курсом химиотерапии, включающей
в себя прием глюкокортикостероидов, которые,
предупреждая реакции антиген-антитело, снижают
образование гистамина [2]. При введении имунофа-
на на фоне химиотерапии наблюдается рост уровня
гистамина, главным образом в лимфоцитах (на 53
- 58% в зависимости от нозологической группы).
Гистамин играет роль важного промежуточного
звена при многих аллергических реакциях [10]. Од-
новременное увеличение гистамина и серотонина
во всех структурах периферической крови при хи-
миотерапии на фоне имунофана наводит на мысль
о субклинически текущей аллергической реакции.
Уровень катехоламинов увеличивается в обеих
группах больных, преимущественно в лимфоци-
тах (в группе Х – на 36-49%, в группе Х+И - на 34-
54%). Наибольший рост отмечается в группе Х+И.
Норадреналин, действуя через цАМФ, усиливает
иммунные процессы. Г.Х. Божко (1984) отмечает,
что норадреналин активирует иммунокомпетентные
клетки стимуляцией генной транскрипции и увели-
чением синтеза РНК, повышает хелперный эффект
Т-лимфоцитов, стимулирует антителообразова-
ние. Опираясь на данные литературы и результаты
собственных исследований, можно предположить
участие катехоламинов в стимуляции иммунных
процессов в клетках крови при проведении хими-
отерапии на фоне имунофана, в меньшей степени
- при проведении только химиотерапии.
Известно, что для правильного суждения о био-
аминной обеспеченности органов и тканей и их
функционального состояния имеют значение не
только и не столько показатели содержания отде-
льных биоаминов, но и их соотношение [4].
Соотношение катехоламины/серотонин во вре-
мя изолированной химиотерапии уменьшается (за
счет повышения серотонина) во всех структурах пе-
риферической крови, доказывая супрессирующее
действие химиотерапии (в плазме у больных с ОГШ
и эритроцитах больных РМЖ в 2 раза). На фоне
введения имунофана изучаемый коэффициент сни-
жается в сравнении с группой, получающей хими-
отерапию без иммуномодуляции, меньше (намеча-
ется тенденция к увеличению этого коэффициента:
в плазме больных МРЛ и НМРЛ он увеличивается в
1,2 раза).
Выводы
1. Применение имунофана во время химиотера-
пии снижает токсичность лечения (уменьшает ко-
личество больных с лейкопениями всех степеней на
22%, лимфопениями 1-2 степени - в 3 раза, с откло-
нениями в биохимических показателях крови (АЛТ,
АСТ) - в 2 раза, сокращает время восстановления
числа лейкоцитов периферической крови на 20%).
2. При низком уровне иммунорегуляторного
индекса лечение более эффективно у больных, по-
лучающих сочетанную терапию. При нормальных
показателях иммунорегуляторного индекса эффек-
тивность в обеих группах больных (Х и Х+И) почти
одинакова.
3. Химиотерапевтическое лечение влияет на
биоаминную обеспеченность структур перифе-
рической крови. В обеих группах (Х и Х+И) после
химиотерапии выявлено увеличение серотонина,
обладающего супрессирующим действием на им-
мунную систему. Наблюдается уменьшение коэф-
фициента катехоламины/серотонин, что также сви-
детельствует об иммуносупрессирующем действии
лечения. В группе больных, получающих лечение
на фоне имунофана (Х+И), отрицательные сдвиги
в биоаминной картине крови проявляются в мень-
шей степени (намечается тенденция к увеличению
коэффициента катехоламины/серотонин).
4. Добавление имунофана в химиотерапевти-
ческое лечение ведет к увеличению общего ответа
на лечение на 11%, продлевает продолжительность
ремиссии в среднем на 2 месяца, у больных с ис-
ходно низкими показателями иммунорегуляторно-
го индекса способствует повышению эффективнос-
ти лечения на 9% и снижает риск возникновения
вирусных заболеваний в 1,4 раза.
Список литературы
1. Автандилов Г.Г. Компьютерная микротелефо-
тометрия в диагностике гистоцитопатологии. - М.:
РМАПО, 1996. – 256 с.
2. Бережная Н.М., Сепиашвили Р.И. Тучные
клетки и гистамин: физиологическая роль // Ал-
лергология и иммунология. - 2003. - Т. 4. - № 3. – С.
29-38.
3. Божко Г.Х. Влияние катехоламинов на синтез
белков и нуклеиновых кислот // Проблемы эндок-
ринологии. - 1984. - № 2. – С. 3-5.
4. Вайнсфельд И.Л., Кассиль Г.Н. Гистамин в
биохимии и физиологии. - М.: Наука, 1981. – С. 80.
5. Возный Э.К., Добровольская Н.Ю. 15-летний
опыт комплексного лечения больных местнорасп-
ространенным раком молочной железы с исполь-
зованием неоадьювантной химиотерапии // 10
Российский онкологический конгресс. - М.: Из-
дательская группа РОНЦ им. Н.Н. Блохина РАМН,
2006. – С. 14-15.

Креативная хирургия и онкология
23
ОРИГИНАЛЬНЫЕ СТАТЬИ
6. Волкова З.В. Причины развития инфекций у
онкологических больных // 9 Российский онколо-
гический конгресс. - М.: Издательская группа РОНЦ
им. Н.Н. Блохина РАМН, 2005. – С. 36-38.
7. Гилязутдинов И.А. Нейроэндокринная патоло-
гия в гинекологии и акушерстве // И.А. Гилязутди-
нов, З.Ш. Гилязутдинова. - М.: МЕДпресс-информ,
2008. - 431 с.
8. Девойно Л.В., Альперина Е.Л Подгорная Е.К.,
Поляков О.В., Идова Г.В. Характер распределения
серотонина и его метаболитов в структурах мозга и
развитие иммуносупрессии у субмессивных мышей
// Российский физиологический журнал им. И.М.
Сеченова. - 2002. – Т. 88. - №1. – С. 106-112.
9. Калмыков В.Л. Современные методы количес-
твенного определения катехоламинов и серотонина
// Лаб. Дело. - 1982. - №7. – С. 31-36.
10. Караулов А.В., Кокушков Д.В. Иммуномоду-
ляторы: классификация, принципы и практика при-
менения при инфекциях дыхательных путей у детей
// Детские инфекции. - 2007. – Т. 6. - №4. – С. 68-
70.
11. Крохина Е.М., Александров П.Н. Симпати-
ческий (адренэргический) компонент эффекторной
иннервации сердечной мышцы // Кардиология.
– 1969. - Т. 9. - №3. - С. 97-102.
12. Мирюнусов Н.М., Даминов Б.Т., Латипова
Н.С., Расулева Н.Б., Кучкарова С.К. Динамика пока-
зателей иммунного статуса при иммунокорригирую-
щей терапии рибомунилом у больных хроническим
гломерулонефритом, леченных циклофосфаном //
Иммунология. - 2002. - № 5. – С. 305-307.
13. Переводчикова Н.И. Руководство по химио-
терапии опухолевых заболеваний / Под ред. Н.И.
Переводчиковой. - М.: Практическая медицина. -
2005. - С. 86.
14. Смирнова Т.Л., Сергеева В.Е., Ястребова С.А.
Биоаминсодержащие структуры тимуса при бере-
менности и воздействии Т-активина // Аллерголо-
гия и иммунология. - 2007. – Т. 8. - №1. – С. 313.
15. Труфакин В.А., Шурлыгина А.В. Проблемы
гистофизиологии иммунной системы // Иммуно-
логия. - 2002. - № 1. – С. 4-8.
16. Франциянц Е.М., Бандовкина В.А., Кучкина
Л.П. и др. Сравнительная характеристика некото-
рых показателей моноаминергической системы при
доброкачественных и злокачественных новообразо-
ваниях молочной железы // Известия высших учеб-
ных заведений. - Северо-Кавказский регион: серия:
Естественные науки, 2007. - № 4. – С. 123-125.
17. Чиссов В.И., Старинский В.В., Петрова Г.В.
Злокачественные новообразования в России в 2007
году (заболеваемость и смертность). – М.: ФГУ
«МНИОИ им. П.А. Герцена Росмедтехнологий»,
2009. – 253 с.
18. Юденфренд С. Флуоресцентный анализ в
биологии и медицине. – М.: Мир, 1965. – 484 с.
19. Cross S.A., Ewen S.W., Rost F.W. A study of meth-
ods available for cytochemical localization of histamine
by fluorescence induced with o-phtaldehyde or acetalde-
hyde // Histochem.J. - 1971. - Vol. 3. - №6. - P. 471-476.
20. Rolston K.V., Rubenstain E.B. Textbook of Fe-
brile Neutropenia / ed. by K.V.I. Rolston. – Martin Du-
nitz, 2001. - 329 p.

Креативная хирургия и онкология
24
ОПЫТ НАУЧНЫХ И ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ
ËÀÏÀÐÎÑÊÎÏÈ×ÅÑÊÈÅ ÎÏÅÐÀÖÈÈ
ÏÐÈ ÊÎËÎÐÅÊÒÀËÜÍÎÌ ÐÀÊÅ
Р.Т. Аюпов, А.П. Ройзман, Ю.М. Акмалов, А.И. Каримов
ГОУ ВПО Башкирский государственный медицинский университет,
кафедра хирургии и онкологии с курсами онкологии и патологической анатомии
ГУЗ Республиканский клинический онкологический диспансер, г.Уфа
Аюпов Рустем Талгатович, врач-онколог РКОД,
доцент кафедры хирургии и онкологии с курсами онкологии
и патологической анатомии БГМУ, канд. мед. наук,
450054, Россия, Республика Башкортостан, г. Уфа, пр. Октября, 73/1,
тел. 8 (347) 237-36-71,
e-mail: ru2003@bk.ru
В статье представлена хирургическая техника и непосредственные результаты ла-
пароскопически ассистированных и лапароскопических операций у 27 больных коло-
ректальным раком. Наложение карбоксиперитонеума и изменение положения тела
во время операции влияют на гемодинамические и дыхательные изменения, имею-
щие уникальные отличия при лапароскопических операциях в сравнении с открыты-
ми хирургическими процедурами. Опыт выполнения лапароскопических операций
при колоректальном раке и отличительные особенности анестезиологического посо-
бия рассмотрены в статье.
Ключевые слова: колоректальный рак, лапароскопическая колоректальная хи-
рургия, анестезия при лапароскопической хирургии.
LAPAROSCOPIC COLORECTAL SURGERY
R.T. Ayupov, A.P. Royzman, J.M. Akmalov, A.I. Karimov
Bashkir State University of Medicine, Surgery and Oncology Chair
with Oncology and Pathoanatomy courses
Clinicial Oncology Dispensary, Ufa
The article presents surgical techniques and the results of short-term follow-up in 27
patients who had received laparoscopic-assisted and laparoscopic procedures for colorectal
cancer. Overlay karboksiperitoneuma into the peritoneal cavity and positioning changes
result in intraoperative cardiovascular and pulmonary changes that are uniquely different
in laparoscopic compared to open surgical procedures. The experience of the laparoscopic
colorectal surgery and particular qualities of the anesthetic management are analyzed in
the article.
The key words: colorectal cancer, laparoscopic colorectal surgery, anesthesia for
laparoscopic surgery.
Первая лапароскопическая операция при ко-
лоректальном раке выполнена в 1990 году [12]. С
тех пор многочисленными рандомизированными
исследованиями доказана сопоставимость непос-
редственных и отдаленных результатов открытых
и лапароскопических операций [6]. Современный
подход к проведению видеоэндоскопических опе-
раций при раке толстой кишки подразумевает не
только обсуждение хирургических возможностей,
но и обеспечение адекватной анестезиологической
защиты [3]. Основной особенностью обеспечения
условий выполнения эндоскопических операций
при колоректальном раке является необходимость
нагнетания в брюшную полость углекислого газа,
что ведет к повышению внутрибрюшного давле-
ния, и использование положения Тренделенбурга
[7]. Создание карбоксиперитонеума оказывает вы-
раженное неблагоприятное действие на систему
дыхания и вызывает биохимические изменения,
происходящие вследствие всасывания углекисло-
го газа в системный кровоток [13]. Самыми значи-
мыми из этиологических факторов этих сдвигов
является внутрибрюшная гипертензия и позицио-
нирование во время операции [1]. При введении
углекислого газа в брюшную полость под давлени-
ем (12-15 мм рт. ст.) возникает компрессия органов
брюшной и грудной полости. В ответ на снижение
преднагрузки и депонирования крови в брюшной
Креативная хирургия и онкология
25
ОПЫТ НАУЧНЫХ И ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ
полости при создании карбоксиперитонеума адап-
тивными реакциями системы кровообращения яв-
ляются повышение общего периферического сосу-
дистого сопротивления, артериального давления,
частоты сердечных сокращений и контрактильнос-
ти миокарда [3,4]. Для достижения оптимальной
мышечной релаксации целесообразным является
применение комбинированной анестезии с низким
потоком свежего газа, которая уменьшает расход
анестетика и позволяет поддерживать оптималь-
ный микроклимат в дыхательном контуре, снизить
стоимость анестезиологического пособия, сделать
ингаляционную анестезию гигиенически и экологи-
чески безопасным методом анестезии, с использо-
ванием эпидурального обезболивания [5].
В Республиканском клиническом онкологичес-
ком диспансере освоение эндовидеохирургических
операций началось в 2009 году. Операции с лапа-
роскопическим доступом выполнены у 27 больных,
в 12 случаях произведена конверсия (5 - плановых,
5 - в связи с местным распространением опухоли, 2
- в связи с кровотечением). У 15 больных выполне-
на 1 гемиколэктомия справа, 5 экстирпаций прямой
кишки, 1 лапароскопическая низкая передняя ре-
зекция прямой кишки, 5 лапароскопически ассис-
тированных резекций прямой кишки с выполнени-
ем минидоступа, 3 наложения колостомы. В группе
пациентов было 20 мужчин и 7 женщин в возрасте
от 57 до 73 лет. Продолжительность операций со-
ставила от 30 до 240 минут.
В связи с ограниченностью показаний к видео-
эндоскопическим вмешательствам проводился тща-
тельный отбор больных: оценивались локализация
первичной опухоли и её местное распространение,
конституциональный тип, тяжесть течения сопутс-
твующего заболевания и пр. С учетом отсутствия
возможности интраоперационной ручной пальпа-
торной ревизии кроме стандартных методов иссле-
дования (эндоскопического и рентгенконтрастно-
го исследований толстой кишки, ультразвукового
исследования органов брюшной полости и малого
таза, рентгенологического исследования органов
грудной клетки) проводились уточняющие методы
– компьютерная томография или МРТ (оценка со-
стояния забрюшинных лимфатических узлов, мест-
ного статуса опухоли).
Техническое обеспечение: видеоэндоскопичес-
кая стойка Karl Storz, оснащенная электрохирур-
гическим генератором; ультрасонический скаль-
пель Harmonic, электрохирургический генератор
ForceTriad (интегрированный LigaSure).
При операциях на прямой кишке применялись
четыре точки ведения троакаров – 12 мм над пуп-
ком, 12 мм в мезогастральной области слева, 5 мм
в подвздошных областях с обеих сторон (рис. 1). В
отличие от классической схемы операционная бри-
гада состояла из хирурга, располагающегося справа
от пациента, одного ассистента (располагающего-
ся слева от пациента), выполнявшего также роль
cameraman, и операционной сестры. Второй ассис-
тент выполнял манипуляции со стороны промеж-
ностного доступа.
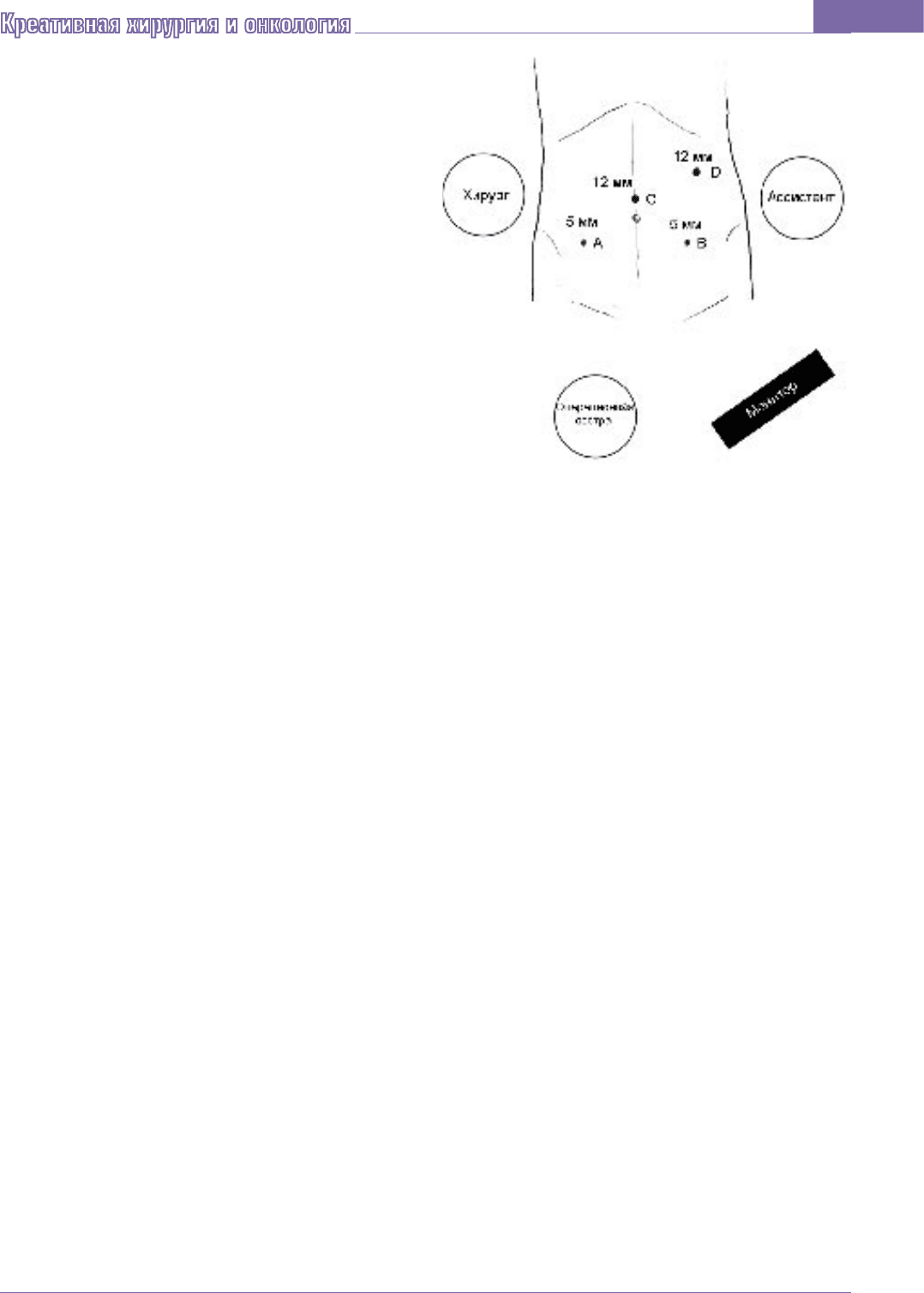
Рис. 1. Схема расположения операционной бригады
и точек доступа. A, B – 5 мм троакары
для инструментов хирурга, С – 12 мм троакар
для введения эндоскопа, D – 12 мм троакар
для инструмента ассистента
Во всех случаях проводилась комбинированная
низкопоточная ингаляционная анестезия на осно-
ве севофлурана и эпидуральное обезболивание с
использованием ропивакаина гидрохлорида. Ин-
траоперационный мониторинг включал в себя: не-
инвазивное измерение артериального давления,
частоты сердечных сокращений, электрокардиог-
рафию, плетизмографию, пульсоксиметрию, кон-
центрации анестетика на вдохе и в конце выдоха,
концентрации СО2 на вдохе и в конце выдоха, кон-
центрации О2 в газовой смеси, дыхательный объ-
ем, минутный объём вентиляции, давление в дыха-
тельных путях, BIS – мониторинг (А -2000 ХР Aspect
Medical System Inc, США).
Техника выполнения видеоэндоскопических
операций на толстой кишке подробно описана в ли-
тературе. После проведения видеоэндоскопической
ревизии у основания брыжейки ректосигмоидного
отдела справа рассекается париетальная брюшина,
разрез продолжается до переходной складки (ректо-
пузырной, ректоматочной), такой же разрез выпол-
няется слева. Мобилизация прямой кишки начина-
ется по задней полуокружности между собственной
фасцией прямой кишки и фасцией крестца, соблю-
дая принципы футлярности. Визуализируется и се-
лективно выделяется нижняя брыжеечная артерия.
Для лигирования сосудов используются различные
методы: наложение клипс эндоклипаторами, зава-
ривание сосудов генератором LigaSure с помощью
эндоскопических насадок 5 мм и 10 мм (рис. 2).
Нижний уровень резекции контролируется хирур-
гом со стороны промежности пальцевым ректальным
исследованием при низком расположении опухоли.
При лапароскопически ассистированных резекциях
выполняется нижнесрединная лапаротомия разре-
Креативная хирургия и онкология
26
ОПЫТ НАУЧНЫХ И ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ
зом длиной до 7–10 см в зависимости от толщины
подкожной жировой клетчатки. Проводится ручное
пальпаторное определение нижней границы опухо-
ли. Отступя 5 см дистальнее нижнего края опухоли
линейным степлером (Contour), прямая кишка пере-
секается, препарат удаляется через лапаротомный до-
ступ. Анастомоз формируется аппаратным способом.
Выполняется перитонизация и дренирование малого
таза, производится послойное ушивание раны.
При лапароскопической резекции после пересе-
чения кишки на уровне дистальной границы резек-
ции выполняется минилапаротомия в левой под-
вздошной области до 3 см длиной, в рану выводится
резецируемый отдел кишки, и выполняется резек-
ция толстой кишки. В приводящий отдел вводится
головка от одноразового сшивающего аппарата и
фиксируется кисетным швом, после чего головка
погружается в брюшную полость, и формируется
аппаратный анастомоз. Проверяется герметичность
анастомоза под видеоэндосокпическим контролем.
С учетом того, что перитонизация малого таза не
производится, при необходимости выполняется на-
ложение превентивной трансверзостомы.
При экстирпации прямой кишки техника моби-
лизации не отличается от вышеописанной. После
пересечения сигмовидной кишки в левой подвздош-
ной области извлекается порт, доступ расширяется
и формируется концевая сигмостома. Промежност-
ный этап выполняется стандартно с ушиванием про-
межностной раны и дренированием пресакрального
пространства. Повторно накладывается карбоксипе-
ритонеум, дренируется малый таз, целостность тазо-
вой брюшины не восстанавливается (рис. 3).
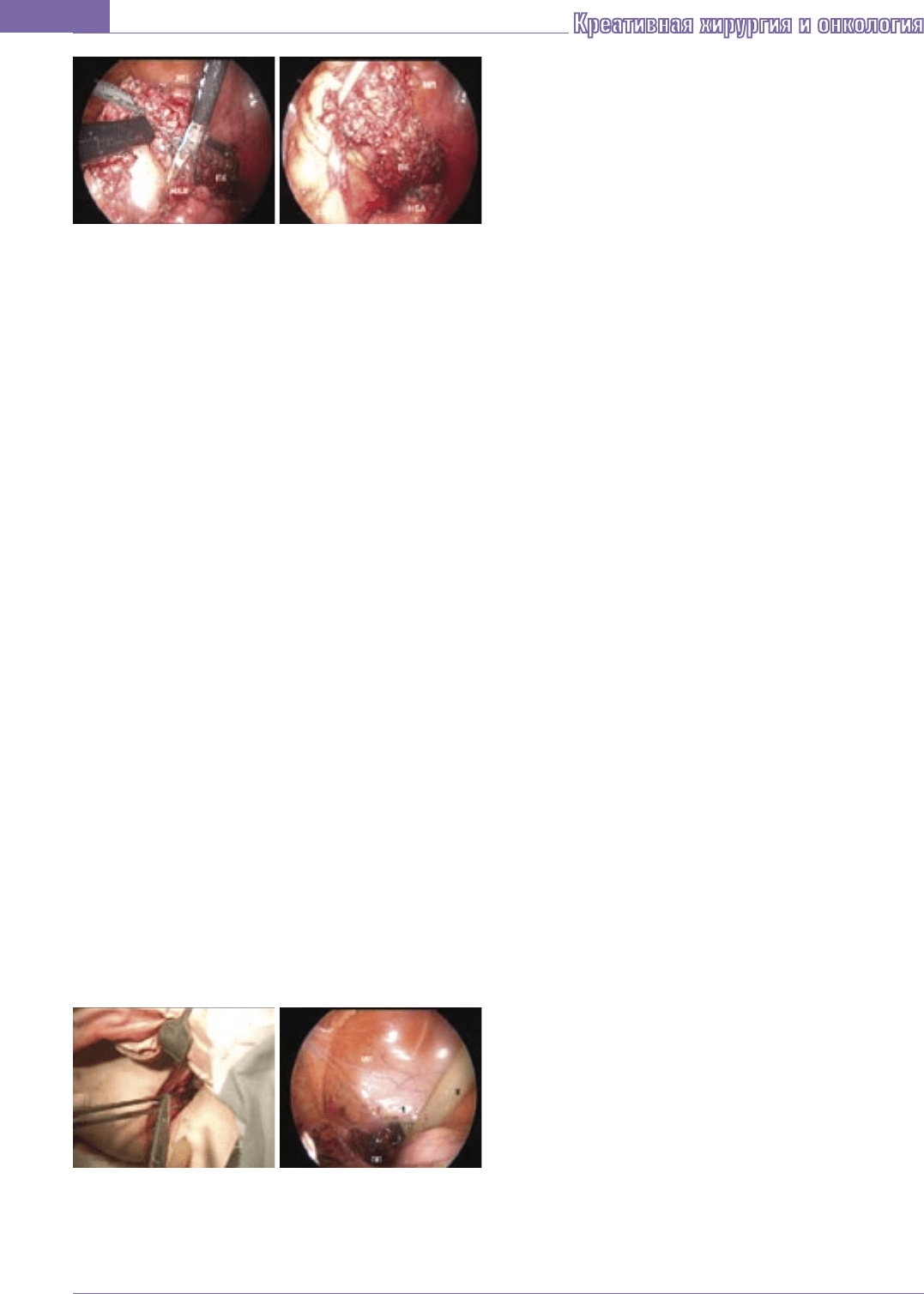
Рис. 3. Справа – ушивание промежностной раны,
слева – вид малого таза после дренирования
пресакрального пространства (ПП) двумя
активными дренажами со стороны промежности (1)
и брюшной полости (2)
Интраоперационные осложнения отмечены у
двух больных: при ранении артериальных сосудов
(верхняя ректальная артерия при мобилизации,
правая наружная подвздошная артерия при смене
порта) выполнить гемостаз эндоскопически не уда-
лось, произведена конверсия.
Все случаи анестезиологического пособия про-
текали при стабильных гемодинамических показа-
телях, пробуждение с последующим переводом на
спонтанное дыхание и экстубацией трахеи выпол-
нялись в операционной в течение 6-18 минут после
окончания операции, включая пациентов старшей
возрастной группы и при наиболее длительных
операциях. Послеоперационное наблюдение и мо-
ниторинг подтверждает отсутствие постнаркозной
депрессии сознания и дыхания. Ни в одном случае
не потребовалось проведения продленной искусст-
венной вентиляции лёгких, что могло бы противо-
речить концепции высокотехнологичного оператив-
ного вмешательства. В раннем послеоперационном
периоде осложнений и летальных исходов не было.
Отмечены более ранние сроки активизации боль-
ных и раннее восстановление кишечной моторики.
Применение режима респираторной подде-
ржки с обратным соотношением фаз вдоха и выдо-
ха позволяет минимизировать негативное влияние
карбоксиперитонеума во время эндоскопических
операций при колоректальном раке на биомехани-
ку дыхания. Низкопоточная ингаляционная анесте-
зия севофлураном в комбинации с эпидуральным
обезболиванием ропивакаином гидрохлорида с
изменением режимов вентиляции легких непос-
редственно во время искусственного повышения
внутрибрюшного давления - качественный и бе-
зопасный метод анестезиологической защиты па-
циента при эндохирургических вмешательствах на
толстой кишке.
Лапароскопически ассистированные операции
также позволяют значительно снизить травматич-
ность доступа и активизировать больных в ранние
сроки после операции, что имеет особое значение у
пожилых и ослабленных больных.
Таким образом, комбинированная низкопоточ-
ная анестезия на основе севофлурана и эпидураль-
ное обезболивание ропивакаином гидрохлорида
является адекватным методом анестезиологическо-
го пособия, а описанный выше мониторинг обес-
печивает необходимый уровень безопасности
пациента при проведении эндохирургических вме-
шательств при раке толстой кишки. Увеличение
продолжительности операции не влияет на течение
послеоперационного периода, а снижение травма-
тичности доступа позволяет активизировать боль-
ных в более ранние сроки. Более тщательный отбор
и обследование больных на дооперационном этапе
даст возможность снизить частоту конверсий.
Список литературы
1. Губайдуллин P.P., Бутров А.В. Общие закономер-
ности гемодинамических реакций на быстрое измене-
ние внутрибрюшного давления // Анестезиология и
реаниматология. - 2003. - № 3. – С. 20-23.
Рис. 2. Лигирование и пересечение нижней брыже-
ечной артерии (НБА) LigaSure 5 мм (слева). Справа
– мобилизованная прямая кишка (ПК) и культя НБА.
(МП – мочевой пузырь, СК – сигмовидная кишка)

Креативная хирургия и онкология
27
ОПЫТ НАУЧНЫХ И ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ
2. Караваев Б.И., Головкин А.С., Стамов В.И. При-
менение методики транспищеводной эхо- и доппле-
рографии для оценки изменений показателей гемоди-
намики при лапароскопических операциях // Вестник
интенсивной терапии. - 2006. - №3. – С. 48 - 51.
3. Качалов Н. Безопасность операции: новая па-
радигма развития эндохирургии // Эндоскопическая
хирургия. - 2006. - Т. 12. - №2. - С. 50-55.
4. Лебединский К.М., Шевкуленко Д.А. Прогнос-
тическое моделирование реакции кровообращения на
спинальную анестезию // Анестезиология и реанима-
тология. - 2005. - №4. – С. 23-26.
5. Овечкин A.M., Федоровский Н.М. Регионарная
анестезия: реалии и перспективы // Современные тех-
нологии в анестезиологии-реаниматологии. — 2003.
- С. 83-84.
6. Пучков К.В., Хубезов Д.А. Малоинвазивная хи-
рургия толстой кишки: Руководство для врачей. – М.:
ОАО «Издательство «Медицина», 2005. – 280 с.
7. Старков Ю. Г., Шишкин К. В. Профилактика тром-
боэмболических осложнений при лапароскопической
холецистэктомии. - М.: “Русский путь”, 2003. - 71 с.
8. Саидов А.С, Батиров У.Б., Сабиров Д.М. Тради-
ционная искусственная вентиляция легких у больных с
интраабдоминальной гипертензией // Вестник интен-
сивной терапии. - 2005. - №6. – С. 87-89.
9. Сапанюк А.И., Бухарин А.И., Куклова И.И., Ма-
медов Х., Хачатрян Д.В. Прогнозирование гемодина-
мического ответа при выполнении лапароскопичес-
ких холецистэктомий // Эндоскопическая хирургия.
- 2006. - Т. 12. - №2 . - С . 96.
10. Alpiger S., Helbo-Hansen H.S., Ording Н. Efficacy of
A-line AEP Monitor as a tool for predicting acceptable tracheal
intubation conditions during sevoflurane anaesthesia // Br.
J. Anaesth. - 2005. - Vol. 94. - №5. - P. 601-606.
11. Calvey T.N., Williams N.E. Principles and practice of
pharmacology for anaesthetists // Fourth Edition. - 2007.
- P. 91-95.
12. Phillips E.H., Franklin M., Carroll B.J. et al. Laparoscop-
ic colectomy // Ann Surg. – 1992. – №216. – P. 703–707.
13. Salihoglu Z., Demiroluk S., Cakmakkaya S. Influence
of the patient positioning on respiratory mechanics during
pneumoperitoneum // Middle East Anesthesiol. - 2002.
- №16(5). - P. 521 - 528.
14. Yon Нее Shim, Cheung Soo Shin, et al Optimal
end-tidal sevoflurane concentration for the removal of the
laryngeal mask airway in anesthetized adults // Anesth.
Analg. - 2005. - №101. - P.1034-1037.

Креативная хирургия и онкология
28
ОПЫТ НАУЧНЫХ И ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ
ÑÎÂÐÅÌÅÍÍÛÅ ÏÎÄÕÎÄÛ Ê ÏÐÎÔÈËÀÊÒÈÊÅ ÐÀÊÀ
ØÅÉÊÈ ÌÀÒÊÈ ÏÓÒÅÌ ÎÏÒÈÌÈÇÀÖÈÈ ÌÅÒÎÄÎÂ
ËÅ×ÅÍÈß ËÅÉÊÎÏËÀÊÈÈ
Ф.Ф. Бадретдинова, Т.Б. Трубина, В.Б. Трубин, А.Н. Додонов
ГОУ ВПО Башкирский государственный медицинский университет
Бадретдинова Флорида Фуатовна, ассистент кафедры акушерства
и гинекологии №2 БГМУ, канд. мед. наук,
450000, Россия, Республика Башкортостан, г. Уфа, 40 лет Октября, 1,
тел. 8 (347) 264-96-50,
e-mail: f.badretdinova@mail.ru
В статье приводятся результаты комплексного обследования женщин с лейкоп-
лакией шейки матки. Изучение результатов лечения лейкоплакии в сравнительной
группе явилось обоснованием для создания научно обоснованной программы опти-
мизации лечебных, профилактических и реабилитационных мероприятий.
Разработана и применена программа оптимизации хирургического лечения с
использованием новых технологий (разработаны и применены 2 новые технологии
реконструктивно-пластических операций), позволившая улучшить результаты про-
филактики рака шейки матки.
Ключевые слова: лейкоплакия, программа оптимизации лечения, рак, шейка
матки.
CURRENT APPROACHES IN TREATMENT
OF LEUKOPLAKIA OF THE CERVIX
F.F. Badretdinova, T.B. Trubina, V.B. Trubin, A.N. Dodonov
Bashkir State Medical University
The paper presents results of a comprehensive survey of women with leukoplakia of
the cervix. Study results of treatment of leukoplakia in the comparative group was the
justification for establishing a science-based program for optimization of treatment,
preventive and rehabilitative measures. Developed and applied program of optimization of
surgical treatment using new technologies (two new technologies of reconstructive plastic
surgery were developed and implemented) which can improve the results for cervical
cancer prevention.
The key words: leukoplakia, a program of treatment optimization, cancer, cervix.
Введение
Лейкоплакия занимает особое место в структу-
ре заболеваний шейки матки. Данные литературы о
частоте лейкоплакии в структуре заболеваний шей-
ки матки вариабельны от 5,2% до 12,5%. Лейкопла-
кия шейки матки имеет большое значение с точки
зрения возникновения и развития злокачествен-
ных заболеваний. Злокачественная трансформация
многослойного плоского эпителия, по данным лите-
ратуры, наблюдается у 31,6% больных с лейкопла-
кией шейки матки [3]. В настоящее время наиболее
приемлемой для клиницистов считается клинико-
эндоскопически-морфологическая классификация
И.Я. Яковлевой и Б.Г. Кукутэ, в которой простая
лейкоплакия без атипии относится к фоновым про-
цессам, а лейкоплакия с атипией – к предраковым
состояниям.
Лейкоплакия шейки матки – это заболевание,
которое характеризуется нарушением основных
функций многослойного плоского эпителия и воз-
никновением ороговения. Морфологически лей-
коплакия характеризуется избыточным ороговени-
ем, паракератозом и акантозом [3].
В зависимости от интенсивности процесса оро-
говения, от плотности и толщины ороговевшего слоя
различают нежную, тонкую, легко слущивающуюся
лейкоплакию и толстую, грубую бородавчатую, в виде
плотных бляшек, спаянных с подлежащей тканью [1,3].
По современным представлениям лейкоплакия
шейки матки является полиэтиологическим забо-

Креативная хирургия и онкология
29
ОПЫТ НАУЧНЫХ И ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ
леванием, в основе которого лежит ряд предрас-
полагающих факторов, таких как инфекционные
заболевания гениталий, нарушения иммунного ста-
туса, гормонального гомеостаза, травматические
акушерские повреждения шейки матки (при родах,
абортах), неадекватное лечение патологии шейки
матки в анамнезе [1].
В последние годы местный иммунитет вызывает
особый интерес клиницистов и иммунологов. Дока-
зана роль иммунных механизмов в возникновении
и развитии предраковых заболеваний шейки мат-
ки. Развитие патологии шейки матки происходит на
фоне дисбаланса иммунного статуса, что, в основ-
ном, проявляется снижением функциональной ак-
тивности Т-лимфоцитарной системы [3].
Современная диагностика лейкоплакии шейки
матки складывается из комплексной оценки различ-
ных методов обследования больных. У большинс-
тва больных заболевание протекает бессимптомно
и выявляется лишь на профилактическом осмотре
или гинекологическом обследовании по поводу
других заболеваний. Лишь незначительное число
женщин предъявляет жалобы на обильные бели и
контактные кровотечения, которые настораживают
в отношении малигнизации. Для диагностики лей-
коплакии наиболее информативны кольпоскопи-
ческие и гистологические методы [5].
В настоящее время применяются различные
методы лечения больных с лейкоплакией шейки
матки: диатермохирургический, криогенное воз-
действие, высокоинтенсивное лазерное излучение,
хирургическое лечение. Ряд авторов не отрицают
возможность применения медикаментозных мето-
дов [5]. Однако до сих пор среди клиницистов нет
единого мнения о показаниях к тому или иному виду
лечения лейкоплакии шейки матки. Спорным оста-
ется вопрос о выборе метода лечения лейкоплакии
у нерожавших женщин, у женщин с выраженной
деформацией шейки матки. По данным различных
авторов, частота рецидивов после электрохирурги-
ческого лечения составляет от 6,2% до 36,6%, пос-
ле лазерохирургического - от 4,2 до 15,6% [3].
Таким образом, существующие современные
методы лечения лейкоплакии шейки матки недо-
статочно совершенны, четко не разработана пре-
доперационная подготовка и послеоперационное
ведение с учетом сочетанных заболеваний генита-
лий. В то же время радикальные методы лечения
лейкоплакии (лазерохирургический, криохирурги-
ческий, диатермохирургический, хирургический)
не являются этиотропными способами лечения, ос-
таются только хирургическими методами, не обес-
печивающими положительного влияния на звенья
патогенеза заболевания.
Цель исследования
Улучшение результатов лечения лейкоплакии
шейки матки путем разработки и реализации ле-
чебных, профилактических и реабилитационных
мероприятий с использованием высокоинтенсив-
ного и низкоинтенсивного лазерного излучения,
применения реконструктивно-пластических опера-
ций и оптимизации предоперационной подготовки
и послеоперационного ведения.
Материалы и методы
При выполнении работы обследованы и проле-
чены 178 женщин в возрасте от 17 до 55 лет с лейкоп-
лакией шейки матки. Пациентки были разделены на
две группы: основную (80) и сравнительную (98).
В основной группе применена разработанная про-
грамма оптимизации лечебных, профилактических
и реабилитационных мероприятий с использовани-
ем лазеротерапии, реконструктивно-пластических
операций, оптимизации предоперационной под-
готовки и послеоперационного ведения. В сравни-
тельной группе лечение лейкоплакии проводилось
с использованием высокоинтенсивного лазерного
излучения согласно общепринятым установкам.
При обследовании женщин, наряду с традици-
онными, применялись следующие методы: бактери-
ологическое исследование содержимого влагалища,
уретры и цервикального канала, определение био-
ценоза влагалища, исследование местного иммуни-
тета, иммунофлюоресцентный метод (определение
хламидий, уреаплазм, микоплазм), цитологический
на АТК, эндоскопический (обзорная и расширенная
кольпоскопия), гистоморфологическое исследова-
ние биоптатата шейки матки и соскобов слизистой
оболочки цервикального канала.
Средний возраст пациенток составил 31,8±2,34
и 32,3±2,25 года. По социальному статусу более
половины (74,3%) были работающими, остальные
- учащимися (10,9%) и домохозяйками (14,8%).
Средний возраст менархе в основной и сравнитель-
ной группах составил 12,3±0,98 и 12,5±0,82 года
соответственно. На одну женщину основной и срав-
нительной группы приходилось соответственно 2,8
и 2,5 беременностей. Нерожавших было 27 юных
женщин в возрасте от 17 до 24 лет. В анамнезе все
пациентки имели экстрагенитальные заболевания:
2,4 и 2,6 на одну женщину соответственно в основ-
ной и сравнительной группах.
Лейкоплакия шейки матки сочеталась с други-
ми гинекологическими заболеваниями: вагиниты
различной этиологии диагностированы у всех об-
следованных пациенток как основной, так и срав-
нительной группы; хронические сальпингоофори-
ты (34,4% и 36,2%); миомы матки (2,5% и 3,5%),
киста яичника (1,3% и 1,4%); цервициты (83,2% и
85,4%), нарушения менструальной функции (8,3%
и 7,9%) соответственно в основной и сравнитель-
ной группах.
Результаты и обсуждение
Во всех наблюдениях, как в основной, так и
сравнительной группах имели место нарушения
биоценоза влагалища. При цитологическом иссле-
довании был подтвержден диагноз лейкоплакия
во всех наблюдениях. Результаты кольпоскопии:
простая лейкоплакия на фоне неизмененного мно-
гослойного плоского эпителия шейки матки (34,2%
и 33,4%); простая лейкоплакия в сочетании с эк-
топией (31,6% и 29,8%); лейкоплакия в сочетании

Креативная хирургия и онкология
30
ОПЫТ НАУЧНЫХ И ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ
с основой лейкоплакии (6,3% и 5,8%); лейкопла-
кия с образованием полей лейкоплакии (13,9% и
12,4%); лейкоплакия на фоне железисто-мышечной
гипертрофии шейки матки и старых глубоких раз-
рывов (13,7% и 12,6%) соответственно в основной
и сравнительной группах. При бактериологическом
исследовании содержимого цервикального канала
обнаружена различная микрофлора: кокки, стреп-
тококки, кишечная палочка, грибы рода Сandida,
микробные ассоциации. Роста не обнаружено в
2,7% наблюдений.
Результаты изучения местного иммунитета по-
казали, что у больных с лейкоплакией шейки матки
была увеличена концентрация IgA, sIgA и IgG в цер-
викальной слизи. Достоверное увеличение имму-
ноглобулинов A, sIgA и G (р<0,05) свидетельству-
ет об усилении активности местного иммунитета.
Появление IgM в цервикальной слизи у женщин с
лейкоплакией шейки по сравнению со здоровыми
пациентками указывает на инфицирование церви-
кальной слизи.
При гистологическом исследовании биоптатов
шейки матки были выявлены различные морфологи-
ческие картины: лейкоплакия шейки матки (15,9%);
выраженный акантоз (7,59%); стационарный эн-
доцервикоз с явлениями паракератоза (8,86%);
стационарный эндоцервикоз с явлениями параке-
ратоза и акантоза (24,05%); пролиферирующий эн-
доцервикоз, простая лейкоплакия (5,06%); диспла-
зия легкой степени тяжести (3,8%); стационарный
эндоцервикоз с явлениями гиперкератоза и параке-
ратоза (32,91%). Таким образом, гистологическое
исследование подтвердило диагноз лейкоплакии.
Оценку результатов лазерохирургического ле-
чения у 98 пациенток сравнительной группы про-
водили через 3 месяца. При осмотре шейки матки
в зеркалах было установлено: субконическая шейка
(26%), цилиндрическая шейка (74%), в том числе с
рубцовой деформацией – 21,6%. При кольпоскопи-
ческом обследовании установлена здоровая шейка
матки у 86 пациенток (87,8%). Рецидив лейкопла-
кии диагностирован у 12 (12,2%) пациенток на фоне
рубцоводеформированной шейки матки. Данная
подгруппа пациенток была в возрасте от 32 до 43
лет. У 12 пациенток с рецидивом заболевания име-
ли место сопутствующие гинекологические заболе-
вания (вагиниты – 12, цервициты – 12, хроничес-
кий сальпингоофорит – 5, трихомоноз – 2). У всех
12 женщин с рецидивом лейкоплакии в анамнезе
проводилось лечение фоновых заболеваний (при-
обретенная эктопия – 8, лейкоплакия – 4). Ранее
применялись следующие методы лечения: диатер-
мохирургический (7), лазерохирургический (5).
Таким образом, комплексное обследование па-
циенток с рецидивом заболевания позволяет сде-
лать заключение, что их лечение проводилось пов-
торно на фоне ранее проведенного лечения.
Изучение результатов лечения лейкоплакии в
сравнительной группе явилось обоснованием для
создания научно обоснованной программы опти-
мизации лечебных, профилактических и реабили-
тационных мероприятий, представленной тремя
этапами: первый – предоперационная подготовка;
второй – лечение с дифференцированным под-
ходом в зависимости от возраста, клинико-мор-
фологического состояния шейки матки; третий
– рациональное ведение раннего и отдаленного
послеоперационного периода.
Первый этап. В предоперационном периоде
– комплексное обследование (описано в разде-
ле «методы обследования»), проведение санации
генитального тракта в соответствии с выявленным
возбудителем согласно современным установкам и
проведением контрольного бактериоскопического
исследования мазков.
Второй этап. Дифференцированный подход к
выбору метода лечения. Лазероэксцизия с исполь-
зованием аппарата «Ромашка-2», работающего на
базе СО
2
–лазера, применяется при простой лейкоп-
лакии на 4-7 день менструального цикла: глубина
эксцизии тканей шейки матки с захватом здоровых
тканей на 3 мм, диаметр пятна - 1,5–2,5 мм, время
экспозиции - 1-5 минут.
Комбинированный метод лечения лейкоплакии
шейки матки, разработанный авторами, сводится
к одномоментному применению электроножа для
иссечения патологических тканей шейки матки и
последующего облучения раневой поверхности
высокоинтенсивным (СО
2
) лазером, целью кото-
рого является удаление термического струпа после
воздействия электроножа и образование на по-
верхности раны стерильной биологической коагу-
ляционной пленки (предупреждение образования
грубого рубца). Показания для описанного метода:
сочетание лейкоплакии шейки матки с железисто-
мышечной гипертрофией и рубцовой деформаци-
ей, рецидивирующая лейкоплакия с рубцовой де-
формацией, сочетание лейкоплакии с дисплазией.
Раны после лазерохирургического облучения зажи-
вают с меньшей лейкоцитарной инфильтрацией,
без лейкореи при сокращенной фазе экссудации и
пролиферации.
Реконструктивно-пластические операции на
шейке применяются при лейкоплакии на фоне ги-
пертрофии, удлинения и деформации шейки, обус-
ловленной старыми разрывами.
Все операции на шейке матки производятся в
первую половину менструального цикла (первые
4-7 дней), чтобы к моменту наступления очередной
менструации наступило заживление раны.
Авторами разработаны и применены 2 новые
технологии реконструктивно-пластических опера-
ций (патент на изобретение №2197909 зарегистри-
рован в Государственном реестре по изобретениям
РФ 10.02.2003; патент на изобретение №2184503
зарегистрирован в Государственном реестре по
изобретениям РФ 10.06.2002).
Третий этап. При ведении послеоперационного
периода с целью улучшения репаративных процес-
сов через 2-3 дня после радикального лечения лей-
коплакии шейки матки используются интраваги-
нальные свечи с метилурацилом (по 1 свече в день
в течение 10 дней). Облучение гелий-неоновым ла-
зером назначается через 2-3 дня после хирургичес-
