Грасси Н. Химия процессов деструкции полимеров
Подождите немного. Документ загружается.

Введение
21
С другой стороны, фотохимические реакции исследовались в интервале тем-
ператур 160—190". При температурах около 160"' полимер находится в полу-
твердом состоянии или представляет собой очень вязкую жидкость; поэтому
для диффузии осколков мономерных размеров в газовую фазу понадобятся
десятки или даже сотни секунд. Такая задержка в выделении летучих из
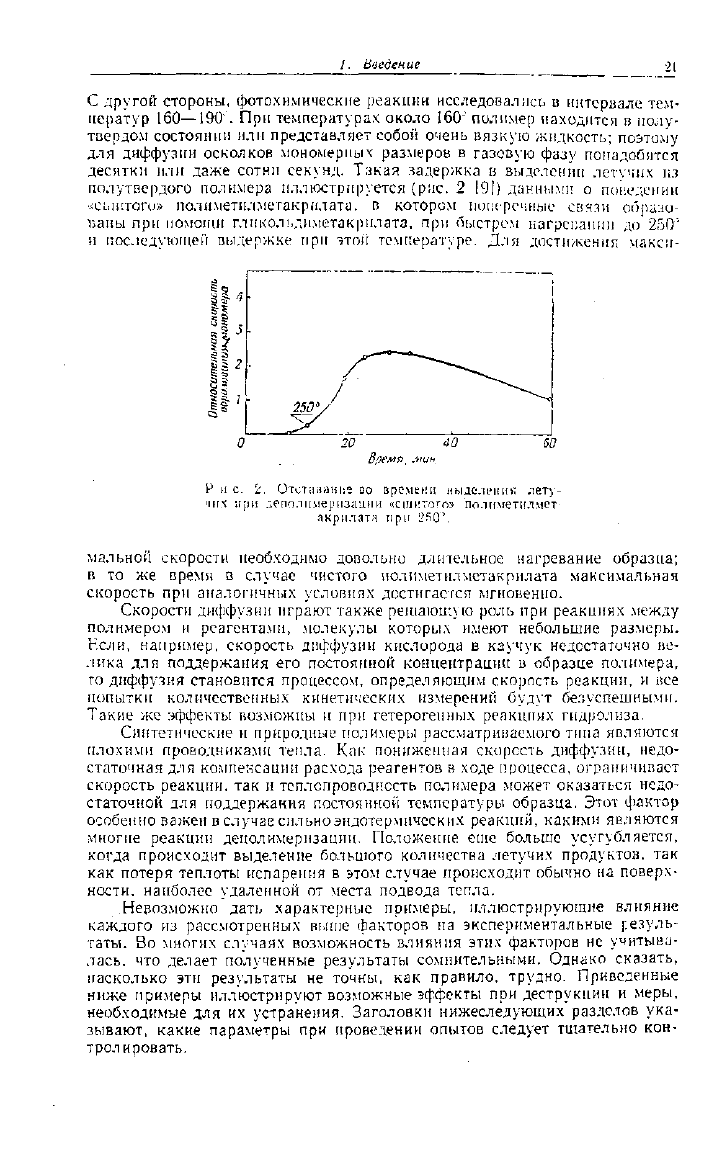
полутвердого полимера иллюстрируется (рис. 2 191) данными о поведении
«сшитого» полнметнлметакрилата. в котором поперечные связи образо-
ваны при помощи глпкольдпметакрнлата, при быстром нагревании до 250"'
и последующей выдержке при этой температуре. Для достижения макси-
мальной скорости необходимо довольно длительное нагревание образца;
в то же время в случае чистого полиметилметакрилата максимальная
скорость при аналогичных условиях достигается мгновенно.
Скорости диффузии играют также решающую роль при реакциях между
полимером и реагентами, молекулы которых имеют небольшие размеры.
Б.сли, например, скорость диффузии кислорода в каучук недостаточно ве-
лика для поддержания его постоянной концентрации в образце полимера,
го диффузия становится процессом, определяющим скорость реакции, и все
попытки количественных кинетических измерении будут безуспешными.
Такие же эффекты возможны и при гетерогенных реакциях гидролиза.
Синтетические и природные полимеры рассматриваемого типа являются
плохими проводниками тепла. Как пониженная скорость диффузии, недо-
статочная для компенсации расхода реагентов в ходе процесса, ограничивает
скорость реакции, так и теплопроводность полимера может оказаться недо-
статочной для поддержания постоянной температуры образца. Этот фактор
особенно важен в случае сильно эндотермических реакций, какими являются
многие реакции деполимеризации. Положение еще больше усугубляется,
когда происходит выделение большого количества летучих продуктов, так
как потеря теплоты испарения в этом случае происходит обычно на поверх-
ности, наиболее удаленной от места подвода тепла.
Невозможно дать характерные примеры, иллюстрирующие влияние
каждого из рассмотренных выше факторов на экспериментальные резуль-
таты. Во многих случаях возможность влияния этих факторов не учитыва-
лась,
что делает полученные результаты сомнительными. Однако сказать,
насколько эти результаты не точны, как правило, трудно. Приведенные
ниже примеры иллюстрируют возможные эффекты при деструкции и меры,
необходимые для их устранения. Заголовки нижеследующих разделов ука-
зывают, какие параметры при проведении опытов следует тщательно кон-
тролировать.
60
Р и с. 2. Отставание во времени выделения лету-
чих при деполимеризации «сшитого» полиметилмет-
акрилата при 250°.

22
/. Введение
Давление
Некоторые факторы, замедляющие диффузию летучих продуктов, вы-
деляющихся из полимера, можно устранить, проводя реакцию в высоком
вакууме. Этот метод обычно применяется при кинетических исследованиях.
Термическая деструкция политетрафторэтилена представляет интерес-
ный пример возможного влияния внешнего давления. При давлении в
несколько миллиметров может быть достигнут 100%-ный выход мономера
(C..F,).
При повышении давления увеличивается количество дпмера и появ-
ляется соединение, имеющее формулу C,F,.; при атмосферном давлении выход
этих продуктов составляет 84% от общего количества летучих продуктов
(гл.
2, табл. 8). Это явление объясняется тем, что при повышении внешнего
давления мономер, являющийся главным продуктом реакции, остается
в течение длительного времени внутри горячего полимера, вследствие чего
возрастает вероятность его участия в последующих реакциях. Протеканию
этих вторичных реакций способствует высокая температура (600'), необ-
ходимая для разрыва связей в этом полимере.
При проведении реакций, скорости которых определяются диффузией
реагентов в полимер, идеальными с точки зрения давления будут как раз
обратные условия, и поэтому при кинетических исследованиях предпочти-
тельны более высокие давления. В результате равновесная концентрация
реагента внутри полимера будет выше, а благодаря более высоким скоро-
стям диффузии будет быстрее пополняться убыль участвующего в реакции
реагента. Прекрасным примером, иллюстрирующим этот эффект, являются
не реакции какого-либо полимера, а процессы в жидких олефннах, которые
использовались как модели молекул каучука при изучении окисления моле-
кулярным кислородом (гл. 4). В этом случае растворение кислорода в жид-
кой фазе может ограничивать скорость реакции, т. е. оно играет ту же роль,
что и диффузия в случае твердых полимеров. Поэтому при определении кон-
стант скоростей всех элементарных стадий цепной реакции окисления оле-
финов необходимо проводить опыты в широком интервале давлений. Однако
полный и надежный анализ полученных данных очень труден, поскольку
процесс растворения определяет скорость реакции при низких давлениях
кислорода (гл. 4, стр. 158).
Скорость реакции
Чем меньше скорость реакции, тем медленнее тепло и реагенты должны
передаваться от одной точки к другой в результате диффузии. Поэтому при
прочих равных условиях, чем меньше скорость реакции, тем меньше вероят-
ность того, чтобы диффузионные процессы тепло- или массопередачи стали
процессами, определяющими скорость реакции. Рис. 62 (гл. 4, стр. 159),
иллюстрирующий автокаталитическую природу реакции окисления каучука
в «массе», подтверждает эту точку зрения. Низкие скорости в начальной
стадии реакции совершенно не зависят от толщины образца, и, следователь-
но,
диффузия кислорода в полимер в этом случае не определяет скорость
реакции. Однако при увеличении скорости реакции кривые, относящиеся
к образцам различной толщины, начинают расходиться, так как диффузия
уже не может обеспечить достаточной концентрации кислорода в толстом
образце.
Толщина слоя
Чем тоньше слой реагирующего полимера, тем меньше вероятность,
что диффузия будет процессом, определяющим скорость реакции. Достаточ-
ным доказательством того, что диффузия не определяет скорость реакции.
/. Введение
является независимость скорости, рассчитанной на единицу веса полимера,
от толщины образца. Это условие выполняется на начальных участках кри-
вых рис. 62 (гл. 4); последующее расхождение кривых обусловлено тем, что
более толстые образцы реагируют с меньшей скоростью, что наглядно ил-
люстрирует повышение роли диффузии как процесса, определяющего ско-
рость реакции в сравнительно толстых образцах. Эти данные показывают,
что максимальная толщина образца, применимого для количественного
изучения окисления каучука, составляет 0,25—1,0 м.и при 80—100 п давле
пни кислорода 0,05—1.0 чт НО].
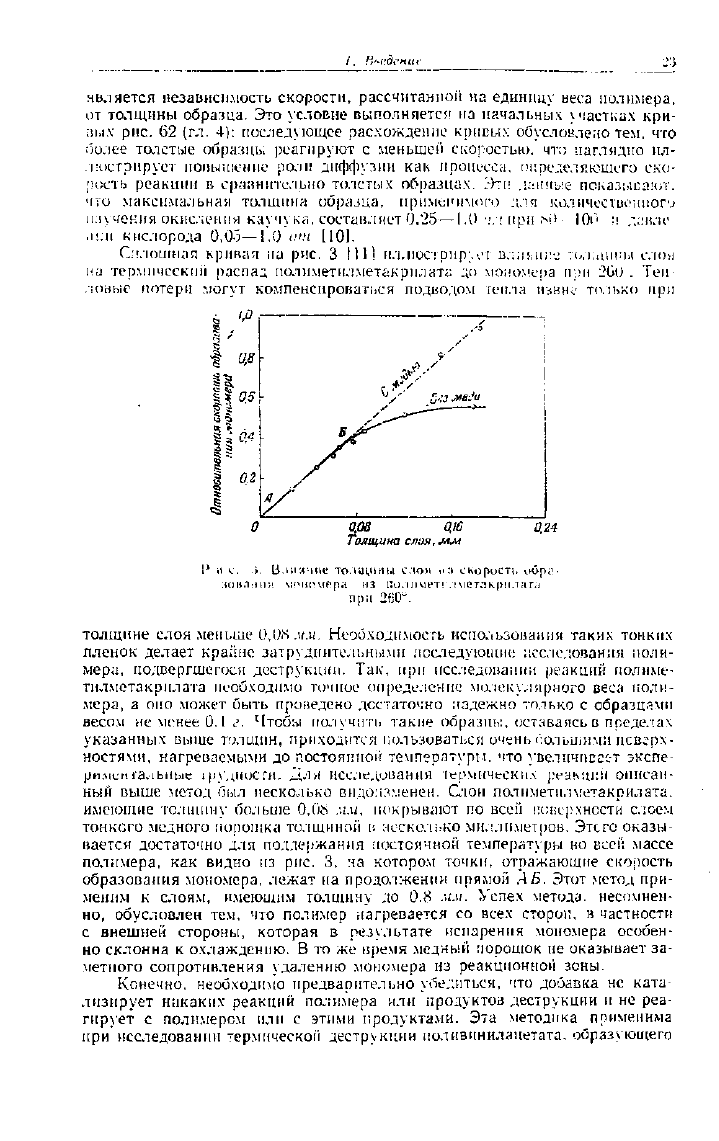
Сплошная кривая на рис. 3 111] иллюстрирует влияние толщины слоя
на термический распад иолиметилметакрилата до мономера при 260 . Теп-
ловые потери могут компенсироваться подводом тепла извне только при
толщине слоя меньше 0,ОМ .и.и. Необходимость использования таких тонких
пленок делает крайне затруднительными последующие исследования поли-
мера, подвергшегося деструкции. Так, при исследовании реакций полиме-
тилметакрнлата необходимо точное определение молекулярного веса поли-
мера, а оно может быть проведено достаточно надежно только с образцами
весом не менее 0,1 г. Чтобы получить такие образцы, оставаясь в пределах
указанных выше толщин, приходится пользоваться очень большим;! поверх-
ностями, нагреваемыми до постоянной температуры, что увеличивает экспе-
риментальные фудности. Для исследования термических реакций описан-
ный выше метод был несколько видоизменен. Слои полнметплметакрилата,
имеющие толщину больше 0,08 мм, покрывают по всей поверхности слоем
тонкого медного порошка толщиной в несколько миллиметров. Этого оказы-
вается достаточно для поддержания постоянной температуры во всей массе
полимера, как видно из рис. 3, на котором точки, отражающие скорость
образования мономера, лежат на продолжении прямой .4 6". Этот метод при-
меним к слоям, имеющим толщину до 0,8 мм. Успех метода, несомнен-
но,
обусловлен тем. что полимер нагревается со всех сторон, в частности
с внешней стороны, которая в результате испарения мономера особен-
но склонна к охлаждению. В то же время медный порошок не оказывает за-
метного сопротивления удалению мономера из реакционной зоны.
Конечно, необходимо предварительно убедиться, что добавка не ката-
лизирует никаких реакций полимера или продуктов деструкции и не реа-
гирует с полимером или с этими продуктами. Эта методика применима
при исследовании термической деструкции поливннилацетата. образующего
О
0,08 0,16
Толщина слоя, мм
0,24
| с. 3. Влияние толщины слон на скорость обра-
зования мономера из полпметнлметакрплата
при 260°

24
1.
Введение
при низких температурах в качестве летучего продукта только уксусную
кислоту [12]. Правда, наблюдается некоторая тенденция к распаду уксус-
ной кислоты, катализируемому медью, однако этот распад никогда не бывает
значительным, что позволяет сделать соответствующие поправки. Если же
медный порошок заменить железным, то уксусная кислота распадается
полностью. В то же время медь совершенно непригодна при изучении пиро-
лиза поливинилхлорнда, так как она разрушает образующийся хлористый
водород. В этом случае наиболее пригодно серебро 113].
Использование растпоров
Проводя реакции в растворе, можно избежать трудностей, обусловлен-
ных слишком низкими скоростями теплопередачи; правда, при этом возни-
кают некоторые осложнения, связанные с возможностью протекания побоч-
ных реакций с участием растворителя. Однако даже при использовании со-
вершенно инертного растворителя данные, полученные для реакций в рас-
тзоре, можно экстраполяционно применять к реакциям в твердом состоянии
только очень осторожно. Это особенно надо учитывать, например, при ра-
дикальных реакциях, в которых часто имеет место равновесие между реак-
циями разрыва и «сшивания» цепей, являющееся непосредственной мерой
относительных скоростей следующих реакций диспропорционировання:
и рекомбинации:
CR,
—
CHX —
ОН» —
СХ
—
CR, > CIL -CHX-+CH, = CX-CR
CR,
—
CX
—
CR
—
CHX \ i CR,
— CX
—CR—CHX
-J !
CR,
—
CX
—
CH,
—
CHX )
1
CR, —CX—СИ., -CHX
Скорость второй, бимолекулярной, реакции уменьшается с разбавлением
значительно быстрее, чем скорость первой. В результате процесс, приводя-
щий в твердой фазе к образованию межмолекулярных связей в полимере,
в растворе может превратиться в типичную реакцию разрыва цепей. Иссле-
дование таких процессов в растворе часто позволяет изолировать реакцию,
приводящую к деструкции молекул.
При проведении в растворе реакций окисления возникают те же затруд-
нения, что и при проведении реакций в твердом полимере: скорость раство-
рения кислорода должна быть достаточно высока, чтобы предотвратить
уменьшение его концентрации в растворе в результате реакции. Таким обра-
зом, и в этом случае желательны тонкие слои, низкие скорости реакции
и высокие давления кислорода. Однако преимуществом работы в растворе
является возможность увеличения скорости растворения реагента путем
перемешивания (при помощи механических мешалок, встряхиванием, барбо-
тированием кислорода через раствор).
Обычным критерием того обстоятельства, что диффузия не является
процессом, определяющим скорость реакции, является независимость ско-
рости реакции от степени перемешивания. Так, для проверки условий, при
которых можно определить истинные скорости окисления, Джордж, Райдил
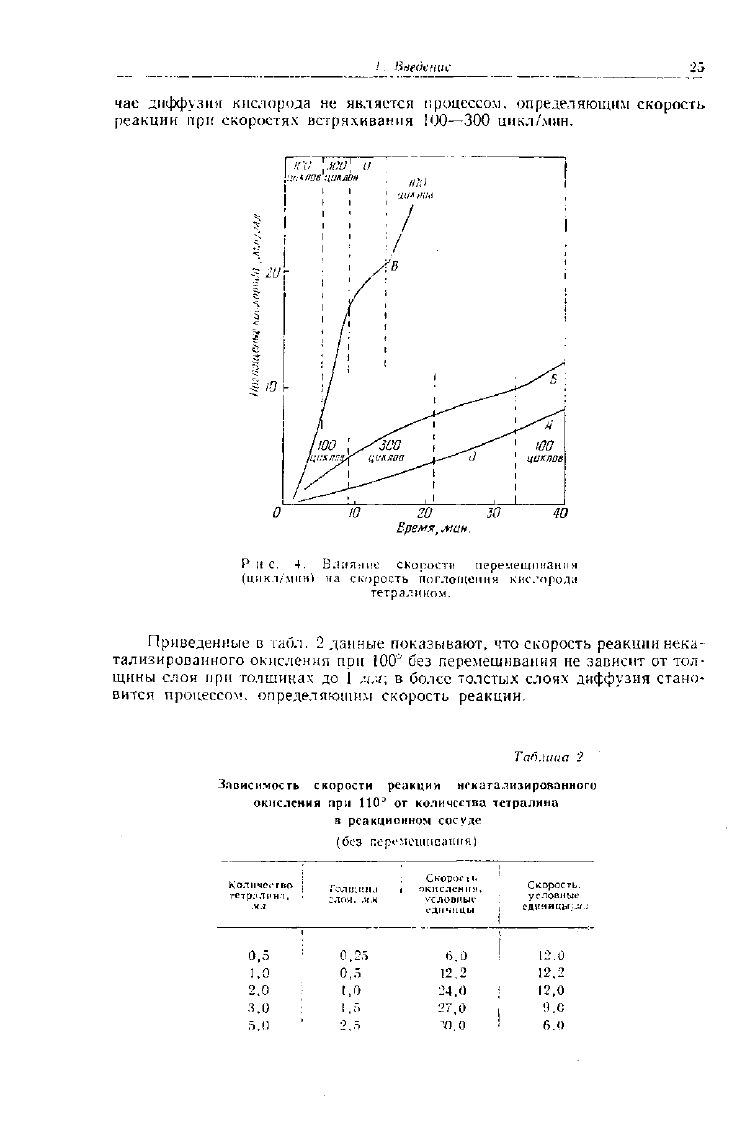
и Робертсон [14] исследовали влияние скорости встряхивания на скорость
поглощения кислорода тетралином. Экспериментальные данные для 1 г ве-
щества при 108" приведены на рис. 4, на котором кривая А соответствует
некатализированной реакции, а кривые Б и В—реакциям в присутствии
ускорителей. Низкие скорости реакции в случае А совершенно не зависят
от встряхивания, в то же время более высокие скорости в случае В повы-
шаются при увеличении скорости встряхивания. Однако и в последнем слу-
/. Введение
25
чае диффузия кислорода не является процессом, определяющим скорость
реакции при скоростях встряхивания ¡00—300 цикл/мин.
Р не. 4. Влияние скорости перемешивания
(цикл/мин) на скорость поглощения кислорода
тетралином.
Приведенные в табл. 2 данные показывают, что скорость реакции нека-
тализированного окисления при 100° без перемешивания не зависит от тол-
щины слоя при толщинах до 1 мм; в более толстых слоях диффузия стано-
вится процессом, определяющим скорость реакции.
Таблица 2
Зависимость скорости реакции нокатализированного
окисления при П0
Э
от количества тетралина
в реакционном сосуде
(без перемешивания)
Количество
тетралннл,
ТОЛНИОК!
СЛОЯ, мм
Скорость
окислен
НЯ.
условные
еДНЫШЫ
Скорость,
условные
единицы...:;.
0,5
•
,о
2,0
.1,0
5.0
0,25
0,5
1,0
6.0
12.2
24,0
27,0
ло.о
12.0
12,2
12,0
Ч.С
6.0

26 . RjiedcHm
1
л
11
т f.
p
л
т
у р
л
1.
Robert s D. Е.. J. Res. Nat. Bur. Stand.. 44. 221. 1950.
2.
Lewis E. E.. N а \ I о г M. Д.. J. Лго. Chem. Soc, 69. 1968, 1947.
.».
В a w п С. К. П.. Flic Chembtry vi Hink Polymers, p. 180, ßiitterwcrths Scienti-
fic
Publicai'Oiis.
!94v
-1.
4 e
1
v i 1
1
с II. \V.. В и г к e : t <i. Л1.. J. Poiyin. Sei.. 13. 417. 1954.
5.
С r a w i о r il .1. W C. J. Soc. l.hem. ln:i.. 6S. 201. 1949.
О, В а с Ii ni а ri tj. К et'ai.. J. О-ц. f.hcin.. 12. H'S. 1947.
Г Bulla Ii ri J. i. .•! al.. Quart. Kev.. .4. 74'' В i t о ш a t: I., oi a!.. Quart.
Rev.. S,
I
17 1954.
S. Mar\e!l (\ S.. The OtremiHn of l.ar^e Vunecule-. chap. 7. Burk R. £..
G r u m in . '. Ü.. Interscience. X. Y.. 194.,
9. G r a a s i e N.. Л1 с I v i t I e 11. U'., Proc. Roy. Soc. A199, 39, 1949.
10.
К о h m э и О. Т.. J. Phys. Cue;-.:.. 33. 226. 1929: S к e
1
t о n J. P.. 'A i n n H.,
lnd. Eng. Chem.. 38, 71. 1946; S h e
1
t о n J. R.. С о x W. L., Irul. Eng. Chem.,
45,
392. 195.У
ll.Crassic N.. Melville H.W.. Proc. Roy. Soc, A199. I. 1949.
12.
Grassie N.. Trans. Faraday Soc. 48, 379, 1952.
13.
G r a s s i e N.. M a t h e w s о n D. J., неопубликованная работа.
14.
George P.. R i d e a I E. K.. Robertson Д., Proc. Roy. Soc, AI85,
1946.

• ДЕПОЛИМЕРИЗАЦИЯ
ВВЕДЕНИЕ
Развитие промышленности пластических масс вызвало у исследо-
вателей повышенный интерес к реакциям деполимеризации полимеров.
Первые работы в этой области были посвящены исследованию кинетики гид-
ролитического разрыва молекул углеводов, при котором в качестве конеч-
ного продукта образуется мономер. Было также показано, что при нагре-
вании полистирола, наиболее широко применявшегося в то время синтети-
ческого полимера, образуется мономер с высоким выходом. Поэтому не уди-
вительно, что в первых работах по выяснению механизма реакции деполиме-
ризации синтетических полимеров в качестве модели использовался гидро-
лиз полисахаридов.
Гидролитическая деструкция, рассмотренная в гл. 3. представляет
собой процесс, протекающий по закону случая. В первом приближении мож-
но считать, что все связи между звеньями в каждой молекуле одинаково
уязвимы для гидролизующего реагента. Реакция деструкции, идущая по
такому механизму, имеет две интересные особенности. Во-первых, наблю-
дается заметное уменьшение средних молекулярных размеров, особенно
в начальной стадии процесса. Начальная среднечпс.товая длина цепи, рав-
ная,
например, 10
:1
(молекулярный вес порядка 200 ООО, если звеньями
являются остатки глюкозы), уменьшается вдвое при разрыве только 0, Г'о свя-
зей между звеньями. Во-вторых, заметные количества мономера образуются
лишь на последних стадиях реакции, так как вероятность гидролиза двух
соседних связей мала до тех пор, пока не прореагирует значительная часть
полимера.
Подробное исследование термической деполимеризации полистирола
показало, что данные об уменьшении молекулярного веса не позволяют рас-
считать количество выделившегося мономера, если исхидичь из представле-
ний о разрыве цепи по закону случая. Так, количество мономера, образую-
щегося на ранних стадиях реакции, в 10
3
—10
1
раз превышает количество,
рассчитанное по данным об уменьшении молекулярного веса 11]. Эти ре-
зультаты, а также данные, полученные при исследовании других полиме-
ров,
показали, что такая простая теория разрывов по закону случая вообще
не применима к процессам деполимеризации полимеров, полученных мето-
дами полимеризации. Общей особенностью этих двух процессов является
только наличие мономера в продуктах реакции.
ПОЛИМЕТИЛМЕТАКРИЛАТ
Введение
При рассмотрении деполимеризации в гл. 1 отмечалось, что полимет-
акрилаты при нагревании распадаются почти количественно до мономера.
Единственным исключением среди полимеров метакриловых эфиров низших
28
2.
Деполимеризация
спиртов являются эфиры, полученные этерификацнен третичных спиртов,
которые отщепляют соответствующий олефнн (например, изобутилен от
поли-трет-бутилметакрнлата) при температурах, более низких, чем те,
при которых можно было бы ожидать деполимеризацию.
Такие неизменно высокие выходы мономера как будто бы указывают на
то,
что реакции, приводящие к деполимеризации этих полимеров, сравни-
тельно не сложны. Эта кажущаяся простота в сочетании с тем, что течение
этих реакций может быть легко исследовано просто измерением количества
образовавшегося мономера, сделала метакрилаты удобными объектами, с ко-
торых началось изучение механизма и кинетики реакций деполимеризации.
На рис. 1 было показано, что полиметилметакрнлат является наиболее устой-
чивым полимером из этой группы пластиков; однако он вызывал значитель-
ный интерес как полимер, имеющий большое практическое значение.
Термическая реакция
при высоких температурах
Линейные полимеры
Первая серьезная попытка выяснить механизм термической деполиме-
ризации полиметилметакрилата была предпринята Вотиновым. Кобеко
и Марее.м {21. Ошибочность вывода о том, что при реакции происходит раз-
0 шо
Деполимеризация да
мономера,
%
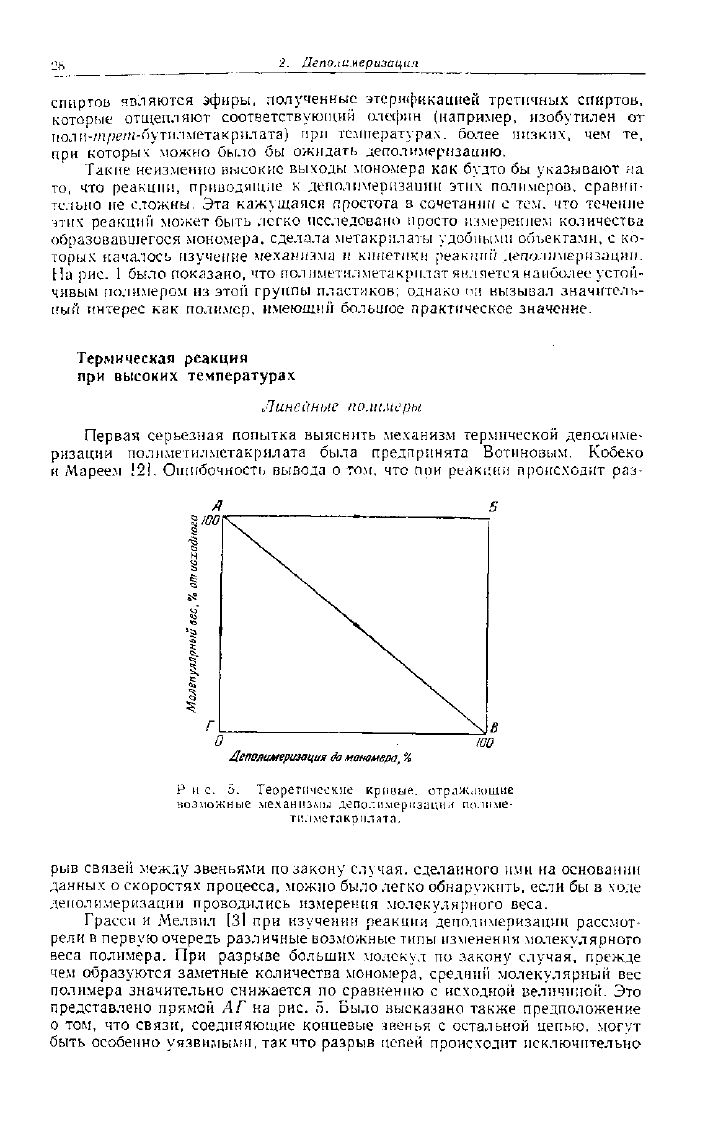
Р и с. 5. Теоретические кривые, отражающие
возможные механизмы деполимеризации полпме-
тилмстакрилата.
рыв связей между звеньями по закону случая, сделанного ими на основании
данных о скоростях процесса, можно было легко обнаружить, если бы в ходе
деполимеризации проводились измерения молекулярного веса.
Грасси и Мел вил [3] при изучении реакции деполимеризации рассмот-
рели в первую очередь различные возможные типы изменения молекулярного
веса полимера. При разрыве больших молекул по закону случая, прежде
чем образуются заметные количества мономера, средний молекулярный вес
полимера значительно снижается по сравнению с исходной величиной. Это
представлено прямой АГ на рис. 5. Было высказано также предположение
о том, что связи, соединяющие концевые звенья с остальной цепью, могут
быть особенно уязвимыми, так что разрыв цепей происходит исключительно
Полиметилметакрилат
29
по этим связям. Такой процесс был назван «ступенчатой деполимеризацией»;
уменьшение молекулярного веса в этом случае должно было бы быть пропор-
ционально количеству образовавшегося мономера (см. рис. 5, прямая АВ).
Третьим возможным механизмом деполимеризации является процесс,
обратный реакции полимеризации. В этом случае инициирование сводится
к образованию свободных радикалов в результате разрыва цепи. Затем лтн
полимерные радикалы быстро отщепляют мономерные единицы и в конце
і і . , ^
О ,20 40 60 80 ¡00
Деполимеризация
до
мономера,
%
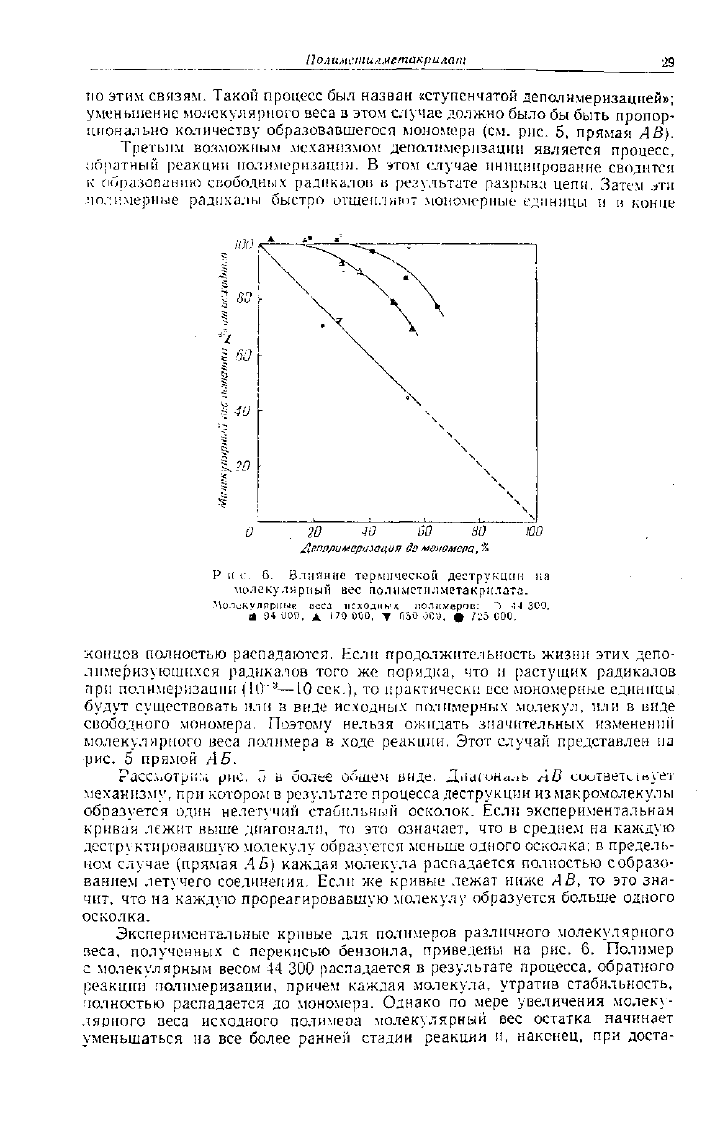
Р и с. 6. Влияние термической деструкции на
молекулярный вес полпметилметакрплата.
Молекулярные псса исходных полимеров: -М 300,
а 94
иОО.
X
170
ООО, т Г)50 000, 0 /25
ООО.
концов полностью распадаются. Если продолжительность жизни этих депо-
лимеризующихся радикалов того же порядка, что и растущих радикалов
при полимеризации (10~
а
—10 сек.), то практически осе мономерные единицы
будут существовать или в виде исходных полимерных молекул, или в виде
свободного мономера. Поэтому нельзя ожидать значительных изменений
молекулярного веса полимера в ходе реакции. Этот случай представлен на
рис.
5 прямой АБ.
Рассмотрим рис. Г) в более общем виде. Диагональ АВ соответствует
механизму, при котором в результате процесса деструкции из макромолекулы
образуется один нелетучий стабильный осколок. Если экспериментальная
кривая лежит выше диагонали, то это означает, что в среднем на каждую
деструктпровавшую молекулу образуется меньше одного осколка; в предель-
ном случае (прямая .45) каждая молекула распадается полностью с образо-
ванием летучего соединения. Если же кривые лежат ниже АВ, то это зна-
чит, что на каждую прореагировавшую молекулу образуется больше одного
осколка.
Экспериментальные кривые для полимеров различного молекулярного
веса, полученных с перекисью бензоила, приведены на рис. 6. Полимер
с молекул'ярным весом 44 300 распадается в результате процесса, обратного
реакции полимеризации, причем каждая молекула, утратив стабильность,
полностью распадается до мономера. Однако по мере увеличения молеку-
лярного веса исходного полимера молекулярный вес остатка начинает
уменьшаться на все более ранней стадии реакции и, наконец, при доста-

30
Деполимеризация
точно высоких молекулярных весах экспериментальные точки ложатся на
диагональ. Невероятно, чтобы механизм реакции изменялся при изменении
молекулярного веса. С другой стороны, это явление можно легко объяснить
протеканием реакции обрыва цепи, прежде чем произойдет полный распял,
макромолекулы. Рост полимерных цепей обычно прекращается в результате
взаимодействия пар радикалов, которые или соединяются друг с другом,
или дпспропорцнонпруют. Аналогичная реакция возможна и а случае дест-
рукции ценен, обусловленной
i
икледовател ьньп
s
отрывом мономериы\
звеньев от цепи. ¡ 1ри увеличении исходного молекулярного веса распад
нее большей части деструктирующнхея молекул прекращается в результате
i гон реакции; такой обрыв происходит до тех мор. пока размер всех очень
больших молекул не уменьшится до определенной величины. Снмха,
Уо.1.1
и Б.татц [4] обработали математически эту схему и дали удовлетворительное
качественное объяснение экспериментальным кривым, полученным Грасси
и Мелвилом. Подробнее эта работа рассмотрена на стр. 04 и сл.
Можно ожидать, что молекулярные веса полимеров, имеющих не очень
высокий начальный молекулярный вес, будут несколько уменьшаться уже
з самом начале реакции. Однако эти очень малые изменения трудно обна-
ружить, что осложняется еще и широким распределением по молекулярным
весам, характерным для этих полимеров. Так, например, полимер, имеющий
молекулярный вес 179 ООО, содержит определенное количество небольших
молекул, способных к полной деструкции. Поэтому ход экспериментальной
кривой определяется двумя факторами: с одной стороны, удаление малых
молекул приводит к увеличению молекулярного веса, с другой—частичная
деструкция больших молекул уменьшает его.
Общим свойством, а также обычным методом определения свободно-
радикальных цепных реакций является их ингибирование сравнительно
небольшими количествами некоторых веществ. Низкие давления и высокие-
температуры, при которых проводится деполимеризация, заставляют при-
менять в качестве ингибиторов только нелетучие соединения. Низкомолеку-
лярные хиноны и другие вещества, применяемые обычно в качестве ингиби-
торов полимеризации, быстро улетучиваются из зоны реакции. Установлено,
что низкой летучестью в сочетании со строением, необходимым для ингиби-
рования, обладают некоторые стабильные при высоких температурах антра-
хпионовые красители; я частности, показано, что 1,4-диаминоантрахинон
о
:¡ NH.
С i
•У
í
:
; :
/V/
С :
íl NH.
;
О
является эффективным ингибитором реакции деполимеризации. Дини-
трил тетрафенилянтарной кислоты также был использован в качестве ин-
гибитора фотоинициированной реакции, которая будет рассмотрена ниже.
Изменение молекулярных весов и возможность ингибирования являются
доказательством радикальной природы реакции, однако эти данные не
дают никаких определенных указаний о месте начального разрыва, приво-
дящего к образованию свободных радикалов. Возможны два крайних случая:
1) разрыв цепи происходит только по закону случая, 2) разрыв цепи проис-
ходит преимущественно на концах цепи. В обоих случаях начальная ско-
рость реакции должна быть пропорциональна произведению числа мест
в образце, в которых возможно инициирование, на число молекул мономера.
