Дамаскин Б.Б., Петрий О.А., Подловченко Б.И. и др. Практикум по электрохимии
Подождите немного. Документ загружается.


мации можно пояснить следующим образом. Так как в водородной об-
ласти в первом приближении [см. уравнение (3.95а)1
г
~
н
* (3.104)
ТО
с\Е
Г
-V р .
йЕ
г
(3.105)
а поскольку степень заполнения
поверхности водородом равна
вн
Л
Н
то
й
Е
г
(3.106)
Предположим, что каждый
из пиков в водородной области
отвечает адсорбции водорода
по изотерме Лэнгмюра:
I
(3.107)
е.
1-е,
н
2
где Р — константа адсорбцион-
ного равновесия. В соответ-
ствии с уравнением Нернста
сПпрн 2Р ••
1ЛП
— (3.108)
АЕ
Г
ЯТ
Рис. 3.35. Ячейка для изучения адсорб-
ции ионов меди на гладкой платине
а потому из уравнения (3.107)
следует
&Е
Г
ЯТ
(3.109)
Условием максимума на I, С
г
-кривой является —^-==0 или, соглас-
но (3.106),
Из уравнения (3.109) получаем
<1
2
0«
/72
&е1
Я*Т 2
(3.110)
откуда следует, что максимум^ тока соответствует 0н = 1/2. При этом
ток в максимуме согласно (3.106) и (3.109)
1 р*
*шах =
4
V
^н
в
н
(1
—0
Н
).
(3.111)
(3.112)
101$
ят
Из уравнения (3.107) и уравнения Нернста Е
г
— ^р 1п/?н
2
можно
получить зависимость между Е
т
и 0
Н
в виде
ят ят / е„ \
(ЗШ)
Так как потенциал максимума /:
г
-кривой "
ЯТ
= (3.114)
то расчет I, 5"
г
-кривой выполняют далее следующим образом. Рассчи-
тывают по уравнению (3.112) зависимость / от 0
Н
. По заданным значе-
ниям 0
Н
рассчитывают Е
г
по уравнению (3.113) и строят I, ^-кривую.
Аналогичные операции выполняют для каждого из максимумов водо-
родной области и, суммируя рассчитанные кривые, описывают водо-
родный участок потенциодинамической кривой.
Такой же расчет можно выполнить, предположив, что адсорбция
водорода отвечает двум изотермам Фрумкина с различными парамет-
рами. Изотерму Фрумкина для адсорбции водорода представим в ви-
де
• (З.П5)
1-е
н
Из этого уравнения следует
ят ят е
н
ят
Е
г
1пр——•— 1п
1
__
е
+ -у- 2«в
н
. (3.116)
(3.117)
Так как при выполнении изотермы Фрумкина
/
а9
н _
р 9
н
О
—
е
н)
&Е
Г
ЯТ [I —2а 8
Н
(1
—6ц)] '
то ток в потенциодинамических условиях равен
р* ОТТ —
н 1_2ае
н
(1-е
н
) • <
ЗП8
>
Легко убедиться, что и в этом случйе максимальный ток достигается
при 0
Н
==
1
/
2
и тогда
а
ЯТ ят
— (3.120)
Расчет г, 5
г
-кривой пс( изотерме Фрумкина проводят следующим об-
разом. Из экспериментальной кривой определяют /
тах
для одного
201

из максимумов и, задавшись величиной Лн, рассчитывают а по урав-
нению (3.119). Зная а и Е
Гг тах
, находят 1п|3, после чего для каждого
выбранного 8
Н
по уравнениям (3.118) и (3.116) вычисляют ток десорб-
цйи водорода и соответствующие им потенциалы. Проводят такие рас-
четы для каждого из водородных максимумов в отдельности, а затем
находят суммарную 5
г
-кривую.
2. ИЗУЧЕНИЕ ПОВЕДЕНИЯ АДАТОМОВ МЕДИ
НА ПЛАТИНОВОМ ЭЛЕКТРОДЕ
Потенциодинамический метод может быть использован вместо ме-
тода кривых заряжения при выполнении любой из работ, которые пред-
ставлены на с. 185—196. При достаточно высоких скоростях разверт-
ки потенциала 20 мВ/с) при выполнении этих работ вместо плати-
нированного платинового электрода можно использовать гладкий
платиновый.
Потенциодинамический метод имеет определенное преимущество
в информативности перед методом кривых заряжения, как и любой
метод определения производной искомой функции перед интеграль-
ным методом. Это особенно проявляется при изучении образования
адсорбированных атомов — адатомов, возникающих из ионов раст-
вора при их адсорбции на поверхности электродов до того, как ока-
зывается термодинамически возможным образование соответствующей
фазы («дофазовое» выделение вещества). Фактически рассмотренную
выше адсорбцию водорода и кислорода на платине можно трактовать
как процесс образования адатомов, так как слой Я
адс
возникает из
ионов Н
3
0
+
значительно раньше (на 0,35—0,4 В), чем начинается
выделение молекулярного водорода, а адсорбированные атомы кисло-
рода образуются за счет разряда молекул воды или ионов ОН
-
" при
потенциалах, лежащих отрицательнее обратимого кислородного на
0,5—0,6 В. Образование адатомных слоев (иод субмонослоев) до дости-
жения равновесных потенциалов соответствующих систем описано в
настоящее время при адсорбции большого числа катионов (Си
2
*.,
РЬ
2
+, ВР+, 5п
2
+, Щ1+, Т1+ и др.) и анионов (Г~, 5
е
- и др.) на
электродах из Р1; КЬ, Рс1, Аи и других материалов. Причина этого яв-
ления состоит в том, что энергия связи между металл ом-субстратом и
атомом-адсорбатом оказывается во многих случаях значительна боль-
ше, чем энергия связи между атомами в фазе адсорбата.
Для изучения поведения адатомов меди на гладком платиновом
электроде используют ячейку, изображенную на рис. 3.33. В этой ячей-
ке предусмотрен сосуд I) для введения добавок в используемый фоно-
вый раствор, причем раствор, содержащий добавку, может быть пред-
варительно очищен от кислорода воздуха продуванием инертного газа.
Первоначально центральную часть ячейки А, отделения вспомога-
тельного электрода В и электрода сравнения С заполняют 0,5 М раст-
вором Н
2
50
4
. Рабочий электрод, тщательно промытый бидистиллятом,
вводят в ячейку, электролит продувают инертным газом, а через
192
электрод сравнения продувают водород. После того как устанавли-
вается потенциал электрода сравнения, с помощью потенциостата
с треугольной разверткой начинают циклировать потенциал рабочего
электрода в интервале Е
г
= 0,05-М ,4 В со скоростью 50—100 мВ/с.
Циклируют рабочий электрод до получения воспройзводимой потенцио-
динамической кривой, типичной для поликристаллического гладко-
го платинового электрода (рис. 3.36, кривая 1). На гладком платино-
вом электроде в некотором интервале скоростей развертки потенциала
можно наблюдать в водород- /
ной области три максимума
десорбции водорода. С повы-
шением скорости развертки
средний максимум смещается
в анодном направлении и
сливается с более анодным о -
максимумом прочно связан-
ного водорода.
Прекратив циклирование
потенциала, устанавливают
Е
т
= 0,30 В и добавляют
раствор сульфата меди на Л
1
фоне 0,5 М Н
2
30
4
в исследуе-
мый раствор в таком ^количе-
Рис 3 36
Потенциодинамические кривые
егве, что в рабочей части гладкого платинового электрода
*
в 0,5 М
ячейки образуется раствор Н
2
50
4
(1) и в присутствии 10~
2
М
состава 0,5 М Н
2
50
4
+ 10-
2
М
Си8
°4 <*) .
Си50
4
. Снова циклируют
потенциал электрода, но в интервале 0,30—1,4 В и после установления
воспроизводимой /, 21
г
-кривой фиксируют ее. Выбор в качестве исход-
ного потенциала 0,30 В позволяет избежать образования фазы меди
на платине.
Типичная потенциодинамическая кривая в присутствии адато-
мов меди в сравнении с фоновой кривой представлена на рис. 3.36
(кривая 2). Десорбция адатомов меди характеризуется тремя пиками,
причем средний из них имеет перегиб (пологое плечо) на восходящей
ветви. Уменьшая исходный потенциал Е
т
, можно наблюдать появление
максимума, связанного с десорбцией фазового осадка меди, который
располагается перед максимумами десорбции адатомов. Этот макси-
мум растет по мере осаждения фазы меди (например, при задержке
потенциала в течение некоторого времени при Е
г
< 0,30 В), тогда
как максимумы десорбции адатомов при этом не изменяются.
Вычисляют и сопоставляют площадь под водородным участком
потенциодинамической кривой и площадь, соответствующую десорб-
ции адатомов меди (заштрихована на рис. 3.36). Учитывая, что при
десорбции адатомов меди освобождается два электрона, отношение
этих площадей можно использовать как меру степени заполнения по-
верхности медью.
7 Зак. 434 102

Очень сложная форма кривой десорбции адатомов меди свиде-
тельствует как о наличии на поверхности различных дискретных ти-
пов адсорбционных центров, отличающихся энергией связи Р1 —
— Си
адс
, так и о возможном образовании, по крайней мере на неко-
торых местах, второго слоя адатомов меди, поведение которого, как
и первого слоя, отличается от поведения фазы меди.
Определение адсорбции анионов серной кислоты на платинированной плати-
тине методом измерения электропроводности. Образование двойного электричес-
кого слоя сопровождается переходом ионов из объема раствора на границу раз-
дела электрод/раствор или, наоборот, от границы раздела в объем жидкой фазы.
Рис. 3.37. Ячейка для изучения адсорбции кислоты на
платиновой сетке методом измерения электропровод-
ности:
А
—
рабочая часть ячейки, В
—
отделение для измерения элек-
тропроводности, С— электрод сравнения
Это явление может быть зафиксировано, если электрод имеет большую поверх-
ность, а объем раствора, находящегося в контакте с электродом, невелик, так
что изменение состава раствора оказывается в пределах, регистрируемых анали-
тическими методами, методом радиоактивных индикаторов или каким-либо фи-
зическим методом. В некоторых системах для этой цели может быть применен
метод измерения электропроводности раствора.
Для проведения измерения адсорбции ионов с помощью метода электропро-
водности используют ячейку, изображенную на рис. 3.37. Так как электропро-
водность зависит от температуры, центральную часть ячейки (А) и отделение
для измерения электропроводности (В) необходимо термостатировать, пропус-
кая термостатирующую жидкость через рубашки, которыми снабжены эти части
ячейки. В данной ячейке анодное и катодное пространства не разделены для того»
чтобы исключить искажение результатов за счет процесса переноса электролита
при пропускании тока.
Электропроводность измеряют с помощью двух жестко закрепленных парал-
лельных друг другу слабо платинированных электродов в виде дисков диамет-
192 7 Зак. 434 193
ром 0,5 см, находящихся в сосуде В*на расстоянии
1 — 1,5
см. Объем раствора в
рабочей части ячейки А составляет ~20 мл.
В качестве рабочего электрода используют свернутую в рулончик Р1/Р1-сет-
ку с видимой поверхностью 50—80 см
2
и истинной поверхностью не менее 5 м
2
.
Для определения истинной поверхности измеряют кривую заряжения исследуе-
мого электрода в 0,5 М Н
2
50
4
. Электрод должен быть подвергнут предваритель-
ной «тренировке» для того, чтобы его истинная поверхность в ходе измерения
адсорбции ионов не изменялась.
Рабочий электрод, тщательно промытый бидистиллятом, помещают в ячейку,
заполненную 2,5 • Ю
-3
М раствором Н
2
50
4
. Ячейку термостатируют при 25 °С.
Через ячейку продувают водород до приобретения рабочим электродом обрати-
мого водородного потенциала. Затем часть раствора передавливают в сосуд В и
измеряют электропроводность этой порции раствора, после чего порцию возвра-
щают в рабочую часть ячейки. Эту операцию проводят несколько раз до полу-
чения воспроизводимых результатов.
С помощью потенциостата задают электроду потенциал Е
т
= 0,05 В, вы-
держивают электрод при этом потенциале до тех пор, пока ток не упадет практи-
чески до нуля и при отключении потенциостата потенциал электрода не будет из-
меняться. Через раствор продувают инертный газ. Снова измеряют электропро-
водность раствора, как это описано выше. Затем опять увеличивают потенциал
на 50 мВ и повторяют измерения. После достижения Е
г
~ 0,9 В начинают по-
степенно уменьшать потенциал- до Е
г
= 0. Сопоставляют кривые, снятые при
увеличении и последующем уменьшении потенциала.
Изменение концентрации кислоты в растворе при изменении потенциала
рассчитывают по формуле
А
0
—А —к (Со—с), (3.121)
где Л
0
и А — электропроводность исходного раствора при Е
т
= 0 В и раствора
при заданном значении потенциала (в Ом""
1
); с
0
и с — концентрации исходного
раствора и раствора при заданном потенциале; к — коэффициент пропорциональ-
ности. Для определения к в сосуде В измеряют электропроводность 4—5 раст-
воров серной кислоты, концентрация которых лежит в интервале 5 • 10~
4
—
3- Ю
-3
М, и строят калибровочную прямую Л — с.
В растворах без добавки посторонней соли гиббсовская адсорбция кислоты
на электроде Г
НА
равна гиббсовской адсорбции ионов водорода, которая, в
свою очередь, равна гиббсовской адсорбции анионов:
Г
НА
= Г
Н+
=Г
А
_. (3.122)
Гиббсовскую адсорбцию анионов рассчитывают по уравнению
(с с)1М0
3
, _
Г
А
_
=
—
1
— , (3.123)
5
И
сТ '
где V — объем раствора в рабочей части ячейки, мл; з
ист
— истинная поверх-
ность электрода, см
2
; концентрации выражены в моль/л.
При Е
т
= 0 гиббсовская адсорбция Г
А
__ равна нулю, что можно обнаружить
экспериментально, если исследуемый электрод, насыщенный водородом, ввести
в контакт с сухим электродом, также насыщенным водородом. Равенство Г
А
_ =
= 0 объясняется тем, что при небольших Е
т
поверхность платины заряжена от-
рицательно, причем отрицательные заряды возникают за счет ионизации части
адсорбированного водорода, а образующиеся при этом ионы водорода составля-
ют обкладку двойного слоя. Таким образом, состав раствора и его концентрация
при образовании двойного слоя не изменяются.
По полученным данным строят график в координатах Г
А
_ — Е
т
,

Зависимость адсорбции анионов серной кислоты от потенциала платинового
электрода проходит через максимум при Е
т
= 0,8 В (рис. 3.38). Снижение ад-
сорбции при Е
г
> 0,8 В связано с вытеснением анионов адсорбирующимися на
электродах атомами кислорода, образующими диполи Р* — О
адс
, отрицатель-
ные концы которых обращены к раствору.
Дифференцируя Г
д
_, В
г
-кривую в интервале Е
т
— 0,4—0,7 В, получают
величину Р^ которую в первом приближении можно приравнять емкости
с\Е
Т
НГ
А
_ <*
А0
двойного электрического слоя. Сравнивая Р
.
п
- с , т. е. с поляризационнои
йс
г
и Ь
г
емкостью электрода, можно убедиться,что в сернокислых растворах на платине
имеет место перекрывание областей адсорб-
ции водорода и кислорода.
Аналогично может быть определена за-
висимость адсорбции других кислот (соля-
ной, бромоводородной и т. д.) от потенциала.
Определение зависимости свободного за-
ряда поверхности платинированной платины
от потенциала методом адсорбционных кри-
вых. Методы кривых заряжения и потенци-
одинамических кривых позволяют найти за-
висимость полного заряда поверхности
т> ^.оо о я (точнее, АР') от потенциала электрода. Для
нис. Зависимость адсорб- определения зависимости свободного заряда ц
ции анионов серной кислоты
от похенциала
используют метод адсррбцион-
от потенциала платинирован-
ных кривых> который
"
б
ыл предложен А. Н.
ного платинового^ электрода в ф
румк
и
иньш
,
А
.
И
Шлыгиным и В. М. Медве-
р створе до-ш м довским. Метод основан на регистрации изме-
24
нения концентрации водородных (или гидро-
ксильных)^ионов, т. е. гиббсовской адсорбции ионов водорода Г
н+
при об-
разовании двойного электрического слоя в растворе, содержащем избыток по-
стороннего электролита. В таком растворе катионы электролита полностью вы-
тесняют ионы водорода из двойного слоя и, следовательно, Л
н+
= 0. При этом
в соответствии с уравнением (3.11)
= (3.124)
По условию электронейтральности в растворе соли СА, подкисленном кисло-
той НА,
Г
Н+
= Г
А
__-Г
С+
, (2.125)
где Г
с+
— гиббсовская адсорбция катионов. Так как в растворе с большим
избытком соли ионы водорода не участвуют в образовании ионной обкладки
двойного слоя, то
д = РТ
А
„-РТ
с+
(3.126)
(3.127)
Таким образом, определив Г
н+
, находят свободный заряд поверхности.
Для определения свободного заряда поверхности методом адсорбционных
кривых используют ячейку, изображенную на рис. 3.39. Отличительная особен-
ность этой ячейки — наличие сосуда О сравнительно большого размера, в кото-
ром рабочий раствор можно насыщать водородом или инертным газом. Рабочее
отделение А следует откалибровать (поставить на нем несколько отметок, соот-
192
ветствующих различным объемам электролита в интервале 15—25 мл). Калиб-
ровка осуществляется путем добавления в сухую ячейку, содержащую сухой
электрод, порций воды из бюретки.
Наличие капилляра Луггина в данной ячейке не обязательно, так как по-
тенциал электрода измеряют при отсутствии поляризующего тока.
Для измерений используют стабилизированный предварительной тренйров-
кой Р1/Р1-электрод с истинной поверхностью не менее 5 м
2
.
В качестве рабочего раство-
й- II
ИгМг
•^Ъг? А
( " \\//
ра в данной работе применяют
0,01 М НС1 + 1 М КС1, в кото-
2
Г*
ром, как следует из дальнейшего, т
можно найти чисто «двойнослой
ную» область потенциалов и по-
тенциал нулевого полного заряда
платинового электрода. При изме-
рениях необходимо соблюдать та-
кую последовательность опера-
ций. <
1. Электрод после предвари-
тельной очистки (см. работу 1 с.
185) тщательно промывают биди-
стиллятом, встряхивают от капе-
лек воды и подсушивают, прика-
саясь кончиком электрода к филь-
тровальной бумаге.
2. Помещают электрод в су-
хую ячейку. В сосуд О заливают
порцию рабочего раствора 0,01 М
НС1 + 1 М КС1 и пропускают
через сосуд О водород цз электро-
лизера.
3. Из центральной части
ячейки в течение 15—20 мин то-
ком инертного газа вытесняют
воздух, затем пропускают водо-
род в течение 40—60 мин.
4. Из сосуда О вводят в со-
суд А определенную порцию ра-
бочего раствора (до одной из
меток), продувают водород через
сосуд А для тщательного переме-
шивания раствора.
5. Отбирают порцию рас-
твора из отделения
А /
и титруют
ее раствором щелочи. Наиболее
точные результаты получают при
титрований горячего раствора с
фенолротом в качестве индикато-
ра. Титруют несколько порций раствора из сосуда А и несколько порций ис-
ходного раствора. По результатам титрования рассчитывают гиббсовскую
адсорбцию ионов водорода и, следовательно, свободный заряд поверхности
при Е
т
= 0В.
6. Заполняют сосуды С и В раствором из центральной части ячейки и сосуда
В и пропускают водород через электрод сравнения.
7. Через рабочую часть А и сосуд Б продувают азот» включают анодный ток
(0,1—0,2 мА/см
2
видимой поверхности) и доводят потенциал электрода до Е
г
=
= 0,1 В. Постепенно уменьшая ток, стабилизируют потенциал при заданном
значении, добиваясь такого состояния, чтобы потенциал электрода оставался
Рис. 3.39. Ячейка для измерения адсорб-
ционных кривых на Р1/Р1-электроде:
А — отделение рабочего электрода; В
—
вспомо-
гательный электрод; С — электрод сравнения;
О — сосуд для замены раствора в ^отделении А
7 Зак. 434 104
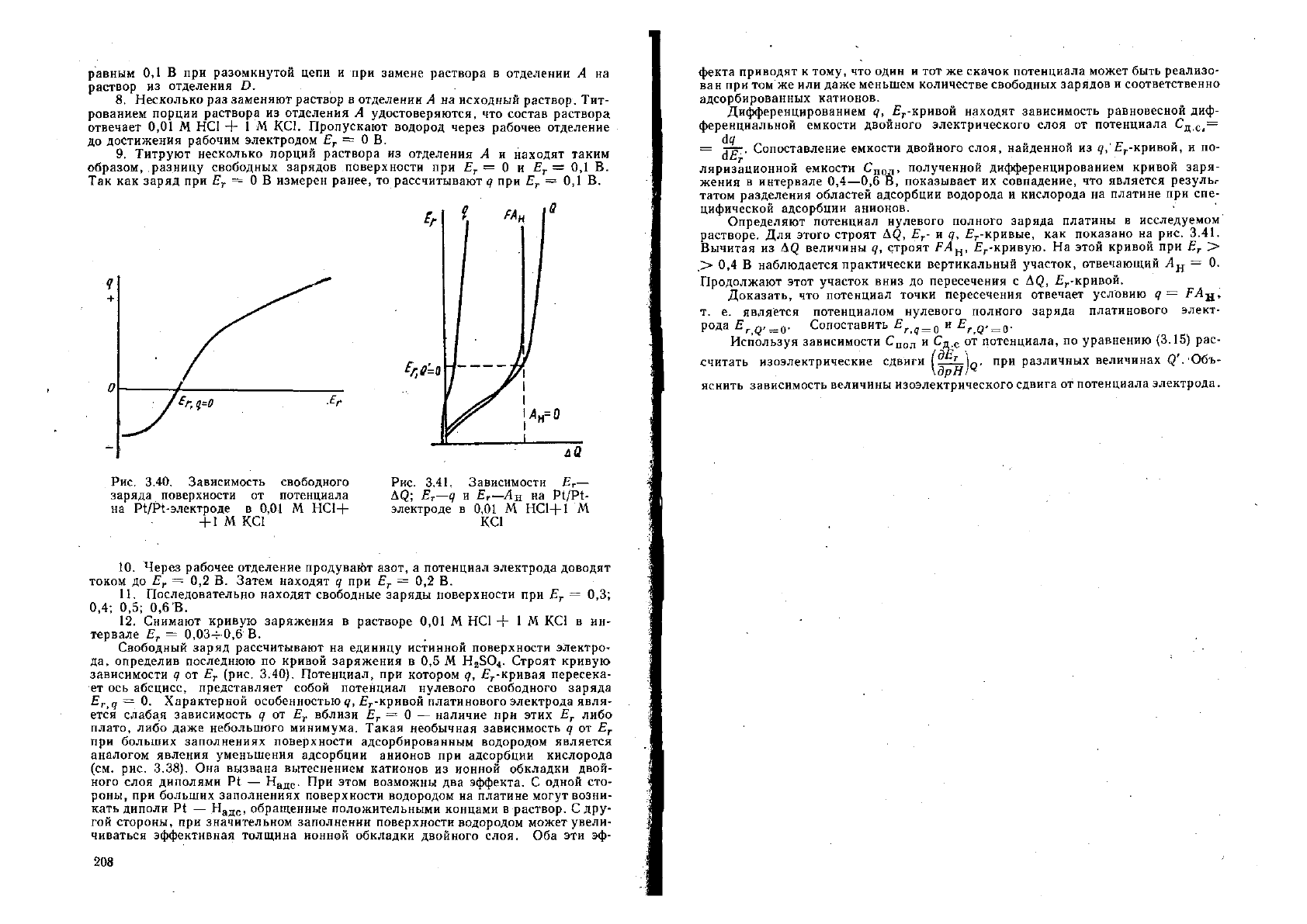
равным 0,1 В при разомкнутой цепи и при замене раствора в отделении А на
раствор из отделения О.
8. Несколько раз заменяют раствор в отделении А ла исходный раствор. Тит-
рованием порции раствора из отделения А удостоверяются, что состав раствора
отвечает 0,01 М НС1 + 1 М КС1. Пропускают водород через рабочее отделение
до достижения рабочим электродом Е
г
= 0 В.
9. Титруют несколько порций раствора из отделения А и находят таким
образом, разницу свободных зарядов поверхности при Е
г
= 0 и = 0,1 В.
Так как заряд при Е
т
= 0 В измерен ранее, то рассчитывают ц при Е
т
= 0,1 В.
'Сг.^о
Рис. 3.40. Зависимость свободного
заряда поверхности от потенциала
на Р1/Р1-электроде в 0,01 М НС1+
+ 1 М КС1
Рис. 3.41. Зависимости Е
г
—
АС; Ег—Я.т Е
г
—АЦ на Р4/Р1-
электроде в 0,01 М НС1+1 М
КС1
10. Через рабочее отделение продувают азот, а потенциал электрода доводят
током до Е
г
= 0,2 В. Затем находят
<7
при Е
г
= 0,2 В.
11. Последовательно находят свободные заряды поверхности при Е
г
= 0,3;
0,4; 0,5; 0,6 В.
12. Снимают кривую заряжения в растворе 0,01 М НС1 + 1 М КС1 в ин-
тервале Е
г
= 0,03-5-0,6- В.
Свободный заряд рассчитывают на единицу истинной поверхности электро-
да, определив последнюю по кривой заряжения в 0,5 М Н
2
30
4
. Строят кривую
зависимости
<7
от Е
г
(рис, 3.40). Потенциал, при котором <7, /Г
г
-кривая пересека-
ет ось абсцисс, представляет собой потенциал нулевого свободного заряда
~ 0- Характерной особенностью
<7,
Я
г
-кривой платинового электрода явля-
ется слабая зависимость <7 от Е
т
вблизи Е
т
— 0 — наличие при этих Е
т
либо
плато, либо даже небольшого минимума. Такая необычная зависимость ц от Е
т
при больших заполнениях поверхности адсорбированным водородом является
аналогом явления уменьшения адсорбции анионов при адсорбции кислорода
(см. рис. 3.38). Она вызвана вытеснением катионов из ионной обкладки двой-
ного слоя диполями Р1 — Н
адс
. При этом возможны два эффекта. С одной сто-
роны, при больших заполнениях поверхности водородом на платине могут возни-
кать диполи Р1 — Н
адс
, обращенные положительными концами в раствор. С дру-
гой стороны, при значительном заполнении поверхности водородом может увели-
чиваться эффективная толщина ионной обкладки двойного слоя. Оба эти эф-
105$
фекта приводят к тому, что один и тот же скачок потенциала может быть реализо-
ван при том же или даже меньшем количестве свободных зарядов и соответственно
адсорбированных катионов.
Дифференцированием <7, Я
г
-кривой находят зависимость равновесной диф-
ференциальной емкости двойного электрического слоя от потенциала С
д>с<
=
= Сопоставление емкости двойного слоя, найденной из <7,\Е
г
-кривой, и по-
ляризационной емкости С
пол
, полученной дифференцированием кривой заря-
жения в интервале 0,4—0,6 В, показывает их совпадение, что является резуль-
татом разделения областей адсорбции водорода и кислорода на платине при спе-
цифической адсорбции анионов.
1
Определяют потенциал нулевого полного заряда платины в исследуемом
растворе. Для этого строят Е
т
- и ц, /Г
г
-кривые, как показано на рис. 3.41.
Вычитая из АС? величины <7, строят Р.А
Н
, Е
г
-кривую. На этой кривой при Е
г
>
> 0,4 В наблюдается практически вертикальный участок, отвечающий Л
н
= 0.
Продолжают этот участок вниз до пересечения с А<2, Е
г
-кривой.
Доказать, что потенциал точки пересечения отвечает условию
<7
= РА
н
,
т. е. является потенциалом нулевого полного заряда платинового элект-
рода
=
Сопоставить Е
пд==0
и
Используя зависимости С
пол
и С
д
.
с
от потенциала, по уравнению (3.15) рас-
считать изоэлектрические сдвиги при различных величинах <2'. Объ-
\дрНп
яснить зависимость величины изоэлектрического сдвига от потенциала электрода.

Глава 4
ЭЛЕКТРОХИМИЧЕСКАЯ КИНЕТИКА
фТеоретические основы
# Электрохимическая кинетика на ртутном капельном электроде
1^!™Г
ХИМИЧеСКаЯ К|шетика на
вращающемся дисковом электроде
•Электрохимическая кинетика на стационарном электроде бе/разм сшива-
• Импедансный метод изучения электрохимической кинетики
§ 4.1. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ
Скорость электрохимической реакции (фарадеевского процесса)
определяется числом заряженных частиц (электронов или ионов) пе-
реходящих в единицу времени границу между электродом и раство-
ром и отнесенных к единице поверхности электрода. Так, например
скорость катодной реакции
определяется числом электронов, переходящих в единицу времени с
единицы поверхности платинового электрода на катионы трехвалент-
ного железа, а скорость анодной реакции
Си~+ 2е- (Си) +Си
2
+
определяется числом катионов Си
2
+, переходящих в раствор в едини-
цу времени с единицы поверхности медного электрода.
Следует иметь в виду, что на границе электрод/раствор одновре-
менно с указанными процессами протекают и обратные реакции
окисления Ре
2
^ до Ре
3
+ и восстановления Си
2
+ до Си
0
. Эксперимен-
тально это можно установить с помощью соответствующих радиоак-
тивных изотопов. Таким образом, в общем случае электрохимическую
реакцию записывают в виде
Ох + шг- (М) (Д)
Суммарная скорость реакции (А) определяется плотностью фара-
деевского тока ^
н
I -Л, (4,1)
где I — скорость прямого (катодного) процесса, А/м
2
; 7— скорость
обратного (анодного) процесса.
106$
Формула (4.1) соответствует выбору положительного знака для
катодного тока, поскольку при
*
> г величина *
ф
> 0. Наоборот, для
анодных электрохимических реакций ь> г и I
<ь
< 0, В условиях
электрохимического равновесия ц = 0, а ( - I = /
0
, где /
0
~~ плот-
ность тока обмена. При помощи радиоактивных изотопов можно непо-
средственно измерить скорость превращения Ох* в Неё* в условиях
электрохимического равновесия.
Если электрохимическая реакция протекает в стационарных усло-
виях, то заряд электрода ц и поверхностные концентрации А^ раз-
личных компонентов на границе электрод/раствор не изменяются во
времени. В этих условиях протекающий через электрохимическую
цепь ток / равен плотности фарадеевского тока *ф, умноженной на
площадь поверхности электрода 5. Таким образом, с методической
точки зрения исследование электрохимической кинетики в стацио-
нарных условиях осуществляется наиболее просто,
В нестационарных условиях величины ^ и А / зависят от времени
I и общий измеряемый ток 7 уже не равен В самом деле, положи-
тельный фарадеевский ток 1
Ф
связан с расходом Ох и образованием
Ней [см. реакцию (А)1; причем в реакций участвуют как адсорбиро*
ванные частицы Ох, так и частицы, поступающие из объема раствора,
а продукт реакции Кед распределяется между поверхностью электрода
и объемом раствора. Следовательно,
= + (4.2)
(где /ох и /р
е
а — потоки веществ Ох и Кед у поверхности электрода.
Одновременно часть подводимого к электроду тока затрачивается на
заряжение его поверхности. Плотность тока заряжения равна *
8
=
= —дц!д1, где знак минус показывает, что принятый положитель-
ный катодный ток уменьшает заряд ц на поверхности электрода. Об-
щая плотность тока I = + а потому
Если Ох и Кед специфически адсорбируются на поверхности элект-
рода, то заряд
<7
зависит от поверхностных концентраций Ло
х
и Л^есь
В этих условиях разделить полные заряды ф" = ц + пРАо
х
и 0,' =
~ ц — пРАъел
На
отдельные составляющие с помощью одних только
электрических измерений экспериментально невозможно. А посколь-
ку, как следует из уравнения (4.3),
дСГ д<3'
ЫеЛ-
Н
^
то из величины полученной в опыте, невозможно выделить и ско-
рость фарадеевского процесса ц. Для решения этой проблемы необ-
ходимы неэлектрические методы, с помощью которых можно было

бы регистрировать зависимость А
0х
и
от
*
в очень короткие про-
межутки времени. Такую возможность открывают оптические методы
изучения поверхности электродов, однако к настоящему времени эта
проблема остается открытой.
Если же Ох и Ней не обладают специфической адсорбируемостью
на|границе электрод/раствор, то при избыточной концентрации фоно^
вого электролита Ло
х
^ ^Кей ^ 0. В этом случае
I «/ф—д<7/д/, (4.5)
где ток заряжения —дц!д1 можно определить, либо измеряя его в чис-
том растворе фона, либо экстраполируя значения * к I = 0 (в предпо-
ложении, что процесс заряжения двойного слоя происходит быстрее
фарадеевского процесса).
Любая электрохимическая реакция представляет собой сложный
многостадийный процесс. В самом деле, реагирующее вещество йз
объема раствора должно вначале подойти к поверхности электрода
(етад*№ массопереноса), затем войти в двойной электрический слой
(стадия адсорбции), а после непосредственно электрохимической ста-
дии переноса заряда через границу электрод/раствор (стадия разряда—
ионизации) продукты реакции должны десорбироваться с поверхности
электрода и уйти в объем раствора (стадии десорбции и массопереноса).
Во многих случаях электрохимическую реакцию сопровождают стадии
химического превращения реагирующих веществ и (или) продуктов
реакции, которые могут протекать как в объеме раствора вблизи элект-
рода (гомогенные химические стадии), так и на поверхности электрода в
адсорбционном слое (гетерогенные химические стадии). Кроме того,
если в электрохимической реакции участвуют твердые или газообраз-
ные вещества, то процесс осложняется стадиями образования или раз-
рушения новой фазы (например, процессы электроосаждения и элект-
рорастворения металлов, электролиз воды и др.).
/ Как и для любого многостадийного процесса, скорость электрохими-
ческой реакции лимитируется наиболее медленной из последователь-
ных стадий. Это означает, что закономерности суммарного процесса
определяются кинетическими закономерностями лимитирующей ста-
дии. Зная последние, можно, во-первых, на основании эксперимен-
тальных данных для суммарного процесса выявить его лимитирующую
стадию, а, во-вторых, изменяя условия проведения электрохимической
реакции, изменять ее скорость. В дальнейшем мы рассмотрим кине-
тические закономерности лишь двух основных стадий электрохимичес-
кого процесса: стадии массопереноса и стадии разряда — иониза-
ции, — предполагая, что все остальные стадии протекают практи-
чески обратимо.
Массоперенос реагирующего вещества к электроду и продуктов
реакции от электрода в объем раствора может осуществляться по трем
механизмам: диффузией, миграцией и конвекцией. При этом два по-
следних механизма не имеют самостоятельного значения, так как
всегда лишь накладываются на основной диффузионный механизм
107$
переноса. Так, влияние электрического-поля на перемещение заряжен-
ных частиц в диффузионном слое (миграция) можно формально опи-
сать с помощью эффективных коэффициентов диффузии, а ускорение
массопереноса за счет размешивания раствора (конвекция) можно
передать эквивалентным уменьшением толщины диффузионного слоя.
Первые теоретические представления о закономерностях диффузион-
ной кинетики электродных процессов были сформулированы В. Нернс-
том на рубеже XIX и XX вв.
Предположим, что электрохимическая реакция (А) протекает на
большом плоскрм электроде и лимитируется скоростью массоперено-
са веществ Ох и Кед по механизму диффузии. При отсутствии специфи-
ческой адсорбции веществ Ох и Ней (а также в условиях стационарной
диффузии) зависимость фарадеевского тока ц от потенциала электрода
может быть найдена на основе следующих трех уравнений диффузи-
онной кинетики:
1ф
= п Р Э
0х
(д с
0х
/дх)
хяв0
=— п Р Э
ш
(дс
Пе6
/дх)
х
^
0
, (4.6)
кт Г с
Ох
(х = 0) ]
Я
==Е
о
+
__
1п
—^ — , (4.7)
дс
Ох _
п
д
2
Сф дс
Яей
д*с
яы
— дх* ' }
4
'
В)
где х — расстояние от поверхности электрода; с
0х
и — концент-
рации веществ Ох и Кед, которые являются функциями х и 1\ Б
0х
и
— коэффициенты диффузии; Е
ь
— стандартный равновесный
потенциал для реакции (А).
Уравнение (4.6) получается из сочетания закона Фарадея с первым
законом диффузии Фика; оно означает, что скорость электрохимичес-
кой реакции определяется скоростью диффузионных потоков реаги-
рующего вещества к электроду и продукта реакции от электрода. Урав-
нение (4.7) представляет собой приближенную форму уравнения Нернс-
та (2.47). Оно означает, что равновесие стадии разряда—ионизации в
условиях замедленной стадии массопереноса не нарушается, а изме-
нение потенциала электрода Е по сравнению с его равновесным значе-
нием Е обусловлено отличием концентраций с
0х
(
х
= 0) и с#
ей
(х = 0)
от их объемных значений с&
х
и Поэтому говорят, что поляриза-
ция электрода в условиях лимитйрующей стадии массопереноса име-
ет концентрационный характер. Наконец, система уравнений (4.8)
отражает второй законг диффузии Фика и позволяет найти функции
со
х
(х, I) и си
ей
(х, (), если заданы одно начальное й два гранич-
ных условия для каждого из веществ. Знание этих функций дает
возможность рассчитать с
0х
(х = 0), с
Яеа
(х = 0), (дс
Ох
/дх)
х==0
,
(дсъ
еа
/дх)
Хв=
о и после их подстановки в. уравнения (4.6) и (4.7) по-
лучить зависимость от Е, т. е. поляризационную кривую электро-
химического процесса.
I 1ш\
1
*

Предположим, что начальные и граничные условия соответствуют
потенциостатическому методу проведения эксперимента, при котором
задают некоторый потенциал электрода Е = соп$1 и регистрируют либо
стациойарный ток, либо зависимость от времени; затем то же самое
повторяют при других Е — сопз!. В этих условиях, как следует из
уравнений (4.6)—(4.8), уравнение поляризационной кривой имеет
вид
ехр [пР {Е
-Е
1/г
)/ЯТ} .
Н-ехр [пР(Е-Е
1/2
)/КТ]
(4.9)
где г
{
°р и — предельные диффузионные токи соответственнно
по электровосстановлению вещества Ох (когда с
0х
(х = 0) '= 0) и по
Рис. 4.1. Обратимая ка-
тодно-анодная волна,
рассчитанная по уравне-
нию (4.9)
?
Рис. 4.2. Зависимость концентрации
электроактивного вещества от рас-
стояния до поверхности электрода в
условиях предельного диффузионно-
го тока
электроокислению вещества К её (когда ск
е
а (я = 0) = 0); Ех
/%
— по-
тенциал, при котором /ф = [*<°
х
> — *<
к
^>]/2 (потенциал полуволны).
В нестационарных условиях при построении поляризационной
кривой токи 1ф, и должны соответствовать вполне опре-
деленному времени I после наложения на электрод заданного значе-
ния Е = сопз!. ^
Рассчитанная по уравнению (4.9) поляризационная кривая при-
ведена на рис. 4.1. Как видно из рисунка, фарадеевский ток стремит-
ся к /<°
х)
или—
п
р
И
потенциалах, которые соответственно ли-
бо значительно отрицательнее 2?1/
2
, либо значительно положитель-
нее Е1/
2
. Физический смысл выхода диффузионного тока на предел
связан со стремлением к нулю поверхностной концентрации электро-
активных веществ: при со
х
(х = 0) 0 и
при скеа (л: = 0) 0, В этих условиях зависимость концентрации
электроактивного вещества от расстояния до поверхности электрода
имеет вид, представленный на рис. 4.2.
192 7 Зак. 434
Зависимость предельных токов и потенциала полуволны от коэф-
фициента диффузии 1), и эффективной толщины диффузионного слоя
О/ может быть выражена уравнениями:
, *<°
х>
4х/«Ох{ (4Л0)
ЯТ / А?ес1
б
Ох \
Физический смысл эффективной толщины диффузионного слоя ясен
из рис. 4.2. В условиях стационарной диффузии 6; определяется гео-
метрией электролизера и гидродинамическим режимом размешивания
раствора, в нестационарных условиях зависят от времени с момен-
та наложения импульсов потенциала или тока и формы этих импуль-
сов. . ,
Итак, в условиях лимитирующей стадии массопереноса нарушение
электрохимического равновесия локализовано в прилегающем к
электроду диффузионном слое и характеризуется разностью концент-
раций электроактивных веществ:
со**—
с
0к
(х = 0) и с$
е
а —
—
спей
(х = 0); при этом равновесие, связанное с переходом заряжен-
ных частиц через границу электрод/раствор, практически не наруша-
ется. В условиях замедленной стадии разряда—ионизации, наоборот,
нарушается равновесие перехода заряженных частиц через фазовук>
границу, а градиентом концентрации в диффузионном слое можна
пренебречь.
Причины медленного протекания стадии разряда — ионизации
связаны с квантово-механической природой перехода заряженных
частиц через границу раздела электрод/раствор. В самом деле, со-
гласно принципу Франка — Кондона, безызлучательный процесс
перехода электрона с металла на частицу Ох в реакции (А) или обрат-
но с частицы Кес! на металл возможен лишь при условии, если пол-
ные энергии электрона в начальном и конечном состояниях прибли-
зительно одинаковы. Для реализации этого условия необходимо из-
менить ориентацию диполей растворителя вблизи реагирующей час-
тицы, что требует затраты определенной энергии активации. .Кроме то-
го, вероятность элементарного акта разряда—ионизации при выпол-
нении принципа Франка—Кондона в общем случае не равна единице;
она зависит от перекрывания волновых функций начального и ^конеч-
ного состояний, а потому резко убывает с удалением реагирующей
частицы от поверхности электрода. В результате принимают (или от-
дают) электроны только адсорбированные на электроде частицы Ох
(или Ней).
Первый вариант теории замедленного разряда был предложен
М. Фольмером и Т. Эрдей-Грузом (1930). Существенное уточнение
в эту теорию внес А. Н. Фрумкин (1933), который учел зависимость
скорости стадии разряда — ионизации от строения двойного элект-
рического слоя. Современные представления о механизме элементар-
193

ного акта перехода заряженных частиц через границу раздела элект-
род/раствор, дающие физическое обоснование теории замедленного
разряда, были сформулированы в 60-х годах XX в. в работах советс-
ких и зарубежных ученых.
Количественное рассмотрение процесса перехода заряженных час-
тиц через границу металл/раствор приводит к следующим основным
уравнениям теории замедленного разряда: '
__
п
)р
к
{ изм).
а
Ох
Уф
ехр
а пР (Е—Е°)
•
ехр
(1-
ЯТ
-а) пР (Е~Е
к
{
"
ш)
=к°
8
ех р
О-
ЯТ
ЯТ
ехр
Г(« п—г
0х
)Ру
г
ЯТ
(4.12)
(4.13)
(4.14)
где к1 и &<
изм
> _ абсолютная и измеряемая константы скорости
электрохимической реакции; а — коэффициент переноса, удовлет-
воряющий условию 0 < а < 1; §о
х
и §к
е
<1 — абсолютные значения
стандартной энергии специфической адсорбции веществ Ох и-Кед;
аох
и а
яеа — их активности в объеме раствора; г о
х
— зарядовое чис-
ло вещества Ох с учетом знака; % — потенциал в плоскости локализа-
ции электрических центров адсорбированных реагирующих частиц,
отсчитанный от потенциала в объеме раствора; Е° — стандартный
равновесный потенциал реакции (А)- — коэффициент активности
активированного комплекса.
В условиях малого заполнения поверхности электрода всеми ком-
понентами раствора, за исключением растворителя,
(4.15)
где уо
х
и
Ткед — коэффициенты активности веществ Ох и Кед в объе-
ме раствора. При выполнении соотношения (4.15) из уравнений (4.12)
и (4.13) следует
(4Лег)
( Г апру) ] Г (1—а)пРх\1)
= п |ехр —]-«Р [-.. да. \)'
где ц = Е
р
— Ё — перенапряжение и
-пРк™ (4)'-
а
(4ее)"
(4.17)
Частным случаем величины при равновесном потенциале Е
= Е
р
является ток обмена /
0
:
(4.17а)
109$
где различие между &<
изм)
и , а также между 1
0
и *о обуслов-
лено зависимостью от потенциала электрода величин г^, |Го
х
и
[см. уравнение (4.14)].
В условиях, когда можно пренебречь зависимостью (о от Е, поля-
ризационная кривая, рассчитанная по уравнению (4.16), имеет вид,
изображенный на рис. 4.3. Если учитывать экспоненциальное воз-
растание катодного или анодного фарадеевского тока с увеличением
|т)|, то для графического изображения поляризационной кривой
стадии разряда—ионизации удобно использовать полулогарифмичес-
кие координаты: ц — 1б1*ф|«(рис. 4.4). В соответствии с уравнением
Рис, 4.3. Форма поляризационной Рис. 4.4. Поляризационная кривая,
кривой для стадии разряда — иони- приведенная на рис. 4.3, в полулога-
зации ь рйфмических координатах
(4.16) при 1о — г
0
= сопз! экстраполяция линейных участков зави-
симости т) от 1&|/ф| к т] = 0, как показано на рис. 4.4, отсекает на оси
абсцисс величину 1§г
0
, а тангенсы углов наклона этих участков опре-
0 059
деляют коэффициент переноса а: 1§<р = 2,3 ЯТ/апР &
'-
1
—^
и =
0 059
= 2,3#7У(1 — а)пР «
П
Р
И
известных а, со
х
и ск
е
а по
уравнению (4.17а) можно рассчитать константу скорости электрохими-
ческой реакции /г
(и
|
м
>. .
Линейную зависимость ц от впервые наблюдал И. Тафель
(1905) для реакции разряда ионов Н
3
0
+
на различных электродах:
2Н
3
0+ + 2г- —> Н
2
+2Н
2
0 (Б)
В связи с этим эмпирическое уравнение
х\
= а-{-Ы%1ф (4.18)
называют формулой Тафеля. Формулу (4.18) можно получить из урав-
нения (4.16) в условиях <о —
*о
и ц > Ц'Т/пР; при этом
Ь
= 2,ЗЯТ/апР
и а — — Ы§/
0
. Для выполнения условия /о = *о необходимо, чтобы
зависимость
11?!
-потенциала от потенциала электрода была подавлена
избытком поверхностно-неактивного электролита фона (см. §3.1), а^о
х
и
Йкед либо равнялись нулю, либо были практически постоянны-
ми в исследуемом интервале потенциалов. Если же эти условия не вы-
183

полняются, то форма поляризационной кривой, отвечающей стадии
разряда — ионизации, усложняется.
Наиболее резко влияние двойного электрического слоя на форму
поляризационной кривой сказывается в ржбавленных растворах при:
электровосстановлении анионов, например, для реакции
3
2
0|- + 2<г- ^ 2502- (В)
В реальных условиях электровосстановйение аниона 5
2
08~ происхот-
дит настолько необратимо, что скоростью обратного процесса можна
пренебречь (/ > /) и, следовательно, /ф ^ Кроме того, на многих
металлах реакция (В) протекает при
отрицательных и небольших положи-
тельных зарядах электрода, когда
можно пренебречь специфической
адсорбцией ионов 5
2
01~ и 30|~,
Т. е. ПреДПОЛОЖИТЬ, ЧТО
При этих условиях из уравнений
(4.12) и (4.13) получаем
-^ох)^!
/ф зё пР
Щ
ехр
(а п-
Рис. 4.5. Характерные зависимо-
сти тока электровосстановления
анионов от потенциала электрода
при лимитирующей стадии разря-
да—ионизации. Переход от кри-
вой / к кривой 2 соответствует
увеличению концентрации элект-
ролита фона
X ехр
КТ
апР
{Е—Е<>)
X
ЯТ
(4.19)
Форма поляризационной кривой,
соответствующая уравнению (4.19)
при 2о
х
< 0 и при условии, что
^-потенциал равен падению потен-
циала в диффузном слое и может
быть рассчитан по формуле (3.20)
(см. §3.1), приведена на рис, 4.5. Как видно из рисунка, по-
ляризационная кривая электровосстановления анионов проходит
через максимум в области небольших положительных, зарядов по-
верхности и чёрез минимум при^<0. Повышение концентрации
электролита фона приводит к понижению максимума и к увеличе-
нию фарадеевского тока в минимуме (переход от кривой 1 на рис. 4.5
к кривой 2). При потенциале нулевого заряда Е
ч==0
поляризацион-
ные кривые, отвечающие со
х
= сопз! и различным концентрациям по-
верхностно-неактивного электролита фона, пересекаются. Эти зако-
номерности, вытекающие из теории замедленного разряда, хорошо
согласуются с экспериментальными данными для реакции (В), а также
для реакций электровосстановления других анионов (Н. В/ Федоро-
вич),
С физической точки зрения появление ниспадающей ветви на поля-
ризационной кривой вблизи (рис. 4.5) объясняется резким умень-
шением в этой области поверхностной концентрации восстанавливаю-
щихся анионов, поскольку их притяжение положительными заряда-
192
ми электрода при переходе через потенциал нулевого заряда сменя-
ется электростатическим отталкиванием от отрдцательно заряженной
поверхности. Как следует из теории двойного электрического слоя
(см. § 3.1), этот эффект проявляется тем* сильнее, чем меньше общая
концентрация электролита. При более отрицательных потенциалах,
когда зависимость г|)
а
от ц становится менее резкой, ускорение
электродного процесса за счет снижения энергии активации пре-
валирует над уменьшением его скорости, обусловленным дальней-
шим падением поверхностной концентрации Ох. В результате при
достаточно больших отрицательных значениях Е вновь наблюдается
рост /ф (рис. 4.5).
С помощью уравнений (4.19), (3.21) и (3.22) можно получить сле-
дующее необходимое условие возникновения ниспадающей ветви на
поляризационной кривой стадии разряда—ионизации в растворе,
содержащем поверхностно-неактивный г
у
2-валентный электролит
фона:
У~ <-г
0х
ЯТС§
2
(<7
= 0)/ 1г\РА ап, (4.20)
где с — общая концентрация электролита; С§
2
(д = 0) — емкость
плотного слоя Со2 при = 0; А ='
0
ЯТ — параметр теории диф-
фузного слоя (см. § 3.1). Поскольку все величины, входящие в правую
часть неравенства (4.20), положительны, за исключением гох* то это
условие выполняется лишь при электровосстановлении анионов, ког-
да г
Ох
<0.
Если условие (4.20) выполнено, то экстремумы на Я-кривой от-
вечают следующим значениям заряда электрода:
Формула (4.21), вытекающая из уравнений (4.19), (3.21) и (3.22),
может быть использована для нахождения коэффициента переноса
а на основе опытных значений ^
экс
и С§
2
(<7 = ?
Э
кс)- Однако удобнее
с этой целью использовать угол наклона так называемых исправлен-
ных тафелевских зависимостей (и.т.з.):
^/ф+гох/^/ЯГ от -(Е-Е*—^).
В соответствии с уравнением (4.19) поляризационная характеристика
стадии разряда—ионизации в этих координатах должна представлять
прямую линию с тангенсом угла наклона апР/ЯТ и начальным зна-
чением ординаты, равным \п(пРк1со
х
). Следовательно, для исследуе-
мой электрохимической реакции в данном растворителе при со
К
=
= сопз! и. т. з. не должны зависеть ни от концентрации поверхностно-
неактивного электролита фона, ни от природы металла электрода, ес-
ли, конечно, выполняются условия, положенные в основу вывода урав-
нения (4.19). Эти выводы теории хорошб согласуются с эксперимен-
тальными данными для реакции (В) при использовании электродов из
7 Зак. 434 110
