Журбенко Л.Н., Никонова Г.А., Никонова Н.В., Нуриева С.Н., Дегтярева О.М. Математика в примерах и задачах
Подождите немного. Документ загружается.

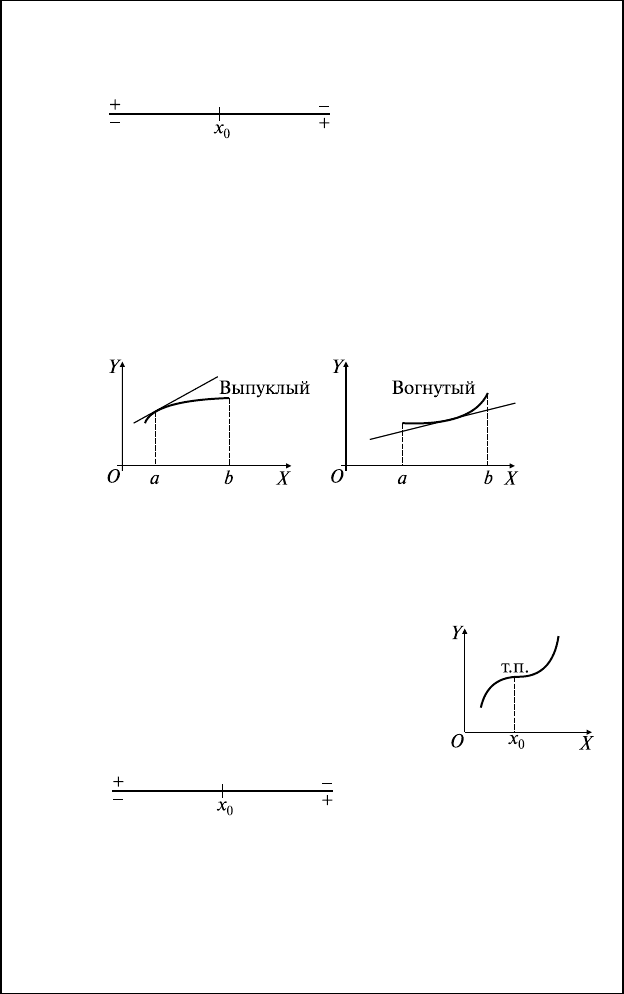
101
x
0
— подозрительная на э. ⇔ f ′(x) = 0∨∃\
Достаточный признак э. I:
f(x) ∈ C
[a,b]
, x
0
∈ (a, b) — подозрительная на э.,
f ′(x):
⇒=
⇒=
fx y
fx y
()
()
max
min
0
0
10.5. Достаточный признак экстремума, использующий вторую
производную
Достаточный признак э. II: f ′(x
0
) = 0,
′′
<⇒
>⇒
fx
x
x
()
.max,
.min
0
0
0
0
0
—
—
т
т
10.6. Выпуклость, вогнутость
Достаточный признак:
′′
<∀∈⇒∩
>∀∈⇒∪
fx
xab
xab
()
(, )
(, )
0
0
10.7. Точки перегиба (т.п.)
т. x
0
— подозрительная на перегиб ⇔
⇔ f ″(x
0
) = 0∨∃\
Достаточный признак: f(x) ∈ C
[a,b]
,
x
0
∈ (a, b) — подозрительная на перегиб
f ″(x):
⇒ (x
0
, f(x
0
)) — т.п.
10.8. Асимптоты
Асимптота ⇔ прямая L: d(M, L) → 0 при М → ∞ по графику.
Вертикальная асимптота: x = a. Необходимое и достаточное
условие:
lim()
xa
fx
→±
=∞
0

102
Наклонная асимптота:
y = kx + b,
k
fx
x
bfxkx
xx
==-
→±∞→±∞
lim
()
,lim [()]
Задачи к разд. 10.1, 10.2
Задача 1. Вычислить пределы:
а)
lim
ln
;
x
x
x
→
-
1
3
1
б)
lim
arctg
ln
;
x
x
x
→∞
-
+
π 2
1
1
в)
lim
ln
.
x
x
x
→+∞
2
3
Решение: Пределы а), б) дают неопределенность
0
0
,
в) —
∞
∞
,
поэтому воспользуемся правилом Лопиталя:
а)
lim
ln
lim
()
(ln)
limlim
xxx
x
x
x
x
x
x
→→→
-
=
=
-
′
′
==
1
3
1
3
1
2
10
0
13
1
xx
x
→
=
1
3
33;
б)
lim
arctg
ln
lim
xx
x
x
x
x
x
→∞ →∞
-
+
=
=
-
+
+
-
π 2
1
1
0
0
2
1
1
1
11
1
2
22
2
2
2
1
2
21
2
=
+
+
=
=
∞
∞
=
+
=
∞
∞
→∞
→∞
lim
()
()
lim
(*)
x
x
xx
x
x
x
==
→∞
2
2
2
2lim;
x
(Начиная с места (*) можно найти решение, поделив числитель и
знаменатель дроби на х
2
.)
в)
lim
ln
lim
ln
lim
xx x
x
x
x
x
x
→+∞→+∞ →+∞
=
∞
∞
=
⋅
=
∞
∞
=
2
32
2
1
3
2 ⋅⋅
=
==
→+∞
1
9
2
9
1
0
3
x
x
x
x
lim.
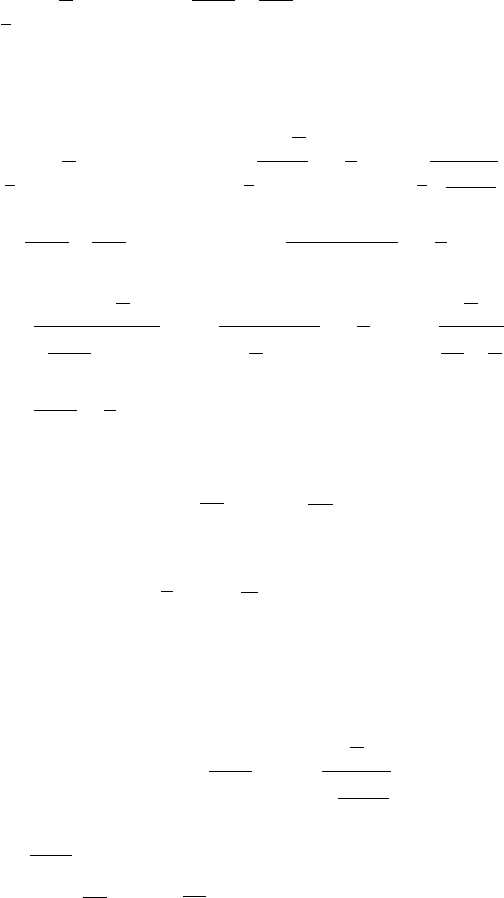
103
Задача 2. Вычислить пределы:
а)
limtg;
x
xx
→
-
π
π
2
2
б)
lim
ln
.
x
x
xx
→
-
-
1
1
1
Решение: От неопределенностей {0 ⋅ ∞}, {∞ - ∞} необходимо
перейти к неопределенности {0/0}, чтобы применить правило Ло-
питаля:
а)
limtg{}lim
ctg
lim
xxx
xx
x
x
→→→
-
=⋅∞=
-
=
=
πππ
π
π
22
2
0
2
0
0
22
2
1
1
1
-
=-
sin
;
x
б)
lim
ln
{}lim
ln
ln ()
xx
x
xx
xxx
xx
→→
-
-
=∞-∞ =
-+
-
=
11
1
11
1
0
0
=
=
+⋅-
-
+
=
-+
=
=
→→
lim
ln
ln
lim
ln
ln
li
xx
xx
x
x
x
x
x
x
x
11
1
1
1
1
1
0
0
mm
lim.
x
x
x
x
x
x
x
→
→
+
=
=
+
=
1
2
1
1
11
1
1
2
Задача 3. Вычислить пределы:
а)
lim;
tg
x
x
x
→+0
б)
lim(ln );
ln
x
x
x
→+∞
2
1
в)
lim.
x
x
x
→
-
1
1
1
Решение: Неопределенности а) {0
0
}, б) {∞
0
}, в) {1
∞
} преобразу-
ем в неопределенности
0
0
или
∞
∞
,
используя формулу
lim()
()
lim()ln()
xa
x
xx
x
xa
→
=
→
ϕ
ψ
ψϕ
e:
а)
lim;
tg
limtgln
x
x
xx
xe
x
→+
===
→+
0
0
0
1e
limtgln{}lim
ln
ctg
lim
sin
lim
xxx
x
xx
x
x
x
x
→+ →+ →+
=⋅∞= =
-
=
=-
000
2
0
1
1
→→+
⋅=
0
0
sin
sin;
x
x
x
б)
lim(ln );
ln
lim
ln
ln(ln)
x
x
x
x
xe
x
→+∞
===
→+∞
21
1
1
2
0
e
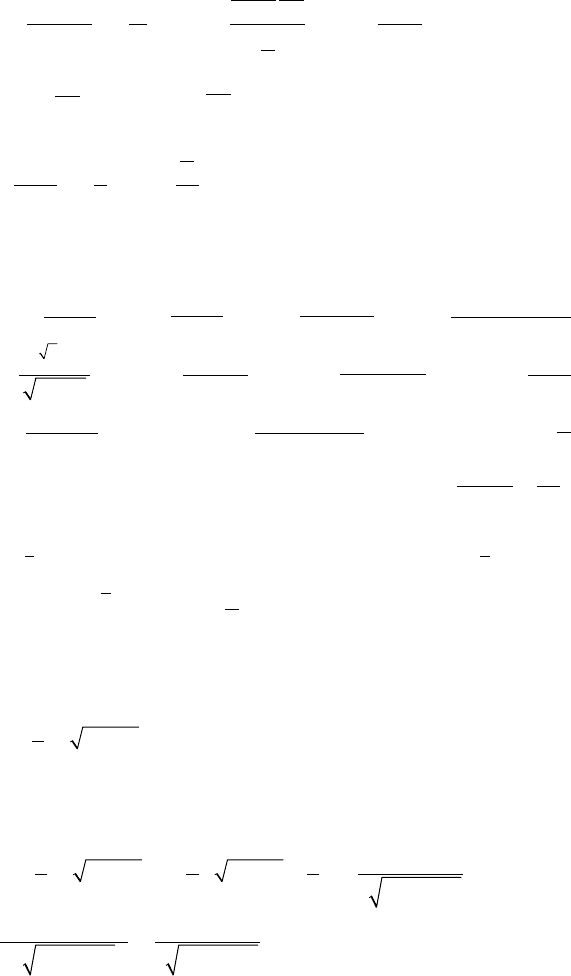
104
lim
ln ln
ln
lim
ln
lim
ln
xxx
x
x
xx
x
x
→+∞→+∞ →+∞
=
∞
∞
===
2
1
2
2
2
1
1
2
0;;
в)
lim;
limln
x
x
x
x
x
x
→
-
∞
-
-
=
{}
==
→
1
1
1
1
1
1
1
1
ee
lim
ln
lim.
xx
x
x
x
→→
-
=
=
-
=-
11
1
0
0
1
1
1
Задачи для самостоятельного решения
Вычислить пределы:
1)
lim
sin
;
x
x
x
→
-
0
1e
2)
lim
sin
ln
;
x
x
x
→1
π
3)
lim;
xa
mm
nn
xa
xa
→
-
-
4)
lim
sin
;
x
xx
x
xx
→
-
--
-
0
2ee
5)
lim
sin
;
x
ax
bx
→
-
0
1e
6)
lim
lncos
;
x
x
x
→0
7)
lim
tg
sin
;
x
xx
xx
→
-
-
0
2
8)
lim
ln
ctg
;
x
x
x
→+0
9)
lim
lnsin
lnsin
;
x
x
x
→0
2
10)
lim;
x
x
xx
→+∞
+-
e
3
32
23
11)
limsin ;
x
x
a
x
→∞
12)
limsin ln ;
x
xx
→+
⋅
0
13)
lim( )ctg ;
x
x
x
→
-
0
2
1e
14)
lim
sin
;
x
xx
x
→
-
0
2
11
15)
lim(sectg);
x
xx
→
-
π
2
16)
limsin ;
tg
x
x
x
→0
17)
lim(tg );
x
x
x
→
-
π
π
2
2
18)
lim( );
x
x
x
x
→
+
0
2
1
e
19)
limln;
x
x
x
→
0
1
20)
lim(cos) .
ctg
x
x
x
→0
2
Задачи к разд. 10.3–10.8
Задача 1. Найти интервалы монотонности и экстремумы функ-
ции
yxx=-
2
3
67
2
3
.
Решение: Проводим решение по следующей схеме:
1) находим D( f ): x ∈ (-∞, +∞);
2) находим точки, подозрительные на экстремум:
′
=-
′
=-+⋅
-
=
=
-+
yxxxxx
x
xx x
2
3
67
4
3
67
2
3
6
36 7
46 7
3
2
33
2
2
3
()
()
(
667
28 1
36 7
2
3
2
3
x
xx
x-
=
-
-)
()
()
;
105
y′ = 0 ⇒ x(x - 1) = 0 ⇒ x
1
= 0, x
2
= 1 — подозрительные на
экстремум точки;
y′ ∃/ ⇒ 6x - 7 = 0 ⇒ x
3
= 7/6 — подозрительная на экстре-
мум точка;
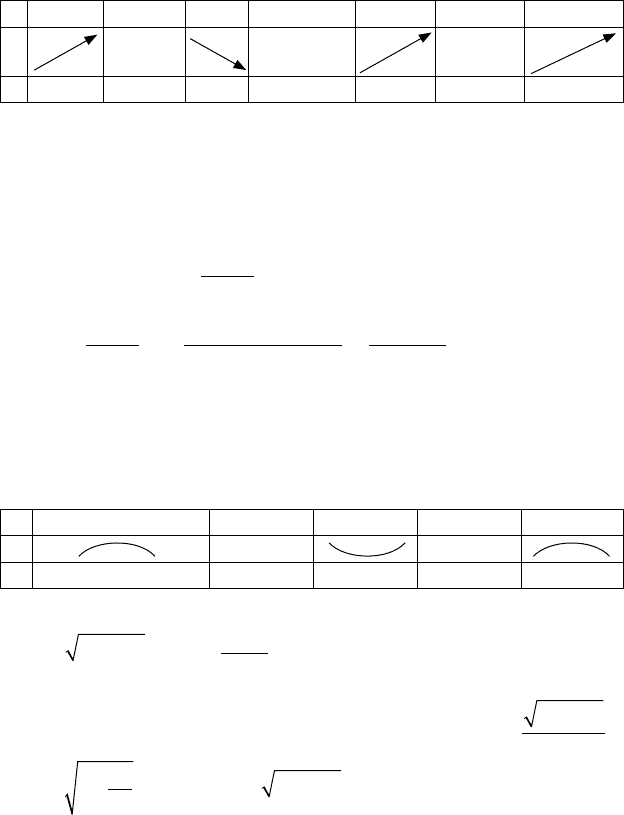
3) разбиваем D( f ) на интервалы монотонности, составляем
таблицу интервалов монотонности, экстремумов:
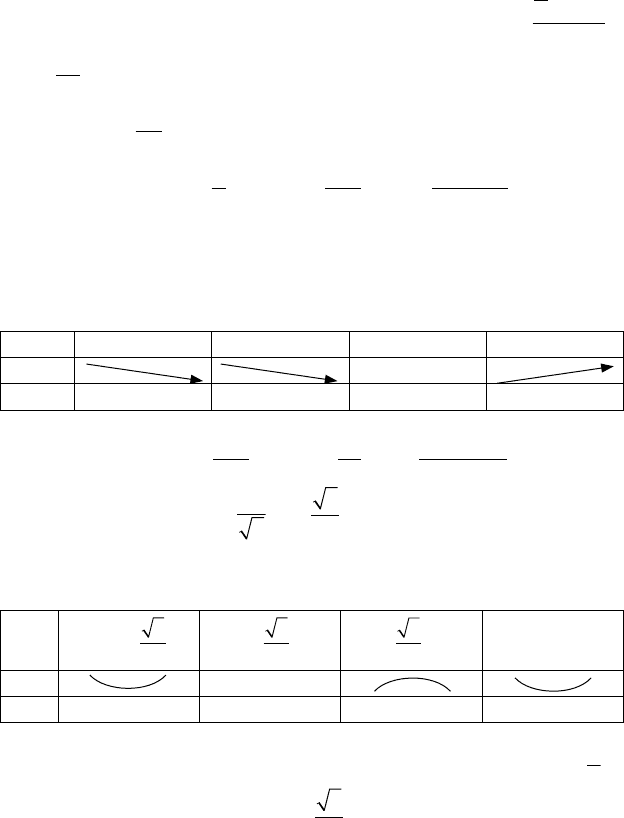
x (-∞, 0) 0 (0, 1) 1 (1, 1
1
/
6
) 1
1
/
6
(1
1
/
6
, +∞)
y y
max
= 0 y
min
= -2/3
Экстре-
мума нет
y′
+
0
-
0
+
∃/ +
Задача 2. Найти интервалы выпуклости, вогнутости, точки пе-
региба функции y = ln(1 + x
2
).
Решение: Проводим решение по следующей схеме:
1) находим D( f ): x ∈ (-∞, +∞);
2) находим точки, подозреваемые на перегиб:
′
=+
′
=
+
⋅
′′
=
+
′
=
+-⋅
+
yx
x
x
y
x
x
xxx
(ln( )) ,
()
(
1
1
1
2
2
1
21 22
1
2
2
2
2
xx
x
x
22
2
22
21
1)
()
()
,=
-
+
y′′ = 0 ⇒ 1 - x
2
= 0 ⇒ x = ±1 — точки, подозрительные на
перегиб, y′′ ∃ при х ∈ (-∞, +∞).
Разбиваем D( f ) на интервалы выпуклости, вогнутости, состав-
ляем таблицу интервалов выпуклости, вогнутости, точек переги-
ба:
x (-∞, -1) -1 (-1, 1) 1 (1, +∞)
y y
т.п.
= ln2 y
т.п.
= ln2
y′′ – 0
+
0 –
Задача 3. Найти асимптоты графиков следующих функций:
а)
yxx=-
3
3
3 ;
б)
y
x
x
=
+
e
2
.
Решение: а) вертикальных асимптот нет, так как нет точек раз-
рыва. Наклонные асимптоты: y = kx + b,
k
xx
x
x
=
-
=
→±∞
lim
3
3
3
=-== --=∞-∞ =
→±∞→±∞
lim,lim( ){ }
xx
x
bxxx1
3
13
2
3
3
3
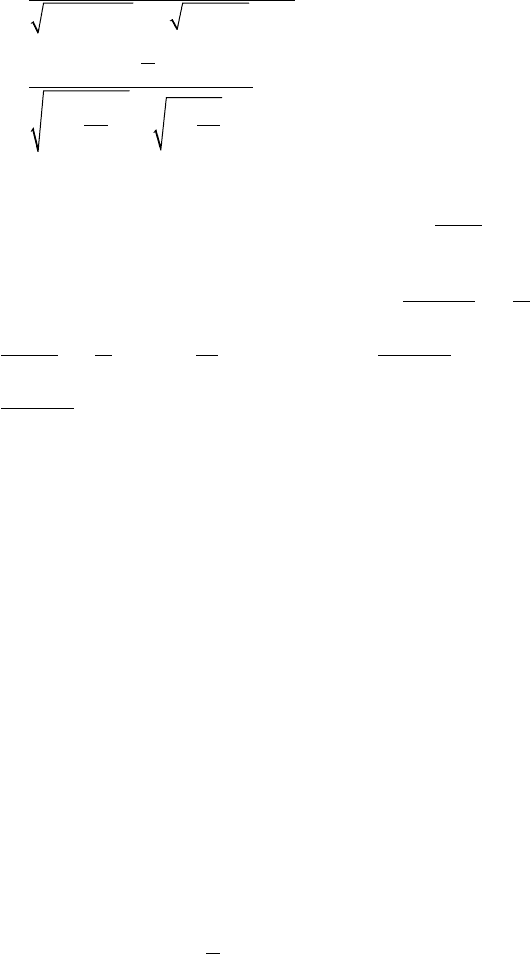
106
=
--
-+ -+
=
→±∞
lim
()
x
xxx
xxxxxx
33
32
3
3
3
2
3
33
=
-
-
+- +
=
→±∞
lim.
x
x
xx
3
1
3
1
3
1
0
2
2
3
2
3
y = x — наклонная асимптота;
б) точка разрыва х = -2, поэтому нужно проверить необходи-
мое и достаточное условие
lim()
xa
fx
→±
=∞
0
:
lim
x
x
x
→- ±
+
=
20
2
e
∞ ⇒
⇒ x = -2 — вертикальная асимптота.
Наклонные асимптоты: y = kx + b,
k
xx
x
x
=
+
=
∞
∞
=
→+∞
lim
()
e
2
=
+
=
∞
∞
==∞
→+∞→+∞
limlim ;
x
x
x
x
x
ee
22 2
k
xx
x
x
=
+
=
→-∞
lim
()
;
e
2
0
b =
=
+
=⇒
→-∞
lim
()
x
x
xx
e
2
0
горизонтальная асимптота у = 0 при
х → -∞.
Задача 4. Исследовать функцию и построить график: у =
= 1/x + 4x
2
.
Решение: Исследование функции производится по следующей
схеме:
1) находим D( f ), точки разрыва;
2) находим асимптоты графика функции;
3) проверяем симметрию графика, периодичность;
4) находим интервалы монотонности, экстремумы;
5) находим интервалы выпуклости, вогнутости, точки переги-
ба;
6) находим точки пересечения с осями координат;
7) проводим, в случае необходимости, исследование графика
на концах D( f );
8) строим график функции.
Итак, данную функцию исследуем по предложенной выше схе-
ме:
1) D( f ): x ∈ (-∞, 0) ∪ (0, +∞); x = 0 — точка разрыва;
2) вертикальная асимптота: проверяем для х = 0 необходимое
и достаточное условие:
lim
x
x
xx
→±
+
=∞⇒=
0
2
1
40
— вертикальная
107
асимптота. Наклонная асимптота: y = kx + b,
lim
x
x
x
x
→±∞
+
=
1
4
2
lim
x
x
x
→±∞
+
=∞⇒
1
4
2
наклонной асимптоты нет;
3)
fx
x
xfxfx() () ()-=
-
+≠ ≠- ⇒
1
4
2
функция общего вида;
4) находим
′
=+
′
=
-
+=
-+
y
x
x
x
x
x
x
1
4
1
8
18
2
2
3
2
;
y ′ = 0 ⇒
⇒ 8х
3
- 1 = 0 ⇒ х = 1/2 — подозрительная на экстремум, у′ ∃
всюду в D( f ). Точка x = 0 — точка разрыва, она не может быть
точкой экстремума. Составляем таблицу интервалов монотонности
и экстремумов:
x (-∞, 0) (0, 1/2) 1/2 (1/2, +∞)
y y
min
= 3
y′ – – 0
+
5) находим
′′
=
-
+
′
=+=
+
y
x
x
x
x
x
1
8
2
8
24 1
23
3
3
()
;
y ″ = 0 ⇒
⇒ 4x
3
+ 1 = 0 ⇒ x =
-
1
4
3
=
-
2
2
3
— подозрительная на перегиб,
у′′ ∃ всюду в D( f ). Составляем таблицу интервалов выпуклости,
вогнутости, точек перегиба:
х
-∞ -
,
2
2
3
-
2
2
3
-
2
2
0
3
,
(0, +∞)
у у
т.п.
= 0
у′′
+
0 –
+
6) находим точки пересечения с осью ОХ: у = 0 ⇒
1
x
+
+ 4x
2
= 0 ⇒ 4x
3
= -1 ⇒ x =
-
2
2
3
— точка перегиба. Точек пе-
ресечения с ОY нет: х ≠ 0;
7) строим график функции (рис. 10.1).
Задача 5. Газовая смесь состоит из окиси азота и кислорода.
Требуется найти концентрацию кислорода, при которой содержа-
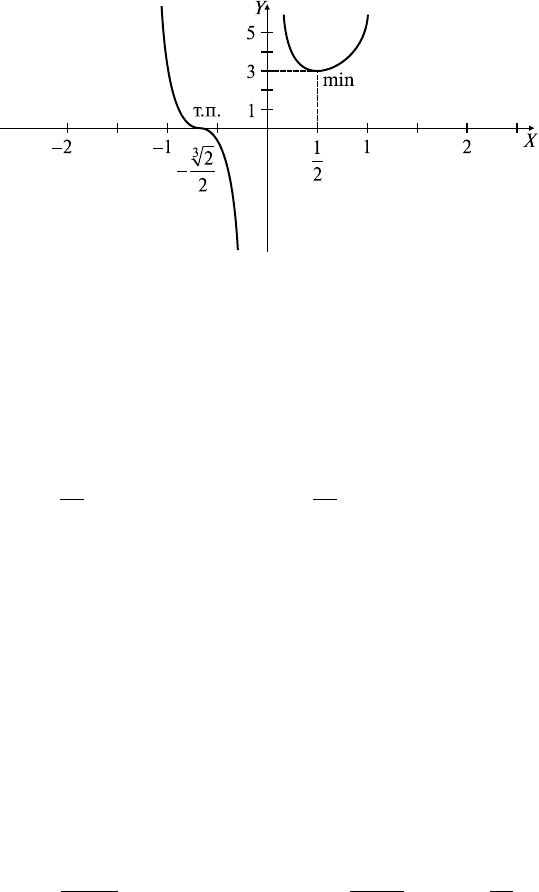
108
щийся в смеси оксид азота (II) окисляется с максимальной скоро-
стью.
Решение: В условиях практической необратимости скорость ре-
акции 2NO + O
2
= 2NO
2
выражается формулой v = kx
2
y, где х —
концентрация NO в любой момент времени; у — концентрация O
2
;
k — константа скорости реакции, зависящая только от температу-
ры. Тогда у = 100 - х, v = kx
2
(100 - x) = k(100x
2
- x
3
).
Найдем
d
d
d
d
v
x
vk xx
v
x
x
=
′
=-⇒=()2003 0
2
при х
1
= 0, х
2
= 66,7%
(k ≠ 0). Для того чтобы установить, какое из полученных значений
х соответствует максимальной скорости окисления, вычислим вто-
рую производную v″
xx
= k(200 - 6x); находим v′′(x
1
) = v′′(0) > 0,
т.е. при х
1
= 0 — min; v′′(x
2
) = k(200 - 6 ⋅ 66,7) < 0, откуда сле-
дует, что функция v, т.е. скорость окисления, при х
2
= 66,7% име-
ет максимальное значение.
Когда х = 66,7%, у = 100% - 66,7% = 33,3%, т.е. скорость
окисления оксида азота будет максимальной в том случае, если в
газовой смеси содержится 33,3% кислорода, т.е. при стехиометри-
ческом соотношении х = 0,5.
Задачи для самостоятельного решения
Найти интервалы монотонности и экстремумы функций:
21)
y
x
x
=
-
2
2
4
;
22) y = lncosx; 23)
y
x
x
=
+
2
1
;
24)
y
x
x
=
e
.
Найти интервалы выпуклости, вогнутости, точки перегиба
функций:
Рис. 10.1
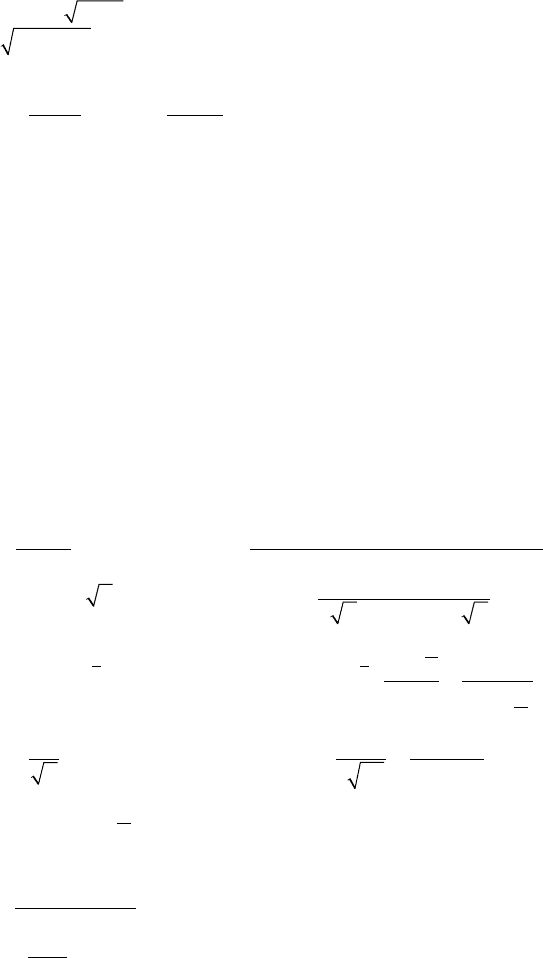
109
25)
ya xb=- -
3
;
26) y = x - ln(x + 1); 27) y = x
3
- 3/x;
28)
yx x=-
32
3
2 .
Найти асимптоты функций:
29)
y
x
=
-
1
1e
;
30)
y
x
x
=
-
3
2
3
.
31) Исследовать полностью функции задач 2, 3, 21–30 и по-
строить их графики.
32) Материальная точка движется по прямой по закону s =
= 6t
2
- t
3
. Какова ее наибольшая скорость?
33) Кривая полных издержек имеет вид k = x
3
- 6x
2
+ 15x
(x — объем производства). Рассчитать, при каком объеме произ-
водства средние издержки минимальны.
34) Реакционный аппарат имеет форму открытого сверху ци-
линдрического бака. Каковы должны быть радиус основания R и
высота Н, если на его изготовление отпущено заданное количество
материала, чтобы его объем был наибольшим?
варианты контрольной работы
Вариант № 1
1.
y
x
x
=
+
3
2
5
sin
;
y′ = ? Ответ:
′
=
--
y
xx xxxx
x
(sin coscos )
sin
.
32 10
2322
22
2. y = lnarctg
x
; dy = ? Ответ:
d
d
y
x
xx x
=
+21()arctg
.
3.
yx
x
= (tg) ;
ctg
2
2
y′ = ? Ответ:
′
=-
yx
x
x
x
x
x
(tg)
ctg
sin
ln(tg)
sin
.
ctg
2
4
2
4
2
2
2
2
2
4.
y
x
x
x=+34
3
tg ;
y″ = ? Ответ:
′′
=- +y
x
x
x
2
3
32 4
4
4
3
3
sin
cos
.
5.
xt
yt
=+
=
sincos ,
sin;
π
5
2
y″
xx
= ? Ответ: y″
xx
= 2.
6.
lim
cossin
?
x
xx x
x
→
-
=
0
3
Ответ: -1/3.
7.
lim?
ln
x
x
x
→
+
=
0
3
1
Ответ: e
3
.

110
8. Найти интервалы монотонности, экстремумы y = xln
2
x. От-
вет: у
max
= y(1/e
2
) = 4/e
2
, y
min
= y(1) = 0.
Вариант № 2
1.
yx
x
=
2
3
e
sin
;
y′ = ? Ответ:
′
=+y
x
xx
x
e
sin
(cos ).
3
23
3
2. y = arcsinln
2
x; dy = ? Ответ:
ddy
x
xx
x=
-
2
1
4
ln
ln
.
3.
yx
x
=
tg
;
1
y′ = ? Ответ:
′
=-
yx
x
x
x
x
x
x
tg
tg
ln
cos
.
1
22
1
1
4. y = arctgx
5
; y″ = ? Ответ:
′′
=
-
+
y
xx
x
10 23
1
310
10 2
()
()
.
5.
xt
yt
=
=+
arctg,
ln();1
2
y″
xx
= ? Ответ: y″
xx
= 2(1 + t
2
).
6.
lim
ctg
sin
?
x
x
x
→
-
=
π
4
1
4
Ответ:
-
1
2
.
7.
lim
arctg
?
x
xx
→
-
=
0
11
Ответ: 0.
8. Найти интервалы выпуклости, вогнутости, точки перегиба
функции y = arctgx - x. Ответ: у
т.п.
= y(0) = 0.
расчетное задание
Пусть α β γ δ — цифры номера группы, n — номер студента по
списку.
Задание 1. Исходя из определения производной вычислить зна-
чение у ′(х), если
yx
fxxx xk
xx
j
k
()
()()()
()
,=
++ -
-+
+
0
0
1
1
1
σ
σ
где k =
k =
+++
+
αβγδ
2
1;
σ=
+
n
2
3;
j
n
=
+
+
γ
4
1;
a
n
=
+
+
α
5
2;
b
n
=
+
+
β
3
1;
f
j
(x), x
0
находятся из таблицы:
j 1 2 3 4
f
j
(x) sin(ax + b) ln(x + a) tg(ax + b)
xa+-1
x
0
-b/a 1 - a -b/a 1 - a
