Волейник В.В. Высокотемпературная электрохимия и физическая химия ванадия
Подождите немного. Документ загружается.

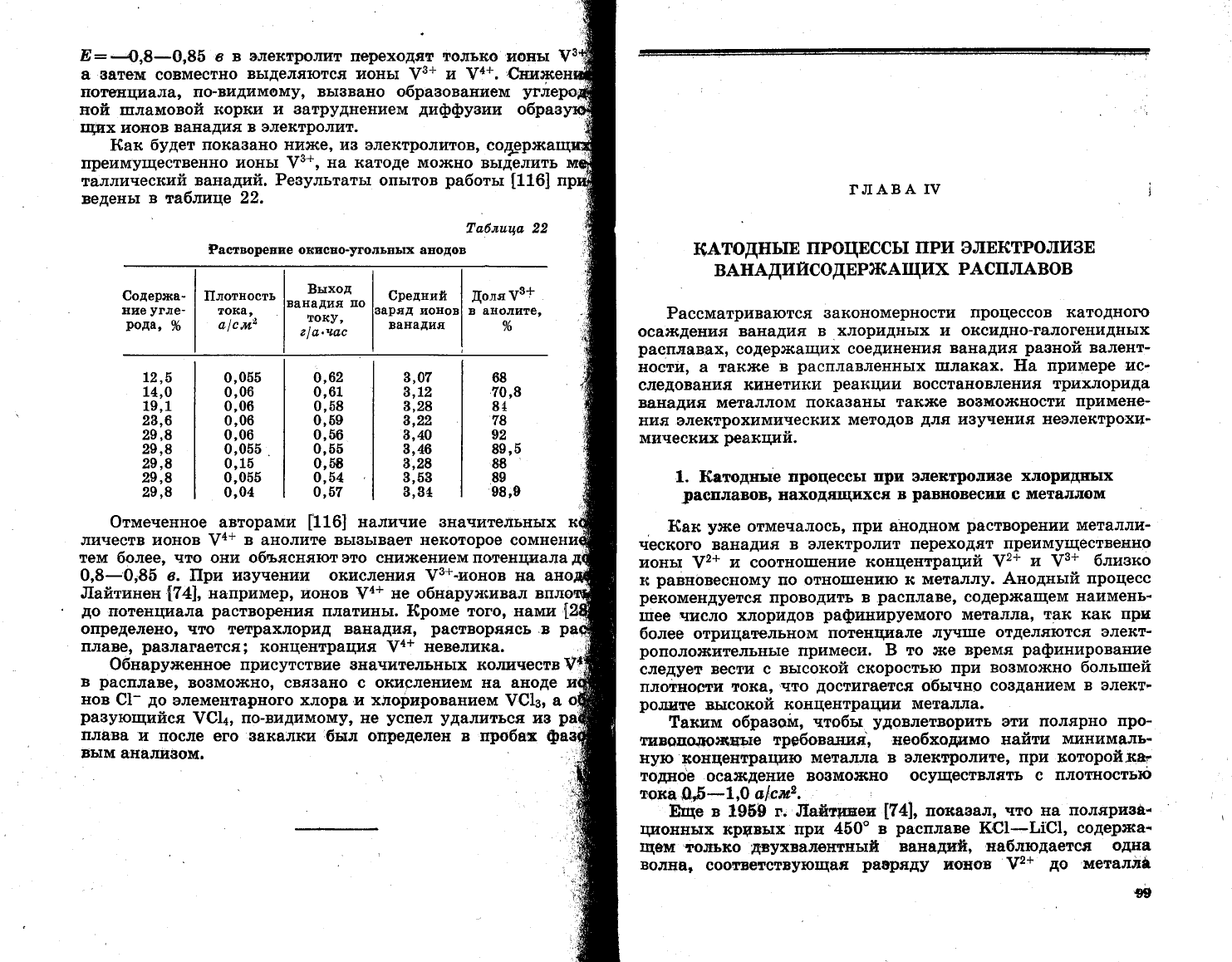
8:_018_0,85
в
в элект|х)лит переходят только
ио'ть1
а ватем
совместно
вь1деля1отся
ионь1
уз+
и
у4+.
пот0}тциала' т7о-в|1дтамому'
вь1звано обрааованием
пой
тпламовой
корки
и 3атрудне1{ием
диффуаии
о6раз
щ![х
иопов
ва1тадия
в электролит.
$ак
будет
пока8ат1о }{и'*се' и3 электролит0в'
преимущественно
ионь1
!3+,
на катоде мо}|сно
вьтделить
таллическттй
занадттй. Результать1 опь|тов
работьт [116}
ведень1
э та6лпце 22.
€одеряса-
|||{е
угле-
рода'
уо
|1лотность
!''*;;:^".
;]:2'
|
,7:::;
$р9дний
заряд
ва'тадия
3,07
3,12
3,28
3,22
3,40
3,46
3,28
3,58
8,94
6тмеченное авторами
[116]
наличие з}|ачительнь1х
личеств ионов
!{+
в
анолите
вь1зь1вает
некоторое
тем
более,
что
они
объяснятотато сни}кениемпотенциала
0,8_0'85 с.
[1ри
и3учении
о1сисления
93+-ионов на
]1айтинон
[74],
например' ионов
[{+
не
обнаруясивал
до
потенциала
растворения
платинь1.
$роме
того' нами
определено' что тетрахлорид
ва}тадия'
растворяяеь
в
плаве'
р83лагается;
ко}{центрация
\/{+
невелика.
Фбнаруэгсенное присутствие 8начитель}тьтх ко]1ичеств
в
расплаве'
возмо'{сно' свя8ано с окислением на ат{оде
нов
€1-
до
элеме1ттар1[ого хлорв,и хлорированием
!€1з, а
раву:ощийся
!€1+,
по-видимому' не
успел удалиться
и3
12,5
|4,о
19,1
23,6
29,8
29,9
29,8
29,9
29,8
0,055
0,06
0,06
0,06
0,06
0,055
0,15
0,055
0,04
0,62
0,61
0,58
0'б9
0,56
0'б5
0,58
о'64
0,57
Растворевпе окпсво-угольпь'х аподов
|о6лшцо 22
{оля
13+
в анолите'
%
г']АвА
1у
!сАтоднь1п
пРоцвссь1
пРи алвктРоли3в
вАнАдиисодвРэ|сАщих
РАсплАвов
Рассматрива}отся
закономерности
процессов
катодного
оса'|сд9ния
ванадия
в хлориднь1х и
о1ссид|{о-галоге1{иднь]х
расплавах'
содер'1сащих
соедине1тия
ванадия
разной
валент-
ностй, а так'*ее
в
расплавле1{нь1х
|шлаках. Ёа примере
|4с'
следования
ки1{етики
реакции
восстановления
трихлорида
ванадия металлом
показ&нь1 так3*се
воамоа16}{ости
примене_
ния алектрохимических
методов
для
и3уче}1ия неэлектрохц'
мическ1{х
реакций.
!!.
Ёатодньте
процессъ1
шри
эдетстрол|пае
хлориднь[х
эа€плавов'
паходящпхея
в
равповесии
с м€т&ллом
1{ак
уэ.се
отмечалось'
при анодном
растворении
металл1{_
ческого ва!{адия
в электролит
переходят
преимуществеЁно
ионь1
\2+
тт соот1то]цение
концентращ!й у2+
и
у3+
6лизко
к
равновесному
по отно11]ен!по
к
металлу.
Анодттьтй
процесс
рекоме}{дуется
проводить в
.расплаве'
содерэ{сащем
}!аимень'
1пее число
хлоридов
рафинируемого
металла'
так как пр|д
более отрицательном
поте]{циале
луч1ше
отделя1отся
элект'
рополо'|сительнь1е
примеси.
3 то этсе
вре1шя
рафинирование
следует
вести с
вь:сокой
скоростьто при
вовмо,ткно боль:пей
плотнооти
тока''что
достигается
обьтчно
соад&нием
в 9л9$Р'
род|дте
вьтсокой
концентрации
металла.
1аким образой, чтобь1
удовлетворить
эти
полярно
про-
тивопоАпо|{лтъте
тр96оваттия,
шеобходамо
найти
миним&,!ь'
т{у|о
концентраци1о
мета]т]!а
в элекц)олите'
при
лсоторойка'
тодное
оса'|{де1{ие
во3мо$с}1о
осуществлять
с
плот!{остБю
тока$Ё-1-,9
о|см2.
[ще в 1950 г. ]1айттдшвп
[?4],
повавал'
что на
поляриз*'
1{ио]{нь1х
крцэых
при
4б0" в
расплаве
кс1_[!с1'
со.{е!}1{а'
щ6м'толь'со двухвало:*тньт*
ванадзтй, набл:одается
од1та
вол11а'
соответствук)щ&я
ра8р'1ду
!!онов
у2+
до
металй|
68
70,8
81
78
92
39,5
88
89
0в,0
90

'(рис.
48). 3
дальнейцтем
бьтдо
проведено
детальное
вание
катод}{ого
оса}*сде}{ия
ванадия
из
электролитов'
ких
по
составу
к
равновесньтм
с
металлическим вана-
дием
[117].
Руте. 48, 8ависимости сила то1са
-
потенциал в
расплаве
[|с1
-
кс1
-
_
!€1э при 45о".
9€12,
моль|
лз ]
_
0'00793;
2
0'0199;
3_0'0630; 4
-о,094в,
11лощадь
микроэлектродь !,\3 л.м2,
.
//о
/п
е
н
ц
ца,7
о/,
н
о сц п
ел
6
н о
электтро?а
ср
аЁненоп
Р!
/
Р[
/|;
)
о,о33 ['
3анадийсодер'*сащие
электролитьт готовили'
хлором
расплав'
помещеннь1й в графитовьтй
тигель'
на
хоторого
,тась1пали
карботермический
ванадий.
по
1{ии продувки
расплав
в течение часа вь]дер'*сивали в
такте с металлическим
ванадием
для
восстат{овления
'6олее
вь1сокой валент1{ости' которь1е
могли
образоваться
глубине эле1{тролита
при о1сислении хлором
го
ванадия.
1ипичнь:е
поляризационньте
кривь]е в
кс1_шс1*\/61э и
1(€}_$а€1_ус12 приведеньт 1{а
рисун
ках 49_51.
|!ри
кот{центрацион1той
поляривации
мость
потенциала катода от
плотности тока вьтра
уравнением
3:0\,уя1
+2$т9
&'{Ф.м"о:
2Роу2+
а+
9#($е€1_121,8)
'
2?9уа+'
€'уау_ объемная
концентрация
ваттадия
расплаве'
е
.
шон|с!у!,3.
А''"
алекц)олита 1(€1_1'[ас1_3,1%\ при.
700'
форму
\эимет
вид
Ф
90
20
!0
о
-!0
-
о,1 -0,5
-0,9
-|,3
612
ь'
х:а'
\
'
(1у_1}
Р!
}
!
$а
{
/о
|оттенцаап
з,скттрсФ,'
6
Рпс. 49,
3ависимость
потенциала
катода
от
плотности тока в
расплаве
}сс1
_
$а€1
_
3'1у0
у
при
700".
-1
-
моли6деновьтй катод; 2
_
расчетная
кривая!
Б иштервале
5.10-3-1
о|см2 экспериментальнь1е и
рас-
четнь1е
даннь1е
полность1о
совпада1от за искдк)чением
не-
1соторого
отклоне1{ия
рассчитанной
величинь1 предельного
тока
от экспериментально
найденной' что объясняется
не_
соответствием
истинной
площади катода
геометринеской
поверх}{ости'
особенно
при
длительньтх
экспо3ициях
при
каясдой
плотности
тока. кроме
того' !1ст141111ая'
толщи1{а
диффу3ионного
слоя
1шо}|сет отличаться от
принятой в
рас-
нете 0,01
см.
(ледовательно'
поляризация катода
дейетви-
тель}|о
чисто
ко1{центрационная.
3
о6дасти
низких
(<5':.о-'
о|см2| и
вь|соких
(}1
о|с:ш2)
плотн6стей
тока
уравт{ение
(19-1)
::е
отраа*сает
на6людае-
мьтх }1а опьтт6явлений.
11ри низких
плотностях
тока на
поляризационт{ь1х
кри.
вь:х образуется характерньтй
участок
остаточ1{ого тока'
часть
которого
связана
с перезарядом
катионов
щедочт!ь1х
металлов
до
субионов
(ата
величина
достигает
3'10
-3
о|см2,
101:
(1у-

(рис.
б0), а
часть
_
с
восстановле11ием ионов
\/3*
до
Р+ п
оксикатионов
ванадия.
8
равновес1{ь][х
по отно}цени1о
к
ме-
таллу
расплавах
доля
точного тока'
связанная
с
переварядом \/3+
до
92+ от'
сутствует.
Бстествет*но,
}|ако'
что
дая{'е
тФи
тельной вь1дер,}|ске в
такте с
металлом'
1{е
!€!' образовав:шийся
хлорировании,
успеваег
вос-
ста:{авливаться
до
весной
концентра1щи.
'|!о
достиясении
:той плотности тока
равряда
ионов
\/2+
потенци
ал
катода в
соответствии
вь1раясением
(1у*1)
мится 16
_
ф'однако
достигает
величи}{'
при }со-
Рис.
50. 3ависимость
потенциала
молибденового
катода
от
плот}|ост|{
тока
пт'и 500"
в
эвтектической
сме_
си
|!€1
_
кс1
с
ра3личнь|м
содер_
'ка'{ием
ванадия'
вес.
0/о
: 7
_
3'32;
2-
1,09;
3
-
0,716; 4-0,195;
,
5_о.
торь1х
начи}тается
ние
щелочнь1х
|[роцессьт, проте1са]ощие
вь|1пе предельной,
щ)оанали3ированньте
в
боте
[118]' дол'шны
у1
место
и в
ва:{адийсодера*сащих
расплавах. ]
|[овь:цтение
концентращ(и
ва1тадия в
электролите
увё'
личивает
предельнь]й
диффузио}{нь|й
ток в соответствии ё
/0
-15
-2,5
-15
€,€
-/,5
катоде при плотностях
Рддс.
51.
3авпсишость поте1!цпала
молибдепового
катода
от плотностш
токд
в
р&сплаве
|,|Ф
-
_
кс1
_
1,0906
9 при температуре:
]
_
?([}';
'
2
_
500..
!0
|о2
формулой
(лу-1) и
выэь1ваег
ше}соторь1й
сдвиг
]1суг€1!циала
ватода
в егоро1{у
более
поло'1сительн'ь!х
вначений
(см.
!й".'ооь
3а
сйт
увеликения
тока
перезаряда
ионов
у3+
до
!!/2+
вов1ветает
и
величина
остаточ1{ого
]гока'
.
[1овьп:дтоние
температурь1
оказь1вает
аналогичноо
влия-
}1|де
}та
ъ*1р, оаъу|су1моетей
Б-:.в
й*
(рис.
51)
в ос1товном
за
сч9[
во3р&ста11|1я
величинь1
коэффициента
ди(}фузии
ион0}
у2+.
2. !{атоднь!е
процессь1
при
электрол!!3е
расцлавов'
'
содерпсащих
9€1з
11оляризация
электродов
в
распдавах'
содер:тсащих
!61з,
исследовал
аеъ
11а
примере
расплава
кс1_т,ю1_9€1з'
Ёа
полярограммах
обнаруэкень|
две
волньт
(9цр.
ья1'_!дт{а
и3
й*Ё'"
96ъяснялась
перезарядом
ионов
!3+
АФ
92*,
а
вто_
рая
_
вь1делением
металлического
ванадия.
!
Рътс.
52.
3авис:тмость
сила
тока
_
по'
^]
те||циал
в.
расплавах
1,!с1
-
кс1
_
х
-
ус12
-
$€1з
при
4б0".
}!овцентра-
[
цшя
9(ттт)
и
у
(|!),
моль|л:
,
_
о'0216
;
\г
[11);_
'
2
_
о,о412
у
(]1т)'
0'0474
_\
т
(ш;
3
_
0,00286
у
(|11)'
0'о660
\
-
'\|
(11);
4
_
о'о94в
9
(1!). |!лот!тадь
мик'
роодектрода
Ф,35
мм2.
-0,!
-о'5
-в,9
- /.3 -{,1
'2|
2огпенцсал
ап|осцпе'ь
но
э2ек'
а?оаа
<?овненФ
/]/'/Р|/т)!о31 м
$атодная
поляризация
изучалась
и
в
расплавах
кс1-
\а€1-!€ъ
[119].
Ёа
рисунках
53_56
представлень1
ти]1ич_
1{ые
3ависимости
потенциал
_
плотность
тока
при
700_
850"
в
эдектролит,*
-йё:-ша€1,
содер}тсащих
0,9_10,20/о
]['€1з"
Б
''л".'ие
от
расплавов'
содер'кащих
преимущественпо
двухвадентньтй
ванадий,
выделеник)
мета*"9'Р"дРч:у.*
б''ьц'ие
остаточ}{ь1е
токи'
достига1ощие
|'б
о|см',
прит{ем
подяривационные
кри_вь1е
в о6ласти
катодной
плот1тости
то'
ка 10-{-5
.10-|
о/см2
состоят
из
характер1{ь1х
учасдков'
$сли
бы
весь
остаточный
ток
соответствовал
реакции
у9++
|е:\э*,
то потепциал
катода
менялся
бьт
с
плотностьк)
тока соглас|1о
уравнению
Ё
:8\э+рз+*1,984.
10_4?1в
(-1+
_
ж)
0у_3)
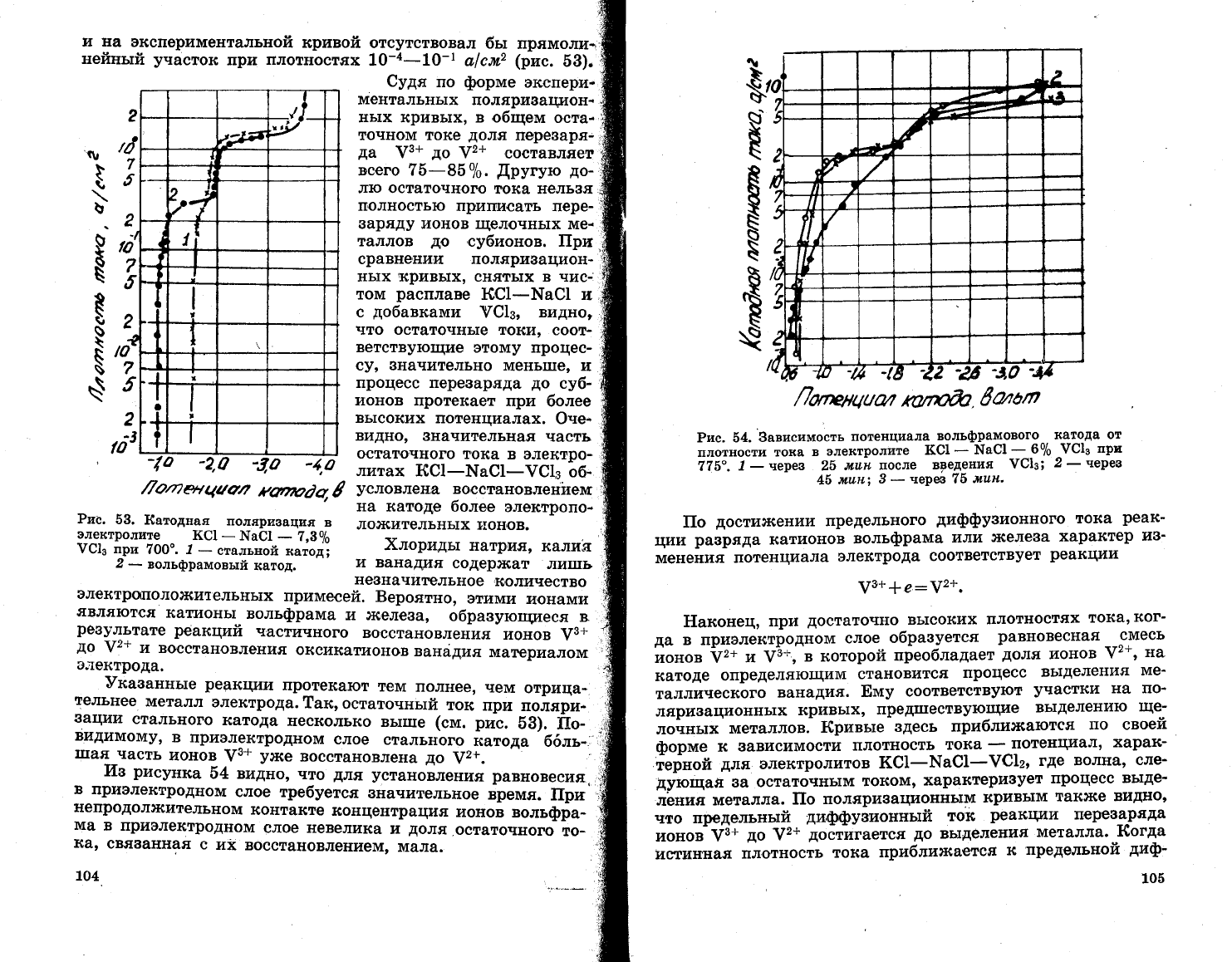
и на
экспоримента]ть1{ой
кривой отсутствовал
6ьт
прямоли-,
нейньтй
участок
при
плотностях
10-4_10-1
о|с;п2
(р*тс.
53).
}
| ьа ! !|;;;;;;'ьк)при1!исатьпере-
\
ч
"!
д] | ! [ [|й;;;'прот1кает'при'более
2ь|!
! ! | !!
вь|сокихпотенциалах.Фче.
)(лоридьт
натрия'
кали1я
у!' ванарр!8.
содер}кат
ли1пь
не3начитель1{ое,количество
ус}3!1!'1
!
!!
::*:*'':::^-::::":т^-".1":"
2огпетчсаа
натттоёч
8
условлена
восстановленйе:ш
'
на катоде
более
эл9кт!ФпФ-
Рис.
53.
1{атодная
поляризация
в
ло'кительнь1х 1!онов.
электрол1тге
кс1
_
шас1
_
7,80/0
?€13 п!и
7оо". 1
_
стальной
к8тод;
2
_
вольфрамовь:й
катод.
электрополо'|сительньтх
примесей.
3ероятно'
этими
ионами
явля}отся
катионь|
вольфрама
и }1селеаа'
образутопцаеся
в
роаультате
реакций
частичного
восстановления
ионов
\/3+
Ао
уэ+
и восстановления
оксикатиот{ов
ван{дия
*,,"р**''*
электрода.
]/казан:*ь:е
реакции
протека1от
тем
полнее'
чем
отрица*
тельнее
металл
электрода.1ак,остаточньтй
ток
при
пойяри-
8ации
стального
катода
несколько
вь|]це (см.
рис.
53).
11о_
видимому'
в
приэлектродном
слое
стального
йатода
66лъ-.,
т]тая
часть
ионов
!3+
уа*се
восстановлена
до
!2+.
[1з
рисунка
54 видно'
что
для
уста1'овле}{ия
рав}{овесия,
в
приэлектродном
слое требуется
а}!ачительное
время.
11ри'
непродол}|сительном
контакте
концёнтрация
ионов
вольфра-
ма
в приэлектродном
слое невелика
и
доля
'остаточного
то_
1са'
свя3а1{ная
с
и*
восстановле1{ием'
мала.
1о4
1атргуцца'т
Аой
6ототп
Рттс. 54.3ависимость
потенциала
вольфрамового
катодв
от
плот1{ости
то1!&
в
электролите
кс1
_
}1а€1
-
60/о $€1з
пРш
775".
1_через 2б
мшн
после
вРеде1|ия
!€1з;
2_через
45
мшн;3
-
терез 7б
мшн.
|[о
достиясении
предельного
диффузионного
тока
реак-
ции разряда
катио1{ов
вольфрама
или
3!селеза
характер
и3_
1шенения
потенциала
электрода
соответствует
реакции
у3+.ь9:!2+.
[аконец,
при
достаточно
вь1соких
плотностях
тока'ког-
да
в приэдектродном
слое
образуется
равновесная
--смесь
ионов \2+
ут !3*,
3 которой
преобладает
доля
ионов
у'-'
на
катодеопределя1ощи1цстановитсяпроцессвь1деления1у!е.
таллического
ват{адия.
[му
соответству1от
участки
на
по'
ляризационнь1х
кривь1х'
пред1пеству1ощие
выделе1{и1о
ще-
лочнь]х
металлов.
1{ривьте_здесь
приблилсатотся
по своей
форме
к
зависимости
плотность
тока
_
потенциал'
харак_
Берной
ддя
электролитов
1{€1-}'[а€1_!€}}э'
где
волна'
сле_
ду1ощая
3а
остаточнь1м
током'
характеризует
процесс
вь1де'
лёния
металла.
|[о
поляризационнь1м
кривь1м
так}!се
видно'
что
предвльнь:й
диффузионньтй
то1с
реакц}1и
переза^ряда
и'шоЁу6*
до
у2+
достигается
до
вь]деления
метадла.
1{огда
исги}гная
плотность
тока
прибли'кается
к
предольной
диф-
105

0"
а/от'
?
!о'
Ф7
{0
*
о2
о'/,
$?
\л
*2
Ё
,;'
\;
.$
./
{?
-1
70!
Рис. 55.
3ависимость
потенциала
вольфрамового
катода
от
плот1{о-
сти
тока
в эдектролите
кс1
_
}.1а€1
_
7,30/9
9@13 при
темпера-
туре:
.1_700';
2_776"3
3_
850'.
фузионной
величине
#'1,,
€у3*,
катоднь:й
по,ге1тци&л
чинает
во'зр&огать
до
анате*тий,
соответству|ош{их
ни|о
щелочнь1х
ме{галл0в.
€
повьттцо:лием
температурь]
полярива1щот{[{ые
сдвигак)тся
в
ск)рону
болев поло)|сительнь|х
вначений
1гв]тциала
и
уве.т!ичива6шся
цредельнь|й
диффувлтонньтй
всех
реакц1!й,
проте:са|ощих
в
разлиннь1х
ин!!ервалах
шости тока
(ри9.
55).
Р,величо}гие
[со!{ценц)&]||ии
ваЁадия' }{ак
|{
'товь|1ц€'яие
тем|твратуры'
и&моняег
з|]д
лщр{&айиот11!ь1х
}сривь|х
(р!!с.
56): с
ув€личонием
рацци
\[€}в
кРивьте
сдвшга|отся
в
сто1}ону
болео
Рис.
56. 3двисимость
вольфрамового
катода от п
тока в
олектРолитах 1(€1
-
}.1а€1
_
усь
при
77б" |1
!ё13,
о/6:
1-0,9; 2-3,\;3
!/
п!ы;к
по1€|1]{!!&лов
и
уведичивается
предельнь:й
дшффузион_
:тьпй
готс
всех
рвак1ц4й.
8се
эт:т
явления
характврй{ы
для
щ)о]{ооеов'
'р**.йщ''*
в
'облаети
деффузиошвой
ки'не_
'гр!11:,\.
Бьтход
по
току
при
эдектролизе
расплавов'
содер)|сатцих
!€1з,
зави'сит
от
уе7ов*тй
процеоса
и
преэ{сде
всего
от
|{а-
чаль:*ой
плотности
!'*,.
1!а1тример,
в
расплаве^
*€1_1'[а€1_
75,40|о
]/€1з
лрп
775'
пдотностй
тока
0,5;
0'7;
0'9;
1'1;
]]6'
'{'ь
||]т
"['"
ооответствует
вь1ход
полоку_(з
пересч9ге
;;Бй;ф;,;
12;
зо;
39;-48;
54;
361
тоь'
11эч'
1ь:1_оких
шлотноегяхтокачаетьметаллавосетанавливаетсявглуби-
1!е
эдектролита
вь1деля1о|]1|'1мся
н.а
катоде
щелочт{ь1м
метал_
;;;-;_;;р;;'.;.
п;;
пониясенной
плотно,сти
тока
больп:уто
дол1о
3а1{имает
,'"р*''р"д.
Бообще
в
ванне
6ез
диафрагмьт'
т. е.
в
том
случае,
когда
в
электролите
1{е
накапливается
й"/!"'"""т*,й
ванадий,
н
а-и
больц:ий
теор_етинески
вовмо'к'
ньтй
вьтход
по
току
йойе'
б-ь:ть
около
66'6%
в
пересчето
на
восстановление
ионов
!3+.
Фбразу1оцщеся
в
реэультате
вос_
становле}{ия
ионь1
у2*
диффундиру:от
от
катода
в
глубину
о',2+
элекц}олита
со
окоростьк)
--+су2+
и
затом
окисляк[пея
т1а
а![оде.
Рассмотрев
изло'{сен}{ое'
мо]1сно
сделать
следу:ощий
зь1вод.
11реэтсде
всепо'
о
трудности
осуществлет{ия
элекц)олиза
с вь1соким'
вь1ходом
по
току
в
ваттнах
бев
диафрагмьт.
[ей-
ствителъно'
интервад
|*,
в
котором
вь]деляется
металл'
не_
3е]|!'114'
и
всегда
есть
опасность
расходования
больтшой
доли
тока
на
пере3аряд
ионов
у31
до
!2*,
8
1!е
на
вь1деление
ме-
талличоского
ванадия.
|{о_видимо'му, для
осуществле1{ия
эдектродиза
с
вь1'соким
вь1ходом
метадла
по
току
нейхо'
д*"'
йост*ий
автоматический
коштроль
за
потенц1'1адом
}са_
фода
и
по
мере
нарастания
на
электроде
осадка
пр'ограмми_
рова,нное
ивмене1{ие
общей
сильт
тока'
3.
@лектроосаз|сдепие
ва,]адия
из
расплавов
с
рав]1п|['1ой
средпей
ва]!ептностьк)
вападпя
!{ри
эдок1ролитичес1сом
разло}*€о[{ии
соединоний
в
элок'
ц}од!1темо,16етполучитьсяраздичноесооп[!о1]]е1{иет{.о1тц9г|т.
й''*''*
двух'
и трехв&де[тт}{ого
занадддя'
3
зав|4сшмосг![
от
фли!г*1|ь1
9того
соо|г1{ош[ен:гл!
измфтяотся
и|ггерв8л
плоп[1Ф'
ш|д
трш,ц в
1{,0тородд
}18
катодэ
вь1де'1я€тся
мет::лл'
въ!ход
в8ша{]ц{'8
по'1п0ку
!'
круп1{о@Б
щ}[{сг8длов
в ооадках'
;
й6ляри3а'1]{'о||:{ь1е
кр
авь1е
для
!т}[о1угног0-_1са1года
в
рас-
]1л&в8х,
содер}|6&щ!гх
однов1}емФ|но
\[€1э
и
9€1з,
име1ог
про_
10?
1о,2.

ме'гсуточнь1й
характер
по сравне|{ик)
с вазисимостям]д
0-\в1
в электр'олитах'
гдо находятся
только
ионь1
!2+
ил:д
!3+.
Ёа
рисунке
б7 представлена
совокуп1{ость
кривьт*,
!|о.
л!дтеннь1х
в эле}стр,олите
1(б1-]ч}а€1_961з,
находив1]1емся
Ртте.
57.
3ависимость
потенциала
вольфрамового
'сатода
от плотности
тока
при
температуре
700'.
!геця
вь|дер)*ски
100
а
расйлава
}(ё]
_
$а€1
_
3'30/0
ус13
в контакте
-с
10 е
металлического
ванадия'
мшъэ
7_|з
2_10;
3_25э
4_35;
5_4б;6-Б5,
ра3личн,ое
время
в }0онтакте
е
металличоским
ванадием.
Фстаточньтй
ток,'соответствутощий
реакции
частич}того
вос-
становления
ионов
!3* на
катоде'
умень1цается
по
мере
уво_
личения
вь1дер'тски
расплава
в
контакт9
с металлом.
}1нтер-
вал
плотности
тока'
в
котором
происходит
вь1делени@
$€.
талла,,соответственно
увеличивается.
![одобньто
вависим0_
91ч_бь:д_ч
получень]
и |.
]]айтиненом
[74]
в
расплавах
1(€1-
т,!с1_ус12-ус13
при
450" (см.
рис.
52,.
'
'
8ьтход
по
тотсу
ванадия
при
одттой
и той
ясе
плотт!о|ети
цока
уве.7п'1чивается
щри
умень1це|тии
средней
в&]18н!ЁФ9г!{э.|
|1тр1*",, :щ
эде11Роли3е
раоплавов'!(61_$а€1:'сЁ'
у9ь
('1:1,3
а|см2,77Б')
сродйм
вале.нтно"''*
б;_2,в']
э,в;
-д,4'
2'21 2
ооответствует
следутошцй
вьтход
по
току
(в
пе"
р^осч€|1!е
на
ра3ряд
иот|ов
уз+):
361'
47;
51;
62;
3б;'9то1,.
}€ристалльт
в
катод}1ь1х
осадках
укрупня]отся.
тйк,
''р"
'ех
108
п
|о
уё
?|се
условиях
количество
кристаллов'
размером
лтенее
320-р'
изменяется
.''"дуйй"*
'о6разом,
йес.
0/о
з
84,
79,
78'
71, т\.
4.
[|оляризация
э[сид!сих
}сатодов
}(ак
6ьтло
отмечено
ранее'
скорость
процесса
анод}того
растворения
черновь1х
оплавов
лим]тгируется
тшлашпообра-
!Бй!й"'.'*.
[ля
йоддер}|са'{ия
€е
на
доляс;ом
уров11е
требует-
ся
периодичоски
удалять
1цлам'
что
в
прит1ципе
не
всогда
удается:
как
раз
удалет1ие
тшлама
зачасту1о
делает
шро_
]дБсс
рафинированйя
периодическим'
![спользование
в
ка_
чостве
анодов
)|сидких
сплавов'
в
которь1е
тем
14л!а-
ау\1ъ\м
спооо6ом
введе1{
нерповой
мегалл
и
откуда
он
спосоое}1
се'
дектив]!о
вьтделятьёя'
иногда
мо'кет
ре1цить
вопрос
непре'
Бй""'*
рф""ир9'|ттия.
|{римеси
рафинируемопо
метад_
ла
дол'кнь1
'в
атом_'случае
хоро1цо
р&створяться
в
металде_
[т|ос]дгеле.
€ледует
,отметить'
что
электролиз
с
'*сидким
анодом
об_
ладает
,существенЁ{ь1ми
преимуществами
ли:шь
в
том
слу-
"'"|
*"''
ра+финируемьтй
металл
вводится
в
металл-1{о'си_
тель
отн'осительно
йростьтм
и
детшевь1м
споеобом
(например,
электролизом
хлоридов,
электролизом
с
анодами
и3
загряв-
!{еннь1х
,соединений),
а
не
готовится
!опдавл€'ние'м
компот{ен'
тов
при
томпературе'
превь11ша1ощеи
точку
плавления
рафи-
д{ируе1шого
металла.
-_
'о''р'д"денньтй
интерес
представляет
и
примен€ние
}1сид-
ких
катодов
и3
металлов
с
вьт',сокой
упругость1о
пара'
кото-
|"'"
*'"у'
бьтть
сепарировань1
от
вь1деляемого
метадла
в
{1*,,*".
Б
последние
годь1
этот
путь
привдекает
в1тимат{ие
иес'Ёдо"а'елей
[1
20,
1 21].
?1з
скаванного
вьт1ше
мо${но
сформулироватъ
о'пределен-
ньто
требования
к
металлам_н'осителям'
составляюц{|{м
о'с'
11ову
}|сидких
а[{одов.
-
-Ё_-^^_-
1трейде
всего'
металльт-носители
дод31снь1
образовьтвать
ясидкие
сплавь1
с
достаточно
вь1сокой
концентрацией
ра-
финируемого
метадла
при
температуре
эдектроли3а;
во_
йторьтх,
они
дода{сньт
обладать
эдектрополо'{сительнь1м
по_
.
те:тциалом
в хдориднь1х
электролитах'
э|сидк"е
катодьт,
из
которьтх
3атем
отго1{яется
металл_
оастворитель' дод}*сньт
удовлетворять
первому
тре6ованито'
Ё;;#;ъ;;;,
?б'''д,'"-
вь:сокой
упругостьк)
пара'
1акими
'-метадлами-носителями
для
вь1деления'
т!апример
ванадия'
й'"у'
6ытъ
%п,
са,
в!,
РБ,
$п,'6а'
сплавь1
электроподояси_
|пельнь1х
*"'*''''.]'(;;;;й;р;'5б';
в1,
-
?ч%-Рь'-
20}9
$п.,
;;;
:
9'6;
;'
ьъ
,;
й1;';т;ъБ;
й,'й'ъф
| 2,5
у,
-
$'',
Ё,,,
:
60'б"
ц
др.).
109
!,{
соолсаленик)'
растворимость
ь&т1ад'тя.
в этшх
1}1етадлах
при
температурах
500*900'
точно
не
на.
Фднако'
исследуя
катод1{у}о
поляризацик)
1!!€[&.1!7[Ф8.;
ванадийсодер)1сашщх
расплавах
и
проводя
длительное
оса
девельству}ощие
о
целесообрааности
плц
применения
э{сидких
металлов
при
электроли3е
ъаЁ.ад*{
д€р'|{ащих
расплавов.
*
;Ё
$
$
{
-ф
\
/7о:пенцоал
катто0о,
€ольтп
!3:-с,
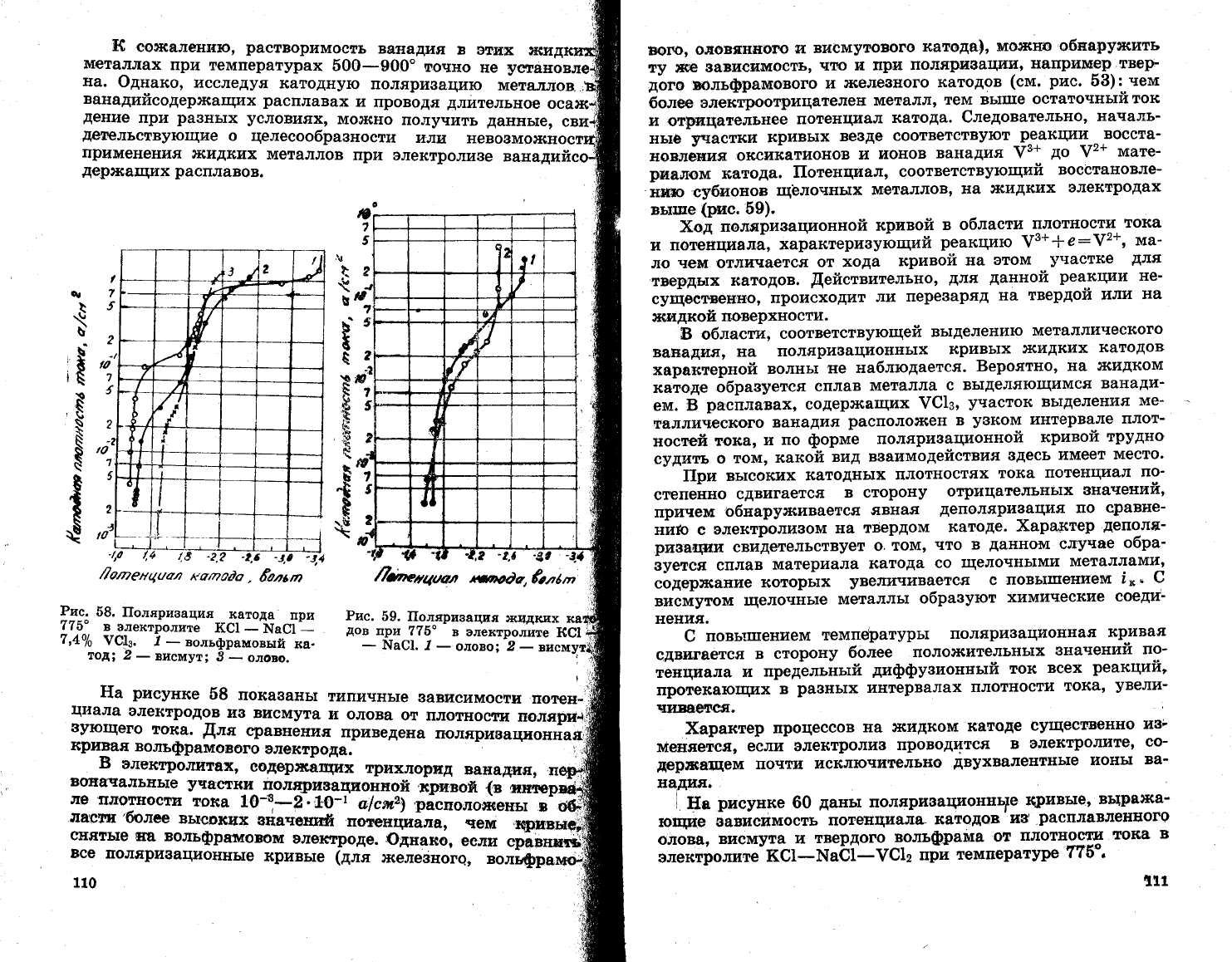
58.
11оляризация
катода
при
77б"
в электролите
}(€1
_'}'та€1
_
7,4о|о
\([з.
.1
_
вольфрамовый
ка.
тод; 2
_
вис1\{ут;
3
_
олово.
ц!4ала
электродов
и3
висмута
и олова
0г
плотноепи
зук)щего
тока.
для
став1!ения
приведена
ттоляриващ}|онная
в@8чальнь]е
учаегк-и^
полцривацпон|той,|сдш!зой
{з
лв
тд9т}1ости
тока
1о-:-2.
||-|
о|см2|'рйсполойеньх
в
'дасш;'флее высоких
зт!ач&т:м
пйепциада,
чем
спять1е
на вольфрамовом
ало1сгроде.
Фдшако'
е"',
ф
все
поляриаацио}!нь|е
кривь1е (для
а*селезног9,
110
1
7
5
2
уб'
7
5
/,в '2,? -2,6 -'.о
:т4
дение
при
ра3нь|х условиях'
моа{сно
получить
даннь[е'
сви
вого'
одовя}1!то!!о
и
висмутового
|сатода},
мозпсно,обпаруэтсить
ту
'п{э
вависи1}1ость'
что
и при
поляр}1защии'
напришер
'твеР
дого
вольфраш!ового
и
,1{1еле3яого
катодов
(см.
рис.
53):
нем
болод
элек1роотрицателен
1шеталл'
тем вь11ше
остаточ]{ь1и
ток
и
от[}ицательнее
поте}{циал
катода.
6ледовательно'
началь-
нь1о
!гт|астки
кривь1х
зевде
соответству1от
р_еакциц
^
зосста_
новлёния
о1{си1{атионов
и
ионов
ванадия !3*
до
!2+
мате-
р||а'1ом
катода.
|[отенциал'
соответству1ощий
восстановле*
тт|||о субио|{ов
щёлочшь1х
металлов'
1{а
'|сидких
электродах
вът|пе
(рдс.
б9).
)(од
поляри3ационной
кривой
в области
плотности
тока
и поте|тциада'
характеризуйщий
реакцито
$3++е:!2+,
#4'
ло 1тем отличаетея
от хода
кривой
на
этом
участк@
ддя
твердь]х
1сатодов.
[ействительно'
для
данной
реакт1ии
1{е-
сущоетве!{Ёто'
происходит
ли
пере3аряд
на
твердои
у!|||1
на'
а|(,идкой
поверх1{ости.
3 област:а'
соответству1ощей
вь1делени1о
металлического
вавадия'
на
поляризационнь1х
кривь1х
3{сидких
катодов
хара1стерной
волнь1
не
на6лтодается.
8ероятно,
:{а
'1сидком
к&тоде
обра3уется
сплав
металла
с
вьтделя1ощимся
ва\1адтл-
ем.
в
ра[сплавах'
содер}1сащих
9€1з,
участок
вьтделения
ме_
т&лличес|оогованадиярасполо'{сенву3коминтервалеплот-
носшй
тока'
и
по
форме
поляривационной
кривой
трудно
еудить
о
том'
какой
вид вваимодействия
здесь
имеет
п!есто'
|[ри
вь:соких
1сатоднь|х
плотноетях
тока
потенциал
по_
степе}{но
сдвигается
в сторону
оц)ицательнь1х
значений'
причеш
обнаруэ*сивается
явная
деполяриаация
по ерав]{е-
нию
с
электроли8ом
}1а
твердом
катоде.
)(араа*тер
'деполя-
риза[п{и
свидетельствует
о,
том'
что
в
дан}{о}!
с,[учае
обра-
зуется сплав
материала
катода
со
щелоч}1ь[ми
металлами'
содер)1сание
которь1х
увепи([ивается
с
повь11пением
'в"
с
висмутом
щелочнь1е
металль1
образу1от
химические
соеди-
}|ения.
€
повьттпением
темпфатурьт
поляри3ационная
кривая
сдвилается
в сторону
6ойее
поло'!{ительнь1х
значений
по_
тенциала
и
предельньтй
диффувионньтй
то1с
всех
реакций,
протекаю1щ{х
в
раз:ть1х
и|:тервалах
плотности
тока'
увели-
чивФ91\ея.
)(арактер
процессов
|та 3*сидком
к8тоде
существен1|о
и3;
йезтяется,
если
электролив
проводится
в
электролите'
ео-
д€р!'0а1цем
почти
искл1очитель11о
двухвалент}{ь1е
ионь1
ва_
"]*Ё:'
рисунке
60
даньт
поляризационнте
-т{р-и|19,_
]Р:Р"*"-
топтпе 3ависймость
поте]тциа;1&
катодов'и8
распдавле||цого
олов&'
висмута
и
твердого
волъфрама
от
плот1|остл|
тока
в
э""'йй""""""кст_ш"ё:_ус:,
п$'й
температуре
тт5о.
!11
Рйссацс:ал
аэтоёц
{о:тв
тп
Рис.
59. |[оляриза'1пя
'*чдк|{х
дов
при 775-
в электролите
1!61
_
|.[а€1.
-1
_
олово;
_2
_
висму:
}1а
рисунке
58
показань1
типичнь]е
вависимост}|
попен-

Б
област*:
невьтсо1{их
значений
пдот}тости
то1са'
когда
ша
катоде
протекает
уаке
процесс
ра3ряда
ионов
92+
до
:ше-
Ф
\
{
\
у
Ё
<!
$
ч
$
ч
{
$
/7о.п енс1
оа л
нс;о о
ёа, €оа6 ;о
Рис. 60. 8ависимость
потенциада
катода
от плот!|ости
тока
при
775"
в
расплаве
кс1
_
}.1а€1
_
8,2оь
уо\2. /
_вольфрам;
2-
одово; 3
-
висмут.
це]ттра1ц,1ей,
полуним
.
€корость
оса'*сдения
металла
и8 электролита
равна
9,,я+
_$.сс;'+_€т2+),
(1у_5)
а
скорость
диффузии
атомов
ванадия
от
поверх1тост]!
9лектрода
в
глу6ину
металла
_
{.с",_4>.
8еличиньт
[!'*]
и
[9] должсньт
бьтть связагтьт
с
плотно_'{
стьто
тока.
[ля установив!цегося
стацио1!арного
процесса
оба
териалъньтх
пото1са
дол'*снь1
бьтть
равньт
и
потоку
алектрических
зарядов
119
[
талла'
,потен]{14ал
'|сид]{.их
эле1стродов
несколько
Ё![,}|(Ф;
чем
твердог1о'
и и3меняется
с
увеличе!{ием
плотности
то[са.
3атем
обе
кривь:е
почп!.1
сли_
ва1отся'
и ли1ць
когда поте1|-
циалопределятощей
€!аЁовгт!,.
ся
реак|ц{я
вь1дрления
щФ7|оч_
пого
металла'
вновь
наблто.
дается
деполяризация
'{сид-
ких катодов.
1акой
характер
и3менения
потенциала
э{сид!со_
го катода
мо'*сет
бьтть
объяс_
}|ен,следу1ошщми
причинами.
![отенциал
тсатода
опре'(е.
ляется
величиной
каэ*{ущегося
стандартного
электрод[{ого
по-
тенциала
ванадия
Ё\,,э1и
ат<-
тивность1о
ванадия
в
пов€рх_
ностном
слое ,}]{ид1{опо
като-
да.
3аменяя
приблиясенно
ак_
тивн,ость
атомнодолевой
кон-
)
|',э+
'
"{{с;,*
_€уэ+):
{с"_с;\:#,
су-7)
где
с-
ко}]цетттрация
в е
-шон|см3
'\л*т
а.
атом|
см3';
Б",-
толщина
диффу3ионного
слоя в электролите, см1
8ц"_
толщина
диффузионного
слоя в а'сидком
металле'
см.
1аким
образом,
концентрация
ванадия и его ио}{ов
в
поверхностнь1х слоях мо'*сет 6ьтть
вьтра}|се}та
чере3 катод-
ну|о плотность
тока.
Бсли
велинину
6у2* вь]разить через
предель1ту1о
диф'
фузионну:о
плотность тока !'', и при1{ять'
что катод
перво-
1тачально не
содер}|сит оса;кдаемого
металла' то
для
элект-
ролитов
с
невь1сокой концентрацией оса'кдаемого
металла
формула
примет вид
Ё:соп$!
+$тв(?_'),
тогда как
для
оса)!сде}{ия
на твердом катоде
2.3лт
.8=сопв|1
*
'
19
(!"р_
|).
(ту-8)
(1у_9)
8:Б\,рэ+'#''%+
(1у_{)'
€равнение
последних
двух
уравнений
с
опь1тнь1ми по-
ляри3&ционнь11ши
кривь1ми
показь|вает'
что
раствориш|ость
ва1{адия в
'1сидком
олове' висмуте у{ тал]1у|у|,
вероят1{о'
низ'
ка при температурах
электролиза.
|{роведеннь]е
опь|тьт
по
длительному
электролизу
ванадийсодер'1сащих
электрол1.!-
тов на оловянном'
висш[утовом и
галлиевом катодах
пока-
аали' что
ванадий оса}}(дается
на поверхности
электрода
в
виде
дендритов
твердого сплава' и
растворимость
его
в }*сид-
ких катодах
достигала
лу!!71ь
долей
процента
(максималь-
ная 0,3% в
,тсид1{ом $п).
Аендритнь:й
осадок
содер'кит
3на-
чительное
количеетво
ванадия
(например'
на галлии
160/о
9).
|{ри оса,}[{дении
на
цин}совом
катоде
лри [:'|5Ф'
удает-
ся
достигнуть
концентрации
ват1аду1я. в сплаве
2п_\
до
3
0/9,
о'(нако неи3вестно'
является ли сплав гомогеннь1м
рас'
твором'
а
не суспенвутей
мелких кристаллов
ванадия
или
его
хим.ических соединений с
цинком
в ,[сидком
цинке.
Б настоящее
время еще
недостаточно
даннь1х для
одно-
значного
ре1:|ения
вопроса о
во3мо'1сности
приме}!ения
хс}|д-
}сих электродов при
электролизе
ванади1тсодер}|сащих
рас'
плавов. Ёеобходимь1
систематические
исследова1{ия
с
рав-
нь1ми
металлами
и их легкоплавкими
сплавами.
8-76
(1у
113

5.
[1роцессь[ прп элештрол1|ве
расплавов'
содер,[сащих
о!спс][ь|
ванад]!я
3опросам
электроли3а
расплавов
распдавленнь1м
галогенидам'_
та}с
дера1сащих
кислот и
расплавле1{нь1м
боль:шое
внимание
исследовател,ями.
[€ото0нъое
процессъ[ в ?ало?енш0нъох
распловах,
в
част-
}{ости'
в системе кс1-т,!с1_!2Ф5
п!и 450'
детально
ивуне-[
нь: .}1айтиненом
и Родсом
[1221.
,{ля
вскрьттия
механизма
использовались
хронопотенциометринеский !т вольтампер_
метрический
методьт;.измерялись вь1ход
по току
и
потен_
тц|1ал
раз.л1лчньтх
электродов в
расплаве.
}становлено'
что
в
ревудьтате
восстановления
по
реак_!
[
ции
69:Фь
*
21,{+
*
4е
-*БэФ
.
2\эФц.
49яФь
*Ф2-
при
потенциале
0,26
относ!ттельно
платинового электрод!
обравуется' литийванадатная
бронза,
плохо
растворимая
в
расплаве.
||оказатто такэ*се' что в
динамических
условиях
на'
восстановление молекуль1
!2Ф5
!асходуется
0,5_017
элект-,
рона'
в
равновеснь1х
условиях
0185. }1з
уравнения
Ёерпста
следует' что
9та,величина 1{е
долЁсна
превь1|шать 0'67. Ф6ъ-
яснением' по мЁенито
авторов'
.
мо)|сет слу'|сить'
адсорбция
\/эФь или
ванадатио1{ов
:{а поверхности
бронаьт и полупро-
водниковь]е свойства
последней.
,Б
расплаве
6а€1я,
содер'|сащем
растворе|1}тук)
поляри3ационнь]х
кривьтх обнаруа*сеньт вол}|ьт'
вутощие
реатсции
частич1{ого
восстановле|{ия
причем
потенциал' при котором
протекает
реакция'
и
чиньт
пдотности то|{а
и3меня]отся
с
уведиченфм
концент-
ращм
!эФь
и температурь1.
![ри
длительном'элекц>оли3е
}{а катоде
появля1отся
ниа1|:ие окисльт ванадия
[31].
11ри
электролизе
расплавов
А18гз_1(3т_!эФь
на
1!а-
тоде
вь1деляется
окисел
$Ф:, а пРи электроливе А1€1з-,
_кс1-ъФь
осаАки не о6раау:отся
[123].
-
9летс{Ролшз
\эФь
в
р('сплавленнъ'х
боротох
ш
фосфотах-
3ависийости
потенциала относительно
платинового
рода
от
плотности
то1са' полученнь]е
нами
{31]
для
вов
1ттацРэФт_\[':Фь
и }.[аэ3+Фт_9яФь,
свидетельствук)т
том' что
поляри3ация
катода коттцентр8ционна. 11ри
тельном электроли3е
ив та}(их
раст!лавов
на
к8тоде
ются
окисльт
\[Ф и
!э@з.
3
работо [124] указьтв&етоя'
щ)и
эле]{тролизе
фосфатньтх расплавов
образуется
ванадия
уР
[1241,
а из
расплавленнь1х
6ората лития
и
пия'
содер}|сащих
у9о5
[125],
вь:деля:отся ]1'пине]1и
\'1
116
тшлакам)
уделялось
\/яФь,
н&
соответст-
1т19Ф_тйяФз
у\л||
],|эФ_$яФз.
3
слабощелочнь1х
расплавах
ос&э|сдается
\/Р,
в сильнощелочнь1х
расплавах'
тте содер]*са_
щих
хлоридов'
вьтделяется уо
[126,
127].
йеталлический
занадий
не бь:л
оса)1сде1{
ни
в одном случае.
7€ото0нъье
прощессъ[.
в
ра,спл('вленнъ'х
1!'ло1сах. 1[атод'
}тая поляр'1вац!1я
в
1цлаках на
основе 6аФ
ивунена
в
рабо'
то
[128]
с
цель1о
определения
характера
лимитирук)щих
сф{дутйт1вар$'да
разря'ка1ощихся
ио]|ов. 1|а
рисунке
61
при'
веденьт поляривациот{нь1е
кривь1е'
получе1|ньте
на
Бе-1
катоде
(до
50/о \/)
при
15б0_1570"
для двух
растворителей:
42,б
(аФ;
50,0
А1:Фз ут 7,50|о
1!19Ф
(кривьте 1, 2) п
42,0 |а9,25,0
А1эФз; 28,0 $!Фэ
тт
7,|о|о
[!1ф
(кривые
3,4|.
1{
растворителям
добавляли
соответственно
1,5;
3,0;
\,4
п2,8\э@ь.
Рис. 61.
11оляривациоввые
кривые
для
р8спл&'
вов
€аФ
*
1!18Ф
_
А1яФз
_
51о2 с
добаввамп
9:Фь. ] ц
2
_ддя
распл8вов
с
добавкой
1'5
и
8,00/о 1эФь;
3 *т
,:1_
для
расплавов
с
$1Ф2 п
дФ
бавкой
!,4
т. 2,80|1
\эФь'
5
_
для
первых
участ'
ков
кривь1х в координата"
ц
_
ц(1-*).
11редельньте
токи при катодной
поляризации
6ь:ли
про-
пор1{ио|1альт1ь1
еодер'1сани1о
9зФь
в
1||лаках' и
поляризация
ц
связана
с плотность1о
тока соотно|цением
-чу31-т,
(т_д'!.
где п,=5.
(1у_10)
!,р)'
'
А9
'э
\_
'
Авторьт
[1281
полага:от'
что на катоде
пятивалентный
ватладий восстанавдив1:н:;':"""."'".
.
]1ри
этом скорость
процесса
димитируется
диффузией
иот:ов
95+.
1!оэффит{ттенть:
диффузии
в э{сидком
э|селезё
!
/ц
значительно
больтше,
чем в
расплавленнь1х
окислах'
и
чле1т'
входящий
в
урав}{ение
конце:'трационной поляризации
_#'"(т+ф),
близок
нул}о'
так как |.',')!*.
Ёа
вторьтх
участках
кривой 2
долясен
ра3ряэ*{аться
алк)-
миний,
а
на криво{1 4
-
кремний.
1аким
образом,
в подоб-
1{ь1х
расплавах
во3моэ1сно
раздельное
осаясдение
ва!1^д9|я |1
кремния.,{ля
подтвер}|сдения
этого
полоэкения
изучалась
поляри3ация
в
расплавах
с небольтцими
добавками
$!Ф2 и
9эФь. Ёа
рису}|ке62
кривая-/
полунена при
1550"
на €ц-
9 катоде
для
расплава'
содер}1сащего' вес.
0/о
:
40
€аФ;
50А12о3; 6]у1вФ; 2$|о2
тт 2,4\оФв.
Ёа кривой
.1 имеется
две
ветви
(1",7|,2
и
0,б о|см2), которь1м
в координатах
ц-
_1в(1-
91
''"е*ают
прямь|е
3
п
4.
]['гловьте коэффициен-
дпР
ть1
этих прямь]х
соответству1от числу
алектроттов'
участву_
}ощих
в
реакции,
тт 6лэтвкп
к
пяти
и четь]рем,
[. €. первая
ветвь
кривой соответствует
разряду
ио}{ов ванади'1'
а
вто_
рая
-
разряду
ионов
кремния.
0сли
в
расплаве
име1отся
ионь1
}келеза'
то наполяри_
зационной
кривой 2
обра-
зуется
три волнь1'
а в
коор_
[-а7саР
'?.нЁ
!о-' /ш
/а
20о
-?,/пв
ц
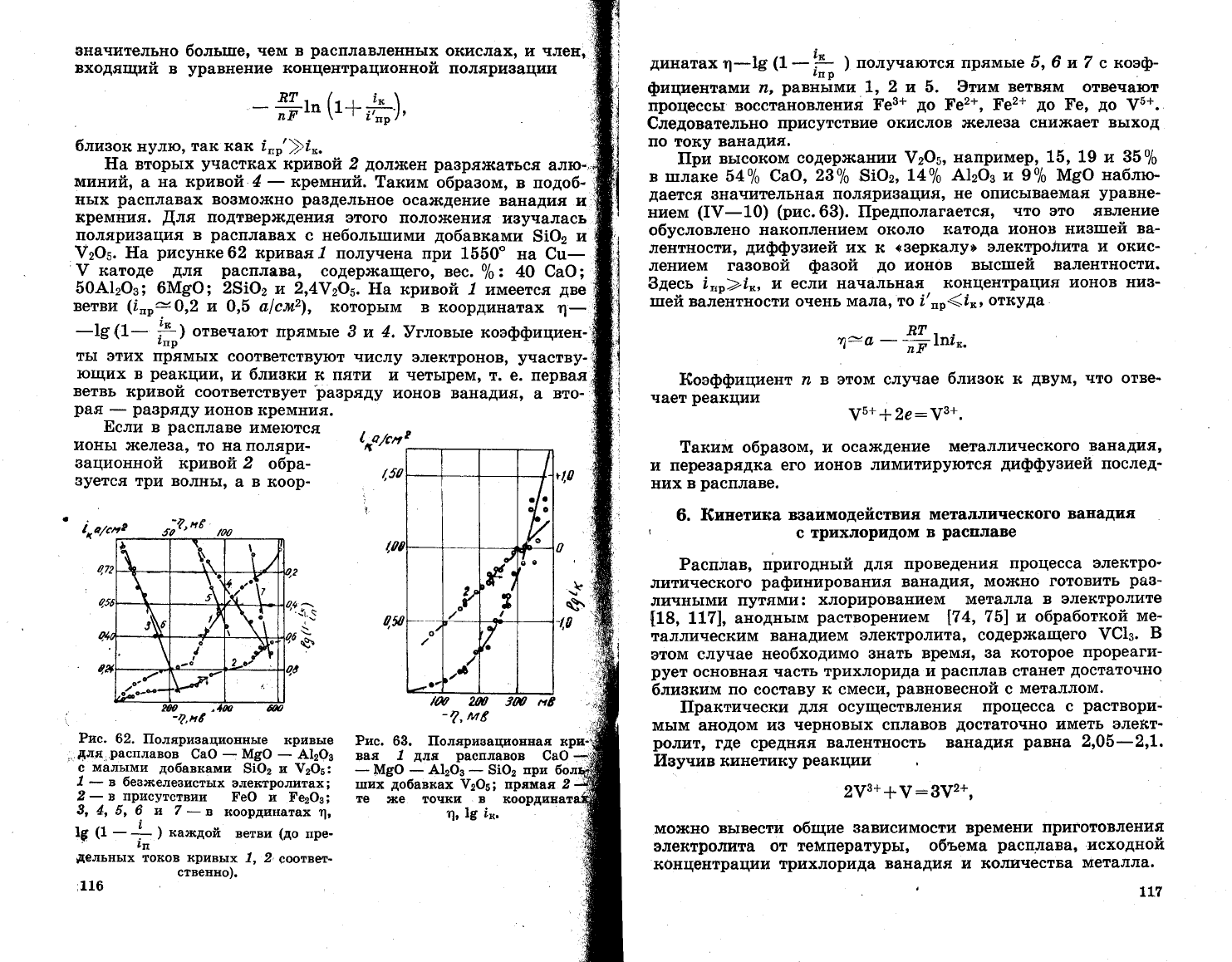
Рис. 63. 11оляризационная
вая 7
для расплавов
€аФ
_
1}1в9
_
А1:Фз
_
$!Ф2
п}и
:пих
добавках
$2Ф5; прямая 2
те
''се
точк![
'
в
т!' 19 |^.
150
\1.
\
\
ф
-?,й6
Рпс. 62.
11оляризационньте
кривь]е
'''
для
раеплавов
€аФ
-
1!19Ф
-
А1эФз
с маль|ми
до6авками
$!Ф2 и !2Ф5:
/
_
в безэкелезисть1х
элекгролитах;
2_в прттсутствии
РеФ
и РеэФз;
31
4,5,6 п 7
_в
шоордин&т8:<
!:
1в
(:
_
"
)
ка:кдой
ветви
(до
пре-
'!7
дельнь]х
токов кривь!х
1, 2,
соотвег_
ственно).
116
ь
чь
дин&тах
т!_19
(1
_
р )
полунатотся прямь1е
5, 6
*т 7
с
коэф-
|пр
'
фициетттами
2'
равнь1ми
1'
2 ут
6.
9тим
ветвям
отвеча1от
процессьт восста}1овления
т'е3+
до
Ре2+, Ре2+
до
Ре,
до
!5+.
€ледовательно
присутствие
окислов'|селеза сни'{сает
выход
по току ванадия.
|1ри
вьтсоком
содер}|сании 9:Фь'
например, 15, 19 и 35%
в 1плаке 54о|о
(а0,23$
$!Ф:,
\40|о
А\эФз
ц 90|о 1!19Ф
набл:о'
дается
3начительная
поляризация'
не опись1ваемая
уравне_
нием
(19-10)
(рис.63).
|[редполагается'
что это явление
обусловлено
накоплением
около
катода ионов
низ]|]ей
ва-
лентности'
диффувией
их
к
(3еркалу}
электро,ита
и
окис-
лением газовой
фазой
до
ионов
вь1с1шей
валентности.
3десь 1'',}-[*,
'1
если началь1{ая
концентрация
ионов низ_
ц:ей валёнтности очень мала'
тФ !/'рх{!3,
откуда
!{оэффициент п
в этом случае
близок к
двум'
что отве'
чает
реакции
у5+_!2е:у3+.
1аким образом,
и
оса)|сдение
металлического
ванадия'
и пере3арядка
его ионов
лимитиру}отся
диффу3ией
послед'
них
в
расплаве.
6.
}€пнетика вваимодействия
металлического
вападпя
!
стрихлоридом
в
расплаве
Расплав, пригодньтй
для
проведения
процесса
электро'
литического
рафинирования
ванадия'
моэ*сно
готовить
раз-
личнь1ми
путями:
хлорированием
металла
в электролито
[18,
117],
аноднь1м
растворением
[74'
7б1
и обработкой
ме_
таллическим
ванадием
электролита' содер;*{ащего
\[€1з.
Б
этом
случае
необходимо
3Ёать
вре1ця'
за которое
прореаги-
рует
основная
часть
трихлорида и
раеплав
станет
достаточно
6лизким
по
составу
к смеси'
равновесной
с
металлом.
11рактинески
для
осуществления
процесса
с
раствори-
мь1м
анодом и3
черновь1х сплавов
достаточно
иметь
элект-
ролит'
где
средняя
валент}{ость ванадия
равна
2,05_2,|.
!1зувив кинетику
реакции
2уз++у:3у2+,
мо}1сно вь1вести
общр:е
вависимости
времени
приготовле}!ия
электролита
от температурь1'
о6ъема
расплава'
исходной
конце11трации
трихлорида ванадия
и количестБа
металла.
117
