Волейник В.В. Высокотемпературная электрохимия и физическая химия ванадия
Подождите немного. Документ загружается.


3
заклточе}{ие следует отметить'
что
если
повёдение
ва-
}{адия
в
расплавленнь:х
хлорид&х
иаучено
достаточно
пол_
]{о
и веесторон}{е'
то
атого нелъ{]я
ска3ать
о
расплавле1{нь1х
!пдаках.
1{ео6ходи:шо
проведение
систематических
исследФ.
ваний,
направленнь1х
в ос1товном
на
количествен1тое
опре_
деление
конста1!т
равновесия
меясду
металлом
и
его иона-
ми
всех вале|{тностей и
вьтяснение
влияния
природь1
т]1ла-
1са-растворителя
на эти
величинь1.
|
глАвА 11т
кинпти[сА
элшктРохимичвского
окислвния
вАнАдия,
пго
сплАвов
и
сошди1|пнии
1!!ногочисле1тнь1ми
работами
в области
кинетики
вь1со-
котемпературнь1х
электроднь1х
прощессов
показано'
что
тотси обмен&
достигак)т
десятков
ампер
на
квадратдть:й
еан-
тиметр
и обьтчно
стадией,
лимитиру:ощей
максималь|{о
во8мо'{снук)
скорость
при
данной'
температуре'
является
диффуаия
исходнь1х
веществ
или
продуктов.
|]оэтому
пер_
воочередная
задача
-
определен11е
коэффициентов
диф_
фузтти
ионов
ванадия
разлинной
валентпости
или
}сомпле{к-
снь|х
группировок'
в составе
которь]х
они
вь1ступа1от
комп_
лексообразователями.
Фдним
и3 основ}{ых
приемов'
приме1!яемь1х
д]]я
изу}ения
кинетики
аноднь1х
про-
цессов'
так}|се
является
и3мерение
анодной
поляривации
и
вь1хода по току
в
равлич]тьтх
условиях.
3нание
величин
коэффициентов
диффузии'
3ависимо_
,стей
плотгтость
тока
_
потенциал
электрода'
плот1{ость
то-
к&
_
вь1ход по
току'
наряду
с
данньтми фазового
а1|адиза
продуктов [1&
электродах
и электролитов'
позволяет
прове-
сти од1{означ1{ое
количествен}{ое
сопоставле}{ие
ревультатов
экспериме1{та
с теоретическими
моделями
электроднь1х
процессов.
3ьт6ор
оптимальнь1х
параметров
промь1!|1ден_
ного
электролива
(плотность тока'
ко1|центрация'
те1у[пе_
ратура)
в
значитедьной
мере базируется
на
таких
мо'
делях.
8 настоящей
главе
приведеньт
акспериментальнь1е
дан'
т{ь1е
и
рассмотре}[
меха1{изм
анодного
р&створения
м€тал-
лического
ванадия'
его
соединений
(у'с,
уш,
\/Р, 9$),
не_
воторь|х
сплавов
и
окисно_уголь}|ьтх
а11одов.
3начительное
в|тимание
уделено
так'|се
вь|яснени}о
влияния
анод}1ого
1плама'
проме}|суточнь1х
соединений
и
материада
токопод'
зода
1{а
процесс
анодного
растворения.
59

1.
1(оаффициенть|
диффузии
ионов
ва}{адия
Б
хлорш0нь|.х
росплаас*.
$оаффициенть1
диффузии
двух
и
трехвалентного
ва}тадия
в
эквимолярной
расплавленно|
смеси хлоридов
калия
|1 натрутя
в
интервале
температур
850"
бьтлй
измереньт
авторами
раоойй-й-"
метричооким
(гальв&ЁФт€1а[й{еским)
мйодо,м.,{альнейтпее
развитие
он шолучил
в последние
годь1
и |широко
п!им€}|ял.
ся
4гя
изучония
диффузтч
в солевь1х
расплавах
и_т,''"ка*.1
,{ля
определеттия
коэффициентов
дй66у""*
"''й-!."._
дия
исполь3овалась
электролитическая
ячейка
и элекц)и_
ческая
схема
и3мерения,
подобная
применяв]цейся
в
рабо_
те
[97].
}1ндикаторнь:м
катодом
слу'тсили
полирова|т:1ь1е
молибденовьте
цилин
др|!11у1'
осаэ|(дение
на
которь1х
провод{-
лось
только^один
раз.
Результать1
изштерений
йредст1вленьт
на
рисунт(е
27,
тде
1{а){сдая
точка
является
средним
арифме*
тическим
8начением
пяти-]|]ести
эксперимейтально
:тайден-
нь|х
величин.
1о'
.
6ч
о$
'
/о7т
!ттс,
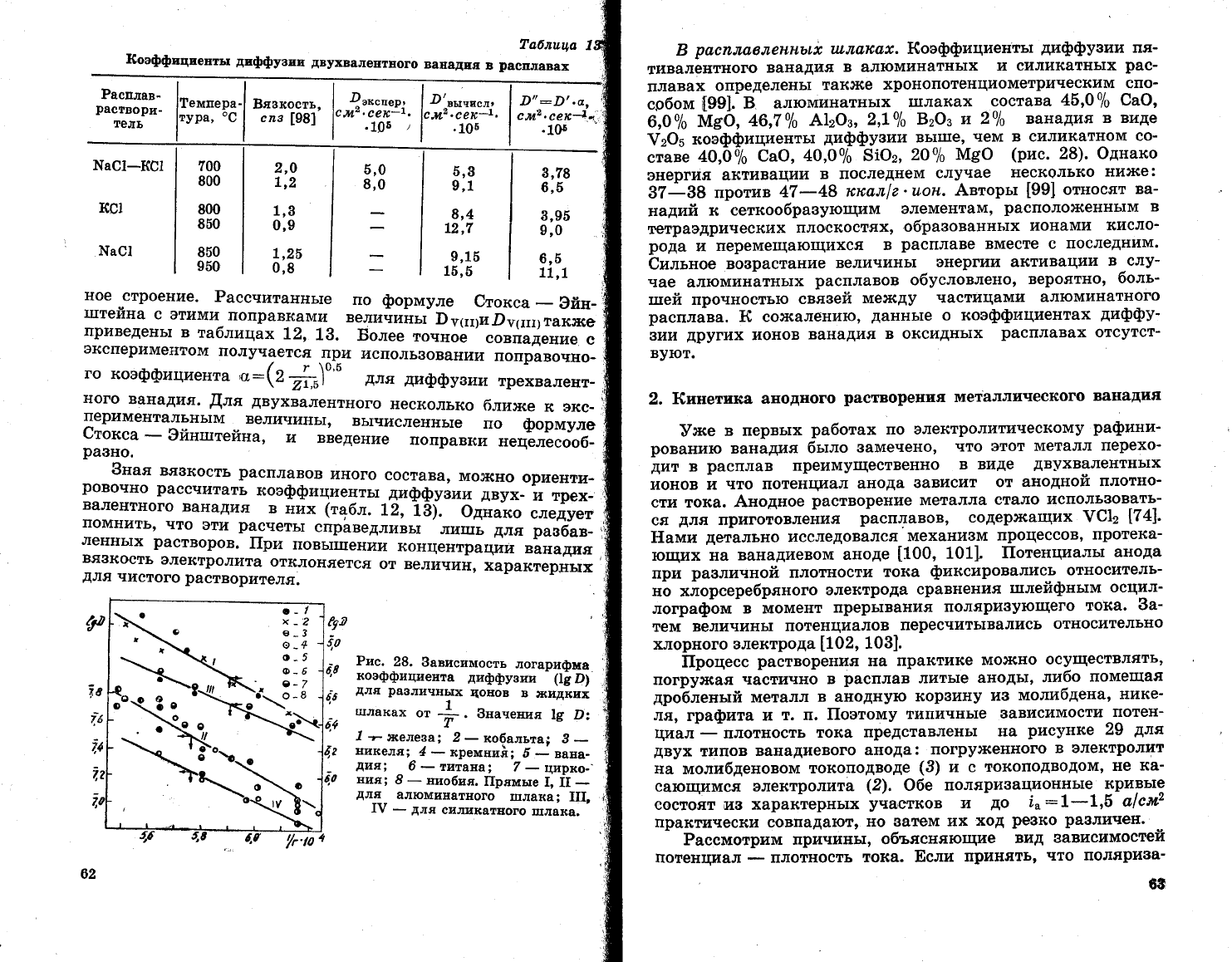
27.
1емпературная
3ависимость
коаффициентов
ванадия
в
расплаве.
7
_
для
двухвале|{тного
ванадия;
ного.
1!1етодом
наимень|цих
квадратов
вь1ведень:
уравнения
прямь|х'
отвеча}ощих
зависимостям
19 о:о_
}.
Фни
име:от
следу:ощий
вид:
для
тй'
(1])
13
2:-1,860-2,40.
10'.
+
-[
0,065;
для
9(111)
2
79
|
:
-
1,7 0-2,7
2.10,.
+
+
0,04в.
60
.7
1-
1;
5
!
\
с
\3
\
ф
3десь
о:|901,
2оу(тт):1:38'
10-2
сл[2'
€€$_\,
2от(]]т):2:0'
10-2
ель2' сею-\!
0:8!23'303
8,
где
8
-
энергия
активации:
8уктт;:110
00
кол|лооль;
г
8
у
кттт\:|2400
п
ол
|
м'оль'
1{ак
видно
из
таблиц
|2
ут
\3,
экспериментадьно
найден'
}{ь1е
и
рассчитаннь1е
по
уравненик)
€токса
_
9йнцттейна
6тт!
(т1т_2)
?о6лшцо
72
1!оэффпциепть:
дйффузпв
т|юхвалевтвого
ва1|адпя
в
расплавах
0":0'.а,
с1ут.2
.
сек_1.
.106
о':#.
ведичиньт
2у(тт)
и 2т1::'/не
совпадак)т'
если
считатъ'
что
диф-
фундирутот
<(прость1е)
1{атионьт
\2+
п !3+.
[ействите'1ьно'
в
й''Ё
|-б"''''
йоказано,
что
двух-
и
трехвалентньтй
ванад*тй
1{аходится
в
расплаве
в основном
в
виде
октаэдрических
"Бйй!"й"Б'й
усь.-
и ус163-
и
тетраэдрических
'.{ё\'э-
'
уёт,-.
суд*
'''
величине
отклонения
рассчитанньтх
коэф_
фициентов
диффувии
от
экспериментально
измере1тттьтх'
комплексьт
трехвалентного
ват{адия
более
устойнивьт'
чем
двухвалентного.
![о-видимому'
часть
двухвалентного
вана-
дия
перемещается
в виде
<прость1х'
катионов
по
меха1{из_
му
перескока
во
втору1о
координацио1{ну:о
сферу
и
далее
в-вак|нсии.
1рехвалентньтй
ванадий
перемещается
в
рас-
1ш1аве в
основном
в
виде
о'кта9дрических
цруп11ировок
9бцз_
и
частично
тетраэдрических
961д-
(при вьтсоких
тем-
пературах).
'в
|^'о'|е
|97]
предло}1{ена
поправка
к
формуле
€токса
_
3йн:шйейна'
учить1ва1ощая
электростатическу1о
природу
взаимодействия
частиц
в ионнь1х
'кидкостях
и
их
реаль-
с9
диффузии
иовов
2
_
трехвалент_
(ттт_1}
}[а€1-{€1
ко1
}.1а@1
700
800
800
850
850
9б0
1,3
0,9
1,25
0,8
3,16
5,75
_
5,3
9,75
9,0
13,6
9,8
16,7
2,т
4,95
4,6
6,95
5'0
8'бб
2'0
|,2
|
,,*".",,
!''".''"',
\с :п2
|ё
е|!т.
|с,м.2
.
с е
к_|
!
.:оь
!
.:0ь
|!
61
Расплав_
раствори-
тель
}{аб1_1(Ф1
}со1
1.1а€1
1о6лшцо
7
1|оаффпцпевтьп
дпффуапп
двухвалептвого вавадпя
в
р8сплавах
8
роспловленнъ[х
1шлок('х.
[[ооффицие}тть1
диффу3ии
пя-
тивалентного
ват{адия
в
ал]оминатнь1х
и сил!!катт{ь1х
рас-
плавах
опредедень1
так,}}се
хронопотенциометрическим
спо_
србом
[99].-в
алк)минатнь1х
1шлаках
состава
4б,|0|о |аФ'
6,00/о
йвб'
46,7%
А1эФз,
2,!о|о
в,эФз
п 2о|о
ванадия
в виде
1эФь
коэффициентьт
диффу3ии
вь11це'
чем в силикатном
со-
ставе
40,о%
€аФ,
40,0% $!Фэ,
200/о
1!19Ф
(рис.
28). Фднако
энергия
активации
в
последнем
случае
несколько
ниясе:
37-38
против
47-48
ю1оол| ?'шон.
^вторьт
[99]
относят
ва_
над*тй
к
сеткообразу1ощим
элементам'
располо;1{еннь1м
в
тец)аадрических
плоскостях'
образованнь|х
иот{ами
кисло_
рода
и
перемеща1ощихся
в
расплаве
вместе
с
последни1\{'
€ильное
во3растание
величинь1
энергии активации
в слу-
чае алк)минатнь|х
расплавов
обусловлено'
вероятно'
боль_
шей прочность1о
связей
ме'*сду
частицами
ал1оминатного
расплава.
}( соясалени1о'
даннь1е
о
коэффициентах
диффу_
зии
других
ионов
ванадия
в оксиднь1х
распдавах
отсутст_
вук)т.
2.
1|пнети!са
аподпого
растворения
металлического
ва1{адия
]['агсе
в
первь1х
работах
по электролитическому
рафини_
ровани1о
ванадия
бьтло
3аменено,
что этот
металл
перехо_
дит
в
распдав
преимущественно
в виде
двухвалентнь1х
ионов и
что потенциал
анода
зависит
от
а11од:{ой
плотно_
сти тока.
Анодное
растворение
металла
стало
испольаовать-
ся
для
приготовления
расплавов'
содер}|сащих
ус|2
[т41'
Ёами
детально
исследовался
механизм
процессов'
протека-
1ощих на
ванадиевом
аноде
[100'
1011.
![отенциаль1
анода
при
ра3личной
плотности
тока
фиксировались
относитель-
но хйорсеребряного
электрода
сравнения
тшлейфньтм
осцил_
лограф_ом-в
йомент
прерь1ва}|ия
поляризук)щего
тока.
3а-
тем величит{ь1
потенциалов
пересчить1вал||еъ
относительно
хлорного электрода
[102'
103].
11роцесс
растворения
}|а
практике
мо'|(}{о
осуществлять'
погру'{сая частично
в
расплав
лить|е
анодь]'
либо
поштеп|ая
дро6ле:тьтй
металл
в
анод}{у1о
корзину
из
молибдена'
нике-
ля,
графита
у1
т. п.
![оэтому
типичнь1е
вависимости
потен_
циал
_
плотпость
тока
представлень1
на
рису1{ке
29
для
двух
типов
ванадиевого
ат{ода:
погру'*сеннопо
в электролит
па
молибденовом
токоподводе
(3)
и с
токоподводом'
не
1са-
са1ощимся электролита
(2'.
Фбе
шоляризационнь1е-
кривь1е
состоят из характернь1х
уча,егков
и
до
|,:1*\'6
о/су*2
практически оовпадаклг'
но затом
их
ход
ревко
раздичен.
_
Рассмотрим
прйниньт'
о6ъяс1{як)щие
вид
аависимостей
потенциал
-
плотность
то:са.
Бсли
принять'
что подяри8а-
!!
! 4"*"''"р, !
)'".'""',
|ё.м2.
е
ек-|.
!с лс2. с ек-|.
|
.:0ь,|
.106
!!
|":0'.а,
сл'2.
сек4.'
.1ф
3,79
6,б
3,95
9,0
6,5
11
,1
700
800
800
850
850
950
2,о
712
1,3
0,9
5,0
8,0
5,8
9,1
8'4
72,7
9,15
16,5
7'2б
9'8
ное
строение.
Рассчитанньте
:,штейна
с
этими
поправками
по
формуле
бтокса
_
9йн-
величинь1
}
у1111и
2у11тт)
?&$)$ё
приведень1
в таблицах
12,73.
Более
точ1{ое
совпадение
с
экспериментом
получается
при
использовании
поправоч}{о_
го
коаффициента
'.:(2
*\",
для
диффу8ии
трехвадент_
:того
ва}{адпя.
['ля
двухвалентного
несколько
блиэтсе
к экс-
периментальнь|м
величинь|'
вь1числепнь1е
по
формуле
€токса
_
3йн:птейна,
ц
введение
поправки
нецелесооб-
раано.
3ная
вязкость
раеплавов
и1того
состава'
мо)кно
ориенти_
ровочно
рассчитать
коэффициентьт
диффузии
двух-
и ,ре*-
валентного
ванадия
в
них (та6л.12,
13).
Фднако
следует
помнить'
что
эти
расчетьт
спр!а.ведливь:
ли[ць
для
разбав_
леннь|х
растворов.
|{ри
повьтлшении
концентрации
ванадия
вязкость
электролита
отклоняется
от
величи1т'
характер]{ь1х
для
чистого
растворителя.
о-1
х
-'2
о-3
о-+
о_5
Ф-6
'
о-7
,\
.\о-ё
'\-,
\.ь\
|91
$о
с8
ёр
6р
р
то
/в
14
Рпс.
28.
3ависимость
логарифма.
коэффицие}'та
диффуз|{и
0а
')
для
различвьтх
цовов
в
:{{идк|'х
1
1длаках
''
Ё
.
3:*атения
16 0:
"[
т,?]сел€38!
2_
кобальта;
3_
цикеля;
4
_
кремгти};
5
--|
вава_
д'1я}
-6_титава;
7_цирко_'
ния;
8
_
ниобия.
|[рямьте
],
'т
_
для
ал:о1|!ин8тного
тшлака;
1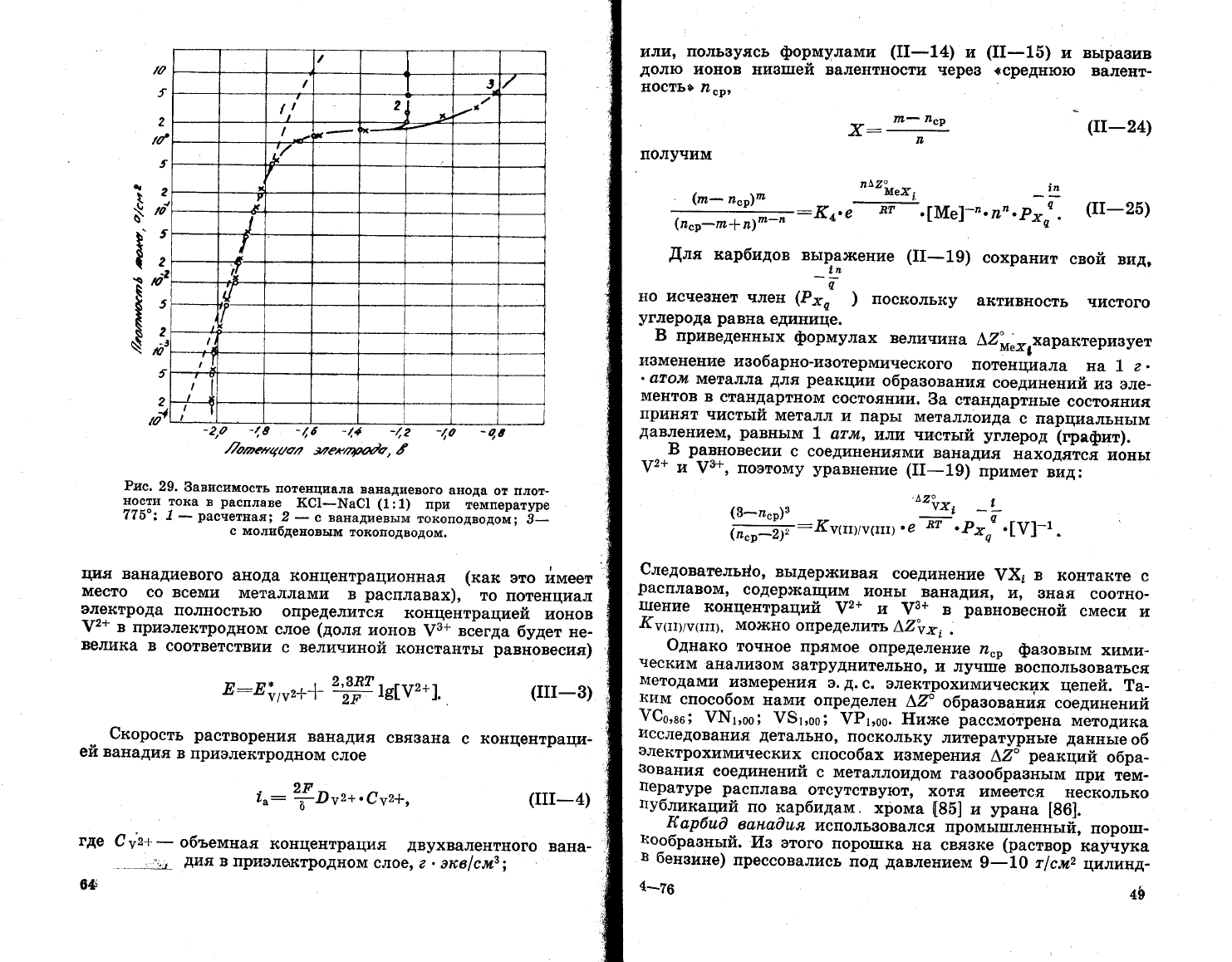
/0
,
2
Ё
,
2
-2,о
-/,8 -16
-14
$
$
/7о:тэенцоао
*тенф, /
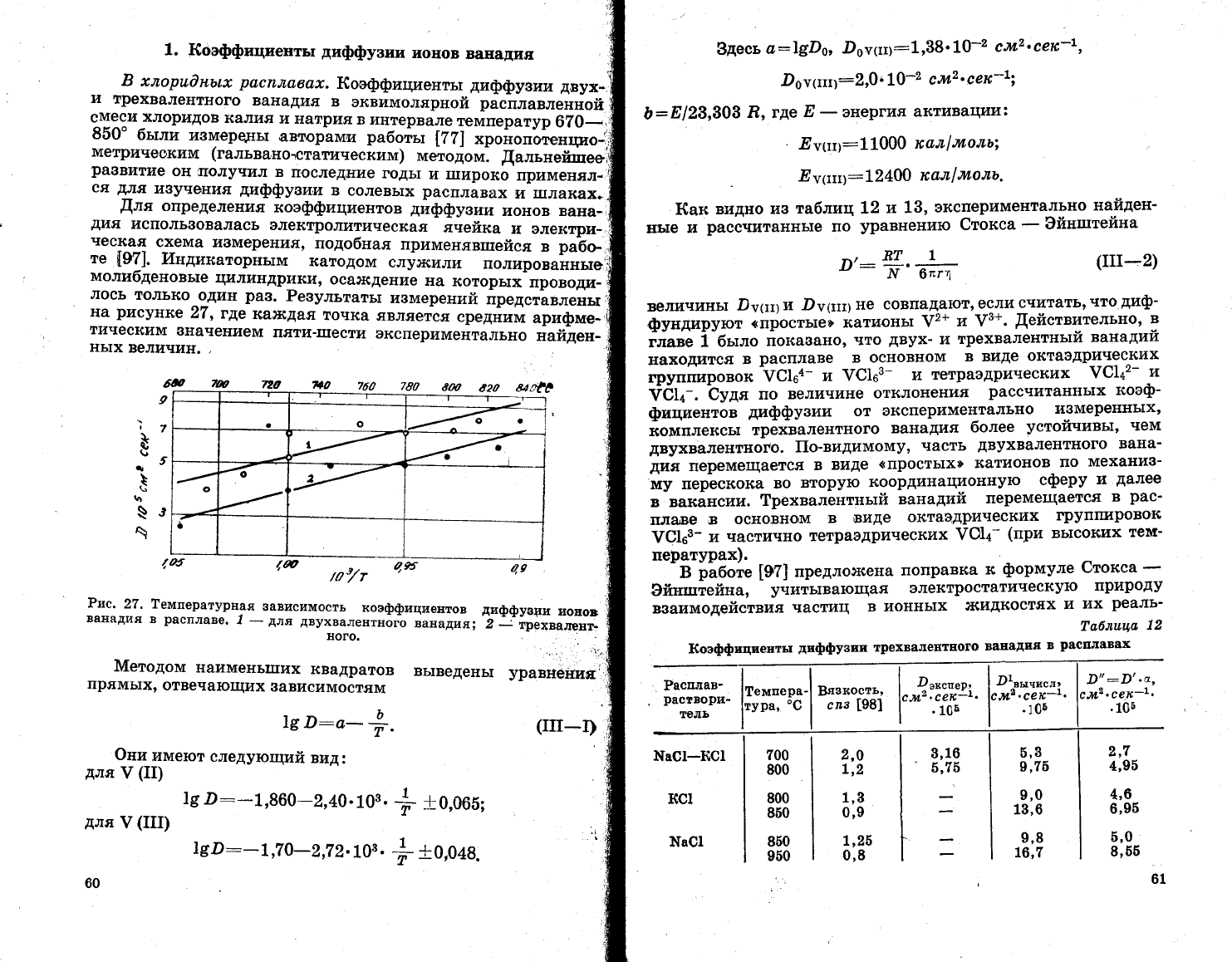
Рпс.
29.
3ависимость
потенциала
ванадиевого
а1|ода
от плот-
ности
то}{а
в
расплаве_
1(€1_}т1а€1 (1
:1) при
температуро
7 7 5"
з
7
_
,"""у;ъ;;
а;:#";#"."ъч*й
"'
лй' !'11
;
5
:-
ция
ванадиевого
анода
концентрационная
(как
это
й*""'
место
со всеми
металлами
в
расплавах),
то
потенциал
эл€ктрода
полностьк)
определится
концентрацией
ионов
\/2+
в
приэлектродном
слоё
(доля
ионов
\/3* всегда
буде1 не_
велика
в
соответств'ту|
е величиной
константь1
равновееия)
Б:0\рэ*+
'#
19[т:+1. (]11-3)
..
€корость
растворения
ванадия
свя3ана
с ко}{центраци;
ей ванадия
в
приэлектродном
слое
ц:2{ота+.(у2*,
(1тт_4)
где
6й+_
объемная
ко1тце1!трация
двухвалентного
вана-
::!|
дия
в приэлвк1родт{ом
слое'
?
,
экв|
ем3;
64.
или'
по]1ьзуясь
формулами
(11_14)
и
(11_15)
и
дол]о
ио|тов
низц:ей валент:лости
чере3
(средн1о1о
1{ость}
л}ср'
тп- п^6
х-
-'
п
получим
вь!рас}ив
валент-
(тт-24)
(тп-
п"р|п
(п"'-тп|п)п_п
"''\"*,
^у
:6
'.9-3-.[1т19]*'.
,".
'*!.
(1т-25)
.(ля
варбидов
вь1ра}|сение
(11_19)
сохранит
свой
вид'
-т
1{о исче3нет
нлен
(Р3,
)
поскольку
активность
чистого
угдерода
равна
единице.
3
приведе1{}ть1х
формулах
величина
[2*"*'хаоактеризует
измене}{ие
изобарно_ивотермического
потенциала
на
! а.
.
('том
металла
для
реакции
образования
соединений
из
эле-
!\{е1{тов
в
стандартпом
состоянцът.
3а
стандарт1{ь1е
состояния
принят
чистьтй
металл
и парь1
металлоида
с парциальнь1м
давлением'
равнь|м
\
огм,
!1лу|
ч'!стьтй
углерод
1графит).
__^
8
рарновесии
с соединениями
ванадия
находятся
ионь1
\2+
п
9а+, поэтому
уравнение
(11-19)'приме!
й*'-
(3-а"р)3
^'33
_'
(и$_Ёу(1|)/у(]]:)'еБ'Р*,''[,]_'.'
€ледовательЁо,
вьтдер)|сивая
соединение
\/8;
в
т{онтакте
с
расплавом'
содер'|сащим
ионь|
ванадия'
у['
з1{ая
соотпо-
]цение
концентраций
у2+
и
93+
в
равновесной
смеси
и
бу(тт);у(лт:),
мо}1сно
определить
А2уха
.
Фднако
точное
прямое
определение
7}ер
фазовьтм
хими_
ческим
ат1али3ом
3атруднительно'
и луч|ше
восполь3оваться
методами
измерения
э.
д.
с.
элект_рох]тмических
цепей.
1а-
ким
способом
нами
определен
А2"
о6равования
соединений
!€о,во;
9$:,оо]
98:,оо;
_!Р:,оо.
}!иэтсе
рассмотрена
методика
исследования
детально'
поскольку
литературньте
данныеоб
электрохимических_
спосо6ах
измерения
А,2'
реакций
обра_
зова}тия
соединений
с
металлоидом
газообрав'ь]м
при
тем_
пературе
расплава
отсутству1от'
хотя
и1утеется
несколько
публикаций
по
карбидам.
хрома
[35]
и
урана
[86].
Ёарбш0
вона0ша
использовался
промьтштленнь:*,
поро1|1_
|*ообразньтй.
|1в
этого
поро1|]к&
на
свявке
(раствор'кау'у*'.
в
бенвине)
прессовались
йод
давлением
о_]о т1с)сэ
цйл*тнд-
4-76
4ь

рические
1цтабики
диаметром
6
мм, которь1е
затем
спека-
лись в зась1пке
у13
са}ку|'
в
аттшосфере
аргона
в течение
4 ча-
сов при
температуре
800'.
|]о
окончании
операщии
(процес_
са)
поверхность
:птабиков
зачищалась.
'
Ёштрш0 вона0шя.
Ёоптпактньте
а}{одь1 состаБа
!1{:,оо
го_
товили
вьтдер:*ской
:штабиков,
спрессованць|х
под
давле_
ниетш
5-6
т|с:ш2 из
поро:шкообразного
электролитически
рафинированного
ва11аду\я
вэл'2,
в
атмосфере
а3ота
при
120о'в
течение
4 часов.
(улъфш0
вана0шя
!Бт,оо
получа.ли
синтезоу{
из
стехио-
метрических
кодичеств
поро1цкообразного
ванадия
марки
вэл-2
и серь1
в кору}{довь1х
тиглях'
по1цещеннь1х
в эвак}и';
рованнь1е
кварцевь1е
ампуль1'
при
температуре
горяней
зо;
ньт 1000-1300"
и
вь1дер}кке
48 часов.
|[родукт
представлял
со6ой
п0ристу1о'
но
достаточно
прочну1о
однороднук)
массу'
из
которой
вь1ре3ались
цилинд-
рические
образцьт.
Фосфш0 воно0шя !Р;,оо
готовили
синтезом
из
стехиоп{ет_
рических
количеств
поротпкообразного
ванадия
вэ]1-2
у[
красного
фосфора.
Банадпй
в корундовом
тигле
по1у1ещался
в один конец
эвакуированной
запаянной
кварцевой
ап{пу-
ль1'
красньтй
фосфор
-
в
другой.
Ампульт
вь[дерх{ивались
в печи в
течение
8 суток
(температура 3оньт синте3а
посте-'
пенно
повьт1шалась
от 600
до
1200',
температура
зонь]'
где
помещался
красньтй
фосфор,
-
200_450).
Ёомпактньте
образцьт
готовили
таким эке
образом'
как
и
из сульфида
ва_
надия.
9лектрод
из получент{ь1х
соединений'
прикрепленньтй
к:
молибденовому
токоотводу'
помещали
в один
из полуэле_
ментов }{-образной
кварцевой
ячейки
(рис.
26). 9лектродом
сравнения
слу)кил
хлорсеребряньтй
электрод.
3анадий
вводили
в электролит
анод1ть1мрастворениемметаллическо-
го
прут1{а. |[осле
этого
в
расплав
погруэ1{али
электрод
из
соедд.!не}{ия'
и
во вспомогательной
камере
температура
по-
вь1|шалась
до
90-130'.
1ем самь!м
в полуэле1ше1{те
создава_
лось определенное
парциальное
давление
паров
метал-
лоида'
расчет
которого
проводился
по справочнь1ш!
даннь1м
[58].
9асть
дихлорида
ванадия'
взаимодействуя
с
парами
металлоида' превращалась
в трихлор'1д
|1 соед|1нение
9)(
3с\/61:*_8
ц:2ц\|\з*цу
х
'
Реакция
дол'|сна
протекать
вплоть
до
образования
в
электролите
смеси хлоридов
со средней
вадент11ость1о'
удов-
летворяк)щей
уравненито
(11-25).
3она
вспомогательной
камерьт'
где
располо'1сена
лодоч_
50
Рттс.
26.
€.хема электролитической
ячейки
для
изучения
равновесия
;..дт:111-:'тд"1
с
расплавамуу.
7 _*'ар:!е'*"
1т-оораз"ЁЁ_*й**а;
.
_
раст|лав;
3_
молибденовь:й
катод;
4_графитоЁьтй
*окоот"од;
5
_
асбестовая-диафрагма1
6
-
"р;б;;'
из
вакуумной
резиньт;
7
-
у_чрцевая
пробка;
8
_-термостатирова1{ная
кайера;
р
]-
'оБ*."ц
""
х/*.;
10.7
термоп8рь1;
77
-!
металличесйий
блок;
12
_корпус
алектро_
пеяи;
13
_
крь1|шка
пеяи;
7,:!
_
т1агревательнь1е
элемевтьт;
-15
_
элек-
трод
сравце1{ия.
ка
с металлоидом'
дол'1с}{а
бь:ть
наиболее
холодной
во
всей
уста1{овке'
ли||1ь
при
таком
условии
температура
зоньт
бу-
дет
определять
давление
1шеталло|1да
в
системе.
€
этой
цельк)
все
переходньте
тру6ки
и
верхняя
чаеть
}1-образной
ячейки_обогревались
специальньтми
трубнать1ми
".й!"!*'*_
лями.
1[о
достиясении
состояния
равновесия
и3мерялась
€|
_
э.д.с.
цепи:
х' ух|уо12,
ус13,
(€1,
1ч|а€1(рдспл.)

пот6нциала
в
реакции
о6разования
соединения
из
э'!еме:т'
тов
по
следу:ощей
методике.
1. Рассчить1вался
окислительно_восстановительнь1и
т1о'
те1|циал эле1{трода
и3 соединения
от:|осительно
хлор:{ого
электрода
ф::
€:
*
8я:
г'{€ 82
_
э.
д.
с.
цепи
Ав(Ав@1,
1(€1,
$а€1(р0спл.)
||
кс1,
1{а61(рв",,л.)
|с|2,
о.
2.
|[о
величине
окислительно_восстановительного
потен-
циала
определялась
средняя
валентность
ванадия
в эле1ст_
ролите'
контактиру]ощем
с соединен!4ем
'[
металлоидом
-
\_х
1д--
@
'-1\,ъурз1)'0,239Р
2'3пт
'
(тт-2т'
1ср:3_х'
_
3.
Раесчить1вался
равновеснь:й
потенциал
металличе_
ского
ванадия
относительно
хдорного
электрода
через
кон'
центраци}о
двухвале11тнь]х
ионов
в полуэлементе
с
соед]''
нение1}1
ч2:Б\рэ++'#
1в*[!].
4. }1вменение
изобарного
потенциала
реакции
образова'
]{ия соединения
и3
элементов
в стандартнь1х
условиях
(при
парциальном
давдении
паров металлоида'
рав:{ош[
однойат'
мосфере) составит
\
2
, *:
п
",
Р.
(у'_р')'-''2,'''. Р
у
,
тс
ал
|
о.
отпол' ва}тадия.
(11-28)
Аля
азота
и серь]
4:2,
для
фосфора
-
4
[87]'
Ёайден'
1{ь1е
методом
наимень1цих
квадратов
зависимости
и8мене-
ния стандартного
изобарного
потенциала
от
температурь1
представленьт
во втором
ра3деле
1|астоящеи
главь|.
8
процессе
исследования
концентрация
ванадия
в
элект_
ролите
бьтла
пример1{о
одинаковая
_
013_0,б
вее.
%.
йвмерив
потенциал
электрода
ив соединений
при
одной
температуре'
но при
двух
различнь1х
конце}{трациях
вана'
д|тя'
в электролите'
п1о}1сно применять
для
расчета
Ё!'э41уз+
тетод
э.
д.
с. [од
раснетов
сохра:{яется'
ли]дть
в
уравнепиях'
ь2м.х,
--
Б2м"ха
('11_10),
(1т_11)
добавляется
чден
_
-*т_
тт
_ф?
82
2[2Ф51*1ф\/{*1
]
59Ф21*1,
ба
соответственно.
1ак
как температура
в
обоих
опь1тах
оди_
накова
и
мо''с|{о
задать
одинаковое
парциальное
давлепие
паров
металлоида'.Р
п;р]т
раснетё
Ар эти
величинь1
сокра_
щато|пся
((фрмула
(11_16).
8
этом
случае
(фрмула
ст1_]в:
принимает
вид
т#т*"э";ф:7{*,
(1т:-29),
а вь1ра}|сение
(11_19)
не
изменяется
по
той
ясе
причине'
что
и
(11_16).
Фднако
величинь1
(1_*)
в
случае
|^"Б"'""-
сия
электрол|1та
с
соеди}{е}1ием
}тамного
больш:е,
йем
при
равновесии
с металлом
(ср.
0,1_0,5
_
при
равновесии
электролита
с нитридом
!}.[:,оо
и
0,001_0роо#
с метал-
лом).
1}оатому
относителъная
оц:ибка
при
определен|7|1
х 1т
*(п_п*'т
2у"ц"-+
намного
мень|це.
11роще
всего
при
работе
по этой
методике
пользоваться
электродами
из
карбидов,
но кар6ид
3а\{ад'1я
недостаточно
термодинамически
щ)очен'
т1
ве
л!1чи-
ньт (1_л)
получа}отся
все
еще
очень
небойьш:ие.
4.
?ермодинамичес!сие
свойства
окислов
ванадия
в 1цлаках
3ападий
в
металлургических
]шлаках
мо'*сет
иметь
раа_
личнук)
степень
окисления.
1ак,
в
марте}1овских
1шлаках
он
}{аходится
преимуществен}|о
(на
87_90}9)
в
трехвалентном
соотоянии
[88].
1о
}$е
самое
относится
и
к йонвертор|ть1м
|цлакам.
|!ри
охлаясдении
ванадий
входит
в
соединение
ти-
па ванадиевой
:ппине
л!т
|1
л!4
1ппинелида.
3
кисль:х
|плаках'
контактиру}ощих
с чугуном
,[89],
ва_
надий
так'|се
трехвалентен.
Ёа йранице
}!{'е
с атмос6ерой
он
-мо'1сет
находиться
и в
6олее
окисленной
форме.
в
рйоо-
те
[90]
установлено'
что
если
1шлаки
находятся
в
ко}{такте
со
сплаЁами'
содерх{ащими
повы|]тенное
количество
вана_
дия'
то
в
1тих
преоблада:от
ионьт
92+. 11ри
пони'|сении
со-
дер'|сания
ват{адия
в
сплавах
в
|шлаках
воарастает
дол'я
трехвале||т}{ого
ванадия.
Бели
пренебрень
взаимодействием
окислов
ванадия
о
растворителем' то
ив термодинамических
да1{нь1х
{5в] для
окислов
ва}1адия
мо'{с:то
при6лизительно
рассчитать
тсон-
ст&нтьт
рав:{овесия
реакций
(снитая,
что
9Ф
и
!:Фз нахо_
дяфся
в |цлаке'
а ванадий-й
сплавах
в
услов1{о
''{идком
состоянии):

1
'4'
1€ Ё
_ж
+
13,9
|9|_48,5.
3!Ф:с*:*]/(ж)
]
2\/2Ф31д11,
[93*1с
1
'сь:
[,711з'
от'
|в Ё
:
'$_+,ьь1в?*16,1.
9зФзк*:*]/сэкт
3
3!Ф(алс:,
[т2+1з
1
[т3+1:
4у'
|в Ё
:
_1$ _
:.,ьт
1в?*6,1.
8 соответств!а||
е
ве]тичинами
констант
равновесия'
на-
пример при температуре 1500',
активности
ва|1адця. в
спла-
ве 0,01 и общем содер,жсании
ванадия
в 1шлаке в
виде
окис_
лов
окодо
1%
доля
ионов
92+
додэкна
составитт,
450|о' ионов
у3+
-
около 55о|о, ионов
!{+
около 10_8%
и 95+
около
|о_\2о|о. 8 контакте со сплавом, |А€ активность
ва11ад'1я
равна
0,1, при тех }ке
условиях
доля
!2+
составит 650/о,
у3+
-
около
350/о,9{+
-
10_90/о'
у5+
-
10_13%.
Б
реальньтх
1шлаках
окисль1 ванадия
взаи:шодейству1от
с
растворителеш|'
причем
для
!Ф
и
!:Фз
энергия
этого в3а-
имодействия
различна
у!' следовательно'
ра3линньт
коэффи-
циенть1
активности
Фсновной характер ни31цих окислов
ванадия проявля_
ется в
ряде
3аконо:шерностей,
наблтодав1шихся в
реальнь|х
]шлаках.
}{апритиер, обнаруэкено
|[91]'
что
количество
ва-
надия'
воестановленного и3
дош1енного
1цлака
углеродом
(коэффициент
распределения),
возрастает при
увеличении
основности
1цлака'
т. е.
в
более кисдь|х
1цлаках окисльт
!Ф
и
!:Фз связань1 прочнее.
€ледует
о'|сидать' что в кисль|х 1шлаках несколько
силь_
1{ее
взаимодействовать
с
растворитедем
дол'{сна
$Ф,
обла_
дак)щая
основнь|ми
свойствами
в
боль:шей
степени' чем
амфотерная \/эФз. |[оэтому в
равновесии
с
]\4еталлом здесь
будут
преобладатъ
ионьт
!2+.
ут.
^.
Батолин,
о. А.
Бсин, Б. А. Абраштов пь1тались
ко-
личественно
определить
константь]
равновесия
реакции
54
2у3++у:3!2+
в
расплавленнь|х
1цлаках'содер)*сашцах
40_
42о|о
ёаФ, 44-46о10 3|о2,
9-110|о
А1эФз, 0,30/9 [49Ф
1-
2о|о 3э9з, 1,б-20|о
окислов ва1{адия
(в
пересне1'!е на !эФь)
[$21.
[{амерялась
э.
д.
с. концентра|4](оннь1х
цепей:
Ре,
!/€аФ,
$!Ф:,
А1эФз, Б:Фз, !эФз/Ре, у
(39'50/0).
Ёонцентрация
ванадия в
сплавах
менялась от 0,54
до
330/о.
€сь:лаясь на
работу
п[90],
авторь1
предполо'{сили' что
на
электроде
ер!внения
потенциалопределятощей
является
реакция
у2++
2
е!\".
1огда
поте1{циал эдектрода сравненияопределяется
из
уравнения
ё",:Бао*
$1,!"-,
(ш-:30)
!А€ @эо
_
активность ионов $2+
в тшлаке;
а,о,_ активность
ва!1ад1!я в сплаве
электрода сравне-
ния.
Ёа электроде
из спдавов с
вь1соким
содер'1санием
вана_
дия
поте1{циалопределятощей
является та ,{се
реакция
и
Ё:Бэо
+
#'"1.
э.
д.
с. ячейки
мо'1сно представить
вьтраэтсенйем:
е:0_&етэ:#ь*#
=
'"{т"\
(11-32)
9кспЁриментальнь|е
значения э.
д.
с. совпада1от
с
вь1-
численнь|ми по этой
фор:шуле
в предполо,}|сении'
9тФ {19:ф
для
сплавов' содерэ|сащих
14-33'3%
!.
|!ри
невь1соких
концептрациях
ват{адия
в сплаве поте}!циалопределяющей
является
реакция
у3++3
е:у"
&:Бзо
*$т"},
(1т_31)
(11-33)
и
а
э.
д.
с.
ячейки
55

9кепериментальнь|е
8наче1{ия э.
д.
с. совпадатот
с
рас-
счита|{нь!ми
по
этой
формуле
для
сплавов'
содер'тсащих
ме_
нее
5
0/о
ванадия.
3 ц:лаках'
находящихся
в
равновесии
со
сплавами'
со_
дер}|сащимут
5_14о|о
!,
ионы
13+
и 92+ присутствук)т
в со_
поставимь1х
количествах.
}1а основа1{ии
экспериментальнь1х
даннь1х
бь:ла
оцене-
на
константа
равновесия
реакции
к:
*=
1*#;т;
:
!%{.
(11-35)
[(ак
у:*се
6ьтло
показано,
л{'*':.|й2
!еализ}ется
до
дйо)
>-о,148.
|1ри
этом
к.}г0:
.2\['3
($*"_$э)2
(11-36)
>1
ттли Ё}6,3
до
.$9-={0,55
-}[*,'=/{'.
3десь
к]у0:
!щ*ф-',
т. е.
-&{18.
{т1*37)
€ледователь11о' при
температуре
экспериметтта
1550"
18>к>6,8. Авторьт:[92]
за значение
константь: принимают
величину'
равнук)
10. 11одтверхсдается
предполо)1сение
о
более пронной
свя3и
!Ф,
тем
!эФз
в 1шлаке.
Фднако следует
учить|вать'
что это
значение найдено
исходя и3
равенства
активности ио}[ов
ват{адия
в 1|!лаке и
сплаве
ионнь1м и'
со-
ответственно' атомнь1м
долям'
и
пользоваться
в
расчетах
им ну'*сно
с
и3вестной
остороэтсность1о. Ёроме
того'
вь1ра'тсе-
чия
(11_36
и 37)
весьма приблихсеннь1.
Ёе исклточено' что
в 1|1лаках'
контактиру|ощих
со спла-
вами' где активность
ванадия очень ни8ка'
могут сущест-
вовать
ионь| и более
вьтсокой валентности.
}ерптодинамику
в3аимодействия
трехокиси
ванадия
о
}{селезисть1ми 1плакам!4 113учалт1 Р. А. }€арасев,
А. 1Ф. |{о-
ляков' А. с. €амарин
[90].
Ёайдена температурная
зависи-
мость
константь1
равновесия реакции
*гек*:*|у]+
2го]
:
+
РеФ.!2Ф31'"1,
|в к:\в|%9][с']':_
'#+
10,95.
56
67
8 последние
годьт
бьтло вьтполнено
несколько
и€€л€,(о.
ваний по определени1о
термодинамических
характеристи:с
пятиокиси
ванадия
в
1шлаках. }{оэффициет{ть[ активности
\/эФь
в |]|лаках
€аФ_!эФь
(20_800ь)
найденьх методом
э.
д.
с.
и
расчетом
по
диаграмме
состояния
{93]
19
1
т,о,
:
_
!,27
0 }\т
!''+1,005ш
3"'.
Расплавь:
€аФ-уэ@ь
характериэу|отся
заметнь]ми от'
рицатель1{ь1ми
отклонениями
от идеальности'
причем
ко_
э66ициент активности !:Фь
нахоАится
в пределах 0'т_
0,695
в исследованном
интервале
концентраций
пятиокиси
с минимумом
(0,432)
при 600/о.
3 том
,}'{е
интервале
кон-
центраций
теплота
растворения
изменяется
для
9:0ь
от
2'2
до
0,5
кюал|;полъ.
?ермогравиометрическим
метод'ом
изучена
[94]
термодт-
т1амика систем
!эФь-€аФ,
!:Фь-РБФ,
!:Фь-А1яФз,
$яФь:РзФь
\1
уэФь-€аФ_$|Фэ_А1:Фз .
]|'становлено'
что величина *
в
формуле
\/эФь*#,
!.
€.
нестехибметрич1{ость
пятиокиси
ванадия'
увеличивается
е
повь11шением
температурь1
и по}тиэ|сением
парциального
давления
кислорода
*
:
сопв!!.Ро],в.
Б
охлаэлсденнь1х
1шлаках обнару:тсена
\/Ф2 и
не ока3алось
\/:@з.
€равнивая
вь1численнь1е константьт
равновесия
реак-
ции
диссоциации
чистой и
растворенной
пятиокиси
вана-
А!\$>
авторь1
закл!очили'
что в системах
€аФ_!эФь
и
Рьо_ъо5 набл:одатотся
сильнь|е отрицательнь1е
отклоне-
ния
от идеальности
в
области ооставов'
отвеча1ощих
хими-
чес1{им
соединениям
€аФ.!:Фь
у1
2РБ@.9эФь.
}1спользуя метод измерения
9.
А.
@.:
мо'|сно
определить
так)|се
активностъ
ванадия
в
различнь1х
сплавах по
фор-
мулам
типа
(11_32)'
(]т_34).
1аким
путем
найдена актив-
1{ость
занадия
в сплавах Ре-!_€
[95]'
а
нами
6ь:ли
опре-
делень1
актив}{ости
ванадия в сплавах
Ре_!_Р.

8
заклточение
следует отметить'
что если
поведение
ва-
1|ад'1$'
в
расплавде}{нь1х
хлоридах
изучено
достаточно
пол_
1{о
и всесторонне'
то этого не.ль3я
ска3ать
о
расплавленнь1х
1шлаках.
Ёеобходимо проведение
систематических
исследо_
ваний,
направленнь1х в
основном
на
количественное
опре_
деление
констант
равновесия
1ие'*{ду
металлом
и его
ио}{а_
ми
всех
валентностей
и вьтяс}тение
влияния
природьт
1]]ла_
ка-растворителя
на
ати
велйчинь:.
глАвА
11т
кинштикА
элвктРохимичпского
окислвния
вАнАдия,
шго сплАвов
и совдинвнии
1!1ногочиеленнь1ми
работами
в области
кинетики
вь1со_
1сотемператур1{ь1х
эдектроднь1х
процессов
пока3ано'
что
токи обйена
достига1от
десятков
а1у[пер
на
квадратнь:й
сан_
тицдетр
и обь1чно
стад!1ей,
лиштитирутощей
макси1цаль11о
возмо'1сну1о
скорость
при
данной
температуре'
является
диффузия
исходнь1х
веществ
или
продуктов.
поэтому
пер-
воочеред1{ая
3адача
-
определен1!е
коэффициентов
диф_
фузии
ионов
ванаддя
разлинной
валентности
или комплек-
с}{ь1х
группировок'
в составе
которь1х
они
вь1ступа1от
кош!п-
лексообразователями.
@дним
и3
основнь|х
приемов'
приме}{яемь1х
для
ивучения
кинетики
а}{однь1х
про-
цессов'
так,)1се
является
измерение
ацодной
поляривации
и
вь]хода по
току
в
рааличт{ь1х
условиях.
3нание
величи|{
коэффициентов
диффузии'
зависимо-
стей
плотность
тока
_
потенциал
электрода'
пдотность
то_
ка
*
вь]ход
по
току'
наряду
с
даннь1ми фавового
аналиаа
продуктов
на электродах
и электролитов'
позволяет
прове_
сти од1{означное
количественное
сопоставление
ревудьтатов
эксперимента
с
теоретическими
моделями
электроднь1х
процессов.
3ьтбор
опти1у[альнь|х
параметров
промь1]цлен-
ного электроли3а
(плотность тока'
конце1{трация'
те1ипе-
ратура)
в значительной
мере
6азируется
}{а
таких
мо_
делях.
8 настоящей
главе
приведень|
э}ссперименталь1{ь1е
дан_
т{ь1е
и
рассмотре|{
механизм
анодного
растворения'метал-
лического
ванадця'
его
соединений
(у'с,
уш,
!Р,
\/$)'
не-
которь]х сплавов
и
окис1{о-угольньтх
анодов.
3начительное
внимание
уделено
так}|се
вь1яс}{ени1о
влияния
анодного
111лама'
проме'|(уточнь]х
соединений
и
материала
то}сопод_
вода
на
процесс
анодного
растворения.
59
1. }{оффпциенть[
диффузпи
иопов
в8надпя
3
хлорш0ных
р('сплаас.т.
$оаффициенть1
диффувии
двух-
и
трехвалентного
ванад].!я
в
эквимолярной
расплавлеттной
щ99и
хлоридов
калия
и натрия
в интервале
температур
670-
850'
бь:ли
ивмерф{ь1
авторами
рабоЁьт
{77]
хройо""'й"й';
мещ)ичеоким
(гальв&Ё@:€1&[Ё9еским)
методом.
[альней:пее
раввитие
он
]получил
в
последние
годьт
и 1широко
применял_
ся'
р\]!я'
изучо[1ия
диффузии
в солевь1х
расплавах
и 1''лаках.
,(ля
определе11ия
коэффициентов
дйффу3ии
ионов вана-]
д!4я
т1еполь3овалась
элекц)олитичес1{ая
ячейка
и элекц)и*,
ческая
с;(ема
и3мерения,
подобная
применяв1цейся
в
рабо_
те
[97}
}1ндикаторнь:м
катодом
слу'1сили
полированнь1о
молибденовь1е
цилиндрики'
оса}1сдение
на
которь1х
проводи-
лось
толь1со_один
раз.
Результатьт
измерений
йредставленьт
на
рисунке
27'тде
ка'|сдая
точка
является
средним
арифше*
тическим
3начением
пяти-|шести
экспериментально
найден-
нь1х
величин.
..
17
!
е
5
\
\3
\
6Ф
9
.о5
о
5.
о
-'
-
вцо?ё
4'
диффу3|!и
иовов
9
---:
тре:1валовт:
'}|
вь]ведень|
уравне}1ия
(111-0
(о
то3/т
4$
Ри'с.
27. 1емпературвая
зависимость
коэффицие,{тов
ванадия
в
расплаве.
7
_
для
двухвалентног1 ванадия;
ного.
1!1етодом
наимень111их
}свадратов
прямь1х'
отвеча1ощих
зависимостям
|в о:о_
}.
Фни
иметот
следутощий
вид:
для
9
(]1)
19
):-1,860-2,40.10,.
+
*0,065;
для
\/
(111)
19
|
:
-1,70-2,7
2.10,.
+
+
0,04в.
60
3десь
а:|909,
)9т1тт1:1138'
10_2
сл'2'
с€Ё_\,
Роу(|т|):2:0'
10-2
с'м2' еек_|1
0:$!23,808
Ё, где
8
_
эн9ргия
активации:
'
8у(:т):11000
тсол|':шолъ;
.
Бус:т:::12400
псал|]у'оль'
1!ав
видно
из таблиц
!2
ух \3,
эксцеримента',[ь1{о
найден_
}1ъте
и
рассчитаннь]е
по
уравнени1о
€токса
_
9йнш:тейна
6тгт]
(1т1-2)
о':#.
зеличиньт
!у(тт)
и
Ру(:тд)
не
совпадак)т'
е'сли
считать'что
диф-
фундиру:от
(прость1е)
катионь|
\2+
п $3+.
[ействительно'
в
Ёйаве !-б"'ло
йоказано,
что
двух_
и
трехвалентнь1й
занадий
находится
в
расплаве
в основном
в виде
октаэдрических
йу!й|'''',
ус1'*-
и ус163-
и
тетраадрических
9€1'э-
'
уёь-.
ёуд*
''о
величине
отклонения
рассчитан1{ьтх
коэф-
фициентов
диффузии
от
экспериментально
измереннь1х'
комплексь]
трехвалентного
ванадия
более
устойнивьт'
чем
двухвале11тного.
|!о-видимому'
часть
двухвалент}{ого
вана-
дия
перемещается
в
виде
(прость1х}
катионов
по
механиэ_
:шу перескока
во
втору1о
координацио}{ну1о
сферу
и
далее
в вакйнсии.
1рехвалентньтй
занадттй
перемещается
в
рас_
1ш1€!ве
в
основном
в
видо
октаадриче,ских
труп1тир'овок
9€1с3-
и частично
тетраэдрических
!б1+-
(при
вьтсоких
тем-
пературах).
'в
|_аоойе [97]
предлоясена
поправка
к
формуле
€токса
_
3йнтдтейца'
учить1ва1ощая
элекц)остатическу1о
природу
взаимодействия
частиц
в ионнь1х
){сидкостях
и
их
реаль-
|о6лшцо
12
Ёоэффпцпе:пть:
дпффувип
тр€хвалептвого
вавадпя
в
распл&вах
Расдлав-
рас!вори-
тель
}[а61__!{€1
ко|
}.]в€1
!**',","'|
3язкость,
|тгга,
"6
|
спз
|о81
700
800
8ш
8б0
850
950
2,о
\,2
1,8
0,9
\'2б
0,8
)"*.'"р,
эп2
.
с ек_|.
.
106
3,16
5,т 5
и
вь1ч!{сл'
]уь2
.
сек*\.
.
105
б'3
9,76
9,0
13,6
9,8
\в,7
|":0'
.а,
ль2
.
с е1с_|.
.106
2,7
4,95
4,6
6'9б
6,0
8,56
61
