Лесникова Н.П. Физическая химия. Самостоятельное решение задач по химической термодинамике, электрохимии и кинетике
Подождите немного. Документ загружается.

31
1.22. Вывести уравнение зависимости теплового эффекта от
температуры для реакции диссоциации карбоната кальция
гтв
СОСаОСаСО
тв 23
.
Определить количество теплоты, поглощенное при разложении 1 кг
карбоната кальция при 1000
0
С. Теплота диссоциации карбоната
кальция при 900
0
С равна 178,0 кДж/моль. Зависимость молярной те-
плоемкости веществ от температуры описывается уравнениями:
.1053,81004,914,44
,1095,61052,463,49
,1094,251092,215,104
253
253
253
2
3
ТТС
ТТС
ТТС
гР
Р
Р
СО
тв
СаО
твСаСО
Ответ: 1760 кДж.
1.23. Теплота испарения воды при 303 K равна 2427 кДж/кг, а
при 293 K теплота испарения равна 2452 кДж/кг. Определить сред-
нее значение молярной теплоемкости водяного пара в интервале
температур 293 ─ 303 K, если молярная теплоемкость жидкой воды
равна 75,31 Дж/(моль¶K). Сравнить полученное значение с таблич-
ным значением 33,56 Дж/(моль¶K).
Ответ: 30,31 Дж/(моль¶K).
1.24. Определить протекающей при 798 K и постоянном давле-
нии тепловой эффект реакции
.422
2
2
2
OHClOHCl
Все участники реакции – газы; теплоемкости всех веществ не зави-
сят от температуры.
Ответ: 117,1 кДж
1.25. Составить уравнение зависимости теплового эффекта ре-
акции от температуры (температурный ряд теплового эффекта) и
рассчитать тепловой эффект реакции при 500 Κ, если при стандарт-
ных условиях ДжН
r
164987
0
298
(все вещества газы), и
.42
2
2
2
4
НСООНСН
значения молярных теплоемкостей всех веществ (Дж/моль∙Κ) соот-
ветствуют уравнениям:
32
.10502,01026,328,27
;1054,81004,914,44
;1033,01071,1000,30
;1043,171066,7432,14
253
253
253
263
2
2
2
4
ТТС
ТТС
ТТС
ТТС
Н
СО
ОН
СН
Р
Р
Р
Р
Определить тепловой эффект реакции при 500 Κ, используя
точное уравнение Кирхгофа (1,25), а также с использованием спра-
вочных данных о средних значениях теплоемкостей в интервале
температур 273 − 500 Κ. Сравнить три полученных значения тепло-
вых эффектов реакции.
Ответ: ≈ 174 кДж.
1.26. Зависимость теплового эффекта реакции (Дж) от темпе-
ратуры выражается уравнением:
.1088,1010184,455,11185276
15230
32
TTTH
СaСОСОСаО
T
r
Молярные теплоемкости CaO и CO
2
выражаются уравнениями:
.1054,81004,914,44
;1053,61052,483,48
253
253
2
ТТС
ТТС
СО
СаО
Р
Р
Найти уравнение зависимости молярной теплоемкости СаСО
3
от температуры.
Ответ: .1094,251092,2152,104
253
3
ТТС
СаСО
Р
1.2. Второй закон термодинамики
Второй закон термодинамики устанавливает возможность, на-
правление и предел протекания самопроизвольных процессов.
Никакая совокупность процессов не может сводиться к
превращению теплоты в работу, тогда как превращение работы
в теплоту может быть единственным результатом процессов
(Томсон).
Для определения возможности, направления и предела проте-
кания самопроизвольных процессов часто используется метод
термодинамических функций: для каждых конкретных условий

33
существования термодинамической системы подбирается вполне
определенная термодинамическая функция так, что протеканию
самопроизвольного процесса соответствует изменение выбранной
функции в сторону увеличения или уменьшения, а при достижении
состояния равновесия – ее максимальное либо минимальное значе-
ние.
Самопроизвольный процесс может протекать лишь в сторону
достижения соответствующей термодинамической функцией экс-
тремального значения; при равновесии системы эта функция прини-
мает свое экстремальное значение.
Энтропия
В изолированной системе критерием самопроизвольного про-
текания процесса и достижения состояния равновесия является эн-
тропия (S).
В изолированных системах самопроизвольно могут протекать
только процессы, которые сопровождаются увеличением энтро-
пии. Это означает, что состояние устойчивого термодинамического
равновесия в изолированной системе отвечает максимуму энтропии:
dS >0; S → растет.
При переходе из состояния 1 в состояние 2 изменение энтро-
пии определяется соотношением
,
T
Q
dS
(1.28)
где знак равенства относится к обратимому процессу, а знак нера-
венства - к необратимому. Соотношение (1.28) является математи-
ческим выражением второго закона термодинамики.
Объединенные уравнения первого и второго законов термоди-
намики, пригодные для обратимых и необратимых процессов можно
записать в виде:
.WdSTdU
W
dU
dS
T
(1.29)
В связи с тем, что энтропия является функцией состояния сис-
темы, ее изменение при протекании как обратимого, так и необра-
тимого процесса одинаково. Поэтому, вычисляя изменение энтропии
для необратимого процесса, нужно мысленно заменить его одним
или несколькими последовательными обратимыми процессами, со-

34
хранив неизменными начальное и конечное состояния системы. Так
как только в случае обратимых процессов в выражении (1.28) стоит
знак равенства.
Изменение энтропии в сложном процессе равно сумме измене-
ний энтропии в отдельных стадиях процесса:
.
21 nобщ
SSSS
(1.30)
Абсолютное значение энтропии какого либо вещества при лю-
бой температуре можно рассчитать, если известна абсолютная вели-
чина энтропии S
1
при какой-либо одной температуре:
,
1
2
SSS
(1.31)
где значение S
1
– величина справочная и часто соответствует значе-
нию
0
298
S при стандартном давлении 1,013∙10
5
Па.
Изменение энтропии можно вычислить по следующим уравне-
ниям:
1. Для процессов фазовых превращений, совершающихся при
постоянной температуре
,
tr
tr
tr
T
Hп
S
(1.32)
где
trtr
TH,
- соответственно, теплота фазового перехода 1 моль
вещества и абсолютная температура фазового перехода; п – количе-
ство молей этого вещества.
2. Для процесса диффузии при смешении идеальных газов (P =
const, T = const, т.е. изобарно-изотермический процесс)
,lnln
2
2
1
1
V
V
n
V
V
nRS (1.33)
где п
1
, п
2
– число молей первого и второго газов; V
1
, V
2
- начальные
объемы обоих газов; V – конечный объем смеси газов (V = V
1
+ V
2
).
Если при тех же условиях смешиваются две порции одного и того
же газа, то никаких изменений в системе не происходит, ΔS = 0 (т.
е. уравнение 1.33 уже не применимо).
3. При изотермическом расширении идеального газа
.lnln
2
1
1
2
P
P
nR
V
V
RnS (1.34)
4. Нагревание вещества без изменения его агрегатного со-
стояния (простой нагрев).
Изобарный нагрев
:; TfCdTCdHQ
PPобр
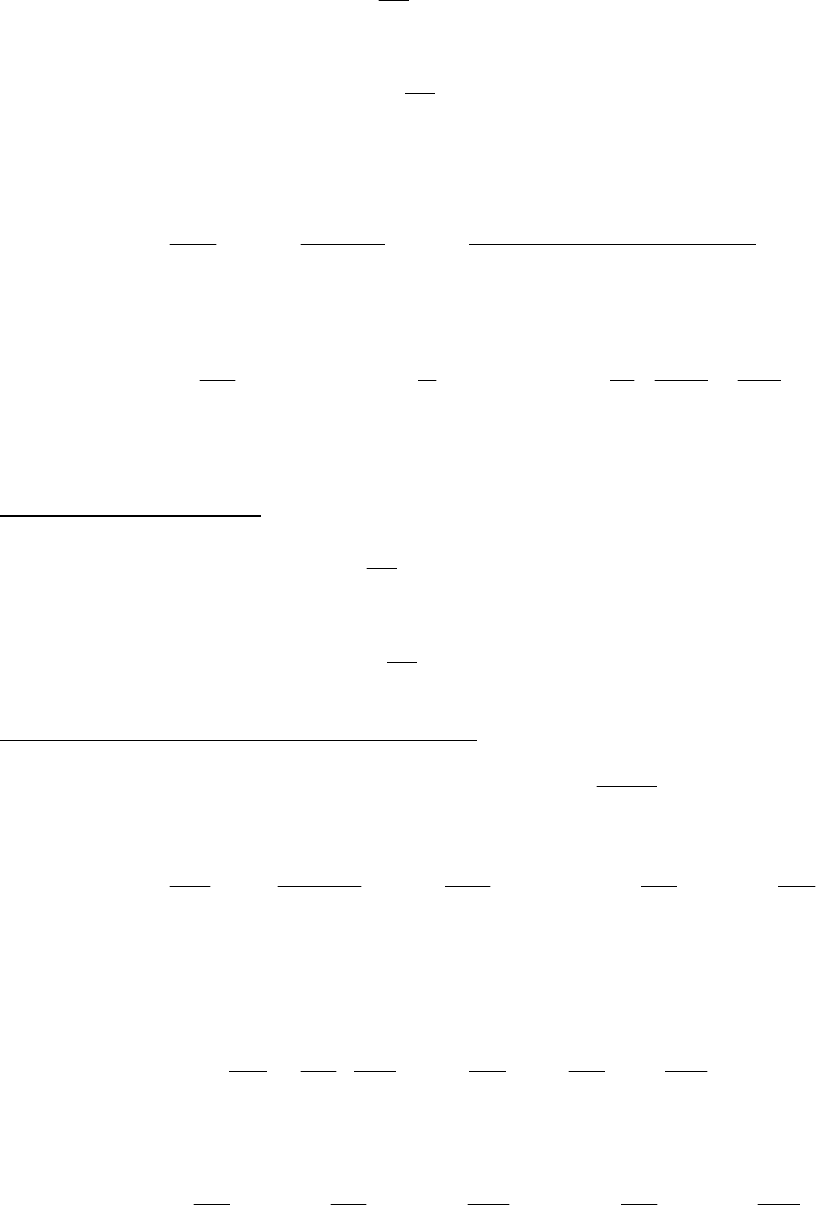
35
.ln
;1ln
1
2
1
2
веществамольпдля
T
T
CnS
веществамолядля
T
T
CS
P
P
(1.35)
Если
,..,
22
TccTbTaCетTfC
P
P
то
.
2
1
1
2
2
1
2
2
1
2
2
2
12
1
2
ln
,
2
1
22
2
1
2
1
T
T
c
TT
c
TTb
T
T
anS
dT
T
T
T
TccTbTa
n
T
T
T
dT
P
C
n
T
T
T
dH
nS
(1.36)
Изохорный нагрев :dTCdUQ
Vобр
.ln
;1ln
1
2
1
2
веществамольпдля
T
T
CnS
веществамолядля
T
T
CS
V
V
(1.37)
Любой процесс с идеальным газом - теплота процесса равна:
,dV
V
nRT
dTCpdVdUdHQ
Vобр
тогда
.
1
2
ln
1
2
ln
2
1
2
1
2
1
V
V
nR
T
T
V
CdV
T
T
V
V
TV
RT
n
T
dT
V
C
T
Q
S
(1.38)
Логарифм соотношения объемов можно выразить в виде:
.
2
1
ln
1
2
ln
1
2
ln,
2
1
1
2
1
2
p
p
T
T
V
V
p
p
T
T
V
V
Тогда, изменение энтропии равно:
.
2
1
ln
1
2
ln
2
1
ln
1
2
ln
1
2
ln
p
p
nR
T
T
P
C
p
p
nR
T
T
nR
T
T
V
CS
(1.39)
Это уравнение является универсальным, т.к. позволяет опреде-
лить изменение энтропии при различных условиях для n – молей
идеального газа:

36
.
1
2
ln
2
1
ln
,
1
2
ln,
1
2
ln
V
V
nR
p
p
nRSconstT
T
T
V
nCSconstV
T
T
P
nCSconstp
(1.40)
5. Сложный нагрев. При таком нагреве изменяется агрегатное
состояние вещества. Поэтому, данный процесс с помощью справоч-
ных данных следует разбить на ряд обратимых процессов. Учиты-
вая, что энтропия обладает свойством аддитивности, то после выра-
жения ее изменения для каждого обратимого процесса, определяет-
ся изменение энтропии в целом:
.
2
1
54321
T
к
T
T
dT
Р
С
К
Т
исп
H
Тк
T
T
dT
Р
С
пл
Т
пл
H
пл
T
T
T
dT
P
C
S
SSSSSS
г
пл
жтв
(1.41)
6. Химические реакции. Для реакции типа
аА + вВ = сС + дД
изменение энтропии можно представить следующими уравнениями:
,
00
,
0
исх
S
jпрi
S
i
S
r
(1.42)
.
298
0
298
298
,
0
,298
298
,
0
,298
298
,
0
,298
298
,
0
,298
0
,
0
,
0
,
0
,
0
T
T
dT
P
C
S
r
T
T
dT
BP
C
B
S
T
T
dT
AP
C
A
S
T
T
dT
DP
C
D
S
T
T
dT
CP
C
C
S
BT
S
AT
S
DT
S
CT
S
T
S
r
r
BA
DC
BADC
(1.43)
Окончательное решение данного уравнения определяется зако-
номерностями изменения теплоемкости от температуры:

37
.
298
11
2
298
2
298
298
ln
,..,
;
298
ln,
22
22
0
298
0
22
0
298
0
T
c
T
c
Tb
T
aSS
тогдаTccTbTaCетTfС
T
CSSтогдаTfC
rTr
PrРr
PrrTrPr
(1.44)
Пример 15. Нагревают 14 кг азота при 273 K и постоянном объ-
еме до тех пор, пока его температура не станет равной 373 K. Опре-
делить изменение энтропии в этом процессе, считая азот идеальным
газом. Зависимость теплоемкости азота при постоянном объеме от
температуры выражается уравнением:
./1027,456,19
3
мольДжTC
V
Решение. Изменение энтропии для изохорного процесса можно
определить по формуле (см. уравн.1.37 и 1.40):
.
2
1
T
T
V
dT
T
C
nS
Учитывая зависимость теплоемкости от температуры и грани-
цы интегрирования, получим:
./1026,32733731027,4
273
373
ln56,19
2
10
1027,456,19
28
1014
33
3
373
273
33
Дж
dT
T
T
S
Пример 16. Определить абсолютную энтропию 1 моля воды
при 473 K и 1.013¶10
5
Па, используя справочные данные. Считать
теплоемкость газообразной воды величиной постоянной и равной
34,4 Дж/(моль∙Κ).
Решение. Абсолютное значение энтропии можно определить
по уравнению 1.31:
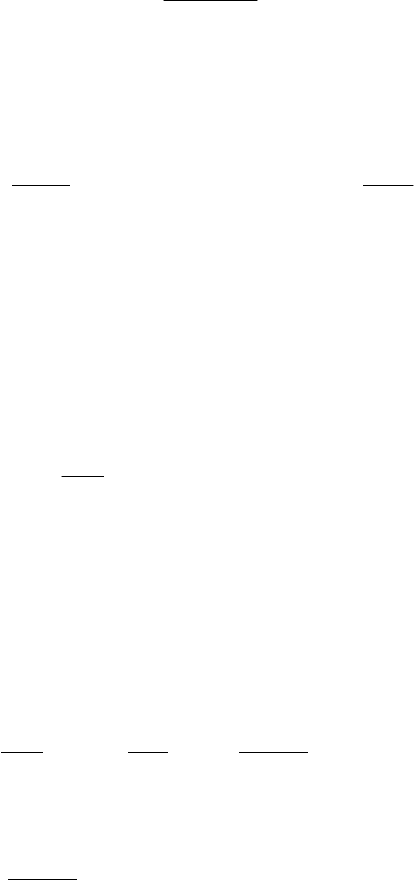
38
,
1
2
SSS
которое при указанных условиях задачи применимо в виде:
.
298
0
298
0
dT
T
C
nSS
T
газP
T
Из справочных данных [1] для воды в газообразном состоянии
,/74,188
0
298
мольДжS тогда
./63,204
298
473
ln4,3474,188
4,34
174,188
473
298
0
473
мольДж
dT
T
S
Пример 17. Определить зависимость энтропии от объема для
термодинамической системы, которая описывается уравнением со-
стояния (для одного моля):
TRbV
V
а
Р
2
.
Решение. Из объединенного уравнения первого и второго за-
конов термодинамики для обратимых процессов (см. уравн. 1.29)
можно выразить частные производные энтропии по различным тер-
модинамическим переменным. Зависимость энтропии от объема от-
вечает уравнению:
.
bV
R
T
P
V
S
V
T
После интегрирования данного равенства, получим:
,ln constbVRdV
b
V
R
S
V
где const зависит от температуры.
Пример 18. Определить изменение энтропии при превращении
2 г воды в пар при повышении температуры от 0 до 150
0
С и давле-
нии 1,013¶10
5
Па. Мольные теплоемкости воды равны:
./3,75
,/103,1113,30
3
мольДжС
мольДжТС
ж
пар
Р
Р
Скрытая удельная теплота парообразования воды Δ
исп
Η = 2,255
кДж/г. Температура кипения воды 100
0
С.

39
Решение. Данный необратимый процесс следует разбить на
следующие обратимые процессы: 1) нагревание жидкой воды от 0
до 100
0
С; 2) переход жидкой воды в пар (испарение) при 100
0
С; 3)
нагревание водяного пара от 100 до 150
0
С. Общее изменение энтро-
пии складывается из трех составляющих этих процессов.
1. Изменение энтропии для первой стадии определим по фор-
муле (1.35), с учетом, что мольная теплоемкость жидкой воды не за-
висит от температуры:
/61.2
273
373
ln3,75
18
2
1
1
ДжdT
Т
C
nS
исп
T
T
ж
Р
.
2. Изменение энтропии для второй стадии (испарение) опреде-
лим по уравнению 1.32 (учитывая размерность):
./09,12
373
10255,2
2
3
2
мольДж
Т
Н
nS
исп
исп
3. Изменение энтропии в третьей стадии находим по формуле
1.36:
./49.0
373423103.11
373
423
ln1.30
18
2
3
423
373
3
мольДж
dT
Т
C
nS
пар
P
О
бщее изменение энтропии составит:
./19.1549.009.1261.2
3
2
1
мольДжSSSS
Пример 19. Определить изменение энтропии при образовании
1 моля воздуха смешением азота и кислорода при 298 K. Воздух со-
стоит из 80% (объем.) азота и 20% (объем.) кислорода.
Решение. Процесс смешения газов является необратимым
процессом, для которого изменение энтропии соответствует нера-
венству 1.28. Известно, что если обратимый и необратимый процес-
сы проводятся в одних и тех же граничных условиях, то изменение
энтропии ΔS
обр
= ΔS
необр
.
Поэтому всякий необратимый процесс можно мысленно про-
вести обратимо в несколько стадий в тех же граничных условиях и
определить изменение энтропии для каждой обратимой стадии.
Сумма изменения энтропии этих стадий будет равна изменению эн-
тропии необратимого процесса.

40
В данной задаче общее изменение энтропии можно заменить
суммой изменения энтропий за счет расширения каждого газа по от-
дельности (уравнение 1.33):
.lnln
2
2
2
222
O
O
N
NON
V
V
n
V
V
nRSSS
Число молей и соответствующие объемы каждого газа находим из
условия, что 1 моль любого газа занимает объем 22,4 л. Тогда:
./19,4
48,4
58,22
ln2,0
1,18
58,22
ln8,031,8
.58,2248,41,18
.48,42,04,22,2,0
1,188,04,22,8,0
22
22
22
ДжS
лVVV
лVмольп
лVмольn
ON
OО
NN
Пример 20. Написать математическое выражение изменения
энтропии для рабочего тела, участвующего в каждом из следующих
процессов:
1) свободное расширение 1 моля идеального газа от объема V
1
объ-
ема V
2
; обратимое расширение 1 моля идеального газа при таких же
объемах;
2) обратимый изотермический фазовый переход;
3) обратимое адиабатическое расширение 1 моля идеального газа
от объема V
1
до объема V
2
.
Решение. Из уравнения второго закона термодинамики (1.28)
общее изменение энтропии можно представить равенством:
.
T
pdVdU
T
Q
dS
обр
обр
1) При свободном расширении, а также обратимом расширении
1 моля идеального газа
0
dU
, следовательно:
.ln,1,ln
,
1
2
1
2
2
1
V
V
RSмольn
V
V
nR
V
dV
nRS
V
dV
nR
T
dV
V
nRT
T
pdV
dS
V
V
2) При обратимом изотермическом фазовом переходе:
