Кондратьев В.Н., Никитин Е.Е. Кинетика и механизм газофазных реакций
Подождите немного. Документ загружается.

До
столкновения j Момент^столнно^
После столмнобения
%
1
it
II
А
1 1
1 1
- М \ ® ! —' —
i
с
1 'i
4
.,
I 1
i
I
срывнь/е
J
1
8
в
1
с
i
I
риношетные
^
0
р ! А В ! А
! ! ^ов ^
1 1
с
1 I 1
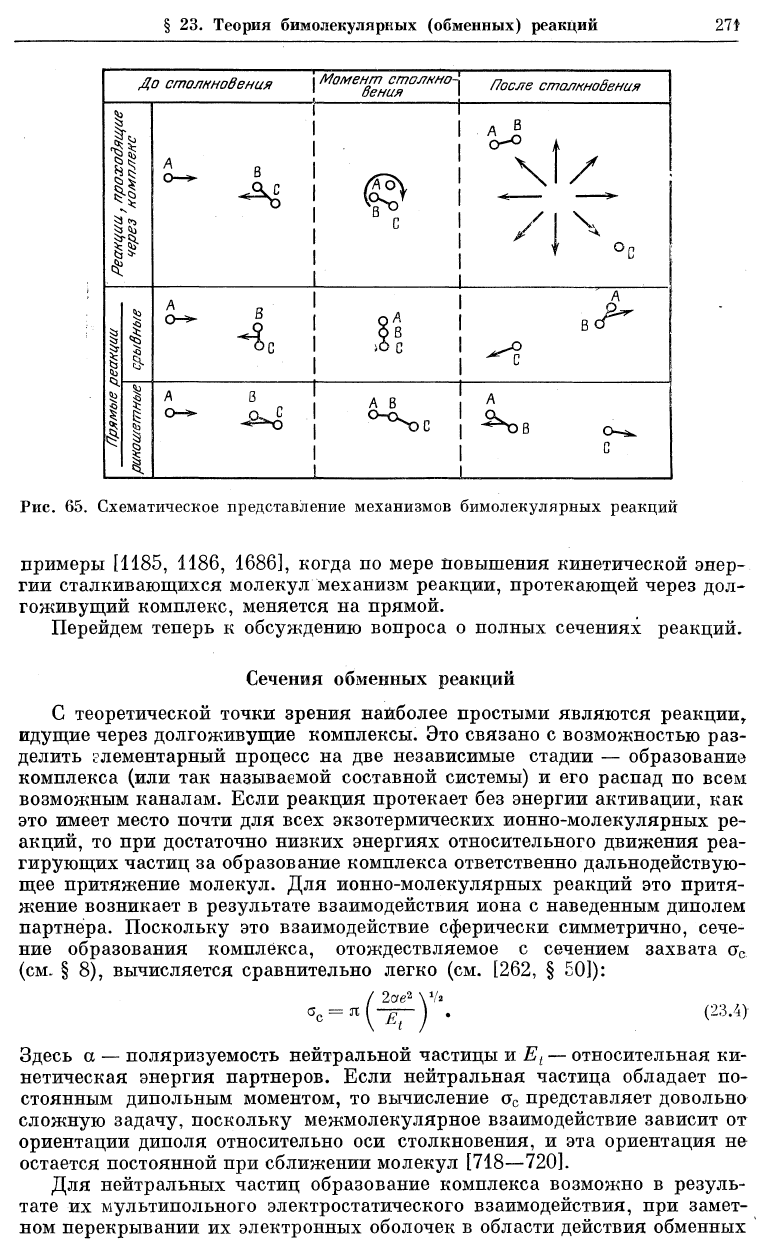
Рис. 65. Схематическое представление механизмов бимолекулярных реакций
примеры [1185, 1186, 1686], когда по мере повышения кинетической энер-
гии сталкивающихся молекул механизм реакции, протекающей через дол-
гоживущий комплекс, меняется на прямой.
Перейдем теперь к обсуждению вопроса о полных сечениях реакций.
Сечения обменных реакций
С теоретической точки зрения найболее простыми являются реакции,
идущие через долгоживущие комплексы. Это связано с возможностью раз-
делить элементарный процесс на две независимые стадии — образование
комплекса (или так называемой составной системы) и его распад по всем
возможным каналам. Если реакция протекает без энергии активации, как
это имеет место почти для всех экзотермических ионно-молекулярных ре-
акций, то при достаточно низких энергиях относительного движения реа-
гирующих частиц за образование комплекса ответственно дальнодействую-
щее притяжение молекул. Для ионно-молекулярных реакций это притя-
жение возникает в результате взаимодействия иона с наведенным диполем
партнера. Поскольку это взаимодействие сферически симметрично, сече-
ние образования комплекса, отождествляемое с сечением захвата о
с
(см. § 8), вычисляется сравнительно легко (см. [262, § 50]):
/
2ае
2
\Va
= ) • (23.4)
Здесь а — поляризуемость нейтральной частицы и E
t
— относительная ки-
нетическая энергия партнеров. Если нейтральная частица обладает по-
стоянным дипольным моментом, то вычисление а
с
представляет довольно
сложную задачу, поскольку межмолекулярное взаимодействие зависит от
ориентации диполя относительно оси столкновения, и эта ориентация не
остается постоянной при сближении молекул [718—720].
Для нейтральных частиц образование комплекса возможно в резуль-
тате их мультипольного электростатического взаимодействия, при замет-
ном перекрывании их электронных оболочек в области действия обменных

сил, либо же при образовании ионной пары, которая стабилизируется
переходом электрона с одной молекулы на другую. Если образование комп-
лекса сопряжено с преодолением потенциального барьера, то расчет обра-
зования составной системы требует детального знания той части поверхно-
сти потенциальной энергии, которая лежит на пути от исходных молекул
к комплексу. Одномерный профиль пути реакции такого типа показан на
рис. 26, б. Вершине потенциального барьера сопоставляется переходный
комплекс (активированное состояние), введение которого иногда облегча-
ет расчет сечения захвата. Потенциальной яме сопоставляется долгоживу-
щий комплекс, в котором происходит перераспределение энергии между
различными степенями свободы. Это перераспределение может быть опи-
сано движением изображающей точки только внутри многомерной потен-
циальной ямы, поэтому одномерная схема реакции является крайне услов-
ной.
После образования комплекса вероятности его распада могут быть рас-
считаны в рамках достаточно хорошо разработанной теории мономоле-
кулярных реакций, поскольку по существу долгоживущий комплекс ни-
чем не отличается от активной молекулы. Вероятность распада по некото-
рому каналу i определяется через константу скорости распада к
{
(Е) со-
отношением
Р.(Е) = К.(Е)1^К;(Е), (2.3.5)
j
где Е обозначает полную энергию комплекса, а величины к
{
(Е) вычисля-
ются по формулам § 19. Сечение реакции по каналу i выражается через се-
чение образования комплекса а
с
(E
t
) и вероятность распада Р
{
(Е) — фор-
мулой:
c
i
(E
v
E)=--e
c
(E
t
)P
i
(E).
(23.6)
Если в реакции (23.1) имеется всего два канала распада комплекса —
в направлении реакции (константа к
г
) и в обратном направлении (/с_
х
),
то выражение для сечения реакции принимает вид:
С(Е„ Е) =
0С(
Я,)
AL(£)
*;
(
F
L(
L) • (23.7)
Эта формула получена на основе упрощенных предположений, игно-
рирующих зависимость констант от полного углового момента комплекса.
При точных расчетах эта зависимость должна быть, конечно, учтена (см.
[262, § 31). Тем не менее, выражение (23.7) демонстрирует основную осо-
бенность реакций, протекающих через образование комплекса: сечение ре-
акции зависит только от относительной кинетической энергии E
t
и
полной энергии Е сталкивающихся молекул. Этот вывод доступен непо-
средственно экспериментальной проверке. Более того, неизменность сече-
ния при вариации распределения внутренней энергии партнеров (при неиз-
менном Е) является важнейшим аргументом в пользу статистического ха-
рактера распределения энергии.
Для экзотермических реакций, протекающих при энергиях, малых по
сравнению с теплотой реакции, энергия над порогом распада в экзотерми-
ческом направлении заметно превышает энергию распада в эндотермиче-
ском направлении. В этом случае к
г
(Е) ^> к.
г
(.Е), так что сечение реакции
в экзотермическом направлении просто совпадает с сечением образования
комплекса,
—
С
с• (23.8)

Для реакции в обратном направлении при той же полной энергии сечение
сг_! оказывается намного меньше сг
с
[262, § 31].
Примерами достаточно подробно экспериментально и теоретически ис-
следованных реакций, протекающих через образование долгоживущих
комплексов, могут служить процессы
R+ +
На
- н+ + Н
и
С+ + Da CQ+ + D,
первый из которых экзотермичен, второй — эндотермичен. Расчет сече-
ний первой реакции проводился в работах [260, 1684], второй — в работе
[1607].
Переходя к прямым реакциям, отметим, что реакции срыва допускают
более простую трактовку, чем рикошетные. В частности, для реакций сры-
ва А + ВС
—к
АВ -J- С было обнаружено, что переход атома В от молеку-
лы ВС к атому А почти не сопровождается отдачей, и поэтому скорость ато-
ма С до и после столкновения изменяется мало. Для таких реакций, иду-
щих по механизму «наблюдатель — срыв» (поскольку атом С фактически
является только наблюдателем, а не участником реакции), оказывается
возможным сравнительно просто вычислить угловое и энергетическое рас-
пределения продуктов и таким образом подвергнуть проверке основные
предположения о кинематике процесса.
Угловое распределение продуктов* характерное для срывных реакций,
может быть обусловлено взаимодействиями различных видов/ Для реак-
ции щелочных металлов М с молекулами галогенов Х
2
М. Полани еще в
1935 г. и Маги в 1940 г. (см. [498]) предложили модель реакции с переходом
электрона, позднее получившей название «модели гарпунирования» [372]:
при сближении М и Х
2
на некотором расстоянии происходит перескок
электрона, приводящий к образованию ионной пары М
+
— Х
2
. Затем
отрицательный ион Х
2
диссоциирует S поле положительного иона М
+
;
образующаяся при этом ионная пара М
+
Х~ представляет собой молекулу
MX : М + Х
2
->- М
+
+ Х
2
MX + X (подробности см. в работах [504,
1113]). Эта модель позволяет оценить порядок величины сечения реакции.
Переход электрона происходит на расстоянии Н
с
, которое соответствует
квазипересеченйю начальной ковалентной поверхности потенциальной
энергии с ионной поверхностью пары М — Х
2
(см. § 10). Условие квази-
пересечения записывается в виде равенства кулоновского притяжения ио-
• нов и разности потенциала ионизации /м атома М и электронного сродства
АХ
2
молекулы Х
2
: '
«
а
/Д
0
= /
м
-
А
х
2
- (23.9)
Полагая, что каждое образование ионной пары ведет к реакции, получим:
а=лЯ
2
с
. (23.10)
Таким образом, эта модель предсказывает независимость сечения реакции
от относительной энергии молекул и увеличение сечения при уменьшении
разности /м:
—
АХ
2
. ВычислениеR
c
из уравнения (23.9) показывает, что пере-
ход электрона происходит на расстоянии порядка 10 А. Вследствие боль-
ших значений R
c
столкновения с прицельным параметром превышающим
i?
c
, ведут только к упругому рассеянию молекул. Отсутствие каких-либо
неупругих процессов, конкурирующих с упругим рассеянием и реакцией,
позволяет оценивать сечение реакции по искажению дифференциального
сечения рассеяния. Именно при малых углах рассеяния, соответствующих
прицельным параметрам Ъ R
Ci
дифференциальное сечение упругого
18 В. Н. Кондратьев, Е. Е. Никитин

рассеяния следует классическому закону, справедливому для потенциала
взаимодействия U (R) = — C
e
/i?
6
(см. § 8) [372]:
При некотором значении угла Ф = ^ и Ъ — R
c
происходит резкое па-
дение интенсивности рассеяния, которое следует интерпретировать как
следствие начала реакции. Соответствующий этому значению угла при-
цельный параметр определяет сечение реакции обмена. Выраженное через
угол Фс сечение реакции равно [482]:
а = (^-С
6
)'
/а
(Я^сГ'Ч (23.12)
Измерение сечений гарпунных реакций подтверждает следствие, выте-
кающее из простой модели, об увеличении сечения при уменьшении потен-
циала ионизации атома щелочного металла (табл. 18). Эта модель предска-
Таблица 18
Корреляция сечений гарпунных реакций с потенциалами ионизации
атомов щелочных металлов (при E
t
= 0,12 эв) [482, 728]
Партнеры
I
M
, as o, A*
Партнеры
I
M
, эв
о, A*
К + J
2
4,32
125—140
Na+ J
2
5,138
97
Rb+ J
2
4,176
167
Na' + J
2
3,04
210
Cs+ J
2
3,87
180-195
зывает далее независимость сечения реакции от относительной кинетиче-
ской энергии молекул. Что касается внутреннего состояния молекулы
Х
2
, то оно может влиять на сечение реакции только вследствие зависимо-
сти электронного сродства Х
2
от начального колебательного состояния.
Для рикошетных: реакций сечение обычно существенным образом зави-
сит от энергии относительного движения и внутренних состояний реаги-
рующих партнеров. В настоящее время имеется большое число работ по
расчету сечений (или вероятностей) реакций такого типа. Основная цель
этих работ состоит в установлении корреляции сечения реакции с особен-
ностями поверхностей потенциальной энергии. Результаты таких расче-
тов, допускающие наиболее простую интерпретацию, относятся к реакции
Н + Н
2
->Н
2
+ Н,
поскольку поверхность потенциальной энергии этой реакции отличается
особенно простой структурой. Сечение реакции зависит от трех парамет-
ров — относительной кинетической энергии E
t
и начальных значений вра-
щательного (j) и колебательного (и) квантовых чисел молекулы Н
2
.
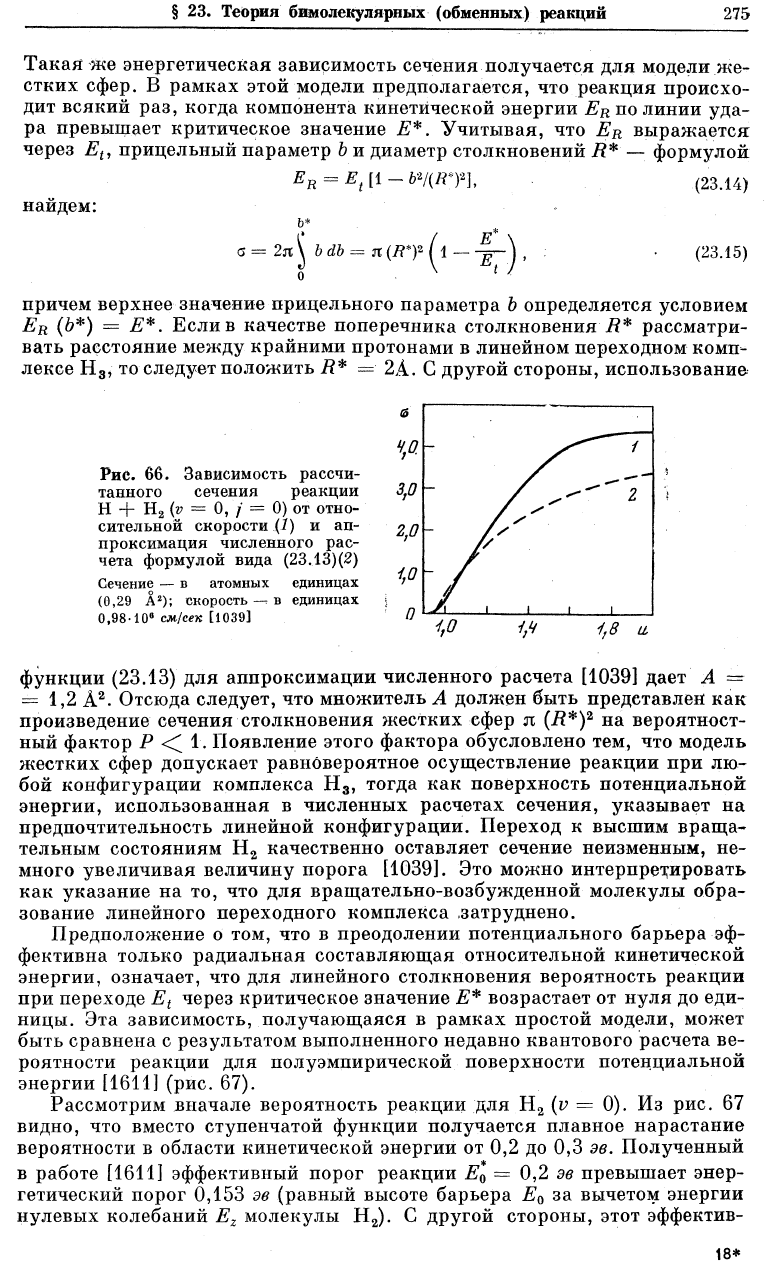
Квазиклассический численный расчет сечения реакции для основного
колебательного и вращательного состояния Н
2
дает монотонно-возрастаю-
щую функцию энергии E
t
от порога .Е*, величина которого меньше энергии
активации Еа, фигурирующей в методе переходного состояния (рис. 66,
кривая 1) [1039]. Если рассматривать Е* как некоторый эффективный
барьер, то приближенно сг может быть описано функцией (пунктир на
рис. 69, кривая 2):
в (E
v
/. = 0, у = 0) — Л (1 — EVE
t
),
(23
.13)
E*/E
t
< 1.
Такая же энергетическая зависимость сечения получается для модели же-
стких сфер. В рамках этой модели предполагается, что реакция происхо-
дит всякий раз, когда компонента кинетической энергии E
R
по линии уда-
ра превышает критическое значение Е*. Учитывая, что E
R
выражается
через Е
и
прицельный параметр
Ъ
и диаметр столкновений i?* — формулой
E
R
= Е. [1 - Ъ*/(1ГП
найдем:
ь*
' =
2л;
^
Ъ
db = я (i?*)
2
—
(23.14)
(23.15)
причем верхнее значение прицельного параметра
Ъ
определяется условием
ER (Ь*) = Е*. Если в качестве поперечника столкновения /?* рассматри-
вать расстояние между крайними протонами в линейном переходном комп-
лексе Н
3
, то следует положить i?* — 2А. С другой стороны, использование
Рис. 66. Зависимость рассчи-
танного сечения реакции
Н + Н
2
(v = 0, / = 0) от отно-
сительной скорости (1) и ап-
проксимация численного рас-
чета формулой вида (23.13)(2)
Сечение — в атомных единицах
(0,29 А
2
); скорость —г в единицах
0,98-10® см/сек [1039]
-f
}
8 LL
функции (23.13) для аппроксимации численного расчета [1039] дает А ~
= 1,2 А
2
. Отсюда следует, что множитель А должен быть представлен как
произведение сечения столкновения жестких сфер л (В*)
2
на вероятност-
ный фактор Р 1. Появление этого фактора обусловлено тем, что модель
жестких сфер допускает равновероятное осуществление реакции при лю-
бой конфигурации комплекса Н
3
, тогда как поверхность потенциальной
энергии, использованная в численных расчетах сечения, указывает на
предпочтительность линейной конфигурации. Переход к высшим враща-
тельным состояниям Н
2
качественно оставляет сечение неизменным, не-
много увеличивая величину порога [1039]. Это можно интерпретировать
как указание на то, что для вращательно-возбужденной молекулы обра-
зование линейного переходного комплекса .затруднено.
Предположение о том, что в преодолении потенциального барьера эф-
фективна только радиальная составляющая относительной кинетической
энергии, означает, что для линейного столкновения вероятность реакции
при переходе E
t
через критическое значение Е* возрастает от нуля до еди-
ницы. Эта зависимость, получающаяся в рамках простой модели, может
быть сравнена с результатом выполненного недавно квантового расчета ве-
роятности реакции для полуэмпирической поверхности потенциальной
энергии [1611] (рис. 67).
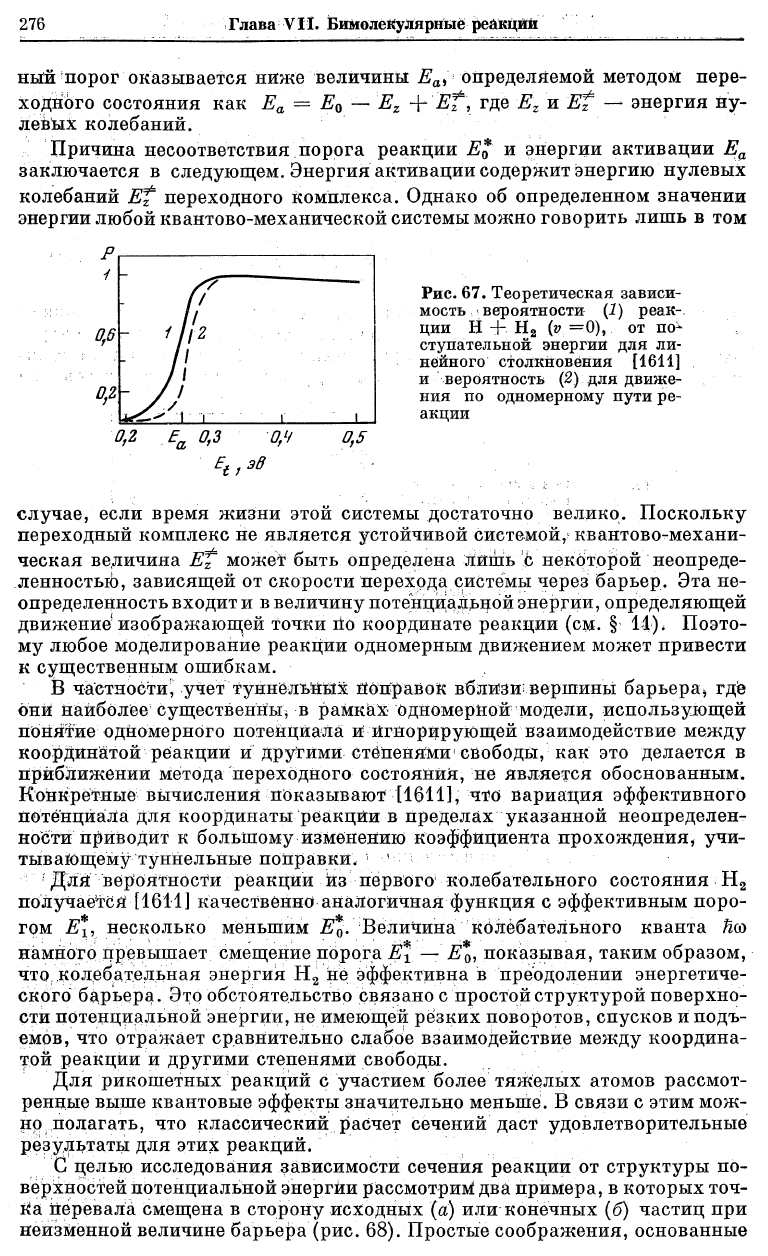
Рассмотрим вначале вероятность реакции для Н
2
(v = 0). Из рис. 67
видно, что вместо ступенчатой функции получается плавное нарастание
вероятности в области кинетической энергии от 0,2 до 0,3 эв. Полученный
в работе [1611] эффективный порог реакции Е
0
= 0,2 эв превышает энер-
гетический порог 0,153 эв (равный высоте барьера Е
0
за вычетом энергии
нулевых колебаний E
z
молекулы Н
2
). С другой стороны, этот эффектив-
ный порог оказывается ниже величины Е
аь
определяемой методом пере-
ходного состояния как Е
а
= Е
0
— E
z
+ Ef , где E
z
и Ef — энергия ну-
левых колебаний.
Причина несоответствия порога реакции Е* и энергии активации Е
а
заключается в следующем. Энергия активации содержит энергию нулевых
колебаний Ef переходного комплекса. Однако об определенном значении
энергии любой квантово-механической системы можно говорить лишь в том
Рис. 67. Теоретическая зависи-
мость вероятности (1) реак-
ции Н +. Н
2
(v —0), от по^
стунательной энергии для ли-
нейного столкновения [1611]
и вероятность (2) для движе-
ния по одномерному пути ре-
акции
случае, если время жизни этой системы достаточно велико. Поскольку
переходный комплекс не является устойчивой системой, квантово-механи-
ческая величина Ef может быть определена лишь с некоторой неопреде-
ленностью, зависящей от скорости перехода системы через барьер. Эта не-
определенность входит и в величину потенциальной энергии, определяющей
движение изображающей точки rio координате реакции (см. § 11)
<
Поэто-
му любое моделирование реакции одномерным движением может привести
к существенным ошибкам.
В частности
•
учет туннельных йоправок вблизи вершины барьера* гдё
они наиболее существенны* в рамках одномерной модели, использующей
понятие одномерного потенциала и Игнорирующей взаимодействие между
координатой реакции и другими степенями свободы, как это делается в
приближении метода переходного состояния, не является обоснованным.
Конкретные вычисления показывают [1611], что вариация эффективного
потенциала для координаты реакции в пределах указанной неопределен-
ности приводит к большому изменению коэффициента прохождения, учи-
тывающему туннельные поправки, >
г
Для вероятности реакции из первого колебательного состояния Н
2
получается [1611] качественно аналогичная функция с эффективным поро-
гом Е*, несколько меньшим 2?*. Величина колебательного кванта /гсо
намного превышает смещение порога Е\ — Е*
0г
показывая, таким образом,
что. колебательная энергия Н
2
не эффективна в преодолении энергетиче-
ского барьера. Это обстоятельство связано с простой структурой поверхно-
сти потенциальной энергии, не имеющей резких поворотов, спусков и подъ-
емов, что отражает сравнительно слабое взаимодействие между координа-
той реакции и другими степенями свободы.
Для рикошетных реакций с участием более тяжелых атомов рассмот-
ренные выше квантовые эффекты значительно меньше. В связи с этим мож-
но полагать, что классический расчет сечений даст удовлетворительные
результаты для этих реакций.
С целью исследования зависимости сечения реакции от структуры по-
верхностей потенциальной энергии рассмотрим два примера, в которых точ-
ка перевала смещена в сторону исходных (а) или конечных (б) частиц при
неизменной величине барьера (рис. 68). Простые соображения, основанные
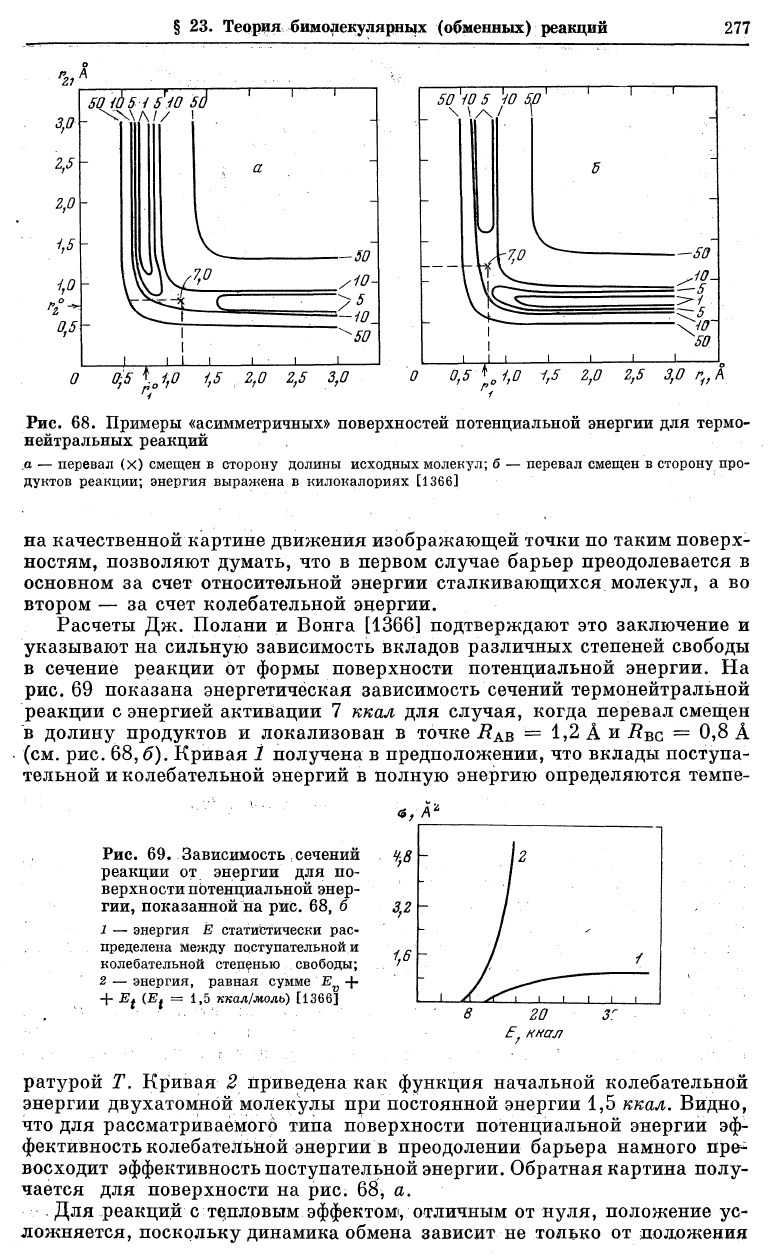
а — перевал (х) смещен в сторону долины исходных молекул; б — перевал смещен в сторону про-
дуктов реакции; энергия выражена в килокалориях [1366]
на качественной картине движения изображающей точки по таким поверх-
ностям, позволяют думать, что в первом случае барьер преодолевается в
основном за счет относительной энергии сталкивающихся молекул, а во
втором — за счет колебательной энергии.
Расчеты Дж. Полани и Вонга [1366] подтверждают это заключение и
указывают на сильную зависимость вкладов различных степеней свободы
в сечение реакции от формы поверхности потенциальной энергии. На
рис. 69 показана энергетическая зависимость сечений термонейтральной
реакции с энергией активации 7 ккал для случая, когда перевал смещен
в долину продуктов и локализован в точке i?
AB
= 1,2 А и с = 0,8 А
(см. рис. 68,б). Кривая 1 получена в предположении, что вклады поступа-
тельной и колебательной энергий в полную энергию определяются темпе-
G,
А*
Рис. 69, Зависимость сечений
реакции от энергии для по-
верхности потенциальной энер-
гии, показанной на рйс. 68, б
1 — энергия Е статистически рас-
пределена между поступательной и
колебательной степенью свободы;
2 — энергия, равная сумме E
v
+ E
f
(E
t
= 1,5 ккал/моль) [1366]
ратурой Т. Кривая 2 приведена как функция начальной колебательной
энергии двухатомной молекулы при постоянной энергии 1,5 ккал. Видно,
что для рассматриваемого типа поверхности потенциальной энергии эф-
фективность колебательной энергии в преодолении барьера намного пре-
восходит эффективность поступательной энергии. Обратная картина полу-
чается для поверхности на рис. 68, а.
. Для реакций с тедлрвым эффектом, отличным от нуля, положение ус-
ложняется, поскольку динамика обмена зависит не только от положения
и нал

барьера, но и от того, какая из долин соответствует более низкой энергии
[1063,1358а].
Исследование этого вопроса [1266, 1336, 1361] в рамках полуэмпири-
ческого метода показывает, что для экзотермических реакций при умень-
шении энергии активации барьер сдвигается в сторону исходных молекул.
Эта корреляция, совместно с ранее обсуждавшимся соотношением между
энергией активации и теплотой реакции (см. §11), устанавливает связь
между теплотой реакции и положением активационного барьера, позволяя,
таким образом, сделать некоторые качественные заключения о зависимо-
сти сечения реакции от поступательной и колебательной энергий молекул
в ряду однотипных реакций обмена. Именно для экзотермических реак-
ций наиболее эффективной в преодолении активационного барьера должна
быть поступательная энергия молекул, а для эндотермических — колеба-
тельная. Разумеется, в таком общем виде это утверждение справедливо
лишь качественно, и от него возможны отступления, обусловленные кон-
кретными особенностями динамики реакции.
Одна из таких особенностей, называемая аномалией легкого атома [970,
1109, 1362], состоит в том, что колебательная энергия молекулы BG в эн-
дотермической реакции обмена А+ ВС —AB-f- С не эффективна в прео-
долении потенциального барьера, если масса атома В намного меньше
массы атомов А и С. В результате сечение реакции оказывается сравни-
тельно слабо зависящим от колебательного состояния ВС.
Распределение энергии по степеням свободы
в продуктах реакции
Распределение энергии по степеням свободы продуктов реакции (23.1)
зависит от распределения энергии по степеням свободы реагирующих мо-
лекул и от деталей взаимодействия атомов в промежуточном комплексе.
Распределение энергии характеризуется функцией распределения по со-
стояниям возникающих молекул, пропорциональной скорости их образо-
вания в заданном состоянии. Соответствующая константа к
1ш
выражается
через сечение реакции c
i
j
}lm
(u) и начальные функции распределения
к
I т
= 2 lm(«) /а («а) /в (»в)
d
"A *U
B
. (23.16)
Здесь через г, j обозначена совокупность начальных квантовых чисел реа-
гирующих молекул; и — их относительная скорость, через I, т — сово-
купность квантовых чисел молекул — продуктов реакции. Современные
методы экспериментального исследования реакций позволяют во многих
случаях измерять функции распределения, и одна из задач теории состоит
в том, чтобы по известным функциям распределения получить информа-
цию относительно сечений реакций.
В общем случае по величине к
1т
нельзя восстановить сечение c
i
j
ylm
.
Однако для экзотермических реакций, в которых выделяющаяся энергия
намного превосходит среднюю энергию реагирующих молекул, можно ожи-
дать, что
К
Х
т
будет слабо зависеть от функций распределения ХА, ХВ, /А,
/
в
. Тогда без большой погрешности усреднение по начальным состояниям
можно опустить, заменяя квантовые числа Z, j и скорость и их наиболее
вероятными значениями jf, й. В этом случае (23.16) принимает вид:
к = (Z), (23.17)
1 ш
г
j,
I
т
ч
4
что позволяет выразить сечение реакции а
{
j
ilm
через функцию распределе-
ния возникающих молекул.

Поскольку сечения прямого и обратного процессов связаны соотношением
детального равновесия (8.38), выражение (23.17) может быть использовано
для вычисления сечения эндотермической реакции как функции кванто-
вых чисел Z, т при условии постоянства полной энергии. Таким образом,
может быть получена ценная информация относительно зависимости сече-
ний эндотермической реакции от энергии индивидуальных степеней сво-
боды реагирующих молекул. Такого рода расчет, выполненный для реак-
ции HF + Н = F + Н
А
— 34 7
ккал
[1365] и реакций НС1 + J HJ +
+ CI — 33,9 ккал и НС1 + С1 ->- Н + С1
2
— 48,6 ккал [413] на основании
экспериментальных функций распределения энергии по степеням свободы
в обратных реакциях, показывает, что сечение увеличивается на порядки,
если большая часть энергии является колебательной энергией исходных
молекул. Эти примеры подтверждают сделанный ранее вывод о том, что в
преодолении энергетического порога эндотермической реакции основную
роль играет колебательная энергия реагирующих молекул.
Теоретический расчет распределения энергии реакции по степеням сво-
боды молекул в общей постановке задачи сталкивается с теми же трудностя-
ми, что и расчет сечений. Исключение представляют лишь реакции, проте-
кающие через образование долгоживущих комплексов. В этом случае ста-
тистическая теория позволяет сравнительно просто получить функции рас-
пределения. Такого рода расчеты выполнены для ряда ионно-молекуляр-
ных реакций [809, 1271, 1685], а также для некоторых реакций, идущих с
участием нейтральных частиц [1153, 1609, 1610].
Для прямых реакций простые результаты можно получить лишь путем
значительного упрощения модели. Длясрывных реакций А + ВС-*- АВ +
+ С такое упрощение состоит в том, что атом С считается лишь «наблюда-
телем» процесса, и его скорость не меняется при переходе атома В к атому
А (см. выше). Такое предположение соответствует тому,что основной вклад
в сечение рассеяния дают малые углы (предельный случай рассеяния впе-
ред, характерного для реакций срыва). В этом случае закон сохранения
полного импульса однозначно определяет относительную кинетическую
энергию возникающих молекул, для которой оказывается справедливым
выражение:
bE
t
= E
t
-E
t
=-E
t
1
1
2 т
А
+ га
р
(23.18)
где E
t
и E
t
— энергия исходных частиц и продуктов реакции.
Отсюда на основании закона сохранения полной-энергии получаем
следующее выражение для полной внутренней энергии молекул — продук-
тов реакции:
AZ?
BH = (23.19)
Вопрос о распределении внутренней энергии по степеням свободы не может
быть решен в рамках этой простой модели.
Уточнение этой модели путем учета небольшого притяжения партне-
ров в начальном и конечном состояниях [940] приводит к появлению до-
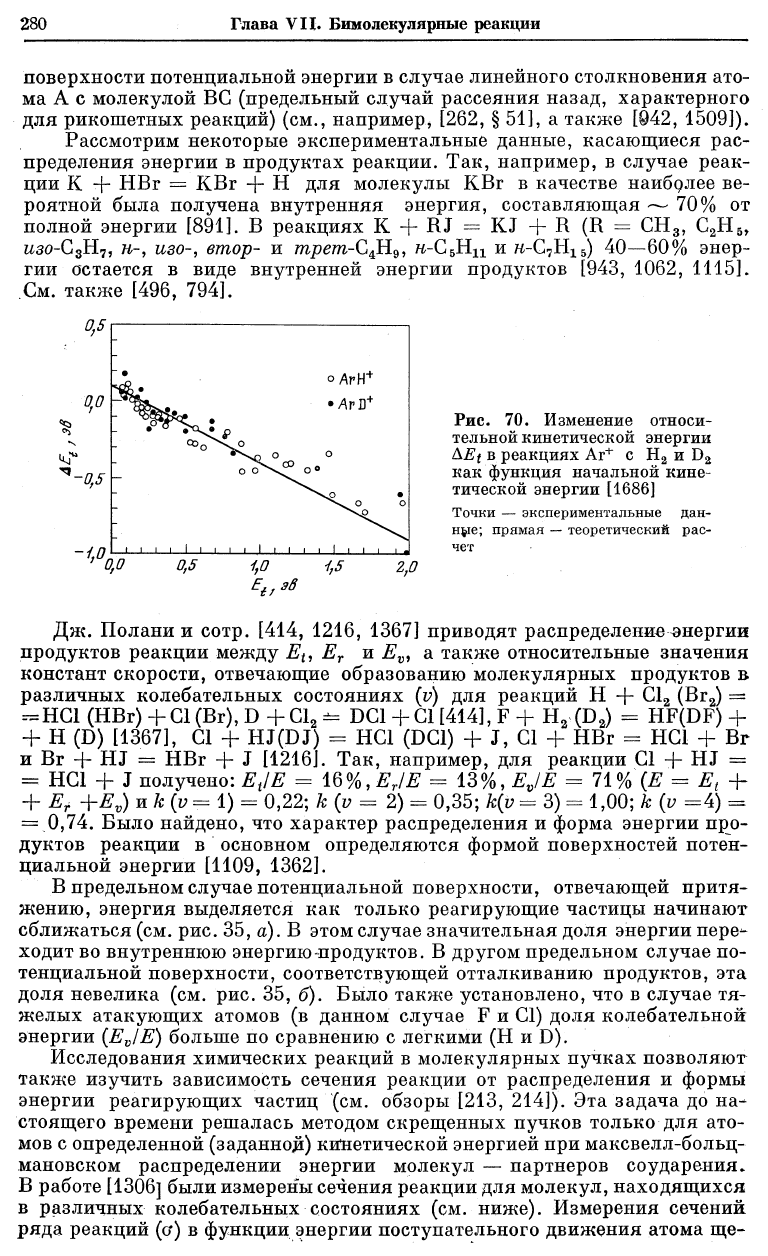
полнительного постоянного члена в правой части (23.19). Рисунок 70 ил-
люстрирует предсказываемую соотношением (23.18) линейную зависимость
AE
t
от E
t
для реакций
Ar+ + Н
2
—
АгН
+
+ Н,
Аг
+
+ — ArD+ + D.
Для рикошетных реакций некоторые представления о распределении
энергии можно получить при исследовании движения тяжелой точки по
поверхности потенциальной энергии в случае линеиного столкновения ато-
ма А с молекулой ВС (предельный случай рассеяния назад, характерного
для рикошетных реакций) (см., например, [262, § 51], а также [042, 1509]).
Рассмотрим некоторые экспериментальные данные, касающиеся рас-
пределения энергии в продуктах реакции. Так, например, в случае реак-
ции К + НВг = КВг + Н для молекулы КВг в качестве наибрлее ве-
роятной была получена внутренняя энергия, составляющая — 70% от
полной энергии [891]. В реакциях К + RJ = KJ + R (R = СН
3
, С
2
Н
5
,
изо-С
3
Н
7
, н-, изо-, втор- и mpem-CJI
9
, w-C
6
H
n
и и-С
7
Н
15
) 40—60% энер-
гии остается в виде внутренней энергии продуктов [943,1062,1115].
См. также [496, 794].
Рис. 70. Изменение относи-
тельной кинетической энергии
AEf в реакциях Аг
+
с Н
2
и D
2
как функция начальной кине-
тической энергии [1686]
Точки — экспериментальные дан-
ное; прямая — теоретический рас-
чет
Дж. Полани и сотр. [414, 1216, 1367] приводят распределение энергии
продуктов реакции между Е
и
Е
Т
и E
v%
а также относительные значения
констант скорости, отвечающие образованию молекулярных продуктов в
различных колебательных состояниях (v) для реакций Н + С1
2
(Вг
2
) =
=
НС1
(HBr)+Cl(Br),D +С1
2
±= DC1 + C1[414],F+H
2
(D
2
) = HF(DF)+
+ Н (D) [1367], CI + HJ(DJ) = HC1 (DC1) + J, CI + НВг = HC1 + Br
и Br + HJ = HBr + J [1216]. Так, например, для реакции CI + HJ =
= HC1 + J получено: EJE = 16%,E
r
/E = 13%, EJE = 71%(E = E
t
+
+ E+ +E
V
) и к (v = 1) = 0,22; к (и = 2) = 0,35; k(v = 3) = 1,00; к (и =4) =
= 0,74. Было найдено, что характер распределения и форма энергии про-
дуктов реакции в основном определяются формой поверхностей потен-
циальной энергии [1109, 1362].
В предельном случае потенциальной поверхности, отвечающей притя-
жению, энергия выделяется как только реагирующие частицы начинают
сближаться (см. рис. 35, а). В этом случае значительная доля энергии пере-
ходит во внутреннюю энергию-продуктов. В другом предельном случае по-
тенциальной поверхности, соответствующей отталкиванию продуктов, эта
доля невелика (см. рис. 35, б). Было также установлено, что в случае тя-
желых атакующих атомов (в данном случае F и С1) доля колебательной
энергии (E
v
/E) больше по сравнению с легкими (Н и D).
Исследования химических реакций в молекулярных пучках позволяют
также изучить зависимость сечения реакции от распределения и формы
энергии реагирующих частиц (см. обзоры [213, 214]). Эта задача до на-
стоящего времени решалась методом скрещенных пучков только для ато-
мов с определенной (заданнод) кинетической энергией при максвелл-больц-
мановском распределении энергии молекул — партнеров соударения.
В работе [1306] были измерены сечения реакции для молекул, находящихся
в различных колебательных состояниях (см. ниже). Измерения сечений
ряда реакций (а) в функции энергии поступательного движения атома ще-
