Каплан Г.Е., Силина Г.Ф., Остроушко Ю.И. Электролиз в металлургии редких металлов
Подождите немного. Документ загружается.


238
3лектролц3
с
пол!ценце1,''
льталлов
в
твероом
состоянцц
анода
применяли
трубку
из
с;пектрально
чисто'го
угля'
катодом
слух{и{3
пр,оволока
и]3
металличеокого
тория.
в
:{ачеетБе
конт_
!Фльн:ой
]цеп'и
соа'в:н'ени|я
прим'е}гял'и
ра'спла!влен'ную'си'стему
А9/А9€!,
(€1,
}',|а€||€12.
к;йй";.,"
*у*'ла
проволока
из
чистого
сор-ебра.
Анод
приготовляли
из
спектрально
чистого
цаф_ита.
Ёи>ке
приводятся
результать|
'измерения
э.
д.
с.
цеп}?
ть'ктьг5,
}.{а€1,
кё:/с:, ,р"''"й,Бр''ур.
743
4-3'€
в
;;;;-
мости
о'т величиньт
молярной
доли
(т!гь:
'
}{олярная
доля
ктьР5
.
.
.
9,!9045
0,00179
0,00623
0.008в6
3'д.с.,в
.
.....
.э',тоэ_
''']б5-
,',6;0'";:Ё#.
Беличиньт
э.д.
с.
шепи
1|/ктьР5,
5г€12,
\а€1/€12
п!и
темпе-
ратуре
747
-|
3'
€
в
зависимости
от
содерйа""!
к1йг,',р',.д.-
нь!
ни)ке:
€одержание
ктьР6,
|6
(вес.)
0,8
2
4
э.
д.
с.,
в
. .
.
2,49
2,47
2,47
этих
системах
имеет
меет,о
перена-
'образом
за
счет
аноднь1х
пРо(ессов
ре3ультате лиффузион1{ого
перена-
Авторь:
считают'
что
в
пря)кение'
:вер
оятно',главнь1'м
:.т
частично
мох(ет
бьтть
в
прях{ения
у
катода.
,&1инц,
!д;фдльски1
ц
лР.
{130,
131]
предло>кили
чието
фторил_
}у^1^::""{
с повьтгпенной
температурой
электро'".^
?:1оо3
с:.
чоста.в
эл'екпо'ол'и'та' ,следующий:
72,|,
тьг4,
5,6%
7пРэ,
22.4о|о
€аРэ.
3йектроли3
.
про,водили
в
атмосфере
аргона
с гра-
фитовым
анодо.м
и'
молибде"""й
_,
'тодом''
Ёр1йЁ{й!йющи,!'
:99'й
}Р}ток,
вРащающийся
со
.*.ро.",ю
150
об/мин,
при
катодной
пло,тнос.ти
то'ка
-
6,5
а|
см2.
'й',
й.'д.
"!"1д"'"'.,
с1плав
тория
и
ц|1нка' при
;переплавке
^кото-рого
(12066)
цин;с
испа'рялся (темпеоатура
кипенйя
ц"".!
эо/с)._бс;;;;;
со4еР-
>кал
94.4о|9
ть,
2,]о|о
Ё.
.
А[?с'й,/'ц""*'.
1!роцесс
получения
тория
электролизом
хлоридно-фторил_
|{ьтх
электролитов
с )кидким
цинк0вь]м,катод0м
изунали
€мирнос;
и-14вановский
[101].
Авторь:
,рй.''Б'''и
в
лабораторнь|х
усло-
виях
сплав
тория
с
цинком^путем
электроли3а
расп!та,вленного
эле.ктролита'
содерх{ашего
30о/. (вос.)
фтор'л'
йрй!
!_'*,'',_
лекулярной
сме,си
хлоридов
калия
й йат$ия.
сплав
-'..р*'',
окол,о
15%
('вес.)
1}:.
торщ
,обладает
ограниненной
раство,римостью
в
)кидком'
}1119.
пр"
тем'пературе
3атвердеванЁя
ц*,й'
?11э.-с1,р'.','-
ри.мость
'тория
в
нем
линтох<но
мала'
а при
температуре
к",е"',,
(907"с)
дости,гает
1,5%
(веФ|Б.
йь;
нась|щении
х<идкой
фазьт
вь1падает
твердое
интерметалли,ческое'соедине'ние
т,ь'7п'''
та-
ким
образо'м'
в
интервале
темпера}Р
+:э-эб7;ё;";';;;
тория
с
цин.ком'
содер)кащие
вьтше
1,50/9 (Бес.)
1[:,
прелста"'".!
собо{:
цвухфазную
систему.
|]озднее''"'''й,"у'
рй'"у
',уб'"*о'али
@гава
и
лр.
[132].
5'"*"щлй';;";;й''а
расплавленная
смес!}
].{а€1
_
кс1
-тис1ц.
3лектролиз
проводили
в
гра'фитовом
тигле,
кото'рый
одно'временно
являлся
анодом'
в
качестве
катода при-
меняли
1расплавленньтй
цин,к'
1емпература
электроли3а'соста.в_
.пяла 8о0"
с.
(огда
оодерйкание
тория в
цинке_
достигало
15-200|о
(вес.),
1катод становил'ся
тест'ообразньтм.
|!о'сле
этого
катод
вь1в'одили
и3
ваннь1
и
цинк
отгоняли
в вакууме
при
1!Ф'€;
остаток
представлял
собой
губватый
металлический
торий'
|7 о л
ц
н е
н
ш е
т о
р
ш
я
*':::-1'':"";у
:
:
ф'
?,
ш0
н о
-
о к
с
ш0
н ь
с
х
Ёекоторьтй
интерес
представляет
работа
/!1ейера
[|33]
по
по-
лучению
тория элейролйзом
фторидно'оксидной
утлут
хлоридно_
ойсидн,ой
ванн,
так
как
приготовление
окиси
то'рия весьма
про_
сто.
Автор
вьтбрал
эл0ктролитияескоё,
а
не металлотер'миче'ское
восстановлениеокиситория'вовя3истем'что.процеесэлектро-
ли3алегко'организоватьв'непрерь1'в'номвариан,те'атак)кепото.
п,|у''что
при
металлотермичееких
методах
во'сста1{овления
окиси
тория
получается
весьма
тон{<о
диспер'сный
металл
с
размером
ча'стиц'около
7-8
мк'
3лектролиз
про'водили
в
графитовом
тигле
,вьтсотой
45
см'
диаметром
7,5
сй с
толщиной
стенки
|,2
ом, слу}кив1шем
:о.[,нов!е'
менно
ано,дом.
Банну
помещали
в
,(Ам€Р},
в
которой
подАеРж4'
Ё''й
,'"'.феру
гели1
(99%
).
}(атод
изготовляли
из
6-мм
молиб_
ден,овогопрутка;вотдельнь1х.опь1.тахисг1ь1ть1валикатодь1и.]
та,нтала
14
т|1та]11а.
Бьтли
изучень1
электролить[
следующего',
со_
става.
1.
Фторидно-оксидная
ванна,
содерх(ащая
-расплавленнь1и
двойной
61орил
то,рия
|1||,<алия
[70?о
(вес')
тьг4] 'с
доба'влением
окиси
тори"._
Ёерастворимьтй
в
воде
двойной
фторил
тория
'||
кал|||я
г0то'види
добавлелп'у'е:м
избьттка
фторила
ка|л|\я
к
рас-
тв0ру
н;и'т!8,т8
т0рия'
тор'ий
Ф:€!1}{А?.,1€[
п}8(т[|1!081{[{
'пол|ностью.
Рас1:ворийоеть
окиси
тория
в
расплаве
составила
1примерно
1
%
(:вес.).
'-2.
!,лорилно-оксидная
ванна'
содер)кащая
распла'вленную
смесь
хлоридов
натрия
у| калия
с
добавлением
окиси
тория'
Б этом
слунае
определ,еннь1х
да'ннь1х
о
растворимости
оки,си
то_
рия
в
расг1лавленн,ой
смеси
получено
не
бьтло'
'
3лектролит
напревали
в течение
2_3
час'
до
дости|>кения
ну>кной
темг1ературы
и
затем
'катод
попру)кали'в
расплав'
Аля
фторилно-6ксидной
ваннь! температу_ра
электроли,за'со'ставляла
|оо0"
ё,
для
хлоридно-оксидной
800"
€.
||лотность
тока
и3менял}!
от 0,35
до
3,8
а,|см2,3а}1етного
влия|1'|я
и3менения
плотност1',1
тока
на
о,сно|внь1е
показатели
лроцесса
не
устано'влен'о'
||осле
окончания
электролиза
катод
с
осадком
помещали
в
камеру над
ва'нной
для
охла}кдения
и
процесс
возо6новлялтц

24о
металлов
в
м
состоян!'ц
с новьтм
катодом.
1(атодньтй
;п'родукт'
полуненный
из
,фторидно_
оксидно'й
ваннь1'
обра6ать:вали
-
слелую]щим
образой:
снять:й
с о|хлах(ден!|0го
катода
продукт
измельчали,
п'ро'сеивали
чере3
сито и'вь|щелачивали
водой.
||осле
измельчени
я 20-40оБ
осадка
проходило
чере3
,сито
0,074
мм,3ту
фракшию,
содерх(айую
от 5
до
14%
,тория'
далее
не о'бра,бать:в_ал7,
а
во3в'ращали
в про,цесс
электролиза.
^Фракцию
с
размерами
частиц
+0,074
мм
о6раба-
ть]вали
10-20
мин.
в
кипящем
водном
'растворе
нитрата
алю-
ми1111,я
для
,растворения
фторила
тория.
||ри
п-ромьтвке
осадка
в
верхнем
слое )кидко'сти
образуется
тонко
дисперсньтй
осадок
окиси
тория
и металла'
ко'торьтй 1мо}{(,но
,отделять
йутем
центри_
фугирования.
Фб'ра;ботка
катодного
осадка'. получен'но,го
олектроли3ом
хло]
ридно-оксиАной
'ваннь:,
п'роще'
так
как
хл'оридь1
щело,чнь1х
ме_
таллов
и тория
растворимьт
в воде.
Б
этом
случае
осадо'к'
снятьтр]
с катода'
та|к_>ке
лро'6илп
и
обрабатывали
водой,
остаток
пред.
ставлял
собой
поро[цок
тория.
()казалась
полез'ной
предварительная.
подготовка,поверх_
ности
катода
с
целью
увеличения
'сцепления.с ним
осадка
тория.
(атод
обра'батьтвали'песко'м,
обезх<ири,вали
парай''рйй''р'""-
л,ена
и протравливали
подходящим
агентоп{'
затем
'промь|вали
дистилли,рованно,й водой
и
су1пили
на
во3духе.
}{аблюдения
по_
казали,
что
яаилуч1пим
материалом
кат0да'
обеспечивающи,м'
в
частности'
ма,ксимальньтй
вьтход
-1!1еталла'
является
молибден.
Аля
фторидно.о,ксидной
-ванны
в
ра3личных
условиях
прямос
извлечение
металла
'колебалось
о,т
,3,2
до
4!,о0|0
(в
среднем
13,37о).
6реднее 'отно1пение
веса
полученного
металла
;к,€}ммаР.
ному
весу
осадка'
включающему
3ахваченнь]е
соли
|и
окись
то-
Рия,
сос'тавлял!о
39'3%'
и3меняясь
от
18,2
ло
67,90/9.
|1риме,рно
6\
,70|0'вьтделен,н]о,го
1металла
цбцдо
крупностью
+0,55
'';
^',"-
чество
металла
крупностью
-0,074
]у|м'с'остаьляло
от 2
до
70|,.
^оличество
нерастворимого
в с'оля'ной
ки,слоте осадка
и3меня_
лось.
от
0,10
до
2,30о|о,'составляя
в еред}!ем
0,630/0.
||ри
работе
с хлоридно-оксидной'ванной
.р.дй..
'прямое
и3_
влечение 'металла
ооставлял1о
27,20|о'
и3меняясь
от
13,9./о
до
55,00/0.
Бес
вьтделенно,го
металла
по
отно1шению
к в'есу
всего
0садка
,соста,влял
в
:9!€!н'оп|
22,Бо|0
('от
10,9
ло
43,30/9).
&оли-
1{ество
_ _нераетв,оримого
в
оолянот}
ки'слоте
остатка
бьтл,о вьтсо-
ким
1,92_!2,20|0.
Разплерьт
частиц
металла
бьтли
гора'д'
".,,_
*е:
чем в
случае
применения
фторилно-оксидйой
ван,ньт.
б
оольтпинстве
опь|тов
весь продукт
имел
крупность
_0,|5
мм с
ра3мерами
ча'стиц
10-50
мк.
Ё{есмотря
на
т'о
чт,о
электроли3
хлоридн,о-оксидной
'ваннь1
мо)кно
п'ро'водить
при
более
ни3ких
темпера|турах
и о,бработка
катодного
о'садка
дов,ольно
проста'
автор
считает'
что
более
вьт-
годнь1м
я]вляется
использование
фторидно-о'ксидной
ваннь1'
так
[орцй
241
как при
эт0м получается
металл более вь{сокого
качества
с
больтцими
размерами
частиц. |(роме того,
фторидьт'
3ахваченнь1е
с
металлом, мо}кно.
непосредственно
возвра1щать
в
процесс' в
'го
в'ремя
как
хло'рид
тория
,при
обработке
катодного
осадк0
!8ст:
в0ряется
в
воде и
Аля
ег,о
во'3вра'га
необходима
'специальная
переработ,ка
раствора
с получением
безводного хлорида.
€одерх<ание
п'римесей иоеновн0го
вещества в металле'
полу'
ченном
йз
фторилн,о-оксидной
ваннь|'
0/9,'сле.{}юш{ее:
0'06
0'0ш9
0,009
<0'0000б
0,07
0,025
'
0,1
0,0035'
Бь:л,о определено
напря)кение
разло}|(ен|ия
оки!си т0рия
для
ра[спла'влент!ой
фторидно-оксидной'смеси,
его
ве4ччи.на
колеба_
ла,сь
'в
пределаг
\,в7-2,\5
в
(в
среднем
1,92-'+-0,11
а),
для_р_ас-
плавлонн'ой
хлоридно-оксидной сист.емь|
она соета1вутла
'\,92
!'
-у
0,27 в.
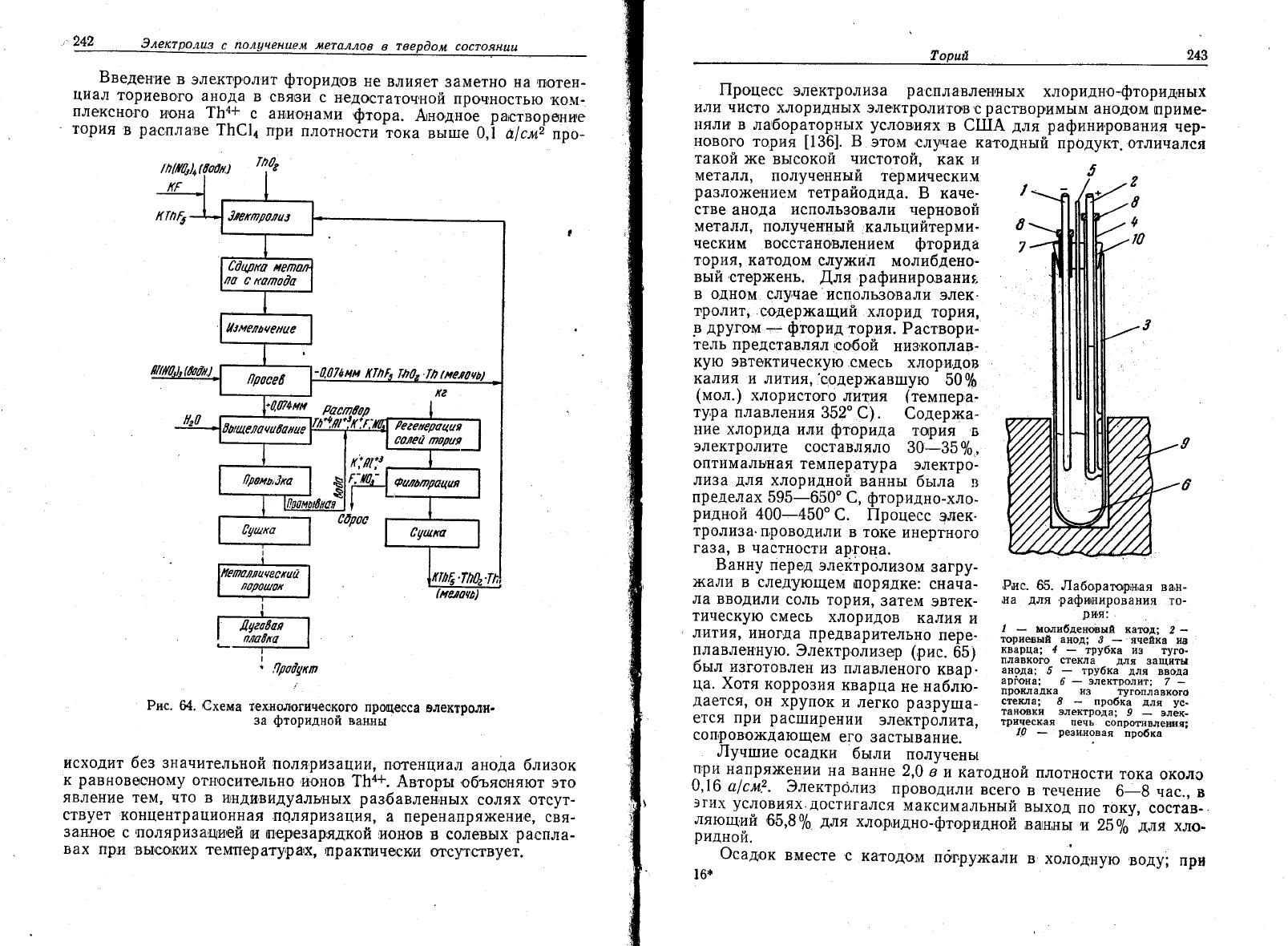
€хема технологическ0го
процесса
прои3в'одства
т.ория
элек_
тр'оли3о,м
фторидно-оксидн,о]го
олектролйта
приведена
на
рис.
64.
€лелует
отм,етить. что самую
мелкую
фракцию,
состоящую
и3
то|нко
ди'спер!сного
металлического тория
и'солей,'содер)кащихся
в
электролите,
ли,б'о
окисляли
при
нагревании
кисл|ородом
во3-
духа
с
целью
превращения
'м,еталличес'кого
тория
1в
'окись
и
!по_
лучения
п'родуктов.
вФ3Б!3!{2;€мь!х
в электролитную
ван|т{у,
либо
непосредственно
на,п'ра,вляли,в-ванну.
1ор,и[, содерх(а'щийся
в
промьтвнь!х
растворах'
мо}кет
бь:ть
возвращен
в
п'роцесс
в виде
двойного
фторила
тори'я
|1 кал14я оса>кдёнием
этой соли
обь|чнь|м
опособом.
3лектролш3
с
растворшмь!мш
ано0амш
€мирнов
с
!сотрудниками
[134-135]
изунали
процесс
а1нод_
,6р6
;р3ёт8орения
'тория
в
ра1еплавле1н,нь|х
смесях
хлор|идо]в
1ц'е_
лочнь]х
'металл,ов'
Бьтло
устан,овлен'о'
нто торий
переходит
в
эле.к-
тоолит в
виде
двухвале!!тньтх
!тонов, так'как
равновесие реакци1}
{ь
+
1}:{+ср'"'1
?)1[:2+(раст)
€й€щ0но
в
,сол'ево'м
расплаве
в сто_
рону
образ'ова!н'ия
субионов.
Раопдав|при
этом
прио:брета9т
силь-
но восетановительнь1е'свойетва
и
разру1пает
алюмориликатнь|е
футеровоннь|е
материальт.
||ри
и3учении
поля'ри3ации
ториевого
анода бьтло
устан'овлено.
что когда.в
|приа1нодном
слре
электро-
лита
'образуется
равновесная
смесь.
тьс14
и
1[:!1э,
.
ц619цт{и8,т[
анбда
цра'ктически
перестает
меняться.
1
::
16
заказ
1677
оА1
в
€а
са
€г
€ц
Ре
|*19
с
полцченцем
леталлов
в
т
Бведен'ие
в
эле'ктр'олит
фторидов
не влияет
заметно
на
{п|отен_
циал
ториево'го
анода
в
свяви с
недостаточ,ной
проч|ностью
ком_
плекс}{ого
иона 1}:{+
с анио'нами
,фтора.
Анодное
рас,твороние
тория
в
рас,плаве
тьс|4
при
плотности
]тока
вьт:пе 0,!
а|см,
п,ро-
гл|ф)*
кг
|( гпг'
1|1епаллцчеспцс] !
|
лорошок
|
_|_€
!
|
!що8ао
!
|
п'а0/а {
*-тд
'|ро0цп
Рис.
64. €хема
технологичФск0го
процёсса
9лектролш.
за
фторидной
ва;ннь|
исходит без значительной
поляри3ации'
потенциал
анода
близок
к
равновесн'ому
отн|осительно
и,0нов
1!{+. АвторБ1
:Фб599ц9''
,''
явление тем, что
в и1нди'видуаль'ных
раз'бавлен'нь!х
солях
,отсут-
ствует концентрационная
поляри3ация,
а перенапряж{ени,е'
свя_
3ан,н,ое
с
|поляри3ащи'ей
и
п'ёре3д*,*ой
и'он'ов
в солевь|х
распла-
вах
при
высоких температура|х,
практически
0тсутствует.
!с1[у
!оршй
243
||р,оцесс
электролиза
расплавлен|ных
хлоридно_фторидных
или
чисто хлориднь1х
электролит0в'с
раствор,имь|м
анодом
приме_
няли в
ла1бораторнь1х
усл,овиях
в €1]-!А
для
рафини'рования
чер-
нового
тория
[136].
в
этом
'случае
катоднь:й
пролуйт' о'тличался
такой
х(е
вь|сокой
чистотой'
как
1|
металл'
полученный
терми'неским
разло)1(ением
тетрайодида.
в
каче_
ствеанода исполь3.овали
нерн'ово*1
металл' получе|т1|ый
кальцийтерми-
ческим
восста1!овлением
фторила
тория, катодом
слух(ил
молибдено-
вь:й сторх<ень.,[,ля
рафиниро'вани',
в одном.
случае
исполь3о,вали
элек.
тролит' с_одерх(ащий
хлорид
тория'
р
другом
--
фторид
т0рия.
Раствори_
тель представлялсобой
н.из'коплав_
кую
эвтектическую
смесь
хлоридов
кал|1я у| л|ттия,
]с:одерх<автшую
509о
(мол.)
хлористого
л|\тия
(темпера_
тура плавления
352"
€). 6одерх<а-
пие хлорида
\4]\п
фторила
т0рия
Б
электролите
составляло
30-35%,
оптималь'ная
температура
электро-
л143а
для
хлоридной
ванньт
бьтла
в
пределах 595-650'
6,
фторидно-хло-
ридной
400-450"
с. ||роцесс
?дек.
тролиза.
п'роводили
в
токе
инертного
га3а' в
частности
ар'гона.
/
а
7
2
0
4
/0
9
0
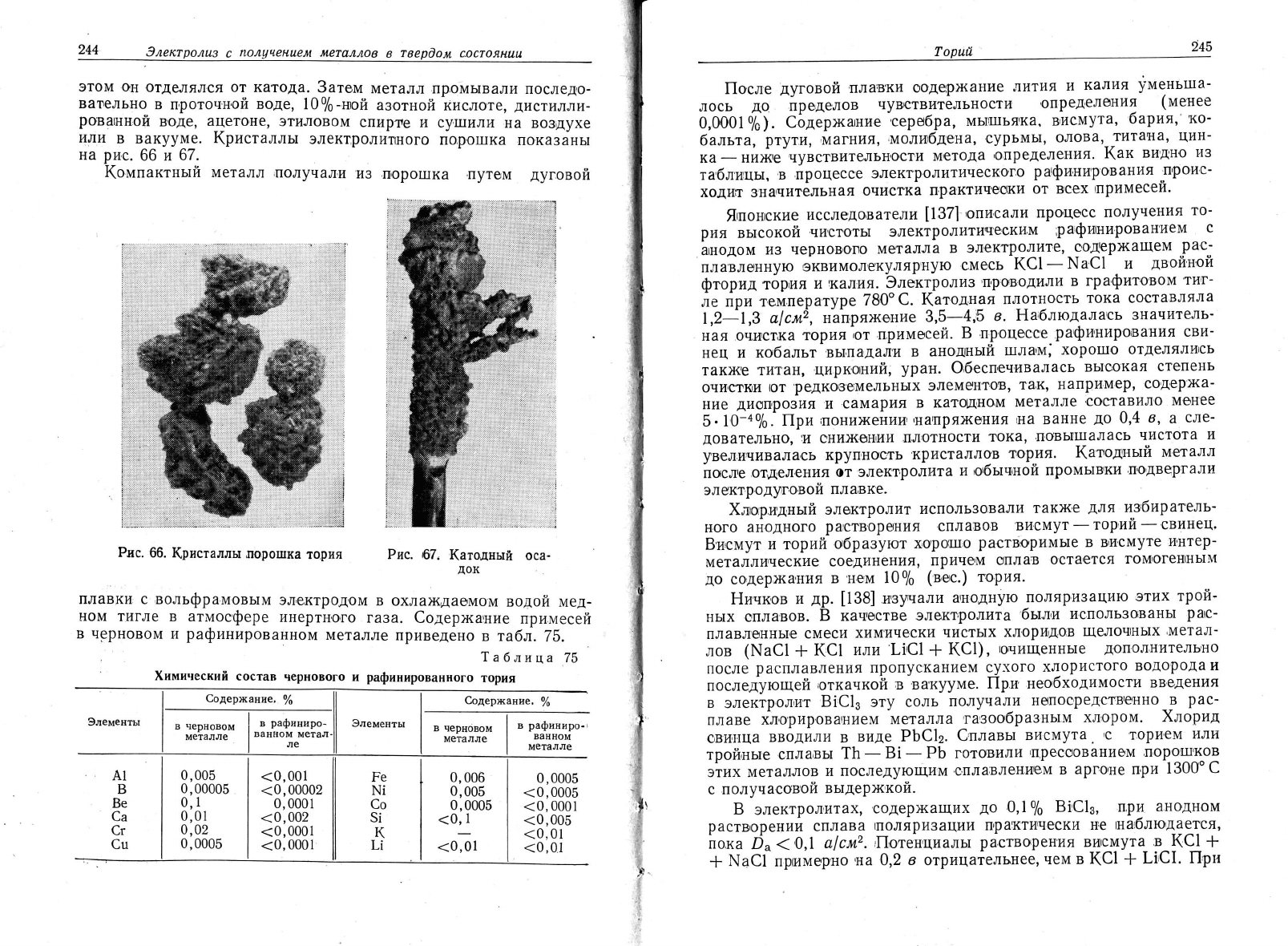
Банну
перед
элейтролизом
загру-
)кали
в следующем
порядке:
снача_
Рис.
65.
.).|або'раторш'ая
ва'н_
ла
вводили
соль
тория'
затем
эвтек-
,}{а
для
рафипнирования
то_
тическую
'смесь
хлоридов
кал|\я
|1
-
р}!я:.
лития,
иногда
предваритель}!о
пере-
;*"**гъ%ту?1-#:*,';
плавлен'ную'
3лект0олизщ
(рис.
65)
;::3".3:"'";;:'6*;";"""Ря
был изготовлен
из 1лавленого
квар.
анода;
}
_
|Бу6к{-йя'ввода
ца.
{,отя
коррозия
кварца
не
наблй-
;3у#а-,,
_;;"*#Ё;*"|'-]*
дается'
он хрупок
и
легко
ра3руша_
стек]1а;
8
-
про6ка
для
ус.
ется
при
рас1|]ирении
электролита' |Ё;-ЁЁ#""-3#'1}''"",,"3#*;
сопрово)кдающем
его
3асть1вание.
'[0
_
резиновая
прФка
.[|уншие
осадки
бь:ли
получень1
при
напрях(ении
на ванне
2,0
Ё
и
йатодной плотности
тока
около
0'16
а|см?.
3лектролиз
проводили
всего
в
течение
6-8
нас.,
в
)тих
условиях.достигался
максимальньлй
вь|ход
по току'
состав_
9"ющий
65,8%
для
хло,р!идно_фторидной
вандьт
и
2'5о|]
1''я
*ло.
Ридной.
Фсадок
вместе
с
ка'тодом
пс}грух<али
в
холодную
воду;
при
16ф
этом
он
отделялся от катода.
3атом
металл пр.омь1вали
последо_
вательно
в проточ'н'ой
воде,
100/о-ной
азотной
кисл,оте'
дистилли-
рова:нн,ой
в'оде'
адето,не'
этиловом
спирте
и су'1лпл\4
на
во3духе
||ли
в вакуум€.
(ристаллы
электролитного
по'р,о1пка
показань|
на
рис.
66 и
67.
(омпактньтй
металл
;п@.т|}!|?л,}1
и3
,поро1пка
'путем
луговой
244
3лектрол1]3
с
полученцем
металлов
в
твер0о1
состоянцц
€одерх<анпе'
%
9лементьт
Рис'
66. |(ристаллы
порошка
тория Рис.
67.
'}(атодный
оса-
док
плавки с вольфрам'овь1м
эл'октродом
в охла}кдаемом
водой мед-
ном
тигле в атмос,фере
инертн'о|го
га3а. €одер>кание
п,римесей
в черновом
и
рафинированном
металле
приведено
в та6л.75.
1абли
ца
75
]
*,",ческий
состав
чернового
и
рафинированного
тория
€одер:кание'
0/6
!1
,,""*"
1[
А1
в
8е
€а
(г
€ш
в черновом
металле
0,005
0,00005
0,1
0,01
0,02
0,0005
в
рафиниро_
ванном
метал
ле
в черновом
металле
0,006
0,005
0
,0005
{0,1
<0,01
в
рафиниро-'
вапном
металле
0,0005
<0,0005
<0,0001
<0,005
<0,01
<0.01
<0,001
<0,00002
0,0001
<0,002
<0,0001
<0'0ф1
Ре
ш|
€о
5|
к
[!
!оошй
245
|1осле
дуговой
плавки
0одер)кание
лития
и
кал||я
уменьтпа-
лось
до
првделов
чувствительности
'определени!
(менее
0,0001
%).
6одер)ка!ние'сер0бра,
мь1ш]ья'ка.
8'|4€}у1}121,
оария''
ко_
балъта,
ртути'
,магния'
'молибдена,
'сурьмь|,
олова'-
титана'
цин-
ка
-
них(|е чувствительн,ости
м,етода
,Ф'||РёА€л€[1{я.
как
видно
из
та'бл'и|цьт,,в'йроцесее
электр,олитическо'го
ра|финирования
проис_
ходит з'начительная
очи'стка
п'рактиче0ки
от всех
1примесеи'
[!понпские
исследователи
[137]
'опи,сали
процесс
получения
то-
рия
вь|сокой
чи,стоть|
электролитически,м
;ра!фини'рован'ием
с
а!нодом
и3 чернов,опо
металла
в электролите'
оодерх(ащем
рас--
пла'вленную
эквимол'екулярную
с'месь
-(61
-
}'{а€1 и
двой'ной
фторид
т6р,ия
|4
|кал'\4я.
3лектролиз
'пр'оводи'ли
в
графит0вом
'тиг-
ле
при тем'пературе
780"€.
1(атодная
плотность
тока составляла
|,2-:\3
а|см,,
напрях<ение
3,5-4;5
с'
Ёаблюдалась
значитель-
ная
'оч'ист,ка
тория
,от
п,римесей.
Б прошесее_рафинир0вания
сви-
нец и
к0бальт
вьт,|\адад,4
в
аноднь1й
]пла'м;
хоро(по
отделяли|сь
такх('е
титан'
,цирк0ний;
уран.
Ф'бесп'ечивалась
вь!оо'кая
степень
очистки
|от'редко3'емельнь1х
элемен'тов'
та,к'
напри'мер'
содер'}ка-
ниедис|прозия||самариявкато{дномметалле'составил,ом.он'ее
5.10_{0/о.
при
{пони}кении'
,напря}кен|19':|\2
ванне
до
0,4
6,
а
сле_
довательно'
1и
они)к'ен;}'1}1
,||й'Ф1}1Фёти
'тока'
повь]1палась
чистота
и
ув'еличивала,сь
круп'н0сть'кристаллов
тор.ия.
1(атодньтй
металл
посде
'отделения
от электрол\4та
|! обьтчной
пр,омь|в|ки
,подвер1гали
электродуговой
плавке.
[л:оридньтй
электролит
исполь3овали
так>ке
для
из'биратель-
}{,ого
анодного
ра|ств'орения
сплаво,в
висмут
-
торий
-
свинец.
в'исмут
и торий
обра3уют
хо'ро{1п,о
растворимьте
в вй'смуте
и'нтер_
металлические
соединения'
причем
0плав
оста|ется
том|о'геннь1п{
до
содерх{а,н'ия
в
'нем
100/о
(вес.) тория.
Ёи'чков
и
др.
[138]
'и3щали
а|н'одную
поляризацию
этих
трой'
нь|х оплавов.
Б кач'естве
элоктрол.ита
'бь1л,и
использовань1
рас-
плавл'еннь|'е
смеси
хим'ически
чисть1х
хл'оридо,в
щелоч!нь|х,метал-
лов
(\а€1
+ кс1
или
'!!1с1
+
кс1)
'
точищеннь|е
доп'ол'нительно
после
ра'сплавления
пропусканием
Фхого
хл-ористого
водорода
и
последующей
|откачкой
в ва'кууме.
||ри
.необходимости
вв'одения
в
электр'ол'и'т
в|с13 эту соль
получали
непоередств|енно--в
рас-
плаве
хл'орир'ова|нием
металла'га]зо0бразнь|.м
[/{0'РФ]!1.
{,лорид
овиц{ца
вводили
в
виде Рьс12.
€'плавьт
висмута.
!с
тори'ем
или
трой'ньте спла'вь!
ть
-
в1
-
РБ
готовили
]п,рес,сованием
поро|1ш1ков
этих металлов
и последующим'спла;влен.и|ем
в арго|не при
1300'€
с'получ
асов1ой
вьтдерх{кой.
Б
электролитах'
'содер)кащих
до
0,10/9
Б1,€13, п,ри
анодном
!а8твп9!€}'{1.|и
сплава
|поляризации
практически
}те
:на,блтодается,
|ока
б.
/-0,\
а|см2.
:|1;Ф'19н,(и2ль1
ра,створения
висмута
;в
(€1
*
*
\а€|
пример]но
\1а 0,2
6
отрица{ельнее'
чем в
кс1
*
[1'€1.
|!р:т
246
34ектролцз
с
полцценцел
мета!тлов
в
твер0ом,
состоянцц
больттт6[
|*
ко'нцен'тРаци'я
Б!
в приэл,ектродном
!слое
ра,стет'
та,к
как 'скор'ооть
!отвода
ионов
висмута
в
электролит
мены1пе'
чем
€(о,р6'6'1,
их
поступления
за счет
растворения
ан,ода.
3то
вьтзьт-
вает
появление
поляриза'ции.*|{ри
растворении
|в'ис,мута
образу-
|0тся
главнь:м
образом
ионы
Б|3+,
но,
кр,оме
.1Ф|Ф,
:}!'ио,ньт
низ1пих
валентн,оетей.
Бсл'и
электроли,т
содер>кит
боль,тше
Б|61з,
то
ви,смут
раство-
ряется.при
более
,||'Ф,т]:Ф*:[1€/|ьном
'потенциал'е, пока .}"
"ё
вьттше
|-2
а|см2.
|1ри
далынейт:лем
росте
|^
анодттьтй
'потейциал
с'а-
н'овится
|одина'ко'вь|м
во
всех
электролитах
и
процесс идет
без
!|0./!яр:и3,дгцци.
|1отенциал
в|и|0мутов01по
ан,ода
соста|вля'ет
-
0'76-
0,78
в.
€'п,они>кением
температурь|,потенциаль|,ви|смуто|вьтх
анодов
становятся
'более отрицатель'йь:ми:
лрп |^:0,\
а/см2
и
электро_
лите 1-!€1
+
кс1 +
|у0
в!,с|3
он'и
ра'Ё'нь::
. 700
600
500
450
.
_0'94
-1'00
_1'23
_1'з0
Растворение
свинцо.вого
а|нода
идет
при
значительно'более
о'три-
цательнь1х
потенциалах
и
лоляри-
3ация
анода
начи'нается
п,ри
бо_
лее
низкой
плот1{ости
тока. Раст_
ворение
т0риевого'
анода
происхо_
дит
с обра3о'ва,нием
[[:2+
при
еще
более
вь|сок0м
отри,цательном
3,начен,ии
'потенциала'
чем
для
свинца.
Б
работе
приведены
результа_
тьт
0пытов
ра,створения
сплавов
ви'смута
9
2,50|о
(:вес.)
тория
и
р4-3ньтм
количествой
ёв}1т}!1'{1
[5
г:
1
%
(вес.)].
Бсли
содорх(ание
9вш}тц?
вд1ш.е
{9о,
то
да}ке
п,ри
|а:4-5
а|см2
не
удается
до_
сти'гнуть
потенциала
висмута.
|!ри
2^
:
1--5 а|см2
растворйет-
'ся
свинец.
Р'сли
х<е
|сплав
содер_
>кит
1
0/о
Рб,
то в
тех х(е
предела)|
!,
потенциал
анода
близок
к
'по-
тенциалу
висмута.
Блияниё
а,нод_
'1{ие
!к0м|п0н0Ё[Ф3
г€||./|?'"
'
,"*''##
#*ъ}:.'аЁ.
тока
на
р
астворе_
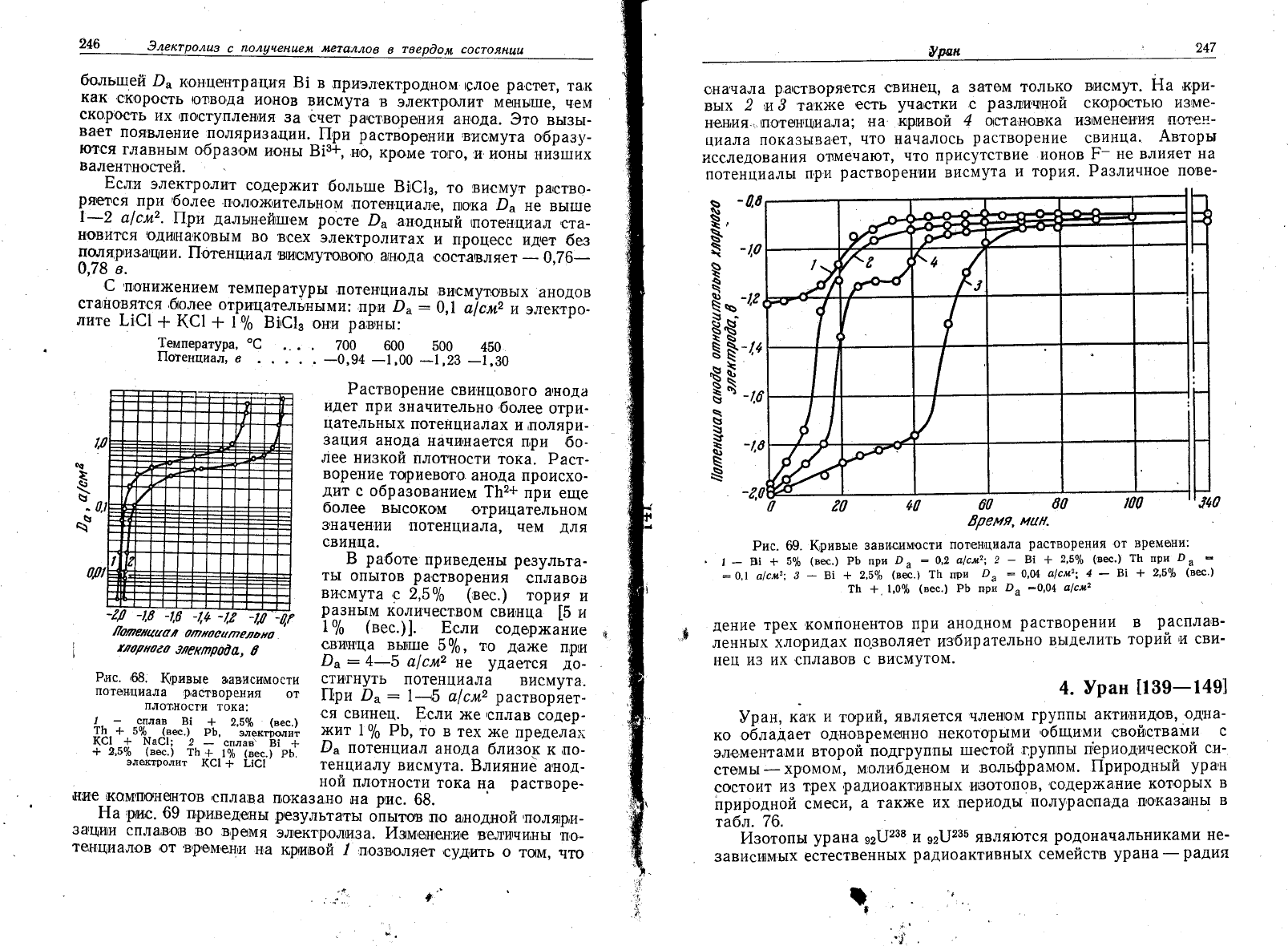
Ёа
рис.
69 пргиведень1
р|езультатьт
оп-ьттов
по
анодн0й
,поляри-
3аци1и
€|1./18;8:Ф|8
во
в,ремя
электр'олиза.
йзм'еше':т|и'е
в,еличинь|
по-
те}1циалов
'Ф!
в'!'01!1'ён:и
н'а
кривой
.1
,п,Ф3Б,Фля'ё1
'судить
о
т0м,
что
Рдс.
,68.
(ривь:е
аависимости
поте1!циала
р'астворения
от
плот}]о'сти
тока:
1-.
-
сплав
в!
+
2,5%
(вес.)
1}:.
* 5%-
(вос.)
Рь'
электро.,!ит
(€1
!
!т{а€|;
2
_'сплав
Б;
+
+
2'ьо|о
(вес.)
ть
+
!о/0
(зес.)
РБ'
электФолит
кс1 +
|-|с|
с! -|'8 -1'6
-|4 -/'-:1!э'Р
//олт,еац
ц а л
о/7? //о
с ц
/п ело
||
о .
$
в
\
\
\
ъ
\
з
$
Б
€
5
\
ч
\
ч
\
Ё
$
с,на'чала
ра|створя'ется
свипец'
а
3атом только
висмут'
!{а кри-
вьтх
2 :и 3
так>ке
есть
уча|стки
с
раз.гп'тнн'ой
ско|р'о|стью
и31ме_
н,е}!!ия.|'|пот9чтщцала!
на
кривой
4 о:с'та,шов'ка
из!мен'ен'и'я
шо'т'ан-
цт1ала
пока3ь1вает'
что
началось
растворецие
свинца.
Ав'торы
исследования
отмечают'
что присутствие
ионов
Р-
не влияет
на
потенциаль1
п,р'и
растворен'ии
висмута
и тория.
Различное
пове'
Рис. Ф.
&ривьте
3авиоим0сти
потенциала
растворения
'от
времони:
,
,_в1
*50/о
(вес.)
РБпри!^:1,2а!см2;2-в|
*2,5о/о
(вес')1[:п!и2'
-
:0,|
а|см21
3
-в1
+
2,5%
(вй.)
1[при
!'
:0,04о!см214_в|
+
2'5%
(вес')
ть
+,
1,0о,6
(вес.)
РБ лри
|^
-0,04
а|сло2
дение
трех
компонентов
при
анодном
растворении
в
р.асплав-
леннь]х
хлоридах
по.3воляет из'бирательно
вь1делить
торий
и сви-
нец
из
ихсплаво'в
с висмутом.
4.
}ран
1139-149]
9ран,
[''*
,
'торий,
является
'член|ом
гру-ппь1
акти'нид1ов'
'одна-
ко обладаег
одно'врем'енно
некоторь1ми
общими
'свой|ствами
с
эл,е'м'ента,ми
второй подгруппь!
1шестой
|руп|пь1
пфиодинеской
си-
стомь1-хр'омом'
молибденом
и вольфрам'ом.
|1риродньтй
уран
состоит
и3
трех
радиоактивнь|х
и1зото|пов'
'содерх(ание
которь]х
в
приролной
смеси'
а такх{е
их
п'ериоды
полураспада
по'ка3а{нь|
в
та6л. 76.
й.''о,ь'
урана
92ш23в
и
эу|}2з6
являьтся
родоначальниками
не_
3ависим'ь1х
естественнь|х
радиоактивнь1х
семейств
урана
-
раА\4'\
1
|
-
1,0
-13,
-14
-1.6
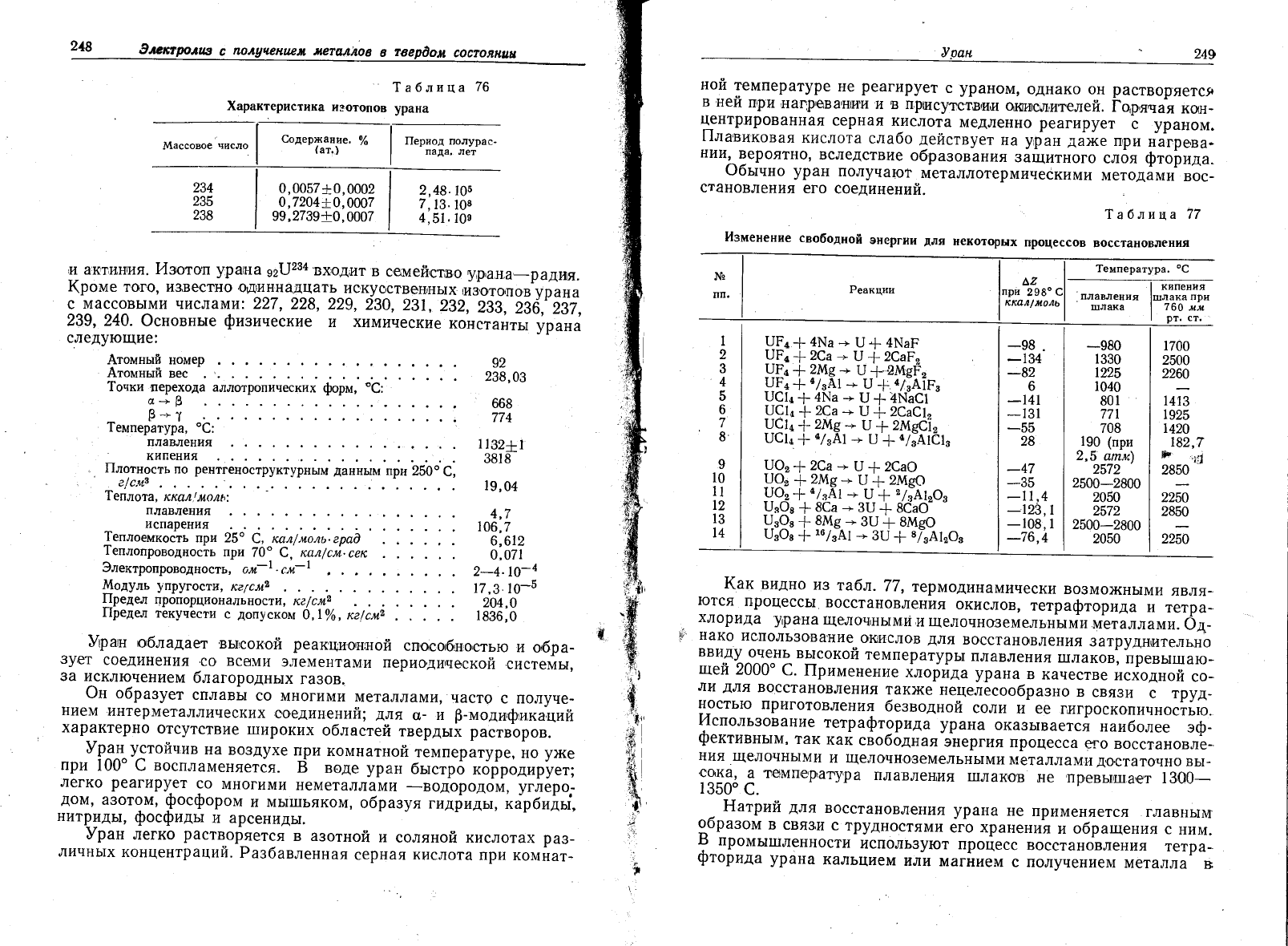
1а6лтаца
76
[арактеристика
изотопов
урана
234
23Б
238
0,0057*0,0002
о,7204!0
'ооо7
99,2739+0,0007
2,48.
105
7,13.
108
4,51.100
[ут-
акт14'11ия.
14зотоп
ур
а]н а
ээ|)2з+
входит
в
оом
ей'ств
о
ур,а'н'а-р
адия'
1(р
о
м е того' и3,в
естн о одй:тя адца ть_и
ск_ус|ственнь|х
;и3]ото,п
ов
ур
ан
а
с
массовь|ми
числам.и: 227,228,229,
230,
231,
232,
233,
236,'237,
239' 240.
Фсновньте
физинеские
и химические
конста"",,
ур'",
следующие:
Атомнь:й номер
92
Атомный
вес
:зв,оз
1онки
перехода аллотропических
форм,
'(,:
с*0
668
774
плавления
плавления
1
132+
1
3818
19,04
4,7
1о6
'7
6,612
0,071
2_4.\о_4
17.3
10-5
2о4'о
1
836,0
}!ра:н,6'6дд.(3Рт
ЁБ|:€Фкой
реакцион;ной
сп'о1со|б|н]о'стью
и
о'бра_
зует
соединения
'со'
всеми
элементами
периодической
'системь|,
за
исключением
благороднь|х
га3ов.
Фн образует
сплавь|
со
многими
металлами'-часто
с получе_
нием
интерметаллических
ооединений;
для
с-
и
р-модд,ф:ика,ций
характерно
отсутствие
1цироких
областей
твердь|х
растворов.
[ран
устойч,ив
на
во3духе
при
комнатной
температуре,
но
у>ке
при
100' € воспламеняется.
в
воде
уран
бь:стр6
ко!род'руе";
легко
реагирует
со
многими
неметаллами
-водородом'
углеро._
дом'
а3отом,
фосфором
и мьт!|]ьяком,
образуя
гид$иды,
к6рбидь{'
нитридь|'
фосфильт
и арсениды.
9ран
легко
растворяется
в азотной
и
соляной кислотах
раз_
лич}|ь1х
концентраций.
Разбавленная
серная
кислота
при комнат_
!оан
249
ной
температуре
не
реагирует
с
ураном'
однако
он
растворяется
в ней
при,н8гр'93д'"''"
и в п'рисутс{в'ии
окиолителей.
}оряная
кон_
центрированная
серная
кислота
медленно
реагирует
с
ураном.
|]лавиковая
кислота
слабо
действует
на
уран
да)ке
п)ри
наг!е'ва.
нии'
вероятно'
вследствие
обра3ованпя
зайитного
сл6я
фторида.
Фбьтчно
уран
получают
металлотермическими
методЁ*,
"ос-
становления
его
соединений.
^[
а6лица
77
Р|зменение
свободной
энергии
для
некоторых
процессов
восстановления
м
пп.
Реакции
!',
!при
298'
(
|ккал/лсоль
?емпература,
'€
плавле||ия
1плака
1
2
3
4
5
6
7
8
{-1Рд{4$а*1-1
*4}.{аР
],[д*?9а*1_]*2€аРя
!]&
+
?мв
*
{-1
--{-91т18Ёя
!-]|*
*
ц
/
зА1,
*
ш
+
4/;А]г3
шс14+4!.{а*ц+4шъс1
_
ч!14+|(а*у|2€а|12
!]!|*
+
2!!19
*
|}
{
2й9€!,
шс14
+
ц/3А1-
|-]
+
4/а|с|3
-98
-134
-82
6
-141
-131
-55
28
1700
2500
2260
1413
\925
|42о
182,7
р ..!
2850
22ю
2850
225о
*980
1330
1225
1040
801
771
708
190 (при
2'5
ап.м)
2572
2500-2800
2050
2572
2500-2800
2050
9
10
11
12
13
14
{-]Фя*2(а-ц*2(аФ
1)Ф+2|{р-ш+2мРо
!-]Ф-,
*
ц
/
зА1
*
ш
+
?/а|2о3
|-]вФв
*
8€а
=
3ш
*
вёа6
_
!-]_з9в
*
8й9
*
3{-]
{
31т19@
[1зФв
*,в
/'^|
*
3ш
+
в/"3А12о3
6'
|(ак
видно
из
табл.
77,
термодинамически
во3мо}кнь]ми
явля.
ются
процессь1.
восстаг1овления
окислов'
тетрафторида
и
тетра*
хлорида
ура'на
1{ё.[Ф9:нь|мй
и
щелочн0земельнь|ми
'металлами.
6д-
нако
исполь3ова'ние
о'кислов
для
восстановления
затруднитель'но
вв
иду_
_оч_е_нь-
вьтсокой
тем
п
ер атур
ьт
пл авлен
ия
!шл
аков'
превь|[|]
аю
-
щей 2000"
€.
|!рименение
хлорида
урана
в качестве
исходной
со-
л|1
для
восстановления
так}ке
нецелесообра3но
в
связи
с труд-
н-остью
приготовления
безводной
соли
и ее
пигроскопичностью.
?^'_т:-у::"ние
тетрафторида
урана
ока3ь|ваетсй
наиболее
эф-
фективнь|м,
так
как
свободная
энергия
пРоцесса
его
восстановле-
ния
.щелочнь|ми
и
щелочно3емельньтми металлам,и
до'статочно
вь1_
'с0ка'
а ?Фй[€0т2?!'!а
плавлен'ия
1плако'в
не превь1'ша,ет
1300-
1350"
с.
-
Ёатрий
для
восстановления
урана
не
применяется
главнь]м
3бра3ом
в связ,и
с
трудностями
ёго хране"ия
и обрашения
с
ним.
|]
промь]|пленности
используют
пРо1{,есс
восстановления
тетра_
фторида
урана
кальцием
или
магнием
с получением
металла
в

25о
3лектролцз
с
полццен|!е7,],
металлов
в
твер0ом состоянцц
расплавленном
состоянии;
при охлах(дении
обра3уется компакт_
нь|й
слиток.
|1опь:тки
получения
урана
электролизом
воднь|х
растворов
€го
солей,
например
хлор,идов'
не привели
к.полох(ительнь!м
ре-
зультатам'
так
как
уран
в
воднь1х
растворах
стоит
в
ряду
напря-
а(ений
отрицательнее
водорода. воднь1е
растворь|
исполь3уются
ли|пь
для
восстановления 1_}6+
до
1-1{+ в
свя3и
с получением тет_
рафторида урана [150-154].
|1роводились
опь|ть|
вь|деления
ура-
на и3 водного
раствора
его тетрахлорида
на
ртутном
катоде
с
получением амальгамь1.
Фстаток после отгонки
ртути
в вакууме
представлял
собой тонко
дисперсный
поротшкообразнь:й
металл'
которьтй са!мо|в0опламенялся
на воздухе
[155].
Фпубликовань|
исследования по
электролитическому
вь1деле-
нию
урана
и3
его
солей, на|п;ри'м1ер хл'орида'
сулыфата,
а'цетата
и оксалата
урана'
Б @!,гд'рцч*оких
раств'орителях
_
пир1идине'
диэтиловом
эфире, амиловом
спирте и этилацетате,
тетраброми-
де
урана
в
бенз:оле,
этилен|бро'миде'
диотилА['Ф1{€8'}{'€,
а,цетоне' эти_
ловом
спирте.
9довлетворительнь1х
ре3ультатов
получено
не бь!-
ло
[156-157].
Более
успе1пны.ми
оказались
работьт
'по
применению
элоктроли-
3а
расплавленнь|х
солей как
с
целью
восстановления
металла и3
ег6
с6единеций, так |1
для
электролитического
рафинирования
чернового
урана.
|1роцессьт
электролиза'
судя по опубликованнь|м
данньтм'
не имеют
еще существенного
значения в
современной
урановой
промь111]ленности;
в л,итературнь1х
источниках приводит"
.ся
много
рецептов
ванн
различного
состава' среди которь|х
труд-
но вь1делить
наиболее перспективные
электролить|
и
ре>*(имь1
тех_
'нологического
процесса' пригоднь|е
для
промьт1шленного
исполь-
'3ования.
1(ак
указь:валось
вь|1ше' в зависимости
от температурь| плав-
ления металла
и вь:бора температурь|
электроли3а
уран
мо}кно
получать
на
катоде
как в
виде поро1пка' так
и в
расплавленноп[
"состоянии.
|1оэтому
шелесообразнее
построить
классификацию
электролитических
.методо,в,получен)ия
урана
из
расплавленнь1х
сред в зависимости
от
температурь1 электроли3а.
|( первой
группе относятся
процессь1
с температурой
электро-
ли3а них(е
точки плавления
урана;
металл вьтделяется
на 1{атоде.
в виде поро1пка
или губнатой массьт. 8
свою
очередь
эту
группу
'процессов электролиза
мо}кно
разделить
следующим
образом:
1. ||рошессьт
электролиза' протекающие
при температуре
375-425"
€
с применением
легкоплавких
электролитов;
для
этой
цел1и
в
качестве основного
ра'створителя
обьтчно
,используется
эв-
тектическая
смесь хлоридов
литпя
'и кал|4я
[590/о
(мол.)
!1с1
п
410/9
(мол.)
кс1'
температура
плавления
352" €]. 9ран
вводится
в
эвтектику в
виде
тр||-
|\ли тетрахлорида1
или тетрафторида.
!рон
2.
|[рошессы
электролиза
в
пределах
температурь1
800-
900'с,
с
исполь3ованием смесей
солей,
имеющих точки плавления
несколько
ни)ке
указанного
предела
температур
и
не
обнару>ки-
вающих
заметной
летучести
в
условиях
электроли3а. Б
качестве
растворителя
в
этих процессах
применяется
эквимолекулярная
смесь
хлоридов
кал14.я
и натрия или
(чафе)
расплавленная
смесь
хлоридов
каль|1ия и
натрия
с
ра3личными
соотно1пениями
этих
компонентов.
}ран
вводят
в
,пер,еч,исленнь1е
смес'и' как
и
в пре_
дь|дущем
случае' в виде
хлоридов или
тетрафторида,
а иногда
и окислов.
|(о второй группе относятся процессь|
с температурой
элек-
тролиза
1175-,1200'€, п,ревьттпающей
точку
пла,вления
урана'
вследствие чего,
металл вьтделяется
на катоде
в
ра,сплавле,н,ном
состоянии
и
после
и3влечения и3 ванны
мо}{(ет
быть полунен
в
виде
компактного
слитка. 3ти
процессы
рассмотрень|
вы|ше.
8
данном
ра3деле рассматривается
первая
группа
![Роцессов
электролиза
с
получением на катоде
твердого
продукта.
2Б1
}
Ё
цз
кот
е
мпе
р
ат
у р
нь[е'п
р
о
це
с с ь' э
ле кт
р
ол!! 3
а
1(ак
указывалось
вы1пе, основным
растворителем
в
этих
про_
цессах
является
эвтектическая
смесь [|с1
-
}(€1,
отрицательньтм
свойством которой
является гигроскопичность;
рех(е
применяется
тройная
смесь
кс1-
}х1а€1-
[!€1. |1итание
ваннь| прои3водится
шсь,
шс14 или [_]&.
{_}€11 применяется
ре>{<е
в
связи с
довольно
вь:сокой
летучестью' одн4ко он
более
устойнив
в
расплаве'
чем
[-]с13.
Б
системе [1с1-
кс1-
|-]€1з наблюдается
заметное
расслое-
ние;
в электроли'те' содер)кащем
в ср'еднем 350/0
0613, проба,
взятая на глу6!тне 2,5 см
от поверхности,
содер>хала \0,20|9_
0, Б
то
время как на глубине
10
см
концентрация
урана
достигала
46,80/9
[158].
1емпература
плавления
электролита'
состоящего
из
эвтектической смеси
[1с1
+
((1
с
добавлением
330/о
0€13
к
весу
этой
смеси' составляет 360" €.
Б
се
пер етисленнь|е,вь|1пе
сиетемь| оостоят из,следующих
солей
:
кс1,
[!с1,
{-}€1з, {_]€1ц,
шц, кроме
того,
в
результате
обменнь:х
реак(ий
в
расплаве
образуются
1-1Р
и
(Б.
Б
табл. 78 приведеньт величины напрях{ен'ия
разлох{ения
пе_
речисленньтх
солей при температуре 700'к
{427,
с),
рассчитан_
нь1е
и3 вел,ичин свободной энергии образования
этих
соединений
по
уравнению
Ё
:
'".'
_пР
где
Ё
_-:
нап!я'{ение
разло)кения;
\\2т
-
и3монение
,свободной
энергии;'
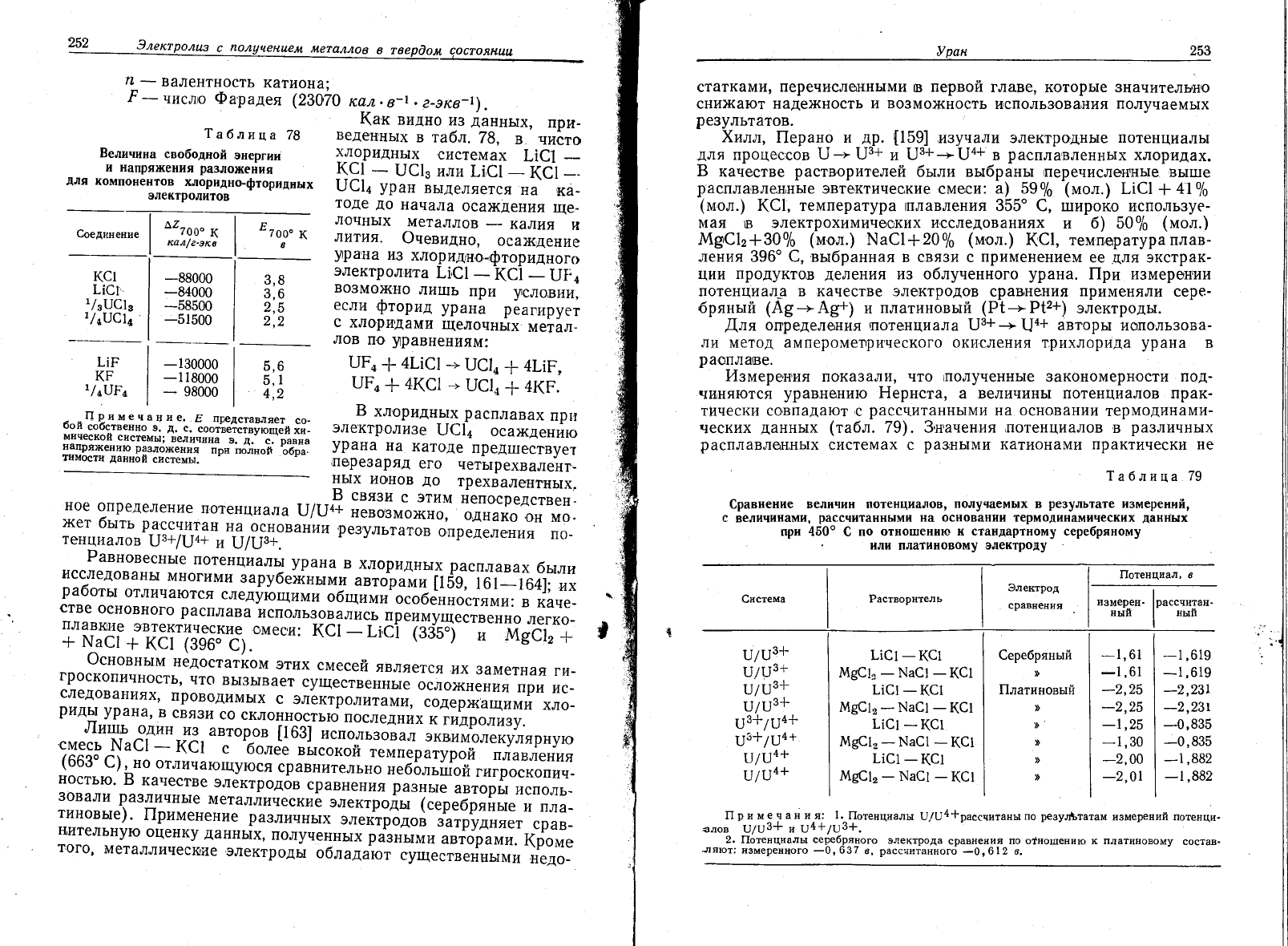
252
3лектролшз
с
полученаем
металлов
в
твер0ом
9остоянцц'
и
-
валентность
катиона;
Р
-
число Фарадея
(2307о
кал.
в-|
,
е-экв_1).
(а'к
видно
и3
данных.
пои_
|
а6лпца
78
веденнь1х
в та6л.
78,
в.',и|:то
""1:*'"
1
Беличина
свободной
энергии
и напря){(ения
ра3ложения
для
!(омпонентов
хлоридно_фторидных
электролитов
хл-ориднь1х
'системах
[1с1
-
ц9|
_
0€13
или
[|с1-
кс1
_.
0€1д
уран
вь1деляется
на
ка-
тоде
до
начала
осах(дения
ще-
лочнь1х
металлов
-
калу1я
|'
лптия.
Фневидно,
оса)кдение
урана
и3
хл,о_ридн,о1фторидног()
электролита
[!€1-
кс1
-
{-}[,д
возмо)кно
лишь
при
условии'
если
фторид
урана
реагирует
с
хлоридами
щелочнь1х
метал-
лов
п'о
уравнениям:
0Р.*4[|€|+шс14+4!;Р,
0Р,
*
4кс1
_*
шс11+
4кР.
Б
хлоридн_ь:х
!асплавах
пр!|
электролизе
0€1ц
осах(дени10
урана
на
катоде
предшествует
1поре3аряд
его
четьтрехвалент-
А27о0'
к
ка!'/е-экв
г
"700'
к
в
кс1
||с1'
1/31_}613
1/4т']с14
-88000
-84000
-58500
---51500
3,8
3,6
2,5
,,
5,6
5,1
4,2
9:}!9!Ё{{
#"1
}."
ъ.
€".1!";ё3{#ЁЁ],
*!:
мической
системы;
величина
э.
д.
с.
равна
н-а-щ)я)кению
разложения при
п<!йно_**
1о]а.
тимости
данной
спстемы.
||г
кг
|
/ а|!Рд
-130000
-118000
-
98000
ъ
нь]х
ионов
до
трехЁалентньтх'
ное
о-пределение
по'тенциала
ш7ш-?
;ж:"ъ#,ъ:
Ёъъ?;ъ.;ж:
х<ет
бьтть
р-а-9считан
на
основании
ре3ультатов
определе,ния
по_
тенциалов
1_]3+/ш++
и
0/цз4.
Равновеснь:е
потенциаль]
урана
в
хлориднь1х
расплава
х
6ьтлп
исследовань1
многими
зарубе1йнь:ми
авторам,
|]Ё9,-1ы|{
6+.,-
их
работьт
отличаются
след!йщими
общйми
особенностями:
в
каче-
стве
основного
расплава
использовались
преимущественно
легко-
плавкие
эвтектические
омес'и:
кс1
-!1'с|
(,'л--';-"йвсБ+
+
шас1
+
кс1
(396.
с)
Фсновнь:м
нёдостатком
этих
смесей
является
их
заметная
ги_
гроскопичность'
что
вь1зь1вает
существеннь|е
ослох(н-"""
-,р,
,--
:|-ч9:,""х'
проводимь1х
с
электролитами'
содер>кащими
хло-
ридь|
урана'
в
свя3и
со
склонностью
последних
к
гйролизу.
.|1итпь
один
и3
авторов
[:оз:
йЁ"''"зовал
эквимолекулярну}о
"смесь
\а€1-
(€1
с
'боле1
"1'.'й'й_
."мпературой
плавления
(
663'
с
)'
но
отлич
ающуюся
ср
авнитель"ы
"ьй;;й.й'."!'рй.'.'*
-
ностью.
Б
качестве
электродов
сравнения
ра3ньте
авторы
исполь-
зовали
различнь1е
металлическиё
электродь:
(серебр"й,,._
и пла-
тиновые).
|1рименение
различньтх
электродов
затрудняет
срав-
н,ительную
оценку
даннь1х' полученньтх
разнь|ми
авторами.
кЁ"*"
того'
метал'лические
9лектродь1
обладают
существеннь1ми
недо-
,
!рон
статками'
перечислоннь1ми
!в
первой
главе'
которые
3начитель']!0
сних{ают
наде)кность
и
возмо>кность
и|спо.'!Б3Ф88,}1[19
получаемь1х
ре3ультатов.
|,илл,
|[ерано и
др.
[159]
,и3учали
электродные
потенциаль|
.для процоссов
1-]_> 1_)3+
и
{-)3*_>(){+
в
расплавленнь|х
хлоридах.
Б
качестве
раств,орителей
бьтли вьтбраньт
1перечисленные
вь|1пе
распла'влен]нь|е
э,втектические
смеси:
а) 590/0
(мол.)
[!с1
+
41%
(мол.)
|(€1,
температура
!плавления
355, с, ]'широко используе_
мая |в электрохимических
исследованиях
и б) 50%
(мол.)
м9с12+300/0
(мол.)
\а61*20%
(мол.)
(€1,
темп'ератураплав-
ления
396'
с,
вьтбранная в свя3и с
применением
ее
для
экстрак_
ции
продуктов
делену|я
|\з облуненного
урана.
|!ри измерон,ии
потенциалз в качестве элоктрод0в
сравнения
применяли
сере-
бряньтй (Ав-*А9+)
и
платиновь1й
(Р[--+Р|2+)
электродьт.
[ля
определония
потенциала
1_)3+--+
[-]{+ авторь:
и0по'льзова-
ли
метод амперомет|ри'ческого оки'сления т'рихлорида
урана
в
раоплаве.
14змерен,ия
пока3али' что 1полученньте закономерности под-
чиняются
урав'нению
Ёернста, а величинь1 потенциалов прак-
тически со'впадают
с
рассчитаннь]ми
на
основании
термодинами-
чееких
даннь1х
(та6л.
79) . 3,нанения
,потенциалов
в
ра3личнь|х
расплавлен,нь]х
системах с
ра3нь|ми
катионами практически не
1аблица 79
€равнение
величин потенциалов'
получаемь|х
в
ре3ультате
измерений,
с
величинами,
рассчитанными
на основании термодинамических
данных
при 459о
с
""'#"""'ж;*г#"г3}Ё*:Ёому
серебряному
||отенциал, с
€истема
Растворитель
электрод
сравнения
253
и3мерен-
|,"."'''"*-
ный
|
ны|1
ш/ш3+
0/ш3+
ш/ш3+
0/[]3+
цз*7ц+*
цз*7ц++
0
|\14+
ц/ц4+
ь1с1-кс1
]!1е€1'-1'{а€!-(€1
|-1с1
-
кс1
]!18€1'_1.]а€1
-(61
1-|с1
_
кс1
!!13€1'-}{а€1_(€:
|-|с1
-
кс1
$Ф1,
_
$а€1-(€1
-
1,61
-1,61
-2,25
-2,25
-1,25
-1
,30
-2,00
-2,01
-1,619
-1,619
-2,231
-2,23\
-0,835
-0,
835
-1,882
-1,882
|[риме ч^нп-я:
1._|{отепциалы
!т71-]4*рассвитаныпо
резу.гБтатам
измерений потенци.
алов т]1ц3* ц 94*7ц3*.
2. ||отенциальт
сере6ряного
электрода
сравнения
по отно!!]еник} к платиповому
соетав.
ляют:
измеренного
-0,
637
о,
рассхитанног6
_0,6
1
2 в.

зави,сят
от
природы-
111иона
раствор-ител_я. мох(но
та'кх(е
сде-
лать
вь|в'од'
что
п'ри
восстан0влении
ш4+
он
сначайа']Ёр-*'д''
в
(]3+
и
п.отом
воостанавливается
до
металла.
!.даоп_41ве'
загряз'ненном
кислородом,,||!,Ф||:€1Ф!ит
окисле_
ние
[)3+
и
ш4+
до
|}6+ (шо;+,1.
3то-прйв'д"..
й'",,|Ёйй}.
*'
*,-
тоде
совместно
с
металлическим
уран'ом
двуокиси
урана
((_}Фэ)-
(
п-осл'ччРму
выводу
при!|]ли
еще
рань!|]е
€мирн'ов
и
|4ва-
новокий
[160]'
которые
изунали
пРоцесс
анцдного
ра|створени'}
элоктродов
и3
двуокиси
урана
!
расплавлеттной эв^тейтической
смеси
хлоридов
л|1тпя
|4
|кал|1я.
Фпь:ты
:|1Ф(!13?./|!!я
что
в пределах
анодной
плотности
тока
0,01_|!0^'а|см2
^"'!
}а.!йй"""."
за
счет
перехода
в
расплав
ионов
цо22+
,которь|е
п!и
раз$яд;;;
;
тоде
дают
осадок
двуоки'си
урана
стехиометрического
состава.
^
Беличина
измеренного
потенциала
|}*{-]!+
,р'*""й.и
не
0тличается
от
расчетной,
в
то время
как
для
проц6еса
[-,з+
.-*
с|,+
различие
ме)кду
этими
величиц1ами
настолько
велико'
что
не
мо_
>кет
бьтть
отнесено
к
допустимо* о:пибкБ
,йБ!!Ёй}'а.'"А;;;;
предполагают'
что
это
расхо'(дение
объясняется^
образованием
устойнивого
хлооидного
комплекса
четь[рехвалентного
урана
[шс15]-
[159].
^--
|р-ч""
и.,0стеринг
для
системь:
0/(]з+
Б.
!8т€|1;18,3ленной
сме_
си 1\с1
-
11с|
с поименением
серебряного
электрода
срав'нения
при
450'
€ полуни)ти
величину
электр9дного
пот0нци
ала
|,294
в,
т.
е. значительяо
отл.ичающуюся
от
даннь!х
предьтдущих
авто_
ров
[161].
Б
более
ра'нней
работе
14нмана,
!,иллса
и
др.
[162]
бъ:ла
сде-
лана
.попь1тка
пр_едставления
механизма
элек!ролиза
распла.в-
ленной
системь]
!!с,1
-
кс1
-
0€13
на
основании
д',",,",
-й'_
лученньтх
ими
при
определении
3ависимости
величинь|
элек_
тРодного
потенциа-ла
уранового
электрода
в
этой
системе
(с
применением
серебряногоэлектрода
сравнения)
отконцентра_
1{ии
урана
в
электролите,
температурь:,
катодной
плотности
то-
ка
и
времени
процесса
в пределах
температур
440-540.
€.
14з-
ч?э+"
?чтРР4"]х<}щую
силу
цепи
ш/'(-]с13;!:с:
+
кс:/!
кс]
1
+!10!'
А9с||А8
|при
условии
ее
термодинамической
обратимо-
сти.
Фпьттьт
пока3али'_
-йто
изменение
электродвих<ушей
силь1
це_
::-
.-|::::уч1шией
0€13
происходит
в
соответствии
с
уравнени-.
ем
пернста.
пи)ке
пр'иводятся
'р.ассчитаннь[е
авторамй
на
осно-
вании
пров-еденнь1х
исследован;ий
величины
коэффициентов
ак_
тивности
0€13 при
различнь]х
моляр'нь|х
концентрациях
этоЁд
соли
в
расплавленной
системе
[!€|
_
кс1
-
шс13
'при
463.
€:
6.д*р*,*".
[!613,
молярвые
доли
1,7.10.-3
3,4.10-3
5,6.10*3
_
}(оэффициент
активности
5.
10_2
8.
10-2
'т
'|о-2
Авторьт
ука3ь|'вают,
чт9
в
соответствии
с
даннь1ми
€альстрома
в,сиетейе
[.;с:-
кс1-А9€1
не
прои,сходит
комплексообразо_
ва\|ия.
1(оэффишиент
активн0сти
в
!пир0ких
пределах
концентра-
шии
А9€1
равен
единице.
0тти
предполагают'
что
в системе
|!с1-
кс1-
1-]€1з
коэффишиентьт
2:(?|{'БЁФ€1[
Б€€[
индивиду'
альнь1х т]{пов
ионов'
вййючая
ш3+,
такх(е
равнь|
единице'
||о-
этому
,на
основани1и
приведеннь|х
вы1ше
данны-х
||!итн}1}12€1'ся'
что
в
ук6занной
системе
ймеет
место
(Ф]у1:||.'|€(€Ф-Фбразование
трехва-
лентного
урана
с
получением
со9ди,нения
1(э{-]€15,
кото!о'м}
со-
ответствует
ан,ион
шс1|_;
уравнение
дисооциации
этого.
ком,п-
лек'са
следующее|
,,.'2_:тт^1
'
о!
0с13-
?0с13
+2с:_.
Авторь:
[162]
раосн|,|талп
такх(е
кон'станть]
диссоциации
это-
го
ком|п;екёа
(
''
величинь1
и3менения
свободной
э'нергии
его
образования
при
температуре
463'
€
(табл. 80)'
таблица
80
[арактеристика
комплексного
аниона
шс|3-
-4,2
-3,7
\илл и
др.
[159]
считают
этот
вь1вод
о':пибочньтм
и
предпола_
гают,
что
*'','-*.''бр','"'"'"
имеет
место
лийь
для
0{+'
Авторьт
[162]
приходят
к
вь|воду'
что
на
катоде
во3мо)ке|{
первинн!тй
разряд
как
1-]3*,
так
и
!|+, в
зависимости
от
концен'
трации
этих
ионов,
катодной
плотности'
тока
и
других
факторов'
Ё'
,*
дан|нь1м'
при
температуре
450"
с
потенциал
вь1деления
)1(идкого
лития
на катоде
составляет
-2,4
в;
урана
из
1]'+-
1,33'
а.
|1реАполагается'
что
при
первич|н'ом
вь|делении
урана
полунаются дендрить],
п-рочно
свя3аннь1е
€
1(316!0\{'
в
то
вре-
мя
как
тонко
д"сперс"ь:й
пороттток
урана'
осыпающийся
с
като-
да,
вь|деля€1€9
;8
результате
вторинной
реакции
во'сстановления
{_}€13 литием'
вь|деляющимся
на
катоде'
_
-{шебетовский
и
1(иш;
[164]
та'к>ке
определяли
величинь]
раР!9:
веснь1х
потенциалов
ш3+/ш4+
и
ш/ш3+
в
расплаве
!(01
-
|1ь|
;;;';;;;;;й']р."
зтт ьт1.
с_
при
этом
для
,системы
0/03+
при
400"
с
бьтла
полунена
величи1на
равнове0н1ого
потенциала
о'тноси_
€одеря<ание
!€|"'
молярные
долп
з'+':о_3
_з
5.6.
10
-

тельно
'серебря.ного
электрода
-1,587
в'
а
для
системы
ш3+/ш4+
при
40'0'с
-0,186
в.
Бьтчйсле"",,й'.Б.."
циал
для
системь[
0|ц++
состав'ил
-|'236
в.
-
Фленга,с
[163]
в
_,отличие
от
,ра;бот,
проведен|нь|х
пер,ечисле'н-
]ь!ми
вь]|пе
ав.тора'ми'
примвнял
в
к]чест"е
эл'ектролита
экви_
Ё:1'Ё|#ё'Ё'/;:#;'#ж,у#т#;,*.]|#,.':;|т,Р'#6*ё
по,отно'[]ен;!!1Ф
|(
39Р,€|брян'ому
элект|:олу'сравнения
(та:бл.
в1).
256
3лект
{_]/ш3+
ц3*7ц++
0/ш4+
Результаты
измерений
потенциалов'
'
'аблица
81
67о
-1
,563
-0,494
-\,295
-1,554
-0,483
-1
,285
*1,519
-0,459
-1,252
*!
,502
-0,450
-
1
,233
800
|{р
и
ме ч ан
п
е.
|{отенциалы
[.]7{-]4+р'."',""""',
лов
цепей
|]/|э3*
ц о/ц4*'
результатов
и3мерений
потенцпа
ста'ндартнь1й :поте'нциал
системы
ш/шс14
[
кё:
+
нению
бьтл
ра,с,считан
\а€1!
по
урав.
0шс:.:
3Ё,'с,"
*
Ё,",,/,",.
(табл.
61).
|1ри
определении
потенц-и^а_ла
ш3+/ш4+
'как
1тпебетовский
и
5тч[|о+:'_так
|! Фленгас
{]6э'_
},р"|"-"''''.
что
.'''"'?Ё"'Ё
ш3+/ш4+
остается
та,ким
х<е,
ка'к
в
исходн0м
расплаве.
Б
,овязи
с
тем
что
трехвалёнтньтй
ура}1
легко
оки'сляется
до
вьтс1пих
валентностей
да>ке
пр"
'а'инй,
с'"до'-
'*"!,й'.'.а
"
эл'ектролите'
применени,е
такой
методики
,не
об'ес,печй!!Ё!
'''у-
чения
наде)кнь}х
ре3ультатов.
(;ми!нов}
и €пкибе
[165,
166]
в
своих
обтпирньтх
исследова_
ниях1
.
п|ос'вященнь1х
электрох.уйии
ра|сплав.ов'
ё'д"р".}ййх
хло-
ридь|
урана
в
расплаБ"1|;0н[Фй
смеси
хлор|идо|в
,натрия
\4 калия.'
удалось
ив'бе:кать
осло)кнений,
имевших'место
'
"Ё-'*дБ,
ан14ях
119у!ех<'ных
авт'оро'в.
€
целью
"',"1!','."'"
полученньтх
ими
результато'в
с приведеннь1ми
вь||пе
данньтми зарубех<ньтх
ав,то_
ров
рабо'тьт
рассматриваются
" '"'''Ё'зделе'
хотя
описание
тех-
цологических
процеосов
9лектролиза
1со
!!е{ней
темпера!урой
и
применение,м
расплавленной
|меси
шас[
+-(ё:
-
,Ёй,.'д;"."
в
1емпература.
'€
!ран
о(1
следующем
ра3деле.
||ри определёнии электродн'ого'потенциала
[-]3+/ш4+
авторы
исполь3овали
метод п!отенциометричеокого
окис-
л'ения
хл'орида
урана
в
расг1ла|в'е'
в
]свя3и
с
чем
ФЁ!{
й;€(.г{1Ф9й"т|:й
о1пи'бки,
/свя3а|н'нь1е
'с
окислени',ем
трехвал0}{1ЁФ:|Ф
ура1на
в
|про-
цессе
и3мерений.
Б качестве основно1го
ра10плава
авторь1
ис-
поль3овали
мало1гигроскопич,ную
экви'молекуд'9;р;н}ю
,смесь
}'[а€1
-
|(€1.
Равновеонь1е
г[отенциал^ь1
в
сис1теме |}/цз+
изучали
в
1пиро,ком
интер'вал,е
тем|ператур
700-930'€
п;ри и3,менени'и
'со-
дер)ка1ния
[-},€13
в
ра,сплаве
'от
0,5
до
28,6}9
(вес.).
Бьтло
уста_
новл'е|но'
что
в
исследован1ном
и|н'тор'ва'ле
|концентраций
для
рав-
но|вес|ного
потенциала
урана
спра1ведлив'о
ура'вн|ен,ие
Ёер'н'ста:
Ё
:
Ёоуоз+
+
''^'5'
1е
[{-]'+]
ч|ч
3л
Ёа
осн+овании
полученнь1х
ре3ультатов
бьтли
,вь]чи|слень|
теп'
ло'ть[
плавления
!-}€1з и с]мо[пения
его
,с
расплавом
]']а€1
+
(€1.
1(роме
т'ого,
.
бьтли
о|пр^еделень1,окислительно-во'сста,н'овительнь]е
потенциаль1
системь1
ш3+/ш4+
в
'расплаве
кс1
-
].'}а,€1
в
интерва-
ле т'емпе]ратур
690-600'
€.
|1олунено следующее
уравнени|е
тем-
пературн,ой
зависим,ооти
величинь1
Ё'з17ц++ :
Ё"..
,3
.
10_4т.
-о3*/ш{*:1,906+4,8
Ёа основа,нии полученнь|х
ре3ультат1ов
бьтла
вьтчи€.[:ёЁ&
[€]!1-
пер атур ная 3
ави'си мость
р
авн
овес'но'го
1потен
циа
ла си|стемь|
0/ц++
в
том
)ке
ра|спла1ве:
Ё,уу'+
_
-
2'434+
6'14' 10_4г'
а
та,к)ке
вь1числень1'и3менения
тер
моди'намических
вел''пчи'н
(А7,
^н, ^5)
,при
см|е1п'ении
)кидкого
тетрахлорида
с
распла'во}1
!.,1а€1
-
(61.
д'19рь1 пр}оизвели
сравне)ние
ре3ульта'то|в,
полученнь1х
зару-
6е>кньтми исследователя'ми,с'получе'н'нь1ми
им]и
ре3ультатами'
с
пересчетом
всех
дан1!ь]х
на
величину
потенциала
{)/[)3+
отно-
ситель|1{о
[л0р'ч91' электроща
сравнения
для
температур
400 и
450" с.
(ак
видн,о
из табл. 32,
р'езультать1'
'п,олученньт1е
€мирновьтм
и
6'киба,
луч11]е всего
,еогласуются
с
результа'та'ми
Флен;га,са
[163],
\илла
и
др.
[159].
Результ атьт
и3
п{ерения
р
ав'новесн
ьтх,потенци алов 1-13+/|}{*,
по-
лучен
нь1е
р
а3личнь1
ми иоследов
ателями с
пер'есч1етотй
!,?'}1ЁБ1[
Ф}-
но1с]ителнно
хл,ор'но|го
эл,ектрода
сравне'ния
при
450', прив,едень]
в
табд.
63.
Бсли
унесть ра3личнь1й
соста,в
растворителя'
то
даннь|е'
по-
лучен|нь|е
€мирно'вым
и
(ки,6а,
вполне
удовлетворительнр
согла-
[/
5,аказ
!б//
