Чугаев Л.В. Металлургия благородных металлов
Подождите немного. Документ загружается.


Осмий и рутений, которые имеют восемь внешних электронов,
способны к проявлению максимальных степеней окисления VII и VIII
(особенно с кислородом и оксигалогенидами). Степень окисления VI,
характерная для рутения, осмия и лишь иногда для платины, иридия
и родия, реализуется, главным образом, в кислородных соединениях.
Для рутения, осмия, платины н иридия наиболее характерна степень
окисления IV, для родия — III, хотя степень окисления III довольно
часто встречается в соединениях рутения и иридия. Низшие степени
окисления (II, I) у родия, рутения, иридия, осмия встречаются реже.
В основном они характерны для их соединений с органическими ли-
гандами. Степенп окисления I и 0 у всех платиновых металлов реа-
лизуются весьма редко, главным образом, в карбонильных соединениях.
Благодаря высоким зарядам, небольшим ионным радиусам и на
личию незаполненных d-орбиталей платиновые металлы представляют
собой типичные комплексообразователи. Так, в растворах все их со-
единения, включая простые (галогениды, сульфаты, нитраты), превра-
щаются в комплексные, поскольку в комплексообразовании участвуют
ионы соединений, присутствующих в растворе, а также вода. Поэтому
гидрометаллургия платиновых металлов основана на использовании их
комплексных соединений.
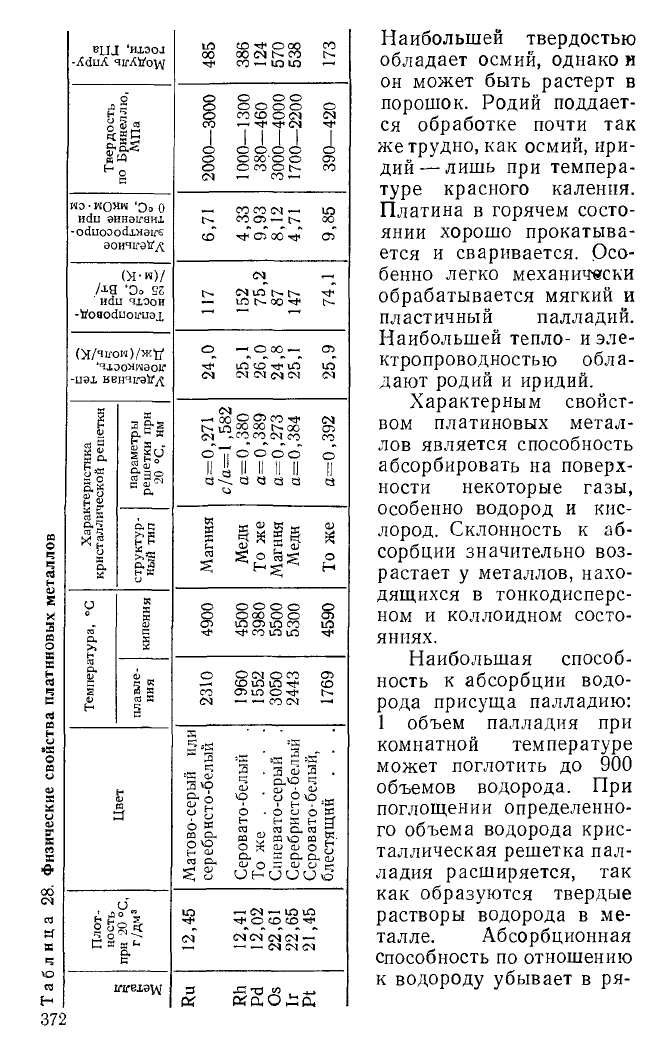
§ 2. Физические свойства
Физические свойства металлов платиновой группы весьма
сходны между собой (табл. 28). Это очень тугоплавкие и
труднолетучие металлы светло-серого цвета разных оттен-
ков. По плотности платиновые металлы разделяют на лег-
кие (рутений, родий, палладий) и тяжелые (осмий, иридий,
платина). Самые тяжелые металлы — осмий и иридий, са-
мый легкий — палладий.
Платина, палладий, родий и иридий кристаллизуются в
гранецентрированные кубические (г. ц. к.) решетки. Кри-
сталлические решетки осмия и рутения — гексагональные с
плотной упаковкой. При воздействии на растворы солей
восстановителями платиновые металлы могут быть полу-
чены в виде «черни», обладающей высокой дисперсностью.
Температуры кипения и плавления металлов в обеих
триадах убывают слева направо — от рутения к палладию
и от осмия к платине, и снизу вверх по вертикали в перио-
дической системе. Наиболее тугоплавкие осмий и рутений,
самый легкоплавкий — палладий. Температуры кипения
платиновых металлов очень высокие. Однако при прокали-
вании на воздухе рутений постепенно, а осмий быстро уле-
тучиваются вследствие образования летучих тетраоксидов.
Наблюдается также улетучивание платины (начиная с
1000 °С), иридия (с 2000 °С) и родия, объясняемое образова-
нием летучих оксидов.
Осмий, рутений, иридий и родий очень тверды и хрупки.
27—7 Об
371
BJJJ 'H130J
•XdnA
4irAtfow
"I
In
II
й
bo
с
WD-MOHW 'Эо 0
Hdo эинэггаш.
oduooodiMaire
эоичтай^
(М-и)/
Ая 'Эо SZ
Hdu '!100Н
-i/oaodnoriio [.
ОТ/чц-оиО/ж^
irai венигай^
я
a
X
ч
VD
«
н
372s
a
5
cs к;
X2
3 frs
&ao
с ш
01
>,=3
е-й
H X
U
^
f
2
^
s
050^
чб"-?
С
я я
ю
00
Th
CD Th
О aO
00 IM
CO
CO — Ю Ю
CO
N
О
0 00
О
0000
0
О
CO CD О (M
IM
СО
1 1 I 1 1
Th
1
1
о
II II
OOOO
1
0
о
О OO'O
0 CD
о
OP) ON
CO
<м
« CO-
—
со со сч —
щ
N WOl
—
N 00
CD
CD 00 Tf
CD
N
СЧ in N N
— lOSGOrf
к
5 «
3
« OJ
3
VD
О
ш
м
V
о
О W
М Он
О VO
н <и
Л
Он
^ OJ
О
— О 00 —
CD
in
CD Tf
in Ю
IM
СЧ СЧ iM СЧ
<М
<м
„ „
00
с
СО тР
t-
m 22
00
t-
00
<M
.со со сч со
а сз а а
IM
CD
со
о
5 £ 5 *
о
н
о о о о о о
О О
СО О О
О
CD
1П ОЭ 1П со
ю
со in in
тр
О СЧ О СО
CD
CD in in TP
CD
CD Ю О TP
N
— — CO СЧ
—
•n
4
aj
Ю
о
>K
ч
«
. 3 0J л
OHVO 4
.
ш А
ш
о Oo
• о
«
и о
w
S h Я
M
s
no n £
a> ш
о г;
К
О. О, ш
" " " ч
о UhUUUo
-нМ-ЮЮ
Th О CD CD те
<М
<М IM <м —
— — (М СЧ СЧ
3
OS
•Я "О
X
LH
"•">
«cuOia.
Наибольшей твердостью
обладает осмий, однако и
он может быть растерт в
порошок. Родий поддает-
ся обработке почти так
же трудно, как осмий, ири-
дий—лишь при темпера-
туре красного каления.
Платина в горячем состо-
янии хорошо прокатыва-
ется и сваривается. Осо-
бенно легко механически
обрабатывается мягкий и
пластичный палладий.
Наибольшей тепло- и эле-
ктропроводностью обла-
дают родий и иридий.
Характерным свойст-
вом платиновых метал-
лов является способность
абсорбировать на поверх-
ности некоторые газы,
особенно водород и кис-
лород. Склонность к аб-
сорбции значительно воз-
растает у металлов, нахо-
дящихся в тонкодисперс-
ном и коллоидном состо-
яниях.
Наибольшая способ-
ность к абсорбции водо-
рода присуща палладию:
1 объем палладия при
комнатной температуре
может поглотить до 900
объемов водорода. При
поглощении определенно-
го объема водорода крис-
таллическая решетка пал-
ладия расширяется, так
как образуются твердые
растворы водорода в ме-
талле. Абсорбционная
способность по отношению
к водороду убывает в ря-

ду: Pd>Ir>Rh>Pt>Ru>Os. Абсорбированный водород
может быть удален при нагревании металлов до 100 °С
в вакууме. Легче всего он удаляется из палладия, труднее—>
из платины и, особенно, иридия.
Платина (особенно платиновая чернь) довольно сильно
поглощает кислород: 100 объемов кислорода на один объем
платиновой черни. Палладий и другие платиновые метал-
лы поглощают кислород значительно меньше.
Вследствие способности к абсорбции газов платиновые
металлы, главным образом, палладий, платина и рутений,
применяют в качестве катализаторов при реакциях гидро-
генизации и окисления. Каталитическая активность их уве-
личивается при использовании черни. Осмий также облада-
ет высокой каталитической активностью, но осмиевые ката-
лизаторы легко отравляются.
§ 3. Химические свойства
Для платиновых металлов характерна высокая стойкость
по отношению к химическим реагентам, которая для разных
платиновых металлов проявляется по-разному. Более того,
стойкость этих металлов в большой степени зависит от сте-
пени их дисперсности. Если компактные платиновые метал-
лы весьма стойки к различным реагентам, даже при повы-
шенной температуре, то дисперсные формы металлов актив-
но взаимодействуют с различными окислителями, особенно
при повышенной температуре.
Платина. При обычной температуре платина не взаимо-
действует с минеральными и органическими кислотами.
Серная кислота при нагреве медленно растворяет платину.
Полностью платина растворяется в царской водке:
3Pt + 4HN0
3
+ 18НС1 ^3H
2
[PtCl
6
] + 4NO + 8Н
2
0. (239)
При повышенных температурах платина взаимодейст-
вует с едкими щелочами, фосфором и углеродом.
С кислородом платина образует оксиды (II), (III) и
(IV): РЮ, Pt
2
0
3
и РЮ
2
. Оксид Р10 получается при нагре-
вании порошка платины до 430 °С в атмосфере кислорода
при давлении 0,8 МПа. Оксид Р1г0
3
можно получить при
окислении порошка металлической платины расплавленным
пероксидом натрия. Оксид РЮ
2
— порошок черного цве-
та— получается при кипячении гидроксида платины (Щ
со щелочью:
2Pt(0H)
2
^Pt0
2
+ Pt + 2Н
2
0.
373s

Гидроксид платины (IV) можно получить осторожным
прилнванием щелочи к раствору хлороплатината калия:
K
2
tPtCl
6
l + 4KOH^tPt(OH)
4
+ 6КС1.
Сернистое соединение PtS — порошок коричневого цве-
та, не растворимый в кислотах и царской водке; PtS
2
—
черный осадок, получаемый из растворов действием серо-
водорода, растворимый в царской водке.
Хлориды платины часто используют в гидрометаллур-
гии и аналитической практике. При 360°С воздействием хло-
ра на платину можно получить тетрахлорид PtCl
4
, который
при температуре выше 370 °С переходит в трихлорид Pt'Cl
3
,
а при 435 °С распадается на хлор и дихлорид PtCb, раз-
лагающийся при 582 °С на хлор и металлическую платину;
PtCi
2
растворяется в слабой соляной кислоте с образованием
платинисто-хлористоводородной КИСЛОТЫ Н
2
[PtCl
4
], при
действии на которую солей металлов получаются хлоропла-
тиниты Me
2
[PtCl
4
] (где Me— К, Na, 1\
т
Н
4
"и т.д.).
Тетрахлорид платины PtCI
4
при воздействии соляной
кислоты образует платинохлористоводородную кислоту
H
2
[PtCl
6
], Соли ее — хлороплатинаты Me
2
[PtCI
6
]. Практи-
ческий интерес представляет хлороплатинат аммония
(NH
4
)
2
[PtCl]e — кристаллы желтого цвета, малораствори-
мые в воде, спирте и концентрированных растворах хлорис-
того аммония. Поэтому при аффинаже платину отделя-
ют от других платиновых металлов, осаждая в виде
(NH4)
2
[PtCIa]
•
В водных растворах сульфаты легко гидролизуются,
продукты гидролиза в значительном интервале рН находят-
ся в коллоидном состоянии. В присутствии хлорид-ионов
сульфаты платины переходят в хлороплатинаты.
^ Палладий химически менее стоек, чем платина. Он раст-
воряется в горячей серной и концентрированной азотной
кислотах:
Pd + 2H
2
S0
4
^PdS0
4
+ S0
2
+ 2Н
2
0;
Pd + 4HN0
3
5tPd(N0
3
)
2
+ 2N0
2
+ 2H
2
0.
С кислородом палладий образует оксид PdO, который
при повышении температуры диссоциирует по уравнению
4Pd0^2Pd
2
0 + 0
2
При температурах выше 870 °С палладий полностью вос-
станавливается. Диоксид Pd0
2
темно-красного цвета, силь-
ный окислитель, медленно теряющий кислород уже при
комнатной температуре. При 200°С Pd0
2
разлагается на
374s

PdO и кислород; Pd0
2
образуется при обработке Me
2
[PdCl
6
J
щелочами.
Из соединений палладия с серой известны PdS и PdS
2
.
С селеном и теллуром палладий образует соединения PdSe,.
PdSe
2
, PdTe и PdTe
2
.
Дихлорид палладия PdCl
2
получается из элементов при
температуре темно-красного каления. При растворении пал-
ладия в царской водке образуется тетрахлорид палладия,
образующий с соляной кислотой палладохлористоводород-
ную кислоту H
2
[PdCle], которая при кипячении переходит»
палладистохлористоводородную кислоту:
H
2
[PdCl
6
]^H
2
[PdCl
4
] + С1
2
.
Соли этих кислот — хлоропалладаты Me
2
[PdCl
6
] и хло-
ропалладиты Ме
2
[PdCl
4
],
Сульфат палладия PdS0
4
-2H
2
0, получаемый растворе-
нием палладия в серной кислоте, подвергается гидролизу с
образованием Pd(OH)
2
. В присутствии соляной кислоты он
переходит в H
2
[PdCI
4
]. Известен нитрат палладия Pd(N0
3
)
2
.
Аммиачные соединения характерны для двухвалентного
палладия. При добавлении избытка аммиака к раствору
хлоропалладита получается тетраминхлорид:
(NH
4
)
2
[PdClJ -i- 4NH
3
^[Pd(NH
3
)
4
]Cl
2
2NH
4
C1.
Если к этому раствору добавить хлоропалладита, то вы-
падает красный осадок соли Вокелена:
[Pd(NH
3
)
4
]Cl
2
+ (NH
4
)
2
[PdCi
4
]^[Pd(NH
3
)
4
] [PdCl
4
] + 2NH
4
C1.
При осторожном добавлении соляной кислоты к раство-
ру тетраминхлорида выпадает светло-желтый мелкокрис-
таллический осадок хлоропалладозамина:
[Pd(NH
3
)
4
]Cl
2
+ 2HCl5t[Pd(NH
3
)
2
Cl
2
] + 2NH
4
Cl.
Соль мало растворяется в воде, что используют при от-
делении палладия от других платиновых металлов.
При прокаливании хлоропалладозамины разлагаются:
3[Pd(NH
3
)
2
Cl
2
]^3Pd + 2НС1 + 4NH
4
C1 + N
2
.
Иридий не взаимодействует с кислотами, щелочами, да-
же царская водка не растворяет компактный иридий. Обыч-
но порошок иридия растворяют спеканием с пероксидом
бария или натрия с последующей обработкой спека соляной
кислотой или смесью соляной и азотной кислот.
Из кислородных соединений иридия наиболее известны
оксиды 1г
2
0
3
и 1г0
2
. Оксид иридия (IV) —сине-черный по-
рошок с металлическим блеском, растворимый в кислотах,
375s

получается из гидроксида 1г(ОН)
4
нагреванием до 350 °С.
Оксид иридия (III) —порошок черного цвета, не раствори-
мый в соляной кислоте и царской водке. Гидроксиды ири-
дия получают из солей иридия (III) и (IV) осаждением
щелочами при нагревании.
При пропускании сероводорода через раствор солей
иридия при 100 °С и выше выпадает осадок тиоиридатной
кислоты H
3
IrS3(Ir
2
S3-3H
2
S). При воздействии на иридий
хлора в зависимости от температуры получаются хлориды
IrCl, IrCl
2
, IrCl
3
. Хлорирование в водных растворах позво-
ляет выделять хлороиридаты
Нг[1 гС1
6
],
которые легко вос-
станавливаются до хлороиридитов Нз[1гС1б]. Эти соедине-
ния в водных растворах легко гидролизуются и переходят
в аквогидроксохлорокомплексы, которые с большим трудом
выделяются из растворов.
Из солей иридийхлористоводородной кислоты большое
значение при аффинаже имеет хлороиридат аммония, ис-
пользуемый для отделения иридия от других платиновых
металлов.
Желтый сульфат иридия (III) состава Ir
2
(S04)3-.rH
2
0
получают растворением гидроксида иридия (III) в серной
кислоте без доступа воздуха. В водных растворах сульфа-
ты иридия находятся в виде сложных аквогидроксосульфат-
ных комплексов, причем состав их значительно меняется в
зависимости от способа получения, поэтому определение
форм нахождения иридия в сульфатных растворах — чрез-
вычайно сложная задача. Обычно наиболее устойчивы мно-
гоядерные сульфаты иридия с разным соотношением атомов
иридия, находящихся в различной степени окисления (III,
IV). Изучение сульфатов иридия необходимо для построе-
ния рациональной технологии извлечения этого металла из
технологических растворов первичного обогащения шла-
мов.
Родий. Так же, как иридий, родий — малоактивный ме-
талл и в компактном виде не растворяется в царской вод-
ке. С кислородом он образует соединения Rh
2
0
3
и Rh0
2
.
При пропускании сероводорода через раствор родиевых со-
лей образуется сернистый родий RI12S3, который при нагре-
вании в токе кислорода или воздуха разлагается с образо-
ванием металлического родия.
Хлорид родия RI1CI3 при растворении в соляной кислоте
образует родиевохлористоводородную кислоту H
3
[RhCl6].
Однако ион [RhCl
6
]
3
~ подвергается акватации уже при кон-
центрации хлор-иона, меньшей 6 М:
376s

[RhCl
6
]
3
- + Н
2
0ч^[ Rh(H
2
0)Cl
5
]
2
~ + СГ.
При рН>2,9 начинается процесс гидролиза родиевых
комплексов:
[RhCl
6
]
3
~ пН
2
0 5t[Rh(H
2
0)„_i (ОН)С1,^
п
1
:3
- + «СГ + Н
+
.
Поэтому в водных растворах трихлорид родия может
существовать в виде катионных, анионных и нейтральных
аквогидроксохлорокомплексов. Такое многообразие форм
затрудняет выделение этого металла из раствора обычны-
ми гидрометаллургическими методами.
Аналогично ведут себя соли родиевой кислоты — хлоро-
родиаты (Na
3
[RhCl
6
], Кз[ИЬС1
6
] и т. д.). При обработке хло-
рородиата аммония нитритом натрия образуется
Na
3
[Rh(N0
2
)6]- Добавка хлористого аммония к раствору
этой соли вызывает выпадение практически нерастворимо-
го аммонийнатриевого гексанитрита родия:
Na
3
[Rh(N0
2
)
6
] - 2NH
4
Cl^(NH
4
)
2
Na[Rh(N0
2
)
6
] + 2NaCl.
При взаимодействии Na
3
[Rh(1\Ю
2
)б] с NH
4
OH образует-
ся триаминнитрит родия:
Na
3
[Rh(N0
2
)
6
] + 3NH
4
0ffi±2[Rh(NH
3
)
3
](N0
2
)
3
+
+ 3NaN0
2
+ 3H
2
0,
который, взаимодействуя с соляной кислотой, дает мало-
растворимый трнаминхлорид родия:
2[
Rh(NH
3
)
3
](N0
2
)
3
+ 6НС1ч^2 [ Rh(NH
3
)
3
Cl
3
] + ЗН
2
0 +
+ 3N0
2
+ 3NO.
Прокаливание триаминхлорида позволяет получить по-
рошок металлического родия. Все приведенные выше реак-
ции используют на аффинажных предприятиях.
Сульфаты родия в водных растворах, как и хлориды,
акватируются и гидролизуются, поэтому в сульфатных рас-
творах родий, так же как иридий, находится в виде катио-
нов, анионов и нейтральных акво- и гидроксосульфатных
комплексов типа:
[Rh
n
(OH)
m
(H
2
0)
6
^J
:v,
~
m
;
[Rh
n
(0HUH
2
0)(S0
4
)/'
,
-'
n
-
2
*.
Рутений. В отсутствие кислорода воздуха на рутений не
377s

действует даже царская водка. Однако содержащая кис-
лород соляная кислота медленно растворяет рутений. По-
рошкообразный рутений полностью переходит в Ru0
2
при
прокаливании в струе кислорода. При температуре выше
600°С образуется летучий тетраоксид рутения Ru0
4
—
сильный окислитель.
Дисульфид рутения RuS
2
может быть получен осажде-
нием сероводородом из рутениевых солей или непосредст-
венным взаимодействием элементов. Выше 1000 °С начина-
ется распад этого соединения на металл и серу. Селенид и
теллурид рутения RuSe
2
и RuTe
2
очень похожи на сульфид,
но менее устойчивы. Трихлорид рутения RuCl
3
образуется
при действии хлора на Ru(OHb, дихлорид RuC]
2
— при
взаимодействии хлора с металлическим рутением. Тетра-
хлорид рутения RuCl
4
— непрочное соединение, разлагает-
ся, отщепляя хлор.
Комплексные хлориды рутения — MeofRuCU],
yMe
4
[Ru
2
OClio] и Me
2
[Ru(H
2
0)CI
5
] — образуются при по-
глощении тетраоксида рутения соляной кислотой. Однако в
зависимости от концентрации соляной кислоты и времени
ее взаимодействия с Ru0
4
могут образоваться самые раз-
личные промежуточные соединения. Комплексные анионы
рутения легко гидролизуются и акватируются с образова-
нием различных аквагидроксохлорокомплексов. Трехва-
лентный рутений в водных растворах образует также легко
акватируемый и гидролизуемый комплекс [Ru(H
2
0)Cl5]
2
^.
Поэтому в реальных хлоридных растворах рутений может
находиться в виде нейтральных, положительно и отрица-
тельно заряженных аквагидроксохлорокомплексов.
Те же самые процессы акватации и гидратации проте-
кают в сульфатных растворах, содержащих рутений. Обыч-
но в сульфатных растворах присутствуют многоядерные
полимеризованные аквагидроксокомплексы рутения (III) и
(IV). При этом в растворе находятся одновременно катион-
ные, анионные и нейтральные комплексы этого металла.
Поэтому выделение рутения из подобных растворов чрез-
вычайно затруднено.
Осмий. Порошок осмия легко окисляется кислородом
до тетраоксида 0s0
4
, который восстанавливается различ-
ными органическими восстановителями до диоксида 0s0
2
.
Дисульфид осмия OsS
2
может быть получен аналогич-
но RuS
2
. Для осмия, как и для рутения, характерно образо-
вание OsSe
2
и OsTe
2
.
Тетрахлорид осмия OsCl
4
получается при хлорировании
осмия. Одновременно может быть получен трихлорид OsCl
3
.
378s

При сплавлении металлического осмия со смесью щелочи к
пероксида натрия (или бария) получается осмиат натрия^
который при растворении в соляной кислоте образует ком-
плексный хлорид осмия:
Na
2
[0s0
4
] + 8HCl5±Na
2
[OsCl
6
] + Cl
2
+ 4Н
2
0.
Это соединение можно восстановить соляной кислотой
до Na3[OsCl
6
]. Свойства водных растворов комплексных
хлоридов осмия напоминают свойства рутениевых комп-
лексов.
В аффинажных операциях большое значение имеет соль
Фреми [0s0
2
(МНз)4]С1
2
, которую получают по реакции:
K
2
[OS0
4
] + 4NH
4
C1^[0S0
2
(NH
3
)
4
]C1
2
+ 2КС1 + 2Н
2
0.
При прокаливании этой соли получается металлический
осмий.
Глава XXII
ПОВЕДЕНИЕ ПЛАТИНОВЫХ МЕТАЛЛОВ
В ОБОГАТИТЕЛЬНЫХ ОПЕРАЦИЯХ
§ 1. Формы нахождения платиновых металлов в рудах
Формы нахождения платиновых металлов в рудах опре-
деляют их поведение в последующих процессах обогаще-
ния. Поэтому их изучение имеет большое значение для вы-
бора технологической схемы переработки платиносодержа-
щих руд н концентратов. В этом разделе мы остановимся
только на основных минералах платиновых металлов, оп-
ределяющих их поведение в последующих процессах, не за-
трагивая глубоко все природные минералы платиновых ме-
таллов.
Металлы платиновой группы мало распространены в-
природе. Они встречаются как в коренных, так и в россып-
ных месторождениях.
Подсчеты содержания платиновых металлов в земной
коре были выполнены Кларком и Вашингтоном, а позднее
И. и В. Ноддак. Первые принимали в расчет только те пла-
тиновые металлы, которые находятся в россыпях и корен-
ных ультраосновных породах, а вторые учитывали также
платиновые металлы, находящиеся в рассеянном состоянии.
Иногда пользуются данными по распространенности пла-
тиновых металлов, приводимыми Гольдшмидтом. Обобще-
ние ряда исследований на основе многочисленных опреде-
лений дано А. П. Виноградовым.
379-'

Т а б л и ц а 29. Содержание платиновых металлов в земной коре, %
Металл
По Кларку
и Вашингтону
По И. и
В. Ноддак
По Гольд-
шмидту
По А. П.
Виноградову
Платина ....
1,2-Ю-
8
5-10—
8
1 •
Ю-
3
5 -10—
7
Палладий . . . 6-Ю-
9
5- ю-
6
5-10—
9
МО-
6
Иридий ....
5-Ю-
10
МО-
6
1 •
ю-
8
1 •
10—
7
Родий
1-Ю-
10
МО-
6
1 •
10—
8
1 •
10—
7
Осмий
9-Ю-
10
5-Ю-
6
ью-
8
5-Ю-
6
Рутений .... 3,6-10-"
5-Ю-
6
МО-
8
5-'10-'
В табл.29 приведены сводные данные о содержании пла-
тиновых металлов в земной коре по Кларку и Вашингтону,
И. и В. Ноддак, Гольдшмидту и А. П. Виноградову.
Месторождения платиновых металлов разделяют на два
основных типа: 1) связанные с ультраосновными породами
(преимущественно дунитами); 2) содержащие, главным об-
разом, в основных породах (иоритах, габбродоллеритах)
скопления сульфидов меди, никеля, железа. Месторожде-
ния первого типа особенно широко представлены в преде-
лах Урала, а второго— (медно-никелевые) в Садбери (Ка-
нада) и Норильске. Дунитовые месторождения находятся
также в Южной Африке, Колумбии, США и других стра-
нах.
Платиновые месторождения. К собственно платиновым
относятся коренные и россыпные месторождения Колум-
бии и др. Поскольку в настоящее время основная масса
платиновых металлов добывается из сульфидных медно-
никелевых руд, эти месторождения потеряли свое значение.
В уральских месторождениях минералы платиновых
металлов генетически связаны с глубинными ультраосновны-
ми породами, главным образом, с дунитами. Платинусодер-
жащие россыпи образуются в результате размыва, разру-
Таблица 30. Средний состав уральской россыпной и коренной
платины, %
Тип месторождения
pt
Ir
Fe
Си Ni
Pd
Rh
Os
Россыпная
Коренная
Средний состав аффини-
руемой платины . . .
77,5
76,7
78,4
7,8
3,6
2,95
14.0
13.1
2,8
5,1
0,1
0,3
0,1
0,33
0,6
0,6
0,5
2,0
0,41
380s
