Буканова Е.Ф. Коллоидная химия ПАВ. Часть 1. Мицеллообразование в растворах ПАВ
Подождите немного. Документ загружается.


площадь поверхности, приходящуюся на одну молекулу ПАВ в мицелле. Но
уменьшение площади поверхности мицелл при их асимметризации может быть
следствием как уплотнения расположения молекул ПАВ в несферических
структурах, так и агрегации ("слипания") сферических мицелл друг с другом. Ответ
на этот вопрос могут дать исследования внутренней структуры мицелл.
Таблица 3.2
Размеры мицелл в растворе нафтената магния в CCl
4
, полученные по данным
светорассеяния (при t=25
0
С)
Параметр До
ККМ
2
После
ККМ
2
Степень агрегации 29 38
Малая полуось, нм 1,16 0,73
Большая полуось, нм 1,66 2,37
Площадь поверхности на один углеводородный
радикал, нм2
0,60 0,55
Объем мицеллы на одну молекулу ПАВ, нм
3
0,328 0,225
3.5. Физико – химические свойства молекул ПАВ в области
перехода сферических мицелл в несферические
Переход мицелл из сферической формы в симметричную связан с изменением
физико – химических свойств молекул ПАВ в мицелле и соответственно с ее
внутренней структурой. Поэтому значение свойств молекул ПАВ и образованных
ими мицеллярных структур при изменении их формы позволяет предположить
механизм этого процесса.
3.5.1. Применение метода спинового зонда для изучения строения
мицелл
Метод спиновых меток широко применяется для исследования жидкостей,
полимеров, биологических систем. Распространение данного метода обусловлено
прежде всего заложенными в нем возможностями, являющимися следствием особой
чувствительности спинового зонда (стабильного свободного радикала) к физико–
химическим свойствам окружающей его среды. Стабильный радикал представляет
собой своеобразный молекулярный датчик структурной и динамической
информации о локальном окружении. Примерами спиновых зондов являются 1–
оксил–2,2,6,6–тетраметилпиперидина (ТЕМПО) в водных растворах ПАВ и 1-оксил-
2,2,5,5-тетраметил-3-бром-4-карбокси-3-пирролина (ТЕМПО БК) в растворах
61
малорастворимых ПАВ в неполярных и малополярных средах. Скорость вращения
молекулы спинового зонда характеризуется временем вращательной корреляции,
т.е. временем, необходимым молекуле зонда для поворота на угол, равный одному
радиану. Любое сокращение времени существования электрона в его
энергетических состояниях вызывает уширение полос спектра. Положение этих
полос, расстояние между ними и их ширина зависят от природы окружения
молекулы парамагнитного зонда.
Как показали исследования, вращательная корреляция ТЕМПО зависит от
концентрации добавляемых в воду ПАВ: хлорида и иодида цетилпиридиния,
хлорида децилпиридиния и миристата сахарозы (рис. 3.11). Время вращательной
корреляции ТЕМПО намного выше, чем в чистых растворителях. Это
свидетельствует о том, что плотность упаковки молекул ПАВ в периферийной части
мицелл значительно выше плотности упаковки низкомолекулярных растворителей.
При ККМ
2
ПАВ наблюдается скачкообразное увеличение времени вращательной
корреляции ТЕМПО. Следовательно, асимметризация сферических мицелл в
водных растворах ПАВ сопровождается уплотнением периферийной части мицелл.
Образование углеводородными цепями молекул ПАВ более упорядоченной
структуры в несферических мицеллах по сравнению со сферическими
подтверждается также результатами изучения спектров комбинационного рассеяния
ПАВ в твердом состоянии и в мицеллярных растворах. К такому же заключению
пришли и другие исследователи, анализируя ЯМР - и ЭПР-спектры водных
растворов ПАВ.
Таким образом, при асимметризации сферических мицелл в водных растворах
ПАВ происходит уплотнение их молекул в мицелле, Отметим при этом, что
плотность упаковки молекул ПАВ как в несферических, так и в сферических
мицеллах значительно больше плотности упаковки воды, углеводородов и других
низкомолекулярных растворителей.
В растворах маслорастворимых ПАВ в СС1
4
и дихлорэтане время
вращательной корреляции ТЕМПО БК также скачкообразно увеличивается при
концентрации, равной ККМ
2
, что свидетельствует об уплотнении полярного ядра
обратных мицелл при их асимметризации.
Подтверждением уплотнения молекул ПАВ в несферических мицеллах наряду
с данными метода спинового зонда является также уменьшение удельного
парционального объема мицелл при их асимметризации в водных растворах
оксиэтилированных изооктилфенолов ОП-7,3; ОП-17,7 и ОП-17,9 (рис. 3.10.). Все
это вместе указывает на то, что асимметризация сферических мицелл при ККМ
2
ПАВ обусловлена не агрегацией сферических мицелл, а изменением внутренней их
структуры, что находит свое отражение в повышении плотности упаковки молекул
ПАВ в мицелле.
Уплотнение молекул ПАВ в мицелле при переходе ее из сферической формы
в несферическую приведет к понижению ее диэлектрической проницаемости.
Диэлектрическую проницаемость мицелл можно определять методом спинового
зонда. Для нитроксильных зондов ТЕМПО и ТЕМПО БК неспаренный электрон
62
находится в основном на 2р-π-атомной орбитали ядра азота. Это характеризуется
определенной константой сверхтонкого взаимодействия (СТВ).
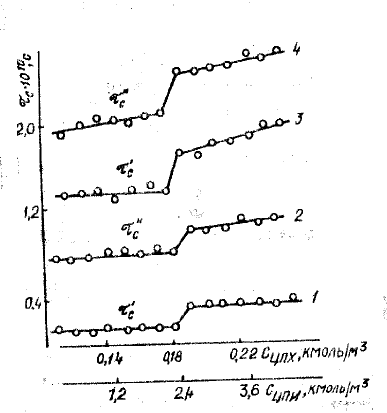
Рис. 3.11.. Зависимость времени вращательной корреляции ТЕМПО от
концентрации (при t=45
0
С) локализованных в мицеллах: 1,2 – иодида
цетилпиридиния (ЦПИ); 3,4 – хлорида цетилпиридиния (ЦПХ)
Из приведенных на рис. 3.12 данных видно, во-первых, что диэлектрическая
проницаемость периферийной части прямой мицеллы меньше, чем воды, но больше,
чем любой из известных органических сред, во-вторых, что при ККМ
2
диэлектрическая проницаемость скачкообразно уменьшается. По мере роста
концентрации ПАВ в воде как до, так и после ККМ
2
диэлектрическая
проницаемость понижается более плавно, чем при ККМ
2
. Уменьшение
диэлектрической проницаемости периферийной части мицелл при их
асимметризации может быть только следствием их обезвоживания. Но степень
гидратации хлорида цетилпиридиния, определенная по поглощению ультразвука, не
меняется. Это свидетельствует о том, что обезвоживание несферических мицелл
происходит за счет вытеснения воды, не связанной с молекулами ПАВ.
В малополярных средах, дихлорэтане и СС1
4
диэлектрическая проницаемость
ядра обратных мицелл при их асимметризации возрастает. Кроме того,
диэлектрические проницаемости одного и того же ПАВ (бромида цетилпиридиния),
но в разных растворителях, различны (рис.3.13). Все это свидетельствует о том, что
в ядре обратной мицеллы находится какое-то количество растворителя. При
63
переходе сферических мицелл в несферические происходит частичное вытеснение
растворителя из ядра обратной мицеллы.
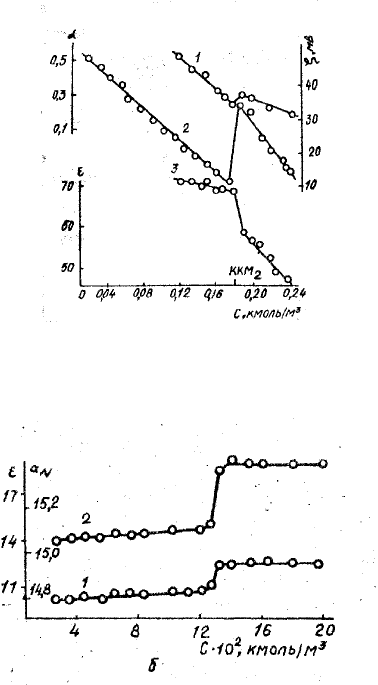
Рис. 3.12.. Зависимость от концентрации в водном растворе (при t=25
0
С): 1 –
степени ионизации молекул хлорида цетилпиридиния (α); 2 – ζ – потенцила; 3 –
диэлектрической проницаемости (ε)
Рис. 3.13.. Зависимость от концентрации (при t=50
0
С) бромида цетилпиридиния в
дихлорэтане: 1 – константы СТВ (αN); 2 – диэлектрической проницаемости ядра
мицеллы (ε)
Итак, при перестройке мицелл из сферической формы в несферическую
вследствие уплотнения молекул ПАВ в мицелле и вытеснения из нее растворителя
диэлектрическая проницаемость в периферийной части прямых мицелл
уменьшается, а в ядрах обратных мицелл увеличивается.
64

3.5.2. Влияние асимметризации сферических мицелл на степень
гидратации молекул ПАВ в мицелле
Уплотнение несферических мицелл при ККМ
2
может происходить вследствие
уменьшения количества воды в них. Площадь поверхности сферической мицеллы,
приходящаяся на одну молекулу ПАВ, значительно больше площади сечения
углеводородной цепи как для ионных, так и для неионных ПАВ, что может вызвать
проникновение воды между углеводородными цепями.
С учетом шероховатости поверхности мицеллы и возможности динамического
выдвижения метиленовых групп за пределы углеводородного ядра данные многих
авторов свидетельствуют о том, что поверхность мицеллы содержит воду до
глубины α – метиленовой группы.
Как было отмечено выше, при переходе сферических мицелл в несферические
повышается плотность упаковки молекул ПАВ, составляющих их, что может
происходить только вследствие вытеснения из мицеллы непрочно связанной с
молекулами ПАВ воды. Косвенным подтверждением такого обезвоживания
мицеллы служит также резкое понижение диэлектрической проницаемости ее
периферийной части (рис. 3.12) Рост диэлектрической проницаемости ядра
обратных мицелл в неполярных средах при концентрации ПАВ, равной ККМ
2
(рис.
3.13), свидетельствует об уменьшении содержания растворителя в несферических
мицеллах по сравнению со сферическими.
Степень гидратации олеата натрия, определенная по поглощению ультразвука,
равна 16 и 14 моль Н
2
О/моль ПАВ при концентрации ниже и выше ККМ
2
соответственно. Меняется также степень гидратации молекул линоленоата натрия,
образующих сферические и несферические мицеллы (табл. 3.3). Степень гидратации
этих ПАВ, определенная по вязкости и рассчитанная с учетом электровязкостного
эффекта, формы мицелл и степени ионизации молекул в мицелле, не отличается от
результатов, полученных по поглощению ультразвука, и слабо уменьшается при
перестройке сферических мицелл в несферические (табл. 3.3). В то же время степень
гидратации додецилсульфата натрия, определенная по поглощению ультразвука,
при концентрации, равной ККМ
2
, резко уменьшается от 17,2 до 12,8 моль Н
2
О/моль
ПАВ.
Таким образом, уплотнение молекул ПАВ в мицеллах при переходе их из
сферической формы в несферическую приводит к обезвоживанию мицеллярных
структур, а иногда и к разрушению первых наиболее прочных гидратных оболочек
вокруг молекул ПАВ в мицелле. Следовательно, при асимметризации мицелл в
растворах ПАВ происходит их лиофобизация, а в некоторых случаях и
лиофобизация молекул ПАВ в мицелле. Обезвоживание несферических мицелл и
понижение контакта молекул ПАВ с водой внутри мицелл вызовут уменьшение
свободной энергии системы, т.е. усилят гидрофобное связывание молекул ПАВ в
мицелле. Выигрыш энергии за счет усиления гидрофобного взаимодействия при
уменьшении площади контакта молекул ПАВ с водой на 0,01 нм
2
, по данным
разных исследователей, составляет от 85 до 105 Дж/молъ. Можно также
65
предположить, что обезвоживание несферических мицелл отразится на степени
ионизации составляющих их молекул ионных ПАВ.
Таблица 3.3
Зависимость структуры мицелл от степени гидратации ПАВ (определена по
вязкости - hв и поглощению ультразвука - hy) (при t=25
0
С)
ПАВ
Область
концентраций,
кмоль/м
3
Форма
мицелл
hв,
моль Н
2
О
моль ПАВ
hy
моль Н
2
О
моль ПАВ
Олеат
натрия
До 0,09
0,10 - 0,19
0,21 - 0,32
Сфера
Сфероид
Цилиндр
15
13
-
16
14
8
Линоленоат
натрия
До 0,10
0,13 - 0,23
0,24 - 0,34
Сфера
Сфероид
Цилиндр
-
-
-
20
17
13
3.5.3. Зависимость степени ионизации молекул ионных ПАВ в
мицелле и ζ – потенциала мицелл от их формы.
Экспериментальные исследования показали, что при ККМ
2
степень ионизации
молекул ионных ПАВ скачкообразно увеличивается (рис. 3.14). Обусловлено это
тем, что уплотнение молекул ПАВ в несферических мицеллах по сравнению со
сферическими приводит к усилению электростатического отталкивания между
ними. Вследствие этого ионные пары противоион - поверхностно-активный ион
разрушаются, а противоионы вытесняются из плотной части двойного
электрического слоя в диффузную, несмотря на уменьшение диэлектрической
проницаемости несферических мицелл.
В результате уплотнения молекул ионных ПАВ на поверхности
несферических мицелл по сравнению со сферическими и связанного с ним
увеличения плотности зарядов на ней резко повышается ζ-потенциал мицелл в
водных растворах ионных ПАВ при ККМ
2
. Повышение ζ-потенциала мицелл при
ККМ
2
ионных ПАВ является также следствием возрастания степени ионизации их
молекул.
66

Рис. 3.14. Зависимость от концентрации: 1 – степени ионизации молекул иодида
цетилпиридиния (при t=45
0
С); 2 – додецилсульфата натрия (при t=25
0
С)
Следовательно, при переходе сферических мицелл в несферические при ККМ
2
увеличивается плотность упаковки молекул ПАВ, повышается их степень
ионизации и ζ-потенциал мицелл. Они частично обезвоживаются, диэлектрическая
проницаемость понижается в периферийной части мицеллы в водных растворах и
повышается в ядрах обратных мицелл в малополярных средах. Из этого следует, что
при асимметризации мицелл усиливаются гидрофобное связывание молекул ПАВ в
них (в результате уменьшения площади поверхности мицеллы на одну молекулу
ПАВ и содержания воды в ней) и электростатическое отталкивание между
молекулами ионных ПАВ на поверхности мицеллы (из-за уменьшения расстояния
между ними, увеличения степени диссоциации молекул ПАВ и понижения
диэлектрической проницаемости периферийной части мицеллы). Эти два вида
взаимодействия являются основными составляющими свободной энергии
мицеллярного перехода. Соотношение их, определяющее знак и абсолютную
величину свободной энергии перехода, должно показать возможность
существования мицелл той или иной структуры.
3.6. Мицеллярные переходы в растворах ПАВ выше ККМ
2
Для многих ПАВ изменение структуры мицелл (сферической их формы в
асимметрическую) при ККМ
2
является единственным переходом. При
концентрациях этих соединений в 1,5 – 2 раза больше их ККМ
2
они теряют
способность растворяться и выпадают в осадок. К таким соединениям относятся,
например хлорид и бромид алкилпиридиния, хлористо – и бромисто – водородные
соли 2 – алкил – 2 имидазолинов и др. Однако для ПАВ иной структуры
зафиксированы и другие критические концентрации.
Изменение структуры несферических мицелл при концентрациях ПАВ выше
ККМ
2
было изучено путем измерения электропроводности растворов ионных ПАВ
различных концентраций. Концентрационные зависимости электропроводности
67
растворов ионных ПАВ обычно используют для определения критических точек
(областей) образования и (или) изменения мицеллярных структур в растворе. Эта
зависимость для удельной электропроводности в большинстве случаев представляет
собой прямые линии, пересекающиеся в некоторой точке, принимаемой за ККМ.
Однако на экспериментальных кривых точки излома, соответствующие
определенным критическим концентрациям мицеллообразования, особенно в
области ККМ высших порядков, не всегда ясно выражены. Более четкие,
скачкообразные изменения дает дифференциальная кривая. Поэтому для
определения переходных областей (ККМ), в которых изменяется мицеллярная
структура раствора, проведено графическое дифференцирование удельной
электропроводности (рис. 3.15). В исследуемой области концентраций олеата
натрия четко выделяются три точки (ККМ
1
, ККМ
2
и ККМ
3
), в которых изменяется
дифференциальная электропроводность, соответствующая образованию и
изменению мицеллярной структуры в растворах олеата натрия.
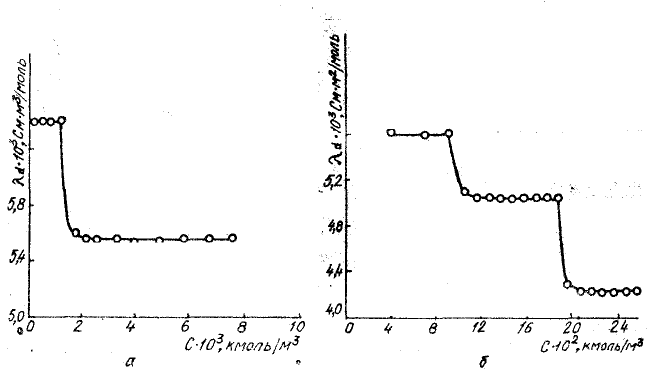
Рис. 3.15.. Зависимость дифференциальной электропроводности (λd) от
мицеллярной концентрации (С) олеата натрия (при t=25
0
С): а – область низких
концентраций; б – область высоких концентраций
Наряду с электропроводностью очень чувствительна к изменениям размера и
формы частиц вязкость. Теория вязкости хорошо разработана для идеальных
случаев невзаимодействующих частиц различной формы, а ее применение к
реальным мицеллярным растворам ионных ПАВ связано с определенными
трудностями из-за того, что поверхность мицелл заряжена и шероховата. Следует
принимать во внимание также степень гидратации мицелл, гидродинамическое
взаимодействие между ними и т.д. Тем не менее, этот метод дает хорошие
68
результаты при изучении мицеллярной структуры раствора в совокупности с
другими методами.
Концентрационные зависимости вязкостных свойств растворов ряда
анионных ПАВ во всех случаях носят аналогичный характер. Для более четкого
определения критических областей концентраций (ККМ
2
и ККМ
3
) использовали
кривые зависимостей дифференциальной приведенной вязкости от мицеллярной
концентрации (рис. 3.16), на которых ясно видны области мицеллярных переходов.
Сходный характер исследованных зависимостей свидетельствует об одинаковых
закономерностях изменения физико-химических параметров мицеллярных структур
при мицеллярных переходах для всех исследованных растворов анионных ПАВ.
Поэтому подробный анализ полученных результатов приведен для олеата, β - [N –
метил – N - оленоил] этансульфоната и частично линоленоата натрия. Для разных
лаурилсульфатов, некоторых солей предельных карбоновых кислот получены
аналогичные результаты.
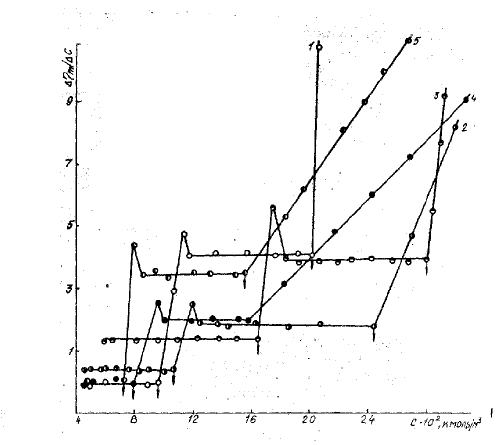
Рис. 3.16.. Концентрационная зависимость (С) дифференциальной приведенной
мицеллярной вязкости (ηm) для растворов (при t=25
0
С): 1 – олеата натрия; 2 –
линоленоат натрия; 3 – β - [N – метил – N - оленоил] этансульфоната натрия; 4 –
лаурилсульфата натрия; 5 – лаурилсульфата никеля. Стрелками показаны ККМ
ПАВ, соответствующие перегибам на кривых
При концентрации ПАВ в растворе существенно выше ККМ
1
частичная
концентрация мицелл, а также объемная доля гидратированной мицеллярной
дисперсной фазы достигают таких значений, при которых взаимодействия между
69
мицеллами ощутимо влияют на вязкостные свойства раствора. Повышение
взаимодействия, в первую очередь, вызвано изменением мицеллярной формы,
однако определенное влияние оказывает и заряд ионных мицелл, т.е. имеет место
электровязкостный эффект.
Исследование вязкости растворов олеата и линолеата натрия при
концентрациях выше ККМ
1
показало, что при переходе от сферических мицелл к
несферическим изменяются гидродинамические параметры мицеллярных растворов
ПАВ (табл. 3.4)
Таблица 3.4
Гидродинамические параметры мицеллярных растворов олеата и
линоленоата натрия (υ=2,5) (при t=25
0
С)
Параметр
Олеат натрия Линоленоат натрия
До
ККМ
2
ККМ
2
-
ККМ
3
До
ККМ
2
ККМ
2
-
ККМ
3
Характеристическая вязкость,
дм
3
/моль
2,48 2,07 1,99 1,82
Гидродинамическая постоянная 0,00 4,23 0,39 1,89
Константа гидродинамического
взаимодействия
0,00 6,20 0,62 3,57
Молярный объем мицеллярного
гидратированного ПАВ,
дм
3
/моль
0,992 0,828 0,796 0,728
В области перехода ККМ
2
– ККМ
3
увеличивается константа
гидродинамического взаимодействия, что свидетельствует об усилении вклада этого
фактора в общую вязкость раствора ПАВ в области выше ККМ
2
. В то же время
молярный объем гидратированной мицеллярной фазы, как видно из табл. 3.4,
уменьшается при переходе в область выше ККМ
2
. Это можно объяснить
асимметризацией существующих в растворе сферических мицеллярных структур,
сопровождающейся увеличением их эффективного объема, что приводит к росту
гидродинамического взаимодействия между ними. Для области концентраций ПАВ
выше ККМ
2
из-за нелинейного характера зависимости нельзя получить численные
значения υ
1
так как она изменяется с увеличением концентрации ПАВ в растворе.
Однако поскольку в данной области характеристическая вязкость уменьшается, в то
время как параметр а повышается, естественно заключить, что в результате этого
резко возрастает υ
1
, т.е. еще больше усиливается гидродинамическое
взаимодействие между мицеллами, которое к тому же все время увеличивается с
ростом концентрации ПАВ в растворе. Изучение электропроводности, вязкости,
степени связывания противоионов, объемной доли гидратированной мицеллярной
фазы показали, что при повышении концентрации ПАВ в растворе мицеллярная
70
