Артюхов В.Г., Ковалева Т.А., Шмелев В.П. Биофизика
Подождите немного. Документ загружается.


ческих соединений (АТФ, ГТФ) в
ходе
обменных реакций или про-
цессов жизнедеятельности (мышечное сокращение).
Для живых организмов в нормальных условиях характерно рав-
новесие
между
первичной и вторичной теплотой, причем уменьше-
ние
первичной теплоты сопровождается возрастанием вторичной.
Это наблюдается при переохлаждении теплокровных.
При
патологических процессах увеличивается доля выделяемой
первичной
теплоты, что сопровождается повышением температуры
тела.
Удельной
теплопродукцией
называют количество теплоты, выде-
ляемое единицей массы животного в единицу времени:
g-Q
T
//<T, (2.4)
где Qr - количество теплоты, выделяемое в единицу времени; ц
г
-
единица
массы; g - удельная теплопродукция.
Теплопродукция пропорциональна массе животного: Q
T
~ k- M.
Теплопродукция организма может быть определена как сумма Q
B
+
+Qc
где Q
B
- теплота, выделяемая при взаимодействии клеток меж-
ду собой и пропорциональная массе тела (М); Qc - теплота, выделя-
емая при взаимодействии организма с окружающей средой, т.е.
пропорциональная
площади его поверхности (Vfri). Таким обра-
зом:
Q
T
- а-М + Ь-М
2/3
, (2.5)
где а - количество клеток, b - площадь поверхности.
Поэтому
q-a
+
b/fo/.
(2.6)
На
основании экспериментальных данных по этим формулам бы-
ли
вычислены коэффициенты а и b для гомойотермных и пойкило-
термных животных.
Удельная теплопродукция уменьшается с увеличением массы
животного (рис. 2.1). Такую зависимость можно объяснить тем, что
с увеличением размера и массы животного уменьшается отношение
его поверхности к объему. Для компенсации большой потери тепло-
ты мелкими животными требуется более высокая интенсивность
метаболизма и, соответственно, потребление большего количества
пищи.
Этим можно объяснить необычайную прожорливость грызу-
нов
и мелких птиц.
Теплопродукция теплокровных животных в
25-30
раз меньше,
чем пойкилотермных, за счет уменьшения теплообмена
между
ок-
ружающей средой и организмом.
Живые организмы - открытые термодинамические системы, су-
61

Рис.
2.1. Зависимость
*
удельной теплопродукции от
,
массы животного: 1 - земле-
ройка; 2 - мышь-малютка; 3 -
,
мышь;
4 - крыса; 5 - кошка; 6
-
кролик; 7 - собака; 8 - овца;
•
9 - человек; 10 - свинья; 11 -
корова; 12-слон
•
шествующие
в
условиях постоянства давления
и
температуры. Поэ-
тому
для
оценки
их
жизнедеятельности важен еще один термодина-
мический
параметр (функция)
-
энтальпия.
Энтальпия
- (от
греч.
-
нагреваю)
- это
сумма внутренней
энер-
гии
системы
и
произведения объема
и
давления:
H-U
+
PV, (2.7)
где
Н -
теплосодержание системы.
Энтальпия
-
термодинамическая функция, которая, подобно
тем-
пературе, давлению, объему
и
внутренней энергии, характеризует
систему. Абсолютное значение энтальпии для рассматриваемой сис-
темы определить невозможно
и в
термодинамических расчетах фи-
гурирует
лишь изменение энтальпии
АН,
происходящее
при
пере-
ходе
системы
из
одного состояния
в
другое.
Для эндотермических процессов изменение энтальпии имеет
по-
ложительный знак,
для
экзотермических
-
отрицательный.
АН (кДж/моль) имеет абсолютное значение
от (±)
сотен
до не-
скольких тысяч. Введенная функция лежит
в
основе закона Гесса
-
основного следствия первого закона термодинамики.
Он
формули-
руется следующим образом: тепловой эффект химической реакции,
развивающейся через
ряд
промежуточных стадий,
не
зависит
от пу-
ти перехода,
а
определяется лишь разностью энтальпий конечных
и
исходных продуктов реакции.
Математическое выражение закона Гесса:
Q
- АН - I/
Hi.k
- X/
Hj.u,
(2.8)
где Z; Hi.k
-
сумма энтальпий
всех
продуктов реакции;
1j
Hj,
u
- сум-
ма энтальпий
всех
исходных веществ;
АН -
изменение энтальпии
химической реакции.
Следует
отметить,
что
изменение энтальпии соответствует вели-
62

чине
поглощенной или выделенной теплоты, которую довольно точ-
но
можно определить с помощью калориметра.
Применяя
данный закон, можно рассчитать тепловые эффекты
любых биохимических реакций. Известно, что биохимические пре-
вращения
в организме проходят множество промежуточных стадий,
которые не всегда выявлены и доказаны. На основании закона Гес-
са, не зная промежуточных звеньев биохимического процесса, имея
данные лишь о начальных и конечных продуктах реакции, можно
вычислить суммарный энергетический эффект.
Пример.
Рассмотрим окисление глюкозы при постоянном давлении:
С6Н12О6
+ 6О2
-+6CO2
+
6H2O
+
Q;
<2-(
6
"со
г
+н
н
2
о
)
-
(
\н
12
о
6
+
ш
о
г
)
-
2Ш
«*
ж
»
оль
~
•
Такое же количество теплоты выделяется при окислении глюкозы в организме жи-
вотных, когда в процессе анаэробного и аэробного гликолиза образуется ряд проме-
жуточных веществ.
Таким
образом, потребление 1 л кислорода или выделение 1 л уг-
лекислого газа организмом сопровождается выделением
2870:
: 134,4 - 21,35 кДж теплоты. Поэтому тепловыделение любого жи-
вотного можно подсчитать путем умножения количества потреб-
ленного кислорода или выделенного углекислого газа на 21,35 кДж.
Это метод непрямой калориметрии для определения теплопродук-
ции.
Закон
Гесса используется для вычисления калорийности пище-
вых продуктов и составления пищевых рационов человека и живо-
тных.
§
2. Второе начало термодинамики и живые организмы
Первое начало термодинамики позволяет
утверждать,
что при
любых процессах, в том числе и тех, которые протекают в живых
организмах, энергия не возникает и не исчезает. Все виды энергии
взаимно
превращаются в строго эквивалентных количествах.
Однако первое начало термодинамики не
дает
ответа на вопрос о
том, почему процесс, связанный с трансформацией энергии, проте-
кает именно в данном направлении; насколько полно осуществля-
ется превращение энергии; каковы реальные пределы протекания
того или иного биохимического процесса.
Второе начало термодинамики позволяет судить о направлении
протекания
процесса и, таким образом, дополняет первое начало
термодинамики.
Формулировку второго начала термодинамики
впервые дали независимо
друг
от
друга
Р.Клаузиус и У.Томпсон
(1850-1851).
Второе начало не имеет столь простой и общепринятой
формулировки, как первое, и формулируется по-разному, в зависи-
63

мости
от той
группы
явлений, к которой оно прилагается. С.Карно:
"Коэффициент
полезного действия
всех
обратимых тепловых ма-
шин одинаков и не зависит от рода работающего тела, а только от
интервала предельных температур, в котором работает машина".
Р.Клаузиус:
"Теплота не может переходить сама
собой
от более хо-
лодного тела к более теплому".
Важной
физической величиной, используя которую можно
сфор-
мулировать
второе начало термодинамики в более общем виде, яв-
ляется
еще один термодинамический параметр систем - энтропия.
Энтропия - это мера неупорядоченности или вероятности
состоя-
ния системы. Энтропия измеряется в тех же единицах, что и тепло-
емкость, - Дж/моль- К, где К - температура по Кельвину.
Энтропия является таким же свойством термодинамической сис-
темы, как температура, давление и др. В любом теле (лист бумаги)
содержится
определенная энтропия; так же, как и
внутренняя
энер-
гия, энтропия системы растет с ее массой и равна сумме энтропии
подсистем,
она увеличивается при
повышении
температуры за счет
усиления теплового движения молекул. Аналогичное увеличение
энтропии наблюдается при переходе вещества из твердого
состоя-
ния в жидкое. Для
вычисления
изменения энтропии AS биохимиче-
ской
реакции поступают так же, как при
вычислении
АН, т.е. из
суммы изменения энтропии продуктов реакции
вычитают
сумму
изменения энтропии исходных веществ.
Изменение
энтропии dS системы равно отношению количества
теплоты
(<5Q),
сообщенного системе, к термодинамической темпе-
ратуре (Т):
dS
-<5Q/T.
(2.9)
Если
ввести понятие энтропии, то второе начало термодинамики
можно
сформулировать так: энтропия изолированной системы воз-
растает
в необратимом процессе и остается неизменной в обрати-
мых термодинамических процессах. Уравнение второго закона тер-
модинамики:
dS><5Q/T.
(2.10)
Сущность второго начала термодинамики для изолированных си-
стем
состоит в том, что все необратимые процессы протекают в та-
ком направлении, в котором энтропия системы увеличивается, т.е.
dS>0,
dF * dU. (F - свободная энергия системы). Это означает, что
далеко
не вся
внутренняя
энергия системы переходит в работу,
часть ее рассеивается в виде теплоты.
64

При
обратимых процессах dS - 0 и dF - dU, т.е. рассеивания
энергии
в пространстве не происходит.
Энтропия
- это часть общей энергии клетки, которая не может
быть использована в данной системе. С увеличением энтропии
энергия,
вовлеченная в обмен, уменьшается и процесс становится
менее обратимым. Согласно второму началу термодинамики энтро-
пия
изолированной системы стремится к максимуму, при котором
достигается равновесие и реакция прекращается. Если атомы в мо-
лекуле упорядочены, то энтропия системы низка.
Второй закон термодинамики показывает, что не все виды
энер-
гии
эквивалентны. По качеству их можно разделить на 3 класса (А,
В, С) соответственно величине энтропии. Такие виды энергии, как
гравитационная,
световая и электрическая, наиболее эффективно,
т.е. с наименьшей энтропией,
могут
быть превращены в
другие
ее
виды, и они относятся к классу А. В класс В (среднего качества) по-
падает химическая энергия. Тепловая энергия относится к классу С
(низкое
качество) - это энергия с максимальной энтропией.
Мы
рассмотрели второй закон термодинамики в применении к
изолированным
системам. Живые организмы - системы открытые, и
изменение
энтропии для них складывается из продукции энтропии
внутри организма за счет необратимых биохимических процессов
(diS) и обмена (deS) энтропии с окружающей средой.
dS-diS + deS.
(2.11)
Индексы
ставятся после знака дифференциала, так как в отдель-
ном
случае
полным дифференциалом является общее изменение
энтропии,
а не каждое из слагаемых в отдельности.
Формулировка второго закона термодинамики для живых орга-
низмов:
скорость изменения энтропии в организме равна алгебраи-
ческой сумме производства энтропии внутри организма и скорости
поступления энтропии из среды в организм.
Уравнение второго начала термодинамики для открытых систем
следующее:
dS/dt - diS/dt + deS/dt,
(2.12)
где dS/dt - скорость изменения энтропии в организме; diS/dt - ско-
рость производства энтропии внутри организма; deS/dt - скорость
обмена энтропией
между
организмом и окружающей средой. В от-
личие от первого закона термодинамики, имеющего абсолютное
значение,
второй закон носит статистический характер. Увеличе-
ние
энтропии в необратимых процессах отражает лишь наиболее
вероятное их протекание. Этот закон соблюдается особенно точно
65

для макроскопических систем с большим количеством компонен-
тов. Впервые статистический характер второго закона термодина-
мики
показал австрийский
физик
Л.Больцман. Он установил
следующую
связь
между
энтропией и термодинамической вероят-
ностью системы:
S
- к
•
lnW,
(2.13)
где к - постоянная Больцмана, равна 1,38
•
10"
23
Дж/К; W - термо-
динамическая
вероятность, равняется числу
всех
перегруппировок
компонентов
в системе и выражается огромными числами. Клетка
содержит 10
9
молекул, W колеблется от 1 до 10
15
более.
Таким
образом, стремление энтропии к росту связано с перехо-
дом системы в менее упорядоченное состояние с большими значени-
ями
термодинамической вероятности W.
Проанализируем уравнение второго начала термодинамики для
открытых систем.
deS/dt > 0 показывает увеличение энтропии системы в результа-
те того, что в организм постоянно поступает поток вещества и
энер-
гии.
deS/dt < 0 означает, что отток энтропии из организма превышает
приток.
Величина diS/dt > 0 (всегда положительна), так как в организме
постоянно
протекают биофизические и биохимические процессы.
При
условии, что diS/dt > 0, возможны следующие три случая:
1) dS/dtX), если deS/dt > 0 или если deS/dt<0, но diS/dt >
deS/dt, т.е. скорость производства энтропии внутри организма бу-
дет превышать скорость обмена энтропией с окружающей средой;
2) dS/dt < 0, если deS/dt < 0, скорость обмена энтропией организ-
ма с окружающей средой превышает скорость производства энтро-
пии
внутри организма deS/dt > diS/dt;
3) dS/dt - 0, если deS/dt < 0, скорость обмена энтропией с окру-
жающей средой равна скорости производства энтропии за счет
внутренних биофизических и биохимических процессов. Послед-
ний
случай соответствует установлению в системе стационарного
состояния.
Такой
анализ уравнения второго начала термодинамики в при-
менении
к живым организмам показывает, что биологические про-
цессы
могут
сопровождаться самопроизвольным уменьшением энт-
ропии,
и позволяет объяснить кажущиеся противоречия
между
жи-
выми организмами и вторым началом термодинамики. Действи-
тельно, рост и развитие организмов сопровождается усложнением
их организации и с точки зрения классической термодинамики вы-
66

глядит как самопроизвольное уменьшение энтропии и увеличение
(накопление)
свободной энергии. Дело в том, что свободная энергия
не
может возрастать лишь в изолированной системе. Живые орга-
низмы,
как системы открытые, в процессе автотрофного и гетерот-
рофного
питания получают свободную энергию из окружающей
среды. Поэтому второй закон термодинамики применительно к жи-
вым организмам надо рассматривать, учитывая их взаимодействие
с окружающей средой. С этой точки зрения уменьшение энтропии и
увеличение свободной энергии фотосинтезирующих организмов
происходит благодаря уменьшению свободной энергии и увеличе-
нию
энтропии в системе Солнце-Земля (ядерные реакции на Солн-
це) и общий баланс энтропии автотрофов соответствует второму на-
чалу
термодинамики.
Точно
так же уменьшение энергии в частях клетки, где идет био-
химический синтез, происходит за счет избыточного увеличения
энтропии
в реакциях диссимиляции, и общий баланс энтропии уве-
личивается. Поэтому живые организмы подчиняются второму нача-
лу термодинамики, когда речь идет о круговороте и превращениях
свободной энергии в системе организм - окружающая среда.
Надо
сказать, что процессы обмена веществ в организме не толь-
ко
подчиняются первому и второму началам термодинамики, но и в
значительной мере зависят от скорости биохимических превраще-
ний,
определяемых деятельностью генов.
§
3. Баланс энтропии при росте и развитии организмов
Общая теория роста и развития организмов на основе представ-
лений
термодинамики была выдвинута И. Пригожиным в 1947
году.
По
данной теории в процессе роста и развития организмов проис-
ходит
уменьшение скорости продуцирования энтропии, отнесенной
к
единице массы объекта.
dS-diS + deS<O.
(2.14)
О скорости продуцирования энтропии можно судить по выделению
потока тепла, который сопровождает необратимые процессы в сис-
теме. Надо сказать что теплопродукция клетки отражает уровень
процессов дыхания или анаэробного гликолиза и поэтому может
быть оценена по характеру поглощения 02 или образованию глико-
литических продуктов.
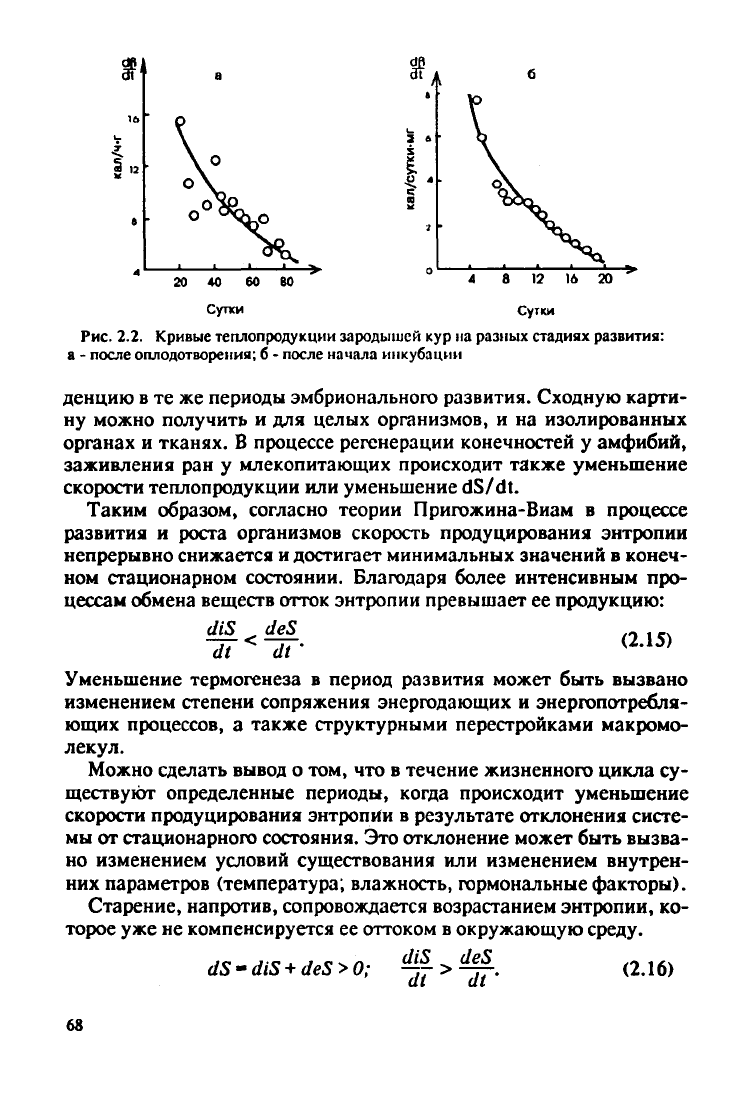
Измерения
скорости теплопродукции ф/соотнесенной к едини-
це массы, показали на различных объектах, что этот параметр
уменьшается, начиная с первых стадий развития организмов.
Измерение
удельной интенсивности дыхания имеет ту же тен-
67
f
20
40
60
Сутки
12
16 20
Сутки
Рис.
2.2. Кривые теплопродукции зародышей кур на разных стадиях развития:
а
- после оплодотворения; 6 - после начала инкубации
денцию
в те же
периоды эмбрионального развития. Сходную карти-
ну можно получить
и для
целых организмов,
и на
изолированных
органах
и
тканях.
В
процессе регенерации конечностей
у
амфибий,
заживления
ран у
млекопитающих происходит также уменьшение
скорости теплопродукции
или
уменьшение dS/dt.
Таким образом, согласно теории Пригожина-Виам
в
процессе
развития
и
роста организмов скорость продуцирования энтропии
непрерывно снижается
и
достигает минимальных значений
в
конеч-
ном
стационарном состоянии. Благодаря более интенсивным
про-
цессам обмена веществ отток энтропии превышает
ее
продукцию:
diS
deS
dt
df
(2.15)
Уменьшение термогенеза
в
период развития может быть вызвано
изменением степени сопряжения энергодающих
и
энергопотребля-
ющих процессов,
а
также структурными перестройками макромо-
лекул.
Можно сделать вывод
о
том,
что в
течение жизненного цикла
су-
ществуют определенные периоды, когда происходит уменьшение
скорости продуцирования энтропии
в
результате
отклонения систе-
мы
от
стационарного состояния.
Это
отклонение может быть вызва-
но
изменением условий существования
или
изменением внутрен-
них параметров (температура; влажность, гормональные факторы).
Старение, напротив, сопровождается возрастанием энтропии,
ко-
торое
уже не
компенсируется
ее
оттоком
в
окружающую
среду.
(2.16)
68

Идет накопление энтропии в системе. Как писал один стареющий
физик,
"меня
съедает
энтропия и целиком и по частям". Скорость
накопления
энтропии различна у разных видов. Энтропия достига-
ет максимального значения при термодинамическом равновесии.
Жизнь
- это постоянная борьба против тенденции к возрастанию
энтропии.
Синтез биомакромолекул, образование клеток со слож-
ной
структурой, организация живых
существ
- мощные антиэнтро-
пийные
факторы.
§
4. Стационарное состояние. Теорема Пригожина.
Термодинамическое равновесие. Устойчивое и неустойчивое
стационарное состояние. Принцип Ле-Шателье
Состояние
системы, при котором ее параметры не изменяются в
течение длительного времени, но происходит обмен веществом и
энергией
с окружающей средой, называют стационарным. В стаци-
онарном
состоянии открытой системы концентрация промежуточ-
ных продуктов не изменяется со временем, что достигается опреде-
ленным
соотношением различных физико-химических процессов,
•ответственных за распад и образование промежуточных соедине-
ний.
Стационарное
состояние в живых организмах достигается
путем
взаимной
компенсации
всех
процессов, связанных с поступлением,
удалением и превращением веществ и энергии.
Живой
организм в каждый момент времени не
отвечает
приве-
денному определению стационарного состояния. Однако, если рас-
смотреть средние значения его параметров за сравнительно боль-
шой
промежуток времени, можно отметить их постоянство и
утвер-
ждать,
что стационарное состояние характерно для организма. Так,
с большим постоянством поддерживается температура определен-
ных органов и тканей у теплокровных животных, сохраняется неиз-
менный
солевой состав и водородный показатель (рН) различных
биологических жидкостей, не изменяются в
ходе
нормальной жиз-
недеятельности величины биопотенциалов покоя, осмотического
давления.
В открытых системах суммарное изменение энтропии в стацио-
нарном
состоянии равно нулю:
dS-deS
+
diS-O.
(2.17)
Это уравнение стационарного состояния. Члены diS и deS, опре-
деляющие внутренние необратимые процессы и процессы обмена
системы с окружающей средой, отличны от нуля.
Стационарное
состояние биологической системы поддерживается
69

при
условии
diS - deS, т. е.
когда увеличение энтропии системы
за
счет происходящих
в ней
необратимых процессов компенсируется
оттоком энтропии
при
взаимодействии
с
окружающей средой.
Особенности стационарного состояния
и
термодинамического
равновесия показаны
в
табл.
2.2.
Таблица 2.2
Различие
между системами, находящимися в термодинамическом равновесии и
стационарном
состоянии
Термодинамическое равновесие
Отсутствие
обмена с окружающей сре-
дой
веществом и энергией
Энтропия системы постоянна и соответ-
ствует
максимально возможному в дан-
ных условиях значению
Полное
отсутствие в системе каких-либо
градиентов
Не
требуется затраты свободной энергии
Система
нереакционноспособна и не со-
вершает работу
против
внешних сил
Стационарное состояние
Непрерывный обмен с окружающей сре-
дой
веществом и энергией
Энтропия системы постоянна, но не рав-
на максимально возможному в данных
условиях значению..
Наличие постоянных по
величине
гради-
ентов
Необходимы
постоянные затраты энер-
гии
В
системе совершаются необратимые ре-
акции, ее работоспособность постоянна
и
не
равна
нулю
Сходство термодинамического равновесия
и
стационарного
со-
стояния
системы заключается
в том, что
стационарное состояние,
так
же как и
термодинамическое равновесие, сохраняет
все
основ-
ные
параметры неизменными. Энтропия системы, находящейся
в
стационарном
состоянии, имеет некоторую постоянную величину,
не
равную максимальной. Поэтому наиболее характерными свойст-
вами стационарного состояния являются стремление системы
к ми-
нимуму ежесекундного прироста энтропии
и
определенная внут-
ренняя
стабильность
и
упорядоченность.
Для
наглядности рассмот-
рим
свойства стационарного состояния системы
на
термодинамиче-
ской
модели, предложенной
А.
Бертоном
в 1939 г.
(рис.
2.3).
Сосуд
S, в
котором уровень жидкости постоянен
(за
счет большо-
го объема
сосуда
S по
сравнению
с
объемом сосудов
А и В или в ре-
зультате
работы насосного механизма), играет роль внешней среды,
а
сосуд
Z -
роль стока,
он
также относится
к
внешней среде. Сосуды
А
и В,
связанные
с
внешней средой кранами
К
о
и K
z
,
представляют
собой рассматриваемую нами открытую систему. Краны Ко
и K
z
ре-
гулируют
скорость поступления
и
оттока воды
и
имитируют
про-
цесс диффузии. Стационарное состояние возникает
при
определен-
ных уровнях жидкости
в сосудах А и В и
определенных положениях
70
