Жилин В.Ф., Збарский В.Л., Юдин Н.В. Малочувствительные взрывчатые вещества
Подождите немного. Документ загружается.

тринитрохиназолин-1-оксид [44,47,55], соль гуанилмочевины и
динитразовой кислоты (FOX-12) [ 44 ] и многие другие.
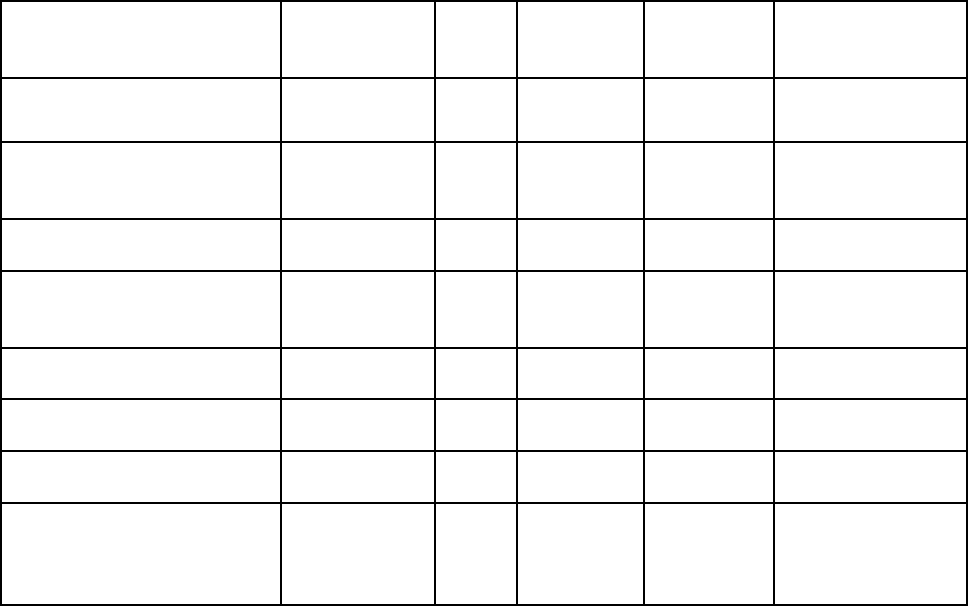
Таблица 1.6
Предложенные к использованизованию МЧВВ
Наименование Аббревиатура Т. пл.,
о
С
Плотность,
г/см
3
Скорость
детонации,
м/с
Чувствительность
к удару
3-Амино-5-нитротриазол
[48]
АNТА 238 1,82 8460 –
4,6-Бис(3-амино-5-
нитро-1,2,4-триазолил)-3-
нитропиримидин [49]
ДАНTNP 330 1,865 – –
2,4-Динитроимидазол
[45,50]
DNI 264-7 – – –
2,6-Диамино-3,5-
динитропиразин-1-oксид
[51]
LLM-105 348 – – –
3,3’-Диамино-2,2’,4,4’,6,6’-
гексанитродифенил [52]
DIPAM 304 – – *
3-Пикриламино-1,2.4-
триазол [53]
PATO >310 1,94 7850 >320 см/2,5 кг
2,6-Бис(пикриламино)-3,5-
динитропиридин [54]
PYX 460 1,75 7450 63 см
2,4,6-Tрис(3,5-
диамино-2,4,6-
тринитрофенил
_
амино)-1,3,5-триазин [55]
PL-1 335 2,02 7860 170 см/50%
*низкая чувствительность к электростатическому разряду >3200 Дж
Сравнение взрывчатых характеристик ТАТНБ, ДАДНЭ и штатных ВВ
проведено в табл. 1.7.
Основной эффект от использования МЧВВ – резкое снижение
опасности случайного инициирования ВВ или взрывчатых составов в
чистом виде или в боеприпасах и, как следствие, значительное сокращение
взрывобезопасных расстояний между объектами, где хранятся боеприпасы.
Таблица 1.7
31
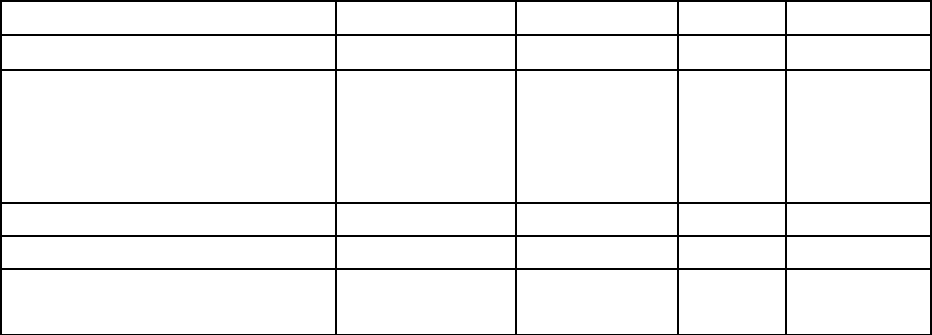
Взрывчатые свойства некоторых МЧВВ
Параметр ТАТНБ [56] ДАДНЭ ТНТ Гексоген
Теплота сгорания, ккал/кг 2841,5± 2,5
1998,6± 2,5
3441 2279
Энтальпия образования,
ΔH
f
exp ккал/моль
кДж/моль
ккал/кг
–39,4±0,6;
–165;
–152,7
–31,0± 0,4;
–130
–224,6
–15
–63
16
67
Теплота взрыва, ккал/кг 920 1090 1030 1320
Скорость детонации, м/с 8000 8700 6950 8860
Толщина минимально
детонирующего слоя, мм
1,94 0,49 0,46 0,11
Указывается [7], что переход от боеприпасов категории опасности HD 1.1
к категории HD 1.2.3, при равной мощности изделий, позволяет почти в 10
раз уменьшить территорию, занимаемую складами (в первом случае для
склада на 500 т нужна площадь в 2 км
2
, во втором для склада на 3000 т – 1
км
2
).
2. ТРИАМИНОТРИНИТРОБЕНЗОЛ
В настоящее время в США ТАТНБ принят как стандартное
малочувствительное взрывчатое вещество (класс IHE), а его смеси с Kel-F
– в качестве стандартного малочувствительного состава [8].
2.1. Физические, химические и взрывчатые свойства ТАТНБ
1,3,5-Триамино-2,4,6-тринитробензол (ТАТНБ, ТАТВ), С
6
Н
6
N
6
O
6
,
(М 258.18) – желтые триклинные кристаллы.
Физические, термодинамические и взрывчатые характеристики
ТАТНБ представлены в табл. 2.1.
Точное значение температуры плавления ТАТНБ не определено, так
как выше 320
0
С начинается разложение в твердом состоянии. При
“мгновенном нагреве” ТАТНБ плавится при 450–451
0
С.
Таблица 2.1
32
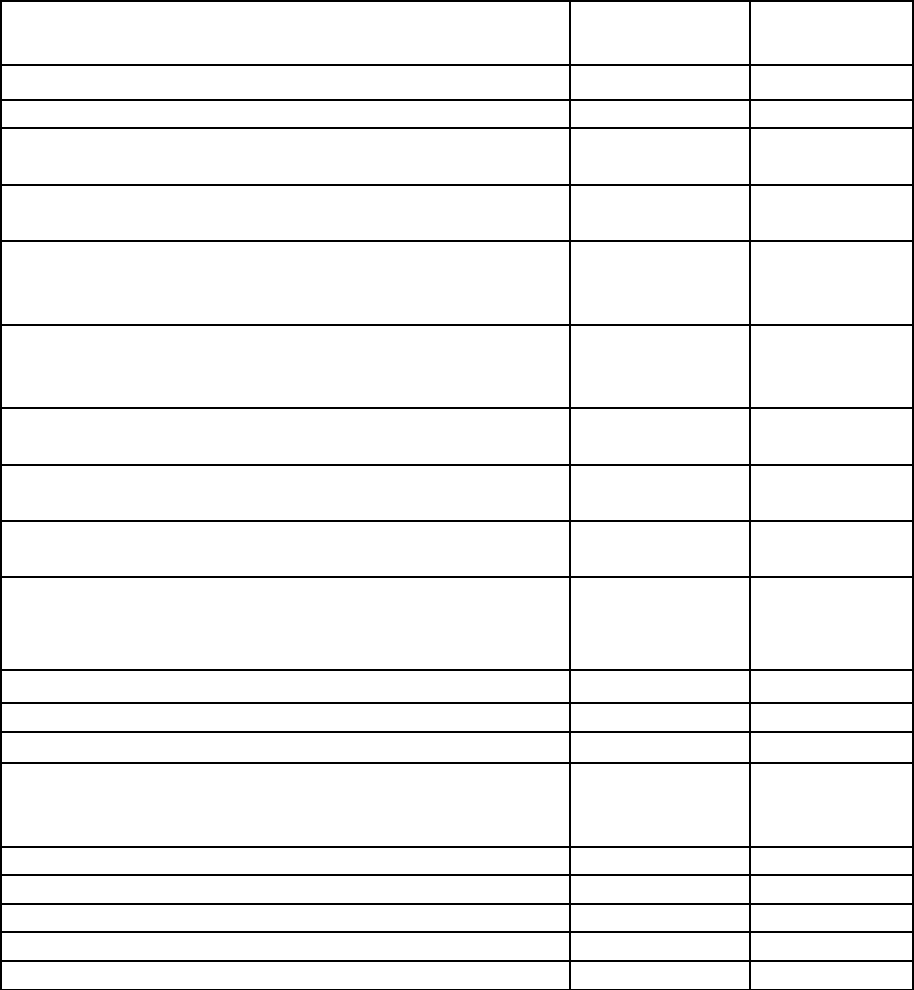
Свойства триаминотринитробензола
Характеристика Величина
параметра
Ссылка
Плотность, г/см
3
1,93 , 1,937*** –
Теплоемкость, кал/ ( г ·
0
С
)
*
0, 25 [57]
Теплопроводность кал/(см · с·
0
С) при плотности
г/см
3
11,2·10
-4
при
1,8410
–
Коэффициент объемный термического расширения,
К
-1
30,4·10
-5
[58]
Коэффициенты термического расширения по осям а – 8.3·10
-6
;
в – 20,9·10
-6
с – 248·10
-6
–
Энтальпия образования, ккал/моль;
кДж/ моль;
ккал/моль
– 39,4±0,6;
–165;
–152,7
–
Теплота сгорания, ккал/моль,
ккал/ кг
735,9
2850
–
Теплота сублимации, кал/ г;
ккал/моль
155,7
40,2
[59]
Энергия активации термического разложения, ккал/
моль
**
59,9
41,8
[60]
[61]
Вакуумная проба, см
3
/(г·ч), при температуре,
0
С 0,5/200****
0,7–1,2 /260
2–2,25 /280
–
Температура самовоспламенения,
0
С
320–325
–
Температура вспышки с 5 с задержкой,
0
С 520 –
Теплота взрыва при 1,87 г/см
3
, ккал/кг
1018± 25
–
Чувствительность к удару (50% взрывов при
падении груза 2,5 кг с высоты), см;
Дж
800
200
[62]
Чувствительность к трению при 440 кг·см 10/10 –
Инициирующий заряд азида свинца, г 0,3 –
Бризантность по песчаной пробе,г 42,9 –
Электростатическая чувствительность (50%), Дж 1,83 – 6,3 –
Диаметр отказа, см 1,3 –
*
Уравнение зависимости теплоемкости от температуры имеет вид
С
р
(Т) = 0,215 + 1.324 · 10
-3
Т – 2· 10
-6
Т
2
.
**
При определении термической стабильности методом дифференциальной
сканирующей калориметрии (ДСК) наблюдают два
экзотермических пика : при 330 и 358
0
С.
*** По данным рентгеноструктурного анализа.
**** 48 ч.
33
Термическое разложение ТАТНБ неоднократно становилось
предметом тщательного изучения. В одной из последних работ при
изучении термического разложения ТАТНБ при температурах 250 – 300
0
С
было установлено, что процесс протекает с постоянной скоростью до
степени превращения 0,8 и может быть описан уравнением Аррениуса:
W = 3,993*10
10
* exp (–19500/T).
Одновременно рассматривалась возможность образования
нитропро
_
изводных бензофуроксана и бензодифуроксана в этих процессах.
Было показано, что термостатирование ТАТНБ при 498 – 573 К в течение
10 ч приводит к образованию 0,001 – 0.005 моль диаминодинитробензо–
фуроксана и 0,0001 – 0,002 моль аминонитробензодифуроксана на 1 моль
исходного ТАТНБ. Параллельно выделяется 0,4 моль N
2
, 0,96 моль NO,
1,14 моль CO
2
, 2 моль H
2
O, 0,91 моль C
2
N
2
и 0,48 моль HCN.
Краткие сведения о детонационных характеристиках ТАТНБ
представлены в табл. 2.2.
Таблица 2.2
Детонационные характеристики ТАТНБ
Плотность,
г/см
3
Скорость
детонации,
м,сек
Давление
детонации,
ГПа
Изоэнтро–
пический
экспонент
Примечание
1,857
*
7606 25,94 3,07 –
1,800 7658 17,46 2,71 –
1,880 Отказ – – D=0,64 cм
**
1,880 7600–7700 – – D=1,27cм
**
*
Расчетная скорость детонации при максимальной плотности –7970 м/с.
**
без оболочки.
Из приведенных данных следует, что КДД для ТАТНБ больше 6 мм
и меньше 13 мм.
Данные по растворимости представлены в табл.2.3.
Таблица 2.3
34
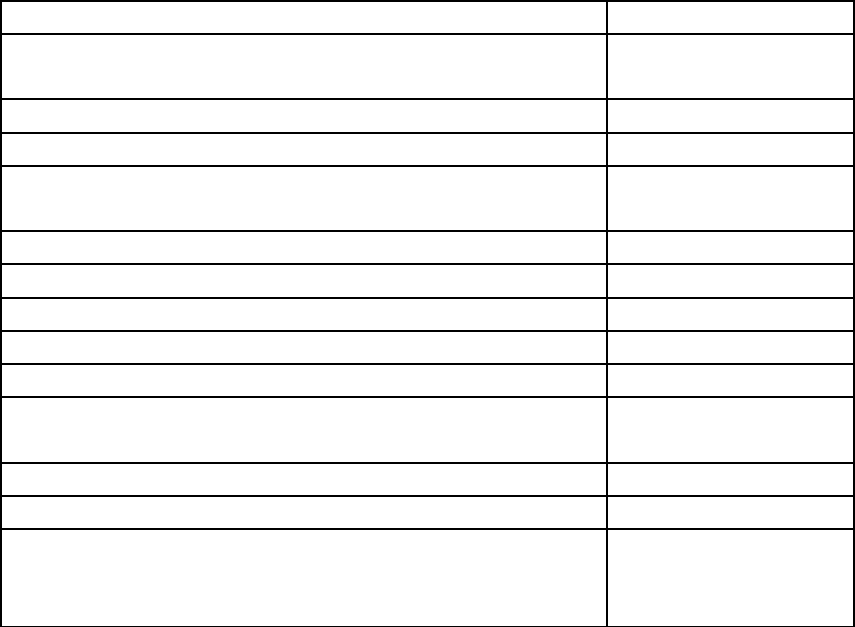
Растворимость ТАТНБ в органических растворителях
(мг в 1000 г растворителя)
Растворитель Растворимость
Метансульфокислота
820
Гексаметилфосфортриамид 150
Этансульфокислота 120
Диметилсульфоксид 70,
0,047% при 21
0
С
N-Метил-2-пирролидон 58
Диметилформамид 27
Концентрированная азотная кислота 14
Пиридин 12
Ацетон 3
Ацетонитрил, уксусный ангидрид,
трифторуксусная кислота
2
Уксусная кислота 1
25% раствор Bu
4
NOH в метаноле 390
Концентрированная серная кислота,
хлорсульфоновая кислота, фторсульфоновая
кислота, трифторметилсульфокислота
>200
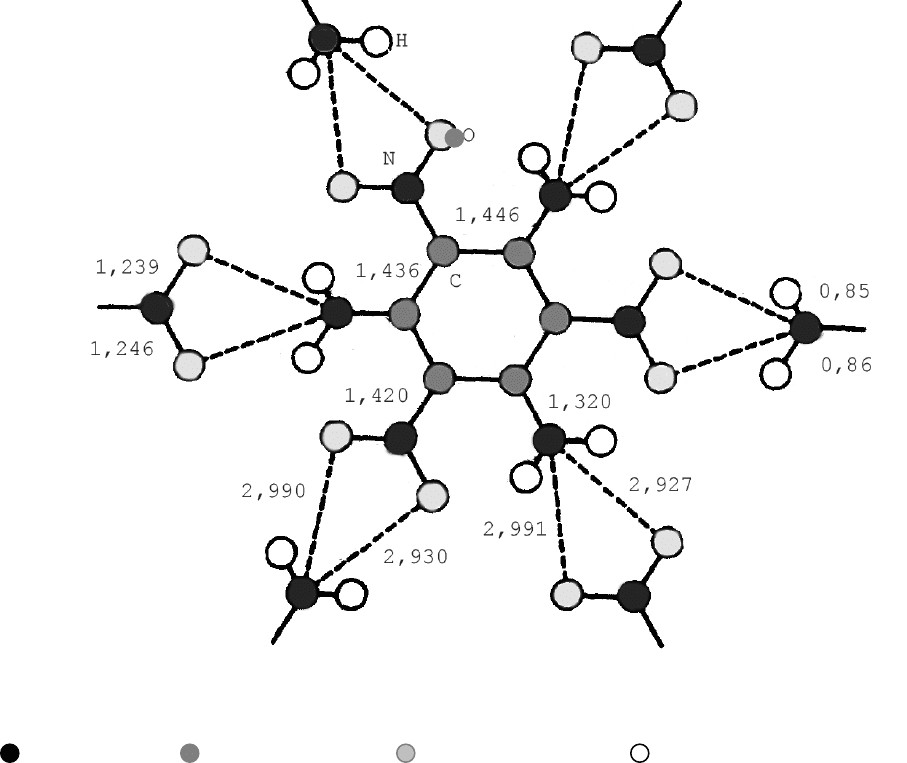
Cтруктура ТАТНБ представлена на рис 2.1
[64,65]. Для нее
характерны очень длинные С – С –связи бензольного кольца, очень
короткие С – N –(амино) связи и 6 зафиксированных водородных связей у
каждой молекулы с окружающими ее молекулами. Межмолекулярное
взаимодействие приводит к образованию графитоподобной структуры.
Вследствие этого ТАТНБ очень плохо растворим практически во всех
органических растворителях.
Изучение структуры ТАТНБ при повышении температуры от 214
до 377 К показало, что молекулярный объем увеличивается на 5,1%,
причем изменение свойств происходит анизотропно.
35
По рентгеновским данным кристаллическая структура ТАТНБ
трехклинная, ячейка состоит из двух молекул: Р1 а = 9,010, в = 9,028, с =
6,812А; α = 108,59
0
, β = 91,82
0
, χ = 119,97
0
.
Для количественного анализа используют методы неводного титрования
и УФ-спектрометрии. Определение суммарного содержания аминов в
ТАТНБ включает длительную обработку последнего (~ 0,003 моль) 0,1 н
раствором хлорной кислоты в уксусной кислоте в течение 48 ч.
Полученный раствор выливают в избыток калиевой соли фталевой
кислоты и методом обратного титрования раствором хлорной кислоты в
уксусной кислоте определяют точку эквивалентности. Точность
определения 0,1%.
Рис. 3.1. Структура молекулы ТАТНБ
(показаны связи с соседними молекулами, длины связей в Å,
–атом азота, – атом углерода, – атом кислорода, – атом водорода )
36
Спектрометрический метод анализа разработал Д. Гловер. ТАТНБ
растворяют в концентрированной серной кислоте и определяют
поглощение при длинах волн 325 и 272 нм. Интенсивность поглощения на
первой из них в 1,93–1,97 раза выше, чем на второй.
В ИК-спектрах наиболее интенсивное поглощение наблюдается в
области 1180–1240 см
-1
(2 полосы). Характерные полосы нитрогруппы
слабо выражены и сильно смещены – 1450 и 1570 см
-1
; две полосы N-H-
связей находятся при 3200 и 3300см
-1
.
2.2. Получение в лаборатории и в промышленности
Впервые ТАТНБ был синтезирован при нитровании 1,3,5-
трихлорбензола олеумно-азотной кислотной смесью и последующем
замещении атомов хлора на аминогруппу под действием аммиака. Позднее
B. Flurscheim и H. Hоlmes получили его при действии 10% водного
аммиака на пентанитроанилин. В 50-е годы в США для его получения
использовали также 1,3,5-трибром-2,4,6-тринитробензол.
Так как 1,3,5-трихлорбензол является малодоступным соединением
и его получают диазотированием трихлоранилина, в МХТИ им. Д. И.
Менделеева к 1960 г. был разработан альтернативный метод получения
ТАТНБ, основанный на окислении трихлоранилина персульфатом
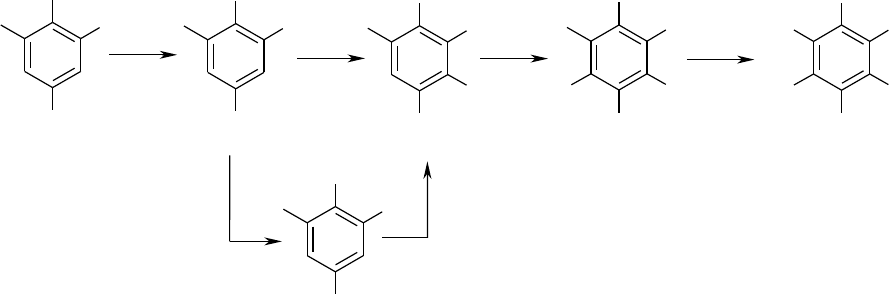
аммония в среде серной кислоты и метанола. Синтез проводили в
соответствии со схемой, приведенной ниже [66].
При получении трихлорнитрозобензола использовали следующую
методику: 10 г (0,05 моль) 2,4,6-трихлорбензола растворяли в смеси 28 г
метанола и 14 г H
2
SO
4
и при 30
0
С присыпали 46,4 г (0, 2 моль)
персульфата аммония и выдерживали 10 ч при 30
0
С. После охлаждения
полученный продукт отфильтровывали, промывали метанолом, водой и
снова метанолом и сушили при 100
0
С. Получали 9,25 – 9,30 г 2,4.6-
37
трихлорнитрозобензола. Выход 86,5%, температура плавления 141 –
142
0
С.
NH
2
Cl
Cl
Cl
Cl
Cl
Cl
NO
Cl
Cl
Cl
NO
2
NO
2
Cl
Cl
Cl
NO
2
NO
2
O
2
N
NH
2
NH
2
NH
2
NO
2
NO
2
O
2
N
Cl
Cl
Cl
NO
2
Позднее в США
[67,68]
и в СССР [69] были разработаны другие
варианты получения трихлорнитрозобензола, основанные на
использовании пероксида водорода вместо персульфата аммония.
Одновременно разрабатывались альтернативные методы получения
ТАТНБ и параллельно с ним – 1,3-диамино-2,4,6-тринитробензол
(ДАТНБ). Так, Бензигер [70] разработал метод получения ТАТНБ из 3,5-
дихлоранизола через тринитропроизводное. В МХТИ [71] при получении
ДАТНБ из тетранитроанилина для уменьшения количества примесей,
образующихся на стадии аминирования, первоначально получали 3-
амино-2,4,6-тринитроанизол и лишь затем проводили аминирование.
В качестве альтернативного можно рассматривать и
усовершенствованный Аткинсом [72] метод Флюршейма, в соответствии
с которым ТАТНБ получают из 2,4,6-ТНТ через 4-амино-2,6-
динитротолуол и пентанитроанилин. В конечном продукте присутствуют
в качестве примеси полинитроаминофенолы. В предлагаемом процессе
38
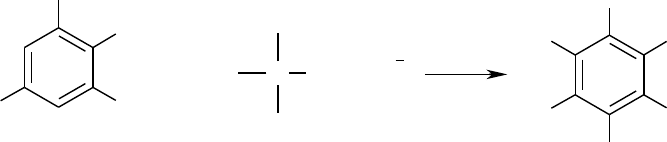
используются недорогие реагенты, но велики затраты, связанные с
обезвреживанием отходов.
В последние годы предложен ряд новых методов получения
ТАТНБ, в которых отказались от использования малодоступного 1,3,5-
тринитро-2,4,6-трихлорбензола. В основе этих процессов лежит
нуклеофильное замещение водорода в основных средах.
В Лаборатории им. Лоуренса в Ливерморе США разработан метод,
основанный на реакции иодида 1,1,1-триметилгидразиния с пикрамидом
в среде диметилсульфоксида (ДМСО) при комнатной температуре.
NH
2
NO
2
NO
2
O
2
N
N
+
NH
2
I
NH
2
NO
2
NO
2
O
2
N
NH
2
NH
2
+
*
Рассматриваемый процесс был создан в рамках программы по
утилизации устаревших боеприпасов. В России имелось около 30000 т
подлежащего уничтожению 1,1-диметилгидразина, а в США – несколько
тысяч тонн взрывчатого вещества «D»
_
пикрата аммония, который может
быть превращен в пикрамид [73].
Реакцию проводят в условиях большого избытка аминирующего
агента (4–5 моль на 1 моль пикрамида) и основания (10 моль). При этом
выход ТАТНБ достигает 89%, а чистота его более 99%. Уменьшение
расхода иодида 1,1,1-триметилгидразиния до 3,1 моль снижает выход до
81%. На качество получаемого продукта сильное влияние оказывает
концентрация пикрамида в растворе. При ее увеличении до 0,2 моль/л
чистота продукта снижается до 97%. Основной примесью в продукте
является диаминотринитробензол, в некоторых образцах зафиксировано
присутствие иода. Процесс характеризуется большим расходом
растворителя (до 40 мас. частей на 1 мас. часть пикрамида), и поэтому
39
ТАТНБ находится в растворе. Реакцию прекращают, разбавляя
реакционную смесь водой или водным раствором минеральной кислоты.
При этом образуются частицы ТАТНБ с размером 0,2 – 1 мкм. При
добавлении органической кислоты (моногидрата лимонной кислоты)
размер частиц увеличивается до 1–10µ ., и продукт имеет более светлую
окраску.
Для синтеза можно использовать как товарный иодид 1,1,1-
триметилгидразиния, так и приготовленный непосредственно перед
синтезом, при добавлении к ДМСО последовательно диметилгидразина и
метилиодида и соответствующей выдержке. Затем к полученному раствору
прибавляют пикрамид, потом щелочь и продолжают реакцию до
завершения.
Выход при обеих методиках близок между собой и составляет
82–88%. Позднее было показано, что в этом процессе метилиодид может
быть заменен более дешевым диметилсульфатом, что одновременно
исключает наличие атомов галогена в ТАТНБ [74,75].
В качестве основания используют метилат или этилат натрия,
причем чистота последних (содержание в них соды) сильно влияет на
выход ТАТНБ. Даже непродолжительное пребывание метилата натрия на
воздухе приводит к существенному снижению выхода целевого продукта.
На качество ТАТНБ сильное влияние оказывают примеси в
пикрамиде, в первую очередь, тринитрохлорбензол (из которого, получали
пикрамид). Их присутствие приводит к значительному потемнению
продукта и изменению его кристаллической структуры.
Полученный этим методом ТАТНБ по всем рабочим
характеристикам подобен продукту, изготовленному из 1,3,5-трихлор-2,4,6-
тринитробензола (ТХТНБ), однако температура разложения, определенная
40
