Сталл Д. Вестрам Э. Зинке Г. Химическая термодинамика органических соединений
Подождите немного. Документ загружается.

342
Часть
2. Термические и
термохимические
свойства
вещесте
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Температуры переходов отобраны Россини, Питцером, Арнеттом,
Брауном
и
Пиментелом [12481.
Тт = 236,70° К и ТЪ = 439,20° К.
№
250.
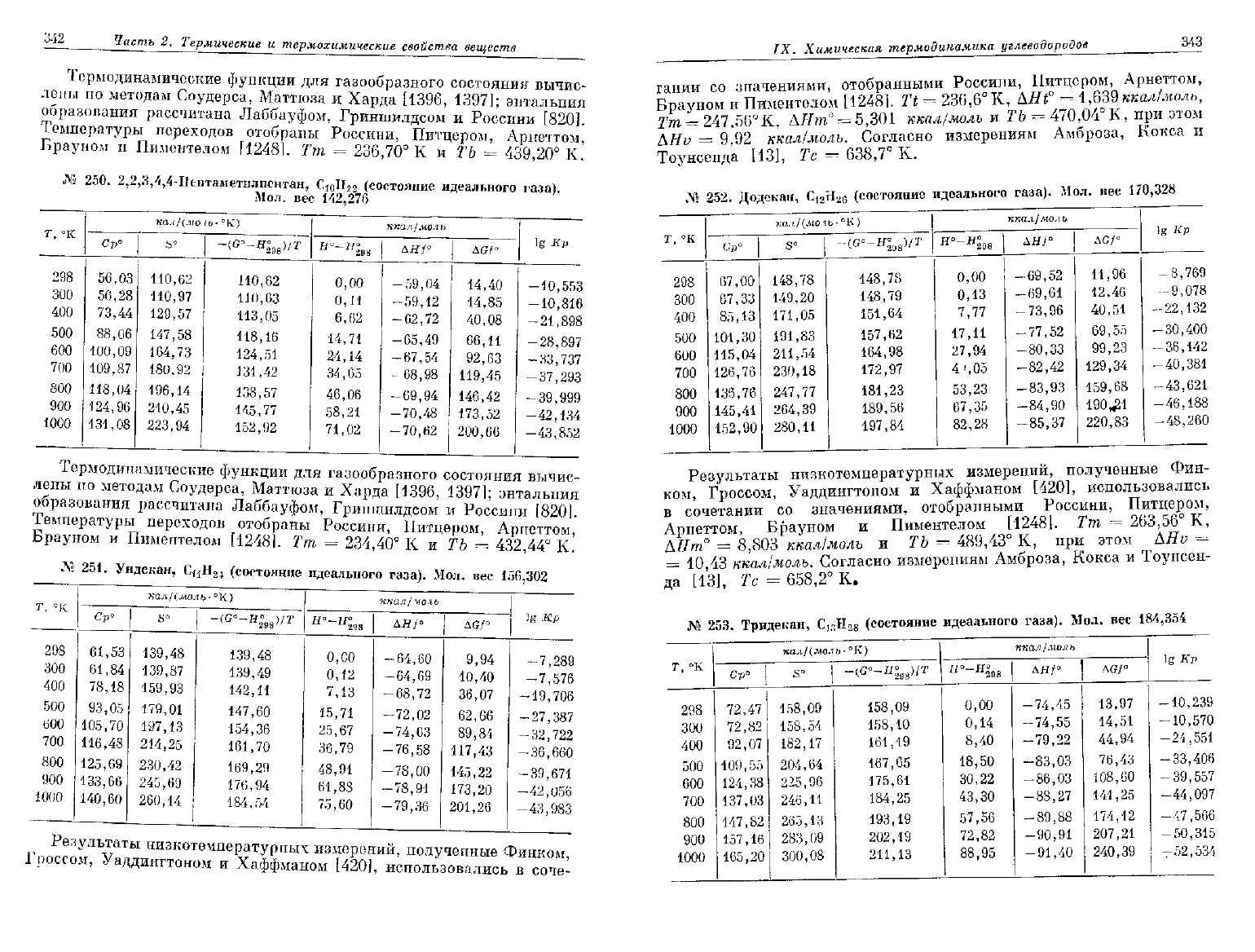
2,2,3,4,4-Пентаметилпентан, СюН
2
-> (состояние идеального газа).
Мол.
вес
142,276
т
°к
298
300
400
500
600
700
800
900
1000
Ср"
56,03
56,28
73,44
88,06
100,09
109,87
118,04
124,96
131,08
кал/(мо
о
110,62
110,97
129,57
147,58
164,73
180,92
196,14
210,45
223,94
!Ь-°К)
-(G°-H°
98
)/r
110,62
110,63
113,05
118,16
124,51
131,42
138,57
145,77
152,92
ккал/моль
0,00
0,11
6,62
14,71
24,14
34,65
46,06
58,21
71,02
ля/°
-59,04
-59,12
-62,72
-65,49
-67,54
-
68,98
-69,94
-70,48
-70,62
|
AGf
14,40
14,85
40,08
66,11
92,63
119,45
146,42
173,52
200,66
lg Кр
-10,553
-10,816
-21,898
-28,897
—
33,737
-37,293
-39,999
-42,134
-43,852
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Грипшилдсом
и
Россини [820].
Температуры переходов отобраны Россини, Питцером, Арнеттом,
Брауном
и
Пиментелом [1248].
Тт = 234,40° К и ТЪ = 432,44° К.
№
251.
Ундекан,
CjfH^
(состояние
идеального
газа).
Мол. вес
156,302
Т, °К
298
300
400
500
600
700
800
900
1000
кал/(моль-°К)
Ср°
61,53
61,84
78,18
93,05
105,70
116,48
125,69
133,66
140,60
139,48
139,87
159,93
179,01
197,13
214,25
230,42
245,69
260,14
139,48
139,49
142,11
147,60
154,36
161,70
169,29
176,94
184,54
пкал/мо
Н°-Н°
дя/°
AGf
Ig
Кр
о,со
0,12
7,13
15,71
25,67
36,79
48,91
61,83
75,60
-64,60
-64,69
-68,72
-72,02
-74,63
-76,58
-78,00
-78,91
-79,36
9,94
10,40
36,07
62,66
89,84
117,43
145,22
173,20
201,26
-7,289
-7,576
-19,706
-27,387
-32,722
-36,660
-39,671
-42,056
-43,983
Результаты низкотемпературных измерений, полученные Финном
Гроссом, Уаддингтоном
и
Хаффманом [420], использовались
в
co*S
I
IX. Химическая
термодинамика
углеводородов
343
тании
со
значениями, отобранными Россини, Питцером, Арнеттом,
Брауном
и
Пиментелом [12481.
Tt = 236,6° К,
AHt°
= 1,639
ккал/моль,
Тт
=
247,58°К,
A#m°
= 5,301
ккал/молъ
и
ТЪ
= 470,04° К, при
этом
АЯУ
= 9,92
ккал/молъ. Согласно измерениям Амброза, Кокса
и
Тоунсенда
[13], Тс = 638,7° К.
№
252.
Додекан, С
12
Н
2
д (состояние идеального газа).
Мол. вес
170,328
г,
°к
298
300
400
500
600
700
800
900
1000
кал/(мо
гь-°К)
Ср°
67,00
67,33
85,13
101,30
115,04
126,76
136,76
145,41
152,90
S-
148,78
149,20
171,05
191,83
211,54
230,18
247,77
264,39
280,11
-<G°-H;
M
>/T
148,78
148,79
151,64
157,62
164,98
172,97
181,23
189,56
197,84
кпал/моль
Н
°~
Н
208
|
0,00
0,13
7,77
17,11
27,94
4i,05
53,23
67,35
82,28
дн/°
-69,52
-69,61
-73,96
-77,52
-80,33
-82,42
-83,93
-84,90
-85,37
AGf
11,96
12,46
40,51
69,55
99,23
129,34
159,68
190^1
220,83
lg Кр
-8,769
-9,078
-22,132
-30,400
-36,142
-40,381
-43,621
-46,188
-48,260
Результаты низкотемпературных измерений, полученные
Фин-
ком,
Гроссом, Уаддингтоном
и
Хаффманом [420], использовались
в сочетании
со
значениями, отобранными Россини, Питцером,
Арнеттом, Брауном
и
Пиментелом [1248].
Тт = 263,56° К,
&Нт°
= 8,803
ккал/молъ
и ТЪ = 489,43° К, при
этом
AHv =
=
10,43
ккал/моль. Согласно измерениям Амброза, Кокса
и
Тоунсен-
да
[13], Тс = 658,2° К.
№
253.
Тридекан,
Ci
3
H
2
8
(состояние
идеального
газа).
Мол. вес
184,354
Т, "К
298
300
400
500
600
700
800
900
1000
кал/(ли>ль-°К)
Ср°
72,47
72,82
92,07
109,55
124,38
137,03
147,82
157,16
165,20
s°
158,09
158,54
182,17
204,64
225,96
246,11
265,13
283,09
300,08
158,09
158,10
161,19
167,65
175,61
184,25
193,19
202,19
211,13
пугал
1
моль
Н
°~
Н
298
0,00
0,14
8,40
18,50
30,22
43,30
57,56
72,82
88,95
АН/
0
]
-74,45
-74,55
-79,22
-83,03
-86,03
-88,27
-89,88
-90,91
-91,40
AGf°
13,97
14,51
44,94
76,43
108,60
141,25
174,12
207,21
240,39
-10,239
-10,570
-24,551
-33,406
-39,557
-44,097
-47,566
-50,315
-52,534
344
Часть
2.
Термические
и
термохимические
свойства
веществ
Результаты низкотемпературных измерений, полученные
Фин-
ном,
Гроссом, Уаддингтоном
и
Хаффманом [420], использовались
в
сочетании
со
значениями, отобранными Россини, Питцером,
Арнеттом, Брауном
и
Пиментелом [1248].
Tt =
255,0°
К,
AHf =
=
1,831
ккал/молъ,
Тт =
267,78°
К,
АНт°
=
6,812
ккалЫолъ
и
ТЪ
=
508,58°
К,
при
этом
AHv =
10,91
ккал/молъ.
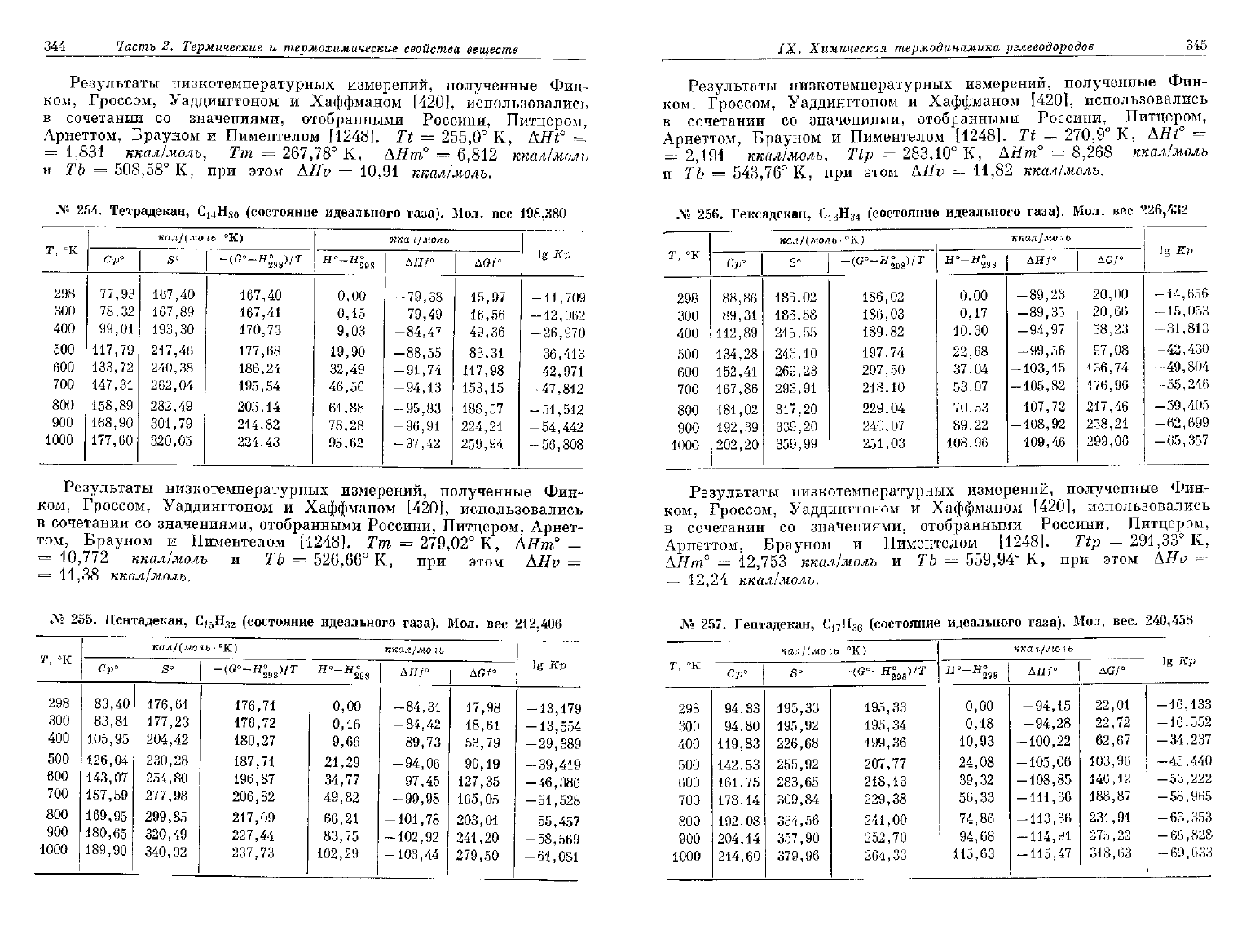
JV° 254.
Тетрадекан, С
14
Н
30
(состояние идеального газа).
Мол.
вес
198,380
IX. Химическая
термодинамика
углеводородов
345
298
300
400
500
600
700
800
900
1000
кал/(мо
1Ь
°К)
Ср°
77,93
78,32
99,01
117,79
133,72
147,31
158,89
168,90
177,60
s°
167,40
167,89
193,30
217,46
240,38
262,04
282,49
301,79
320,05
-(
е
°-
Я
2о
8
^
г
167,40
167,41
170,73
177,68
186,24
195,54
205,14
214,82
224,43
кка
ь/моль
0,00
0,15
9,03
19,90
32,49
46,56
61,88
78,28
95,62
дн/°
-79,38
-79,49
-84,47
-88,55
-91,74
-94,13
-95,83
-96,91
-97,42
AGf°
15,97
16,56
49,36
83,31
117,98
153,15
188,57
224,21
259,94
lg
Kv
-11,709
-12,062
-26,970
-36,413
-42,971
-47,812
-51,512
-54,442
-56,808
Результаты низкотемпературных измерений, полученные
Фин-
ном,
Гроссом, Уаддингтоном
и
Хаффманом [420], использовались
в
сочетании
со
значениями, отобранными Россини, Питцером, Арнет-
том, Брауном
и
Пиментелом [1248].
Тт =
279,02°
К,
АНт°
=
=
10,772
ккал/молъ
и
ТЪ
=
526,66°
К,
при
этом
AHv =
=
11,38
ккал/молъ.
Л»
255.
Пентадекан,
С15Н32
(состояние
идеального
газа).
Мол.
вес
212,406
298
300
400
500
600
700
800
900
1000
Ср"
83,40
83,81
105,95
126,04
143,07
157,59
169,95
180,65
189,90
пал/(МОЛЬ•
S"
176,61
177,23
204,42
230,28
254,80
277,98
299,85
320,49
340,02
°К)
-(G°-
176
176
180
187
196
206
217
227
237
,71
,72
,27
,71
,87
,82
,09
,44
,73
я°-
0
0,
9,
21,
34,
49,
66,
83,
102,
Н
298
00
16
66
29
77
82
21
75
29
ккал/моib
AHf
-84,31
-84,42
-89,73
-94,06
-97,45
-99,98
-101,78
-102,92
-103,44
AGf"
17
18
53
90
127
165
203
241
279
,98
,61
,79
,19
,35
,05
,01
,20
,50
lg
Кр
-13,179
-13,554
-29,389
-39,419
-46,386
-51,528
-55,457
-58,569
-61,081
Результаты низкотемпературных измерений, полученные
Фин-
ном,
Гроссом, Уаддингтоном
и
Хаффманом [420], использовались
в
сочетании
со
значениями, отобранными Россини, Питцером,
Арнеттом, Брауном
и
Пиментелом [1248].
Tt =
270,9° К,
AHf =
=
2,191
ккал/молъ,
Ttp =
283,10°
К,
АНт°
=
8,268
ккал/молъ
и
ТЪ
=
543,76°
К,
при
этом
AHv —
11,82
ккал/молъ.
№
256.
Гексадекан,
С
Т, °К
298
300
400
500
600
700
800
900
1000
16
Н
3
4
(состояние
кал/(моль •
°К)
Ср°
88,86
89,31
112,89
134,28
152,41
167,86
181,02
192,39
202,20
8-
186,02
186,58
215,55
243,10
269,23
293,91
317,20
339,20
359,99
-(G'-H^/T
186,02
186,03
189,82
197,74
207,50
218,10
229,04
240,07
251,03
идеального
газа).
Мол.
вес
226,432
ккал/мол
ь
Н
°~
Н
298
0,00
0,17
10,30
22,68
37,04
53,07
70,53
89,22
108,96
дн/°
-89,23
-89,35
-94,97
-99,56
-103,15
-105,82
-107,72
-108,92
-109,46
AGf°
20,00
20,66
58,23
97,08
136,74
176,96
217,46
258,21
299,00
lg
КР
-14,656
-15,053
-31,813
-42,430
-49,804
-55,246
-59,405
-62,699
-65,357
Результаты низкотемпературных измерений, полученные
Фин-
ном,
Гроссом, Уаддингтоном
и
Хаффманом [420], использовались
в
сочетании
со
значениями, отобранными Россини, Питцером,
Арнеттом, Брауном
и
Пимептелом [1248].
Ttp =
291,33°
К,
АНт°
=
12,753
ккал/молъ
и
ТЪ
=
559,94°
К,
при
этом
AHv
=-
=
12,24
ккал/молъ.
№
257.
Гептадекан,
С
17
Н
36
(состояние
идеального
газа).
Мол.
вес.
240,458
т,
°к
298
300
400
500
600
700
800
900
1000
калЦмо
1Ь
°К)
Ср"
94,33
94,80
119,83
142,53
161,75
178,14
192,08
204,14
214,60
S°
|
-(G'-HJ^/r
195,33
195,92
226,68
255,92
283,65
309,84
334,56
357,90
379,96
195,33
195,34
199,36
207,77
218,13
229,38
241,00
252,70
264,33
тто
ЕГО
Ы
~
Й
298
0,00
0,18
10,93
24,08
39,32
56,33
74,86
94,68
115,63
ккаг/могь
AHf
-94,15
-94,28
-100,22
-105,06
-108,85
-111,66
-113,66
-114,91
-115,47
AGf
22,01
22,72
62,67
103,96
146,12
188,87
231,91
275,22
318,63
lg
Кр
-16,133
-16,552
-34,237
-45,440
-53,222
-58,965
-63,353
-66,828
-69,033
346
Часть
2.
Термические
и
термохимические
свойства
веществ
значения,
отобранные
Россини,
том,
Брауном
и
Пиментелом
[1248].
АНт° =-
9,676
ккал/молъ
и
ТЪ
=
575,30°
К,
=
12,64
ккал/молъ.
Питцером,
Арнет-
Ттп
=
295,14°
К,
при
этом
AHv =
А«
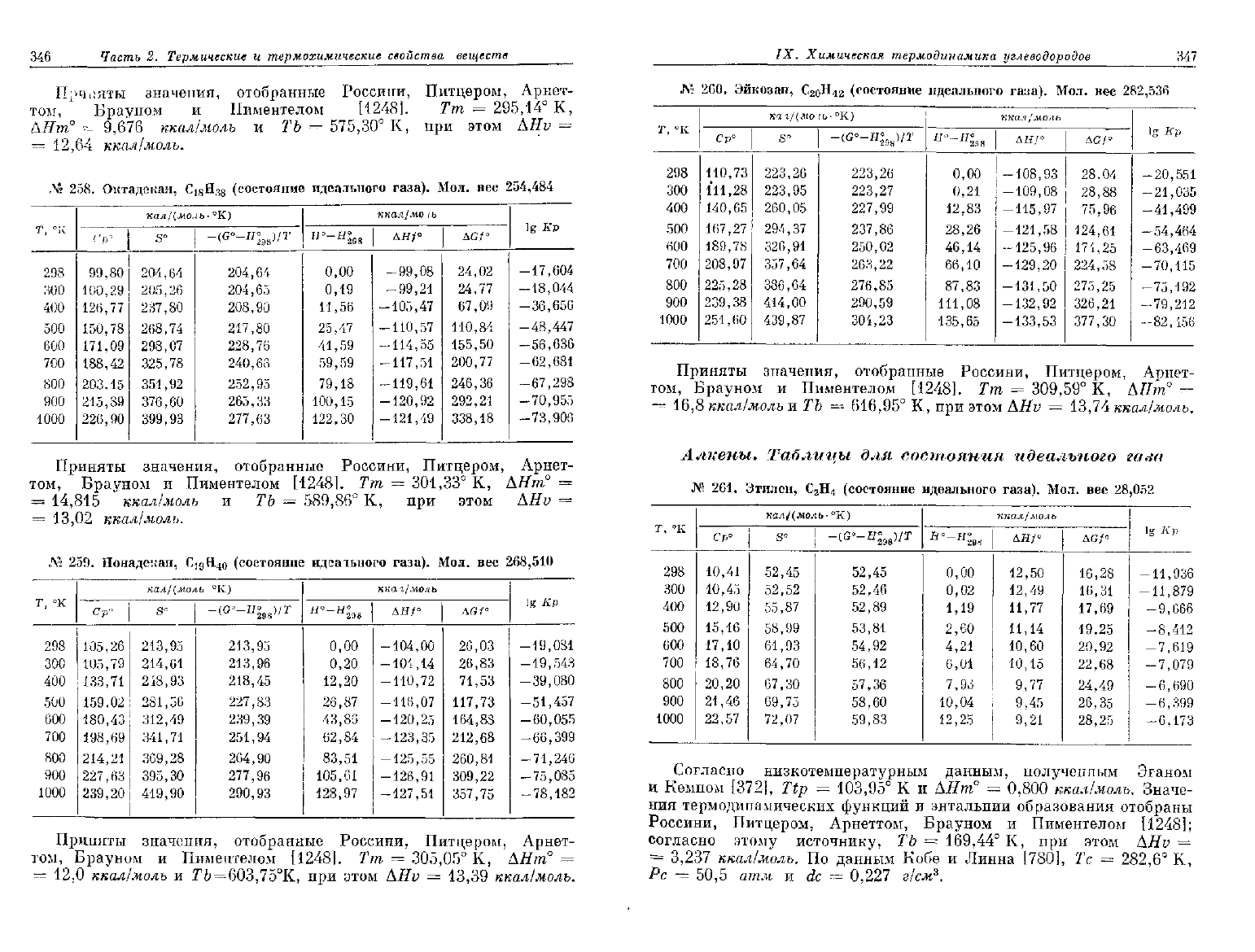
258.
Октадекан,
С
т\
°к
298
300
400
500
600
700
800
900
1000
8
Н
3
8
(состояние
кал/(мо.1ь-"К)
99,80
100,29
126,77
150,78
171,09
188,42
203,15
215,89
226,90
s°
204,64
205,26
237,80
268,74
298,07
325,78
351,92
376,60
399,93
-(С°-Н°
э8
)/Г
204,64
204,65
208,90
217,80
228,76
240,66
252,95
265,33
277,63
идеального
газа).
Мол.
вес
2о4,484
ккал/мо
!Ь
Н
°~
Н
298
0,00
0,19
11,56
25,47
41,59
59,59
79,18
100,15
122,30
ЛЯ/»
-99,08
-99,21
-105,47
-110,57
-114,55
-117,51
-119,61
-120,92
-121,49
AGf°
24,02
24,77
67,09
110,84
155,50
200,77
246,36
292,21
338,18
lg
Kp
-17,604
-18,044
-36,656
-48,447
-56,636
-62,681
-67,298
-70,955
-73,906
Приняты
значения,
отобранные
Россини,
Питцером,
Арнет-
том,
Брауном
и
Пиментелом
[1248].
Тт =
301,33°
К,
АНт°
=
=
14,815 ккал/молъ
и
ТЪ
=
589,86°
К,
при
этом
AHv
=
=
13,02
ккал/молъ.
Л»
259.
Нонадекан,
С
1д
Н
40
(состояние
г,
°к
298
300
400
500
600
700
800
900
1000
105,26
105,79
133,71
159,02
180,43
198,69
214,21
227,63
239,20
кал/(моль
°К)
S
0
213,95
214,61
218,93
281,56
312,49
341,71
369,28
395,30
419,90
-(G°-H°
98
)/r
213,95
213,96
218,45
227,83
239,39
251,94
204,90
277,96
290,93
идеачьного
газа).
Мол.
вес
268,510
кпа
г/моль
Я
°-
Н
298
0,00
0,20
12,20
26,87
43,85
62,84
83,51
105,01
128,97
AHf
-104,00
-101,14
-110,72
-116,07
-120,25
-123,35
-125,55
-126,91
-127,51
AGf°
26,03
26,83
71,53
117,73
164,88
212,68
260,81
309,22
357,75
ig
Kp
-19,031
-19,543
-39,080
-51,457
-60,055
-66,399
-71,246
-75,085
-78,182
Приняты
значения,
отобранные
Россини,
Питцером,
Арнет-
том,
Брауном
и
Пиментелом
[1248].
Тт =
305,05°
К,
АЯтп°
=
=
12,0
ккал/молъ
и
7
т
Ь=603,75°К,
при
этом
AHv =
13,39
ккал/молъ.
IX. Химическая
термодинамика
углеводородов
347
г,
°к
298
300
400
500
600
700
800
900
1000
260.
Эйкозан,
С
2
с
Ср°
110,73
111,28
140,65
167,27
189,78
208,97
225,28
239,38
251,60
н
па г/(мо
ib
со
223,26
223,95
260,05
294,37
326,91
357,64
386,64
414,00
439,87
42
(состояние
"К)
-(G°-H°
29S
)/T
223,26
223,27
227,99
237,86
250,02
263,22
276,85
290,59
304,23
идеального
газа).
Мол.
вес
0,
0,
12,
28,
46,
66,
87,
111,
135,
f
298
00
21
83
26
14
10
83
08
65
ккал/моль
ДЯ/°
-108,93
-109,08
-115,97
-121,58
-125,96
-129,20
-131,50
-132,92
-133,53
AGf°
28.04
28,88
75,96
124,61
174,25
224,58
275,25
326,21
377,30
282,536
lg
Kp
-20,551
-21,035
-41,499
-54,464
-63,469
-70,115
-75,192
-79,212
-82,156
Приняты
значения,
отобранные
Россини,
Питцером,
Арнет-
том,
Брауном
и
Пиментелом
[1248].
Тт =
309,59°
К,
АНт°
=
=
16,8
ккал/молъ
жТЪ
=
616,95°
К,
при
этом
AHv
=
13,74 ккал/молъ.
Алпены. Таблицы для состояния идеального газа
№
261.
Этилен,
С
2
Н
4
(состояние
идеального
газа).
Мол.
вес
28,052
Г,
"К
298
300
400
500
600
700
800
900
1000
Ср°
10,41
10,45
12,90
15,16
17,10
18,76
20,20
21,46
22,57
KQ.JI^(MQJ
со
52,45
52,52
55,87
58,99
61,93
64,70
67,30
69,75
72,07
ь-»К)
-(
6
°-
Я
298^
Т
52,45
52,46
52,89
53,81
54,92
56,12
57,36
58,60
59,83
ккал/моль
Я
°-
Я
298
0,00
0,02
1,19
2,60
4,21
6,01
7,9о
10,04
12,25
дя/°
12,50
12,49
11,77
11,14
10,60
10,15
9,77
9,45
9,21
AGf°
16,28
16,31
17,69
19,25
20,92
22,68
24,49
26,35
28,25
lg
Kp
-11,936
-11,879
-9,666
-8,412
-7,619
-7,079
-6,690
-6,399
-6,173
Согласно
низкотемпературным
данным,
полученным
Эганом
и
Кемпом
[3721,
Ttp =
103,95°
К и
АНт°
=
0,800
ккал/молъ.
Значе-
ния
термодинамических
функций
и
энтальпии
образования
отобраны
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248];
согласно
этому
источнику,
ТЪ
=
169,44°
К,
при
этом
AHv =
=
3,237
ккал/молъ.
По
данным
Кобе
и
Линна
[780],
Тс —
282,6°
К,
Рс
-=
50,5
атм и dc =
0,227
г/см
3
.
348
Часть
2.
Термические
и
термохимические
свойства
веществ
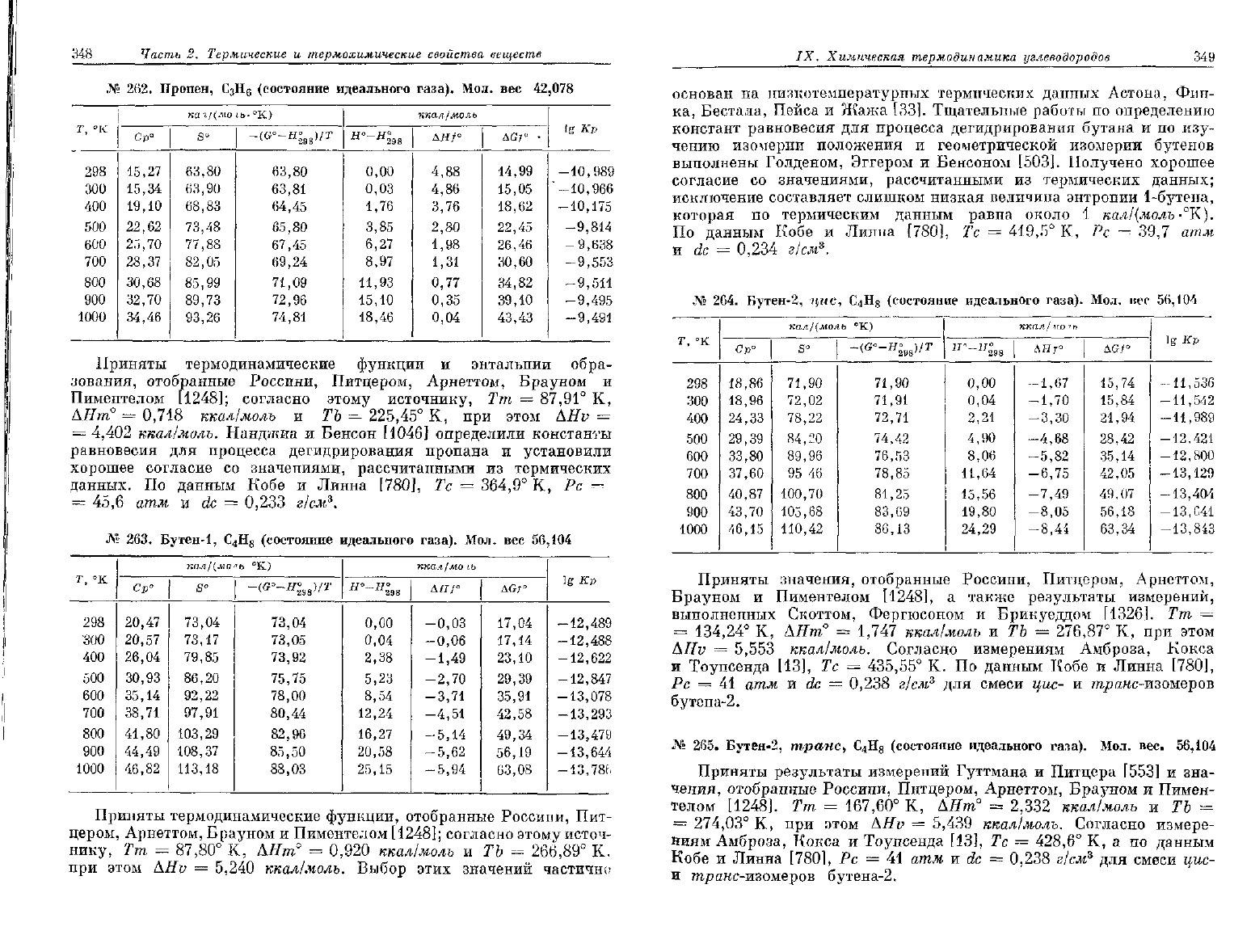
№
262.
Пропен, С
3
Н
6
(состояние идеального газа). Мол.
вес
42,078
т,
°к
298
300
400
500
600
700
800
900
1000
Ср°
15,27
15,34
19,10
22,62
25,70
28,37
30,68
32,70
34,46
каг/(мо
s°
63,80
63,90
68,83
73,48
77,88
82,05
85,99
89,73
93,26
1Ъ-°К)
63,80
63,81
64,45
65,80
67,45
69,24
71,09
72,96
74,81
ккал/моль
Н
°-
Я
298
0,00
0,03
1,76
3,85
6,27
8,97
11,93
15,10
18,46
дн/°
4,88
4,86
3,76
2,80
1,98
1,31
0,77
0,35
0,04
AG;
0
•
14,99
15,05
18,62
22,45
26,46
30,60
34,82
39,10
43,43
lg
Кр
-10,989
-10,966
-10,175
-9,814
-9,638
-9,553
-9,511
-9,495
-9,491
Приняты
термодинамические функции
и
энтальпии обра-
зования,
отобранные Россини, Питцером, Арнеттом, Брауном
и
Пиментелом [1248]; согласно этому источнику, Ттп
=
87,91°
К,
АНтп°
—
0,718
ккал/молъ
и
ТЪ
=•
225,45°
К, при
этом
AHv =
=
4,402
ккал/молъ. Нанджиа
и
Бенсон
[1046]
определили константы
равновесия
для
процесса дегидрирования пропана
и
установили
хорошее согласие
со
значениями, рассчитанными
из
термических
данных.
По
данным Кобе
и
Линна [780],
Тс =
364,9°
К, Рс =
=
45,6 атм и dc =
0,233
г/см
3
.
№
263. Бутен-1, С
4
Н
8
(состояние идеального газа). Мол.
вес
56,104
Т, °К
298
"300
400
500
600
700
800
900
1000
Ср°
20,47
20,57
26,04
30,93
35,14
38,71
41,80
44,49
46,82
кал/(мо
73,04
73,17
79,85
86,20
92,22
97,91
103,29
108,37
113,18
'Ь
°К)
-<в°-я;
и
)/г
73,04
73,05
73,92
75,75
78,00
80,44
82,96
85,50
88,03
ккал/мо
ьь
Я
°-
Я
298
0,00
0,04
2,38
5,23
8,54
12,24
16,27
20,58
25,15
дя/°
-0,03
-0,06
-1,49
-2,70
-3,71
-4,51
-5,14
-5,62
-5,94
AGt°
17,04
17,14
23,10
29,39
35,91
42,58
49,34
56,19
63,08
lg
Кр
-12,489
-12,488
-12,622
-12,847
-13,078
-13,293
-13,479
-13,644
-13,786
Приняты
термодинамические функции, отобранные Россини, Пит-
цером, Арнеттом, Брауном
и
Пиментелом [1248]; согласно этому источ-
нику, Ттп
=
87,80°
К,
АНт°
=
0,920
ккал/молъ
и
ТЪ
=
266,89°
К.
при
этом
AHv =
5,240
ккал/молъ. Выбор этих значений частично
IX.
Химическая
термодинамика
углеводородов
349
основан
на
низкотемпературных термических данных Астона, Фин-
ка,
Бестала, Пейса
и
Жажа [33]. Тщательные работы по определению
констант равновесия
для
процесса дегидрирования бутана
и по изу-
чению изомерии положения
и
геометрической изомерии бутенов
выполнены Голденом, Эггером
и
Бенсоном [503]. Получено хорошее
согласие
со
значениями, рассчитанными
из
термических данных;
исключение составляет слишком низкая величина энтропии
1-бутена,
которая
по
термическим данным равна около
1
кал/(молъ
-"К).
По
данным Кобе
и
Линна [780],
Тс =
419,5°
К, Рс = 39,7 атм
и
dc =
0,234
г/см
3
.
№
264.
Бутен-2,
цис,
С
4
Н
8
(состояние идеального газа). Мол.
вес
56,104
г,
°к
298
300
400
500
600
700
800
900
1000
калЦмоль
°К)
Ср°
18,86
18,96
24,33
29,39
33,80
37,60
40,87
43,70
46,15
s°
71,90
72,02
78,22
84,20
89,96
95
46
100,70
105,68
110,42
71,90
71,91
72,71
74,42
76,53
78,85
81,25
83,69
36,13
ккал/
мо
ib
11
""298
0,00
0,04
2,21
4,90
8,06
11,64
15,56
19,80
24,29
ДН/°
-1,67
-1,70
-3,30
-4,68
-5,82
-6,75
-7,49
-8,05
-8,44
&Gf°
15,74
15,84
21,94
28,42
35,14
42,05
49,07
56,18
63,34
lg
Кр
-11,536
-11,542
-11,989
-12,421
-12,800
-13,129
-13,404
-13,041
-13,843
Приняты
значения, отобранные Россини, Питцером, Арнеттом,
Брауном
и
Пиментелом [1248],
а
также результаты измерений,
выполненных Скоттом, Фергюсоном
и
Брикуеддом [1326]. Ттп
=
=
134,24°
К,
АНтп°
= 1,747
ккал/молъ
и
ТЪ
=
276,87°
К, при
этом
AHv
=
5,553
ккал/молъ. Согласно измерениям Амброза, Кокса
и
Тоунсенда
[13], Тс =
435,55°
К. По
данным Кобе
и
Линна [780],
Рс
= 41 атм и dc —
0,238
г/см
3
для
смеси
цис- и
mpawc-изомеров
бутена-2.
№ 265. Бутея-2,
трапе,
С
4
Н
8
(состояние идеального газа). Мол. вес.
56,104
Приняты
результаты измерений Гуттмана
и
Питцера [553]
и
зна-
чения,
отобранные Россини, Питцером, Арнеттом, Брауном
и
Пимен-
телом [1248].
Тт =
167,60°
К,
АЯтп
0
==
2,332
ккал/молъ
и
ТЪ
=
=
274,03°
К, при
этом
AHv —
5,439
ккал/молъ. Согласно измере-
ниям
Амброза, Кокса
и
Тоунсенда [13],
Тс =
428,6°
К, а по
данным
Кобе
и
Линна [780],
Рс = 41 атм и dc —
0,238
г/см
3
для
смеси
цис-
и
торакс-изомеров бутена-2.
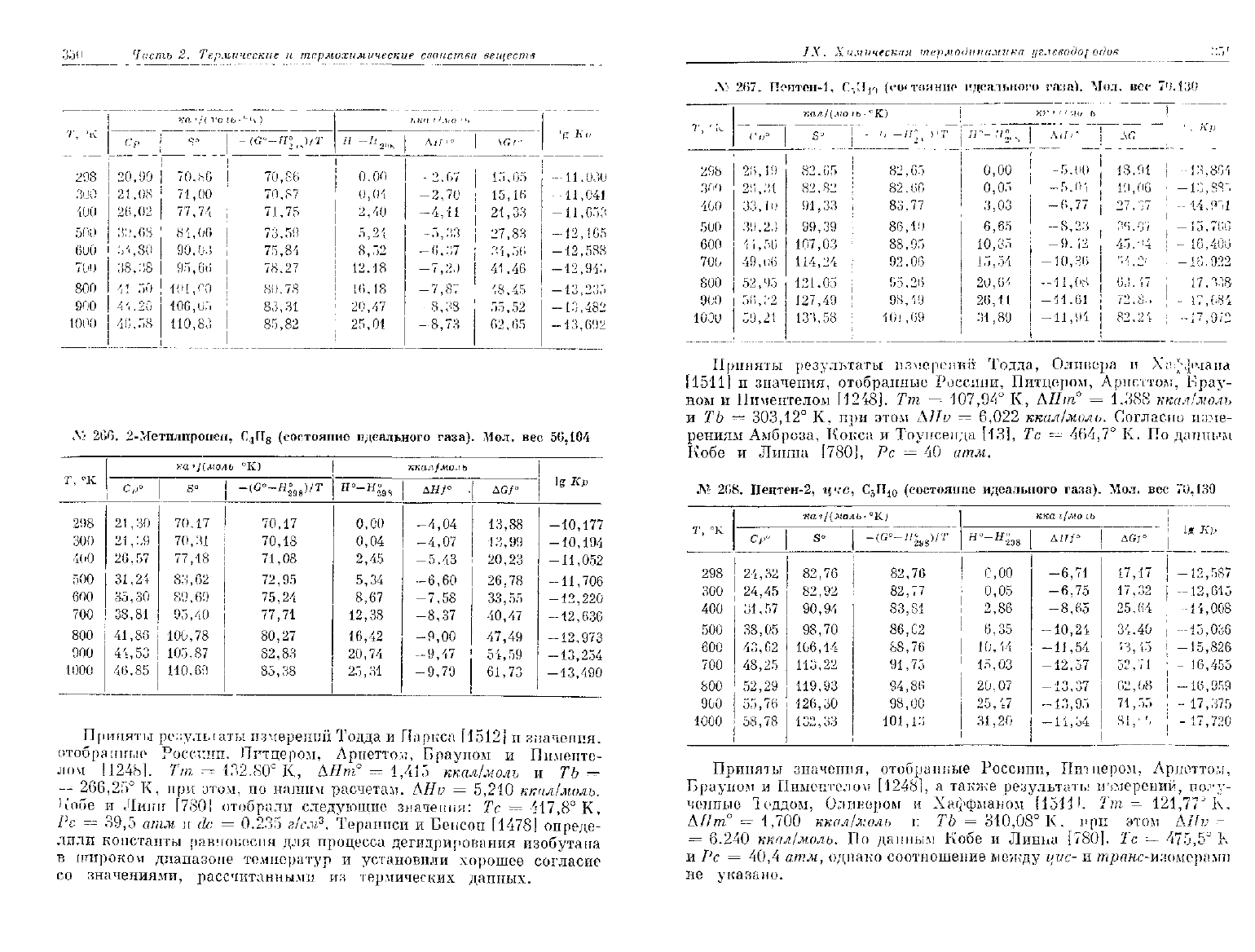
35
О
Часть
2.
Термические
и
термохимические
свойства
веществ
т,
'г:
298
300
400
500
Ср
20
21
26
з:,
1
,99
,08
,02
.63
кп
'/( то гь- '-W )
600
I
700
800
900
1000
38,38
40.58
70.bG
71,00
77,74
81,06
90,0.!
95,66
101,ГО
106,05
110,83
70,86
70.87
71,75
73.59
75,84
78,27
80.78
83,31
85,82
ttWl
>
1
Л(О ' h
0,00
0,04
2,40
5,21
8,52
12.18
16.18
20,47
25,01
All
"
-2,07
-2,70
-4,11
-5,33
-6,37
-7,20
-7,87
-8,38
-8,73
15,05
15,16
21,33
27,83
3i,56
41,46
48,45
55,52
62,65
-11,030
-11,041
-11,053
-12,165
-12,588
-12,945
-13,235
-13,482
-13,692
Л!>
206.
2-Метилпроиен,
С
4
П
8
(состояние
идеального
газа).
Мол. вес
50,104
298
300
400
500
600
700
800
900
1000
с,>°
21,30
21,39
26,57
31,24
35,30
38,81
41,86
44,53
46,85
к
а
7
/(моль
°К)
70,17
70,31
70,17
70,18
77,18 71,08
83,62
89,69
95,40
100,78
105,87
72,95
75,24
77,71
80,27
82,83
110.69
85,38
0,00
0,04
2,45
5,34
8,67
12,38
16,42
20,74
25,31
ккал/моль
ДН/°
.
-4,04
-4,07
-5.43
-6,60
-7,58
-8,37
-9,00
-9,47
-9,79
AGf°
13,88
13,99
20,23
26,78
33,55
40,47
47,49
54,59
61,73
lg
Кр
-10,177
-10,194
-11,052
-11,706
-12,220
-12,636
-12,973
-13,254
-13,490
Приняты
резулыаты
измерений
Тодда
и
Паркса
[1512]
и
значения,
отобранные
Россини.
Пгтцеро.м,
Арпеттом,
Брауном
и
Пименте-
лоч
[124Ы.
Tin =
132.80°
К,
ДЯто°
= 1,415
ккал/молъ
и ТЪ =
=
266,25°
К, при
этом,
по
нашим
расчетам.
ЛЯг; = 5,210
ккал/молъ.
^обе
и
Липн
[780!
отобрали следующие
значения:
Тс =
417,8°
К,
Рс
= 39,5 атм и dc =
0.235
г/см
3
.
Терапией
и
Бенсон
[1478] опреде-
лили
константы
равновесия
для
процесса
дегидрирования
изобутапа
в
широком
диапазоне
температур
и
установили хорошее согласие
со
значениями,
рассчитанными
из
термических данных.
/.Y.
Химическая термодинамика углеводо!
одов
.Y>
267.
Поптен-1,
С,Пп
(состояние
идеального
газа).
Мол. вес
7U.130
г,
-;..
кал/(лю
7
—:~
г
"К)
Г- ,7°
298
300
400
500
600
700
800
900
1000
j
26,
26,
49,
52,
56
Кб
95
56,32
39,21
82,65
82,82
91,33
99,39
107,03
114,24
121,05
127,49
133,58
j
82,05
82.66
83,77
86,10
88,95
92.06
95,26
98,49
101,69
0,00
0,05
3,03
6,65
10,85
15,54
20,6^
26,11
51,89
-
5ДЮ
-5.0',
-6,77
-8,23
-9.
12
-10,36
-11,08
-11.61
-11,94
18.91
19,06
27.37
36.07
45.
"4
'"•I
,2'
63.
17
!
72,8-.
I
82.24
•
' , к
Р
|
-13,864
'
-14,951
I
,
-15,760
!
-
16,406
,
-16,922
17,438
17,684
-17,9/2
Приняты
результаты
измерений
Тодда, Оливера
и ХоЛ\
[1511]
и
значения,
отобранные
Россини,
Питцером,
Арнсттом, Брау-
ном
и
Пштентелом
[1248].
Тт =
107,94°
К,
АПт°
= 1,388
ккал/молъ
и
ТЪ =
303,12°
К, при
этом
AHv —
6,022
ккал/молъ.
Согласно
изме-
рениям
Амброза,
Кокса
и
Тоунсепда
[13], Тс =
464,7°
К. По
данным
Кобе
и
Лиина
[780],
Рс = 40 атм.
JV
268.
Пентен-2,
ц>;с,
С
5
Н
10
(состояние
идеального
газа).
Мол.
вес
70,130
г,
°к
298
300
400
500
600
700
800
900
1000
ка1/(моль-°К)
СР"
24,32
24,45
31,57
38,05
43,62
48,25
52,29
55,76
58,78
S°
82,76
82,92
90,94
98,70
106,14
113,22
119,93
126,30
132,33
-(G°-u^
8
)/r
82,76
82,77
83,81
86,
С2
88,76
91,75
94,86
98,00
101,15
С,
00
0,05
2,86
6,35
10,14
15,03
20,07
25,47
31,20
кпа
i/мо ib
ДЯ/»
-6,71
-6,75
-8,65
-10,24
-11,54
-12,57
-13,37
-13,95
-14,34
AG}°
17,17
17,32
25,64
34,40
V-3,45
52,71
02,08
71,55
81,'
'.
is
Kp
-12,587
-12,015
-14,008
-15,030
-15,826
-
16,455
-16,959
-17,375
-
17,720
Приняты
значения,
отобранные
Россини,
Пшцером,
Арлеттом,
Брауном
и
Пимептелом
[1248],
а
также результаты
измерений,
полу-
ченные
1оддом, Оливером
и
Хаффманом
[151И.
Тт —
121,77°
К.
А/Ут°
= 1,700
ккол/лолъ
i: Tb =
310,08°
К. при
этом
AHv -
=
6.240
ккал/молъ.
По
данным
Fio6e
и
Линна
[780].
Тс —
475,5°
К
ж
Рс = 40,4
атм,
однако
соотношение
между цис-
и
тпракс-изомерадш
не
указано.
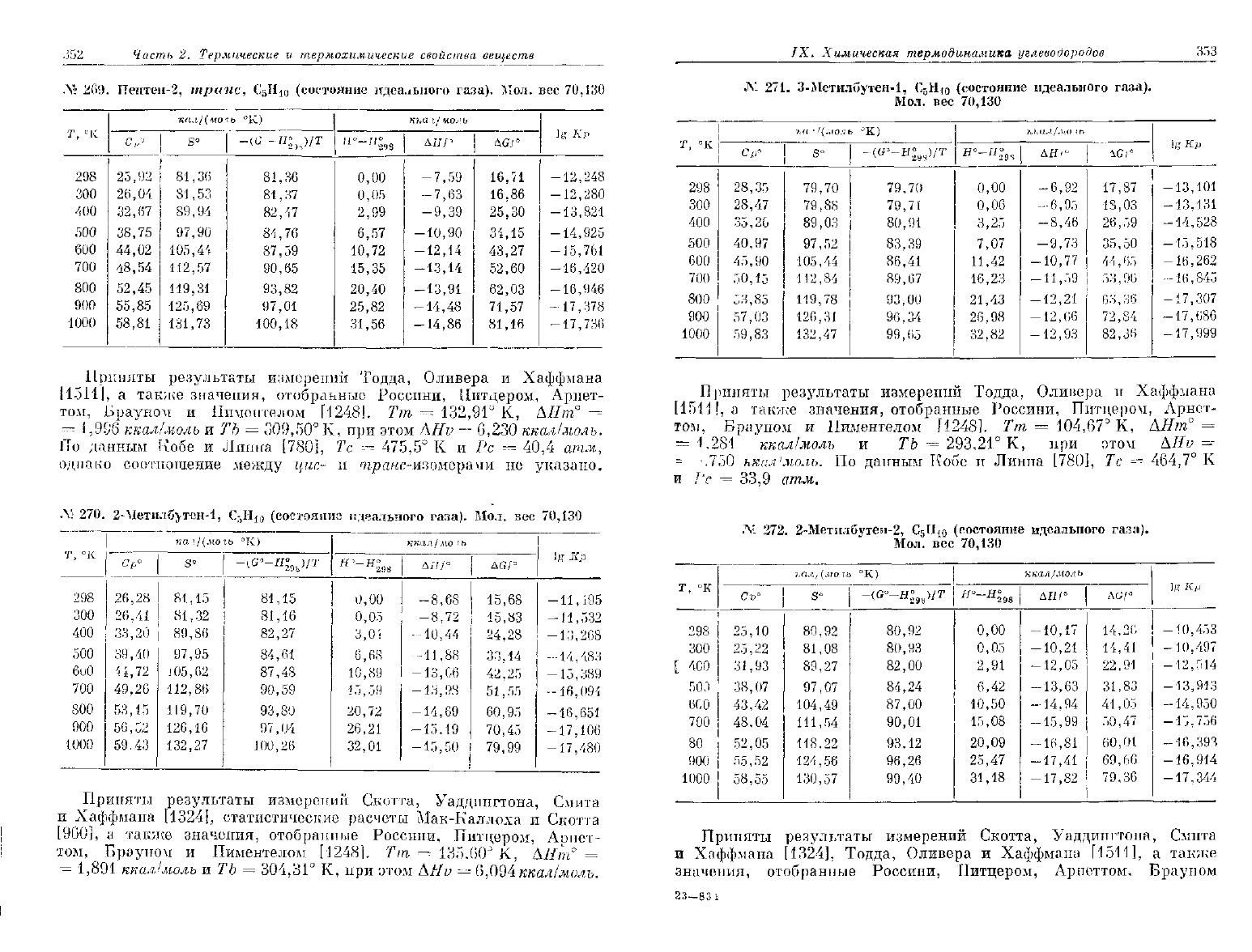
,352
Часть
2.
Термические
и
термохимические
свойства
веществ
ЛГ°
209.
Пептеи-2,
трапе,
С
5
Ню
(состояние
идеального
газа).
Мол. вес
70,130
Т,
С
К
298
300
400
500
600
700
800
900
1000
кплЦчмчь
°К)
25,92
26,04
32,67
38,75
44,02
48,54
52,45
55,85
58,81
s°
81,36
81,53
89,94
97,90
105,44
112,57
119,31
125,69
131,73
-<G
-н;,
з
)/т
81,36
81,37
82,47
84,76
87,59
90,65
93,82
97,01
100,18
п
°-
н
ив
0,00
0,05
2,99
6,57
10,72
15,35
20,40
25,82
31,56
п%а
г/ MOjib
ДНЯ
-7,59
-7,63
-9,39
-10,90
-12,14
-13,14
-13,91
-14,48
-14,86
А&°
16,71
16,86
25,30
34,15
43,27
52,60
62,03
71,57
81,16
lg
Кр
-12,248
-12,280
-13,821
-14,925
-15,761
-16,420
-16,946
-17,378
-17,730
Приняты
результаты измерений Тодда, Оливера
и
Хаффмана
[1511],
а
также значения, отобранные Россини, Питдером, Арпет-
то.м, Брауном
и
Ппмоытелом [1248]. Тт
=
132,91°
К,
АНт°
=
=
1,998
ккал/молъ
и ТЪ
=
309,50°
К, при этом AHv
=
0,230
ккал/молъ.
По
данным Кобе
и
Ляшга [780], Тс
=
475,5°
К и Рс =
40,4 атм,
однако соотношение между цис-
и
эдракс-изомераии
не
указано.
IX.
Химическая термодинамика
углеводородов
353
Л".
271.
З-Метилбутен-1,
С
5
Н
10
(состояние
идеального
газа).
Мол.
вес
70,130
т,
°к
298
300
400
500
600
700
800
900
1000
ка
-'(.ноль
°К)
Ср°
28,35
28,47
35,20
40,97
45,90
50,15
53,85
57,03
59,83
S"
79,70
79,88
89,03
97,52
105,44
112,84
119,78
126,31
132,47
-
(
G°~u;
g%)
/T
79.70
79,71
80,91
83,39
86,41
89,67
93,00
96,34
99,65
0,00
0,06
3,25
7,07
11,42
16,23
21,43
26,98
32,82
АН
I
й
-6,92
-6,95
-8,46
-9,73
-10,77
-11,59
-12,21
-12,06
-12,93
\Gt°
17,87
IS,
03
26,59
35,50
44,65
53,96
63,36
72,84
82,36
lg Кр
-13,101
-13,131
-14,528
-15,518
-16,262
-16,845
-17,307
-17,686
-17,999
Приняты
результаты измерений Тодда, Оливера
и
Хаффмана
[151Ц,
а
также значения, отобранные Россини, Питцером, Арнет-
том, Брауном
и
Пиментелом [1248]. Тт
=
104,67°
К,
АНт°
=
=
1.281
ккал/молъ
и
ТЪ
=
293,21°
К,
при
этом AHv
=
=
-.750
нкал'молъ.
По данным Кобе
и
Линна [780], Тс —
464,7°
К
и
1'с — 33,9 атм.
.Y' 270.
Г,
°К
298
300
400
500
6иО
700
800
900
1000
2Л1етплбутен-1,
Ср°
26,28
26,41
33,20
39,40
44,72
49,26
53,15
56,52
59,43
ка
г/(.ио
S-
81,15
81,32
89,86
97,95
105,62
112,86
119,70
126,16
132,27
С
5
Н
10
(состояние
идеального
газа).
гь
°К)
^
е
°-
П
29Ь
)/Г
81,15
81,16
82,27
84,61
87,48
90,59
93,80
97,04
100,26
Мол.
вес
ккал/мо
>ь
H
'~
H
298
0,00
0,05
3,0'!
6,68
10,89
15,59
20,72
26,21
32,01
АЛ/
0
-8,68
-8,72
-10,44
-11,88
-13,06
-13,93
-14,69
-15.19
-15,50
ДЙ/°
15,68
15,83
24,28
33,14
42,25
51,55
60,95
70,45
79,99
70,130
lg Кр
-11,195
-11,532
-13,208
-14,483
-15,389
-16,094
-16,651
-17,106
-17,480
Приняты
результаты измерений Скотта, Уаддпнгтона, Смита
и
Хаффмана [1324], статистические расчеты Мак-Каллоха
и
Скотта
[960],
а
также значения, отобранные Россини, Питцером, Арнет-
том, Брауном
и
Пиментелом [1248]. Тт
=
135.60
J
К,
АПт°
=
-=
1,891
ккал/молъ
и ТЪ
=
304,31°
К, при этом AHv
=
6,094
ккал/молъ.
."V. 272.
2-Метилбутен-2,
С
5
Н
10
(состояние
идеального
газа).
Мол.
вес
70,130
г,
°к
298
300
[ 4С0
500
600
700
80
900
1000
ьал,(могь
1
1
25,10
25,22
31,93
38,07
43,42
48,04
52,05
55,52
58,55
80,92
81,08
89,27
97,07
104,49
111,54
118.22
124,56
130,57
°К)
-(G°-H°
98
)/T
80,92
80,93
82,00
84,24
87,00
90,01
93.12
96,26
99,40
ккал/моль
Я
°"
Н
298
0,00
0,05
2,91
6,42
10,50
15,08
20,09
25,47
31,18
АН1°
-10,17
-10,21
-12,05
-13,63
-14,94
-15,99
-16,81
-17,41
-17,82
дс/°
14,20
14,41
22,91
31,83
41,05
50,47
60,01
69,66
79.36
**„
-10,453
-10,497
-12,514
-13,913
-14,950
—
15,756
-16,393
-16,914
-17,344
Приняты
результаты измерений Скотта, Уаддингтона, Смита
и
Хаффмана [1324], Тодда, Оливера
и
Хаффмана [1511],
а
также
значения,
отобранные Россини, Питцером, Арнеттом, Брауном
23—831
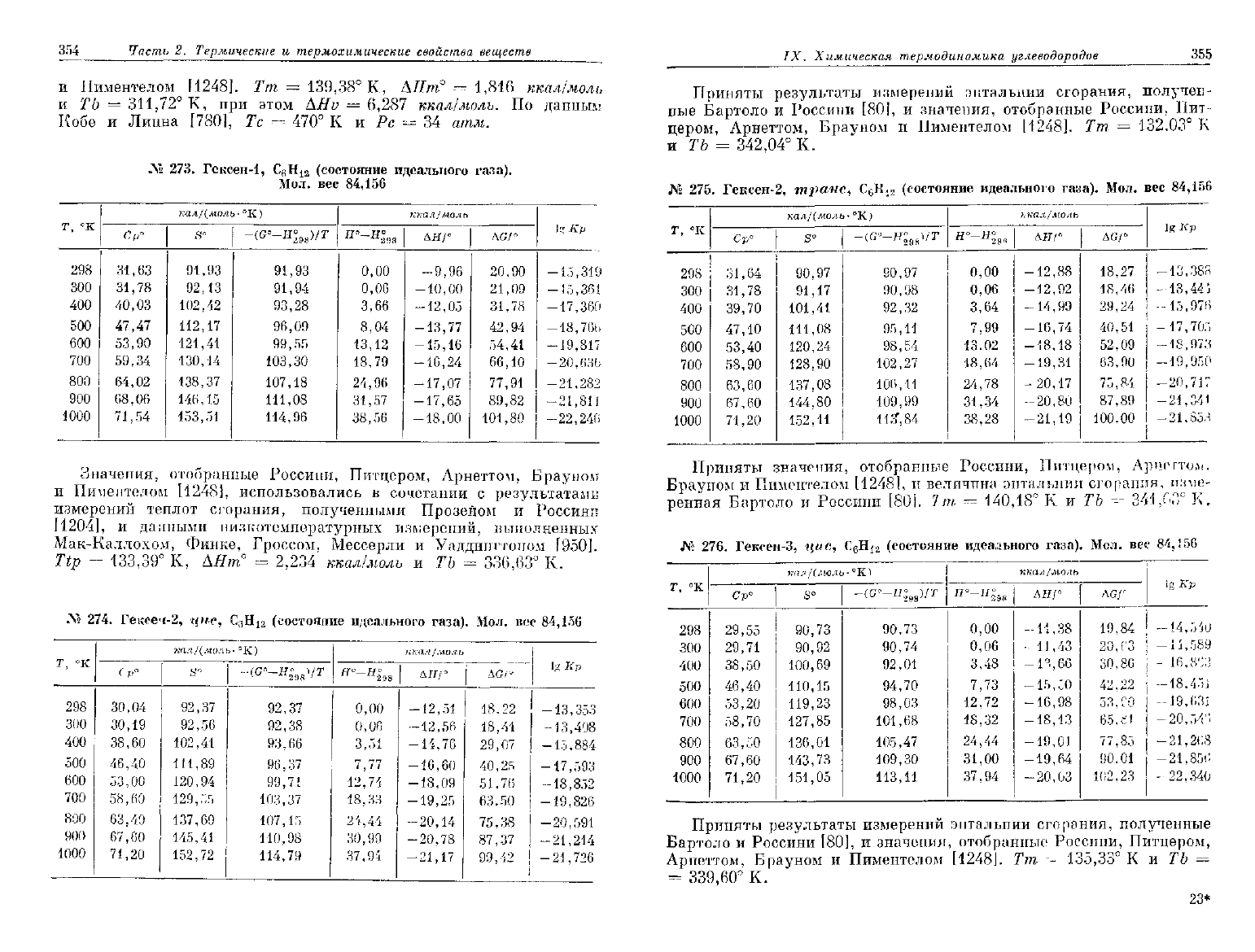
354
Часть
2.
Термические
и
термохимические свойства веществ
и
Пиментелом [1248].
Тт =
139,38°
К,
АНт°
= 1,816
ккал/молъ
и
ТЪ
=
311,72°
К, при
этом
AHv —
6,287
ккал/молъ.
По
данным
Кобе
и
Линна [780],
Тс =
470°
К и Рс = 34
№
273.
Гексен-1,
С
6
Н
12
(состояние
идеального
газа).
Мол.
вес
84,156
г, °к
298
300
400
500
600
700
800
900
1000
Ср°
31,63
31,78
40,03
47,47
53,90
59,34
64,02
68,06
71,54
кал/(мол1
Оо
91,93
92,13
102,42
112,17
121,41
130,14
138,37
146,15
153,51
>-°К)
-(в°-Я|
в8
)/г
91,93
91,94
93,28
96,09
99,55
103,30
107,18
111,08
114,96
ккал/моль
0,00
0,06
3,66
8,04
13,12
18,79
24,96
31,57
38,56
дя/°
-9,96
-10,00
-12,05
-13,77
-15,16
-16,24
-17,07
-17,65
-18,00
лс/°
20.90
21,09
31,78
42,94
54,41
66,10
77,91
89,82
101,80
-15,319
-15,361
-17,360
-18,76()
-19,817
-20,630
-21,282
-21,81!
-22,240
Значения,
отобранные
Россини,
Питпером, Арнеттом, Брауном
и
Пимептелом [1248], использовались
в
сочетании
с
результатами
измерений
теплот сгорания, полученными Прозеном
и
Россини
[1204],
и
данными низкотемпературных измерений, выполненных
Мак-Каллохом,
Финке,
Гроссом, Мессерли
и
Уаддгшгтоттом [950].
Tip
=
133,39°
К,
АНтп°
=
2,234
ккал/моль
и ТЪ =
336,63°
К.
№
274.
Гексеч-2,
цис,
С
8
Н
12
(состояние
идеального
газа).
Мол.
вес
84,156
т,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль-
°К)
(
Р
°
30,04
30,19
38,60
46,40
53,00
58,60
63,40
67,60
71,20
S"
92,37
92,56
102,41
111,89
120,94
129,55
137,69
145,41
152,72
92,37
92,38
93,66
96,37
99,71
103,37
107,15
110,98
114,79
ккал/моль
B
°-
a
Us
0,00
0,06
3,51
7,77
12,74
18,33
2i,44
30,99
37.94
дя/°
-12,51
-12,56
-14,76
-16,60
-18,09
-19,25
-20,14
-20,78
-21,17
АО!"
18.22
18,41
29,07
40,25
51,76
63.50
75,38
87,37
99,42
\g Кр
-13,353
-13,408
-15.884
-17,593
-18,852
-19,826
-20,591
-21,214
-21,726
IX. Химическая термодинамика
углеводородов
355
Приняты
результаты измерений энтальпии сгорания, получен-
ные
Бартоло
и
Россини [80],
и
значения, отобранные
Россини,
Пит-
цером,
Арнеттом, Брауном
и
Пимептелом [1248].
Тт =
132,03°
К
ж ТЪ
=
342,04°
К.
№
275. Гексен-2,
транс,
С
6
К
12
(состояние идеального газа). Мол.
вес
84,156
т,
°к
298
300
400
500
600
700
800
900
1000
Ср°
31,64
31,78
39,70
47,10
53,40
58,90
63,60
67.60
71,20
кал/(моль
s°
90,97
91,17
101,41
111,08
120,24
128,90
137,08
144,80
152,11
90,97
90,98
92,32
95,11
98,54
102,27
100,11
109,99
113*,
84
ькал/моль
0,00
0,06
3,64
7,99
13.02
18,64
24,78
31,34
38,28
АН/°
-12,88
-12,92
-14,99
-16,74
-18,18
-19,31
-20,17
-20,80
-21,19
дсу
18,27
18,46
29,24
40,51
52,09
63,90
75,84
87,89
100,00
Ig
Кр
-13,388
-13,445
-15,97<i
-17,705
-18,973
-19.95С
-20,717
-21,341
-21.85.-!
Приняты
значения, отобранные
Россини,
Питцером, Ариггтод!.
Брауном
и
Пимептелом [12481,
и
величина энтальпии сгорания, изме-
ренная
Бартоло
и
Россини [80].
lm =
140,18°
К в Г6 -
341,03°
К.
№
276.
Гексен-3,
цис,
Т, °К
298
300
400
500
600
700
800
900
1000
Ср°
29,55
29,71
38,50
46,40
53,20
58,70
63,50
67,60
71,20
СеН
12
(состояние
идеального газа)
кси'/(,моль-"К)
Со
90,73
90,92
100,69
110,15
119,23
127,85
136,01
143,73
151,05
-<е°-н;
м
)/г
90.73
90,74
92,01
94,70
98,03
101,68
105,47
109,30
113,11
я°-н|
98
0,00
0,06
3,48
7,73
12,72
18,32
24,44
31,00
37,94
ккал/моль
дну
-11,38
-1J,43
-14,66
-15,
СО
-16,98
-18,13
-19,01
-19,64
-20,03
Мол.
вес
84,156
t±Gj'
19,84
20,
ГЗ
30,80
42,22
53,
СО
65,
й!
77,85
90.01
102,23
ig
Кр
-i4,5iO
-11,589
-
16,8'J;J
-18.4.11
-19,631
-20,54'i
-21,2i;S
—
21,85t-
-22,340
Приняты
результаты
измерений
энтальпии
сгорания,
полученные
Бартоло
и
Россини
[80], и
значения,
отобранные
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248].
Тт -= 135,33° К и ТЪ =
=
339,60° К.
23*
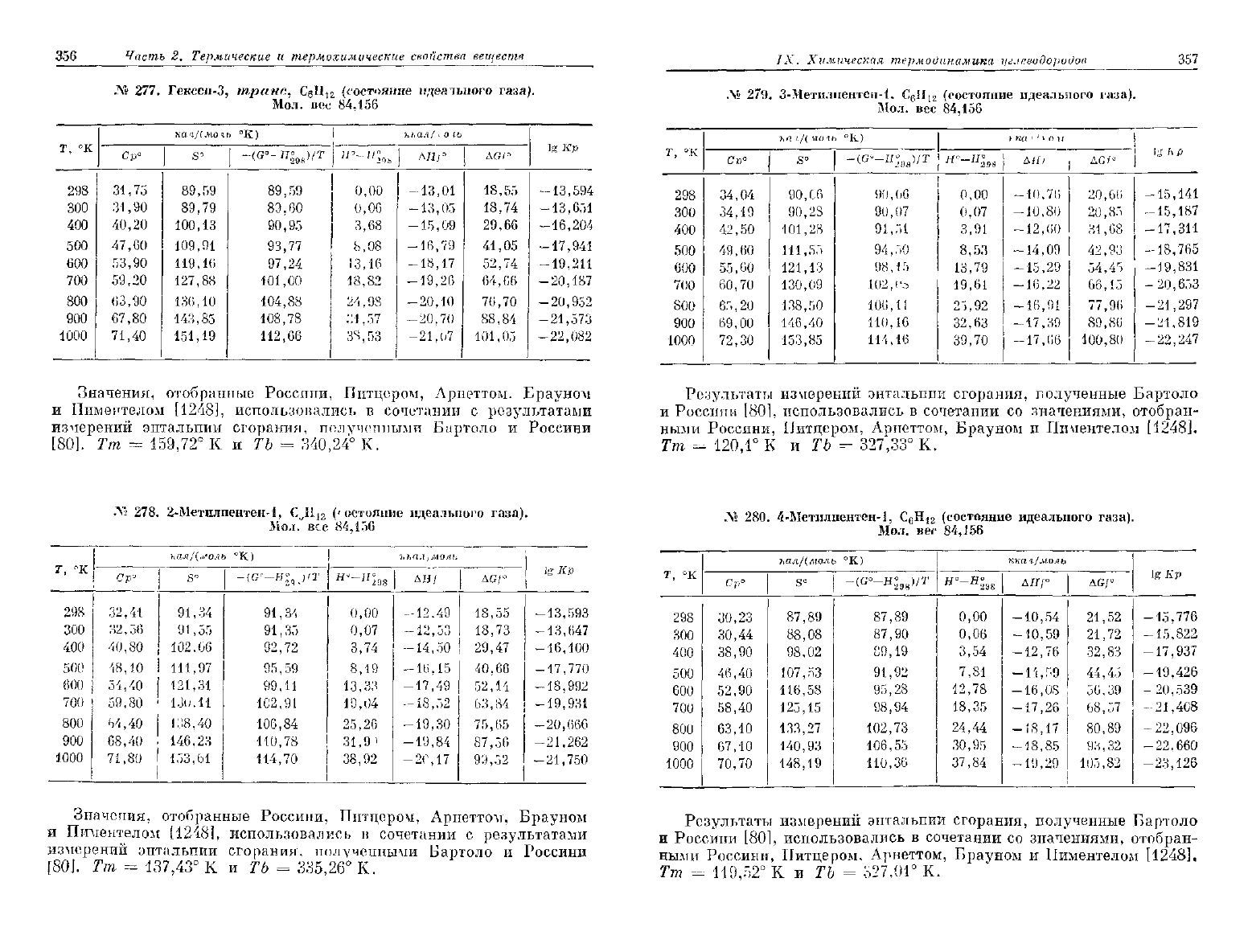
356
Часть
2.
Термические
и
термохимические
свойства
веществ
№
277.
Гексен-3,
трапе,
СбН
12
(состояние
идеального
газа).
Мол.
вес
84,156
Г,
°К
298
300
400
500
600
700
800
900
1000
каг/(М01Ь
°К)
31,75
31,90
40,20
47,60
53,90
59,20
63,90
67,80
71,40
S'
89,59
89,79
100,13
109,91
119,10
127,88
130,10
143,85
151,19
-(G°-H°
ea
)/T
89,59
8Э,60
90,95
93,77
97,24
101,00
104,88
108,78
112,66
>а,ал/
, о (ь
0,00
0,06
3,68
8,08
13,16
18,82
24,98
31,57
3S,53
Mil'
-13,01
-13,05
-15,09
-16,79
-18,17
-19,26
-20,10
-20,70
-21,07
AGP
18,55
18,74
29,66
41,05
52,74
64,66
76,70
88,84
101,05
-13,594
-13,651
-16,204
-17,941
-19,211
-20,187
-20,952
-21,573
-22,082
Значения,
отобранные
Россини,
Питцером,
Арпеттоы.
Брауном
и
Пимег'телом
[1248],
использовались
в
сочетании
с
результатами
измерений
энтальпии
сгорания,
полученными
Бартоло
и
Россини
[80].
Тт =
159,72°
К и ТЬ =
340,24°
К.
IX. Химическая
термодинамика
уг.1ееодороОов
357
Л»
279.
З-Метилпентен-1,
С
6
Н
12
(состояние
идеального
газа).
Мол.
вес
84,156
г,
°к
298
300
400
500
600
700
800
900
1000
С
г,"
34,04
34,19
42,50
49,60
55,00
60,70
65,20
69,00
72,30
ъ а 1/(
мо
it
S°
90,
С6
90,2S
101,28
111,55
121,13
130,09
138,50
146,40
153,85
•К)
_(С--Л°
ов
)/Г
90,06
90,07
91,51
94,50
98,15
102,са
106,11
110,16
114,16
"
298
0,00
0,07
3,91
8,53
13,79
19,61
25,92
32,63
39,70
)
па ' '» о »
Mil
-10,70
-10,80
-12,
SO
-14,09
-15,29
-16,22
-16,91
-17,39
-17,06
&Gf°
20,60
20,85
31,68
42,93
54,45
66,15
77,96
89,86
100,80
-15,141
-15,187
-17,311
-18,765
-19,831
-20,653
-21,297
-21,819
-22,247
Результаты
измерений
энталыши
сгорания,
полученные
Бартоло
и
Россини
[80],
использовались
в
сочетании
со
значениями,
отобран-
ными
Россини,
Питцером,
Арпеттом,
Брауном
и
Пиментелом
[1248].
Тт
=
120,1°
К и ТЬ =
327,33°
К.
Л»
278.
2-Метилпентен-1,
С„П
12
('«стояние
идеального
газа).
Мол.
вес
84,156
т,
°к
298
300
400
500
600
700
800
900
1000
Ср°
32,41
32,56
40,80
48,10
54,40
59,80
64,40
68,40
71,80
кал/(
л
.
0Л
О
91,34
91,55
102.06
111,97
121,31
13u.ll
138,40
146,23
153,61
>
К)
-(С--Н°„,,/Т
91,34
91,35
92,72
95,59
99,11
102,91
106,84
110,78
114,70
0,00
0,07
3,74
8,19
13,33
10,04
25,20
31,9'
38,92
ъьал,моль
ДН/
-12.49
-12,53
-14,50
-16,15
-17,49
-18,52
-19,30
-19,84
-20,17
AG/°
18,55
18,73
29,47
40,66
52,11
63,84
75,65
87,56
99,52
is кр
-13,593
-13,647
-16,100
-17,770
-18,992
-19,931
-20,666
-21,262
-21,750
Значения,
отобранные
Россини,
Питцером,
Арпеттом,
Брауном
я
Пиментелом
[1248],
использовались
в
сочетании
с
результатами
измерений
энтальпии
сгорания,
полученными
Бартоло
и
Россини
[80].
Тт =
137,43°
К и ТЬ =
335,26°
К.
Л»
280.
4-Метшшентен-1,
С
С
Н
12
(состояние
идеального
газа).
Мол.
вес
84,156
т,
°к
298
300
400
500
600
700
800
900
1000
Ср°
30,23
30,44
38,90
46,40
52,90
58,40
63,10
67,10
70,70
ьал/(мол1
s°
87,89
88,08
98,02
107,53
116,58
125,15
133,27
140,93
148,19
°К)
-(G=-H°
98
)/T
87,89
87,90
89,19
91,92
95,28
98,94
102,73
106,55
110,36
ккаг/моль
H
°~
H
29S
0,00
0,06
3,54
7,81
12,78
18,35
24,44
30,95
37,84
дя/°
-10,54
-10,59
-12,76
-14,59
-16,08
-17,26
-18,17
-18,85
-19,29
AG/°
21,52
21,72
32,83
44,45
50,39
68,57
80,89
93,32
105,82
lg
Кр
-15,776
-15,822
-17,937
-19,426
-20,539
-21,408
-22,096
-22,660
-23,126
Результаты
измерений
энтальпии
сгорания,
полученные
Бартоло
и
Россини
[80],
использовались
в
сочетании
со
значениями,
отобран-
ными
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248],
Тт
=
119,52°
К и ТЬ =
527,01°
К.
358
Часть
2.
Термические
и
термохимические
свойства
веществ
№
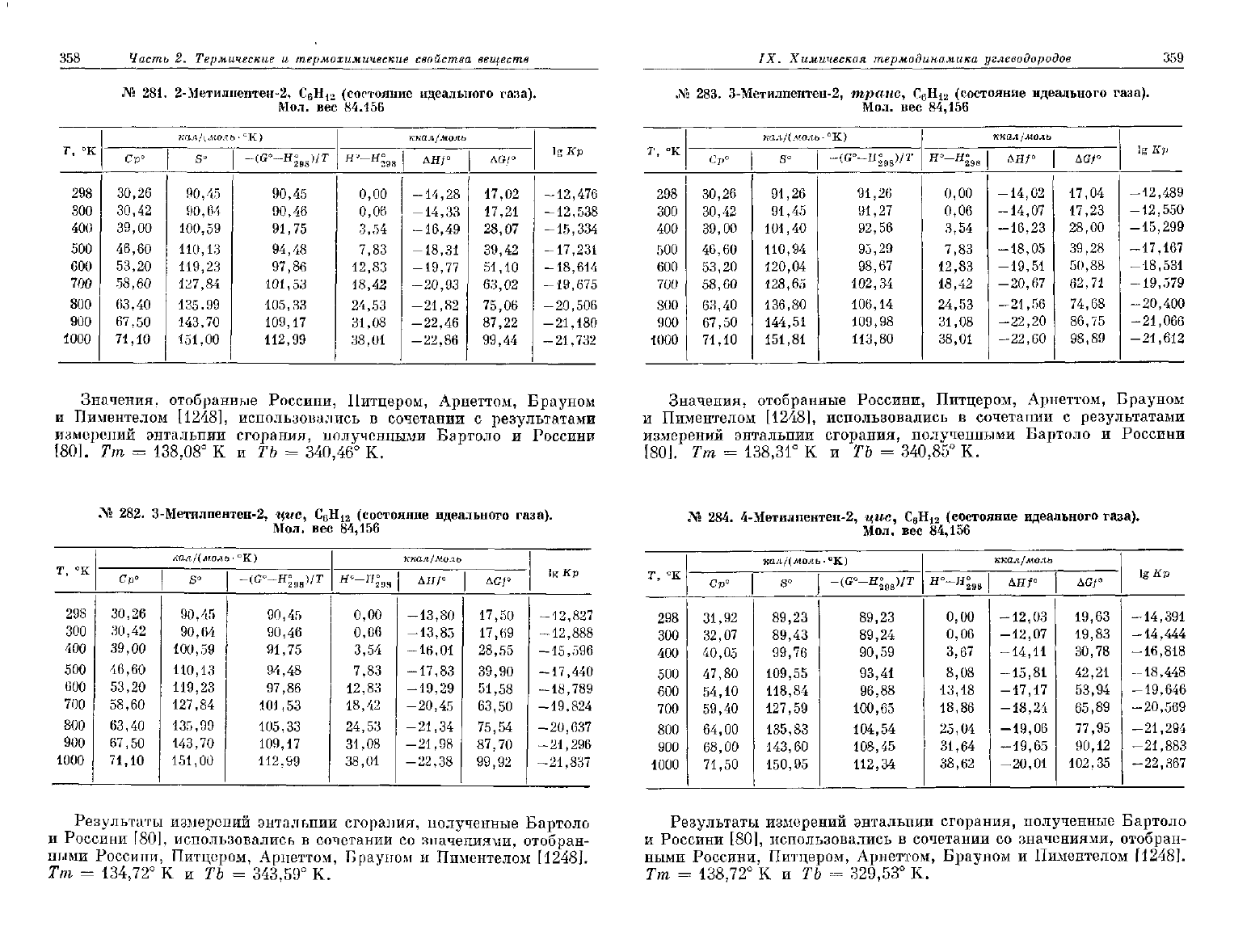
281.
2-Метилпентен-2,
С
6
Н
12
(состояние
идеального
газа).
Мол.
вес
84.156
т,
°к
298
300
400
500
600
700
800
900
1000
Ср°
30,26
30,42
39,00
46,60
53,20
58,60
63,40
67,50
71,10
кал/умол
s°
90,45
90,64
100,59
110,13
119,23
127,84
135.99
143,70
151,00
.••К)
90,45
90,46
91,75
94,48
97,86
101,53
105,33
109,17
112,99
ккал/моль
0,00
0,06
3,54
7,83
12,83
18,42
24,53
31,08
38,01
ДЯ/°
-14,28
-14,33
-16,49
-18,31
-19,77
-20,93
-21,82
-22,46
-22,86
AG/°
17,02
17,21
28,07
39,42
51,10
63,02
75,06
87,22
99,44
is кр
-12,476
-12,538
-15,334
-17,231
-18,614
-19,675
-20,506
-21,180
-21,732
Значения,
отобранные Россини, Питцером, Арнеттом, Брауном
и
Пиментелом [1248], использовались
в
сочетании
с
результатами
измерений энтальпии сгорания, полученными Бартоло
и
Россини
[80].
Тт =
138,08°
К и ТЪ =
340,46°
К.
№
282.
З-Метилпентен-2,
цыс,
C
6
Hi
2
(состояние
идеального
газа).
Мол.
вес
84,156
298
300
400
500
600
700
800
900
1000
Ср°
30,26
30,42
39,00
46,60
53,20
58,60
63,40
67,50
71,10
шл/(мол
S»
90,45
90,64
100,59
110,13
119,23
127,84
135,99
143,70
151,00
ь-°К)
-(G°-H°
98
)/T
90,45
90,46
91,75
94,48
97,86
101,53
105,33
109,17
112,99
ккал/моль
B
'-"h*
0,00
0,06
3,54
7,83
12,83
18,42
24,53
31,08
38,01
j ДЯ/°
-13,80
-13,85
-16,01
-17,83
-19,29
-20,45
-21,34
-21,98
-22,38
1
AGf°
17,50
17,69
28,55
39,90
51,58
63,50
75,54
87,70
99,92
lg-Kp
-12,827
-12,888
-15,596
-17,440
-18,789
-19,824
-20,637
-21,296
-21,837
Результаты измерений энтальпии сгорания, полученные Бартоло
и
Россини [80], использовались
в
сочетании
со
значениями, отобран-
ными
Россини, Питцером, Арнеттом, Брауном
и
Пиментелом [1248].
Тт
=
134,72°
К и ТЪ =
343,59°
К.
IX. Химическая
термодинамика
углеводородов
359
Ли
283.
З-Метилпентен-2,
трапе,
С
в
Н
12
(состояние
идеального
газа).
Мол.
вес
84,156
Т, °К
298
300
400
500
600
700
300
900
1000
Ср°
30,26
30,42
39,00
46,60
53,20
58,60
63,40
67,50
71,10
кал/(моль
S°
91,26
91,45
101,40
110,94
120,04
128,65
136,80
144,51
151,81
•°К)
-(G°-H°
98
)/r
91,26
91,27
92,56
95,29
98,67
102,34
106,14
109,98
113,80
ккал/моль
0,00
0,06
3,54
7,83
12,83
18,42
24,53
31,08
38,01
АЯ1°
-14,02
-14,07
-16,23
-18,05
-19,51
-20,67
-21,56
-22,20
-22,60
AGf
17,04
17,23
28,00
39,28
50,88
62,71
74,68
86,75
98,89
-12,489
-12,550
-15,299
-17,167
-18,531
-19,579
-20,400
-21,066
-21,612
Значения,
отобранные Россини, Питцером, Арнеттом, Брауном
и
Пиментелом [1248], использовались
в
сочетании
с
результатами
измерений энтальпии сгорания, полученными Бартоло
и
Россини
[80].
Тт =
138,31°
К и ТЪ =
340,85°
К.
№
284.
4-Метилпентен-2,
цис,
СвН
12
(состояние
идеального
газа).
Мол.
вес
84,156
Т,
°К
298
300
400
500
600
700
800
900
1000
Ср°
31,92
32,07
40,05
47,80
54,10
59,40
64,00
68,00
71,50
кал/(моль
S"
89,23
89,43
99,76
109,55
118,84
127,59
135,83
143,60
150,95
•°К)
-(G°-H°
98
)/r
89,23
89,24
90,59
93,41
96,88
100,65
104,54
108,45
112,34
ккал/моль
Я
«298
0,00
0,06
3,67
8,08
13,18
18,86
25,04
31,64
38,62
ДЯ/°
-12,03
-12,07
-14,11
-15,81
-17,17
-18,24
-19,06
-19,65
-20,01
AG/°
19,63
19,83
30,78
42,21
53,94
65,89
77,95
90,12
102,35
lg
Кр
-14,391
-14,444
-16,818
-18,448
-19,646
-20,569
-21,294
-21,883
-22,367
Результаты измерений энтальпии сгорания, полученные Бартоло
и
Россини [80], использовались
в
сочетании
со
значениями, отобран-
ными
Россини, Питцером, Арнеттом, Брауном
и
Пиментелом [1248].
Тт
=
138,72°
К и ТЪ =
329,53°
К.
360
Часть
2.
Термические
и
термохимические
свойства
веществ
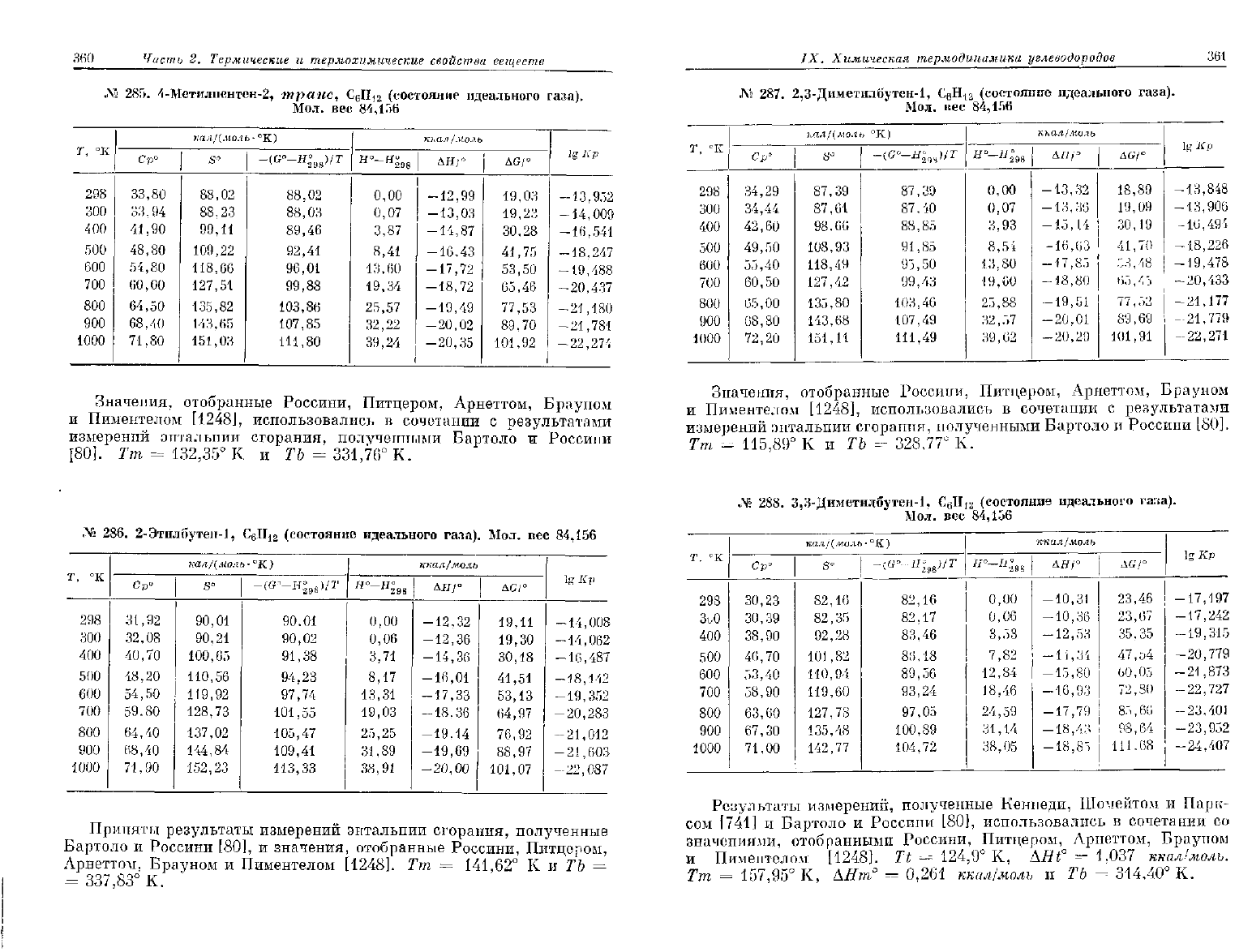
Л° 285. 4-Метилпентен-2, трапе,
С
6
Н
(2
(состояние
идеального
газа).
Мол.
вес
84,156
г,
°к
298
300
400
500
600
700
800
900
1000
кал
[(моль-
°К)
Ср°
33,80
33,94
41,90
48,80
54,80
60,00
64,50
68,40
71,80
со
88,02
88,23
99,11
109,22
118,66
127,51
135,82
143,65
151,03
-(
G
°-
H
2%8>/
T
88,02
88,03
89,46
92,41
96,01
99,88
103,86
107,85
111,80
ккал/моль
тто
TJO
Ы
~~
Н
298
0,00
0,07
3,87
8,41
13,60
19,34
25,57
32,22
39,24
ДН/°
-12,99
-13,03
-14,87
-16,43
-17,72
-18,72
-19,49
-20,02
-20,35
AGf°
19,03
19,23
30,28
41,75
53,50
65,46
77,53
89,70
101,92
lg
Кр
-13,952
-14,009
-16,541
-18,247
-19,488
-20,437
-21,180
-21,781
-22,274
Значения,
отобранные
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248],
использовались
в
сочетании
с
результатами
измерений
энтальпии
сгорания,
полученными
Бартоло
и
Россини
[80].
Тт =
132,35°
К и
ТЪ
=
331,76°
К.
IX. Химическая
термодинамика
углеводородов
361
№
287. 2,3-Диметилбутен-1,
СвН
12
(состояние
идеального
газа).
Мол.
вес
84,156
г,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль
°К)
Ср°
34,29
34,44
42,60
49,50
55,40
60,50
65,00
08,80
72,20
s°
87,39
87,61
98.60
108,93
118,49
127,42
135,80
143,68
151,11
-(О°-Н°„)/Г
87,39
87.40
88,85
91,85
93,50
99,43
103,46
107,49
111,49
ккал/моль
Н
°~
Н
2Э8
0,00
0,07
3,93
8,54
13,80
19,00
25,88
32,57
39,62
ДН/°
-13,32
-13,36
-15,14
-16,63
-17,83
-18,80
-19,51
-20,01
-20,29
AG/°
18,89
19,09
30,19
41,70
53,48
'55,43
77,52
89,69
101,91
lg
Кр
-13,848
-13,906
-16,494
-18,226
-19,478
-20,433
-21,177
-21,779
-22,271
Значения,
отобранные
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248],
использовались
в
сочетании
с
результатами
измерений
энтальпии
сгорания,
полученными
Бартоло
и
Россини
[80].
Тт
=
115,89°
К и
ТЪ
=
328,77°
К.
ЛГ» 286. 2-Этилбутен-1,
СеН
12
(состояние
идеального
газа).
Мол.
вес
84,156
Л° 288. 3,3-Диметилбутен-1,
С
6
Н
12
(состояние
идеального
газа).
Мол.
вес
84,156
г,
°к
298
300
400
500
600
700
800
900
1000
кал
/(моль
-°К)
Ср°
31,92
32,08
40,70
48,20
54,50
59.80
64,40
68,40
71,90
s°
90,01
90,21
100,65
110,56
119,92
128,73
137,02
144,84
152,23
90,01
90,02
91,38
94,23
97,74
101,55
105,47
109,41
113,33
ккал/моль
Н
°-
Н
298
0,00
0,06
3,71
8,17
13,31
19,03
25,25
31,89
38,91
АН
f
-12,32
-12,36
-14,36
-16,01
-17,33
-18,36
-19,14
-19,69
-20,00
AGI°
19,11
19,30
30,18
41,51
53,13
64,97
76,92
88,97
101,07
lg
Кр
-14,008
-14,062
-16,487
-18,142
-19,352
-20,283
-21,012
-21,603
-22,087
Приняты
результаты
измерений
энтальпии
сгорания,
полученные
Бартоло
и
Россини
[80],
и
значения,
отобранные
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248].
Тт =
141,62°
К и
ТЪ
=
=
337,83°
К.
т.
°к
298
ЗьО
400
500
600
700
800
900
1000
Ср"
30,23
30,39
38,90
46,70
53,40
58,90
63,60
67,30
71,00
кал/(моль
S°
82,16
82,35
92,28
101,82
110,94
119,60
127,78
135,48
142,77
82,16
82,17
83,46
86,18
89,56
93,24
97,05
100,89
104,72
ккал/моль
0,00
0,06
3,53
7,82
12,84
18,46
24,59
31,14
38,05
дн/°
-10,31
-10,36
-12,53
-11,34
-15,80
-16,93
-17,79
-18,43
-18,83
AGf°
23,46
23,67
35,35
47,
о4
60,05
72,80
85,60
98,64
111.68
lgXp
-17,197
-17,242
-19,315
-20,779
-21,873
-22,727
-23.401
-23,952
-24,407
Результаты
измерений,
полученные
Кеннеди,
Шочейтом
и
Парк-
сом
[741]
и
Бартоло
и
РОССИРШ
[80],
использовались
в
сочетании
со
значениями,
отобранными
Россини,
Питцером,
Арнеттом,
Брауном
и
Пимеителом
[1248].
Tt =
124,9°
К, AHf = 1,037
ккалЫолъ.
Тт
=
157,95°
К, АНт°
=
0,261 ккал/молъ
и
ТЪ
=
314,40°
К.
