Сталл Д. Вестрам Э. Зинке Г. Химическая термодинамика органических соединений
Подождите немного. Документ загружается.

302
Часть
2.
Термические
и
термохимические свойства веществ
Соудерса,
Маттюза
и
Харда
[1396,
1397].
Температуры
переходов
и
соответствующие
им
энтальпии
отобраны
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248].
Тт =
173,66°
К и ТЪ =
=
406,98°
К, при
этом
AHv — 8,32
ккал/молъ.
IX. Химическая термодинамика углеводородов
303
№
Т, °К
298
300
400
500
600
700
800
900
1000
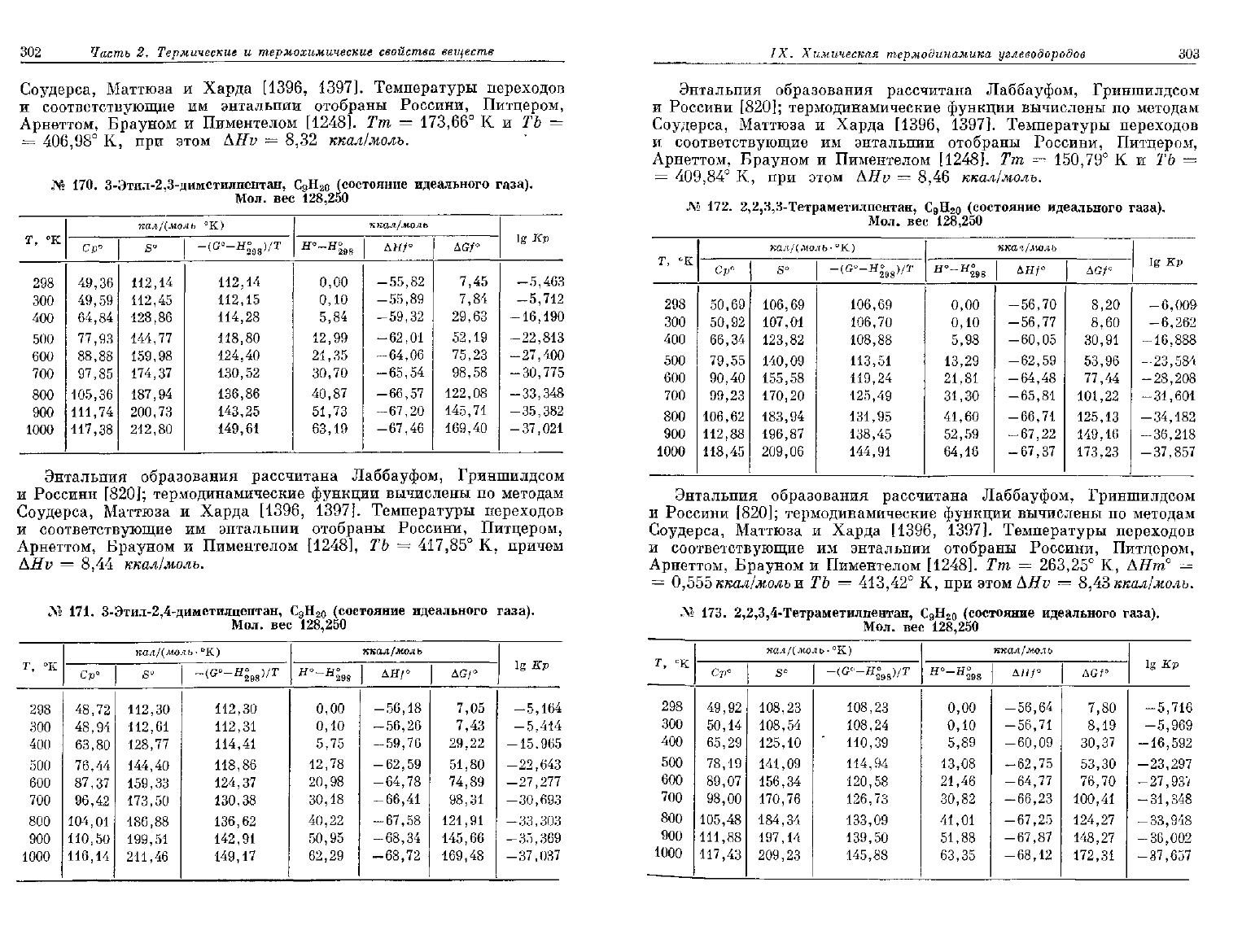
170.
3-Этил-2,3-диметилпентан,
Мол.
вес
кал/(моль
°К)
Ср°
49,36
49,59
64,84
77,93
88,88
97,85
105,36
111,74
117,38
8«
112,14
112,45
128,86
144,77
159,98
174,37
187,94
200,73
212,80
-(
G
°-
H
a°98>/
T
112,14
112,15
114,28
118,80
124,40
130,52
136,86
143,25
149,61
С
9
Н
20
(состояние
идеального
газа).
128,250
ккал/моль
0,00
0,10
5,84
12,99
21,35
30,70
40,87
51,73
63,19
дн/°
-55,82
-55,89
-59,32
-62,01
-64,06
-65,54
-66,57
-67,20
-67,46
AGf
7,45
7,84
29,63
52,19
75,23
98,58
122,08
145,71
169,40
igKp
-5,463
-5,712
-16,190
-22,813
-27,400
-30,775
-33,348
-35,382
-37,021
Энтальпия
образования
рассчитана
Лаббауфом,
Гриншилдсом
и
Россини
[820];
термодинамические
функции
вычислены
по
методам
Соудерса,
Маттюза
и
Харда
[1396,
1397].
Температуры
переходов
и
соответствующие
им
энтальпии
отобраны
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248],
ТЪ =
417,85°
К,
причем
AHv = 8,44
ккал/молъ.
№
г, °к
298
300
400
500
600
700
800
900
1000
171.
3-Этил-2,4-диметилпентан,
Мол.
вес
кал/(моль-°К)
Ср°
48,72
48,94
63,80
76,44
87,37
96,42
104,01
110,50
116,14
112,30
112,61
128,77
144,40
159,33
173,50
186,88
199,51
211,46
-<е°-я°
98
)/г
112,30
112,31
114,41
118,86
124,37
130,38
136,62
142,91
149,17
С
9
Н
2
о
(состояние
идеального
128,250
ккал/моль
Н
°-
Н
2
88
0,00
0,10
5,75
12,78
20,98
30,18
40,22
50,95
62,29
дя/°
-56,18
-56,26
-59,76
-62,59
-64,78
-66,41
-67,58
-68,34
-68,72
AGf
7,05
7,43
29,22
51,80
74,89
98,31
121,91
145,66
169,48
газа).
lg Кр
-5,164
-5,414
-15.965
-22,643
-27,277
-30,693
-33,303
-35,369
-37,037
Энтальпия
образования
рассчитана
Лаббауфом,
Гриншилдсом
и
Россини
[820];
термодинамические
функции
вычислены
по
методам
Соудерса,
Маттюза
и
Харда
[1396,
1397].
Температуры
переходов
и
соответствующие
им
энтальпии
отобраны
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248].
Тт =
150,79°
К и ТЪ =
=
409,84°
К, при
этом
AHv = 8,46
ккал/молъ.
№
172.
2,2,3,3-Тетраметилпентан, СдЩо (состояние
идеального
газа).
Мол.
вес
128,250
298
300
400
500
600
700
800
900
1000
кал/(моль-°К)
Ср°
50,69
50,92
66,34
79,55
90,40
99,23
106,62
112,88
118,45
СО
106,69
107,01
123,82
140,09
155,58
170,20
183,94
196,87
209,06
-(G°-Hj
M
)/r
106,69
106,70
108,88
113,51
119,24
125,49
131,95
138,45
144,91
ккач/моль
Н
°~
Н
298
0,00
0,10
5,98
13,29
21,81
31,30
41,60
52,59
64,16
дя/°
-56,70
-56,77
-60,05
-62,59
-64,48
-65,81
-66,71
-67,22
-67,37
AGf
0
8,20
8,60
30,91
53,96
77,44
101,22
125,13
149,16
173,23
lg Кр
-6,009
-6,262
-16,888
-23,584
-28,208
-31,601
-34,182
-36,218
-37,857
Энтальпия
образования
рассчитана
Лаббауфом,
Гриншилдсом
и
Россини
[820];
термодинамические
функции
вычислены
по
методам
Соудерса,
Маттюза
и
Харда
[1396,
1397].
Температуры
переходов
и
соответствующие
им
энтальпии
отобраны
Россини,
Питцером,
Арнеттом,
Брауном
и
Пиментелом
[1248].
Тт =
263,25°
К,
АНт°
=
=
0,555
ккал/молъ
и ТЪ =
413,42°
К, при
этом
AHv = 8,43
ккал/молъ.
№ 173.
2,2,3,4-Тетраметилпентан,
С
9
Н
2
о
(состояние
идеального
газа).
Мол. вес
128,250
Г, "К
298
300
400
500
600
700
800
900
1000
кал
/(моль
-"К)
Ср°
49,92
50,14
65,29
78,19
89,07
98,00
105,48
111,88
117,43
Со
108,23
108,54
125,10
141,09
156,34
170,76
184,34
197,14
209,23
-(О°-я
2
°
в8
)/г
108,23
108,24
'
110,39
114,94
120,58
126,73
133,09
139,50
145,88
ккал/моль
0,00
0,10
5,89
13,08
21,46
30,82
41,01
51,88
63,35
дн/°
-56,64
-56,71
-60,09
-62,75
-64,77
-66,23
-67,25
-67,87
-68,12
AGf
7,80
8,19
30,37
53,30
76,70
100,41
124,27
148,27
172,31
lg Кр
-5,716
-5,969
-16,592
-23,297
-27,93V
-31,348
-33,948
-36,002
-37,657
304
Часть
2.
Термические
и
термохимические
свойства
веществ
IX.
Химическая
термодинамика
углеводородов
305
Энтальпия образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820]; термодинамические функции вычислены по методам
Соудерса, Маттюза и Харда [1396, 1397]. Температуры переходов
и
соответствующие им энтальпии отобраны Россини, Питцером,
Арнеттом, Брауном и Пиментелом [1248]. Тт =
152,06°
К,
АНт°
—
—
0,124
ккал/молъж
ТЪ =
406,17°
К, при этом AHv = 8,19 ккал/'моль.
№
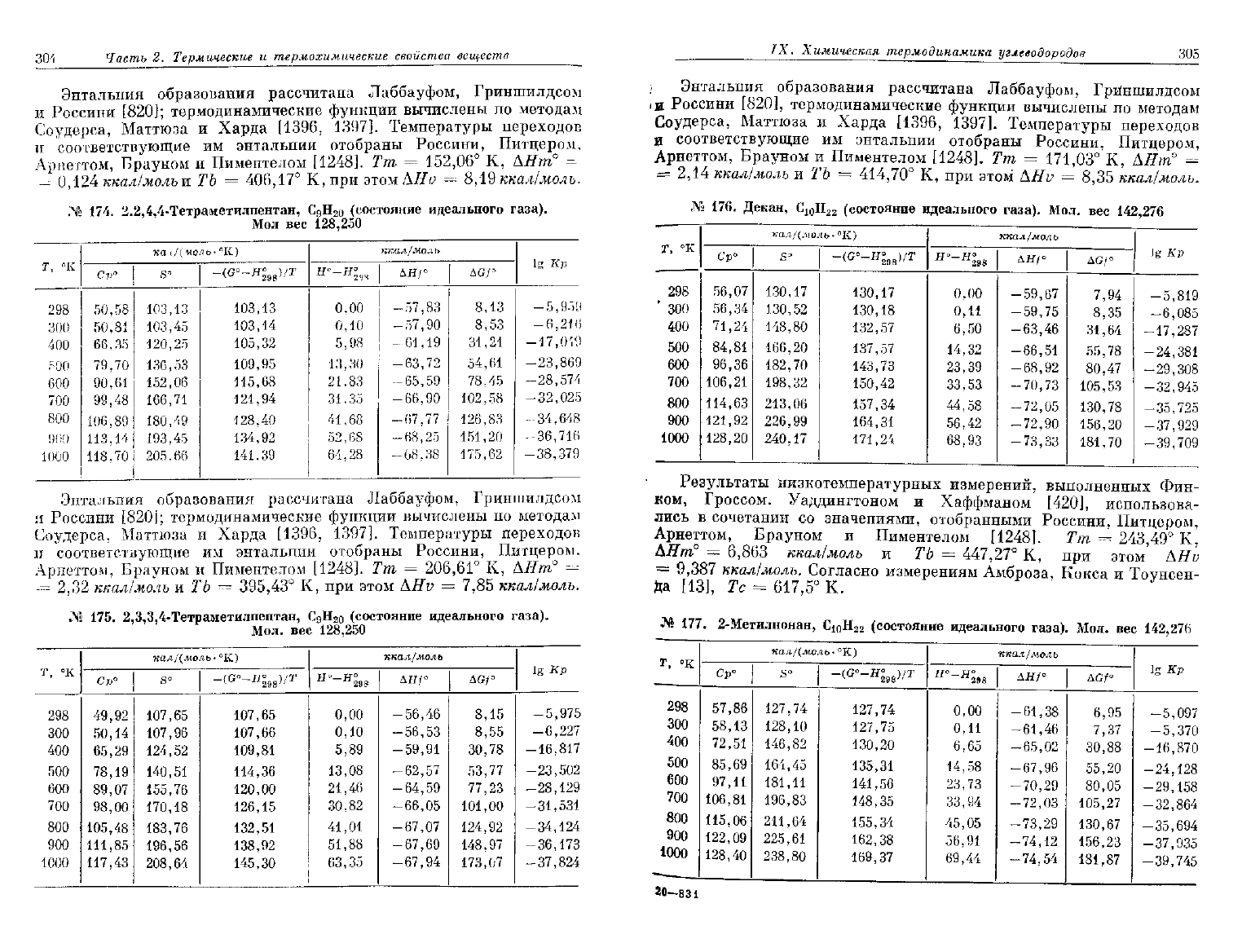
174.
2.2,4,4-Тетраметилпентан,
С9Н20
(состояние
идеального
газа).
Мол
вес
128,250
г, °к
298
300
400
500
600
700
800
900
1000
Ср°
50,58
50,81
66,35
79,70
90,61
99,48
106,89
113,14
118,70
ка
i/( «о
S-
103,13
103,45
120,25
130,53
152,06
166,71
180,49
193,45
205.66
-<-
G
°-
H
°2<>
8
V
T
103,13
103,14
105,32
109,95
115,68
121,94
128,40
134,92
141,39
ккал/моль
0,00
0,10
5,98
13,30
21,83
31,35
41,68
52,68
64,28
AHf
-57,83
-57,90
-61,19
-63,72
-65,59
-66,90
-67,77
-68,25
-68,38
AGf
8,13
8,53
31,21
54,61
78,45
102,58
126,83
151,20
175,62
-5,959
-6,210
-17,019
-23,869
-28,574
-32,025
-34,648
-36,716
-38,379
Энтальпия образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820]; термодинамические функции вычислены по методам
Соудерса, Маттюза и Харда [1396, 1397]. Температуры переходов
и
соответствующие им энтальпии отобраны Россини, Питцером.
Арнеттом, Брауном и Пиментелом [1248]. Тт =
206,61°
К,
АНт°
=
-=
2,32 ккал!моль и ТЪ =
395,43°
К, при этом AHv = 7,85 ккал/молъ.
№ 175. 2,3,3,4-Тетраметилпентан, СдН
2
о (состояние идеального газа).
Мол.
вес
128,250
т,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль-°К)
Ср°
49,92
50,14
65,29
78,19
89,07
98,00
105,48
111,85
117,43
S
0
107,65
107,96
124,52
140,51
155,76
170,18
183,76
196,56
208,64
-(О-н;
и
)/г
107,65
107,66
109,81
114,36
120,00
126,15
132,51
138,92
145,30
ккал/моль
Н
°-
Н
2%8
0,00
0,10
5,89
13,08
21,46
30,82
41,01
51,88
63,35
AHf
-56,46
-56,53
-59,91
-62,57
-64,59
-66,05
-67,07
-67,69
-67,94
AGf
8,15
8,55
30,78
53,77
77,23
101,00
124,92
148,97
173,07
lg Кр
-5,975
-6,227
-16,817
-23,502
-28,129
-31,531
-34,124
-36,173
-37,824
Энтальпия образования рассчитана Лаббауфом, Гриншилдсом
в
Россини [820], термодинамические функции вычислены по методам
'
Соудерса, Маттюза и Харда [1396, 1397]. Температуры переходов
Я соответствующие им энтальпии отобраны Россини, Питцером,
•
Арнеттом, Брауном и Пиментелом [1248]. Тт =
171,03°
К,
АНт°
=
=
2,14
ккал/молъ
и ТЪ =
414,70°
К, при этом AHv = 8,35 ккал/молъ.
№ 176. Декан, Ci
0
H
22
(состояние идеального газа). Мол. вес
142,276
Т, "К
298
"
300
400
500
600
700
800
900
1000
кал/(моль
•
°К)
Ср°
56,07
56,34
71,24
84,81
96,36
106,21
114,63
121,92
128,20
130,17
130,52
148,80
166,20
182,70
198,32
213,06
226,99
240,17
-(G»-H°
98
)/r
130,17
130,18
132,57
137,57
143,73
150,42
157,34
164,31
171,24
ккал/моль
Н
°~
Н
298
0,00
0,11
6,50
14,32
23,39
33,53
44,58
56,42
68,93
AHf
-59,67
-59,75
-63,46
-66,51
-68,92
-70,73
-72,05
-72,90
-73,33
AGf
7,94
8,35
31,64
55,78
80,47
105,53
130,78
156,20
181,70
Ig
Кр
-5,819
-6,085
-17,287
-24,381
-29,308
-32,945
-35,725
-37,929
-39,709
Результаты низкотемпературных измерений, выполненных Фин-
ком,
Гроссом. Уаддингтоном и Хаффманом [420], использова-
лись в сочетании со значениями, отобранными Россини, Питцером,
Арнеттом, Брауном и Пиментелом [1248]. Тт =
243,49°
К,
АНт°
=
6,863
ккал/молъ
и ТЪ =
447,27°
К, при этом AHv
—
9,387
ккал/молъ. Согласно измерениям Амброза, Кокса и Тоунсен-
Да [13], Тс =
617,5°
К.
№
177
298
300
400
500
600
700
800
900
1000
.
2-Метилнонан,
Ci
0
H
2
2
(состояние
идеального
газа)
кал/(мсль-
°К)
Ср°
57,86
58,13
72,51
85,69
97,11
106,81
115,06
122,09
128,40
s°
127,74
128,10
146,82
164,45
181,11
196,83
211,64
225,61
238,80
127,74
127,75
130,20
135,31
141,56
148,35
155,34
162,38
169,37
Мол.
ве(
ккал/моль
Н
~
Я
298
0,00
0,11
6,65
14,58
23,73
33,94
45,05
56,91
69,44
AHf
-61,38
-61,46
-65,02
-67,96
-70,29
-72,03
-73,29
-74,12
-74,54
AGf
6,95
7,37
30,88
55,20
80,05
105,27
130,67
156,23
181,87
з
142,276
lg Кр
-5,097
-5,370
-16,870
-24,128
-29,158
-32,864
-35,694
-37,935
-39,745
306
Часть
2. Термические и
термохимические
свойства
веществ
Результаты низкотемпературных измерений, выполненных Парк-
сом, Уестом
и
Муром [1120], использовались
в
сочетании
со
значения-
ми,
отобранными Россини, Питцером, Арнеттом, Брауном
и
Пимен-
телом [1248]; термодинамические фупкции вычислены по "методам
Соудерса, Маттюза
и
Харда [1396, 1397].
Тт = 198,50° К,
АНт°
=-
=
4,180
ккал/молъ
и ТЪ = 440,15° К.
IX. Химическая
термодинамика
углеводородов
3)7
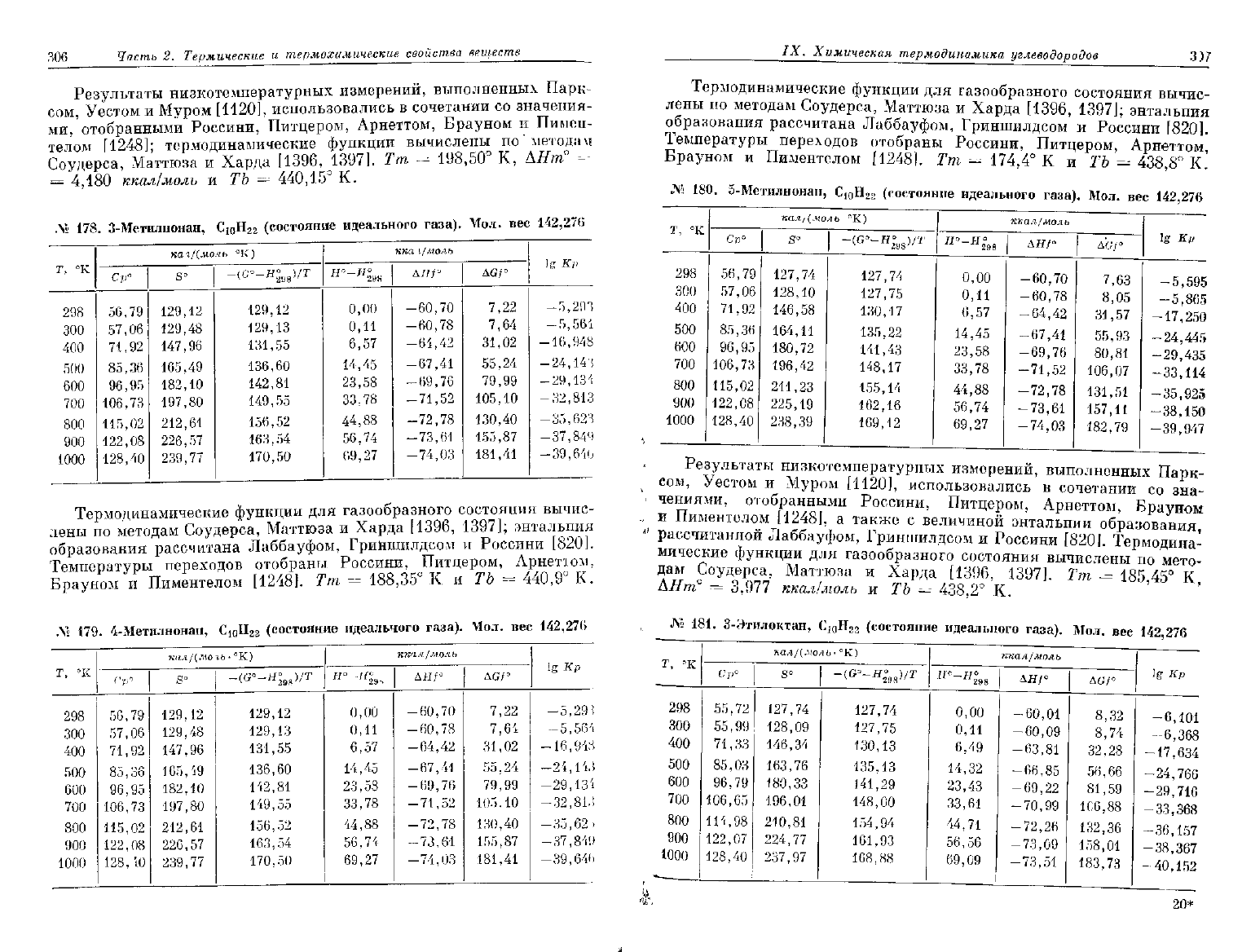
Л« 178
г, °к
298
300
400
500
600
700
800
900
1000
,
З-Метилнонан,
Ci
0
H
22
(состояние
идеального
газа).
каг/(моль
°К)
Ср°
56,79
57,06
71,92
85,36
96,95
106,73
115,02
122,08
128,40
О
129,12
129,48
147,96
165,49
182,10
197,80
212,61
226,57
239,77
-(G=-H°
a8
)/T
129,12
129,13
131,55
136,60
142,81
149,55
156,52
163,54
170,50
Мол.
вес
кка
i/моль
0,00
0,11
6,57
14,45
23,58
33,78
44,88
56,74
09,27
дн/°
-60,70
-60,78
-64,42
-67,41
-69,76
-71,52
-72,78
-73,61
-74,03
7,22
7,64
31,02
55,24
79,99
105,10
130,40
15,5,87
181,41
142,276
-5,293
-5,561
-16,948
-24,
Ш
-29,131
-32,813
-35,623
-37,849
-39,640
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, ГриНшилдсом
и
Россини [820].
Температуры переходов отобраны Россини, Питцером, Арнеиом,
Брауном
и
Пиментелом [1248].
Тт = 188,35° К и ТЪ = 440,9° К.
.\« 179
г, °к
298
300
400
500
600
700
800
900
1000
.
4-Метилнонан,
СюН
2
2
(состояние
идеального
газа).
кал/(могь-°К)
Гр°
56,79
57,06
71,92
85,36
96,95
106,73
115,02
122,08
128,40
129,12
129,48
147,96
165,49
182,10
197,80
212,61
226,57
239,77
129,12
129,13
131,55
136,60
142,81
149,55
156,52
163,54
170,50
Мол.
вес
ккал/моль
0,00
0,11
6,57
14,45
23,53
33,78
14,88
56,74
69,27
дн/°
-60,70
-60,78
-64,42
-67,41
-69,76
-71,52
-72,78
-73,61
-74,03
ДЙ/°
7,22
7,64
31,02
55,24
79,99
105.10
130,40
155,87
181,41
142,270
-5,29!
-5,564
-16,948
-24,
Ш
-29,131
-32,81,!
-35,62.
-37,819
-39,641
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Температуры переходов отобраны Россини, Питцером, Арнеттом,
Брауном
и
Пиментелом [1248].
Тт = 174,4° К и ТЪ = 438,8° К.
Л»
180.
5-Метилыонан, С
10
Н
22
(состояние идеального газа). Мол.
вес
142,276
т
°к
298
300
400
500
600
700
800
900
1000
Сг
56
57
71
85,
96,
106,
115,
122,
128,
79
06
92
36
95
73
02
08
40
каломель
°]
|
S-
127,74
128,10
146,58
164,11
180,72
196,42
211,23
225,19
238,39
1
~
(
G°-f
127,
127,
130,
135,
141,
148,
155,
162,
169,
74
75
17
22
43
17
14
16
12
ккал/моль
н
°-
н
г»й
0,00
0,11
6,57
14,45
23,58
33,78
44,88
56,74
69,27
дя/°
-60,70
-60,78
-64,42
-67,41
-69,76
-71,52
-72,78
-73,61
-74,03
ДО/
0
7,63
8,05
31,57
55,93
80,81
106,07
131,51
157,11
182,79
lg Kf>
5 595
—5,865
-17,250
-24,445
-29 435
-33,114
-38,150
-39,947
Результаты низкотемпературных измерений, выполненных Парк-
сом, Уестом
и
Муром [1120], использовались
в
сочетании
со зна-
чениями,
отобранными Россини, Питцером, Арнеттом, Брауном
и
Пиментелом [1248],
а
также
с
величиной энтальпии образования,
рассчитанной Лаббауфом, Гриншилдсом
и
Россини [820]. Термодина-
мические функции
для
газообразного состояния вычислены
по
мето-
дам Соудерса, Маттюза
и
Харда [1396, 1397].
Тт = 185,45° К,
АНт°
= 3,977
ккал/моль
и ТЪ = 438,2° К.
№
181.
З-Этилоктан,
С
10
Н
22
(состояние
идеального
газа).
Мол. вес
142,276
Т, "К
298
300
400
500
600
700
800
900
1000
кал/(.моль-
°К)
Ср°
55,72
55,99
71,33
85,03
96,79
106,65
111,98
122,07
128,40
s°
127,7'4
128,09
146,34
163,76
180,33
196,01
210,81
224,77
237,97
-(О°-я
2
°
98
)/г
127,74
127,75
130,13
135,13
141,29
148,00
154,94
161,93
168,88
пкал/моль
Н
°-
Н
2
°98
0,00
0,11
6,49
14,32
23,43
33,61
44,71
56,56
69,09
дн/°
-60,01
-60,09
-63,81
-66,85
-69,22
-70,99
-72,26
-73,09
-73,51
|
&Gf°
8,32
8,74
32,28
56,66
81,59
1С6.88
132,36
158,01
183,73
lg Кр
-6,101
-6,368
-17,634
-24,766
-29,716
-33,368
-36,157
-38,367
-40,152
20*
308
Часть
2.
Термические
и
термохимические свойства веществ
Термодинамические
функции
для
газообразного
состояния
вычис-
лены
по
методам
Соудерса,
Маттюза
и
Харда
[1396,
1397];
энтальпия
образования
рассчитана
Лаббауфом,
Гриншилдсом
и
Россини
[820].
Точка
кипения
при
нормальных
условиях
принята
согласно
работе
Россини,
Питцера,
Арнетта,
Брауна
и
Пиментела
[1248].
ТЪ
=
=
439,6°
К.
IX. Химическая термодинамика
углеводородов
309
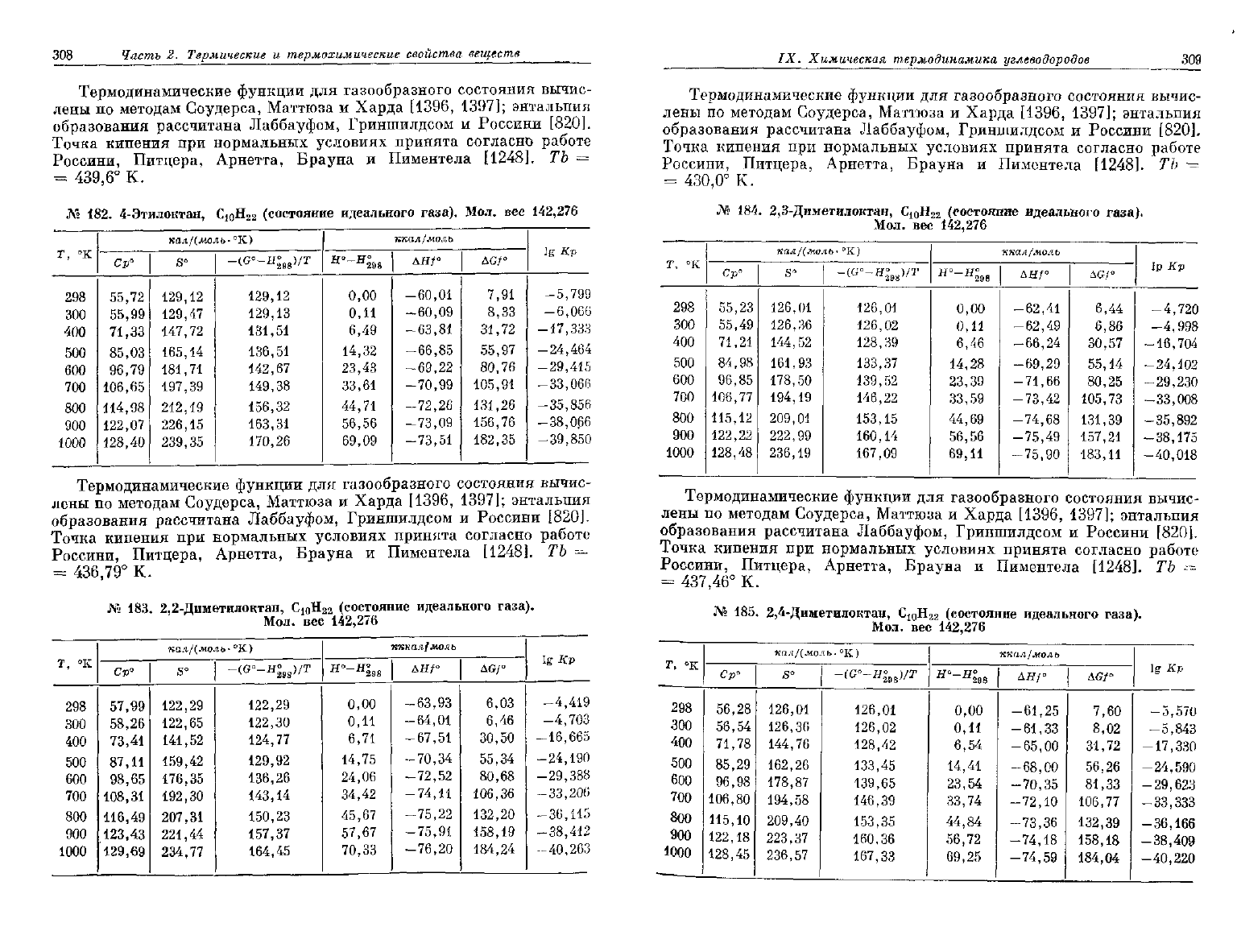
№
182.
4-Этилоктан,
г,
°к
298
300
400
500
600
700
800
900
1000
Ci
0
H
22
(состояние
идеального
газа).
кал/(моль-°К)
Ср°
55,72
55,99
71,33
85,03
96,79
106,65
114,98
122,07
128,40
S*
129,12
129,47
147,72
165,14
181,71
197,39
212,19
226,15
239,35
-(С"-я;
м
)/т
129,12
129,13
131,51
136,51
142,67
149,38
156,32
163,31
170,26
Мол.
вес
ккал/моль
Н
°-
Я
1
98
0,00
0,11
6,49
14,32
23,43
33,61
44,71
56,56
69,09
дн/°
-60,01
-60,09
-63,81
-66,85
-69,22
-70,99
-72,26
-73,09
-73,51
AG/°
7,91
8,33
31,72
55,97
80,76
105,91
131,26
156,76
182,35
142,276
-5,799
-6,066
-17,333
-24,464
-29,415
-33,066
-35,856
-38,066
-39,850
Термодинамические
функции
для
газообразного
состояния
вычис-
лены
по
методам
Соудерса,
Маттюза
и
Харда
[1396,
1397];
энтальпия
образования
рассчитана
Лаббауфом,
Гриншилдсом
и
Россини
[820].
Точка
кипения
при
нормальных
условиях
принята
согласно
работе
Россини,
Питцера,
Арнетта,
Брауна
и
Пиментела
[1248].
ТЪ
=
=
436,79°
К.
№
183.
2,2-Диметилоктан,
СюН
2
2
(состояние
идеального
газа).
Мол.
вес
142,276
т,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль-°К)
Ср«
57,99
58,26
73,41
87,11
98,65
108,31
116,49
123,43
129,69
S°
122,29
122,65
141,52
159,42
176,35
192,30
207,31
221,44
234,77
-(G°-H»
98
)/T
122,29
122,30
124,77
129,92
136,26
143,14
150,23
157,37
164,45
0,00
0,11
6,71
14,75
24,06
34,42
45,67
57,67
70,33
кккал/моль
AHf°
-63,93
-64,01
-67,51
-70,34
-72,52
-74,11
-75,22
-75,91
-76,20
6,03
6,46
30,50
55,34
80,68
106,36
132,20
158,19
184,24
lg Кр
-4,419
-4,703
-16,665
-24,190
-29,388
-33,200
-36,115
-38,412
-40,263
Термодинамические
функции
для
газообразного
состояния
вычис-
лены
по
методам
Соудерса,
Маттюза
и
Харда
[1396,
1397];
энтальпия
образования
рассчитана
Лаббауфом,
Гриншилдсом
и
Россини
[820].
Точка
кипения
при
нормальных
условиях
принята
согласно
работе
Россини,
Питцера,
Арнетта,
Брауна
и
Пиментела
[1248].
ТЪ
—
=
430,0°
К.
№
184.
2,3-Диметилоктан,
С
10
Н
22
(состояние
идеального
газа).
Мол.
вес
142,276
298
300
400
500
600
700
800
900
1000
кал/(л«>ль-°К)
55,23
55,49
71,21
84,98
96,85
106,77
115,12
122,22
128,48
Со
126,01
126,36
144,52
161,93
178,50
194,19
209,01
222,99
236,19
-(G--H|,
g
)/r
126,01
126,02
128,39
133,37
139,52
146,22
153,15
160,14
167,09
ккал/моль
0,00
0,11
6,46
14,28
23,39
33,59
44,69
56,56
69,11
ДЯ/°
-62,41
-62,49
-66,24
-69,29
-71,66
-73,42
-74,68
-75,49
-75,90
де/°
6,44
6,86
30,57
55,14
80,25
105,73
131,39
157,21
183,11
1р
Кр
-4,720
-4,998
-16,704
-24,102
-29,230
-33,008
-35,892
-38,175
-40,018
Термодинамические
функции
для
газообразного
состояния
вычис-
лены
по
методам
Соудерса,
Маттюза
и
Харда
[1396,
1397];
энтальпия
образования
рассчитана
Лаббауфом,
Гриншилдсом
и
Россини
[820].
Точка
кипения
при
нормальных
условиях
принята
согласно
работе
Россини,
Питцера,
Арнетта,
Брауна
и
Пиментела
[1248].
ТЪ
—
=
437,46°
К.
№
185.
2,4-Диметилоктан,
С
10
Н
2
2
(состояние
идеального
газа).
Мол.
вес
142,276
298
300
400
500
600
700
800
900
1000
кал/(моль
•
°К)
Ср°
56,28
56,54
71,78
85,29
96,98
106,80
115,10
122,18
128,45
S
0
126,01
126,36
144,76
162,26
178,87
194,58
209,40
223,37
236,57
126,01
126,02
128,42
133,45
139,65
146,39
153,35
160,36
167,33
ккал/моль
Н
°-
Н
2
9
8
0,00
0,11
6,54
14,41
23,54
33,74
44,84
56,72
69,25
дя/°
-61,25
-61,33
-65,00
-68,00
-70,35
-72,10
-73,36
-74,18
-74,59
AGf°
7,60
8,02
31,72
56,26
81,33
106,77
132,39
158,18
184,04
-5,570
-5,843
-17,330
-24,590
-29,623
-33,333
-36,166
-38,409
-40,220
310
Часть
2. Термические и
термохимические
свойства
веществ
IX. Химическая
термодинамика
углеводородов
311
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЪ =
=
429,0°
К.
№
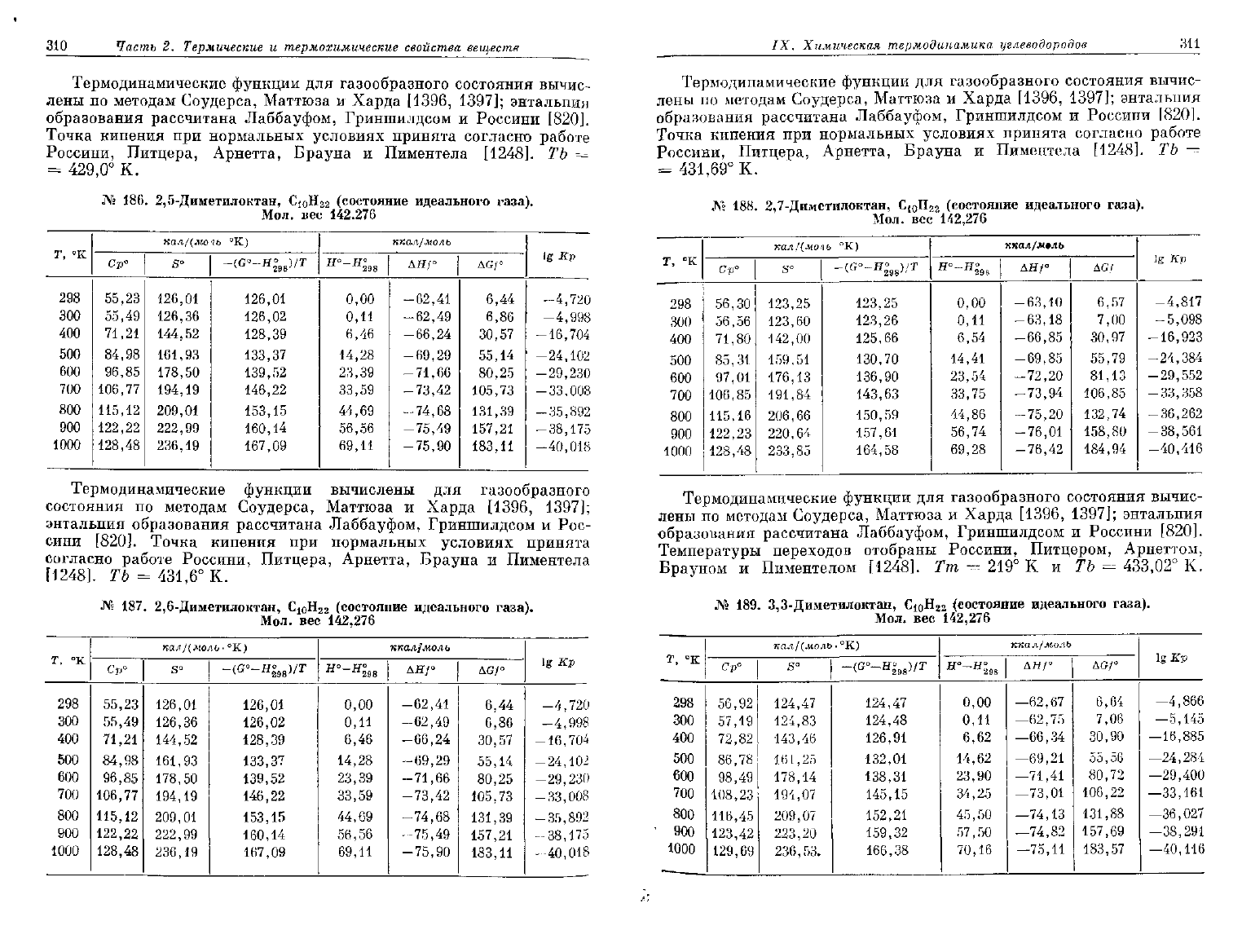
186.
2,5-Диметилоктан,
СюН
2
2 (состояние
идеального
газа).
Мол.
вес
142.276
298
300
400
500
600
700
800
900
1000
кал/(моаь
°К)
Ср°
55,23
55,49
71,21
84,98
96,85
106,77
115,12
122,22
128,48
s-
|
-<с°-я°
в8
)/г
126,01
126,36
144,52
161,93
178,50
194,19
209,01
222,99
236,19
126,01
126,02
128,39
133,37
139,52
146,22
153,15
160,14
167,09
кпал/моль
Н
°-
Н
298
0,00
0,11
6,46
14,28
23,39
33,59
44,69
56,56
69,11
дн/°
-62,41
-62,49
-66,24
-69,29
-71,66
-73,42
-74,68
-75,49
-75,90
AGf
6,44
6,86
30,57
55,14
80,25
105,73
131,39
157,21
183,11
lg Кр
-4,720
-4,998
-16,704
-24,102
-29,230
-33.008
-35,892
-38,175
-40,018
Термодинамические функции вычислены
для
газообразного
состояния
по
методам Соудерса, Маттюза
и
Харда [1396, 1397];
энтальпия образования рассчитана Лаббауфом, Гриншилдсом
и Рос-
сини
[820]. Точка кипения
при
нормальных условиях принята
согласно работе Россини, Питцера, Арнетта, Брауна
и
Пиментела
[1248].
ТЪ =
431,6°
К.
№
187.
2,6-Диметилоктан,
CJQH
2
2
(состояние
идеального
газа).
Мол.
вес
142,276
т,
°к
298
300
400
500
600
700
800
900
1000
кал
1(моль
•
°К)
Ср°
55,23
55,49
71,21
84,98
96,85
106,77
115,12
122,22
128,48
s°
126,01
126,36
144,52
161,93
178,50
194,19
209,01
222,99
236,19
-<«°-
Я
298>/
Г
126,01
126,02
128,39
133,37
139,52
146,22
153,15
160,14
167,09
кпал/моль
0,00
0,11
6,46
14,28
23,39
33,59
44,69
56,56
69,11
ДЯ/°
-62,41
-62,49
-66,24
-69,29
-71,66
-73,42
-74,68
-75,49
-75,90
AGf°
6,44
6,86
30,57
55,14
80,25
105,73
131,39
157,21
183,11
lg Кр
-4,720
-4,998
-16,704
-24,102
-29,230
-33,008
-35,892
-38,175
-40,018
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
«образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
|Точка кипения
при
нормальных условиях принята согласно работе
}Россини, Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЪ =
'=
431,69° К.
№
188.
2,7-Диметилоктан,
С
10
Н
22
(состояние
идеального
газа).
Мол.
вес
142,276
Т,
°к
298
300
400
500
600
700
800
900
1000
Ср°
56,30
56,56
71,80
85,31
97,01
106,85
115,16
122,23
128,48
кал/(мо
S°
123,25
123,60
142,00
159,51
176,13
191,84
206,66
220,64
233,85
ь
-К)
-(G->-Hj,
g
)/r
123,25
123,26
125,66
130,70
136,90
143,63
150,59
157,61
164,58
ККПЛ/МФЛЬ
Н
°~
Н
298
0,00
0,11
6,54
14,41
23,54
33,75
44,86
56,74
69,28
ДЯ/°
-63,10
-63,18
-66,85
-69,85
-72,20
-73,94
-75,20
-76,01
-76,42
AGf
6,57
7,00
30,97
55,79
81,13
106,85
132,74
158,80
184,94
lg Кр
-4,817
-5,098
-16,923
-24,384
-29,552
-33,358
-36,262
-38,561
-40,416
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Температуры переходов отобраны Россини, Питцером, Арнеттом,
Брауном
и
Пиментелом [1248]. Ттп -=
219° К и ТЪ = 433,02° К.
№
189.
3,3-Диметилоктан, С
10
Н
22
(состояние идеального газа).
Мол.
вес 142,276
Т, °К
298
300
400
500
600
700
800
900
1000
Ср°
56,92
57,19
72,82
86,78
98,49
108,23
116,45
123,42
129,69
кал/(моль
8'
124,47
124,83
143,46
161,25
178,14
194,07
209,07
223,20
236,53.
•°К)
-«*--*!,„>/г
124,47
124,48
126,91
132,01
138,31
145,15
152,21
159,32
166,38
кпал/моль
0,00
0,11
6,62
14,62
23,90
34,25
45,50
57,50
70,16
дя/°
—62,67
—62,75
—66,34
—69,21
—71,41
—73,01
—74,13
—74,82
—75,11
AGf
0
6,64
7,06
30,90
55,56
80,72
106,22
131,88
157,69
183,57
lg Кр
—4,866
—5,145
—16,885
—24,284
—29,400
—33,161
—36,027
—38,291
—40,116
312
Часть
2.
Термические
и
термохимические свойства веществ
IX. Химическая термодинамика
углеводородов
313
Термодинамические функции для газообразного состояния вычис-
лены по методам Соудерса, Маттюза и Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом и Россини [820].
Точка
кипения
при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна и Пиментела [1248]. ТЬ =
•=
434,3°
К.
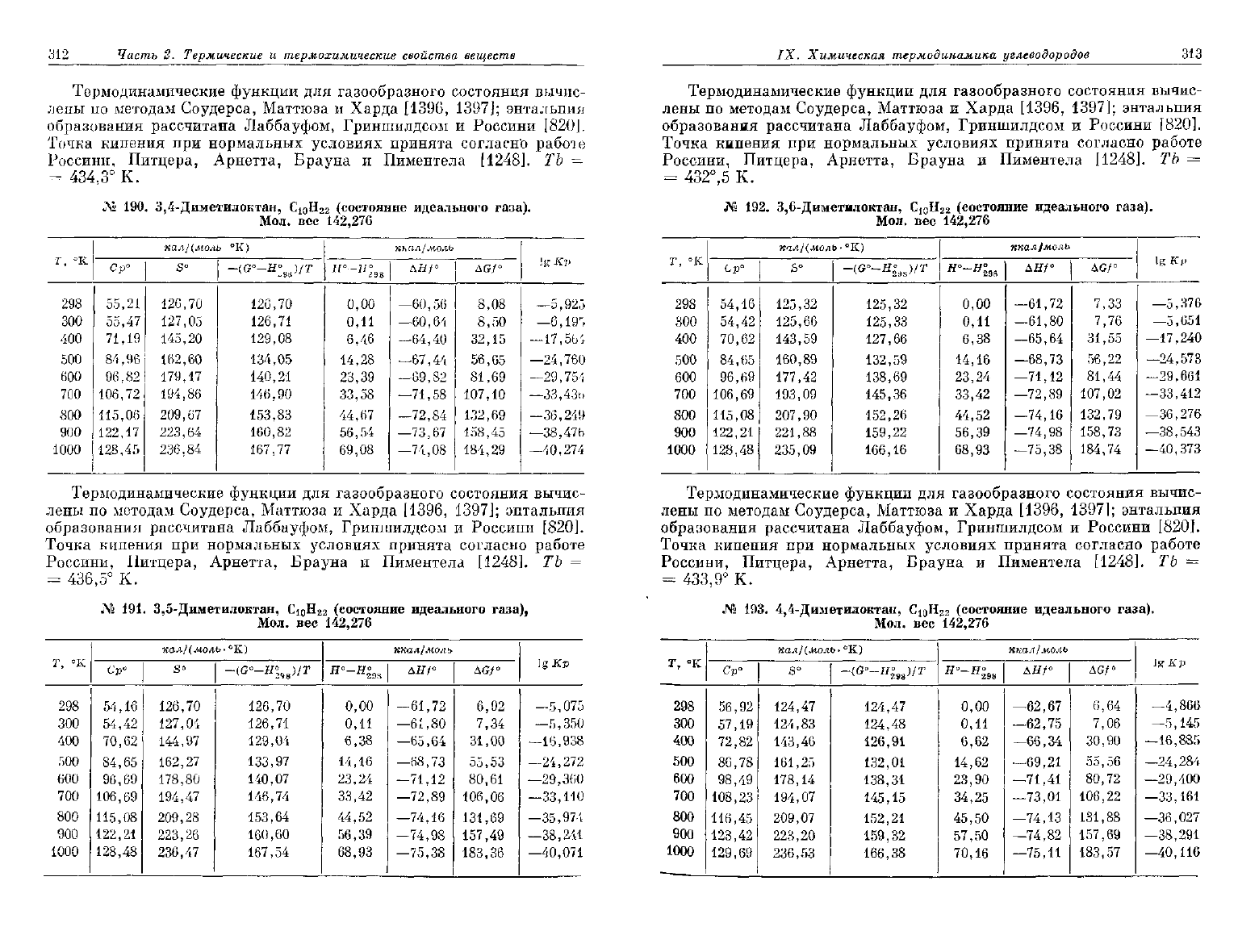
№ 190. 3,4-Диметилоктан, С
10
Н
2
2 (состояние идеального газа).
Мол.
вес
142,276
г, °к
298
300
400
500
600
700
800
900
1000
кал/(моль
°К)
Ср°
55,21
55,47
71,19
84,96
96,82
106,72
115,08
122,17
128,45
Со
126,70
127,05
145,20
162,60
179,17
194,86
209,67
223,64
236,84
-(О°-я_°
98
)/г
126,70
126,71
129,08
134,05
140,21
146,90
153,83
160,82
167,77
ккал/моль
НО
-
Я
?98
0,00
0,11
6,46
14,28
23,39
33,58
44,67
56,54
69,08
дя/°
—60,56
-60,64
—64,40
—67,44
—69,82
—71,58
—72,84
—73,67
—74,08
AGf°
8,08
8,50
32,15
56,65
81,69
107,10
132,69
158,45
184,29
**>
—5,925
—6,195
—17,564
—24,760
—29,754
—33,43t>
—36,249
—38,47b
—40,274
Термодинамические функции для газообразного состояния вычис-
лены по методам Соудерса, Маттюза и Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом и Россини [820].
Точка
кипения
при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна и Пиментела [1248]. ТЪ =
=
436,5°
К.
JVs 191. 3,5-Диметилоктан,
Ci
0
H
22
(состояние идеального газа),
Мол.
вес
142,276
Г,
°К
298
300
400
500
600
700
800
900
1000
кал)(моль
-°К)
C
V
°
54,16
54,42
70,62
84,65
96,69
106,69
115,08
122,21
128,48
s°
126,70
127,04
144,97
162,27
178,80
194,47
209,28
223,26
236,47
-
(
G°-Hi
4s
)/T
126,70
126,71
129,04
133,97
140,07
146,74
153,64
160,60
167,54
ккал/моль
Н
°-
Н
2°98
0,00
0,11
6,38
14,16
23,24
33,42
44,52
56,39
68,93
дя/°
-61,72
—61,80
—65,64
—68,73
—71,12
—72,89
—74,16
—74,98
—75,38
AGf°
6,92
7,34
31,00
55,53
80,61
106,06
131,69
157,49
183,36
igKp
—5,075
—5,350
—16,938
—24,272
—29,360
—33,110
-35,974
—38,241
—40,071
Термодинамические функции для газообразного состояния вычис-
лены по методам Соудерса, Маттюза и Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом и Россини [820].
Точка
кипения
при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна и Пиментела [1248]. ТЬ =
=
432°,5
К.
г, °к
298
300
400
500
600
700
800
900
1000
№
192.
3,6-Диметилоктан,
С
10
Н
К
ад/(.«ол
Ср°
54,16
54,42
70,62
84,65
96,69
106,69
115,08
122,21
128,48
s°
125,32
125,66
143,59
160,89
177,42
193,09
207,90
221,88
235,09
22
(состояние
идеального
газа).
Мол.
вес
142,276
ь.°К)
-(О'-В^)/Т
125,32
125,33
127,66
132,59
138,69
145,36
152,26
159,22
166,16
ккал/моль
Д
°-
Я
298
0,00
0,11
6,38
14,16
23,24
33,42
44,52
56,39
68,93
дя/°
—61,72
—61,80
—65,64
—68,73
—71,12
—72,89
—74,16
—74,98
—75,38
до/-
7,33
7,76
31,55
56,22
81,44
107,02
132,79
158,73
184,74
lg
Кр
—5,376
—5,651
—17,240
—24,573
—29,661
—33,412
—36,276
—38,543
—40,373
Термодинамические функции для газообразного состояния вычис-
лены по методам Соудерса, Маттюза и Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом и Россини [820].
Точка
кипения
при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна и Пиментела [1248]. ТЬ =
=
433,9°
К.
№
193.
4,4-Диметилоктан,
СюНгг
(состоящие
идеального
газа).
Мол.
вес
142,276
Г,
°К
298
300
400
500
600
700
800
900
1000
^—
кал/
(моль
•
°К)
Ср°
56,92
57,19
72,82
86,78
98,49
108,23
116,45
123,42
129,69
s°
124,47
124,83
143,46
161,25
178,14
194,07
209,07
223,20
236,53
-(G°-H|
98
)/r
124,47
124,48
126,91
132,01
138,31
145,15
152,21
159,32
166,38
ккал/моль
Н
~
Н
298
0,00
0,11
6,62
14,62
23,90
34,25
45,50
57,50
70,16
дя/°
—62,67
—62,75
—66,34
—69,21
—71,41
—73,01
—74,13
—74,82
—75,11
AG/°
6,64
7,06
30,90
55,56
80,72
106,22
131,88
157,69
183,57
IK
KP
—4,866
—5,145
—16,885
—24,284
—29,400
—33,161
—36,027
—38,291
—40,116
314
Часть
2.
Термические
и
термохимические
свойства
веществ
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка кипения
при
нормальных условиях принята согласно-работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ
=
=
430,6°
К.
IX.
Химическая
термодинамика
углеводородов
315
Г,
°К
298
300
400
500
600
700
800
900
1000
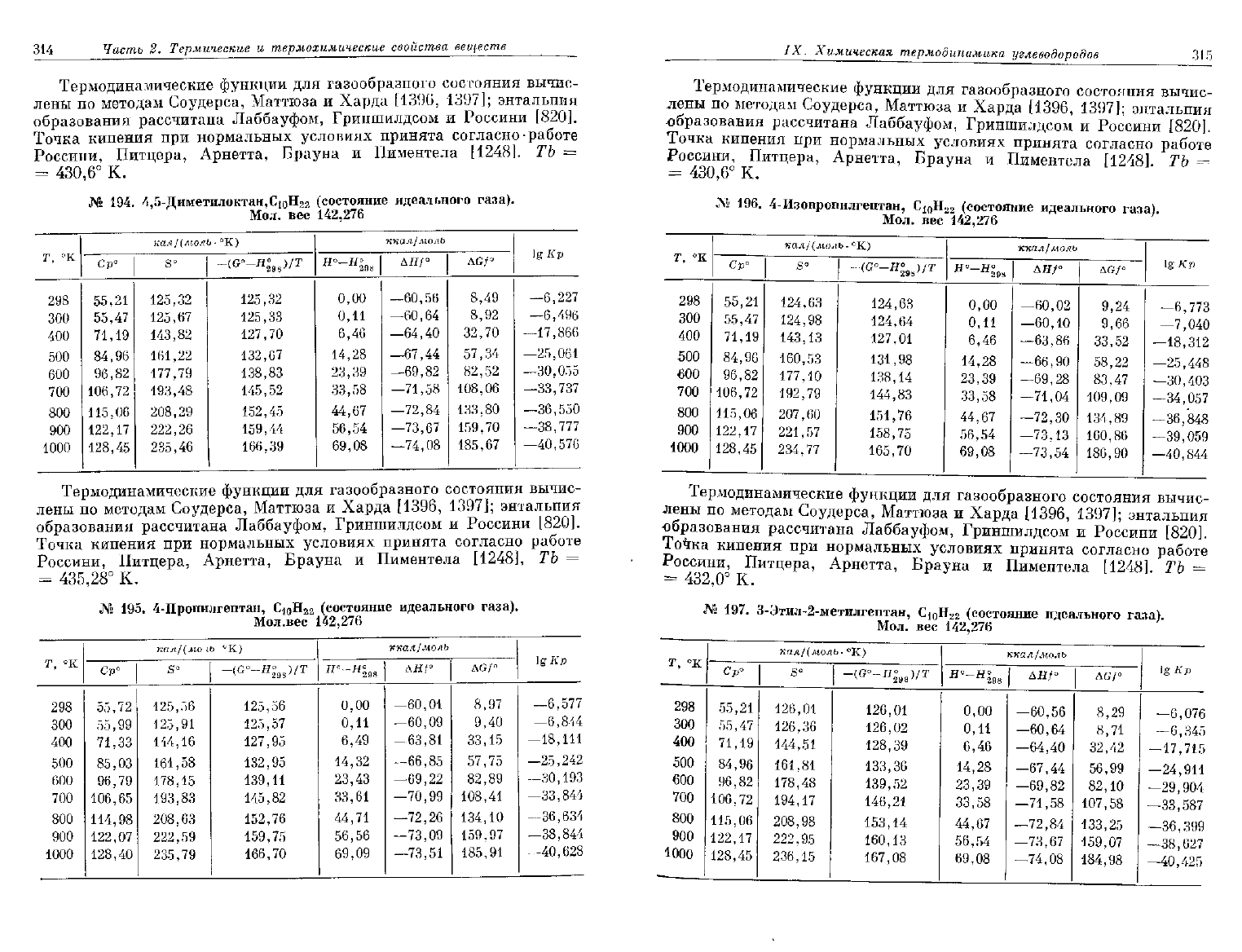
№
194.
4,5-Диметилоктан,С
10
Н
2
2
Мол.
вес
кал /
(моль
•
°К)
C
V
°
55,21
55,47
71,19
84,96
96,82
106,72
115,06
122,17
128,45
s°
125,32
125,67
143,82
161,22
177,79
193,48
208,29
222,26
235,46
-(G°-H°
98
)/r
125,32
125,33
127,70
132,67
138,83
145,52
152,45
159,44
166,39
(состояние
идеального
газа).
142,276
кпал/моль
Н
°-*298
0,00
0,11
6,46
14,28
23,39
33,58
44,67
56,54
69,08
—60,56
—60,64
—64,40
—67,44
—69,82
—71,58
—72,84
—73,67
—74,08
AGf°
8,49
8,92
32,70
57,34
82,52
108,06
133,80
159,70
185,67
lg
Кр
—6,227
—6,496
—17,866
—25,061
—30,055
—33,737
—36,550
—38,777
—40,576
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248],
ТЬ
=
=
435,28°
К.
№
195.
4-Пропилгептан, С
10
Н
2
2 (состояние идеального газа).
Мол.вес
142,276
г,
°к
298
300
400
500
600
700
800
900
1000
кал/(мо
ib °К)
Ср°
55,72
55,99
71,33
85,03
96,79
106,65
114,98
122,07
128,40
s°
125,56
125,91
144,16
161,58
178,15
193,83
208,63
222,59
235,79
-(С°-я
2
°
98
)/г
125,56
125,57
127,95
132,95
139,11
145,82
152,76
159,75
166,70
якал/моль
Ы
~-"298
0,00
0,11
6,49
14,32
23,43
33,61
44,71
56,56
69,09
AHf
—60,01
—60,09
—63,81
—66,85
—69,22
—70,99
—72,26
—73,09
—73,51
AGf°
8,97
9,40
33,15
57,75
82,89
108,41
134,10
159,97
185,91
—6,577
—6,844
—18,111
—25,242
—30,193
—33,844
—36,634
—38,844
—40,628
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ
=
=
430,6°
К.
•N»
196.
4-Изопропилгептан,
Ci
0
H
2
2
(состояние
идеального
газа).
Мол.
вес
142,276
298
300
400
500
600
700
800
900
1000
Ср°
55,21
55,47
71,19
84,96
96,82
106,72
115,06
122,17
128,45
кал!
(моль.
1
S
°
124,63
124,98
143,13
160,53
177,10
192,79
207,60
221,57
234,77
°К)
/по
(.ЦТ
124
124
127
131
138
144
151
158
165
Н
298>/
Г
,63
,64
,01
,98
,14
,83
,76
,75
,70
0,
0,
6,
14,
23,
33,
44,
56,
69,
Н
298
00
11
46
28
39
58
67
54
08
ккал/моль
AHf
—60,02
—60,10
—63,86
—66,90
—69,28
—71,04
—72,30
—73,13
—73,54
AGf
9,24
9,66
33.52
58,22
83,47
109,09
134,89
160,86
186,90
lgKp
—6,773
—7,040
—18,312
—25,448
—30,403
—34,057
—36,848
—39,059
—40,844
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ
=
=
432,0°
К.
№
197.
З-Этил-2-метилгептан,
СюН
2
2
(состояние
идеального
газа).
Мол.
вес
142,276
Т, "К
298
300
400
500
600
700
800
900
1000
пал
1'(моль
•
°К)
Ср°
55,21
55,47
71,19
84,96
96,82
106,72
115,06
122,17
128,45
s°
126,01
126,36
144,51
161,81
178,48
194,17
208,98
222,95
236,15
[
-(с°-я;
и
)/т
126,01
126,02
128,39
133,36
139,52
146,21
153,14
160,13
167,08
ккал/моль
Н
~
Й
298
0,00
0,11
6,46
14,28
23,39
33,58
44,67
56,54
69,08
I
AHf
—60,56
—60,64
—64,40
—67,44
—69,82
—71,58
—72,84
—73,67
—74,08
AGf
8,29
8,71
32,42
56,99
82,10
107,58
133,25
159,07
184,98
ig
Кр
—6,076
—6,345
—17,715
—24,911
—29,904
—33,587
—36,399
—38,627
—40,425
316
Часть
2.
Термические
и
термохимические свойства веществ
IX. Химическая термодинамика
углеводородов
317
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка
кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ —
=
434,3°
К.
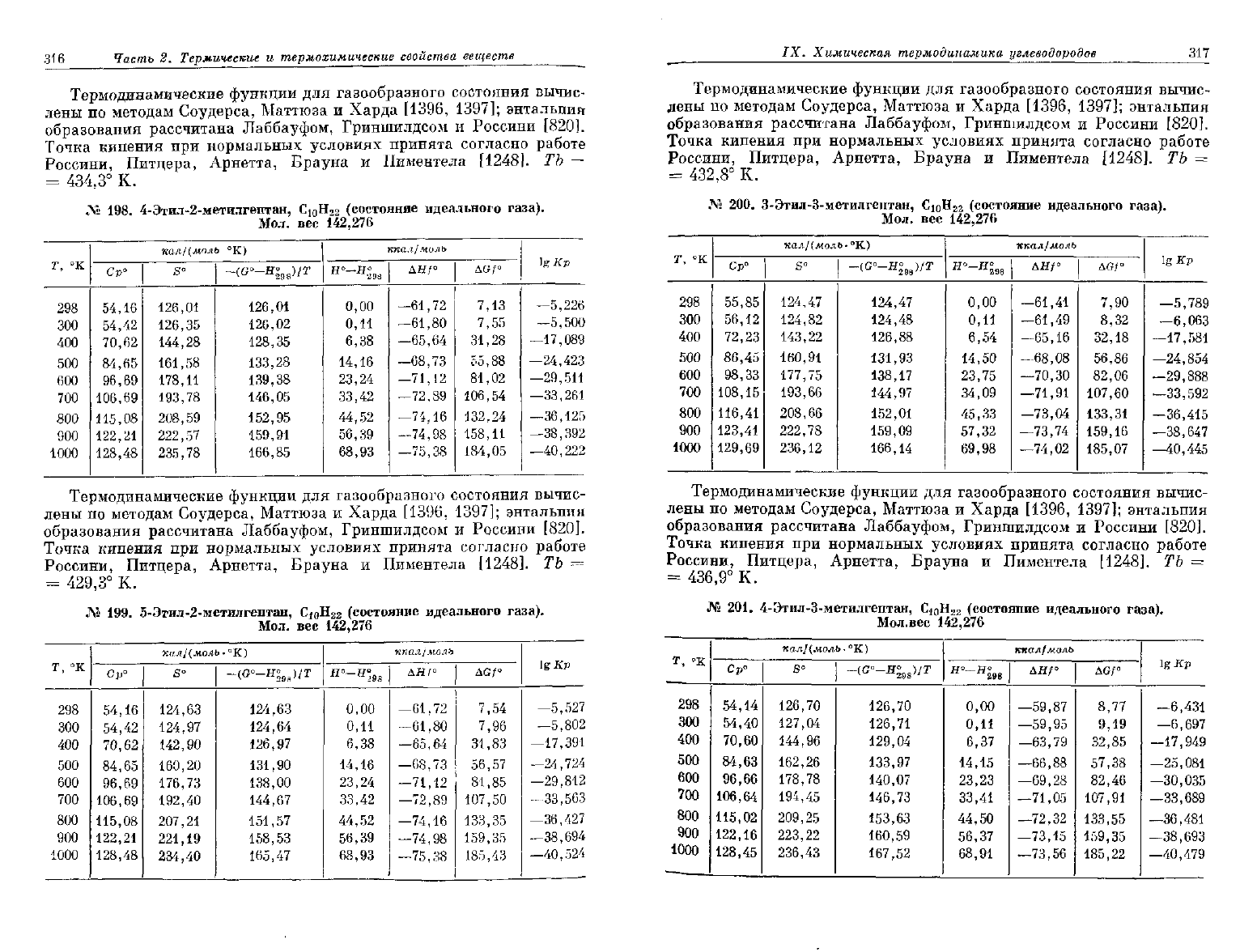
№
198.
4-Этил-2-метилгептан, С
10
Н
2
2 (состояние идеального газа).
Мол.
вес
142,276
г,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль
°К)
Ср°
54,16
54,42
70,62
84,65
96,69
106,69
115,08
122,21
128,48
s°
126,01
126,35
144,28
161,58
178,11
193,78
208,59
222,57
235,78
_(G°-H£
98
)/T
126,01
126,02
128,35
133,28
139,38
146,05
152,95
159,91
166,85
0,00
0,11
6,38
14,16
23,24
33,42
44,52
56,39
68,93
ккал/моль
АН/
0
—61,72
—61,80
—65,64
—68,73
—71,12
—72,89
—74,16
—74,98
—75,38
AGf°
7,13
7,55
31,28
55,88
81,02
106,54
132,24
158,11
184,05
—5,226
—5,500
—17,089
—24,423
—29,511
—33,261
—36,125
—38,392
—40,222
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка
кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ =
=
429,3°
К.
№
199.
5-Этил-2-метилгептан,
СюН
22
(состояние идеального газа).
Мол.
вес
142,276
г,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль-°К)
Ср°
54,16
54,42
70,62
84,65
96,69
106,69
115,08
122,21
128,48
s°
124,63
124,97
142,90
160,20
176,73
192,40
207,21
221,19
234,40
-(
G
°-
H
298><'
r
124,63
124,64
126,97
131,90
138,00
144,67
151,57
158,53
165,47
ккал/моль
H
°-
H
°m
0,00
0,11
6,38
14,16
23,24
33,42
44,52
56,39
68,93
дя/°
—61,72
—61,80
—65,64
—68,73
—71,12
—72,89
—74,16
—74,98
—75,38
AGf°
7,54
7,96
31,83
56,57
81,85
107,50
133,35
159,35
185,43
—5,527
—5,802
—17,391
—24,724
—29,812
—33,563
—36,427
—38,694
—40,524
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка
кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ =
=
432,8°
К.
№
200.
З-Этил-3-метилгептан,
Ci
0
H
2
2
(состояние идеального газа).
Мол.
вес
142,276
298
300
400
500
600
700
800
900
1000
кал/
(моль
-°К)
Ст>°
55,85
56,12
72,23
86,45
98,33
108,15
116,41
123,41
129,69
S°
124,47
124,82
143,22
160,91
177,75
193,66
208,66
222,78
236,12
-(
G
°-
H
298^
T
124,47
124,48
126,88
131,93
138,17
144,97
152,01
159,09
166,14
ккал/моль
по
TJO
0,00
0,11
6,54
14,50
23,75
34,09
45,33
57,32
69,98
дя/°
—61,41
—61,49
—65,16
—68,08
—70,30
—71,91
-73,04
—73,74
—74,02
AG/°
7,90
8,32
32,18
56,86
82,06
107,60
133,31
159,16
185,07
lgKp
—5,789
—6,063
—17,581
—24,854
—29,888
—36,415
—38,647
—40,445
Термодинамические функции
для
газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка
кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ =
=
436,9°
К.
№
201.
4-Этил-З-метилгептан,
Ci
0
H
2
2
(состояние идеального газа).
Мол.вес
142,276
298
300
400
500
600
700
800
900
1000
палЦмоль
•
°К)
Ср°
54,14
54,40
70,60
84,63
96,66
106,64
115,02
122,16
128,45
S»
126,70
127,04
144,96
162,26
178,78
194,45
209,25
223,22
236,43
-(G°-H°
98
)/T
126,70
126,71
129,04
133,97
140,07
146,73
153,63
160,59
167,52
ккал/моль
Н
°-
Н
298
0,00
0,11
6,37
14,15
23,23
33,41
44,50
56,37
68,91
дя/°
—59,87
—59,95
—63,79
—66,88
—69,28
—71,05
—72,32
—73,15
—73,56
AGf°
8,77
9,19
32,85
57,38
82,46
107,91
133,55
159,35
185,22
IgKp
—6,431
—6,697
—17,949
—25,081
—30,035
—33,689
—36,481
—38,693
—40,479
318
Часть
2.
Термические
и
термохимические
свойства
веществ
IX. Химическая
термодинамика
углеводородов
319
Термодинамические функции для газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка
кипения
при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248]. ТЬ
-
=
435,3°
К.
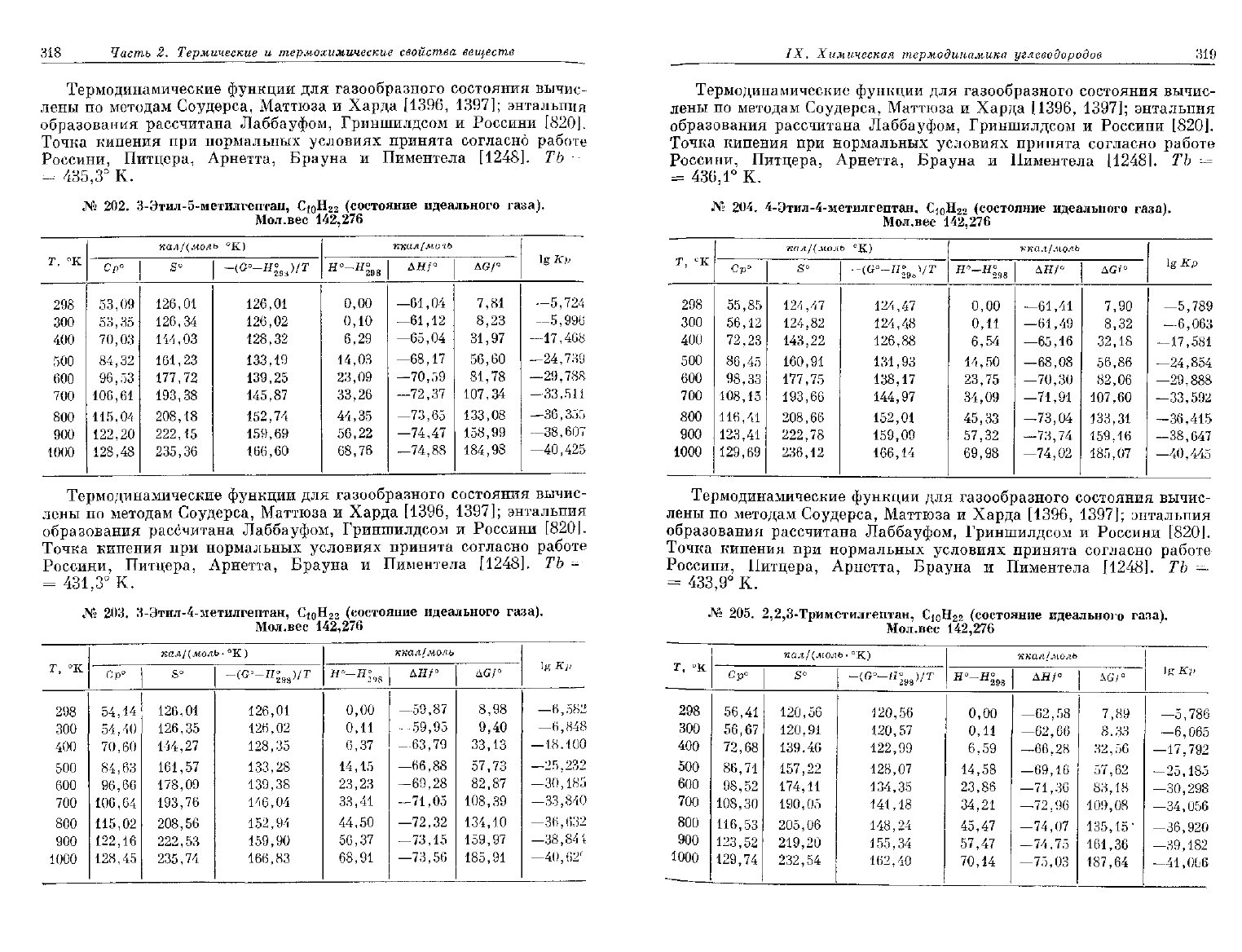
JV» 202. З-Этил-5-метилгептан,
Сц)Н
22
(состояние идеального газа).
Мол.вес
142,276
т,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль
°К)
Ср°
53,09
53,35
70,03
84,32
96,53
106,61
115,04
122,20
128,48
ч°
126,01
126,34
144,03
161,23
177,72
193,38
208,18
222,15
235,36
-(С°-я°
88
)/г
126,01
126,02
128,32
133,19
139,25
145,87
152,74
159,69
166,60
ккал/моъь
0,00
0,10
6,29
14,03
23,09
33,26
44,35
56,22
68,76
дн/°
—61,04
—61,12
—65,04
—68,17
—70,59
—72,37
—73,65
—74,47
—74,88
AGf°
7,81
8,23
31,97
56,60
81,78
107,34
133,08
158,99
184,98
lg
Кр
—5,724
—5,996
—17,468
—24,739
—29,788
—33,511
—36,355
—38,607
—40,425
Термодинамические функции для газообразного состояния вычис-
лены
по
методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка
кипения
при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248]. ТЬ
—
=
431,3°
К.
№
203.
З-Этил-4-метилгептан,
Ci
0
H
22
(состояние
идеального
газа).
Мол.вес
142,276
г,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль. °К)
Ср°
54,14
54,40
70,60
84,63
96,66
106,64
115,02
122,16
128,45
126,01
126,35
144,27
161,57
178,09
193,76
208,56
222,53
235,74
-
(
О'-Н°
т
)/Т
126,01
126,02
128,35
133,28
139,38
146,04
152,94
159,90
166,83
кпал/моль
0,00
0,11
6,37
14,15
23,23
33,41
44,50
56,37
68,91
—59,87
—59,95
—63,79
—66,88
—69,28
—71,05
—72,32
—73,15
—73,56
AGf°
8,98
9,40
33,13
57,73
82,87
108,39
134,10
159,97
185,91
Ig
Кр
—6,582
—6,848
—18.100
—25,232
—30,185
—33,840
—36,632
—38,844
—40,62
f
Термодинамические функции для газообразного состояния вычис-
лены по методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка
кипения
при
нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ =
=
436,1°
К.
№ 204. 4-Этил-4-метилгептан,
С
10
Н
22
(состояние идеального газа).
Мол.вес
142,276
т,
°к
298
300
400
500
600
700
800
900
1000
кал/(моль
°К)
Ср°
55,85
56,12
72,23
86,45
98,33
108,15
116,41
123,41
129,69
124,47
124,82
143,22
160,91
177,75
193,66
208,66
222,78
236,12
-(G
o
-H°
9(i
yr
124,47
124,48
126,88
131,93
138,17
144,97
152,01
159,09
166,14
ккал/моль
0,00
0,11
6,54
14,50
23,75
34,09
45,33
57,32
69,98
дя/°
—61,41
—61,49
—65,16
—68,08
—70,30
—71,91
—73,04
—73,74
—74,02
AGf
7,90
8,32
32,18
56,86
82,06
107,60
133,31
159,16
185,07
lg
Кр
—5,789
—6,063
—17,581
—24,854
—29,888
—33,592
—36,415
—38,647
—40,445
Термодинамические функции для газообразного состояния вычис-
лены по методам Соудерса, Маттюза
и
Харда [1396, 1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом
и
Россини [820].
Точка
кипения
при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна
и
Пиментела [1248].
ТЬ =
=
433,9°
К.
№
205. 2,2,3-Триметилгептан,
СюН
22
(состояние идеального газа).
Мол.вес
142,276
Г,
-К
298
300
400
500
600
700
800
900
1000
кал!(моль- °К)
Ср°
56,41
56,67
72,68
86,71
98,52
108,30
116,53
123,52
129,74
S»
120,56
120,91
139.46
157,22
174,11
190,05
205,06
219,20
232,54
120,56
120,57
122,99
128,07
134,35
141,18
148,24
155,34
162,40
ккал/моль
Н
°-
Н
298
0,00
0,11
6,59
14,58
23,86
34,21
45,47
57,47
70,14
дя;°
—62,58
—62,66
—66,28
-69,16
—71,36
—72,96
—74,07
—74,75
—75,03
7,89
8.33
32,56
57,62
83,18
109,08
135,15'
161,36
187,64
lg
Кр
-5,786
—6,065
—17,792
—25,185
—30,298
—34,056
—36,920
—39,182
—41,006
320
Часть
2.
Термические
и
термохимические
свойства
веществ
Термодинамические функции для газообразного состояния вычис-
лены по методам Соудерса, Маттюза и
Харда
[1396,
1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом и Россини [820].
Точка кипения при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна и Пиментела [1248]. ТЪ =
=
430,7°
К.
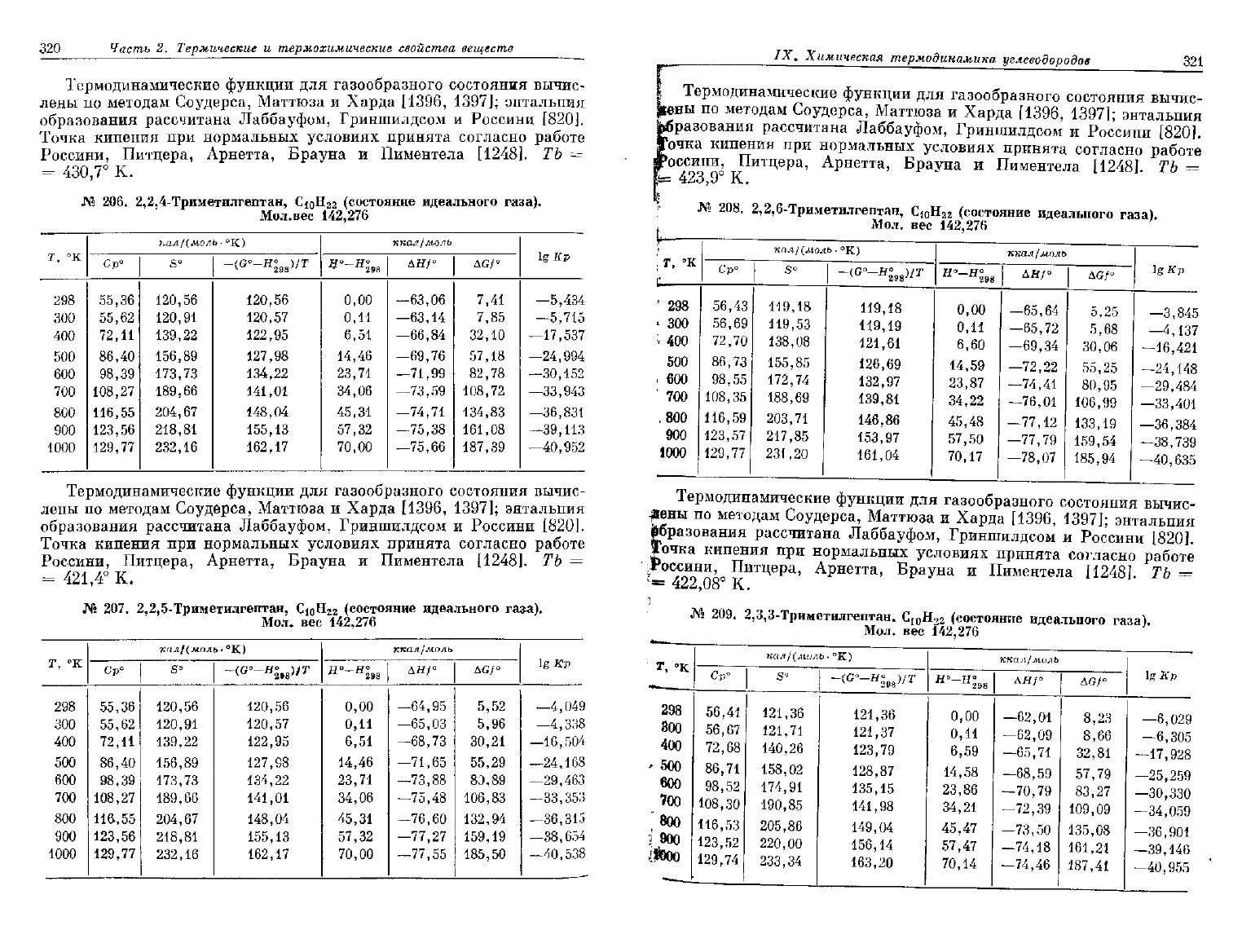
№
206. 2,2,4-Триметилгептан, СюН
2
2 (состояние идеального газа).
Мол.вес
142,276
IX,
Химическая
термодинамика
углеводородов
321
т,
°к
298
300
400
500
600
700
800
900
1000
1^ал/(моль-°'К)
Ср°
55,36
55,62
72,11
86,40
98,39
108,27
116,55
123,56
129,77
О
120,56
120,91
139,22
156,89
173,73
189,66
204,67
218,81
232,16
-(о°-я°
98
)/г
120,56
120,57
122,95
127,98
134,22
141,01
148,04
155,13
162,17
ккал/моль
ПО
XJO
1
Я
298
0,00
0,11
6,51
14,46
23,71
34,06
45,31
57,32
70,00
АН
Г
—63,06
—63,14
—66,84
—69,76
—71,99
—73,59
—74,71
—75,38
—75,66
AGf
7,41
7,85
32,10
57,18
82,78
108,72
134,83
161,08
187,39
lg Кр
—5,434
—5,715
—17,537
—24,994
—30,152
—33,943
—36,831
—39,113
—40,952
Термодинамические функции для газообразного состояния вычис-
лены по методам Соудерса, Маттюза и
Харда
[1396,
1397]; энтальпия
образования рассчитана Лаббауфом, Гриншилдсом и Россини [820].
Точка кипения при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна и Пиментела [1248]. ТЪ =
=
421,4°
К.
№
207.
2,2,5-Триметилгептан,
СюН
2
2
(состояние
идеального
газа).
Мол.
вес
142,276
Г, °К
298
300
400
500
600
700
800
900
1000
кал]
(моль
•
°К)
Ср°
55,36
55,62
72,11
86,40
98,39
108,27
116,55
123,56
129,77
s°
120,56
120,91
139,22
156,89
173,73
189,66
204,67
218,81
232,16
-(б"-я;,в>'
т
120,56
120,57
122,95
127,98
134,22
141,01
148,04
155,13
162,17
ккал/моль
П
298
0,00
0,11
6,51
14,46
23,71
34,06
45,31
57,32
70,00
AHf°
—64,95
—65,03
—68,73
—71,65
—73,88
—75,48
—76,60
—77,27
—77,55
AGf
5,52
5,96
30,21
55,29
8Э,89
106,83
132,94
159,19
185,50
lg КР
—4,049
—4,338
—16,504
—24,168
—29,463
—33,353
—36,315
—38,654
—40,538
Термодинамические функции для газообразного состояния вычис-
1вны по методам Соудерса, Маттюза и
Харда
[1396,
1397]; энтальпия
5разования рассчитана Лаббауфом, Гриншилдсом и Россини [820].
["очка
кипения при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна и Пиментела [1248]. ТЪ =
423,9°
К.
№
208. 2,2,6-Триметилгептан, СюНгг (состояние идеального газа).
Мол.
вес
142,276
Ж
298
Ш
300
Ш
40
°
Ш
50
°
Ж
600
Ж
70
°
Ж
800
Ж
900
в!
1000
кал/(моль-
°К)
Ср°
56,43
56,69
72,70
86,73
98,55
108,35
116,59
123,57
129,77
Со
119,18
119,53
138,08
155,85
172,74
188,69
203,71
217,85
231,20
|
-(в"-я;,
в
)/г
119,18
119,19
121,61
126,69
132,97
139,81
146,86
153,97
161,04
ккал/моль
н
°-
н
°
г98
0,00
0,11
6,60
14,59
23,87
34,22
45,48
57,50
70,17
1
AHf°
—65,64
—65,72
—69,34
—72,22
—74,41
—76,01
—77,12
—77,79
—78,07
AGf
5,25
5,68
30,06
55,25
80,95
106,99
133,19
159,54
185,94
]gKp
—3,845
—4,137
—16,421
—24,148
—29,484
—33,401
—36,384
—38,739
—40,635
Термодинамические функции для газообразного состояния вычис-
t
JHU
по методам Соудерса, Маттюза и
Харда
[1396,
1397]; энтальпия
5разования рассчитана Лаббауфом, Гриншилдсом и Россини [820].
очка кипения при нормальных условиях принята согласно работе
Россини,
Питцера, Арнетта, Брауна и Пиментела [1248]. ТЪ =
5=
422,08°
К.
**
№ 209.
2,3,3-Триметилгептан.
С
10
Н
2
2
(состояние
идеального
газа).
Мол.
вес
142,276
1
Т °К
Г i
>
298
300
400
*
500
600
700
800
й
900
Ср°
56,41
56,67
72,68
86,71
98,52
108,30
116,53
123,52
129,74
кал
/(моль
•
°К)
go
121,36
121,71
140,26
158,02
174,91
190,85
205,86
220,00
233,34
—(G°—Д
121
121,
123,
128,
135,
141,
149,
156,
163,
29s'
/J
36
37
79
87
15
98
04
14
20
я°—
0
0
6,
14,
23,
34,
45,
57,
70,
Н
298
00
11
59
58
86
21
47
47
14
ккал/моль
AHf
—62,01
—62,09
—65,71
—68,59
—70,79
—72,39
—73,50
—74,18
—74,46
AGf
8,23
8,66
32,81
57,79
83,27
109,09
135,08
161,21
187,41
—В
—6
—17
—35
—30
-34
—36
—39
—40
<Р
,029
, ЗЛ5
,928
959
330
,059
901
140
955
-831
