Пожарский А.Ф., Гулевская А.В.и др. Практикум по органической химии
Подождите немного. Документ загружается.


61
дут через горизонтальный вырез, а освещение вещества в капилляре
внутри блока – через второй горизонтальный вырез. Блок обогревают
электричеством или горелкой; передача тепла через металл теорети-
чески идеальна.
Если температура плавления вещества ниже 0 °С, ее также мож-
но определить в капилляре, но вместо описанного выше нагреватель-
ного блока применяют охлаждающий блок или стакан с подходящей
жидкой охлаждающей смесью (использование блока дает более точ-
ные результаты).
Поскольку термометр не полностью погружен в обогреваемое
пространство приборов, изображенных на рис. 34 и 35, рекоменду-
ется вносить поправку в его показания. Если Т
пл
набл.
– наблюдаемая
температура плавления, истинную температуру Т
пл
ист.
рассчитывают
по формуле
Т
пл
ист.
= Т
пл
набл.
+ 0.000154n (Т
пл
набл.
– Т
средн.
),
где Т
средн.
– средняя температура выступающего столбика; 0.000154 –
разница в коэффициентах расширения стекла и ртути; n – число де-
лений (в градусах) шкалы выступающего из жидкости ртутного стол-
бика.
Слежение за процессом плавления под микроскопом (при увели-
чении до 100 раз) позволяет отчетливо наблюдать отщепление воды
от гидратов, полиморфные переходы, возгонку и разложение веще-
ства. Для этих целей сконструирован столик Кофлера для микроско-
па, обогреваемый с нужной скоростью электричеством. Введения по-
правок на выступающий столбик здесь уже не требуется.
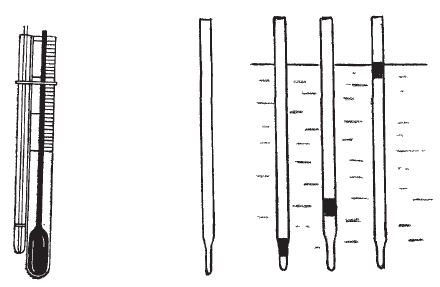
В последние годы введены в практику приборы с автоматиче-
ской и полуавтоматической регистрацией температуры плавления
(рис. 36). Они достаточно точны и позволяют экономить время иссле-
дователя, хотя и отличаются дороговизной. Их описание можно найти
в каталогах известных фирм, выпускающих химикалии, химическую
посуду и мелкое лабораторное оборудование.
Рис. 36. Образцы современных электронных приборов для определения
температуры плавления.

62
2.9.2. Температура кипения
Температура кипения вещества сильно зависит от давления*, и
ее точное определение весьма затруднительно.
В большинстве случаев за температуру кипения принимается
температурный интервал при перегонке вещества. При этом могут
возникнуть искажения, связанные с перегревом паров и недостатками
прибора, например, неправильным положением термометра. Кроме
того, источниками ошибок являются неточные поправки показаний
термометра или неверное измерение давления (например, при оши-
бочных показаниях манометра вакуумной установки). Неудивительно,
что в литературе для одного и того же вещества нередко приводятся
разные значения температуры кипения.
Влияние загрязнений на температуру кипения зависит от харак-
тера примесей. В целом, незначительные примеси оказываются для
температуры кипения гораздо менее существенными, чем для темпе-
ратуры плавления. В то же время, небольшие количества легколету-
чего растворителя могут существенно исказить температуру кипения.
В общем, можно сделать вывод, что температура кипения не являет-
ся таким же строгим критерием чистоты вещества, как температура
плавления.
Температуру кипения можно определять как в паровой, так и в
жидкой фазе. Определение температуры кипения в парах дает более
точные результаты, так как температура пара мало зависит от коле-
баний температуры внутри жидкости, неизбежных при ее нагревании.
Точную температуру кипения определяют эбулиометрами.
Принцип их действия основан на поддержании равновесия между ки-
пящей жидкостью, паром и конденсатом вблизи шарика термометра.
Для этого жидкость нагревают до кипения в приборе с обратным холо-
дильником и измеряют температуру. При соответствующей конструк-
ции прибора исключаются тепловые потери и перегрев паров. Однако
для работы в таких приборах необходимы большие количества веще-
ства (обычно не менее 50 мл).
Поэтому при наличии нескольких миллилитров жидкости проще
снять в приборе для перегонки кривую кипения (раздел 2.5, рис.19).
При этом надо обратить внимание на то, чтобы шарик термометра
полностью омывался парами, был смочен конденсатом и не был по-
гружен слишком глубоко в перегретый пар.
При работе с очень малыми количествами жидкости используют
методы Сиволобова и Эмиха. Согласно методу Сиволобова в широ-
кий капилляр длиной 2.5–3 см и диаметром 3 мм, заплавленный с
одного конца, помещают несколько капель перегнанной жидкости. В
этот же капилляр опускают другой, значительно более тонкий (длина
* Зависимость температуры кипения от давления описывается уравнением
Клаузиуса-Клапейрона: dlnP / dT = ∆
V
H / RT
2
, где Р – давление паров, ∆
V
H –
молекулярная энтальпия испарения, T – температура, R – газовая постоян-
ная.
63
30–35 мм), запаянный на расстоянии 1 см от нижнего края (поверх-
ность жидкости, температуру кипения которой надо определить долж-
на быть выше точки заплавления). Капилляр с помощью резиново-
го кольца прикрепляют к термометру (рис. 37) и нагревают в бане с
подходящим теплоносителем. При медленном нагревании прибора
из внутреннего капилляра начинают медленно выделяться пузырьки
воздуха. Когда выделение пузырьков становится быстрым, жидкость
считается закипевшей. Тогда нагревание прекращают и дают прибору
медленно остывать. Отмечают температуру, при которой выделение
пузырьков внезапно прекратится и жидкость начинает засасываться в
капилляр. Эта температура и является температурой кипения.
Рис. 37. Определение
температуры кипения
по Сиволобову
Рис. 38. Определение температуры
кипения по Эмиху
По методу Эмиха температуру кипения определяют в капилляре
для определения температуры плавления (рис. 38). Предварительно
оттягивают капилляр с одного конца (рис. 38, а), длина вытянутой ча-
сти около 2 см. Затем засасывают туда капельку исследуемой жидко-
сти и заплавляют конец капилляра таким образом, чтобы в конце его
под жидкостью находился пузырек воздуха (рис. 38, б). При нагрева-
нии в приборе для определения температуры плавления этот пузырек
расширяется (рис. 38, в) и поднимает каплю исследуемой жидкости.
При достижении температуры кипения эта капля достигает уровня
жидкости в нагревательной бане (рис. 38, г).
Для обоих методов точность определения температуры кипения
составляет примерно ±1–2 °С.
2.9.3. Определение плотности
Плотность жидкостей обычно выражают в граммах на миллилитр
d
4
t
= М/V. В простейших случаях, например, для серной и азотной кис-

64
лоты различных концентраций, плотность может быть приблизитель-
но определена с помощью ареометра. Однако для этого требуется
довольно много жидкости. Если жидкости мало и нужна повышенная
точность, для определения плотности используют небольшие пикно-
метры (рис. 39, а, б).
Предварительно пикнометр промывают ацетоном, эфиром и вы-
сушивают. Затем чистый и сухой пикнометр взвешивают на аналити-
ческих весах пустым (обозначим его вес М
п
) и наполняют дегазиро-
ванной дистиллированной водой. После термостатирования при 20
о
С
(не менее 10 мин) уровень воды в шейке пикнометра доводят до метки
по нижнему обрезу мениска (рис. 39, а), отбирая лишнюю воду с помо-
щью капилляра. Верхнюю часть шейки со шлифом протирают сухим
кусочком фильтровальной бумаги. Пикнометр закрывают пробкой, вы-
нимают из термостата, тщательно вытирают снаружи и взвешивают
через 5–10 мин на аналитических весах, получая массу пикномера с
водой М
п + Н
2
О
, а отсюда и массу воды в нем при 20 °С: М
Н
2
О
= = М
п + Н
2
О
– М
п
. Используя далее плотность воды при 4
о
С, которая равна
d
4
20
(H
2
O) = 0.99823, определяют объема пикнометра при 4
о
С (V
п
):
V
п
=
М
Н
2
О
d
4
20
(H
2
O)
=
М
п + Н
2
О
– М
п
0,99823
.
Рис. 39. Пикнометры
для определения плотности:
а – Рейшауера;
б – с капиллярной пробкойа б
Затем тот же сухой и чистый пикнометр наполняют исследуемым
веществом Х. Соблюдая все описанные выше приемы, взвешивают
вещество в объеме пикнометра (V
п
) и рассчитывают его плотность d
4
20
(Х) (символом «X» обозначено исследуемое вещество):
d
4
20
(X) =
М
п + X
– М
п
V
п
.
При постоянной работе с одним и тем же пикнометром измеряе-
мой величиной является только М
п+х
, величины М
п
и М
п+Н
2
О
определя-
ются лишь однажды.
65
Наряду с обычными пикнометрами Рейшауера (рис. 39, а) приме-
няются пикнометры с капиллярными пробками (рис. 39, б). Последние
имеют два преимущества: 1) узкий капилляр позволяет точнее опре-
делять объем и 2) через широкое горло легче заполнять пикнометр,
особенно вязкими жидкостями.
Точность описанного метода определения плотности с проверен-
ными пикнометром и термометром составляет ± 0.0005 г/мл.
2.9.4. Рефрактометрия
Для идентификации жидких веществ и проверки их чистоты мож-
но использовать также показатель преломления n.
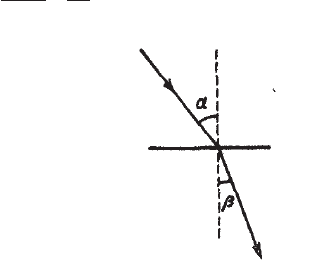
При переходе луча монохроматического света из одной среды в
другую изменяются его скорость и направление (рис. 40, α ≠ 0), при
этом отклонение луча определяется законом Снеллиуса:
n =
sin
α
sin
β
=
c
1
c
2
,
где с
1
и с
2
– скорость света в
первой и второй средах соот-
ветственно,
α
и β – угол паде-
ния и преломления луча света
соответственно при переходе
из первой среды во вторую.
Показателем преломления вол-
ны определенной длины назы-
вается постоянное отношение
sin α / sin β = n.
Показатель преломления
сильно зависит от температуры
и резко меняется с изменени-
ем длины волны света. Обычно
величина n дается для спек-
тральной линии желтого натриевого пламени (D-линия, 589.3 нм).
Температуру и длину волны отмечают индексами, например, n
D
20
.
Показатели преломления определяют рефрактометрами. В орга-
нических лабораториях наиболее часто применяются рефрактометры
системы Аббе, например РЛУ. Они измеряют предельный угол пол-
ного внутреннего отражения и сконструированы так, что при полих-
роматическом (например, дневном) освещении отмечают показатель
преломления для D-линии. Для измерения нужны лишь несколько
капель жидкости, точность измерения ± 0.0001. Обычно повышение
температуры на 1 °С уменьшает показатель преломления. С помо-
щью термостата можно поддерживать во время измерения постоян-
ную температуру с точностью до ± 0.2 °С.
Среда1
Среда2
Рис. 40. Преломление света
на границе двух сред

66
Показатель преломления зависит от концентрации раствора, поэ-
тому рефрактометрию используют также для определения концентра-
ции растворов, для проверки чистоты вещества и контроля процессов
разделения, например при ректификации смеси.
Для определения показателя преломления на рефрактометре
РЛУ поступают следующим образом (рис. 41). Открывают нижнее
полушарие 1 измерительной головки. Маховичком 2 поворачивают
измерительную головку так, чтобы плоскость нижнего полушария 1
приняла горизонтальное положение. На призму наносят пипеткой ка-
плю исследуемого вещества. Следует оберегать призму от царапин,
так как она сделана из очень мягкого свинцового стекла. Осторожно
закрывают нижнее полушарие измерительной головки. Быстро испа-
ряющиеся жидкости вводят в закрытую головку через специальный
боковой паз. Осветительное зеркало 3 устанавливают так, чтобы свет
от источника поступал к осветительной призме и равномерно осве-
щал поле зрения. Вращая маховичок 2 и, наблюдая в окуляр зритель-
ной трубы 4, находят границу раздела света и тени (рис. 42, а). Если
граница света и тени размыта и окрашена в желто-красный или сине-
зеленый цвет, надо маховичком 5, вращая его в любом направлении,
добиться по возможности более полного обесцвечивания границы и
четкого перехода от света к тени. Через окуляр 6 отсчитывают вели-
чину показателя преломления. Например, в случае, изображенном на
рис. 42, б, величина n
D
20
равна 1.4663.
Рис. 41. Рефрактометр РЛУ

67
а б
Рис. 42. Поле зрения (а) и шкала (б) рефрактометра
Для определения показателя преломления при заданной темпе-
ратуре измерительная головка снабжена термометром 7 и патрубками
для подключения термостата 8. После измерения тщательно протира-
ют верхнюю и нижнюю призмы сухой ватой, потом ватой с ацетоном,
эфиром и снова сухой ватой.
Современные цифровые рефрактометры (рис. 43) позволяют
проводить измерения показателя преломления в автоматическом ре-
жиме с разрешением до 0.00001 n
D
и точностью до 0.00002 n
D
.
Рис. 43. Автоматический рефрактометр фирмы KRÜSS

68
Контрольные вопросы
1. Перечислите явления, сопровождающие плавление органиче-
ского вещества.
2. Как определить температуру плавления веществ, плавящихся
вблизи точки разложения?
3. Можно ли определять концентрацию водных растворов уксус-
ной кислоты с помощью ареометра, рефрактометра, прибора для из-
мерения температуры плавления? При ответе используйте табличные
данные: СН
3
СООН Т
пл
16.6 °С n
D
20
1.3695
Н
2
О Т
пл
0.0 °С n
D
20
1.3330
Содержание
СН
3
СООН, вес. %
50
60
70
80
85
90
100
Плотность,
d
4
20
, г/мл
1.058
1.064
1.069 1.070 1.069 1.066 1.0498
4. Оцените важность для идентификации органического соеди-
нения следующих показателей: Т
пл
, Т
кип
(760 мм рт. ст.), Т
кип
(3–5 мм
рт. ст.), d
4
20
, n
D
20
. Также оцените примерное время, требующееся для
определения каждого из них.
2.10. Тонкослойная и колоночная хроматография
Хроматография – важнейший метод разделения и очистки ве-
ществ. Она основана на их неодинаковой адсорбции на специальных
твердых носителях – адсорбентах. Адсорбенты разделяют на два
главных типа:
а) гидрофобные и неполярные адсорбенты, лучше всего погло-
щающие растворенное вещество из полярных растворителей, осо-
бенно из водных растворов. Типичный пример такого адсорбента –
активированный уголь;
б) гидрофильные и полярные адсорбенты, которые предпочти-
тельны при работе с неполярными и малополярными растворителя-
ми. К этой группе относятся, силикагель, оксид алюминия, целлюлоза
и некоторые другие.
Особое значение имеют полярные адсорбенты. Их сродство к
адсорбируемому веществу (адсорбату) возрастает с ростом его по-
лярности. Особенно прочно адсорбируется вода; склонность актив-
ной поверхности адсорбента к адсорбции других, менее полярных
веществ уменьшается по мере того, как большая часть поверхности
покрывается молекулами воды. Для оксида алюминия – одного из
наиболее распространенных адсорбентов – специальными опытами
с красителями установлено пять различных степеней активности, за-
висящих от содержания воды (определение активности по Брокману
см. ниже).
69
Адсорбционная хроматография основана на различии в адсорб-
ционных свойствах компонентов разделяемой смеси. На поверхности
адсорбента имеются активные участки, способные фиксировать мо-
лекулы других веществ. При хроматографировании происходит не-
прерывный обменный процесс сорбции и десорбции растворенного
вещества на сорбенте. Когда число частиц, адсорбирующихся на по-
верхности в единицу времени, становится равным числу частиц, по-
кидающих поверхность (скорость сорбции равна скорости десорбции),
наступает состояние адсорбционного равновесия. В нем каждой кон-
центрации адсорбируемого вещества отвечает определенное количе-
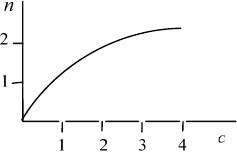
ство его на адсорбенте. Зависимость количества адсорбированного
вещества от его концентрации с в момент равновесия при постоянной
температуре выражается изотермой адсорбции Фрейндлиха и
Лэнгмюра (рис. 43), которая описывается уравнением n = ac
b
, где n –
количество вещества, адсорбиро-
ванного единицей поверхности, a и
b – величины, постоянные для дан-
ной системы (адсорбент – адсор-
бат). Из формы кривой изотермы
адсорбции следует, что увеличение
концентрации раствора выше опре-
деленного уровня не вызывает уве-
личения количества адсорбирован-
ного вещества. Поэтому наиболь-
шая эффективность метода дости-
гается при пропускании через сор-
бент разбавленных растворов.
Чем лучше адсорбируется ве-
щество, тем круче адсорбционная кривая и тем меньше скорость про-
движения вещества по адсорбенту. Поэтому отдельные компоненты
смеси движутся через адсорбент с различной скоростью. Чем хуже
адсорбируется вещество, тем быстрее оно продвигается по колонке
или пластинке в процессе хроматографирования.
Главное требование, предъявляемое к адсорбенту для хрома-
тографии – его химическая инертность к адсорбатам. Второе тре-
бование – его избирательность, т. е. возможно большее различие в
адсорбируемости веществ разделяемой смеси. Немалое значение
имеет степень дисперсности адсорбента. Наконец, чрезвычайно важ-
на стандартизация адсорбента, от чего зависит воспроизводимость
опытов и возможность сопоставления их результатов. В настоящее
время при хроматографических работах применяются почти исключи-
тельно хорошо стандартизированные коммерческие адсорбенты.
При выборе адсорбента в первую очередь нужно исходить из
свойств разделяемых соединений: их растворимости (гидрофиль-
ность – гидрофобность), типа имеющихся в них функциональных
групп. Насыщенные углеводороды адсорбируются слабо или совсем
не сорбируются. Введение двойных связей, особенно сопряженных,
Рис. 43. Изотерма адсорбции

70
увеличивает адсорбцию соединений. Полярные функциональные
группы еще в большей степени усиливают способность вещества к
адсорбции. Адсорбционная способность функциональных групп уве-
личивается в следующем порядке:
-CН=СН- < -ОСН
3
< -СООR < С=О < -СНО < -SH < -NH
2
< -OH < -COOH.
При наличии в молекуле нескольких заместителей, характер их
совместного влияния, естественно, усложняется.
Правильный выбор растворителя (элюента) в адсорбционной
хроматографии имеет существенное значение и тесно связан как с
природой выбранного адсорбента, так и со свойствами компонентов
анализируемой смеси. В связи с этим представляет интерес элюотроп-
ный ряд Траппе (табл. 3), в котором наиболее часто применяемые в
хроматографии растворители расположены в порядке убывания де-
сорбирующей способности с полярных сорбентов. Десорбирующая
способность растворителей, хотя и не строго, но зависит от их диэ-
лектрической постоянной. Для неполярных адсорбентов десорбирую-
щая способность приведенных в таблице растворителей изменяется
в обратном порядке.
Таблица 3
Элюотропный ряд растворителей
Растворитель
Диэлектриче-
ская постоян-
ная
Растворитель
Диэлектриче-
ская постоян-
ная
Вода 78.0 Диоксан 8.9
Метанол 31.2 Хлороформ 5.2
Этанол 25.8 Хлористый метилен 2.2
н-Пропанол 22.8 Бензол 2.3
Ацетон 21.5 Толуол 2.3
Дихлорэтан 10.4 Трихлорэтилен 3.4
Этилацетат 6.1
Четыреххлористый
этилен
2.2
Амилацетат 5.1 Циклогексан 2.0
Этиловый эфир 4.4
Петролейный эфир
(фракция 35–50 °С)
1.9
Из всего многообразия хроматографических методов в синтети-
ческой органической химии чаще всего применяют тонкослойную и
колоночную хроматографию, при этом первый метод обычно исполь-
зуют в аналитических, а второй – в препаративных целях.
2.10.1. Тонкослойная хроматография
Тонкослойная хроматография (ТСХ) – эффективный метод ана-
лиза сложных смесей веществ самых различных классов. Ее преиму-
