Лунин Л.С., Благин А.В., Баранник А.А. Лекции по физике. Часть I. Механика, молекулярная физика и термодинамика
Подождите немного. Документ загружается.


101
Вискозиметр Оствальда-Пинкевича (В.Ф. Оствальд (1853–1932),
А.П. Пинкевич (1883–1939)
) представляет собой U-образную стеклянную
трубку (рис. 8.10) с двумя расширениями 1 и 2 и насосом 3, позволяющим
перегнать жидкость из одного расширения в другое. Для двух жидкостей
используются два идентичных вискозиметра. Так как путь l, проходимый
жидкостями между расширениями одинаков, то, зная время (t и t
0
) ис-
течения одинакового объема
(V=Qt=V
0
=Q
0
t
0
) жидкостей, из формулы (8.14) можно определить вязкость
исследуемой жидкости:
0
0
)14.8(
00
ρ
η
η
ρ
⋅=
tQ
Qt
,
откуда
t
t
⋅
⋅
=
ρ
ρ
ηη
00
0
(8.15)
или
t
t
0
0
ξξ
=
, (8.15')
при данной температуре Т. Зависимость
ξ
=ƒ(T) (
η
=ƒ(T)) является нелинейной.
Если шарик падает в жидкости, простирающейся безгранично по
всем направлениям, не оставляя за собой никаких завихрений, то на него
действует сила внутреннего трения, равная
по закону (1851г.) Д.Г. Стокса
(1819–1903):
rv
F
πη
6
=
, (8.16)
где
r – радиус шарика;
ν
– его скорость.
Если шарик свободно падает в вязкой жидкости, то на него будут
действовать сила тяжести
mg=
ρ
Ш
Vg и выталкивающая сила (Архимеда)
F
A
=
ρ
Ж
Vg, равная весу вытесненной жидкости (V – объем шарика,
ρ
Ш
–
плотность шарика,
ρ
Ж
– плотность жидкости). На основании второго зако-
на Ньютона с учетом соотношения (8.16) получают выражение
rvVgVg
Ш
t
v
m
Ж
πηρρ
6−−=
∂
∂
. (8.17)

102
Сила сопротивления с увеличением скорости движения шарика воз-
растает, а ускорение уменьшается и, наконец, шарик достигает такой ско-
рости, при которой ускорение становится равным нулю и тогда уравнение
(8.17) принимает вид
06)(
4
3
3
=−− rvgr
ЖШ
πηρρπ
, (8.18)
где вместо объема подставили
3
4
3
rV
π
=
. В этом случае шарик движется
с постоянной скоростью
ν
0
. Такое движение шарика называется устано-
вившимся. Решая уравнение (8.18) относительно коэффициента внутренне-
го трения, получают
0
2
9
)(2
v
gr
ЖШ
ρρ
η
−
=
. (8.19)
Скорость шарика
ν
0
можно определить, зная расстояние l, пройденное
шариком, и время t, за которое шарик проходит это расстояние:
ν
0
=l/t. То-
гда из выражений (8.17) и (8.19) следует, что коэффициент вязкости равен
l
gtr
ЖШ
9
)(2
2
ρρ
η
−
=
. (8.20)
Практически невозможно осуществить падение шарика в безграничной
среде, т.к. всегда жидкость находится в каком-то сосуде, имеющем стенки и
дно. Поэтому в формуле (8.20) вводится поправочный коэффициент
R
r
K
4,21
1
+
=
,
где R – радиус цилиндрического сосуда.
Тогда формула (8.20) принимает вид
)4,21(9
)(2
2
R
r
l
gtr
ЖШ
+
−
=
ρρ
η
. (8.21)
103
8.5. Поверхностное натяжение в жидкостях.
Капиллярные явления
(обзор (осн. понятия), более полно см. раздел физики «Молекулярная физика и
термодинамика»)
На частицу (молекулу) жидкости действуют силы притяжения со сто-
роны окружающих частиц. Если частица находится внутри жидкости и уда-
лена от ее поверхности на расстояние больше радиуса сферы взаимодействия
частиц, то эти силы в среднем уравновешиваются.
Если же частица нахо-
дится в приграничном слое малой, сравнимой с радиусом действия час-
тиц, толщины (например, в капле), то появляется результирующая сила,
направленная внутрь жидкости.
Поэтому для извлечения молекулы из
внутренних слоев на поверхность требуется совершить работу.
Работа, ко-
торую надо затратить, чтобы изотермически и квазистатически увели-
чить поверхность жидкости на единицу при сохранении объема неизмен-
ным,
называется поверхностным натяжением жидкости. По-другому,
поверхностное натяжение можно охарактеризовать как свободную поверхно-
стную энергию жидкости, приходящуюся на единицу поверхности.
Жидкости характеризуются различными значениями поверхностного
натяжения, поэтому в случае раствора, содержащего несколько компонен-
тов, состав поверхностного слоя будет отличаться от состава раствора в
его «объемной» части.
Любая система в неравновесном состоянии стремится перейти в
равновесное состояние, характеризуемое минимумом свободной энергии.
Для жидкости, не ограниченной стенками сосуда, формой с наименьшей
поверхностью
(и, следовательно, энергией) является шар. Получению
шаровой (в невесомости) формы капли мешает сила тяжести. Потенциальная
энергия в поле сил тяготения пропорциональна объему, а энергия поверхно-
стного натяжения – площади поверхности капли. Чем больше объем, тем
сильнее влияние силы тяжести, малые же капли практически шарообразны.
На поверхности капли, как правило, имеют полусферическую форму, при-
чем, чем больше капля растекается по поверхности твердого тела, образуя
тонкую пленку, тем о лучшей
смачиваемости поверхности данного тела
(вещества) этой жидкостью говорят. Смачиваемостью поверхности сосуда
жидкостью определяется форма ее поверхности (в случае несмачиваемости
можно налить в стакан воду с горкой, не перелив воду через край стакана).
104
Капиллярами называют трубки малого внутреннего диаметра, что
обусловливает яркое проявление действия сил поверхностного натяжения,
например, в искажении формы поверхности жидкости в капилляре (она
будет либо сферически – выпуклой для несмачиваемых поверхностей, ли-
бо сферически – вогнутой – для смачиваемых). В состоянии равновесия
при искривлении формы поверхности на концах капилляра давления будут
разными, т.е. будет появляться дополнительная разность давлений на кон-
цах, обусловленная поверхностным натяжением.
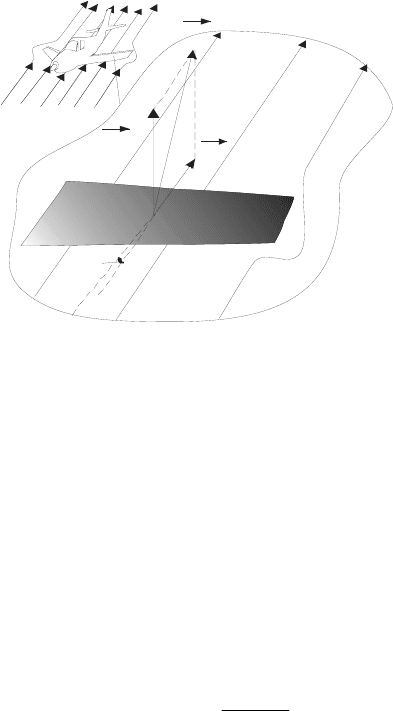
8.6. Движение тел в жидкостях и газах
На тело, движущееся в жидкости или газе
действует сила R,
являющаяся равнодействующей двух сил (рис. 8.10):
ЛС
R
r
(сила лобо-
вого сопротивления,
направленная против движения тела в сторону
потока) и
ПС
R
r
(подъемная сила, направленная перпендикулярно дви-
жению). При движении в идеальной жидкости R
лс
=0.
α
R
лс
R
пс
R
Рис. 8.11
Если тело симметрично, то R
пс
=0, а если несимметрично и не имеет
обтекаемой формы (плавно утончающейся хвостовой части), то погранич-
ный слой вязкой среды «постоянно отрывается» от поверхности тела.
За телом образуется течение, направленное в противоположную на-
бегающему потоку сторону (вихри, вращаются в противоположную сторо-
ну). Лобовое сопротивление зависит от формы и расположения тела отно-
сительно потока:
S
v
лс
C
лс
R
2
2
⋅
=
ρ
, (8.22)

105
где С
лс
– экспериментально определяемый безразмерный коэффициент
сопротивления;
S – наибольшее поперечное сечение тела.
Лобовое сопротивление можно значительно уменьшить подбором
обтекаемой формы, не способствующей завихрению.
Подъемная сила определяется аналогичным образом:
S
v
пс
C
пс
R
2
2
⋅
=
ρ
, (8.23)
где С
пс
– безразмерный коэффициент подъемной силы.
Характеристикой крыла является
качество крыла: K=C
пс
/С
лс
. Для
крыла самолета (подводного крыла) требуется большая подъемная сила
при малом лобовом сопротивлении, это условие хорошо выполняется при
малых углах атаки
α
(угол к встречному потоку).
МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
ЛЕКЦИЯ 9. ОСНОВЫ МОЛЕКУЛЯРНОЙ ФИЗИКИ I
1. Основные понятия молекулярно-кинетической теории (МКТ)
и термодинамики.
2. Газовые законы. Уравнение (Менделеева–Клапейрона) со-
стояния идеального газа (ИГ).
3. Основное уравнение МКТ.
4. Распределение Дж.К.Максвелла молекул по скоростям и энергиям.
5. Барометрическая формула (распределение Больцмана).
9.1. Основные понятия молекулярно-кинетической теории
(МКТ) и термодинамики
Механика имеет дело с отдельными телами (обычно описывает дви-
жение не более трех тел). Молекулярная физика изучает системы, состоя-
щие из огромного числа N∼(N
A
=6,02⋅10
23
моль
-1
) непрерывно хаотически
движущихся частиц.
Исследовать процессы в таких системах с помощью законов механи-
ки практически невозможно. Однако молекулярная физика и термодина-
мика выработали свои особые методы изучения таких систем. Существует
два общих подхода (метода):

106
- статистический – основывается на квантовой теории строения ве-
щества и использует новые – статистические – закономерности, прояв-
ляющиеся только в коллективном поведении частиц системы; оперирует
характеристиками отдельных частиц (скорость, энергия), используя их ус-
реднение (наиболее вероятные значения) для описания всей системы;
- термодинамический (ТД) – изучает общие свойства макросистем
(не вдаваясь в строение, происходящее внутри), находящихся в состоянии
термодинамического равновесия; устанавливает соотношения между мак-
ропараметрами: обычно Р (давлением), V (объемом) и T (температурой)
системы на основе обобщения большого числа опытных данных. Поэтому
термодинамику часто называют феноменологической (от греч. «являю-
щееся») теорией.
Оба подхода тесно связаны и хорошо дополняют, а в ряде случаев
дублируют друг друга.
Дадим ряд определений.
Термодинамической системой (ТДС) называют мысленно выделен-
ную совокупность тел (макросистему), которая рассматривается на основе
ТД подхода.
Открытая ТДС – ТДС, обменивающаяся с окружающей средой
веществом и энергией, закрытая – только энергией. Напротив, изолирован-
ная ТДС
(или замкнутая ТДС) – ТДС, не способная к обмену веществом и
энергией с окружающей средой (идеальный случай, т.к. энергия может излу-
чаться и поглощаться без соприкосновения изолированных тел, для замкну-
той имеется ввиду неспособность обмениваться энергией через совершение
механической работы).
Адиабатная ТДС – замкнутая ТДС, не способная к
обмену энергией с окружающей средой посредством теплообмена (реальные
теплоизолированные системы с малым рассеянием теплоты).
ТД параметры делятся: на интенсивные, не зависящие от количе-
ства вещества в ТДС (P, T), и
экстенсивные, зависящие и пропорциональ-
ные ему (V); на
внешние, зависящие от положения и свойств внешних по
отношению к ТДС тел (например, стенок сосуда – V), и
внутренние, зави-
сящие еще и от координат и скоростей частиц самой системы (Р, энергия).
В 1866г. австрийский физик Л.Больцман (1844–1906), будучи сту-
дентом, доказал, что величиной, характеризующей состояние ТДС незави-
симо от ее микроскопической структуры, может быть средняя кинетиче-
ская энергия поступательного движения одной молекулы:
kT
2
3
=
ε
, (9.1)
где k – постоянная Больцмана, k=1,38⋅10
-23
Дж/К; Т – термодинамическая
температура (по шкале Кельвина (англ.
У. Томсон (1824–1907), за научные
заслуги
лорд Кельвин)) – мера кинетической энергии (теплового движе-
ния) частиц вещества. В настоящее время в международной практике, на-
ряду с термодинамической шкалой, принято использовать международную
107
практическую шкалу Цельсия (швед. A. Celsius (1701–1744))
Т=[t(°C)+273,15°]К. Считается, что при T=0 K – «нуль кельвин» – пре-
кращается всякое движение. Такая температура
не достижима, хотя воз-
можно
сколь угодно близкое приближение к ней.
ТД равновесием называется состояние системы, характеризующееся
при постоянных внешних условиях неизменностью параметров (P,V,T) и
отсутствием потоков вещества и энергии в системе.
Равновесное состояние системы характеризуется следующими
свойствами:
1) оно не зависит от предыстории системы (от предшествующих со-
стояний);
2) переход системы в равновесное состояние необратим;
3) в равновесном состоянии реализуется определенное стационарное
(не зависящее от времени) распределение молекул по скоростям.
ТД процессом называется любое изменение состояния системы, связан-
ное с изменением хотя бы одного термодинамического параметра.
ТД процесс
называется
равновесным, если изменение состояния ТДС происходит при
t→∞ (время), т.е. каждое предыдущее состояние характеризуется мало отли-
чающимися от последующего ТД параметрами (P,V,T).
Реальные процессы
имеют конечную скорость (время) протекания и не являются равновесными,
но
могут быть приближенными к ним – квазиравновесными.
Модель идеального газа (ИГ) основывается на трех допущениях:
– собственный объем молекул пренебрежимо мал по сравнению с
объемом сосуда;
– силы взаимодействия между молекулами отсутствуют;
– столкновение молекул друг с другом и со стенками сосуда в про-
цессе хаотического теплового движения носит упругий характер.
Модель ИГ с успехом применяется для описания реальных газов при
нормальных условиях (н.у.): P
0
=101325 Па=760 мм.рт.ст., Т
0
=273,15 К, а
также при высоких температурах и низких давлениях. При иных условиях
от уравнения ИГ можно перейти к теории реальных газов, вводя в эти
уравнения поправки, учитывающие собственный объем молекул и силы
взаимодействия между ними.
9.2. Газовые законы. Уравнение (Менделеева–Клайперона)
состояния ИГ
Простейшие примеры ТД процессов –
изопроцессы (постоянной оста-
ется масса газа m=const и один из ТД параметров P, V или T). Они описывают-
ся экспериментально установленными законами:
а) изотермический (m=const, T=const) (рис.9.1, а) закон Бойля–Мариотта
(англ. Р. Бойль (1627–1691), фр. Э. Мариотт (1620–1684)):
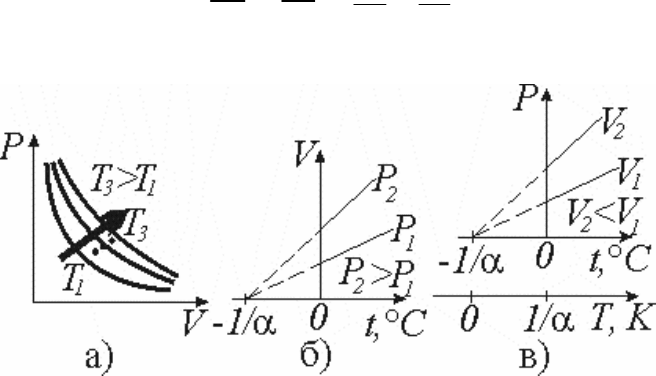
108
PV=const; (9.2)
б) изобарный (m=const, P=const) (рис. 9.1, б) закон Ж.Л. Гей-Люссака
(1778–1850):
V=V
0
(1+
α⋅
t). (9.3)
При н.у. (Р
0
и Т
0
)
α
=1/273,15 K
-1
;
в) изохорный (m=const, V=const) (рис. 9.1, в) закон Ж.Л. Гей-Люссака
(1778–1850):
P=P
0
(1+
α⋅
t). (9.4)
Выражая время t через температуру T законы Гей-Люссака можно перепи-
сать в виде:
2
1
2
1
T
T
V
V
=
и
2
1
2
1
T
T
P
P
=
. (9.5)
Рис. 9.1
Закон А. Авогадро
(1776–1856): 1 моль любых газов при одинако-
вых температуре и давлении занимают одинаковый объем.
При н.у. молярный объем V
m
=22,41⋅10
-3
м
3
(22,41 литра), а число час-
тиц в одном моле любого газа N
A
=6,02⋅10
23
моль
-1
.
Закон Дж. Дальтона (1766–1844): давление смеси газов равно сумме
парциальных давлений газов, входящих в эту смесь:
∑
=
=
n
i
i
PP
1
.
Парциальное давление – то, которое производил бы газ, входящий
в состав смеси, если бы занимал сам весь объем, занимаемый смесью.
Уравнением состояния или термическим уравнением состояния
называется функция f(P,V,T)=0, связывающая все макропараметры систе-
мы (ИГ). Получают его, следуя Б.П.Э. Клайперону (1799–1864) и Д.И.
Менделееву (1834–1907 гг.).
Изменение состояния ИГ в результате двух изопроцессов (сначала
изотермического, а затем изохорного), изображено на рис. 9.2.

109
Соответственно получают: P
1
V
1
=P'
1
V
2
и
2
1
2
/
1
T
T
P
P
=
. Исключая из
уравнений величину P'
1
, получают уравнение Клапейрона:
constB
T
VP
T
VP
===
2
22
1
11
. (9.6)
P
V
P
P
P
1
1
/
2
V
1
V
2
P
1
V
1
T
1
,
,
P
1
VT
1
,
,
P
VT
,
,
/
2
2
2
2
Рис. 9.2
Так как все состояния ИГ были выбраны произвольно, то уравнение
(9.6) выполняется в любом ТД процессе для данной массы m ИГ (значение
постоянной В зависит от природы газа).
Менделеев объединил уравнение Клапейрона с законом Авогадро. Так
как при данных давлении и температуре газы занимают одинаковый объем,
для одного моля газа можно записать:
RTPV
m
=
, (9.7)
где R– универсальная газовая постоянная, не зависящая от природы
ИГ R=
k⋅N
A
=8,31 Дж/(моль⋅К).
Чтобы перейти к произвольной массе газа, заметим, что объем, кото-
рый занимают v молей газа в v раз больше молярного объема V
m
, т.е.
V=
ν
V
m
(по пропорции
Vm
VM
m
(М – масса одного моля (молярная масса)
газа) с учетом
ν
=m/M получают то же V=
ν
V
m
). Тогда
vRTvPV
m
=
(9.8)
или
RT
M
m
PV =
. (9.8')

110
Иногда уравнение (9.8) записывают в виде
nkT
V
TkN
P
m
A
==
, (9.9)
где n – концентрация частиц вещества (атомов, молекул).
9.3. Основное уравнение МКТ
В рамках модели ИГ получим основное уравнение МКТ, связываю-
щее давление газа с механическими характеристиками молекул – скоро-
стью и энергией.
v
∆t
∆S
Рис. 9.3
Пусть одноатомный ИГ находится в сосуде; выделим малую площадь на
стенках сосуда. Импульс, передаваемый площади ∆S одной молекулой при
каждом соударении, равен (см. лекция 3, Теория удара):
∆p
0
=m
0
v
1
–(–
m
0
v
1
)=2m
0
v
1
, где v
1
– нормальная составляющая скорости молекулы.
За время ∆
t с площадкой ∆S столкнутся молекулы, заключенные в
объеме ∆V=∆S
ν
∆t. Далее непрерывное хаотическое движение молекул для
упрощения расчетов заменяют на равновероятное движение молекул вдоль
трех взаимно перпендикулярных направлений, считая, что вдоль каждого
направления движется одна треть всех молекул со скоростью
v. За время
∆
t из тех молекул, что движутся перпендикулярно площади ∆S (рис. 9.3),
столкнутся с ней половина (всего 1/6). Число молекул, которые соударя-
ются с ∆S равно
tSvnnVN ∆∆==
6
1
6
1
.
Суммарный импульс, передаваемый площади ∆S, равен
tSnvmNvmNpp ∆∆=⋅=∆=∆
2
000
3
1
2
.
Тогда давление газа определяют по формуле
2
0
3
1
nvm
S
t
p
S
F
P =
∆
∆
∆
=
∆
=
. (9.10)
