Кондратьев В.Н., Никитин Е.Е. Кинетика и механизм газофазных реакций
Подождите немного. Документ загружается.


диффузией факте, что в ряде случаев вычисляемая из скорости распро-
странения пламени энергия активации оказывается меньше энергии ак-
тивации реакции медленного горения. На основании этих данных Вольф-
гард и Гейдон приходят к заключению, что в случае быстрых реакций
горения либо нужно отказаться от применения закона Аррениуса, либо
под входящей в этот закон энергией активации понимать величину,
имеющую иной смысл, чем тот, какой она имеет в медленных реакциях
16
.
Основания для такого заключения нам представляются, однако, весьма
шаткими и вопрос в целом недостаточно изученным для того, чтобы были
возможны столь далеко идущие выводы. Фактическое положение дела
скорее отвечает обратной картине, так как проверка на опыте основываю-
щихся на законе Аррениуса теоретических выводов, относящихся к
распространению пламен, говорит о достаточно строгом выполнении
этого закона.
Пределы распространения пламени
Как мы видели, при изменении состава горючей смеси изменяется и
скорость распространения пламени. При некотором оптимальном составе
смеси скорость горения имеет максимальное значение и уменьшается
как в сторону бедной, так и в сторону богатой смеси. Начиная с некоторого
предельного состава, пламя не распространяется; иными словами, в
таких смесях и
0
= 0. Этот предельный состав, выражаемый содержанием
горючего в смеси или соответствующей величиной а, характеризует
концентрационные пределы распространения пламени. Опыт показыва-
ет, что при переходе за концентрационный предел распространение пла-
мени прекращается при некотором конечном значении и
0
.
Существование пределов распространения пламени естественно свя-
зать с явлением пределов воспламенения, перенося представления о вос-
пламенении газа в статических условиях на воспламенение свежей смеси
в условиях распространяющегося фронта горения. Из этого, однако,
не следует, что температура (Т
в
) и давление воспламенения (р
в
) смеси
данного состава в условиях пламени и в статических условиях будут
одними и теми же. Дело здесь заключается в том, что если в обоих случаях
условие воспламенения можно выразить равенством скорости разветвления
и скорости обрыва цепей (справедливом также и в случае теплового вос-
пламенения) [1656], то время приближения смеси к состоянию, отвечаю-
щему этому условию, вообще говоря, будет в каждом случае иным. При-
чиной этого может быть, например, различие теплопередачи при проте-
кании реакции в статических условиях и в условиях пламени. В резуль-
тате состояние смеси в момент воспламенения, характеризующееся
величинами Т
в
и р
в
, в обоих случаях будет различным, т. е. различными
будут соответственно Т
в
и р
в
.
Из определения условия воспламенения как равенства скоростей
разветвления и обрыва цепей следует, что все факторы, влияющие на про-
текание этих процессов, будут в той или иной степени влиять на Т
в
и р
в
. Не останавливаясь на анализе различных факторов, отметим, толь-
ко, что тепловой фактор (тепловые потери), по-видимому, играет здесь
доминирующую роль (см. например, [116, 117, 1215, 1349, 1524, 1568,
1569]).
16
С этой точки зрения Гейдон и Вольфгард [827] считают большим шагом вперед раз-
работанную Бехертом [459] формально-математическую теорию распространения
пламени, в которой энергия активации фигурирует как некоторый параметр, значе-
ние которого выбирается таким, чтобы вычисляемая при его помощи скорость пламе-
ни была ближе к измеренной величине.

Одна из первых теорий пределов распространения пламени, в основе
которой лежит представление о доминирующей роли тепловых потерь,
принадлежит Зельдовичу [116, 117], который показал, что потери тепла
приводят к уменьшению скорости пламени. На основании тепловой
теории распространения пламени Зельдовича и Франк-Каменецкого
.(см. выше) Зельдович получает равенство (см. также [365, стр. 312—316])
= ехр (50.21)
где £ =
(UQ/UQ)
2
(и
0
— скорость пламени в отсутствие тепловых потерь,
2%Ф Е 1
и'о— при наличии потерь) и а = , — (и — коэффициент темпе-
С/рро til pi
р
MQ
ратуропроводности, равный
% —
УС
р
р
0
, Я — средний коэффициент тепло-
проводности, Ф — потери тепла за 1 сек путем теплоотдачи во внешнее
пространство, отнесенные к 1 см
3
зоны горения, С
р
— теплоемкость,
Ро — плотность исходной смеси при темцературе Т
0
, Е — энергия
активации лимитирующего процесса, Т
т
— максимальная ^температура
пламени в отсутствие тепловых потерь и Т
т
— при наличии потерь).
Нетрудно показать, что предыдущее равенство ^имеет вещественное
решение только при определенных значениях параметра а, а именно
при значениях, разных или меньших некоторого критического значения
Якрит
==
^
е
• При этом критическом значении получается единственное
действительное решение £ = е, из которого следует
И
0
= Щ/ V7. (50.22)
Это значение величины щ представляет собой минимальное значение
скорости пламени, отвечающее пределам распространения. Таким образом,
в соответствии с опытом минимальное значение величины щ отлично от
нуля.
Зельдовичем также было показано [117, 122], что при определенных
условиях главную роль» играют потери тепла посредством излучения.
Линнетт и Симпсон [1161] (см. также [1172]) находят, что существен-
ное влияние на пределы распространения пламени оказывает конвекция.
О пределах распространения пламени далее см. [223, глава 5, § 12].
Вблизи пределов распространения пламени наблюдаются явления,
свидетельствующие о неустойчивости процесса горения, прогрессирую-
щей по мере приближения к пределам. Эти явления, выражающиеся в
зависимости концентрационных пределов распространения пламени в
вертикальных трубах от направления распространения (сверху вниз
пламена распространяются в более узких пределах концентрации, чем
снизу вверх, т. е. труднее [1666]), в искажениях или в неустойчивости
сплошного плоского фронта пламени [162], наиболее резко выражены
в смесях газов, сильно различающихся по молекулярному весу. Количест-
венное рассмотрение вопроса о неустойчивости пламен вблизи пределов
распространения принадлежит Лейзеру [1135]. См. также [1524].
§ 51. ДЕТОНАЦИЯ
В заключение этой главы кратко рассмотрим детонационное распро-
странение пламени в газовых смесях. Явление детонации газов, открытое
в 1881 г. Малларом и Ле-Шателье [1195] и независимо от них Вертело
[483], имеет огромное практическое значение. Поскольку одно из прояв-
лений детонации связано с ее разрушительным действием, то вполне
естественно, что именно катастрофические взрывы пылевоздушных смесей
в угольных шахтах послужили тем стимулом, который возбудил интерес

к явлениям распространения пламени и привел к открытию детонации
и в дальнейшем к ее всестороннему изучению. К той же категории явле-
ний относится детонация газовых и пылевидных смесей в условиях раз-
личных производств, как и детонация в двигателе внутреннего сгорания,
приводящая к быстрому износу и разрушению двигателя. Не входя, в
рассмотрение явления детонации с точки зрения практики, здесь коснемся
только тех его сторон, которые в той или иной мере связаны с химией
и кинетикой процессов горения.
Детонация возникает под действием ударных волн, в частности, в ре-
зультате самоускорения пламени (при распространении горения в трубах).
Вследствие самоускорения пламени возникает волна сжатия (ударная
волна), в которой благодаря высоким температуре и давлению происхо-
дит самовоспламенение смеси [118, 119., 123, 390].
Таким образом, возникающая при детонации ударная волна сопровож-
дается волной горения; обе волны, в совокупности образующие детона-
ционную волну, распространяются в газе с некоторой скоростью (скорость
детонации), которая значительно превосходит нормальную скорость пла-
мени и обычно составляет 2—5 км/сек.
В основе теории детонации, развитой Чепменом [626], Михельсоном
1239] и Жуге [1029] (см. также 460]), лежит гидродинамическая теория
ударных волн в химически инертном газе, ранее разработанная Риманом
(I860 г.), Ренкином (1870 г.) и Гюгоньо (1887, 1889 гг.). Исходя из гидро-
динамического уравнения непрерывности газового потока (закон сохра-
нения массы),
WoPo
= мр (51.1)
или
Uolvo
= u/v
9
где и — скорость; р — плотность и v — удельный объем газа (v = 1/р,
индекс «0» относится к холодному газу, находящемуся при начальной тем-
пературе Т
0
), и закона сохранения количества движения
и
1 и
2
— + = — +
Р
(51.2)
{р — давление), путем простых преобразований находим (здесь и и и
0
—
••скорости газа в системе координат, движущейся вместе с ударной
волной):
щ
/
р —
Ро
тт
1 Г р
— Ро
И
и = v
I/
г?
0
— г?
у
vo —
v
Определяя скорость ударной волны кдк скорость движения фронта
волны по отношению к холодному газу и отмечая штрихом величины, отно-
сящиеся к газу во фронте волны, для скорости распространения ударных
волн будем иметь:
Соответственно скорость горячего газа относительно холодного
w = — Y(p' — p,)(vo — v'). (51.4)
(.Р' -
ро)
=
Ар
(vo —
v') Ay
Заметим, что при р' — р
0
<<
р
0
и v
0
— v' << v
0
, когда \
р
_
~ '
ВВИД
У адиабатичности процесса при бесконечно малых измене-
ниях р и», получим —Ap/Av = yp/v (у = C
p
/C
v
) и, следовательно,
D=Yvpv7 (51.5)

Последняя формула представляет собой известную формулу Лапласа
для скорости звука. Таким образом, при малых изменениях р и v скорость
распространения ударных волн должна быть близкой к скорости звука.
Состояние газа в ударной волне, наряду с уравнениями (51.1) и (51.2),
определяется также законом сохранения энергии
E
0
+ ^- +
Pi
i
v
0
= E-{-^
r
+ pv, (51.6)
где Е — внутренняя энергия единицы массы газа. Уравнение (51.6) при
помощи (51.1) и (51.2) может быть преобразовано к виду:
E
— Eo
=
l
U(p +
po)(v
0
—
v)
y
(51.7)
или, вследствие
Т'
J
C
v
dT = a
v
(T'-T
0
),
То
к виду:
e
v
(Т* - То) - 1/а сР' + ро) (vo - v'). (51.8)
Уравнение (51.7), носящее название адиабаты Гюгонъо, при мало раз-
личающихся р и р
0
и соответственно v и v
0
в пределе переходит в уравне-
ние адиабаты Пуассона
dE =
—
pdv,
которая отвечает изоэнтропическому процессу.
Следовательно, условия в ударной волне, вообще говоря, отличаются от
изоэнтропических, причем в тем большей степени, чем больше различают-
ся между собой давления и удельные объемы холодного и нагретого газа.
Причина неизоэнтропичности процессов, протекающих в ударной вол-
не,— это их необратимость, обусловленная конечной скоростью измене-
ния состояния газа. Одним из следствий неизоэнтропичности является то,
что газ в ударной волне нагревается значительно сильнее, чем при изо-
энтропическом сжатии до того же давления. Непосредственная причина
дополнительного разогрева заключается в быстром сжатии газа потоком
отходящих горячих газов.
При наличии химической реакции, идущей в волне горения, сопровож-
дающей ударную волну, внутренняя энергия газа кроме энергии сжатия
включает в себя также химическую энергию, выделяющуюся в резуль-
тате реакции. Обозначив энергию, выделяющуюся при превращении 1 г
вещества, через L, в этом случае вместо уравнений (51.7) и (51.8) будем
иметь:
т
Е -
Ео
= jj C
v
dT = 1/2
(Р
+
ро) (vo
-v) + L. (51.9)
То
Поскольку получающаяся из общих законов сохранения формула
(51.3) для скорости ударной волны содержит только величины, характери-
зующие начальное и конечное состояние газа и не использует уравнения
сохранения энергии (51.7) или (51.9), эта формула, очевидно, сохранится
и в том случае, когда ударная волна сопровождается распространяющей-
ся с той же скоростью волной горения. Другими словами, формула, вы-
ражающая скорость детонационной волны, должна быть аналогична фор-
муле (51.3). Различие обеих формул состоит лишь в том, что в ударной
волне конечное состояние газа, определяется величинами р' и г?', отве-
чающими входящей в уравнение (51.8) температуре ТВ детонационной
же волне конечное состояние газа, являющееся состоянием продуктов
горения, определяется величинами
р
т
и у
г
, отвечающими максимальной тем-
пературе детонационной волны (температуре детонации) Т
7
, получающейся
из уравнения (51.9). Таким образом, скорость детонации определяется
посредством уравнения:
D
Рг-Ро
Vo — V
v
(51.10)
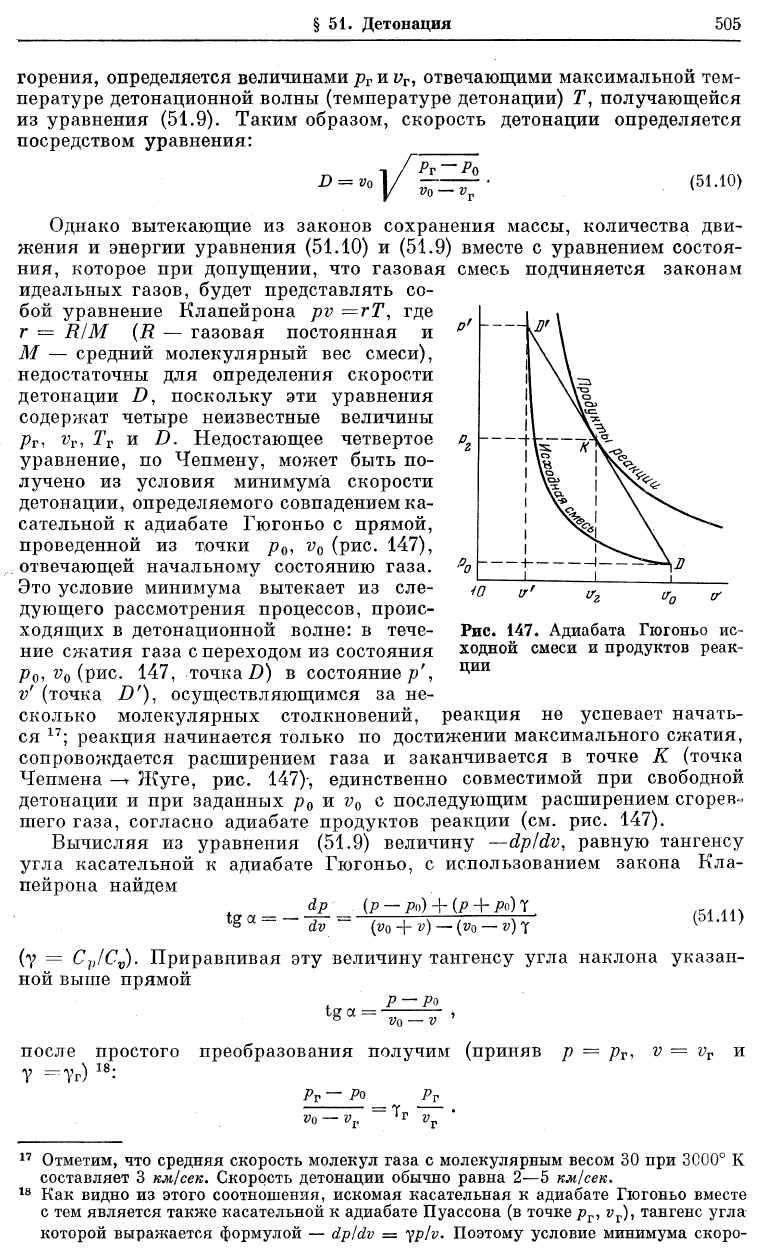
Однако вытекающие из законов сохранения массы, количества дви-
жения и энергии уравнения (51.10) и (51.9) вместе с уравнением состоя-
ния, которое при допущении, что газовая смесь подчиняется законам
идеальных газов, будет представлять со-
бой уравнение Клапейрона pv =гТ, где
г = R/M (R — газовая постоянная и
М — средний молекулярный вес смеси),
недостаточны для определения скорости
детонации Z), поскольку эти уравнения
содержат четыре неизвестные величины
Рт, v
r
, T
v
и D. Недостающее четвертое
уравнение, по Чепмену, может быть по-
лучено из условия минимума скорости
детонации, определяемого совпадением ка-
сательной к адиабате Гюгоньо с прямой,
проведенной из точки /?
0
, v
0
(рис. 147),
отвечающей начальному состоянию газа.
Это условие минимума вытекает из сле-
дующего рассмотрения процессов, проис-
ходящих в детонационной волне: в тече-
ние сжатия газа с переходом из состояния
р
0
, v
0
(рис. 147, точка/)) в состояние //,
v' (точка £)'), осуществляющимся за не-
сколько молекулярных столкновений, реакция не успевает начать-
ся
17
; реакция начинается только по достижении максимального сжатия,
сопровождается расширением газа и заканчивается в точке К (точка
Чепмена
—*
Жуге, рис. 147), единственно совместимой при свободной
детонации и при заданных р
0
и ?;
0
с последующим расширением сгорев-
шего газа, согласно адиабате продуктов реакции (см. рис. 147).
Вычисляя из уравнения (51.9) величину —dpldv, равную тангенсу
угла касательной к адиабате Гюгоньо, с использованием закона Кла-
пейрона найдем
dp
(Р — ро)
+
{р
+
ро) Т ,
,
п
(у = C
p
/C
v
). Приравнивая эту величину тангенсу угла наклона указан-
ной выше прямой
Р — Ро
tg а = ,
6
VQ —
v
1
после простого преобразования получим (приняв р
У =Чг)
18
:
Рис. 147. Адиабата Гюгоньо ис-
ходной смеси и продуктов реак-
ции
р
г
, v — v
T
Ро
Vq — V
= Т
Г «
17
Отметим, что средняя скорость молекул газа с молекулярным весом 30 при 3000° К
составляет 3 км/сек. Скорость детонации обычно равна 2—5 км/сек.
18
Как видно из этого соотношения, искомая касательная к адиабате Гюгоньо вместе
с тем является также касательной к адиабате Пуассона (в точке г;
г
), тангенс угла
которой выражается формулой — dpldv = yplv. Поэтому условие минимума скоро-

Вводя степень сжатия е = vjv
v
и исключая величины р
г
и при по-
мощи равенств p
r
v
r
= г
г
Т
г
и p
0
v
0
= r
0
T
0
(г
г
= R!M
V
, r
0
= R/M
0
) из
уравнений (51.9) — (51.11), преобразуем эти уравнения к виду:
'Д. = в/т
г
г
Р
Г
р
, (51.12)
т
. J = (51.13)
Го
и
Т
г
8
2
- (Т
Р
+
1) е
+• гоГо/г
г
Г
р
= 0. (51.14)
Из этих трех уравнений и могут быть вычислены три неизвестные величи-
ны: D, е и Т
т
. Заметим, что вследствие зависимости величины C
V
!C
V
от
температуры у
г
— у
т
{Т
т
), эти вычисления не сводятся к простому реше-
нию системы трех алгебраических уравнений, а проводятся по методу
последовательных приближений. Вычисления усложняются также необ-
ходимостью учета диссоциации продуктов горения, особенно существен-
ной при высоких температурах.
Изложенная классическая теория детонации была создана Зель-
довичем [115, 117, 123] в 1940 г. (см. также фон Нейман [1287], Деринг
1713], Гриб [76]) на основе одномерной модели устойчивой детонационной
волны. Позднейшие исследования показали (литературу см. в обзоре Стре-
лова [1554], см. также [49]), что действительная газокинетическая и хи-
мико-кинетическая картина детонационной волны гораздо сложнее той
идеализированной картины плоской ударной волны и плоского фронта
химической реакции, которая следует из классической теории и которая
к тому же оказывается неустойчивой, что приводит к изломам и искривле-
нию волнового фронта и связанным с этим нарушениям идеальной кар-
тины детонационных волн.
Было установлено также, что структура детонационной волны сущест-
венным образом влияет на скорость детонации, что существуют так назы-
ваемые сильная и слабая детонации, распространяющиеся со скоростями,
отличными от скорости классических детонационных волн Ченмена —
Жуге, что имеет место взаимосвязь между интенсивностью иниции-
рующей ударной волны и кинетикой химической реакции и т. д.
Все эти особенности детонационных волн не были известны класси-
ческой теории. Поэтому последняя не в состоянии описать все многообра-
зие реально существующих детонационных волн. Пути построения более
совершенной теории детонации в настоящее время только ещз наме-
чаются [1554]. Однако во многих случаях классическая детонационная волна
Чепмена — Жуге оказывается в достаточной мере адекватной наблю-
даемым фактам, что имеет место при оперировании средними величинами
(благодаря чему остается правильной теория скорости детонации и ряд
других положений классической теории).
Это, в частности, можно иллюстрировать сопоставлением вычислен-
ных на основании классической теории и измеренных значений скорости
детонации в смесях Н
2
— 0
2
— N
2
, приведенных в табл. 35. В этой табли-
це, кроме скоростей детонации приводятся значения максимальных дав-
лений и температур (р
г
и Т
г
) в детонационной волне, вычисленные (как
и скорости детонации) [1150] по экспериментальным данным [702, 1341],
а также содержание гидроксила и атомарного водорода в сгоревшем
газе, отвечающее равновесиям Н
2
0 ^ V
2
Н
2
+ ОН и Н
2
^ 2Н.
сти детонации иногда формулируется как условие касания указанной выше прямой
и адиабаты Пуассона или как условие касания адиабаты Пуассона и адиабаты Гюго-
ньо.
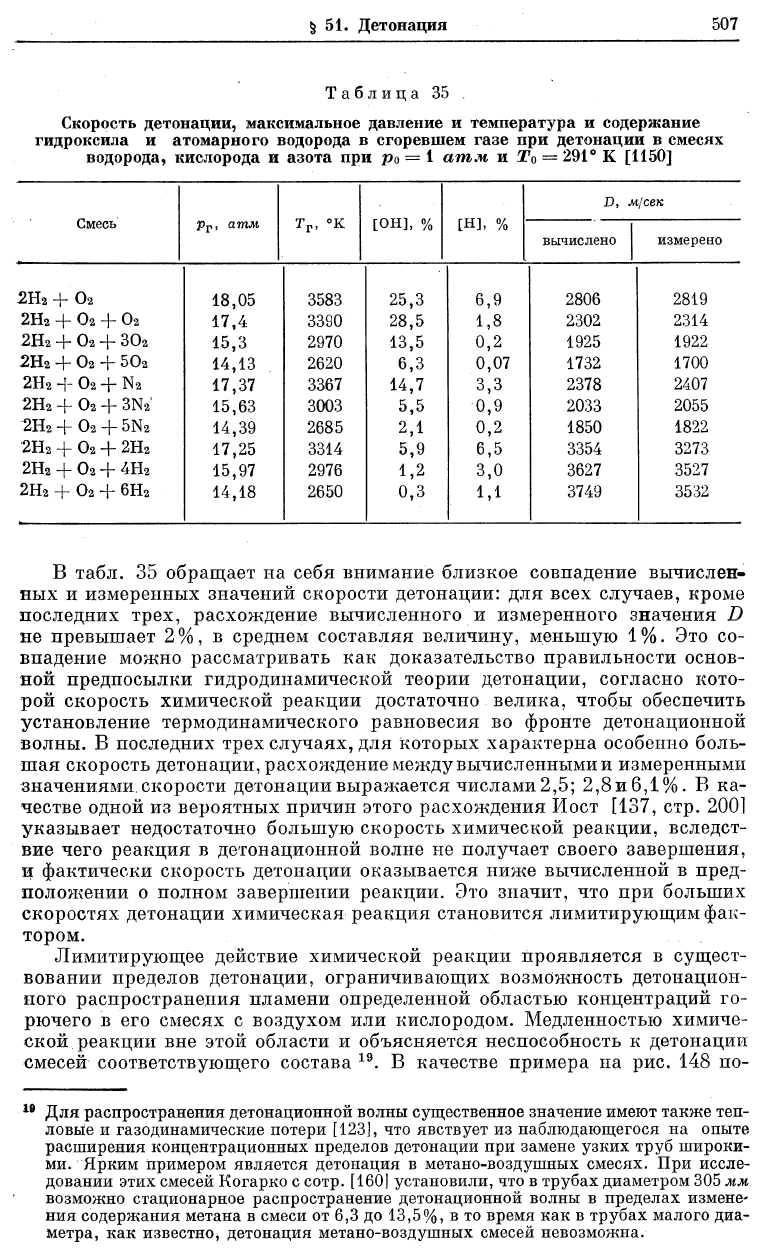
Таблица 35
Скорость детонации, максимальное давление и температура и содержание
гидроксила и атомарного водорода в сгоревшем газе при детонации в смесях
водорода, кислорода и азота при ро = 1 ашм и Т
0
= 291° К [1150]
D, м/сек
Смесь
р
г
, атм
т
г
, °к
[ОН], о/о
[H], % '
вычислено измерено
ЗН
2
+ 0
2
18,05
3583
25,3 6,9
2806 2819
2Н
2
+ 0
2
+ 0
2
17,4
3390 28,5
1,8
2302 2314
2Н
2
+ 0
2
+ 30
2
15,3
2970 13,5
0,2
1925
1922
2Н
2
+ 0
2
+ 50
2
14,13
2620
6,3
0,07
1732
1700
2Н
2
+ 0
2
+ N
2
17,37
3367
14,7
3,3
2378
2407
2Н
2
+ 0
2
+ 3N
2
15,63
3003 5,5 0,9
2033
2055
2Н
2
+ 0
2
+ 5N
2
14,39
2685
2Д
0,2 1850
1822
2Н
3
+ 0
2
+ 2Н
2
17,25
3314 5,9 6,5 3354
3273
2Н
2
+ 0
2
+ 4Н
2
15,97
2976
1,2
3,0 3627
3527
2На + 0а + 6На
14,18
2650
0,3
1,1
3749
3532
В табл. 35 обращает на себя внимание близкое совпадение вычислен-
ных и измеренных значений скорости детонации: для всех случаев, кроме
последних трех, расхождение вычисленного и измеренного значения D
не превышает 2%, в среднем составляя величину, меньшую 1%. Это со-
впадение можно рассматривать как доказательство правильности основ-
ной предпосылки гидродинамической теории детонации, согласно кото-
рой скорость химической реакции достаточно велика, чтобы обеспечить
установление термодинамического равновесия во фронте детонационной
волны. В последних трех случаях, для которых характерна особенно боль-
шая скорость детонации, расхождение между вычисленными и измеренными
значениями, скорости детонации выражается числами 2,5; 2,8и6,1%. В ка-
честве одной из вероятных причин этого расхождения Иост [137, стр. 200]
указывает недостаточно большую скорость химической реакции, вследст-
вие чего реакция в детонационной волне не получает своего завершения,
и фактически скорость детонации оказывается ниже вычисленной в пред-
положении о полном завершении реакции. Это значит, что при больших
скоростях детонации химическая реакция становится лимитирующим фак-
тором.
Лимитирующее действие химической реакции проявляется в сущест-
вовании пределов детонации, ограничивающих возможность детонацион-
ного распространения пламени определенной областью концентраций го-
рючего в его смесях с воздухом или кислородом. Медленностью химиче-
ской реакции вне этой области и объясняется неспособность к детонации
смесей соответствующего состава
19
. В качестве примера на рис. 148 по-
19
Для распространения детонационной волны существенное значение имеют также теп-
ловые и газодинамические потери [123], что явствует из наблюдающегося на опыте
расширения концентрационных пределов детонации при замене узких труб широки-
ми. Ярким примером является детонация в метано-воздушных смесях. При иссле-
довании этих смесей Когарко с сотр. [160] установили, что в трубах диаметром 305 мм
возможно стационарное распространение детонационной волны в пределах измене-
ния содержания метана в смеси от 6,3 до 13,5%, в то время как в трубах малого диа-
метра, как известно, детонация метано-воздушных смесей невозможна.
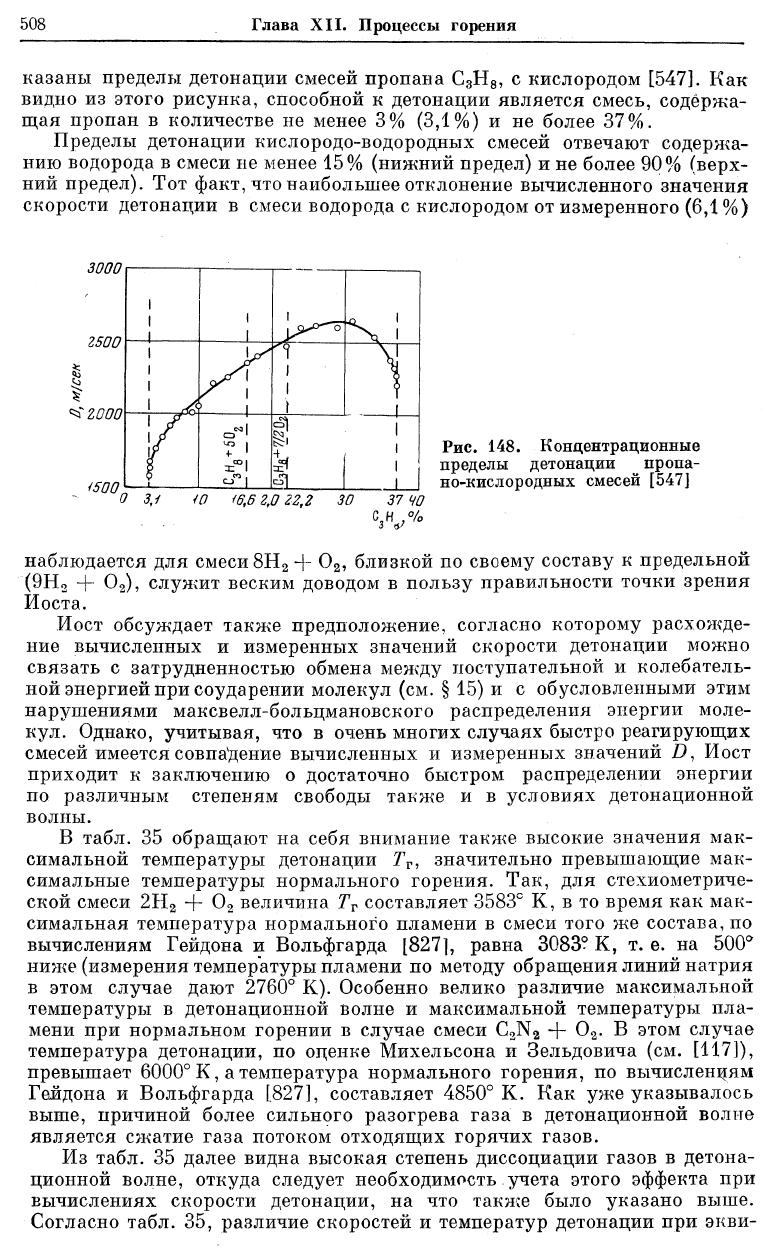
казаны пределы детонации смесей пропана С
3
Н
8
, с кислородом [547]. Как
видно из этого рисунка, способной к детонации является смесь, содержа-
щая пропан в количестве не менее 3% (3,1%) и не более 37%.
Пределы детонации кислородо-водородных смесей отвечают содержа-
нию водорода в смеси не менее 15% (нижний предел) и не более 90% (верх-
ний предел). Тот факт, что наибольшее отклонение вычисленного значения
скорости детонации в смеси водорода с кислородом от измеренного (6,1 %)
наблюдается для смеси 8Н
2
+ 0
2
, близкой по своему составу к предельной
(9Н
2
+ 0
2
), служит веским доводом в пользу правильности точки зрения
Поста.
Иост обсуждает также предположение, согласно которому расхожде-
ние вычисленных и измеренных значений скорости детонации можно
связать с затрудненностью обмена между поступательной и колебатель-
ной энергией при соударении молекул (см. § 15) и с обусловленными этим
нарушениями максвелл-больцмановского распределения энергии моле-
кул. Однако, учитывая, что в очень многих случаях быстро реагирующих
смесей имеется совпадение вычисленных и измеренных значений Z), Иост
приходит к заключению о достаточно быстром распределении энергии
по различным степеням свободы также и в условиях детонационной
волны.
В табл. 35 обращают на себя внимание также высокие значения мак-
симальной температуры детонации Г
г
, значительно превышающие мак-
симальные температуры нормального горения. Так, для стехиометриче-
ской смеси 2Н
2
+ 0
2
величина Т
т
составляет 3583° К, в то время как мак-
симальная температура нормального пламени в смеси того же состава, по
вычислениям Гейдона и Вольфгарда [827], равна 3083? К, т. е. на 500°
ниже (измерения температуры пламени по методу обращения линий натрия
в этом случае дают 2760° К). Особенно велико различие максимальной
температуры в детонационной волне и максимальной температуры пла-
мени при нормальном горении в случае смеси C
2
N
2
+ 0
2
. В этом случае
температура детонации, по оценке Михельсона и Зельдовича (см. [117]),
превышает 6000° К, а температура нормального горения, по вычислениям
Гелдона и Вольфгарда [827], составляет 4850° К. Как уже указывалось
выше, причиной более сильного разогрева газа в детонационной волне
является сжатие газа потоком отходящих горячих газов.
Из табл. 35 далее видна высокая степень диссоциации газов в детона-
ционной волне, откуда следует необходимость учета этого эффекта при
вычислениях скорости детонации, на что также было указано выше.
Согласно табл. 35, различие скоростей и температур детонации при экви-
валентной замене кислорода азотом должно быть обусловлено главным об-
разом различием в степени диссоциации смесей. Действительно, количест-
во молекул воды, дающих при диссоциации гидроксил, согласно схеме
Н
2
0 +
1
/
2
0
2
-^20Н, ИЗ которой следует р
0
я/рн
2
о — Рщо Vpo
t
, увеличи-
вается с возрастанием содержания кислорода в смеси, что и наблюдается
в действительности. Одновременное уменьшение содержания воды, даю-
щей при диссоциации атомарный водород, следует из отвечающей урав-
нению Н
2
0 ^ 2Н + V
2
0
2
зависимости рц/рн
я
о Ря
2
о/УРо
2
- В результа-
те дополнительного поглощения энергии, расходуемой на увеличение
диссоциации, температура детонации при избытке кислорода понижает-
ся, что и приводит к уменьшению скорости детонации.
Аналогичная картина наблюдается также в случае детонации смесей
C
2
N
2
, 0
2
и N
2
, где увеличение скорости и температуры детонации при за-
мене кислорода азотом объясняется происходящим при этом уменьшением
степени диссоциации кислорода. Так, при переходе от смеси G
2
N
2
+ 30
2
к смеси C
2
N
2
+ 0
2
+ 2N
2
, согласно вычислениям Зельдовича ]117],
скорость и температура детонации увеличиваются соответственно от 2135
до 2265 м/сек и от 4095 до 4395° К. Измеренные значения скорости дето-
нации равны: для первой смеси 2110 м/сек (Диксон), для второй смеси
2165 м!сек (Диксон) и 2230 м!сек (Кемпбелл) (см. [117]).
В связи с данными табл. 35 отметим также сравнительно высокие
значения максимального давления в детонационной войне. Однако не-
смотря на это, вследствие высокой температуры, степень сжатия газа в
детонационной волне невелика
20
и доставляет величину, близкую к 2.
Выше, при обсуждении приведенных в табл. 35 данных, следуя Иосту,
мы пришли к заключению о необходимости учета скорости химической реак-
ции в детонационной волне в случае смесей состава, близкого к предель-
ному, когда недостаточно большая скорость реакции горения становится
лимитирующим фактором. Указания на связь между скоростью детона-
ции и скоростью и механизмом химических реакций имеются также и в
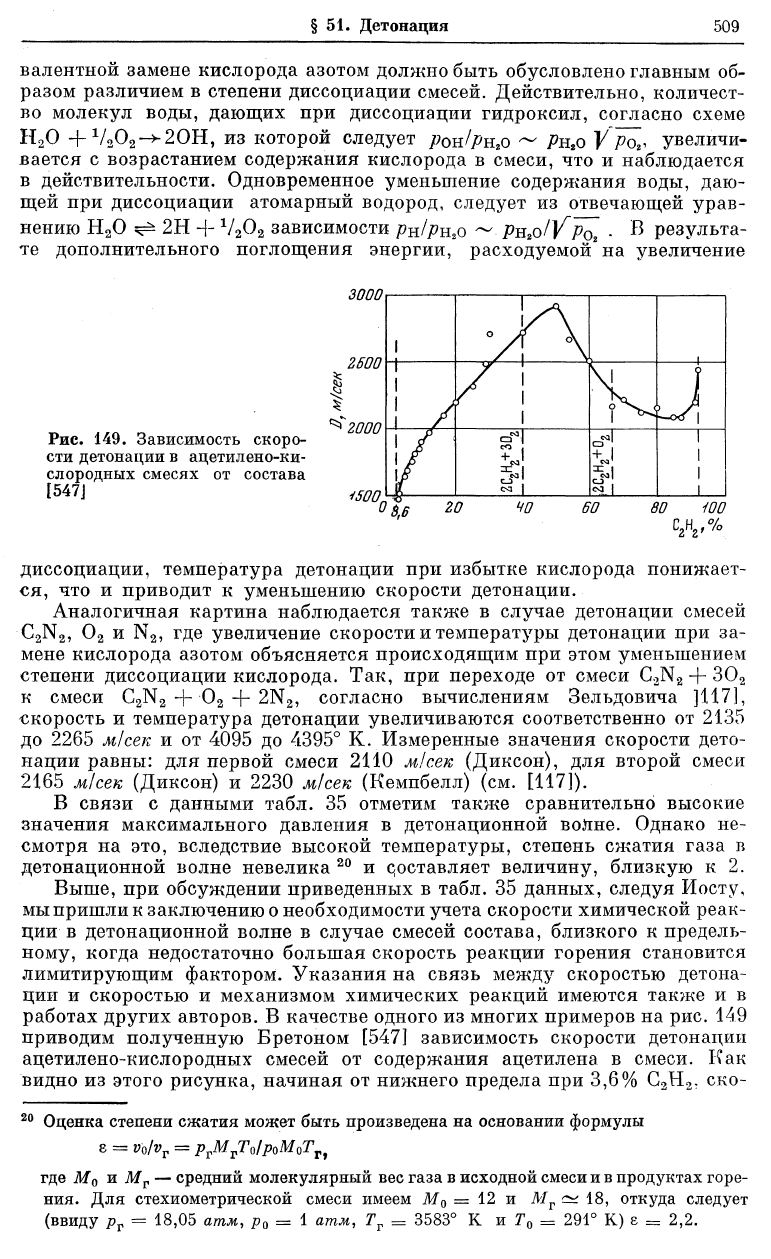
работах других авторов. В качестве одного из многих примеров на рис. 149
приводим полученную Бретоном [547] зависимость скорости детонации
ацетилено-кислородных смесей от содержания ацетилена в смеси. Как
видно из этого рисунка, начиная от нижнего предела при 3,6% С
2
Н
2
. ско-
20
Оценка степени сжатия может быть произведена на основании формулы
8
= v
0
/v
r
= р
г
М
т
Т
0
/р0М
0
Т
тf
где Мо и М
г
— средний молекулярный вес газа в исходной смеси и в продуктах горе-
ния. Для стехиометрической смеси имеем М
0
= 12 и М
г
~ 18, откуда следует
(ввиду p
v
= 18,05 атм, p
Q
= 1 атм, Т
Т
= 3583° К и Т
0
= 291° К) 8 = 2,2.

рость детонации растет, достигает максимума при 50%, после чего умень~
шается, с тем чтобы, пройдя через минимум около 85% С
2
Н
2
, дать резкое
возрастание вплоть до верхнего предела детонации, лежащего около 92—
93% С
2
Н
2
. Согласно Бретону и Лаффиту (см. Иост [137, стр. 210—211]),
такой необычный ход кривой пределов детонации обусловлен двумя раз-
личными химическими реакциями: реакцией горения ацетилена, преоб-
ладающей при малых концентрациях последнего, и реакцией взрывного^
крекинга ацетилена, являющейся основной реакцией при высоких кон-
центрациях С
2
Н
2
, стимулируемой его сгоранием.
Вопрос о взаимосвязи между детонацией и обусловливающей ее хими-
ческой реакцией наиболее четкую постановку впервые получил в работах
Зельдовича [117], который дал и наиболее удовлетворительное его решение
(см. также [713, 717, 960. 1287]). Зельдович прежде всего четко сформу-
лировал положение о прямой связи механизма детонационного распрост-
ранения пламени с реакцией горения. Отправным пунктом здесь служит
высказывавшееся различными авторами утверждение, что механизм рас-
пространения детонации заключается в передаче давления от слоя к
слою, приводящего к воспламенению газа. Зельдовичем совместно со
Шляпинтохом [129] было дано прямое экспериментальное доказательства
возможности воспламенения газа при сжатии его ударной волной (про-
изводимой в горючей смеси пулей, летящей со сверхзвуковой скоростью).
В непосредственной близости от фронта ударной волны происходит
воспламенение сжатого газа, и так как вследствие большой скорости
распространения ударной волны диффузия (как и теплопроводность)
не играет сколько-нибудь существенной роли
21
, то в реакцию вступает
смесь, не разбавленная продуктами реакции и не содержащая активных
центров, образовавшихся в соседних слоях газа в предшествующие мо-
менты времени. По этой причине воспламенение горючей смеси в ударной
волне должно ближе соответствовать самовоспламенению газа в статиче-
ских условиях, чем воспламенению при нормальном горении (где переда-
ча тепла теплопроводностью и диффузия активных центров играют
основную роль). Экспериментальным (качественным) доказательством пра-
вильности этих представлений являются данные по влиянию неболь-
ших концентраций активных примесей, полученные в работах Соколика
[322], Ривина и др. [38, 293]. Из этих работ, в частности, следует, что
активные примеси одинаково расширяют концентрационные пределы де-
тонации (не влияя, однако, на скорость детонации), так же как расширя-
ют пределы и ускоряют самовоспламенение тех лее смесей в статических
условиях.
Одним из наиболее убедительных экспериментальных доказательств
правильности представления о том, что поджигание горючей смеси удар-
ной волной представляет собой чисто тепловой эффект, является резуль-
тат опытов Штейнберга и Каскана [1539], измерявших температуру са-
мовоспламенения и температуру воспламенения в ударной волне смесей
водорода с кислородом и пропана С
3
Н
8
с воздухом. Так, для смеси 2Н
2
+
+ 0
2
они получили температуру самовоспламенения 760—740° К (при дав-
лении 5—7,5
атпм)
и температуру воспламенения в ударной волне 800° К.
Температура воспламенения этой смеси адиабатическим сжатием, по дан-
ным различных авторов, составляет 820—800° К.
В смеси, воспламенившейся в результате сжатия ударной волной, раз-
вивается химическая реакция горения, осуществляющаяся при постоян-
ной скорости распространения. Последнее обстоятельство приводит к вы-
текающему из уравнения (51.10) линейному закону изменения состоя-
21
См., однако, работу [655].
