Ильясов С.Г. Процессы и аппараты упаковочного производства
Подождите немного. Документ загружается.

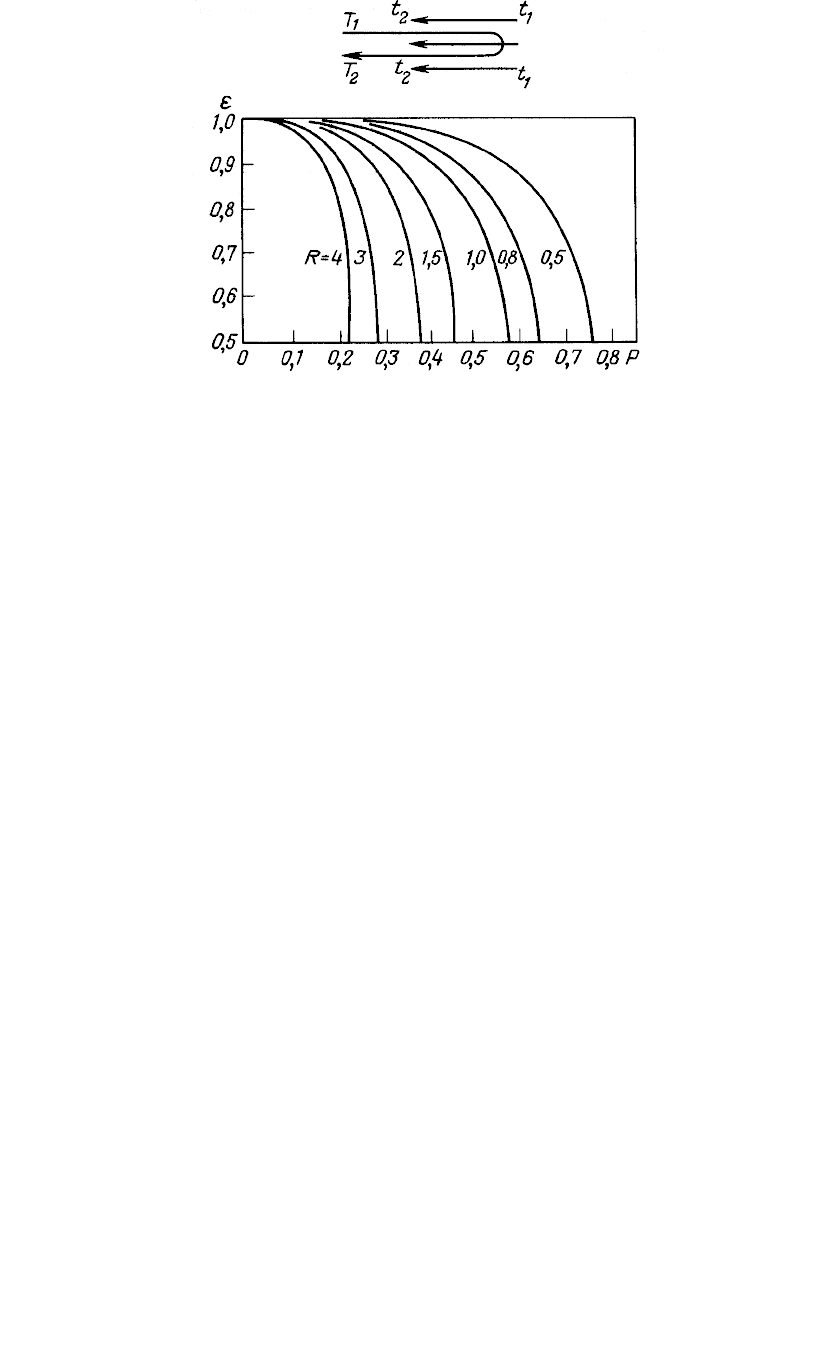
Рис. 11-18. К определению движущей силы процесса теплопередачи при смешанном токе
теплоносителей
При отношении
MБ
tt /
< 2 можно без большой ошибки движущую
силу определить
как среднеарифметическую, т.е.
).(5,0
MБcp
ttt
Для перекрестного и смешанного токов точный расчет величины
cp
t
затруднителен ввиду весьма сложных закономерностей изменения температур вдоль
поверхности теплообмена. Поэтому расчет движущей силы для этих случаев
проводят по упрощенной схеме, основываясь на относительно просто определяемой
величине
cp
t
для противотока и вводя соответствующую поправку
, т.
е.
..протсрcp
tt
Поправочный коэффициент
всегда меньше единицы и находится по
справочникам в зависимости от соотношения температур теплоносителей и
схемы их движения.
Для смешанного тока, например, определение величины
в зависимости
от Р = (t
2K
-t
2H
)/(t
1H
-t
2H
) и R = (t
1K
-t
1H
)/(t
2K
-t
2H
) приведено на рис. 11-18, из которого
следует, что с увеличением R и Р коэффициент
заметно снижается.
4.8.2. Теплопередача при нестационарном режиме

Нестационарный перенос теплоты, который происходит в теплообменных
аппаратах непрерывного действия при их пуске, остановке или изменении режима их
работы, обычно в тепловых расчетах не учитывают, поскольку такие периоды работы
непрерывно действующих теплообменников кратковременны. Вместе с тем в аппа-
ратах периодического действия (например, в регенеративных теплообменниках,
аппаратах с рубашкой и др.) нестационарный перенос теплоты является основным,
и расчет такого процесса нагревания или охлаждения через стенку имеет важное
практическое значение
Рис. 11-19. К выводу уравнений нестационарной теплопередачи
Примем, например, что горячая жидкость в количестве G
1
должна быть охлаждена водой в аппарате с мешалкой (рис. 11-19). Заданными
величинами являются также начальная t
1Н
и конечная t
1К
температуры охлаждаемой
жидкости, начальная температура t
2н
охлаждающей жидкости, поверхность
теплопередачи F. Полагаем, что коэффициент теплопередачи К в течение процесса
практически постоянен, плотности жидкостей в интервале изменения рабочих
температур и давлений остаются постоянными, в аппарате вследствие интенсивно
работающей мешалки создается режим идеального смешения (МИС). Поэтому
температура t
1
=f(
), но всех точках жидкости одинакова в каждый момент
времени
.
В некоторый произвольный момент времени
, когда температура
охлаждаемой жидкости равна t
1
разность температур теплоносителей (движущие
силы теплопередачи) на входе воды составляет
HБ
ttt
21
, а на выходе
M
t
=
t
1
- t
2K
. Поскольку температуры t
1
и t
2 к
изменяются во времени, то изменяется во
времени и средняя разность температур. Поэтому
)]/()ln[()/ln(
2121
22
кн
нк
мб
мб
ср
tttt
tt
tt
tt
t
(11.83)
Выражение (11.83), строго говоря, справедливо при условии пренебрежения
скоростью изменения энтальпии теплоносителя внутри змеевика по сравнению
со скоростью изменения энтальпии теплоносителя в объеме аппарата. Подставим
выражение (11.83) и уравнение теплопередачи
.
)/()(ln
2121
22
d
tttt
tt
KFdQ
KH
HK
(11.84)
По уравнению теплового баланса величину dQ можно выразить так:

dQ=G
2
c
2
(t
2k
- t
2H
)d
(11.85)
Из сопоставления уравнений (11.84) и (11.85) следует :
k
H
tt
tt
cG
KF
21
21
22
ln
, (11.86)
или
(11.87)
Для второго теплоносителя
22
11
1122
)()(
cG
cG
tttt
KHHK
При противотоке таким же образом получаем
.
)exp()/(1
)exp(1
)(
22
11
2211
1122
cG
cG
mKFcGcG
mKF
tttt
KHHK
(11.106)
Для первого теплоносителя
11
22
2211
)()(
cG
cG
tttt
HKKH
Выражения (11.104)-(11.106) позволяют провести сравнение эффективности
прямотока и противотока при одинаковых условиях.
Для прямотока
;
)/(1
)exp(1
)(
2211
2111
cGcG
mKF
ttcGQ
HHПМ
Для противотока
;
)exp()/(1
)exp(1
)(
2211
2111
mKFcGcG
mKF
ttcGQ
HHПТ
Ae
tt
tt
сG
KF
k
H
22
21
21
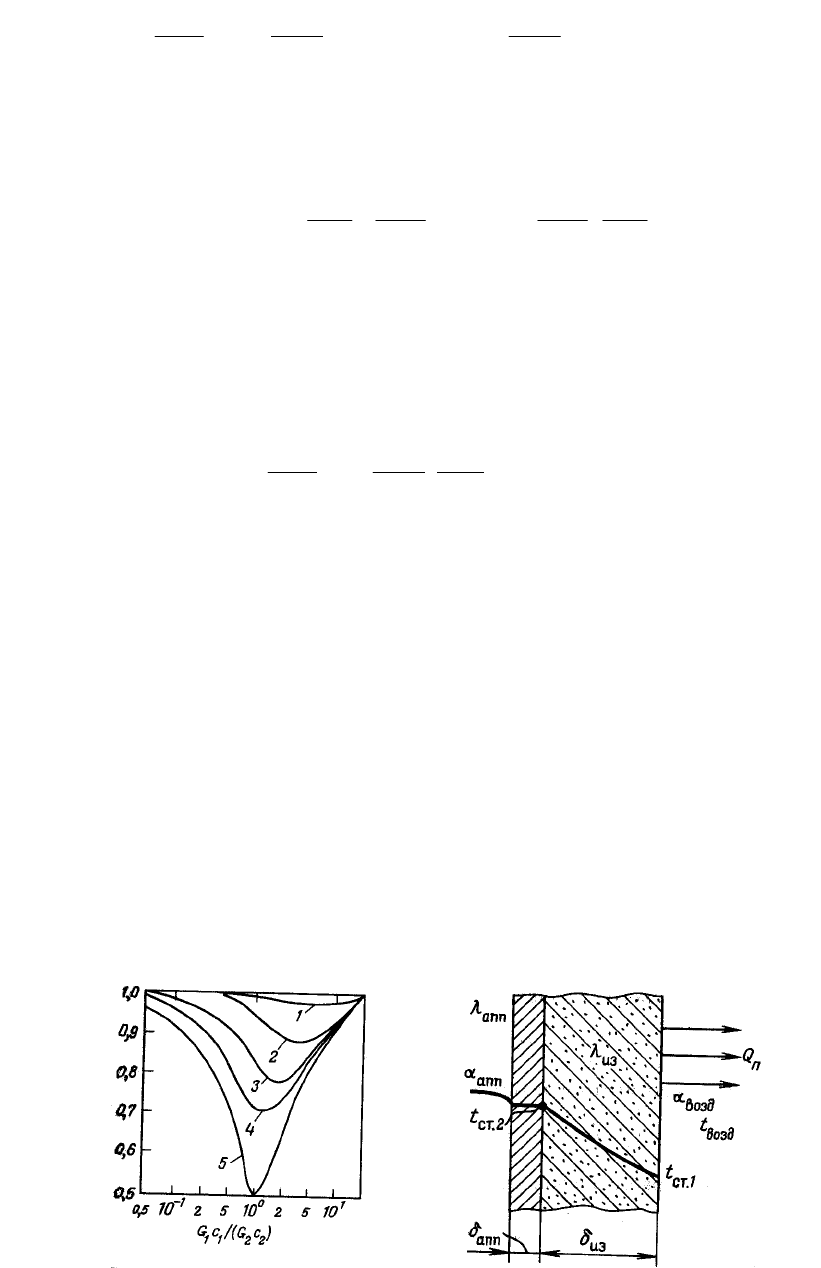
Отношение этих величин
.1/)exp(1
22
11
22
11
cG
cG
mKF
cG
cG
Q
Q
ПТ
ПМ
(11.107)
Поскольку
,1
11
1122
11
2211
cG
KF
cG
cG
KF
cGcG
mKF
можно записать
.,
1122
11
cG
KF
cG
cG
f
Q
Q
ПТ
ПМ
(11.108)
Оба аргумента изменяются в пределах от 0 до
.
Результаты численных расчетов отношения Q
ПМ
/Q
ПТ
приведены на рис.11-21,
из которого видно, что рассматриваемые схемы равноценны в двух случаях: 1)
массовая теплоемкость (Gc) одного из теплоносителей намного превышает
массовую теплоемкость второго; 2) отношение KF/G
1
c
1
близко к нулю.
В первом случае температура теплоносителя с большой массовой
теплоемкостью изменяется слабо, во втором изменение температуры
теплоносителей мало по сравнению с
t
cp
. Во всех остальных случаях при
противотоке при прочих равных условиях поверхность теплопередачи оказывается
меньшей, чем при прямотоке.
Рис. 11-21. Сравнение прямотока и противотока:

1 – KF/(G
1
c
1
)=0,1; 2 – 0,5; 3 – 1,0; 4 – 2,0; 5 -
Рис. 11-22. К определению толщины стенки тепловой изоляции
Определение температуры стенок. При расчете тепловых процессов часто
требуется знание температуры t
CT1
более нагретой поверхности стенки или
температуры t
ст2
менее нагретой поверхности. В некоторых случаях эти
температуры можно определить по уравнению (11.12). Чаще температуру стенки
приходиться определять методом последовательных приближений: задавшись
температурой, определяют коэффициент теплоотдачи
, коэффициент
теплопередачи К, а затем проверяют сходимость расчетной величины t
ст1
с
предварительно принятой по нижеприведенным формулам.
Расчет t
CT1
и t
СТ2
проводят на основе уравнений теплоотдачи и теплопередачи.
Количество теплоты, отдаваемое более нагреты теплоносителем,
Q =
1
F(t
CT2
-t
2
),
г д е t
2
- температура более нагретого теплоносителя.
Из последних уравнений получаем
);/(
111
FQtt
CT
);/(
222
FQtt
CT
По уравнению теплопередачи (11.2а) Q=KF
t
cp
. Из этого уравнения величину
Q подставим в уравнение (11.109) и получим выражения для расчета искомых
значений t
CT1
и t
СТ2
:
;/
111
cpCT
tKtt
;/
222
cpCT
tKtt
Отметим, что температура стенки всегда ближе к температуре теплоносителя с
большим коэффициентом теплоотдачи.
Определение толщины тепловой изоляции. Как правило, все аппараты, в
которых процесс протекает при температуре, отличной oт температуры
окружающей среды (теплообменники, реакторы и др.), покрывают слоем (или
слоями) тепловой изоляции
В качестве теплоизоляционных материалов используют вещества с низкими
коэффициентами теплопроводности
из
, которые обычно имеют значение
из

порядка 0,05-0,2 Вт/(м-К). К ним относят асбест, шлаковую вату, асбослюду и т.п.
Обычно теплоизоляционные материалы имеют пористую структуру, причем поры
материала заполнены воздухом, у которого очень низкий коэффициент
теплопроводности.
Величину
ИЗ
(рис. 11-22) находят из условия равенства теплового потока через
стенку аппарата и слой тепловой изоляции и потока, уходящего от стенки
изоляции в окружающую среду:
;))(/(
12
FttQ
CTCTИЗИЗП
.)(
1
FttQ
ВОЗДCTВОЗДП
Тогда
.
)(
)()(
2
1212
ВОЗДCTВОЗД
CTCTИЗ
П
CTCTИЗ
ИЗ
tt
tt
Q
Ftt
(11.111)
Температуру стенки изоляции t
CT2
со стороны стенки аппарата обычно
принимают равной средней температуре теплоносители в аппарате (например,
если в аппарат подается водяной пар, то t
CT2
принимают равной температуре
пара). Температуру t
CT1
стенки изоляции со стороны окружающей среды выбирают
в интервале 35-45 °С для аппаратов, работающих в помещении, и 0-10°С для
аппаратов, работающих вне помещения (для зимних условий), и затем
проверяют по формуле
ВОЗДCpВОЗДCT
tKtt
/
1
, (11.112)
где
воздиз
из
апп
апп
апп
К
11
1
коэффициент теплопередачи от
теплоносителя в аппарате к окружающей среде.
Величинами 1/
апп
и
апп
/
апп
ввиду их малости по сравнению с
ИЗ
/
ИЗ
+ 1/
возд
обычно пренебрегают. Значение
t
cp
находят обычным путем, а
величину
возд
- по формуле (11.61).
Для аппаратов с плоскими стенками очевидно, что с увеличением толщины
стенки изоляции должно привести к снижению потерь теплоты в окружающую среду
и температуры t
ст1
. В аппаратах с цилиндрическими стенками с увеличением толщины
стенки изоляции возрастает поверхность теплообмена с окружающей средой. Поэтому при
определенных условиях (для цилиндрических стенок малого диаметра - обычно для
трубопроводов, химических реакторов очень малого диаметра и т. п.) потери теплоты с

увеличением толщины стенки изоляции могут возрастать, несмотря на снижение t
ст1
.
Поэтому для данного случая теплообмена можно ожидать существование
экстремума. Из уравнения (11.74) следует, что коэффициент теплопередачи для
цилиндрической стенки К
l
зависит от радиуса наружной стенки изоляции r
2
.
Дифференцируя уравнение (11.75) с учетом уравнения (11.74) по r
2
, получим r
2кр
=
из
/
2
.
Отсюда следует, что функция Q =f(r
2
) имеет максимум при r
2кр
=
из
/
2
,т.е. при этом радиусе потери теплоты в окружающую среду максимальны. Радиус r
2кр
,
соответствующий этим условиям, называют критическим. Поэтому радиус r
2
слоя
изоляции цилиндрического аппарата должен быть больше критического r
2кр
. Если рaдиус r
2
принять меньшим r
2кр
, то потери теплоты возрастут.
Глава 5 МАССООБМЕННЫЕ ПРОЦЕССЫ И АППАРАТЫ
Процессами массообмена называют такие процессы, в которых основную
роль играет перенос вещества из одной фазы в другую. Движущей силой этих
процессов является разность химических потенциалов (см. гл. 2). Как и в любых
других процессах, движущая сила массообмена характеризует степень отклонения
системы от состояния динамического равновесия. В пределах данной фазы вещество
переносится от точки с большей к точке с меньшей концентрацией. Поэтому обычно
в инженерных расчетах приближенно движущую силу выражают через разность
концентраций, что значительно упрощает расчеты массообменных процессов.
Массообменные процессы широко используются в промышленности для
решения задач разделения жидких и газовых гомогенных смесей, их
концентрирования, а также для защиты окружающей природной среды (прежде
всего для очистки сточных вод и отходящих газов). Например, практически в
каждом химическом производстве взаимодействие обрабатываемых веществ
осуществляется в реакторе, в котором обычно происходит только частичное
превращение этих веществ в продукты реакции. Поэтому выходящую из реактора
смесь продуктов реакции и непрореагировавшего сырья необходимо подвергнуть
разделению, для чего эту смесь направляют в массообменную аппаратуру, из
которой непрореагировавшее сырье возвращается в реактор, а продукты реакции
направляются на дальнейшую переработку или использование.
Наибольшее распространение получили рассмотренные ниже массообменные
процессы.

1. Абсорбция- избирательное поглощение газов или паров жидким
поглотителем. Этот процесс представляет собой переход вещества из газовой (или
паровой) фазы в жидкую. Наиболее широко используется для разделения
технологических газов и очистки газовых выбросов.
Процесс, обратный абсорбции, т. е. выделение растворенного газа из
жидкости, называют десорбцией.
2. Перегонка и ректификация - разделение жидких гомогенных смесей на
компоненты при взаимодействии потоков жидкости и пара, полученного испарением
разделяемой смеси. Этот процесс представляет собой переход компонентов из
жидкой фазы в паровую и из паровой в жидкую. Процесс ректификации
используется для разделения жидких смесей на составляющие их компоненты, полу-
чения сверхчистых жидкостей и для других целей.
3. Экстракция (жидкостная)- извлечение растворенного в одной жидкости
вещества другой жидкостью, практически не смешивающейся или частично
смешивающейся с первой. Этот процесс представляет собой переход извлекаемого
вещества из одной жидкой /)азы в другую. Процесс применяют для извлечения
растворенного вещества или группы веществ сравнительно невысоких концентра-
ций.
4. Адсорбция- избирательное поглощение газов, паров или растворенных в
жидкости веществ твердым поглотителем, способным поглощать одно или
несколько веществ из смеси. Этот процесс представляет собой переход веществ из
газовой, паровой или жидкой 1шзы в твердую. Адсорбцию применяют для
извлечения того или иного вещества (или веществ) достаточно низкой концентрации
из six смеси. Процесс, обратный адсорбции, т.е. выделение сорби-рованного
вещества из твердого поглотителя, называют десорбцией.
5. Ионный обмен- избирательное извлечение ионов из растворов
электролитов. Этот процесс представляет собой переход извлекаемого вещества из
жидкой фазы в твердую. Процесс применяют для извлечения веществ из растворов,
в которых эти вещества находятся при низких концентрациях.
6. Сушка - удаление влаги из твердых влажных материалов, ц основном
путем ее испарения. Этот процесс представляет собой переход влаги из твердого
влажного материала в газовую или паровую фазы. Сушку широко применяют в
технике для предварительного обезвоживания перерабатываемых веществ или
обезвоживания готового продукта.

7. Растворение и экстрагирование из твердых тел-это процессы перехода
твердой фазы в жидкую (растворитель). Извлечение на основе избирательной
растворимости какого-либо вещества (или веществ) из твердого пористого
материала называют экстракцией из твердого материала, или выщелачиванием.
Применяют ее для извлечения ценных или токсичных компонентов из твердых мате-
риалов.
8. Кристаллизация-выделение твердой фазы в виде кристаллов из растворов
или расплавов. Этот процесс представляет собой переход вещества из жидкой фазы
в твердую. Применяется, в частности, для получения веществ повышенной чистоты.
9. Мембранные процессы- избирательное извлечение компонен-\ ов смеси или
их концентрирование с помощью полупроницаемой перегородки-мембраны. Эти
процессы представляют собой пере-\од вещества (или веществ) из одной фазы в
другую через разделяющую их мембрану. Применяются для разделения газовых и
жидких смесей, очистки сточных вод и газовых выбросов.
Таким образом, во всех перечисленных выше процессах общим является
переход вещества (или веществ) из одной фазы в другую. Процесс перехода
вещества (или нескольких веществ) из одной фазы ^ другую в направлении
достижения равновесия называют массопе-редачей. В отличие от теплопередачи,
которая происходит обычно через стенку, массопередача осуществляется, как
правило, при непосредственном соприкосновении фаз (за исключением мембранных
процессов). При этом граница соприкосновения-т.е. поверхность контакта фаз-
может быть подвижной (система газ-жидкость, пар-жидкость, жидкость-жидкость)
или неподвижной (газ-твердое тело, пар-твердое тело, жидкость-твердое тело).
Перенос вещества внутри фазы - из фазы к границе раздела фаз или наоборот
- от границы раздела в фазу - называют массоотдачей (по аналогии с
процессом переноса теплоты внутри фазы-теплоотдачей).
Процессы массопередачи обычно обратимы. Причем направление перехода
вещества определяется концентрациями вещества в фазах и условиями
равновесия.
Процесс перехода вещества из одной фазы в другую в изолированной
замкнутой системе, состоящей из двух или большего числа фаз, возникает
самопроизвольно и протекает до тех пор, пока между фазами при данных
условиях температуры и давления не установится подвижное фазовое
равновесие. При этом в единицу времени из первой фазы во вторую переходит
столько же молекул, сколько в первую из второй. Если теперь количество
распределяемого вещества увеличить (например, в фазе Фу) на п молекул, то
распределяемое вещество будет переходить из фазы Фу в фазу Ф^. Причем
скорость перехода будет определяться не общим числом молекул (тА-п)
вещества М, находящегося в фазе Фу, а числом молекул, избыточным по
отношению к равновесному (т). Так как концентрация пропорциональна числу
молекул, то скорость перехода распределяемого вещества из одной фазы в
другую пропорциональна разности между фактической (или рабочей)
концентрацией распределяемого вещества в данной фазе (т+п) и равновесной
(w). А это означает, что чем больше такая разница, тем больше (при всех
прочих равных условиях) перейдет вещества М из одной фазы в другую. Если
эта разница отрицательна, то вещество М переходит из фазы Ф^ в фазу Фу (т. е.
процесс пойдет в обратном направлении).
Таким образом, знание равновесных концентраций распределяемого вещества
позволяет определить направление процесса-из какой фазы в какую будет
переходить вещество М - и в определенной степени-скорость процесса.
Как отмечалось выше, массообменные процессы протекают лишь при
нарушении фазового равновесия. Только при этом условии распределяемое
вещество переходит из одной фазы в другую. При этом различают два вида
переноса вещества - молекулярный и конвективный.
В неподвижной среде распределяемое вещество переходит из внутренних
слоев данной (первой) фазы к поверхности раздела фаз и, пройдя ее,
распределяется по всему объему другой фазы, находящейся в контакте с
первой. Такой переход массы вещества из одной фазы в другую называют
молекулярной диффузией. Она является следствием теплового движения
молекул (ионов, атомов), которому оказывают сопротивление силы
внутреннего трения.
Конвективный перенос (конвективная диффузия) характеризуется
перемещением (переносом) вещества движущимися частицами по-ока в
условиях турбулентного движения фаз. Конвективный перенос вещества под
действием турбулентных пульсаций иногда называют турбулентной
диффузией.
Основным кинетическим уравнением массообменных процессов является
уравнение массопередачи, которое основано на общих кинетических
закономерностях химико-технологических процессов.
Скорость процесса [в кг/(м
2
-с)] равна движущей силе Д, деленной 'ui
сопротивление R:
