Буценко Л.М., Красінько В.О. Технології мікробного синтезу лікарських засобів: Лабор. практикум
Подождите немного. Документ загружается.

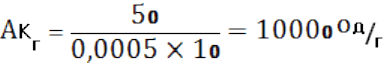
буферного розчину з рН 7,5 і 1 мл
2%-ного розчину о-діанізидіину. Отриманий
розчин доводять до 100 мл
дистильованою водою, перемішують і
використовують для аналізу протягом 10 діб. 5. Розчин глюкозооксидази
готують з розрахунку активності 500 од / г: 50 мг препарату розчиняють в 50 мл
1 М фосфатного буфера, об'єм розчину доводять до 100 мл
дистильованою
водою.
Техніка визначення.
У пробірку місткістю 25 мл вносять 1 см досліджуваного ферментного
розчину та 1 мл робочого розчину, суміш перемішують, а потім швидко
доливають 1 мл розчину глюкози. Вміст пробірки перемішують і інкубують в
ультратермостаті при температурі 37 °С 10 хв. Потім пробірки з реакційною
рідиною поміщають в киплячу водяну баню для інактивації ферменту і
витримують 5-10 хв. Вміст пробірки охолоджують до кімнатної температури,
інтенсивність утвореного забарвлення вимірюють на фотоелектроколориметрі
при довжині світлової хвилі 440 нм у кюветі з товщиною поглинаючого шару 5
мм, в порівнянні з контрольним розчином.
Контрольний розчин готують так. У пробірку вносять 1 мл
розчину
глюкози, 1 мл
попередньо інактивованого кип'ятінням ферментного розчину і 1
мл
робочого розчину. Суміш перемішують і витримують у ультратермостаті
при 37 °С 10 хв. Потім вміст пробірки охолоджують до кімнатної температури і
використовують для колориметрування.
За отриманим значенням оптичної густини знаходять кількість окисленої
глюкози за градуювальним графіком. Його будують за стандартними
розчинами глюкози. Готують розчини глюкози концентрацією від 10 до 100 мкг
в 1 мл. Обрахунок результатів
Активність глюкозооксидази розраховують за формулою:
де С - кількість окисленої в процесі ферментативної реакції глюкози, мкг; а -
кількість ферментного препарату,взятого на аналіз, г; г - тривалість
ферментативної реакції, хв.
Приклад 12.5. Визначити глюкозооксидазну активність ферментного
препарату. 50 мг його поміщають у мірну колбу місткістю 100 мл з попередньо
налитим фосфатним буферним розчином у кількості 50 мл. Об'єм розчину
доводять до мітки дистильованою водою, а =50/100 = 0,5 мг, або 0,0005 г.
Після проведення ферментативної реакції окислення глюкози і подальшого
колориметрування отримана оптична густина, рівна 0,252. За градуювальним
графіком цієї величини відповідає 50 мкг окисленої глюкози.
За формулою розраховують активність глюкозооксидази:
41
Завдання для виконання студентами.
1. Визначити активність амілази та білок за методом Лоурі в заданому
варіанті.
2. Визначити активність протеази та білок за методом Лоурі в
заданому варіанті.
3. Визначити активність -галактозидази та білок за методом Лоурі в
заданому варіанті.
4. Визначити активність глюкозооксидази та білок за методом Лоурі в
заданому варіанті.
5. Розрахувати питому активність ферментних препаратів.
6. Визначити вологість варіанта ферментного препарату методом
сушіння до постійної маси.
7. Визначити вміст ферментів в лікарських препаратах для
покращення травлення. Результати визначення узагальнити в таблиці. Зробити
висновки.
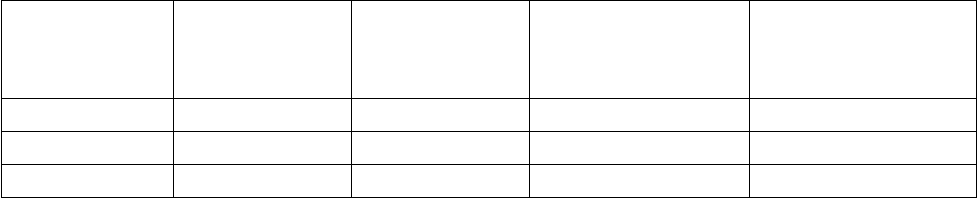
Таблиця 4.1
. Результати визначення активності ферментів
Номер
бригади
Назва
ферментного
препарату
Термін
придатності
Амілолітична
активність
Протеолітична
активність
Контрольні запитання
1. В яких одиницях визначають кількість ферментів?
2. Опишіть основні принципи визначення ферментів.
3. Дайте визначення поняття «стандартна одиниця ферментативної
активності».
4. Принцип методу визначення активності амілази?
5. Принцип методу визначення активності протеази?
6. Принцип методу визначення активності лактази?
7. Принцип методу визначення активності глюкозооксидази?
8. В яких одиницях виражають питому активність ферментів?
9. Як розраховують питому активність ферментних препаратів?
10. Які ферменти входять до складу препаратів для покращення травлення?
4.5. Поверхневе культивування для одержання ферментів (початок).
Вплив вологостi твердого поживного середовища на бiосинтез
ферментiв. Для поверхневого способу культивування продуцентiв ферментiв
ступiнь зволоження твердого поживного середовища має велике значення. За
низької вологостi мiкроорганiзми не можуть використовувати поживнi
речовини середовища, оскільки дифузiя останнiх ускладнена, що призводить
до сповiльнення росту, бiосинтезу ферментiв та інтенсивного спороутворення.
42
Надмiрне зволоження порушує крихку структуру середовища, знижує його
повiтропроникливiсть, що також призводить до сповiльнення росту i зниження
бiосинтезу ферментiв.
Оптимальна вологiсть твердого поживного середовища для бiосинтезу
ферментiв залежить вiд фiзiологiчних властивостей продуценту, складу
поживного середовища i зазвичай повинна бути в межах 65 – 70 %.
На першому занятті готують поживне середовище заданого складу i
вологостi, стерилiзують середовище, контролюють посiвний матерiал,
зволожують середовище i засiвають, розкладають засiяне середовище в кювети
i ставлять кювети для вирощування.
На другому заняттi аналiзують готову культуру, визначають
оцукрювальну або амiлолiтичну активнiсть, вологiсть готової культури i вихiд.
Спiвробiтники кафедри готують посiвний матерiал i стерилiзують посуд.
За 7 днiв до початку заняття пересiвають продуцент A. оryzae 740-А2 iз
музейної пробiрки на свiжоскошений сусло-агар у пробiрки. Пробiрки
вмiщують у термостат iз температурою 30 ºС на 3 – 4 доби. Потiм 1 мл
суспензiї спор (10 мл стерильної води на пробiрку) засiвають стерильне тверде
поживне середовище (15 г пшеничних висівок вологiстю 45 % у колбах
місткістю 250 мл), добре перемiшують i ставлять для вирощування у термостат
з температурою 30 ºС на 2 - 3 доби. Культура в колбах є вихiдним посiвним
матерiалом. Попередньо також стерилiзують кювети для вирощування, посуд
для засiву i зволоження середовища, мiрнi цилiндри, колби з водопровiдною
водою, склянi палички для перемiшування при температурi 120 ºС протягом 30
хв.
Завдання для виконання студентами.
Вивчаючи бiосинтез амiлолiтичних ферментiв на середовищi певного
складу але за рiзної вологостi (45, 55, 60, 65 i 70 %), кожен студент готує
вiдповiдний варiант середовища заданої вологостi у кiлькостi 150 г за
повiтряно-сухою масою.
Варiанти поживних середовищ:
I –100 % пшеничних висівок;
II – 80 % пшеничних висівок i 20 % солодових росткiв;
III – 80 % пшеничних висівок i 20 % деревної тирси;
IV – 80 % пшеничних висівок i 20 % бурякового жому.
Зваженi компоненти добре перемiшують i 100 г одержаного середовища
(А
1
) зважують до стерилiзацiї i заповнення кювети. Середовище вмiщують у
попередньо зважену (а), складену у чотири шари марлеву серветку. Серветки iз
середовищем кладуть у бiкс i стерилiзують протягом 1 год при 120 ºС.
Простерилізовані серветки iз середовищем зважують (В) для визначення
кількості конденсованої вологи n:
n = B – A
1
– a
За час стерилiзацiї вмiщеного у серветку поживного середовища у
залишковому середовищi визначають вихiдну вологiсть W
вих
i розраховують
кiлькiсть води, яку необхiдно додати для досягнення заданої вологостi W
зад
.
43

Вологiсть визначають прискореним методом на приладі Чижової
(див.дод.).
Кiлькiсть добавленої води визначають такими способами:
1. Вмiст абсолютно сухих речовин у середовищi з вихiдною вологістю, г,
A
ср
=
1
вих
А
100
W100
2. Маса того ж середовища iз заданою вологiстю, г,
завд
.р.с2
W100
100
АА
3.Кiлькiсть води, яку необхiдно додати для досягнення заданої вологостi з
урахуванням конденсованої вологи, г,
D = A
2
- A
1
- n
Приклад розрахунку. Приготувати 125 г (А
1
) середовища із заданою
вологістю 60 % (W
зад
). Вихідна вологість середовища 10 % (W
вих
). Кількість
конденсованої вологи – 10 г (n).
A
ср
=
5,112125
100
10100
г - вмiст абсолютно сухих речовин у середовищi.
25,281
60100
100
5,112А
2
г - маса середовища iз заданою вологiстю.
D = 281,25
–125
– 10 = 146, 25 г - кiлькiсть води, яку необхiдно додати
для досягнення заданої вологостi.
Потiм зволожують i засiвають поживне середовище з додержанням
правил асептики у безпосереднiй близькості вiд газового пальника. Вiдому з
розрахунку кiлькiсть води вимiрюють у стерильний цилiндр i використовують
для перенесення посiвного матерiалу в посуд для засiву з поживним
середовищем.
Середовище необхiдно добре перемiшати з посiвним матерiалом рукою у
гумовiй рукавичцi, попередньо промитій спиртом, а потiм перенести у кювету
для вирощування, перфороване дно якої закрите шаром фiльтрувального
паперу. Середовище рiвномiрно розподiляють у кюветi i закривають кришкою.
Кювету необхiдно зважити до заповнення середовища i пiсля засiву для
визначення кiлькостi сухих речовин середовища, поставленого на вирощування
М
1
. Кювети ставлять на 30 год для вирощування у термостат з температурою 29
– 30 ºС, в якому пiдтримують вiдносну вологiсть повiтря 95 – 100 %.
Через 30 год кювети виймають iз термостата, загортають у полiетиленову
плівку i кладуть у холодильник до наступного заняття.
Матеріали та обладнання: компоненти для приготування поживного
середовища (меляса, кукурудзяний екстракт або дріжджовий гідролізат, солі
(NH
4
)
2
SO
4
, KH
2
PO
4
, K
2
HPO
4
, NH
4
Cl, пшеничні висівки, солодові паростки,
тирса, соняшникове лушпиння, буряковий жом); культури продуценти для
поверхневого культивування – A. orizae. ФЕК з набором кювет, апарат Чижової,
рефрактометр, лакмусовий папір; технічні ваги. Крім того, на кожну бригаду
одна стерильна металева кювета, одна колба з 90 мл стерильної водопровідної
води, один стерильний мірний циліндр.
44
Контрольні запитання
1. Дайте загальну характеристику поверхневого методу
культивування.
2. Які методи культивування застосовують при одержанні
ферментівмікробним синтезом?
3. Які фази росту характерні для продуцентів ферментів за
поверхневого культивування?
4. Яке значення має аераціа при поверхневому культивуванні?
5. Охарактеризуйте принципи складання поживних середовищ за
поверхневого та глибинного культивування.
6. Які речовини є індукторами і репресорами при біосинтезі амілаз?
7. Охарактеризуйте продуцентів амілолітичних ферментів.
ЛАБОРАТОРНА РОБОТА 5.
ПОВЕРХНЕВЕ КУЛЬТИВУВАННЯ ДЛЯ ОДЕРЖАННЯ ФЕРМЕНТІВ
(ЗАКІНЧЕННЯ). МЕТОДИ ОЧИЩЕННЯ ФЕРМЕНТНИХ ПРЕПАРАТІВ.
5.1 Поверхневий спосiб культивування продуцентiв ферментiв
(закінчення).
Екстрагування ферментів з поверхневих культур
Після того як культивування закінчено, культуру підсушують і з кювет
вона надходить до загального бункера, з якого поступає на подрібнення. Після
цього культура надходить на стадію екстракції ферменту.
Всі ферменти є водорозчинними білками, тому найкращим екстрагентом
для них є вода. Для видалення ферментів з дріжджових та бактеріальних клітин
їх необхідно зруйнувати використовуючи механічні, хімічні або біологічні
методи, оскільки їхні клітинні стінки мають високий дифузійний опір.
Оболонки міцеліальних клітин мають низький дифузійний опір, тому
дезінтеграція клітин грибів непотрібна.
На повноту екстрагування ферментів впливають багато факторів:
температура, рН, тривалість процесу, конструктивні особливості екстракційних
апаратів.
Серед небажаних процесів, що можуть відбуватися після дезінтеграції
клітин, – протеоліз власними клітинними протеазами цільового ферменту. Цей
процес може відбуватися навіть при підтриманні низької температури,
особливо при очищенні ферменту, оскільки після видалення супутніх білків
фермент стає єдиним субстратом протеази. Інактивацію протеаз здійснюють
обробкою клітинного екстракту специфічними інгібіторами-комплексонами
(ЕДТА, о-фенантролін, оксихінолін), солями ртуті або срібла. Протеази можуть
бути видалені також сорбцією на афінних сорбентах. Якщо протеази
термолабільні, а цільовий фермент термостабільний, їх можна денатурувати
нагріванням клітинних екстрактів.
Денатурацію нуклеїнових кислот в процесі очищення ферментів
обумовлює низька іонна сила чи основність середовища. Можна використати
спеціальні осадники, що утворюють з нуклеїновими кислотами нерозчинні
комплекси. З цією метою використовують бромистий цетилтриметиламмоній,
45

стрептоміцин сульфат, протаміносульфат, поліетиленімін. Інший метод
видалення нуклеїнових кислот використання нуклеаз – панкреатичних ДНК-аз
та РНК-аз.
Завдання для виконання студентами.
Метою роботи є обчислення кількісного впливу вологостi твердого
поживного середовища на накопичення амiлолiтичних ферментiв культурою A.
оryzae 740-А2.
Аналіз вирощеної поверхневої культури
Кювету з готовою культурою продуценту зважують, пiсля чого її вміст
переносять у кристалiзатор, добре перемiшують i вiдбирають середню пробу, з
якої беруть двi наважки для визначення вологостi i двi наважки – для
визначення ферментативної активностi.
Вологiсть готової культури визначають прискореним методом у двох
паралельних пробах i визначають масу сухих речовин у готовiй культурi гриба
М
2
за формулою
М
2
=
1
вих
М
100
W100
Вихiд готової культури вiд маси вихiдного середовища становить, %,
N =
100
M
M
1
2
Таким чином, втрати сухих речовин на вирощуваннi продуцента, %,
= 100 – N.
Для визначення ферментативної активностi готової культури
продуцента готують витяжку iз поверхневої культури за методикою, наведеною
в додатку.
У одержанiй витяжці визначають оцукрювальну активнiсть (ОС) або
амiлолiтичну активнiсть (АС) за методиками, наведеними в лабораторній
роботі 4.
За даними, одержаними групою студентів, які вивчають накопичення
амілолітичних ферментів за різної вологості поживного середовища одного
складу, будують графік залежності біосинтезу амілолітичних ферментів від
вологості поживного середовища. Для цього на осі абсцис відкладають
значення вологості, а на осі ординат – одержане значення ферментативної
активності (ОС або АС).
Результати роботи занести у табл. 5.1 і зобразити у вигляді графіка.
Виходячи із одержаних даних зробити висновок про оптимальне значення
вологості поживного середовища для біосинтезу амілолітичних ферментів на
твердому поживному середовищі для компонента, який вивчають.
Таблиця 5.1
Варіант
середовища
W
вих
W
зад
Маса
сухих
Кількість води
для
Втрати
сухих
ОС або
АС, од/г
46

речовин зволоження
D
речовин N
Матеріали та обладнання: ФЕК з набором кювет, рефрактометр,
лакмусовий папір, технічні ваги, реактиви для визначення амілолітичної
активності (див. лаб. роб. 4).
5.2. Методи очищення ферментних препаратів
Серед багатьох методів очищення ферментів найбільшого поширення
набули методи осадження органічними розчинниками та неорганічними
солями. Розчинність білка визначається розподілом гідрофобних і гідрофільних
залишків на поверхні молекули. Змінюючи деякі властивості білкових розчинів
(температуру, іонну силу, рН, додавання нейтральних солей, водорозчинних
органічних сполук або інших інертних речовин), можна вплинути на гідратний
або сольватний шар і викликати агрегацію білкових молекул і випадання їх в
осад.
Осадження ферментів органічними розчинниками. Ефект осадження білків
пов'язаний з тим, що в присутності органічного розчинника знижується
активність води. Зі збільшенням концентрації розчинника знижується здатність
води до сольватації заряджених гідрофільних молекул ферменту. Діелектрична
постійна розчинника знижується, відбувається витіснення молекул води з
поверхні білкової молекули та їх часткова іммобілізація молекулою
органічного розчинника внаслідок гідратації білка. Тому молекули води,
розміщені на гідрофобних ділянках поверхні білка, можуть бути заміщені на
молекули органічного розчинника. При цьому розчинність білків знижується,
відбувається агрегування і осадження білкових молекул.
Агрегування білків відбувається під дією електростатичних і Ван-дер-
Вальсових сил, що виникають між окремими білковими молекулами.
Гідрофобна взаємодія, ймовірно, має менше значення в результаті впливу
органічних розчинників на неполярні ділянки білкової глобули.
Органічний розчинник, який використовують для осадження, повинен
повністю змішуватися з водою і не зв'язуватися з ферментом. Найбільш
широко для осадження ферментів використовуються етиловий спирт, ацетон і
ізопропіловий спирт. Рідше застосовуються метанол, н-пропанол, діоксан, 2-
метоксиетанол і інші спирти, кетон, ефіри та їхні суміші. Найбільш
перспективним вважається осадження ферментів ізопропанолом. Осадження білків
здійснюється при порівняно низькій його концентрації (52 –53%), і препарати
містять на 40 – 45% менше баластних речовин, ніж за осадження ацетоном і
особливо етанолом.
Різна розчинність ферментів в органічних розчинниках дозволила
розробити способи їхнього розділення.
Осадження ферментів висококонцентрованими розчинами солей
(висолювання). Процес висолювання ферментів в основному залежить від ступеня
гідрофобності білкової молекули. Типова білкова молекула має гідрофобні ділянки
47

на поверхні у вигляді бічних ланцюгів низки амінокислот (тирозин, триптофан,
лейцин, ізолейцин, метіонін, валін і фенілаланін). На гідрофобних ділянках
молекули білка при контакті з водою відбувається утворення шару, що
складається з орієнтованих молекул води.
Але таке впорядкування структур є термодинамічно нестійким, оскільки в
такій системі відбувається значне зниження ентропії в порівнянні з системою
негідратований білок – вільні молекули води. Якщо молекули води
іммобілізувати молекулами небілкової природи, то білкові молекули починають
взаємодіяти і відбувається їхня агрегація. Відомо, що іони солей гідратуються, і при
додаванні значної кількості солі відбувається зв’язування води, білок частково
звільняється від води і створюються умови для агрегації білкових молекул.
Різні білки по-різному реагують на процес висолювання. Це залежить в
першу чергу від кількості і розмірів гідрофобних ділянок на поверхні білкової
молекули. Чим більше таких ділянок, тим легше відбувається висолювання
білків. Існують білки, які навіть при дуже високій концентрації солі в розчині
майже не агрегують і не випадають в осад. При осадженні ферментів зі
складної суміші різноманітних білків має місце явище соосадження. Після
дегідратації білкових молекул в розчині солей молекули білка агрегують не з
ідентичним, а з будь-якими іншими клейкими молекулами, що знаходяться
поблизу. Це приводить до отримання препаратів, збагачених різними супутніми
речовинами. Проте при висолюванні можна досягти не лише осадження всього
комплексу ферментів, але і його фракціонування.
Хоча висолювання білків в основному визначається гідрофобними
взаємодіями, на цей процес істотно впливають і інші чинники: рН середовища,
близькість його до ізозлектричною точкою білка, температура, ступінь чистоти
ферментного розчину, тривалість процесу і т.д.
Для висолювання в основному використовуються нейтральні солі лужних
металів. Висолюючий ефект різних іонів залежить від їх іонної сили. Для
висолювання можуть бути використані сульфат амонію, сульфат натрію, сульфат
цинку і хлористий натрій. Найчастіше використовують сульфат амонію, рідше -
хлористий натрій. Найбільше осадження білків відбувається при концентрації солі
в розчині, близької до концентрації насичення. Але це не завжди зручно, так як в
осад разом з білком захоплюється велика кількість солі, що вимагає додаткового
очищення препаратів і ускладнює їх застосування. Звичайно осадження ведуть
розчином з концентрацією солі 0,5 – 0,9 від повного насичення, але і в цьому
випадку в препарати переходить від 20 до 80% солі від маси осаду.
Найскладніша стадія процесу висолювання – це внесення солі і спосіб її
розчинення. Сіль подрібнюють і поволі додають невеликими порціями при
постійному перемішуванні, щоб уникнути локальних зон підвищення
концентрації солі в розчині. Після введення останньої порції солі
перемішування необхідно продовжити ще 20 – 40 хв до досягнення повної
рівноваги між розчиненими і агрегованими білками. Утворення осаду починається
із слабкого помутніння яке поступово переходить у суспензію із зваженими
пластівцями. Процес формування осаду залежить від температури, об'єму рідини
рН середовища і може тривати від 20 – 40 хв. до декількох годин.
48

При очищенні кожного ферменту важливо підібрати таку концентрацію
осадника, яка дозволить досягнути оптимальної ступені очистки і виходу
ферментативної активності.
Ступінь очистки ферменту показує в скільки разів збільшилася питома
активність ферменту за даного способу очистки порівняно з питомою активністю
вихідного ферменту.
Вихід ферменту – це відсоток загального числа одиниць активності в
очищеному розчині від загальної активності вихідного розчину, яку приймають за
100%.
В = А
заг.очищ.
/А
заг.вих.
*100%
Завдання для виконання студентами.
Для очищення використовують екстракт з поверхневої культури або
неочищені ферментні препарати.
1. Приготувати розчин ферменту 10% концентрації.
2. Профільтрувати приготовлений розчин.
3. Охолодити розчин ферменту та долити осадник (у відповідності до
запропонованого викладачем варіанту) (табл. 5.2).
4. Залишити розчин в холоді до утворення осаду.
5. Відділити осад від розчину (фільтруванням або центрифугуванням
20 хв).
6. Розчинити осад в 5 – 10 мл води.
7. Визначити вміст білка методом Лоурі у вихідному та очищеному
препаратах ферменту.
8. Визначити вміст ферменту (див. методики до лабораторної роботи
4) у вихідному та очищеному препаратах.
9. Розрахувати питому активність ферменту, ступінь очищення ферменту,
вихід ферменту.
10.Результати роботи занести до таблиці 5.3.
Таблиця 5.2.
Концентрацій осадників, що застосовують для очищення ферментів
Ферменти Концентрація осадника
Сульфат
амонію
Ізопропанол Ацетон Етиловий
спирт
Амілолітичні 70-72%
Протеолітичні 52-54%
Таблиця 5.3.
Результати очищення ферментів
Очищуваний
препарат
Метод
осадження
ферменту
Питома активність
препарату, Од/мг білка
Ступінь
очистки
ферменту
Вихід
ферменту
До очистки Після
очистки
49

Контрольні запитання.
1. Опишіть процеси попереднього оброблення культуральної рідини і
біомаси продуценту. Яке значення вони мають для подальшого виділення
ферментів?
2. Проаналізуйте втрати, що можуть виникати при виробництві
ферментних препаратів, та запропонуйте методи їх запобігання.
3. Які фізико-хімічні властивості ферментів дозволяють здійснювати
їх виділення шляхом осадження органічними розчинниками і солями?
4. Яким чином здійснюється фракціонування ферментів за допомогою
органічних розчинників?
5. Які методи дозволяють отримати високо очищені гомогенні
ферментні препарати?
6. Порівняльна характеристика методів очищення ферментів.
7. Розрахунок ефективності методу очищення. Критерії ефективності
очищення.
8. Втрати при очищенні ферментів та заходи, що їм запобігають.
ЛАБОРАТОРНА РОБОТА 6.
ІМОБІЛІЗАЦІЯ ФЕРМЕНТІВ МЕТОДОМ СОРБЦІЇ
Іммобілізовані ферменти можуть бути використані для діагностики і
лікування різних захворювань, а також для створення більш досконалих
протезів і апаратів, що заміщають роботу важливих органів людини. Тому
дослідження в галузі іммобілізації ферментів і клітин надзвичайно важливі й,
очевидно, збережуть своє значення в найближчому майбутньому.
Іммобілізація ферменту це включення молекул ферменту до ізольованої
фази, яка відокремлена від фази вільного розчину, але яка може обмінюватися
з нею молекулами субстратів, продуктів, ефекторів або інгібіторів.
Іммобілізовані ферменти мають низку істотних переваг:
1) гетерогенний каталізатор (фермент) можна легко відокремити від
реакційного середовища, що дає змогу зупинити в необхідний момент реакцію,
застосувати його повторно та отримати чистий продукт, не забруднений
ферментом;
2) використання іммобілізованих каталізаторів робить можливим
проведення ферментативного процесу безперервно, наприклад у проточному
реакторі, і регулювання швидкості каталізованої реакції та виходу продукту
зміною швидкості протоку;
3) іммобілізація ферментів дає можливість регулювати їх каталітичну
активність, змінюючи властивості носія під впливом деяких фізичних чинників,
50
