Укше Е.А., Букун Н.Г. Твердые электролиты
Подождите немного. Документ загружается.


'то
гтзбранттьтм
дефектой
в течение
[о0татотЁо
6ольтпого
Ёромени
},
то
средцее
смещение-7
по
про1!]ествии
времени
|
долнтно
бьтть
равно
нулю
([
:
0).
9тобы
охАрактериаовЁ',
изменение
велитиньт
7,
3""|1у
по]1ятие
о среднем
квадратичном
смещении
(дисперсии)
Р.
б
основе
теории
диффузии
ле}1{ит
фундаментальное
ур1внение,
связывающее
среднее
квадратичное
омещение
хаотически
дви}ку-
щейся
частиць1
с временем
ее
дви}цени".
5''
ур'"".''й"
,1"",
""д
1:
6 |[,
(1.36)
где2
_
коэффициент
диффузии.
[уществует
целый
рядболееили
менее
строгих
способов
доказательства
соотно|пепия
1[.зо1
{61
-65,,
}{а
которых
мь1
здесь
не
будем
останавливаться.
0то соотлто1шение
справедливо
пприменительно
к
лтобой
ивотропной
системе
беспо-
рядочно
дви'кущихся
частиц
-
к молекулам
га3а'
к
коллоидным
частищам
(броуновское
дви}кение),
к ионам
в
растворе
и т.
п.
Фно
применимо
и
к
дви}1{ению
дефектов
в
кубитеских
ретшетках.
,(ля
ре1шеток
другого
типа'
не
обладающих
кубитеской
симметрией,
мон{но
исппольвовать
аналогичное
уравнение'
однако
с
другим
чис-
ленным
коэффициетттом.
Бсли
тастйца
совер1шила
б',,йЁ"й
сло (п)
последовательнь]х
скачков'
длина
которьтх
одинакова
и
равна
г'
то
средпий
квадрат
смещения
частицы
й
общем
случае
р'Ё"*
-
п
-|п_]
|'2
:
пт2
*2.'
.2 _)
йФ;';*1,,
э:1
&::
где
со$
.0],т'*
_
среднее
3начение
косинуса
угла
ме}кду
направле_
::-*1|-:
"
(:
*
ь1-"о
скачка
[20].
}{огда
скачки
совер|пенно
слу_
чаины
и никак
не коррелируют
ме)т{ду
собой,
т.
е.
когд1
направле_
ние
пооледующего
скачка
не
3авиоит
от
направления
предь|дуще_
го?
средвее
значение
сов
0;,71д
дол}1{но
равняться
нулю
и
(1.37)
(1.3в)
|'
:
пг".
|[оокольку
п
ео1ъ
чиоло
перескоков
3а
длитель]1ое
время
|, то,
обо-
3начая
среднее
время.
у9тду
двумя
перескоками
через
т' подучим
п
:
[/т
и'
с
учетом
(1.36),
|
:
г2/6т.
(1.3$)
}1спользование
урав1{ения
(1.39)
для
вычисления
коаффициента
диффузии
"
*'''*р''"'*
у",'"""х
требует
применения
определен-
ттой
модели.
9тобы
проиллюстрировать-схему
расчета'
рассмотрим
самодиффузию
катионов
в
релшБтйе
1\а(1,
идущую
"у'Ё#!.|"меще_|1ия
ваканспй
[201.
1\4ехацизм
диффузии
обьтчно
представляется
следующим
обра-
зом.
1]астица
колеблется
у
своего
поло}кепия
равновесия
с
часто_
той
т
в
течение
некоторого
време11и
т.
3атем
благодаря
]'!'*'де*-
с1вию
с окру}кающими
иоцами
частица
приобретае1
энергию
7,
которой
оказывается
достаточно,
ттобы
''ереск'ни'ь
барЁер,
раа-
деляющий
два
соседних
поло)1{ения
равнов6сия
(т.
о. нормальный
?А
у3ел
и ваканоию). }{
моменту
око}тча}1ия
скачка
частица
теряет
часть
своей энергии'
отдавая ее окруж{ак)щим
ионам'
и
задер}ки_
вается
в новой по3иции.
9ерез некоторое
время
в
образовав1пу|ося
вакансию
т[еремещается
другая
частица
и т.д. 1акой способ пере-
дви}кения
носит на3вание
трансляцион}1ых
скачков.
Бремя осед-
лой
экизни
частицьт
дол}кно
бьтть обратно
прот!орциот{ально коли-
честву
вакансий, находящихся
в
е0
ближсайлпом окру}1{ении.
Аля
катионной
подре1шетки
}т{а61 число бдижсайп:их
соседей одного
3на-
ка
равно
12, л еолп отнооительная
додя
вакансий
равна
15, 1Ф,
очевидно'
т-1
:
\2 п3ш',,
(1.40)
тде
шю
-
вероятнооть того' что
в
едипицу
времени катионная
ва-
кансия
перескочит из одного
у3ла
в
другой.
Расстояние ме}т{ду
блиэтсайтшими
соседями
в
катионпой подретшетке
равно
7
:1/2а, (.41)
!де
а
-
расотояние
ме)кду анионом
и катио}{ом.
!!{, таким образопг,
11олагая
г2
:
2а2,
находим
'|
:
4а2шт,т6'
(1.42)
|{ри
диффузии
с
участием
дефектов
Френкеля
соотно|шения
получаются более
сло:+сными'
так как необходипло
учитывать
дви-
ж{е1{ие ионов
одного
3нака
и чере3
ваканоии'
и цо ме)кдуузлиям.
[ля
кубинеской
ре|петки
вклад ]\{е)кдуу3ельнь1х
ионов
в коэффи-
цие!{т
диффузии
равен
а2ш5ху,
![е ш;
-
вероятность того'
что в еди-
ницу
времени ме'кдуузельный
ион
перескочит и3 одного
поло}ке-
}1ия в
другое'
а
время вы)кидания
трансляционвого
скачка опре_
деляется
вь1ран{ением
т_1
:
6 х1ш;.
Бклад
вакансий
в коэффициент
диффузии
по
аналогии с
нием (\
.42)
равен
4а2ш1пр
и, отало
бьтть,
|
:
о2л{-(тр;
*4ш',).
(1.40',)
уравне-
(1.43\
}1аиболее
сдо;кной задачей
в теории
диффузии
яв;|яется
вь1чис-
"т|е1]ие
вероятности переокока
частиць1 и3 одного
по]|о}1(ения
рав-
новесия
в
другоо.
0та
вероятность
дол?кна
быть пропорциональна
частоте
колебаний
у и
величине ехр
(-п/ьг),
тде 7
_
высота
энергетического
барьера' т. е.
ш
:
\ ехр
(-
ъ/ьт).
(1.44)
Более
точный а1{али3 показывает
(см.,
нашример,
[65!,
стр.
21),
что
частота
скачков
ошшределяется
свободной
энергией
перёмещо-
ния
(миграции),
т.
е. что
ш
:
\ ехр
(з-|Ё)
ехр
(-
ь-/ьт),
(1.45)
где
5п' ь-
-
энтроция
и энтальпия миграции.
т{астота
у оотается
2б

при
этом
достаточ1{о
неоцределенной.
почти
ничего
неи3веот11о
о частотах
колебаний
ионов
вме)кдуу3ельных
позициях.
|!ри
дви-
}{{ениипо
вакансионному
механизму
у
дол?кно
быть
равно
частоте
колебаний
иона'
соседствующего
с вакансией.
Ёа
!'рак'и*е,
од-
нако'
часто
принимают
частоту
т
рав_ной
дебаевской
чаототе
кри-
сталла.
|[оследняя
имеет порядок
1019
сек-т.
Ёапример.
для
ша€!
'0о:
4,91.1012
сек._1,
для
1((1
уо:
4,25.1012
сек'-1";:
;.
1аким
образом,
используя
вьтведеннь|е
ранее уравнения'
оп-
ределя}ощие
концентрацию
дефектов
1!!оттки'
мо'кно'написать'
например'
для
коэффициента
диффузии
катионов
по
ваканоионт1о-
:|[у
механивму
в
ре1петке
типа
1\а(] выра}кение
|т,'
-
4о2мрехр
(ч51)*,
(-
ьл^!пз|2)
.
Анадогттчно'
для
коэффициента
диффузии
анионов
Ря,
:
4а2т5
ехр
(
ъ-
1"вга
)
*,
(_
,,^:;,')
.
||ри
диффузии
дефектов
Френкеля
необходимо
учитывать
два
ме-
хани3ма
мигращии
-
по ваканопям
и' по
ме}кдуу8лиям'
так
что
21р:
2т,
*|т;.
(1.47)
|[ервое слагаемое
определяется
11о
уравнешию
(1.46)
с заменой
па-
раметров
$5
и },5
соответстве|!но
па 53
и },р.
[(оэффициент
диффузии
цо
ме'ждуузлиям
равеЁ
Ру|: а2\*ехр('+*!'ттэ
).",
(_
+)
,
где
уи
-
чаотота
колебаний
иопа в
ме)т(дуузлии;
ветотвенно
антропия
и энтальпия
миграции
иона
пым
позициям.
}равнения
(1.4в),
(1.4в')
и
(1ф
могут
бт,тть
сведены
к обоб-
щенной
форме
|
:
|о
ехр
(-
Бо|]с[),
(.:+9)
тде
Бр
-
э|!ергия
активации
диффузии.
-
|[ри
наличии
бивакаттоий
коэффициепт
диффузии
их
}!о?кет
быть
записап
аналогитпьтм
образой,
т.
е.
|ь:
|оьехр (-
Боь|ь?).
?огда коэффициентьт
диффувии
катионов
соответствепно
|т:
|т,
*
|ь,
Ра:
|',
*
|,
?в
(1.4в)
(1.4в',)
(1.4в)
8|^'11|-
-
соот-
по ме'кдуузель-
(1.50)
и
анионов
будут
равны
(1
.51)
1.4.
(оотно|цецие
Ёернста_3йппптейна.
{[роводшмость
}1а.цичие
цефектов
опроделяет споообтдооть цоп|лых крцсталлов
ппроводить
алектрический ток. Фтевидно,
дол'кна
сущеотвовать
связь
ме}кду
коэффициентом
диффузии
ионов
(|)
п
лх
подви'кцо-
стью
в
элоктрическом поле
(и).
9та
свя3ь
устанавливается
соот}{о-
]пением
}{ернста-3йнштейпа
о:щ,
тде
е
-
абсоллотттое 3наченио
ааряда
э.т|ектрона. }равнение
(1.52)
мо)т(ет
быть шолутено из слодующих сообра;кений
|171.
|[редполо-
)ким'
что чаотицьт' имеющие варяд е' паходятся
в
равновесном
оо-
стоянии
во вне]пнем
электрическом
поле Б
:
-09|0л
(например,
п[ежду обкладкапли
конденсатора)'
$онцентрация
частиц
в этом
случае будет
п{енятьоя вдоль
ооп
п. Бс.:ли частицы
подчиняются
ст11тистике 1![аксвелла-Больцмана' то
распределеппе
их
дол'кно
вь|раж{аться
урав}1ением
({.52)
п
(а)
:
сопв[.ехр
\-
еч
(п)/*[|,
где
р(;г)
-
потепциал' создаваемьтй
ньтй
электрическим полем градиент
|ёп
/
ае\/а9:1
а"
:
-
\тг] \Б/
'
(1.53
полем
в точке с.
Фбуоловлен-
концештрации
равон
|{ри
равновесии
диффузия дол}кна
частиц шод
действием
электричеокого
ся
равепство
потоков
-
п/''\_
-',/ар\
_
"\а"
):'''\а;)
(\.54)
точно компенсировать
дрейф
поля' т. е.
дол'кно
вь1пол1{ять-
(1.55)
]]{з
сопоставления
уравнений
(|'54)
и
(1.55)
можсно шолучить
урав-
цение
(1.52)
|.
1,[опользуя соотно|1]ение Ёорнста-3йнтштейна
у.
уравнения
(1.4в),
(1'46')
и
(1.48)'
определяющие
коаффициепть1
диффуаии,
нетрудно
получить
выра)кевия
для
алектроцроводшости
ионных
кристаллов.
}дельпая
электропроводность свяаана
с
подви}кпо-
стью
частиц
равепством
':
)
|{5еэ[3ш;,
]
(1.56)
где
1'[;
-
чиоло ионов
]-го
сорта
в единице
объема,
{;-
Аоля
в0-
}равпение
[ернота_9йттплтойша
справеддиво
ли|пь в
случае идеальт1ых
растворов'
когда хими!теский
потенциал
дпффундирующих
частиц связан
с
концентрацией
равенством р
:
ро
*
*! 1п
п.
,[,ля.кояденсированвшх
си-
стем
уравЁевие
11.ь21
следует
заме|тйть
па
2
_
|Ё[ш/е,
где
|
:
п
(ар|ап)'|
|]с7
:
о/!с!$
(и
-
объем
ша
одну
частицу,
р
-
изотерми[1еская
сэкиплаемооть)
[61,66,671.'
п

капоий
или
других
подвижньтх
частиц
7-го
сорта, |;
-
1\*' подвия{_
ность.
[оответственно' если' папри1!1ер'
в перет{осе
тока
учаотвуют
катионнь!е
и анионнь|е
вакансии' то шроводимость 1-1-валепт-
ного
криста]!ла
равна
6
:
!у/е
("',ш',
*
тя,шя,)
_
'*,]9."",
[.-,(-
ф*
)
*
/ ь-'-7''*\1
+
ехр
\-
-''т:)1
и' посколь(} #о
:
ехР
!-
(а.
-
?ц)|2Ё?)1
-
равновесная
кон-
центрация дефектов
|[!оттки,
.'
.',#'"".*,
[-
ъ;Р]
[.-,
(-
ф)*
1
ехр
(- ",*;,!'"-)7
"
:
#
4ш2м9ехр(-
'-;#'').-,
(-
ч-)
'1лу|
':
$о,.*,(- #):*.*,
(-+)'
где
6о:]\{е2|о|/с, Бр:Б',
(1.57)
,{,виэкение
нейтральньтх бивака:+сий
не
дает
вк.11ада
в
церецос
тока
и
в т[роводимость.
!сли
диффузией
бивакансий мо)кно пре-
небрень у1
еслу! э}|тальпия активации миграции
ионов
одного
3нака
(например,
катиопов)
существе1{но мень|пе эштальпии активации
миграции
ионов
другого
3пака
(например,
анионов), тогда
(1.58)
(1.50)
(1.60)
т. е.
уравнение
}1ернста_3йнштейна
в этом сдучае
приводит
к про-
стому
соотно1шению ме'кду
коэффициентом
диффуви14
у\
проводи-
мостью кристалла.
Б частности' окааь1ваются
равнь1ми
энергии
активации
диффузии
и проводимости. 14з ска3анного ясно так}ке'
что
такой
ре3ультат
мо)т{ет
бьтть
шолутен не столь
у}к
часто.
3кспериментальная цроверка соотно1пения Ёернота-3йн-
гптейна
для
кристаллов
цоказь|вает' что при
соблюдении
перечис-
ленных
вы|пе
условий
и
равенстве
а}1ергий активации проводимо-
о!и
у!
диффузии,
воцреки
уравнению
(1.60)'
как
правило'
о
6}
/'{е2Ро/}.
9тобьт объясдтить отклонение предэксцо}тенциаль-
ного мно'1{ителя от величины' вычисляемой
по
уравне1!ию
}1ерн-
ста_3йнлштейна,
Бардин и !,еринг
[631
шредло)кили теорию
кор-
р0ляции.
(ущность
этой теории состоит в
следующем
[64,
69' 70].
А'я
и3мерения
коэффициентов
самодиффузии исполь3уютоя
радиоактивцые
индикаторьт.,(,ви:тсение
ионов-индикаторов
в кри-
сталлической
ретшетке формально
расоматривается
как отвечаю_
щее
прицципу
слунайных
блу;кданий. }1а самом
деле
11оло}кенио
28
ш
оказь!вается
более сло'кным.
Ёапример,
при вакансиовном
мехацизме
диффузии
ион-индикатор не
мо}кет
шачать
дви?кение
до
тех
пор' пока
к нему
не
шодойдет
ваканоия.
||оскольку
вероят-
ность
подхода
вакансии
с
любой сторонь|
одинак0ва' 1{аправле}тие
первого
скачка иона-индикатора
действительно
будет слутайным.
Фднако
ситуащия
отановится ивой,
когда
речь
идет о вероятности
второго
и цоследующих
скачков. Б
самом
деле'
после первого
скачка
по соседотву с ионом
у)1(е
имеется
одна
вакансия.
Бероят-
1]ооть
того'
что к
нему
шодойдет еще одна
вакансия и он
обме-
т!яется
с
цей
местами'
очевид}1о' }1ень1пе'
чем вероятность
обрат-
ного
обмена
с первой
вакансией.
1аким образом, 11ашшравлеция
пооледующих
перемещепий инди-
катора
не являются
1|езавиоимь11!1и
-
ме}1{ду
ними существует
корреляция. 3то
шриводит
к топ[у'
что коэффициент
диффузии
радиоактивного
ицдикатора
(0'"')
отлич[1ется
от
коэффицие!{та
диффузии,
вь1т1исляеп|ого 11о
уравнони}о
11ернста-3йнтштейна,
т. е. от
к0}1дуктометрического
коэффициеттта
диффузии
(-}*'',),
поскольку ионь|'
участвую1|1ие
в проводил10сти'
не
отличип{ь1
дру|'
от
друга
и
корреляция
лр'1
их
дви?ке11ии
отсутствует.
}{оэффици_
ентом
корреляции называют
отно1ше}1ие
|^'л||^.,тц:
ф'
(1.61)
3тот
коэффицие!{т 3ависит
от типа
кристаллической
решетки.
1ак,
для
кубитеокой объемно_центрированной
реплетки Ф
:
0'7215,
для
кубинеской
граноцентрированной
ф
:
0,7в15,
\[А
цлоской
гексагонадьной
ретшетки
ф
:
0,560
и т.
д.
[69,
70|. |1ри
дви}кении
ионов
по ме)кдуу3лиям
ввиду того'
что
число
свободных
меж{ду_
узлий
несравнимо
цревь:1шаот
число 3анять1х'
корреляция отсут_
ствует ут |лнд:
2*''',.
Б
случае
(нешшрямого)
ме}кдуузельного
моханизма' когда ме)кдуу3ель}1ь]е
ионь1
дви]кутся'
обмениваяоь
местами
с
ионами
в
порма]|ьнь1х
у3лах
ре]шетки'
ф<
1.
1{еобходимо
отметить'
что экс1]ериментальная
цроверка
теории
корреляции представляет
достаточно
слож{ную вадачу'
поскольку
требует
тщательного
учета
ра3личнь!х
механи3мов
шереноса'
даю-
щих
вклад в
эдектроппроводность
и
диффузию.
Б последнее
время
в
некоторых эксцериментальных
работах
существовашие
эффекта
корреляции
ставится
под сомненле
[7!-73|.
Ёаконец, следует
учить1вать
в
ли,ятту.т'е
взаиплодействия
3ар я)кен_
ншх
дефектов
}{а
алектропроводность.
3
рамках
модели
,[,ебая_
8юккеля
это
влияние
сводится
к тормо3ящему
действию
ионной
атмосферьт
и
мож(ет бьтть
выра:кено
в
форме
коэффициента
€:1-
--1-
(1.в2)
е2х
3вА?
(1
+
{^
(
|
а^а)
({2
+
ах)
е2х
@,
тта
которь:й
т:еобходимо
умно}кить
правую
часть
урав}!ения
(1.58)
.
$роме
того'
и3
а|{тальции
обравования
дефектов
111оттки
в
соответ-
ствии
с
уравнением
(1.28)
следует
вычесть
ведичину хе2|е
[48,51|.

{
.
5. 0пределег1ие
тг
анс||ортнь!х
ковффит1иентов
Фшреде:тение
трансцортных
коэффициецтов'
т.
е. коэффициеЁ-
тов' входящих
в
транспортные
уравнения
(,!'.46),
(1.48)'
(1.50)'
(1.57)
й 1.
А.:
и3 эксперимептальных
даншых
составляет
достаточ_
но оло)кную
задачу.
?рудности
овязапь1
глав}!ым
образом
с
двумя
причипами:
с бодь1шим
числом
неизвест!{ых в
уравнениях
црово-
димости
и
диффузии
и с
отклонениями
свойотв
реальньтх
кристал-
лов
от
идеальпого
поведения'
предска3ываемого
атими
уравнения-
пли.
1ипичные
экоппериментальнь!е
ре3удьтаты
измереция
прово_
12
г,1
т0/г, "к-|
д:.1п[ости
г!риведень]'
на
рис:.
/-п.
!слтт
при
от1]ооитель110 вь]со_
ких томпературах
проводимость
ионного кристалла
довольно
близко следует
экспонепциаль_
}1ому
закону
(1.59)'
то 1]ри
по-
1{и)ке}!ии температуры
всегда
отмечаются сильные
отклонения
от него
(кривая
/).
3то
явлоние
овя3ано
о
пево3мо'кностью
аб-
солютной
очистки
кристалла
от
примесей.
Б самом
деле'
при
}{и3ких
темшературах'
когда
7/,
['0
'['
1,'/
!,
"
с
Ршс.-!'1|!!води1\{ость
мопокриотал-
равновеспая
концентрация
де-
лов
(€!
[72]
фектов
ре]петки
достаточпо
ма-
ла'
она становится
оравнимой
с
концентрацией
примесных
ио-
нов' которые
так)ке
мо}т(но
рас-
сматрйвать
как
дефекты
ре1|]етки.
{ем выше
содер)кание
цри-
месей в
кристалле'
тем
до
более выооких
температур
сказьтвает-
ся
пх
влия}тие
ца
проводимость
(кривая
2).
1!{еханизм
действия
примесой'
по-видимому'
сводится
к сле-
дующему.
|[усть
в криоталло
кс| содер'катся
ионы
5г2+.
3ти иопы
пРи''неболь]шом-их'с.одерж(ании
не
влияБт
на
структуру
кристалла'
а
образуют
твердый
раотвор
эамещеция, 1.
€. занимают
катион-
ные
у3ль1
в
ре1петке
хлористого
калия.
Б
силу
требования
электро-
нейтральнооти
ион
$г2+
долэкен
3аместить
два
иопа
(.+.
1аким
образом,
один
уаел;]катионной
решетки
оказывается
3апять|м'
а
оди}{
_
вакаптпым.
14ными
словами'
добавлоние
$г€1, в
1(€!
сопря'кено
с появлениом
эквивалентного
количеотва
катионных
вакансий.
|[ри
достаточно
пиаких томпературах
число
этих вакап-
сий
моэкет
намного цревысить
количество
(<собственных)
тешловых
вакансий.
]аким
образом, по
3ависимости
от темпора1урь|
мо)кно
вътделить
две
области ионттой проводимости:
собственную'
в
ко-
торой.!ереноо
вещества
осуществляетоя
тоцловыми
дефектами
ре|петки'
и
]несобствеп1!ую
(или
структурно-чувствительную)
об-
ласть'
в
которой
церенос вещества
ооущоствляется
дефектами,
цорожщецными
дримесными
иоцами.
30
!
_<<чиотьтй>
кс1;
9-кс]+6'1
.10-3
мол.
%
$тс],
Ёаряду о
влиянием примесей при низких
температурах
на
ве-
личину
проводимости могут оказывать
действие
и
другие
аффектьт.
}1аиболее
существовные'из них поверхноствая
проводимость
и
3амора)кивание
дефектов.
первый из этих эффектов
характере|1
для
поликристаллических
материалов. 3ерна
поликристаллических
образцов
для
и3мерения
проводимости'
цолученнь|х
при
затвер-
девапии
расплавов
или
прессованием
поро1шшков' имеют сильно
развитую
поворхность. Расшоло:кение
ио|{ов
в
поверхностнь|х
слоях
кристаллов 3аметно отличается
от их
располо'кения
в
у3лах
нормальпой
ро1|1етки'
поэтому энергия
активации
миграции в по-
верхноот}{ьтх
слоях
часто ока3ьтвается намного
мень1пе' чем
эпергия
активации
1миграции
в
о6ъеме
криоталла. 3то
ведет
к шшовы|пению
шроводимости по
грапицам зерен.
Роль поверхно-
стей могут играть
так'т(о
дислокации
и
различные
неоднородцости
в монокристалле.
|!оатому
при исследовании
овойств порепоса
наде}кшые
ре3ультаты
могут
быть полутень|
ли|пь на
хоро1по
сформированных'
оодер'1(ащих
минимальное
количество
дисло-
каций
монокристаллах.
_[вление замора?кивания
дефектов
состоит
в том' тто при
бы-
стром
охла'кдении
кристалла
к0личество
дефектов
при низкой
темшературе
мо'кет в течение
длительного
времени сохраняться
более
вьтсоким' чем
дол}кно
бьтть
при
равновесии.
|[ритина
этого
оостоит
в
медленности
установле}1ия
тецлового
равновесия
ре-
1петки'
для дости}кения
которого
вакапсии
дол}кнь|
продиффун-
дировать
на шоверхность
кристалла или
рекомбинировать
с меж(ду-
увельпыми
ионами
1.
Бсе
перевисленные
труд}{ости
привели
к тому'
что б6льп:ая
чаоть отарых экспериментальных
работ
шо определению
прово-
димооти
и
коэффициентов
диффу3ии
в кристаллах не 3аслуж(ивает
доверия'
а
полученные
ре3ультаты
11у'кдаются
в
реви3ии.
Более
наде}кные
даннь1е
получень1
в
основном
после 1966
г.,
когда Бомон
и
[:кекобс
[531
шредло'кили обоснованную
схему г!роведения
и3-
мерений
и математической
обработки
их
ре3ультатов
на 3Б]\4.
Б оонове
этого
цодхода леж{ит
обязательное
и3мерение
как соб-
ственной проводимости'
так и
проводимости
в присутствии
двух-
заряднь1х
катиовов
и коэффитциентов
диффузии
анионов.
Аруцч:
схема эксцеримента
бьтла
разработана
9андра
и Рольфе
|74,751
и
основана
на
и3мерениях
проводимости
чисть|х
кристаллов
и
кристаллов'
содер)т(ащих
добавки
иновалентнь1х
катионов
и
анио-
нов.
!,ля
тех
случаев'
когда
доминируют
дефекть:
1!1оттки,
проэ9.
димо'сть
в собственной области
определяется
уравнением
(1.57)
с
учетом
поцравок
(1.2в)
п
(|.62).
|[олозкепие
меняетоя
взщФ-
1
Бремя выраввивапия
концептрацип
дефоктов
мо'кет быть оценепо
с
по_
м6щью"фо!мулы
(1
.36), записайвой
в в,'де
'
-
[,2|Р-, тде !
_
лчтейный
раз-
мер'
крйсЁаЁла.
'||рй'
|
-\0-в
см2/сен
п
[
-
0'1,
сл
[
-
106
сек..,
т.
е.
-'12
суткам.
|!оэтойу
для
получепия
равновеснот}
коттцонтраг1ии
дефектов
!теобходимо
и3ме|тять
температуру
кристалла
достаточно
медлен}1о.
а1

ственной
области'
когда концентрация
примесей
доотаточно
ве_
лика.
|[олагая,
что примесь
шредставляет
собой
двухзарядньтй
катио1{'
поро}кдающий
одну катионЁую
ваканси}о'
а основныо
ионы кристалла
од}{о3арядны'
мо)кно представить
себе
два
оостоя-
ния парьт
т1римеснь1х
дефектов
((катион-вакансия\).
3 первом
состоянии
эта
пара
ассоциирована
в
нейтральный комшлеко.
3акомплексованнше
вакансии
не
участвуют
в
переносе
основных
катионов
кристалла.
3
диссоциированном
соотоянии ва]{ансия'
поро}кдепная
примеоью'
не отличается
от
тепловой вакапсии.
Ёоли
общую концентраци1о
примесных
катионов
обозначить
че'
ре3
7п'
а
ко!{цег!трацию
комплексов
_
череа $к, то в
силу электро-
нейтральности
|то
:
|ъ,
*
{,
-1**,
и.
испольвуя
3акон
действующих
маоо'
находим
-]*т
:!212*р
(#):1(,,
где [
-
коэффициент
активности'
выттисляемьтй
по
уравнениям
теории,(ебая-!,юккеля'
ц
л
х-
энтрошия
и энтальшия
образо_
вания
комшлекса'
ко
_
константа
равповесия.
[(оэффициент
<].2>
отра}кает
конфигурацион}тую
энтропию
комплексообразования
и
равен
числу
бли:кайптих соседей
в катионной
подретшетке
(вислу
ориентаций
диг{оля
примесь-ваканоия).
1еплпературЁую
зависимость проводимости
мо)кно
равбить
на
три
участка
(рис.
5). Фбласть высоких
темт{ератур
отвечает
соб-
ственной
проводимости (утасток
1).
|!ри
ни3ких температурах
преобладает
несобственная
проводимость'
причем
утасток
_
11
соответствует
миграции
овободньтх вака:тсий'
а
для
утастка
111
характерна
сильная
ассоциация
вакансий
с ионами примеси.
€ходная
ситуация возмо}к}{а
при
добавлении
в
кристалл
двух-
зарядных
анионов
(например,
ионов
6Ф}- в кристалл
((1).
|{ри
не оли1шком
больтших ко11!{ентрациях
добавки,
ко"да
ассоциация
пренебре:кима,
+:[(#)'*'1"
-(ж){#,
*:г(ж)'*,]"'-(й)
Ё#,
где
$:
ш'/,'
-
ехр
[(з'-
-
вт^)|||ехр
[-
(11'*-ь^)|ь?|,
(1.66)
о|
и'
б2
_
проводимости
кристаллов'
легированнь1х
двухзаряд-
пыми катионащи
и анионами
соответственпо'
о0
-
проводимость
чистого
кристалла'
/|п
!1 /2т1
-
концентрации
двух3арядньтх
ка-
тионов
и анионов ооотвотственъ|о'
1о
_
[1о
:
$ъо
-
ко|{це}1трация
ваканоий
в чистом кристалле.
Бсди
изморения проводятсд
в
9$,
38
(1.оз)
(1.64)
(1.65)
%'"*
'.,
//7
Рис.
5.
[арактер вависимости
металлов
ко'/'''
/,.7
/,'
/[ё/г,
"к'
т'|
для
гапоговидов
щелочпых
* //з
2а
/[0
|
19о7_
40
/0
Рис.
6. 3ависимость
констапты
:(9 от температуры
для
кристаллов
1(€1
с 5.10-2
мол'о/6 $г€1'
[74]
ласти'
где ассоциация примесей
существенна, то 4п2,4ф, п
с
достаточной
степецью точнооти получаем
о'т
:
щ#'[(
{
4&9п7,),/,
-
1]
ехр
(-
пт*:!т^т
)
,
(1.67)
причем
в
атих
условиях
дебаевский
параметр
находится
иа
урав-
нения
х2
:
4ле2
1(1
+
4&9оц)'|'
_
11/(в*||&).
(1.6в)
}}4опольауя
эти соотно1пения, 9андра
и Рольфе
[74,
75|
оцределиди
цараметры
миграции в 1(61,
1(Бг и 1(} с
добавками
5г61,
и
('[Ф3.
[хема
расчета
сводилась к следующему.
$ритерием
правильпости
ревультатов
слу}кила
миними3ация
функции
Р
:
!
[(19
о7)","
_
(|в
б?)р^",]',
(1.60)
где
(о?)рао,
получали цосле
подста}{овки
в
соотвотствующие
уравнения
найденных значепий энтроший и энтальпийлри'
данной
температуре.
Ёа первой стадпи
раочета
анали3ировали
о{
по
урав-
т{ецию
(1.67)
для
примесной шроводимооти кристадлов (см.
рис.
5,
облаоть
1|[)
и
вычисляли 7'^,
8''^
п
Ёо.
|рафики
1ъ
Ё,_7-т
(рис.
6)
отклоняютоя
от линейпости,
нто
обусловлено
дебай-хюккелевским
вваимодейотвием
дофектов.
||4з
хода
этой
зависимости паходили параметры
ц
и
х
в
соответствии
с
урав||епием
({.64).
3атом анали3ировали
ре3ультаты
измерений
проводимости'
отвечающие отсутствию
комплексообразовапия
(ом.
рис.
5, область
т'
.к
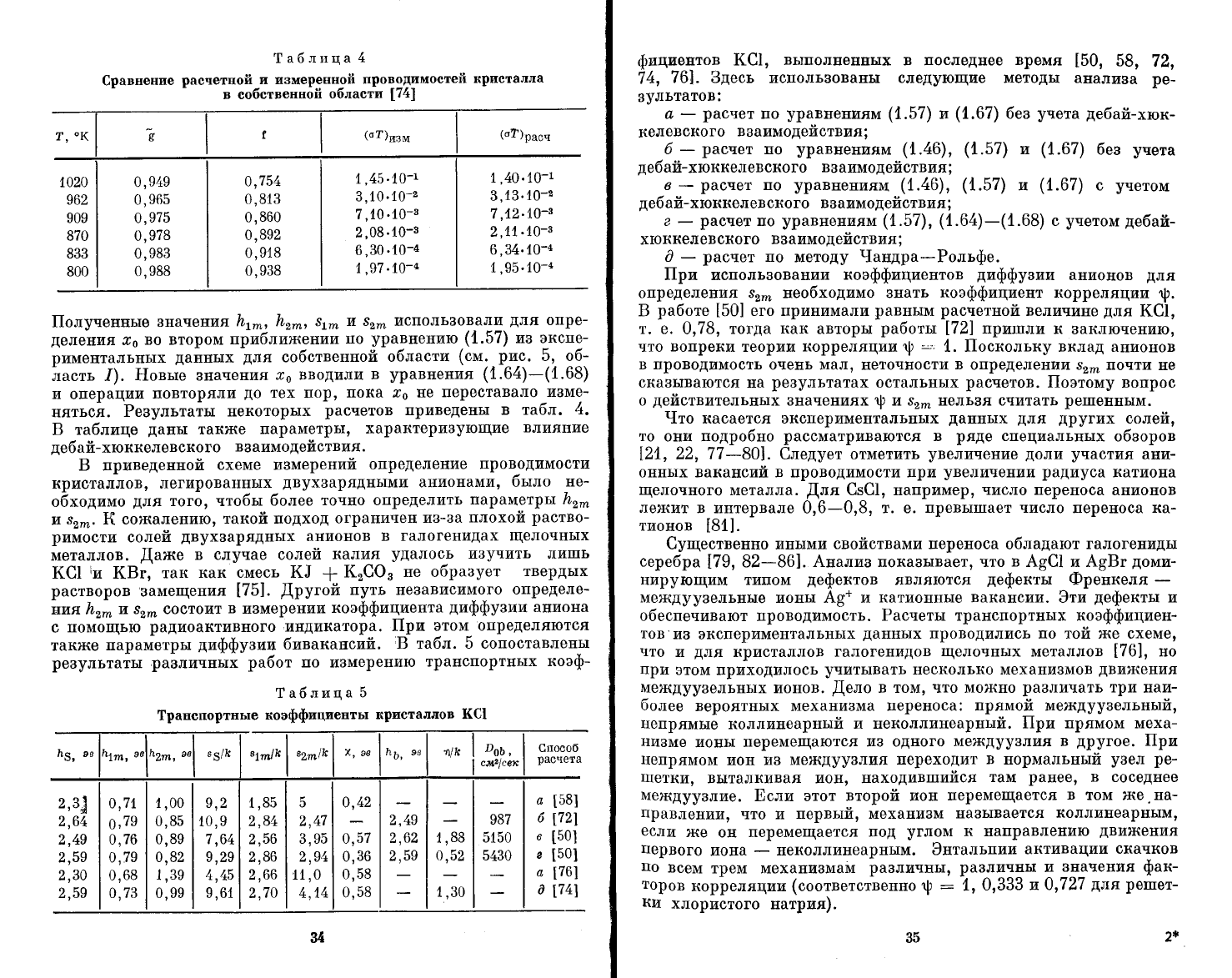
1аблттца
4
(равненпе
раочетпой
и измеренпот!
проводимостей
крпсталла
в собственной
облаетп
|74|
('?)изм
('?)раоч
1020
962
909
870
833
800
0,949
0,
965
0,
975
0,978
0,983
0,
988
0,754
0,813
0,
860
0,892
0,918
0, 938
1,45.10'\
3, ! 0.
10-2
7
,
10
.10-8
2
,08.
10-3
6
,30
.
10-4
1,97.10-4
1,4о.\0-|
3
,1
3.
10-2
7
,72.10-3
2,\1.\о-3
6
,34.
10-4
{
,95
.
10-4
|[олунонныо
3начения
|'*, 7'*, 8!тп
у1 82тп исшоль3овали
для
оцро-
деления
30 во
втором
прибли}кении
1]о
уравнению
(1.57)
из экспе-
риментальтть|х
данных
для
собственпой
области
(см._р_и-с.
5'-
99
ласть .|).
Ёовые 3паче1{ия
,0 вводили
в
уравпения
(1.6{)-(1.68)
и
операции
повторяли
до
тех пор'
цока /0 пе
переставало
изме-
цятьс;.
РезультаБы
цекоторых
расчетов
приведены
в табл.
4.
Б
таблицо
даны
так?ке
цараме1ры'
характери3ующие
влияние
дебай-хюккелевского
взаимодействия.
Б шриведент{ой
схеме и3мерений
ошределение
шроводимости
кристаллов' легированных
двухзаряднь1ми
анионами,
бшло
не-
о6ходимо
для
того' чтобьт
более
точно определить
параметрът 7'*
!
8я^'}( соэкалению'
такой подход ограничен
и3-за
плохой
раотво-
римости
солей
двух3арядных
анионов
в галогенидах
щелочных
металлов.
[а;тсе
в случае солей
калия
удалось
и3учить ли|пь
1((1
!и
(.Бг,
так
как смесь к]
+
к2со3
не образует
твердых
растворов
замеще11ия
[75|.
[ругой
шуть Ёезависимого
определе-
нляп2п
и 82'? оостоит
в
измерении
коаффициента
диффузии
аниона
с
шомощью
радиоактив}1ого
индикатора.
|[ри атом
определяются
так?ке
параметрь1
диффузии
бивакансий.
]Б
табл. 5 оошоставлены
ре3ультаты
ра3личнь1х работ
по измеревию
траЁот!ортных
коэф-
1аблица
5
1рапопортньто
коэффишиепть!
кристаллов 1(61
}г5, эв
в!п|к
1\/к
!оь,
см2|сех
споооб
раочета
а
[58!
6
\721
с
[50]
а
[50]
с
[76]
о
|74]!
2,3А
2,64
2,49
2,59
2,3о
2,59
0,71
0,79
0,
76
0, 79
0,68
0,73
{
,00
0,85
0,89
0,82
1
,39
0,99
9,2
10,
9
7
,в4
9,29
4,45
9
,61
1
,85
2,84
2,56
2,86
2,вв
2,70
5
2'1+7
3,95
2,9/+
11,0
4,14
0,42
0,57
0,36
0,58
0,58
узэ
2,в2
2,59
1ъ
0,52
1
,30
й'
5150
5430
\,
ов
|76'
эв
34 35
2*
фициентов
кс1,
выцодненных
в последнее
вромя
[50,
58,
72,
74,
761. 3десь ио1]ользовапы следующие методы
анали3а
ро-
3ультатов:
а
_
расчет
по
уравненлям
(1.57)
п
(1.67)
без
утета
дебай-хюк-
келевского
в3аимодействия;
б
-
раснет
по
уравнениям
(|],.46),
(1.57)
и
(1.67)
без
утета
дебай-хюккелевского
взаимодействия;
6
_
расчет
по
ураввениям
(7.46)'
(1.57)
л
(1.67)
с
учетом
дебай-хюккелевского
в3аимодействия;
а
_
расчет
по
уравнениям
(1
'57),
(1.64)-(1.68)
с
учетом
дебай-
хюккелевского
вааимодейотвия;
0
_
растет
по
методу 9андра_Рольфе.
|[ри использовании
коэффициентов
диффузии
анионов
для
ошшр0делени$ 8я* пообходимо знать
коэффициент корреляции
ф.
Б
работе
[50]
его цринимали
равньтм
растетшой
величице
для
1((1,
т. е.
0,78,
тогда
как
авторы
работьт
[72|
пришли
к
3аключению'
что
вошшреки
теории
корреляции
ф
-.
1. |[оскольку вклад а}1иоцов
в проводимость
очень мал' неточ}{ости
в
определении $2??? почти
не
сказываются
на
ре3ультатах
остальнь1х
раочетов.
|!оэтому
вопрос
о
действительных
значениях
ф
и ы'- нельзя считать
ре|пенцым.
9то касается эко11ериментальць1х
даннь1х для других
солей'
то
они подробно
рассматриваются
в
ряде
сшшециальных
обзоров
12!,22,77_80].
[ледует отметить
увеличенио
доли
участия
ани-
онньтх вакансий в цроводимости цри
увеличе}{ии
радиуса
катиона
щелочного
металла.
,(ля
(з€1,
например'
число пере}1оса
аниопов
ле}кит
в интервале
0,6-0'8,
т. е.
превы1пает число
переноса
ка-
тионов
|81].
6ущественно ипыми
свойствами пероноса
обладают
галогепиды
серебра
[79,
в2-в6].
Анализ пока8ывает' что
в
А961 и А9Бт
доми-
нирующим тицом
дефектов
явля]отся
дефектьт
Френкеля
_
ме)кдуузельные
иоць| А8*
"
катионнь1е ваканоии.
3ти
дефектьт
и
обесцечивают проводимость.
Расчетьт трансцортных коэффициен-
тов'ив
экспериментальнь]х
даннь|х
цроводились по той }ке схеме'
что
и
для
кристаллов галогенидов
щелочных
металлов
[76],
но
при
этом приходилось
учить1вать
несколько механи3мов
дви)кения
ме}1{дуузельнь1х
ионов'
,(ело
в том' что мо)т{но
ра3личать
три
наи-
более
вероятнь!х механизма
переноса: прямой ме}1(дуузельный'
непрямые
колдинеарный
и неколлинеарнь1й.
|{ри прямом меха-
низме
ионы
перемещаются
и3 одного
ме}т{дуузлия в
другое.
|{ри
|{епрямом
ио}{ и3
ме]кдуузлия
переходит
в
]{ормальный
узел
ре-
1петки'
выталкивая ион' находивтллйся
там
ранее'
в соседпее
ме}кдуу3лие.
Бсли этот
второй ион
перемещается
в
том ж(0.на-
правлении'
что и
первый' мехаци3м
на3ывается
коллинеарным'
если
)ке
он
перемещается
под
углом
к направлению
движ(е11ия
первого
иона
_
неколлинеарным.
3нтальции
активации
скачков
по
всем
трем мехапизмам
различны' ра3личвы
и
зчатения
фак-
торов
корреляции
(соответственно
ф
:
1,
0,333
и 0,727
для
ре]пот-
ки
хлориотого
натрия).
гв3,в4!
!
.вб!
1,55
|
1
,4в8|
7,48
}а.^ (лр.),
эв
!
_
0,27
'о,2881
1,о4
о,о1
!о,о48!
0,63
в'*/Ё
|_1
,19
0,13
!о,688!
2,02
з,-[с
(нк.)
!
_
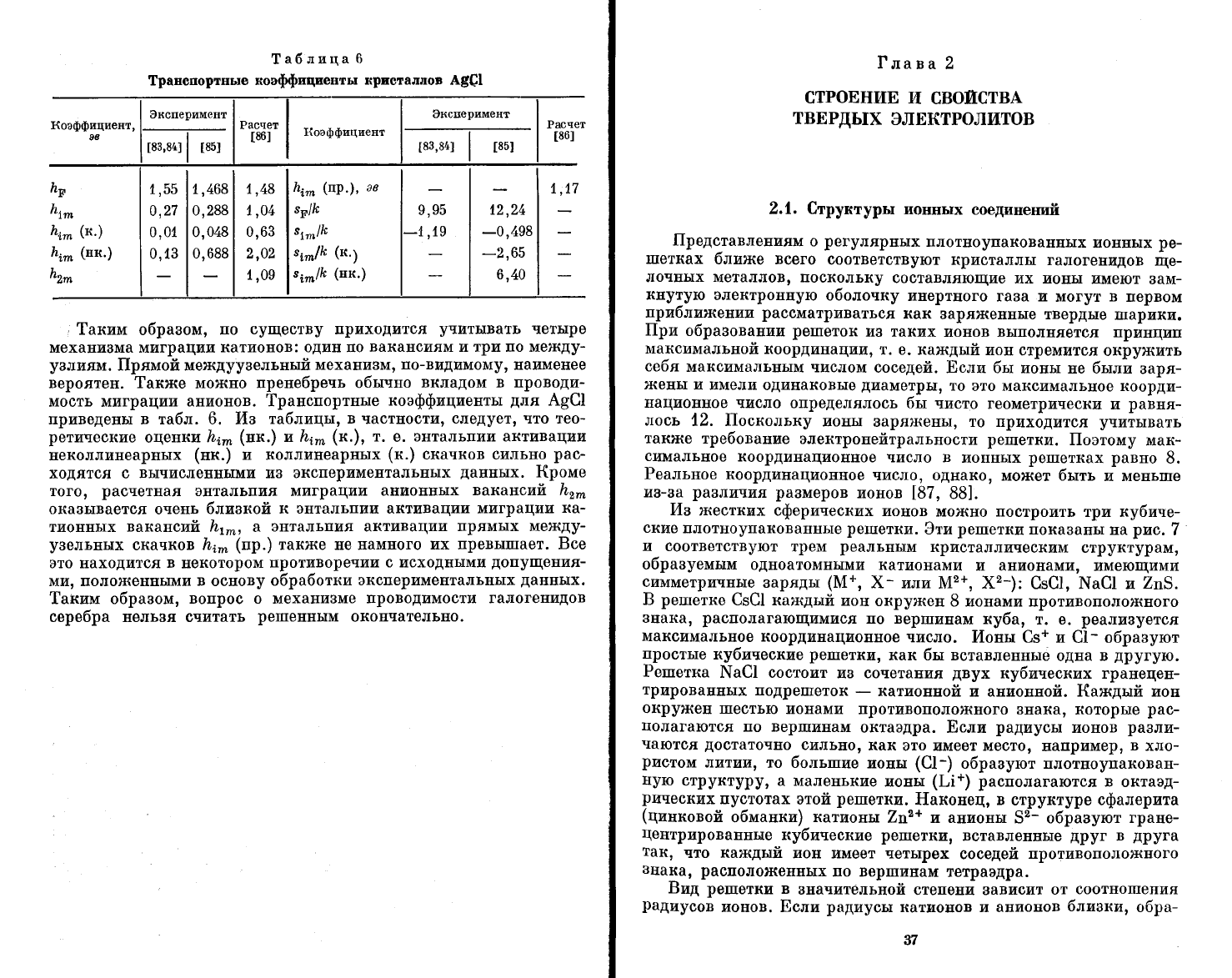
[абдица
6
!рапопортпьте
коо([фпцпе1|ть|
крпоталлов
А$$[
экспер!!мецт
Раочет
|86!
ковффициеят
Ёоаффициент'
ов
п1
||:^
]'о^
(*.)
1т,^
(нк.)
112^
{&3,в4]
|
ш,:
1,77
,1аким
обравом,
по
существу приходится
учитывать
четыро
механи3ма миграции
катионов: один по
ваканоиям и три по ме}кду-
уалиям.
11рямой мо'*{дуузельный
механи3м'
по-видимому'
наимонее
вероятен. 1ак:ке
мо'кно
пренебречь обычно
вкладом в проводи-
мость миграции
анионов. ?ранспортные
коэффиционты
для
А9(|
приведены в табл. 6. }[з
таблицы'
в
частности'
следует' что тео-
ретические
оценки
74*
(нк,)
л 7;^
(к.),
т.
е.
энтальпии активации
пеколлинеарных
(нк.)
и коллинеарных
(к.)
оканков сильно
рас-
ходятся с
вь1численными из эксперимептальных
дан11ых.
}{роме
того'
расчетная
эптальпия миграции
анионнь1х
ваканспй 7'^
ока3ываетоя
очень
близкой
к энтальпии активации миграции
ка-
тионнь1х вакансий |у*, &
энталь11ия активации
прямых ме}1цу-
у3ельных
окачков /',*
@р.)
так)ке не намного
их превь11шает. Бсе
ато 1{аходится
в
векотором
противоречии
с исходными
доцущепия-
ми' поло'кеппыми
в
основу
обработки
экопериментальвь1х
да]{ных.
1аким образом,
вопрос о механи3ме
проводимооти галогепидов
серебра нель!}я считать
ре111опным
оковчательцо.
Р
лава 2
стРовнив
и
своиствА
твшРдь]х
элпктРолитов
2.1. €труктурь1
|(о!|шь|х
соединений
.|!редставлешиям
о
регудярньтх
плотноупакованпых
ионных
ре-
|петках
блиэ*се всего
соответствуют
кристаллы
галогепидов
ще-
лочпых металлов' поскольку
соотавдяющпе
11х ионы
имеют
3ам-
кпутую
эдоктронную
оболотку
ин0ртпого
га3а и
могут
в
первом
приближсонии
рассматриваться
как
заря}кенпьте твердь1о
1парики.
[1ри
образовании
ро1петок
и3
таких ионов выцолняется
цринциц
максимальной
координации'
т. е. ка2кдый
ион
стромится
окру}кить
себя
максимальным
числом
сооедей.
0сли бы ионь1
не были
заря-
,*(ены
и имели
одинаковые
диаметры'
то
это максимальное коорди-
11ацион}{ое
число
опроделялось бьт
чисто
геометрически
и
равня-
лооъ
!!,2.
|[оскольку
ионы
заря?т{ень|' то приходится
учитывать
так)т(е требование
электропейтраль1{ости
ре|петки.
|[оэтому
мак-
симальноо
коордицационное
число в
ионных
ре1||етках равно
3.
Реальное
координациоп!{ое
число' однако'
мо}кет быть
и мень1пе
и8-ва
различия
ра3меров
ионов
[87'
в8].
]]{з
зкестких сферинеских
ионов
мо)кно построить
три кубиие-
ские
пдотноушакованные
ре]петки.
3ти
решетки
показапьт
на
рио.
7
и ооответствуют
трем
реальным
кристалличоским
структурам'
образуемым
од11оатомными катионами
и анионами'
имеющими
симметричные
3арядьт
(м*,
х- или\,,[2+,
{,2-):
(в(|,
1'ц[а61 и
2п$.
Б
реш:етке
(в(1
каэтсдый
ион
окру}кен
8 ионами противошоло'*{ного
знака'
располагающимиоя
цо вер1шинам
куба,
т.
е.
реаливуется
макоимадьпое
координациоп11ое
чиодо.
[оны
(в+
и
(|-
образуют
прооть!е
кубинеские
ре1петки'
как бы вставленные
одца
в
другую.
Решетка
}[а€1 состопт
л8 сочетапия
двух
кубичеоких граноцеп-
трированных
подре|петок
_
катиовпой
и апиошпой. }{аэкдый иов
окру'кен
1шшестью
ио}1ами
противополо}1{ного
зпака' которые
рас-
шолагаются
шшо
вер|шинам
октаэдра. Ёсли
радиуоы
ионов
равли-
чаютоя
достаточно
оильдо'
как
это имеот место'
папример'
в
хло-
ристом
лу1'!!лу!,
то большио
ионы
(61-)
обраауют пдотноупакова!{-
пу1о
структ}Р}, а малонькие
ионы
([!+)
расцодагаются
в
октаэд-
рических
пуототах
этой
ретпетки.
}1аконец' в
структуре сфалерита
(цицковой
обмапки)
катионы
7п2+ л апионы
52_- образуют
гране-
центрировапные
кубитеокио
ре|петки'
вставленныо
друг
в
друга
так'
что ка:кдый
ион имеет
четырох
соседей
цротивоцоло}кпого
зцака'
располо'кенных
по вер1пинам
тотраадра.
3ид
решотки
в
8начительной
степопи 3ависит
от
соотно]!]ения
радиуоов
ионов. [сли
радиусь1
катионов и аниоцов
близки,
обра-
37

.с51осг
.
ш0]осг
.7п?:о
52'
Рпо.
7.
Ёристалливескио
решотки
€з€1
(а),
}.{а€1
(6)
и
7п$
(а)
Рис. 8.
Располоясение
у3лов
и
1\{е)|{-
дуузлий
в кубитеских
ре11{етках
3уотся
ре1петка
(в(|
с
макоимальной
координациой'
3
этой
ре-
1петке
криоталли3уются
так)ко
(вБг
и
(в}.
Бсли^р14иуо
а}1иоца
существен}{о
шревь11пает
радиус
катиона'
ре|петка
[в61
становится
неустойтивой,
потому
что
полость,
образуемая
пдотноуцакован_
ными
анионами'
сли]шком
велика
для
катиона'
Б
атом
сдучае
образуется
ре|петка
1\а[|,
характщн.ая
для
всех остадьных
гало-
гецидов
щелоч]1ь|х
'е'ал1о"
_
от
(вР
до
!1].
4р"
еще
больтшем
ра3личии радиусов
она
так}ке
становится
нестабильной
и
шерехо-
дит
в
ре|шетку
сфалерита.
Фбьтчно
снитайт,
ито
решетка
(з[1
устойнива
до
отно]ше|{ия
,,дйй.']
г-7г*
ч
1,37,
р!-"'к*
1\а[1
-
в интервале.
1'37
<
ч?}-7'*
<[,ц4,
!'
р.-е'й^
сфалерита
лри
г-/г*>,=2,44'
Фднако
в-дейотвительности
даж{е
для
галоге!{идов
щелочнь1х
металлов
это
правило
не
является
совер1пенно
строгим'
11ри
пагревании
6в€1,
}ашример'
шшри 469'
с
[роисходи'т
пе-реотройка
структурь1
и
ион,,
св*_и
61__
образуют
ре1шетку
\а(1.
11ринина
этого
явлеция'
по-видимому'
соотоит
в том'
что
шри
увеличонии
температуры
уведичивается
амшлитуда
топдовьтх
колебаний
тастиц,
нто
ведот
к
1{екоторому
ра3рыхлет{ию
упаковки.
|1оскольку
ра3упорядочивание
кристаллических
ре||1оток
свя-
за11о с
образова!ием
в6кацсий
и меэкдуу3ельных
ионов'
для
овойств
структурь1 ва)+(но
не только в3аимное
расцоло}кение
нормальпых
у3лов'
!{о
тат{?1{е поло}кение
и координат]ия
меэкдуузлий.
Ёа
рис.
8
38
39
1аблица
3аполнеппо п
коордпнация меот
в
1
кубишеских
реш|етках
Ёатиопы
Апионы
1\{еэкдуузлия
а1(662, 12а',
80'1
0{6а2, 7202,8а')
а2(20'462,4а$а2,862)
02(2а$а2,40'802,8а2)
66' 12а)
6ё' |2с1
6а' 126)
6с'
12с1)
и
в табл.
7
даны
характеристики
трех
типов кубитеских
р0шеток.
Б
таблице
ука3аны
занятооть мест а, 6,
с, 0', а так)ке
количество
и тиц
их ближсайших соседей
в
трех
сферах координации
(в
скоб-
ках).
14ндекоы
1
и 2 иололъзованы топько
для
структуры
(з(1.
Б
ретпетках
7п3 и [в(1
имеется по
два
сорта ме'т(дуузельнь1х
шшо-
зиций с
равличной
координацией.
даннь1е'
приведенные в табл. 7
и на
рис.
3,
повволяют оценить характер ближсайшего окру}кения
ка:кдой
структурной единицьт. Б
ретпетке
1\а[1, например'
катио-
ны аапима1от все
узлы
о октаэдрической
координацией,
т.
е.
ка:к-
дьтй
катион в
узле
1ппа
о окру]кон
1пеотью анионами
в
у3лах
типа
},
находящиму1ся
в
вер1шинах правильного октаэдра.
9исло
ме'кдуу3ольцых шозиций вдвоо превы1пает
число }1ормальнь|х
узлов.
Фни
имеют тетраэдричеокую
координацию' т. е. окру}т{ень|
четырьмя катионами
(или
тетырьмя
анионами),
раополо)т{еннь!ми
в вер1пи}1ах
правильного
тетраэдра.
в
реш1етке
типа
(з(1
кристаллизуются
такж(о
соединения
таллия (т|с1,
11Бг,
1|}), хотя
радиус
иона
т1+
(1,36
А)
близок
к
радиусу
к+
(1,33
А).
Фднако
в этом случае ионьт
]1
+
име]от
алектронт1ую
оболовку'
отличную от замкнутой оболочки
инерт-
ного гава.
1акио
ионы
у'ке
нель3я
рассматривать
как
}кесткио
3аря}кенные сферы, а овявь в
криоталлической
решетке
имеет
в
значительной стоцени ковалентпый характер.
Блияние электрон-
ной оболочки ска3ывается л
на свойстБах
солей
серебра и
меди.
(оли
А9Р,
А9[! и А9Бг
криоталлизуются в
ре1потке
$а[1.
Фднако,
как
у)ко
говорилось,
в
отличие от
щелочных
галогенидов'
их
ра-
вупорядоченность
овя3апа о
шшереходом
ионов
А8* , ме}1{дуузель-
т1ь1е
полож{ения
(с
обравованием
дефектов
Френкеля).
!!{одистое серебро при комнатньтх температурах
существует
в
двух
кристаллических модификац1лях1
у-и
$-А3}.
Фаза
т-Ав]
имеет
структуру
сфалерита
(4инковой
обмапки).
3ту
ретшетку
мо?кно
представить как плотноупакованную
кубивескую
отруктуру
ионов
)_.
}{атионьт А9*
располагаются
в тотраэдрических
пусто-
тах
структурьт
-
ка;кдый катион
окруж{ен
четь1рьмя
анионами.
14меется
еще
такое }ке количество
тетраэдричеоких
пустот' оста1о-
щихся
не3анять1ми'
Ё{роме того'
в
аниопной
упаковке
имоются
|
а@аа'
60,
\2а)
|а(с4а,
|ь6'а,а,
6а,
126)
|с(п&ь,
|
,(а'+ь, 6а(с).
12с@)|ь6'+а
'
|
а(+'аь
,6а(с),
12с@))
|а1а'+ь
,
!!

пустотьт
с
октаэдрической
коорди1{ацией
и
чиоло
их
равно
числу
сЁободных
'е'р'эдр",еских
''ус'от.
[толь
рь1хлая
упаковка
обес_
печивает
сравнительно
вь1сокую
шодвижсность
иопов
А9+
[89,
90!.
[1ри комнЁтной
температуре
шроводимо-сть
т-А8]
достигает
10-6,
,
,р" 120' с-10-ц
ой-1.с7_'
1рпо.9).
9то
касаетсямодификации
р-Аа]'
то
она имеет
ре!шетку
вюрцита'
в.которой
ионы
|-
образу1т
гексагонал,"у'
,'''1,ейштуБ
у,аковку
(координационное
тисло
4).
|{роводимость
$-А9}
при 11и3ких
температурах
на
порядок
ни'ке'
тем
уА3}.
[алогеттиды
меди'
как1и
А9},
кристалли-3уются
в
ре!пот-
ке
сфалерита
1.
Бследствие
-4
Рис.
9.
|[роводимость
иодиотого
се-
ре6ра
при
40
нец
с
угольными
элек-
тродами
[90]
..-т_фаза;2_р-фаза
1'6
с
(агг/.
сп1)
,1,[
дз/4
"6-т
1
[оодпнеттття
одновалонтт1оЁт
птеди
|{ительно
высокой электронвой
сильной
поляри3ации
ионов
в
А8],
(шР,
[п(1,
[цБт
и [ц}
связь
в
этих
соедине}{иях
носит
шреимуществонно
гомеополяр-
пый'
а
не ионньтй
характер.
!,ля
ооединений
типа
м'*х;
поло)кенио
еще
более
усло?т(-
няется.
)(арактернь1ми
ре1шет-
ками'
отвечающими
цринципу
плотной
ушаковки'
в этом
слу-
чае являются
ре|шетки
флтоори_
та
(рис.
10)
и
рутила.
Ретпетку
флюорита
(аР,
моэкно
шолучить
и3
гранецентрированной
кати-
опной
ре|шетки'
ра3граничив
ее
на
8
кубиков.
1аким
образом,
кажсдьтй
катио}{
коордиширует
3
аниоттов,
расцоло)кеннь1х
во-
круг
него
по
вер1пинам
куба,
при
комнатной
температуро
обладают
срав-
проводимостью.
цо
2,,
а
кажсдьтй
анион
окру'кен
че-
тырьмя
катионами'
расшолагающимися
по
вер|пинам
тетра'
эдра.
Б
реш1етке
рутила
11Ф,
коо^рпинационнь]о
числа
катионов
и анионов
равнь|
соответственно
6 и
3.
т{ак
и
в
случае
р0шеток
тиша
[:[{,, структура
кристаллов
типа
1\4)(,
3ависит
от
радиуса
ионов:
шри
ув0личении
отно1пенпя
|-!
г
+
цони}кается
координациоп-
ное
число.
Б этих
ре|шетках
кристалли3уются
мт1огие
окислы
и
фторидьт,
"',р'"ер,
€6Р',
(шР',
Рьв'2,
7сФ,
_
в
ре|петке
ф"тюо-
рита,
а
й8Р',
(оР',
}'[|Р',
7пР,
_
9_Рщетке_.рутила'
00ра3уются
так}ке
ре|шетки
типа
антифлюорита
(ь12о, 1('Ф),
в
которых:сатионы
" '''''?'как
бы
цоменялись
местами
по
сравнеЁию
с 6аР''
|[ри
наливии
заметной!гомеополярности
оъя3п
соедипения
типа
$!,''образуют
слоист'.
р"-е'*и
(рис. 11)
типа
60},
и са^с12'
3ти"струк'ур"'
,''у.''ются
нало}1(ением
ряда
пакетов,
ка:кдый
из
которых соотоит
из олоя
катионов'
заключенного
ме}т|ду
двумя
слоят||и
сильно
поляри3ованпых
анионов.
1акую
ре1петку
мо)т(по
'--.
-.1,'-!-
,-,\)
|х]
-,}#{\,
*1,,,:,'^']
)
){Ё-.,эФ-,'
Ф
са'',!
г_
1у,7а,,03-
Рпс.
10. €труктура
флюорита
Рпо.
11. 6труктура
(0},
Рпс.
|2.
[труктура
перовокита
0л,.8,
@о
отчастй
рассматривать
как молекулярную'
составлепную
и3 ори-
ентировапнь1х
полимери3ованных
молекул
са,2,
образующих
пакеты.
Бнутри пакетов
свя3ь преимуществонцо
ионная' а ме'кду
пакетами
действуют
главным обравом
ван-дер-ваальсовы
силы.
|[роводимоотъ
и'
диффузия
ионов
в этих
криоталлах
цракти-
чеоки
т{е иоследованы. }[звестно, что
электроцроводность
поли-
кристаллического
хлористого кадмия'
например'
вблиаи темпе*
ратуры
плавления
(568"с)
достигаот
0,{1
о;ш-1.см-|. 0нергия
активации
цроводимости
составляет
{,03
эв
|7в\.
}1змерялись
ко-
эффициентьт
диффузии
[1_-ионов
[91],
по
точность
атих измерений
неволика.
1!1оэкно о)т{идать
силь1{ую
анизотропию
проводимости
таких
криоталлов.
Фднако,
неясно'
мож{ет
ли
происходить
ра3у-
порядочивание
катионов' оошрово}т(дающееся
их локализацией
ме'кду
цакетами.
(лоистую
структуру
имеют
так)ке 1!19(|', [о[1',
[п€1з,
1\:[9}2
и
другие
соединевия.
41

Бще более сло)кные ситуации
могут во8пикать шшри кристалли-
3ации
многоатом!{ых соединений
_
двойньтх
солей, солей
кисло-
родн|,1х
кислот
и т.
11.
3десь
]!1ь1 отмотим
две
распространеннь1е
структуры
-
структурь1
1]еровскита
и |шпинели. [труктура
перов-
скита
отвечает
соотаву Аво3 и имеет кубитескую элементарную
ячейку'
показанную
на
рис.
72. |4онът А
располо;кень1
в вер111инах
куба, ионы Б
-
в
центре
куба, а ионы
кислорода
_
в
ц0нтрах
грапей. $азкдьтй
катион
А окру:кен
двенадцатью'
а катион
3
_
]пестью
иоЁами
кислорода. Ё[а:кдый ион
Ф2- окруж{ен
четырьмя
катионами А и
двумя
катионами Б. Б структуре перовскита кри-
сталлизуются' [а1!Ф', 1\а[Ф3, }{а1аФ', !(\:[9Р3, 1(}Ф3 и 1.
[.:
причем места А с б6льтпим
коорди}{ационным числом
вашимают
катионы
б6льплего
радиуса.
(труктура
шшеровскита
на
шервьтй
в3гляд
сходна с
другиш'и
плотнь1ми структурами' однако она обладает одной
3ап{ечатедьной
особенностью
-
она ]\{о)кет образовьтватьоя с любой парой
ка-
тиоцов' еоли их суммарцая
валент!]ость
рав}{а
6. 71ндивидуаль1{ь1е
3арядь1 и точ]{ое
распределение
катионов в
ре]петке
имеют
второ-
степенное 3наченио
-
некоторые
катионь|
могут
да'ке
оовсем
отсутствовать
в
структуре' есди только
вьтцолняетоя
требование
электронейтральшости. ||римером мо}т{ет слу)кить натрийволь-
фрамовая
бронза 1\а'\{Ф'. Реальный
состав
бронзы мо)кет
ме-
няться
в ]пироких пределах. |{ри нехватке
натрия
(*
<
1)
часть
}{атриевых
мест
остаотся
цезанятой, а недостаток поло)кительного
заряда
комценоируется
переходом ио}1ов
вольфрама
из состояния
\[6+
в
86+.
|[ри ни3ких
содер}каниях
щелочного
металла
(п
1014|
ре|петка
бронзьт иска)кается' во3никает так на3ываемая тетраго-
цальная структура: соединенньте
углами
октаэдрьт
[Ф6
образуют
каналы'
в
которых
располагаются
ионы шатрия
[921.
,(ругим
ва}кным
примером
слон{ных
ре1петок
является
1ппит{ель
Ав2о4.
3лементарная ячейка
ш111инели содер}кит
32 иона
кислоро-
да,
8
катионов
А
и 16
катионов
Б. $аэкдый
ион А тетраэдрически
коордипировав
четырьмя' а ион 3 октаэдрически
координирован
|]]естью
ионами
кислорода.
3
свото очередь ион
Ф2-
коорди1{ирует
1 ион А и 3 иона 3. Фбьтчно
А
двухвалентньтй
металл' а Б трех-
валентный,
однако'
как
и
в структуро перовскита' здесь
ва)т(ен
лишь
общий заряд
катионов'
обосцечивающий
нейтральность
структуры в
ц0лом.
|[оатому
в структуре 1шцинеди наряду
с
\.{9А1'Ф*
кристалли3уются 7пА\'Ф',
6оА1'Ф*, ш|А12о4,
\4пА|'Фд
и соедине1{ия тица 1|\.{9'Ф*,
\{оА9'Ф*.
Б
некоторых
|шпипельпых
решотках
(так
называемыо
обращенньте 1пцинели) лишь часть
ионов Б
находится
в тетраэдричеоких местах' а остальная часть
вместе
со всеми
ионами
А
распроделена
статистически
по окта-
эдричеоки
коордипированным местам.
$
тислу таких 1ппипелей
отнооятоя'
например' \.{96а'Ф* и 1|[:[9'Ф..
,{ругой
тип тшпилтелей
образует
!!А|6ов, где
11ара
ионов А2+
в
А2в4ов 3аменена
на
!1+
и А18+. Ёакопоц, в
магниевой шпивели \:[9А1'Ф, мо)*{!{о
цостепонно
3амещать
ионьт 1\{92+
на парь| кА}8+
1вакансия))'
получая
твердые
растворы
\{9А1'Ф.
+
А12о3.
Б
конечном счете таким
путем
мож{по
прийти
к
ре|шетке у-А1'Ф3,
имеющей пп!пивельную структуру.
2.2.
Разупорядоче|{|{ь]е структурь|
]аким образом, паряду
с плотпыми ионными
ре|петками'
от-
веча]ощип{и
моделям Френкеля или
1!1оттки'
реальнь!е
кристаллы
}|огут
образовьтвать
дефектные
отруктурьт. 6уществу1от
две
прин-
ципиальные
возмо)кности
во3никновения
дефект1;ь|х
структур:
беопорядотное'
статистическое
распределение
двух
ра3ных
тишов
ионов
по эквивалентным
у3лам
ре]цетки
(например, обращенная
лппинель)
и частичное заполнение
у3лов
ре1петки
(твердые
раство-
рьт
1\49А1'Ф1
+
А1?оз).
(труктурьт
первого типа носят название
дефектньтх
структур с 3авер1шеннь!ми
ре]петками'
а
второго типа
-
дефектньтх
структур с незавер1ше1|}|ь]}!и
ре|петками.
Бакантньте
у3лы
в
дефектттьтх
структурах 1\{огут бь;ть
распределень!
в
опреде-
лен]1ом
порядке или статистически
переме|пань1 с
аанять!ми.
}}1[менно
соединения последнего типа'
т. е.
разупорядоченные
дефоктные
структуры
с
1{езавертшеннь|ми
реш]етками'
которь1е
для
краткости мьт будем }1азывать
просто
разупорядоченными
струк-
турами'
проявляют необьтчно
вь!сокую ио1{ную проводимость'
т. е. являются
твердыми электролитами
в собственном
смь!сле этого
термиЁа. Б
данном
ра3деле
коротко
рассматриваются
и3вестпые
в
настоящее
время соединения, обладающие
ра3упорядоченпь1ми
ре1петками.
[оедшнедия на основе
2гФ'.
Бпервые
бьтла обнару:тсена
высокая
иоц}1ая
шроводимость
у
окиси
циркония
[51.
||ри ни3ких
темпера-
турах 7тФ,
кристаллизуется в плотной моноклинной
структуре,
которая
при
1100'(
переходит
в
тетрагональ}тую.
||ервая и3 этих
фаз
является
алектроннь!м
полупроводником' а
вторая обладает
небольтпой
смеш:анной электронно-ионной
проводимостью.
}1о при
добавлении
к
7тФ2 некоторь1х
других
окиолов' }1апример
[аФ
[93]'
и
при
нагревании
до
1000-1100'
(
вмеото
тетрагот{альттой
модифи-
кации образуется структура
флюорита.
14оньт
(а2+
и
7тц+
разме-
щепь1
по
катионнь1м
местам
ре1шетки
статистически'
а нехватка
3арядов'
обусловленная
тем) что валентность
кальция вдвое
мень-
|пе' чем
циркония'
компе|{сируется
наличием
вакантньтх
ат{ион-
ных
у3лов'
число
которых
практически
равно
числу ионов
са2+.
1акая
структура. ока3ь1вается
стабильной
в ограниченном
интер-
вале
конщентраций
(аФ
(-
|0_20 мол.%).
|[ри температурах
ниэке
900-1000"
с
в системе
происходит
пероход типа
(порядок-
беспорядок))'
т. е.
разупорядоченная
вь!оокотемпературная
фаза
переходит
в
упорядоченную
ни3котемпературную с б6льшим
удельнь1м
сопротивлением.
3тот
аффект извеоте}т
как
((староние))
твердь|х электролитов
на
основе
двуокиси
циркония
194-96].
|[роводимость
флюоритной
модификации 7тФ',
рааумеотся'
вависит от
концонтрацпи
€аФ и макоимальпа
при содоржа1{пп
42
&в
