Сартакова О.Ю. Промышленная микробиология
Подождите немного. Документ загружается.

51
Схема состоит из стадий, в каждой из которых сырье пре-
терпевает определенные технологические воздействия и последова-
тельно превращается во все более сложные полупродукты и, наконец,
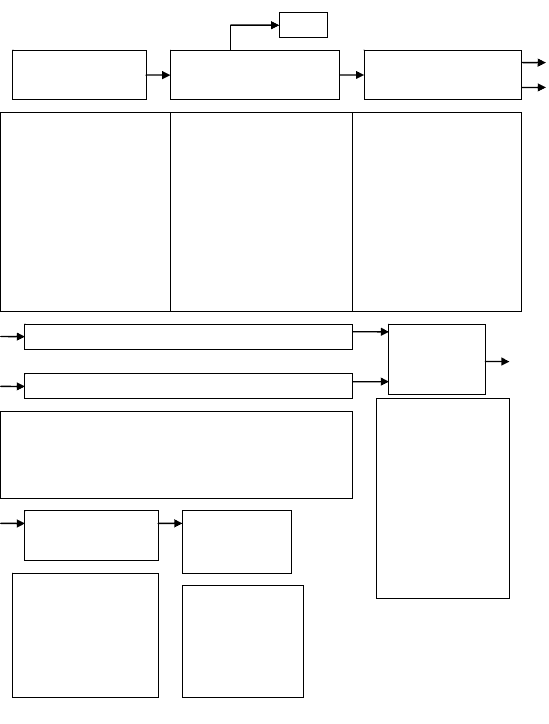
в конечный продукт. Общий вид такой типовой схемы представлен на
рисунке 16.
Подготовительные
стадии
Биотехнологические
стадии
Разделение жидкости и
биомассы
Приготовление
среды
Стерилизация среды
Подготовка и
стерилизация газов
(воздуха)
Подготовка посевного
материала
Приготовление
биокатализатора
Предварительная
об
р
аботка сы
р
ья
Ферментация
Биотрансформация
Биокатализ (реакции с
ферментами)
Бноокисление
Местановое брожение
Биокомпостирование
Биосорбция
Бактериальное
выщелачивание
Биодеградация
Отстаивание
Фильтрация
Сепарация
Центрифугирование
Микрофильтрация
Ультрафильтрация
Коагуляция
Флотация
Биодеградация
Вы
д
еление внеклеточных п
р
о
ду
ктов
Вы
д
еление вн
у
т
р
иклеточных п
р
о
ду
ктов
Экстракция и экстрагирование Осаждение
Центрифугирование Адсорбция
Ионный обмен Отгонка, ректификация
Дезинтеграция Гидролиз
Фе
р
ментолиз Ульт
р
а
ф
ильт
р
а
ц
ия
Очистка
воздуха
Экстракция
Осаждение
Адсорбция
Ионный обмен
Хроматография
Диализ
Ультрафильтрация
Обратный осмос
Ферментолиз
Кристаллизация
Ректификация
Концентрирование
продукта
Изготовление
готовой формы
продукта
Выпаривание
Сушка
Осаждение
Кристаллизация
Фильтрация
Ультрафильтрация
Нанофильтрация
Гранулирование
Дражирование
Таблетирование
Розлив
Фасовка
Ампулированне
газ
Рисунок 16 - Типовая схема, основные стадии и технологиче-
ские процессы в биотехнологических производствах
52
Основная стадия биотехнологического производства. Основной
стадией является собственно биотехнологическая стадия, на которой с
использованием того или иного биологического агента (микроорганиз-
мов, изолированных клеток, ферментов или клеточных органелл) про-
исходит преобразование сырья в тот или иной целевой продукт.
Обычно главной задачей биотехнологической стадии является по-
лучение определенного органического вещества.
Однако биотехнологическая стадия
, как правило, включает в себя
не только синтез новых органических соединений, но и ряд других
биотехнологических процессов, перечисленных далее.
Ферментация — процесс, осуществляемый с помощью культи-
вирования микроорганизмов.
Биотрансформация — процесс изменения химической структу-
ры вещества под действием ферментативной активности клеток мик-
роорганизмов или готовых ферментов. В этом процессе обычно не
происходит
накопления клеток микроорганизмов, а химическая струк-
тура вещества меняется незначительно. Вещество как бы уже в основ-
ном готово, биотрансформация осуществляет его химическую моди-
фикацию: добавляет или отнимает радикалы, гидроксильные ионы, де-
гидрирует и т. п.
Биокатализ — химические превращения вещества, протекающие
с использованием биокатализаторов-ферментов.
Биоокисление — потребление загрязняющих веществ с помощью
микроорганизмов или ассоциации микроорганизмов в аэробных усло-
виях.
Метановое брожение — переработка органических отходов с
помощью ассоциации метаногенных микроорганизмов в анаэробных
условиях.
Биокомпостирование — снижение содержания вредных органи-
ческих веществ ассоциацией микроорганизмов в твердых отходах, ко-
торым придана специальная взрыхленная структура для обеспечения
доступа воздуха и равномерного увлажнения.
Биосорбция — сорбция вредных примесей
из газов или жидко-
стей микроорганизмами, обычно закрепленными на специальных твер-
дых носителях.
Бактериальное выщелачивание — процесс перевода нераство-
римых в воде соединений металлов в растворенное состояние под дей-
ствием специальных микроорганизмов.
Биодеградация — деструкция вредных соединений под воздей-
ствием микроорганизмов – биодеструкторов.
53
Обычно биотехнологическая стадия имеет в качестве выходных
потоков один жидкостной поток и один газовый, иногда только один
— жидкостной.
В случае если процесс протекает в твердой фазе (например, со-
зревание сыра или биокомпостирование отходов) выходом является
поток переработанного твердого продукта.
4 ОСНОВНЫЕ ПОНЯТИЯ БИОКАТАЛИЗА И
БИОТРАНСФОРМАЦИИ
Известно, что биокатализ и
биотрансформация являются процес-
сами химического превращения одного или более веществ, протекаю-
щими под действием катализаторов - ферментов, применяемых в очи-
щенном виде или в составе клеток микроорганизмов, либо изолирован-
ных животных или растительных клеток. При этом биотрансформация
— это относительно неглубокое химическое превращение уже в основ-
ном сформированного химического соединения под влиянием
фермен-
тов. При биокатализе же возможен синтез нового вещества из различ-
ных по структуре реагентов или разложение сложного вещества под
действием ферментов. Объединяет их, прежде всего использование
специфических катализаторов — молекул фермента, имеющих белко-
вую природу. Ферменты также называют энзимами. Наука, изучающая
ферменты и ферментативные реакции, называется энзимологией.
В клетках микроорганизмов одновременно
протекает множество
биохимических реакций. Ферменты, ускоряющие биохимические реак-
ции, имеют высокую каталитическую активность, то есть эффективно
снижают энергию активации, необходимую для осуществления реак-
ции, благодаря тому, что способствуют образованию промежуточных
продуктов, требующих меньшей энергии.
Ферменты вырабатываются клеткой в соответствии с ее потреб-
ностями, их содержание может колебаться в значительной степени.
Ферменты имеют высокую специфичность, а их активность зависит от
различных факторов (температуры, рН, состава питательной среды,
наличия токсичных веществ).
Природа фермента оказывает решающее влияние на кинетику
ферментативных реакций.
В общем случае, механизм действия фермента может быть
выражен следующими структурными схемами:
для одного субстрата S
S + Е ↔ES→ P+E;

54
для двух субстратов S
1
и S
2
S
1
+ S
2
+ Е ↔E S
1
S
2
→ P+E
В обоих случаях реакции превращения субстрата (S) в продукт
(P) протекают через промежуточную стадию взаимодействия энзима
(E) с субстратом (S) и образования фермент-субстратных комплексов
(ES).
Молекула фермента — очень длинный закрученный белок, к тому
же свернутый в виде пространственного упругого клубка причудливой
формы (рис. 17).
Рисунок 17 - Пространственная конформация молекулы
фермента
Спутанность и беспорядок белка не случайны — они строго обу-
словлены чередованием аминокислот в молекуле фермента. В этой
структуре есть участки, куда легко притягивается определенная форма
молекулы субстрата.
Доказано, что скорость реакции на ферменте в 10 млрд. раз боль-
ше, чем без него. Вот почему ферменты
запросто осуществляют мно-
гие процессы, которые кажутся нереальными без них, например взаи-
модействие атмосферного азота с водой, с образованием аммонийных
соединений.
Специфичность действия ферментов
Ферменты имеют разную специфичность и по отношению к суб-
стратам. По степени специфичности ферменты делятся на следующие
основные виды, упоминаемые в порядке снижения специфичности.
1. Стериометрическая субстратная
специфичность – фер-
мент катализирует превращение только одного из возможных стерео-
изомеров субстрата. Это крайний случай специфичности. Например,
фумаратгидратаза катализирует превращение только фумаровой ки-
слоты (присоединение к ней молекулы воды), но не её стереоизомера –
малеиновой кислоты.
55
2. Абсолютная субстратная специфичность – фермент ка-
тализирует превращение только одного субстрата. Например, уреаза
катализирует превращение только мочевины.
3. Абсолютная групповая субстратная специфичность –
фермент катализирует превращение исходной группы субстратов.
Например, алкогольдегидрогеназа катализирует превращение не толь-
ко этанола, но и других алифатических спиртов, хотя и с разной скоро-
стью.
4. Относительная групповая субстратная специфичность
– фермент специфически действует не на группу молекул субстрата, а
на отдельные связи определенной группы субстратов. Например, пи-
щеварительные ферменты – пепсин, трипсин – специфичны по отно-
шению к пептидным связям, образованным определенными аминокис-
лотами в различных белках.
5. Относительная субстратная специфичность – фермент
катализирует превращение субстратов, принадлежащих к разным
группам химических соединений. Например,
фермент цитохром Р450
участвует в гидроксилировании разных соединений (около 7000 на-
именований). Это наименее специфичная ферментная система, участ-
вующая в превращении природных веществ, лекарств и ядов.
Чем же объясняется специфичность действия ферментов? На
этот счет существует две точки зрения. Одна из них – гипотеза Э. Фи-
шера, или, как её называют “ключа
в замке”, или “шаблона”, что в
основе специфичности лежит строгое стерическое соответствие суб-
страта и активного центра фермента. По Фишеру, фермент является
жесткой структурой, активный центр которого представляет собой
слепок субстрата. Если субстрат подходит к активному центру, как
ключ к замку, то реакция произойдет. Если же субстрат (“ключ”) не-
сколько
изменен, то он не соответствует активному центру (“замку”), и
реакция становится невозможной. Гипотеза Фишера привлекает своей
простотой в объяснении специфичности действия ферментов. Однако с
позиции гипотезы “шаблона” трудно объяснимы, скажем, абсолютная
и относительная групповая субстратная специфичность, поскольку
слишком разнообразная конфигурация “ключей” (субстратов), которые
подходят к одному и тому же “замку”.
Объясняет эти внешние противоречия другая гипотеза, пред-
ложенная Кошлендом. Она получила название “вынужденного со-
ответствия”. По мнению Кошленда, молекула фермента не жесткая,
а гибкая, эластичная (что подтверждается современными методами ис-
следования); конформация фермента и его активного центра изменя-

56
ется при присоединении субстрата или других лигандов; и, наконец,
активный центр – не жесткий слепок субстрата, а субстрат вынуждает
его принять соответствующую форму в момент присоединения (отсю-
да и название гипотезы “вынужденного соответствия”).
Иными словами, “замочная скважина”, по Кошленду, сделана из
податливого материала и поэтому принимает окончательную форму
“ключа” при их
контакте. Эта гипотеза также позволяет объяснить, по-
чему происходит превращение близких аналогов субстратов. Если
“ложный” субстрат (квазисубстрат) слабо отличается от природного, и
активный центр принимает конформацию, близкую к истинной, то рас-
становка каталитических групп в таком фермент-субстратном ком-
плексе позволит осуществиться реакции. Этот “обман” фермент как бы
не замечает.
Однако ферментативная реакция пойдет не так быстро,
как с истинным субстратом, поскольку нет идеального расположения
каталитических групп в активном центре фермента. Только в том слу-
чае, если конфигурация квазисубстрата не позволяет правильно раз-
меститься каталитическим группам, то реакция не пойдет. Очевидно,
неодинаковая степень специфичности разных ферментов отражает как
бы диапазон конформационных
перестроек активного центра. Если он
ограничен вплоть до естественно возможной конформации, то фермент
высоко специфичен. Если возможности перестройки велики, то фер-
мент срабатывает и на квазисубстраты.
4.1 Основные группы биотрансформаций
Рассмотрим основные группы технически важных биотрансфор-
маций:
• гидроксилирование различных позиций молекулы вещества
(добавление гидроксильной группы
О
Н
−
);
• введение двойной связи в том или ином месте;
• обрыв боковых цепей у разветвленных молекул;
• окисление молекул спиртов до кетонов;
• дегидрирование;
• изомеризация;
• ароматизация (появление ароматических углеводородных ра-
дикалов).
57
4.2 Основные виды реакций биокатализа
Назовем основные виды реакций биокатализа (практически они
будут совпадать с наименованиями основных групп ферментов) :
• окисление и восстановление;
• перенос химических функциональных групп от одних молекул
на другие;
• гидролиз;
• реакции с участием двойных связей (образование или, наобо-
рот, присоединение к ним химических групп);
• изомеризация, или структурные изменения в пределах одной
молекулы;
• синтез сложных соединений (как правило, требующий энерге-
тических затрат).
Как видно из приведенных перечислений, биотрансформация и
биокатализ являются процессами, сходными по своей природе.
4.3 Классификация ферментов
Существует классификация ферментов, ускоряющих биохимиче-
ские превращения. Все ферменты могут классифицироваться в зависи-
мости
от реакций, которые они ускоряют:
• Оксиредуктазы - ускоряют окислительно-восстановительные
реакции;
• Трансферазы - ускоряют перенос атомной группы радикалов
от одного соединения к другому;
• Гидролазы - ускоряют процесс разложения, протекающие с
участием воды;
• Дегидрогеназы- осуществляют перенос Н;
• Изомеразы – способны ускорять процессы внутренней пере-
группировки молекул;
• Синтетазы – определяют возможность
синтеза сложных со-
единений из простых.
58
4.4 Преимущества и недостатки биокаталитических
процессов
Рассмотрим преимущества и недостатки биокаталитических про-
цессов, по сравнению с превращениями в присутствии химических ка-
тализаторов.
Преимущества
1.Каталитическая активность ферментов высокоспецифична и ог-
раничивается одним типом реакций, так что не происходит побочных
реакций.
2. Ферменты могут сразу атаковать исходную молекулу и осуще-
ствлять превращение, для
которого потребовалось бы несколько вспо-
могательных многоступенчатых химических синтезов.
3. Химические преобразования вещества упрощаются — одна или
две ступени вместо многоступенчатого синтеза.
4. Ферментативные реакции могут протекать с большой скоро-
стью в мягких условиях.
Недостатки
1. Для получения чистого продукта нужен и чистый фермент, а
его выделение очень дорого.
2. В выходящем из
реактора продукте сохраняется фермент, кото-
рый продолжает действовать.
3. Дорогостоящий фермент используется только однократно.
4. Свободный фермент быстро инактивируется (то есть разруша-
ется).
5. В отличие от биомассы, которая самовоспроизводится в про-
цессе непрерывной ферментации, фермент в непрерывном процессе
нужно все время вводить, так как он вымывается с продуктом реакции.
4.5 Основные
понятия иммобилизации ферментов
Чтобы преодолеть описанные ранее недостатки процессов с ис-
пользованием свободных ферментов, надо придумать способ удержан-
ия ферментов в аппарате или легкий способ их выделения из реакцион-
ной жидкости после завершения процесса.
59
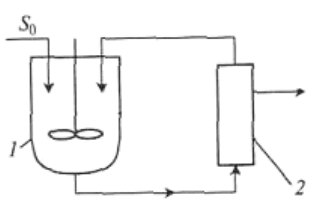
1 - биореактор, 2- проточный мембранный модуль
Рисунок 18 - Схема мембранного биореактора с выносным
модулем
Возможно отделение ферментов с помощью ультрафильтрации.
Схема установки для проведения процесса биотрансформации с ульт-
рафильтрационным выносным модулем представлена на рисунке 18.
Реакционная жидкость может циркулировать через ультра-
фильтрационный модуль, который задерживает выход фермента, не
мешая выходу продукта. Получается непрерывный
процесс, в который
не требуется добавлять фермент. Этот способ, однако, тоже имеет не-
достатки:
- мембранные установки часто выходят из строя, и при их ис-
пользовании часть ферментов «проскакивает», а часть может «застре
вать» на мембране, ухудшая фильтрацию, и, приводя к необратимой
потере фермента;
- многие ферменты, будучи в свободном состоянии (
растворенном в
жидкости или в виде взвешенных коллоидных частиц), подвержены
довольно быстрой инактивации, так что срок службы фермента не-
большой и необходимость расходования свежего фермента, стоимость
которого высока, сохраняется.
Поэтому такой путь совершенствования процессов биотрансфор-
мации большого применения не нашел. Только если сам субстрат не-
растворим или находится в коллоидном состоянии
, применение подоб-
ных систем имеет смысл.
В середине 1950-х годов возникла блестящая идея создания «не-
растворимых», или «прикрепленных к матрице», или «связанных» фер-
ментов, которые позднее стали называть иммобилизованными.
К этой идее и ее реализации имел отношение бывший президент
Израиля Э. Качальский-Катцир. Мы привыкли, что президентами ста-
60
новятся политики, хозяйственники, юристы. Но этот человек до своего
избрания был ученым-биохимиком и после пребывания на президент-
ском посту вернулся в науку и до своей смерти в 1995 г. возглавлял
институт биотехнологии в Тель-Авиве. Термин иммобилизация проис-
ходит от латинского слова «immobilis», что означает неподвижный.
Иммобилизация - это прикрепление фермента к некоторому
не-
растворимому носителю, причем таким образом, чтобы фермент мог
обмениваться с раствором молекулами субстрата и продукта.
Легко можно оценить красоту этого способа. Во-первых, появ-
ляется простая возможность отделять и многократно использовать та-
кой иммобилизованный фермент. Во-вторых, оказалось, что закреплен-
ный фермент сохраняется в активном состоянии гораздо дольше, чем
свободный, растворенный.
4.6 Методы иммобилизации ферментов
Существуют различные способы закрепления ферментов на но-
сителе, основные из которых перечислены ниже.
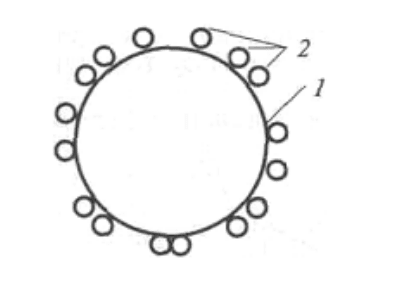
1. Адсорбция на носителе (рис.19). Носителями могут быть: не-
органические материалы (стекло, силикагель, бентонит, оксид алюми-
ния, диоксид титана и др.); природные полимеры (целлюлоза, колла-
ген); синтетические полимеры (нейлон, полиэтилен, полипропилен
).
1— гранула носителя; 2 —молекулы фермента
Рисунок 19 – Иммобилизация фермента методом адсорбции
на носителе
