Куценко С.А. Основы токсикологии
Подождите немного. Документ загружается.

K
Неспецифическая
резистентность
2. Этап изучения
механизмов
Морфология
K
Гуморальный
иммунитет
K
Клеточный иммунитет
K
K
K
Неспецифический
иммунитет
Оценка резистентности
организма
Подсчет числа В- и Т-лимфоцитов в
селезенке
Подсчет колоний клеток, образующих IgG к
Т-зависимым антигенам
Функции цитотоксических лимфоцитов;
Количество перитонеальных макрофагов и
анализ их функциональной активности
Прививка опухолевых тканей:
саркома PYB6
меланома B6F10
Бактериальные модели:
Listeria monocytogenes
Streptococcus spp
Паразитарные модели:
Trypanosoma musculi
Plasmodium yoellii
Вирусные модели:
вирус гриппа
Исследования первого этапа предназначены для выявления потенциальных иммунотоксикантов.
Тесты второго этапа позволяют установить механизм иммунотоксичности и потенциальную
способность вещества нарушать общую резистентность организма. Обычно токсикант вводится
мышам в течение 14 дней, хотя в случае неясных результатов введение может быть продолжено
до 30 и даже 90 суток.
Для изучения иммуносупрессорных свойств токсикантов в лабораторных условиях могут быть
применены животные, зараженные патогенными микроорганизмами. С целью инфецирования
используют: Listeria monocytogenes, Streptococcus pneumonia, Trypanosoma musculi, Plasmodium
yoellii, вирус гриппа, вирус герпеса простого и т.д. В подобного рода исследованиях удаётся
оценить состояние отдельных элементов иммунной системы. Продолжительность анализа - 2 - 3
недели.
Примером хорошо отработанного теста на иммунотоксичность ксенобиотика, является метод
введения мышам, подвергшимся действию токсиканта, культуры трипаносом (trypanosoma
musculi). Эти трипаносомы являются непаразитическими, экстрацеллюлярными
микроорганизмами. Поражение мышей этими организмами на ранних этапах заражения
контролируется врожденными механизмами резистентности, в частности фагоцитозом. В поздние
стадии (10 дней инфекционного процесса) паразитемия контролируется механизмами
антителообразования. Конечный этап (18 - 20 день) инфекционного процесса проходит под
контролем как клеточного, так и гуморального иммунитета. Таким образом, в одном эксперименте
можно определить влияние ксенобиотика на несколько элементов иммунной реакции (фагоцитоз,
выработку антител, клеточный иммунитет). Вызванные токсикантом повреждения фагоцитоза,
либо антителообразования, либо механизмов клеточного иммунитета, проявляются паразитемией
в соответствующем периоде развития инфекции. Эта модель достаточно чувствительна и
эффективна при оценке иммуносупрессорных свойств ксенобиотиков.
Оценка потенциальной способности веществ сенсибилизировать организм проводится в опытах на
лабораторных животных, как правило, на морских свинках. В настоящее время используются три
группы тестов: Draize; Buehler; Magnusson-Kligman. Тесты различаются способами введения
токсикантов: внутрикожное, накожное и подкожное, соответственно; используемыми в
исследовании адъювантами, промежутками времени между сенситизацией и провокацией
реакции. В настоящее время как наиболее специфичный и точный рассматривается тест
Magnusson-Kligman. С методикой проведения исследований можно познакомиться в специальной
литературе.
5. Выявления иммунотоксических эффектов
Не смотря на многочисленные данные об иммунотоксических свойствах веществ, получаемых на
экспериментальных животных, в силу сложности экстраполяции, сведения о влиянии веществ на
человека порой противоречивы. Кроме того далеко не у всех лиц, с признаками
иммунотоксического поражения органов (гломерулонефрит, пневмониты, астма, аллергические
дерматиты, гепатиты и т.д.) удается легко выявить химическую природу этиологического фактора,
определить источник воздействия. Достаточно сложно отличить дисфункцию системы, как
следствие какого либо заболевания или недостаточности питания, от химически обусловленной
патологии. Поэтому для выявления иммунотоксичности вслед за этапом оценки иммунного статуса
обследуемых лиц, должен следовать этап поиска доказательства причинно-следственных связей
между выявленными нарушениями и действием токсиканта.
Исследования должны начинаться с тщательного обследования и сбора анамнеза. Необходимо
особое внимание уделять выявлению классических проявлений и симптомов иммунных
нарушений. Сложные лабораторные тесты могут обеспечить детальную информацию о состоянии
гуморального и клеточного компонентов иммунитета, комплемента, фагоцитарных функциях,
однако проведение этих тестов в подавляющем большинстве случаев совершенно излишне. Для
оценки состояния иммунной системы часто вполне достаточно использовать простые
скрининговые методы. Необходимо иметь в виду, что вследствие высокой лабильности иммунной
системы, получаемые в ходе обследования результаты, характеризуют её состояние только в
данный момент времени.
5.1. Оценка иммунологического статуса
Для оценки статуса человека с предполагаемой иммунной патологией Иммунологическая секция
ВОЗ рекомендует использовать тесты, представленные на таблице 11.
Таблица 11. Тесты клинического иммунологического скрининга
- Подсчет числа форменных элементов крови. Формула
крови
- Количественный электрофорез плазмы крови
Гуморальный иммунитет:
- Количество иммуноглобулинов (IgG, IgM, IgA,
IgE)
- Титры изоантител
Клеточный иммунитет:
- Кожные тесты на отсроченную гиперреактивность
Аутоиммунный процесс:
- Титр аутоантител
Эти исследования следует проводить перед тем, как переходить к более сложным и дорогим
диагностическим процедурам (таблицы 12, 13).
Талица 12. Методы оценка состояния гуморального иммунитета
Функция иммуноглобулинов:
- электрофорез белков
- количество иммуноглобулинов в плазме крови
- титр специфических антител (изогаммаглобулины, антистрептолизин О, антитела к
возбудителям свинки, кори, полиомиелиту)
- антигенный ответ:
- первичное антителообразование
- вторичное антителообразование
Функция В-лимфоцитов:
- количество В-лимфоцитов с поверхностными иммуноглобулинами (нормальное
содержание 4 -10%)
- активация В-лимфоцитов (реакция на митогены, инактивированные антигены, индукцию
клеточного деления)
- пролиферация В-лимфоцитов (измерение интенсивности пролиферации путём изучения
скорости инкорпорации тимидина, меченого тритием)
- дифференциация В-лимфоцитов (определение колоний антителосекретирующих клеток
или определение количества антител в супернатанте культуры клеток; определение
продукции иммуноглобулинов индуцированной митогенами Т- и В-лимфоцитов)
Таблица 13. Методы оценка состояния клеточного иммунитета
Подсчёт лимфоцитов
Тесты на трансформацию лимфоцитов:
- стимуляция митогенами
- воздействие антигенов
- смешанная культура лимфоцитов
Определение лимфокинов:
- фактор ингибирования макрофагов
- фактор угнетения миграции лимфоцитов
- лимфоцитарный хемотаксический фактор
Кожные тесты на отсроченную гиперчувствительность (антигены: свинка, трихофитон,
тетанотоксоид и др.)
Лимфоцитарная цитотоксичность, активность естественных киллеров
Субпопуляции Т-клеток: соотношение хелперы/супрессоры
Электрофорез белков позволяет быстро установить нормально ли у обследуемого содержание
иммуноглобулинов, нет ли дисгаммаглобулинемии. Гипогаммаглобулинемия обычно является
следствием вторичного иммунного дефицита. Определение иммуноглобулинов даёт прямую
информацию о наличии или отсутствии моноклональной или поликлональной
гаммаглобулиноапатии. Основными типами иммуноглобулинов являются IgG, IgM, IgA, IgE их
определение оправдано в тех случаях, когда частью клинического синдрома является
аллергический компонент. Определение специфичных антител методологически сложно (методы
энзимсвязанной иммуносорбции). Наиболее часто развивается дефицит IgA, причем в 50%
случаев при этом отсутствуют признаки патологии. Функция этого иммуноглобулина - защита
слизистых барьеров организма от инфекции.
Нарушение клеточного иммунитета можно выявить, ориентируясь на симптомы заболеваний,
ассоциирующихся с функциями этого механизма резистентности. Как известно, к числу таких
функций относятся: уничтожение внутриклеточных патогенных организмов, отторжение
опухолевых клеток, отсроченные реакции гиперреактивности, в том числе контактные дерматиты,
аутоиммунное повреждение органов и тканей. Наиболее часто дефицит клеточного иммунитета
проявляется учащением инфекционных заболеваний вирусной и грибковой этиологии.
Любое уменьшение числа Т-лимфоцитов, выявляемое при подсчете формулы крови, до уровня 75
- 85% от нормального значения, называется лимфопенией. Определение числа Т-лимфоцитов
различных типов производится путем подсчета розеток, образуемых с эритроцитами барана и с
помощью флюоресцирующих моноклональных антител к зрелым Т-лимфоцитам.
Тест на трансформацию лимфоцитов можно провести in vitro с использованием митогенов
(фитогемагглютинин и др.) и растворимых антигенов, добавляя их к культуре клеток.
Кожные тесты на отсроченную гиперреактивность могут быть выполнены с использованием
обычных антигенов, таких как антиген возбудителя свинки, Trichophyton, Candida ablicans.
Эритематозная кожная реакция с индурацией ткани, размером более 10 мм, спустя 24, 48, и 72
часа после инъекции 0,1 мл антигена под кожу ладонной поверхности предплечия указывает на
серьёзную модификацию клеточных механизмов иммунитета (антиген был распознан
лимфоцитами, произошла его процессия, активированы Т-клетки, секретированы лимфокины,
произошло привлечение в регион несенситизированных лимфоцитов). Позитивный кожный тест на
3 из 5 вводимых антигена выявляется у 95% населения и указывает на адекватную
физиологическую реакцию иммунной системы. Отрицательный результат может быть следствием
не только дефекта иммунной системы, но и неправильно выполненной пробы. Важнейшим
элементом постановки кожного теста является стандартизация используемых антигенов.
Определение аутоантител может оказаться полезным при диагностике системных заболеваний
соединительной ткани, активной фазы хронического гепатита, красной волчанки и т.д. Обычно
выявляемые антитела специфичны в отношении ядер клеток, ДНК, структурных элементов
гладкомышечных волокон, клеток щитовидной железы. Антитела к ядрам клеток иногда
определяются у здоровых людей (особенно пожилого возраста), а также у больных ревматизмом.
Проявления иммунной токсичности ксенобиотиков очень часто ошибочно приниматься за
аутоиммунные заболевания и хронические воспалительные процессы иной этиологии.
С диагностическими целями может быть изучено содержание специфических антител к антигенам,
с которыми человек, как правило, контактировал на протяжении жизни. К числу таких антител
относятся изогемагглютинины, антистрептолизин-О, антитела к кори, свинке, полиомиелиту и т.д.
Для оценки функционального состояния иммунной системы возможно использовать метод
изучения иммунного ответа на первичный контакт с антигеном, а также выраженность вторичной
иммунной реакции. Обычно исследование проводят путем повторного введения тетанотоксоида с
измерением титра вырабатывающихся антител. К действию иммуносупрессоров более
чувствительна иммунная реакция на первичный контакт с антигеном.
Дефицит отдельных компонентов системы комплемнта может сочетаться с различными
заболеваниями. Показаниями для изучения состояния комплемента являются: частые
инфекционные заболевания, системные бактериальные инфекции, подозрения на аутоиммунный
процесс. Ряд клинических синдромов связан с неадекватной активацией комплемента. Это,
например, хроническая уртикарная сыпь, кожные васкулиты, пурпура, артралгии, артриты,
лихорадочные состояния неизвестной природы, нефриты. Снижение содержания в сыворотке
крови компонента С4 указывает на недостаточную активацию системы комплемента. Активация
системы комплемента и наличие высокого титра антител указывает на патологию иммунного
комплекса и аутоиммунный процесс. Позитивная реакция на иммунные комплексы, наличие
аутоантител, активация комплемента - свидетельства органной патологии.
Полная оценка фагоцитарных функций иммунной системы включает:
- подсчет числа нейтрофилов в периферической крови;
- определение скорости восстановления нитросинего тетразолия (НСТ) нейтрофилами;
- изучение хемотаксиса клеток;
- изучение фагоцитарной активности;
Для выявления нарушений нет необходимости проводить все указанные определения. Снижение
количества полиморфноядерных нейтрофилов до уровня 1000 и ниже в 1мм
3
крови сопряжено с
увеличением риска развития инфекционного процесса.
Лейкопению вызывает большое число этиологических факторов, среди них инфекция, токсиканты,
ионизирующее излучение. Причинами нейтропении при действии ксенобиотиков (см. раздел
"Гематотоксичность") могут быть угнетение костного мозга и аутоиммунный процесс,
развивающийся при повторном контакте с токсикантом.
ГЛАВА 6.2. ХИМИЧЕСКИЙ МУТАГЕНЕЗ
Мутации - это наследуемые изменения генетической информации, хранящейся в ДНК
клеток. Различные факторы химической и физической природы способны вызывать мутации.
Наиболее изученными являются последствия действия ионизирующей радиации и таких веществ,
как сернистый и азотистый иприты, эпоксиды, этиленимин, метилсульфонат и т.д. Химические
вещества, способные вызывать мутации называются мутагенами.
Далеко не всякая модификация молекулы ДНК (мутация) является опасной для организма. Более
того, эволюция была бы не возможна без мутаций, поскольку именно она лежит в основе
изменчивости. Опасность представляет случайный, ненаправленный мутагенез, как правило,
несущий для организма негативные последствия. Неблагоприятные эффекты мутагенеза
определяются тем, в клетках какого типа он реализуется: половых или соматических, стволовых и
делящихся или созревающих и зрелых. Результатом грубых мутаций половых клеток и делящихся
клеток развивающегося плода являются: стерильность особи, врожденная патология у потомства,
тератогенез, гибель плода. Мутации стволовых и делящихся соматических клеток сопровождаются
структурно-функциональными нарушениями тканей с непрерывной физиологической регенерацией
(система крови, иммунная система, эпителиальные ткани) и канцерогенезом. Повреждение
токсикантом ДНК зрелой соматической клетки не приводит к пагубным последствиям для
организма.
Основными видами мутаций, вызываемых химическими веществами, являются: 1) точечная
мутация, связанная с модификацией одного нуклеотида в структуре ДНК, (замещение нуклеотида,
выпадение нуклеотида из цепи, включение дополнительного нуклеотида в цепь); 2) хромосомные
аберрации, т.е. изменение структуры хромосом (разрывы молекул ДНК, транслокации фрагментов
ДНК) или числа хромосом в клетке.
1. Точечные мутации
1.1. Замещение нуклеотида
Минимальным повреждением ДНК является замещение нуклеотида или нуклеотидной пары,
называемое точечной мутацией. Если нуклеотид замещается на другой нуклеотид того же типа,
например, пуриновое основание на пуриновое основание или пиримидиновое - на пиримидиновое,
мутация называется транспозицией. Если пуриновое основание замещается пиримидиновым или
наоборот, говорят о трансверсии. При действии химических веществ на организм точечная
мутация происходит тремя способами: путем химической модификации нуклеотида, действием на
нуклеотиды алкилирующих агентов, включением в цепь ДНК токсиканта - аналога азотистого
основания.
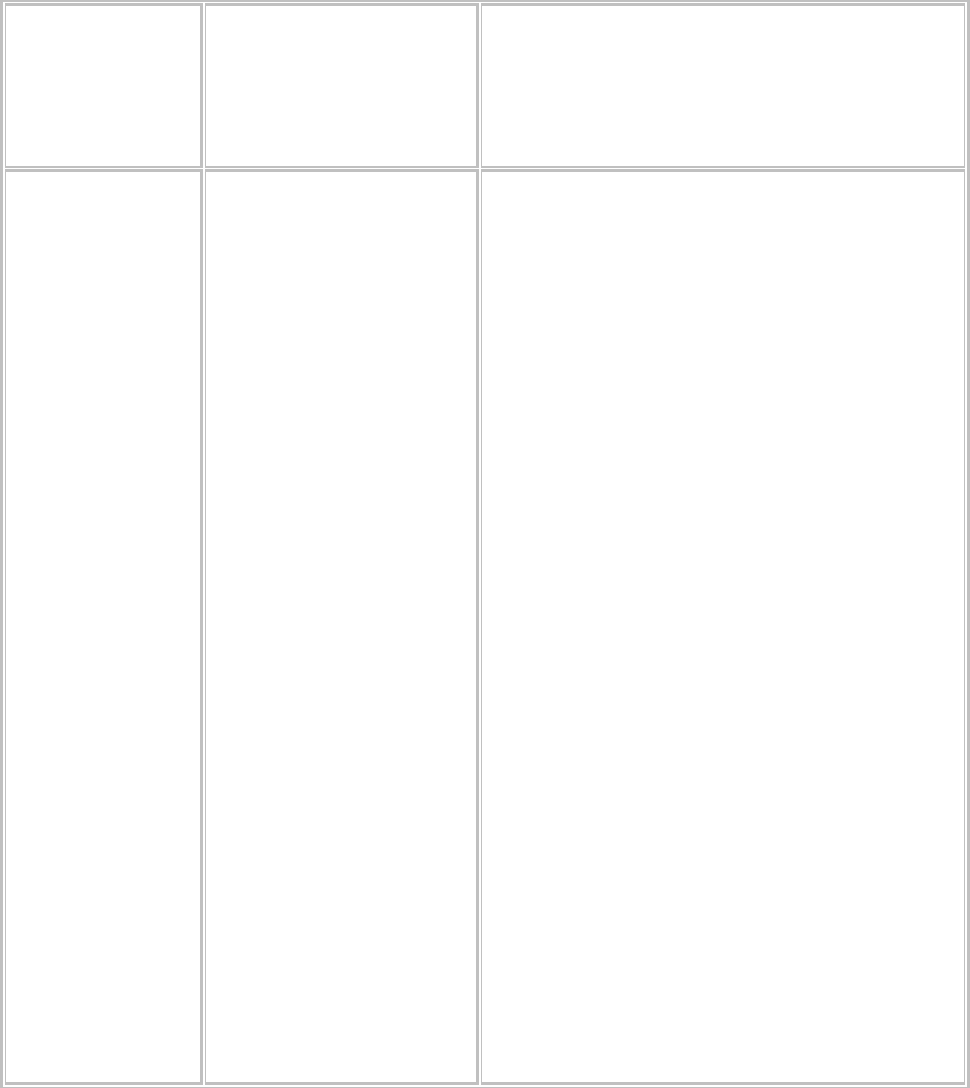
Примером химической модификации является изменение нуклеотида азотистой кислотой.HNO
2
способна превращать цитозин в урацил или аденин в гипоксантин (рисунок 1). Такой тип мутации
выявлен в опытах с фагами, бактериями, микромицетами. У млекопитающих он возможен при
действии активных в химическом отношении веществ, прежде всего на барьерные ткани
(например, эпителий желудочно-кишечного тракта).
Рисунок 1. Превращение цитидина в уридин под влиянием азотистой кислоты
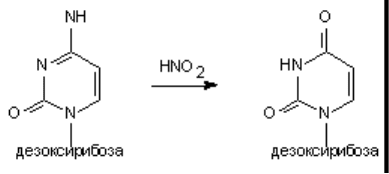
Алкилирующими агентами называются вещества, способные ковалентно присоединять алкильные
радикалы к активным группам нуклеотидов ДНК. Такой способностью обладают сернистый и
азотистый иприты, многие промышленные токсиканты, лекарственные (противоопухолевые)
препараты (производные дихлорэтиламина: циклофосфамид, мелфалан; производные
нитрозомочевины: кармустин, ломустин; алкилсульфонаты: бисульфан; цисплатин и т.д.) (рисунок
2).
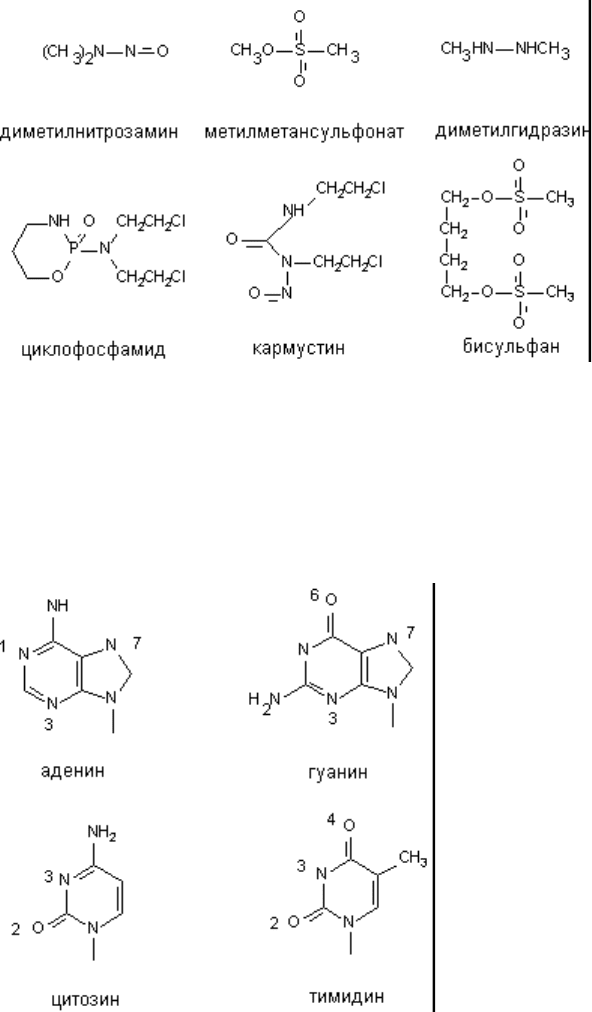
Рисунок 2. Структура некоторых алкилирующих агентов
К числу активных групп пуриновых и приримидиновых оснований, способных к алкилированию
относятся азот в 1, 3, 7 положениях молекулы аденина; азот - в 3,7, и кислород в 6 положении
молекулы гуанина; азот - в 3 и кислород - во 2 - цитозина; азот - 3 и кислород - 2 и 4 - тимина
(рисунок 3). Помимо азотистых оснований алкилированию могут подвергаться фосфатные группы
молекулы ДНК.
Рисунок 3. Участки наиболее вероятного алкилирования ДНК в физиологических условиях
Некоторые вещества, используемые в настоящее время в качестве противоопухолевых средств,
являются структурными аналогами пуриновых и пиримидиновых оснований, входящих в ДНК.
Поступая в организм, они включаются в синтез ДНК опухолевыми клетками, замещают генуинные
нуклеотиды, вызывая летальные мутации. Результатом этого является гибель быстро делящихся
клеток опухолей. К числу таких веществ относятся 5-бромурацил, 5-фтордезоксиуридин, 2-
аминопурин, 6-меркаптопурин и т.д. Поражение этими веществами здоровых клеток организма,
находящихся в фазе деления, может приводить к их мутациям (и пагубным последствиям для
организма).
1.2. Выпадение или включение дополнительного нуклеотида
Выпадение или включение дополнительного нуклеотида в структуру ДНК кардинальным образом
изменяет триплетный код, с помощью которого храниться информация о последовательности
аминокислот в синтезируемом белке. Поскольку выпадение или включение основания приводит к
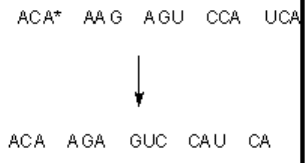
"сдвигу" всей последовательности нуклеотидов (рисунок 4) последствия такой мутации, как
правило, пагубны.
Рисунок 4. Выпадение аденина (А*) приводит к сдвигу цепи нуклеотидов влево и полному
изменению триплетного кода
Некоторые токсиканты, например производные акридина, способны вызывать подобные
изменения в структуре ДНК.
1.3. Репарация ДНК
Клетки обладают способностью корректировать и устранять повреждения ДНК. Вследствие этого
лишь небольшое число мутаций, инициированных токсикантом, сохраняется в процессе
репликации молекулы. Однако если мутация не распознана, извращенная информация
транскрибируется в РНК, а затем экспрессируется в форме неполноценного протеина.
Последствия этого для клетки могут быть либо несущественны, либо критичны, в зависимости от
функций, выполняемых протеином.
Ряд ферментов, участвующих в репарации поврежденных ДНК, в настоящее время хорошо изучен
(см. выше). Например, метилтрансферазы принимают участие в деметилировании О-6-
метилгуанина. Гликозилазы расщепляют связи между азотом-9 пурина, подвергшегося
алкилированию, образуя участки депуринизированной ДНК. Фрагменты нуклеиновой кислоты,
состоящие, как правило, из 3 - 4 нуклеотидов, включая депуринизированный участок, вырезаются
из цепи спомощью эндонуклеаз. В дальнейшем удаленные фрагменты заполняются при участии
ферментов ДНК-полимераз и "встраиваются" в общую цепь с помощью ДНК-лигаз. Сбои в этом
механизме могут приводить к повреждению генетического кода клеток.
2. Хромосомные аберрации
Для обозначения процессов, приводящих к делеции (выпадению), перестройке фрагментов
хромосом или появлению дополнительных хромосом, которые выявляются с помощью световой
микроскопии клеток, используют термин - кластогенез. Наиболее частой формой кластогенеза
являются разрывы хромосом, которые вызываются, например, действием ионизирующего
излучения и многих химических веществ. Алкилирующие агенты, особенно содержащие две
функциональные группы в молекуле (сернистый, кислородный, азотистый иприты и их
производные и аналоги, бисульфан, кармустин и т.д.), образуя поперечные связи с обеими
цепочками молекулы ДНК, могут вызвать её разрыв. В основе разрыва лежит депуринизация
поврежденных нуклеотидов соседствующих фрагментов обеих нитей ДНК, с последующим их
одновременным вычленением с помощью эндонуклеаз (см. выше). Ферментом, принимающим
участие в последующей репарации поврежденной ДНК, является поли-АДФ-рибозилполимераза.
Аккумуляция в ядре клетки фрагментов ДНК активизирует энзим. Субстратом для образования
АДФ-рибозилата, необходимого для восстановления целостности макромолекулы, является
никатинамидадениндинуклеотид (НАД). Если ДНК повреждается значительно, на её репарацию
расходуется большое количество НАД, что приводит к истощению запасов нуклеотида в клетке и
острому энергетическому дефициту. Полагают, что этот феномен также может лежать в основе
гибели клеток, подвергшихся действию мутагенов (например, иприта).
В ходе "сшивания" двунитевых разрывов хромосом весьма вероятны ошибки. Основные виды
нарушений, возникающих при этом, это делеция, транслокация и инверсия частей хромосом.
Увеличение числа хромосом в клетке может явиться следствием нарушения процесса их
разделения в ходе митоза между двумя дочерними клетками. В итоге образуются клетки с
большим или меньшим числом хромосом. Иногда кратно увеличивается весь набор хромосом. Это
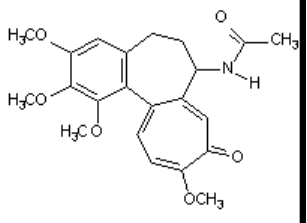
явление называется - полиплоидия. Ряд химических веществ вызывают полиплоидию. К числу
наиболее изученных относится колхицин (рисунок 5), связывающийся с мономерами тубулина,
блокирующий его полимеризацию и за счет этого нарушающий образование митотических
веретен.
Рисунок 5. Структура колхицина
Колхицин блокирует митоз в метафазе, вызывая полиплоидию поврежденной клетки. Другими
примерами веществ, действующих подобным образом, являются производные алкалоида
винкамина (винкристин, винбластин) и подофилотоксин. Полиплоидия у млекопитающих, как
правило, является летальной мутацией (в отличии от растений).
3. Условия действия мутагенов на клетки
Все клетки организма находятся в одной из фаз клеточного цикла:
1. Покоя (фаза G
0
): клетка функционирует или покоится (большинство соматических неделящихся
клеток);
2. Синтеза клеточных компонентов, необходимых для последующего синтеза ДНК (фаза G
1
): идет
накопление необходимого количества пуриновых и пиримидиновых оснований и других химических
компонентов ДНК. В делящейся клетке процесс занимает до 40% общего времени цикла
клеточного деления;
3. Синтеза ДНК (фазаS): осуществляется "сборка" новой молекулы ДНК из наличествующих в
клетке компонентов. Процесс занимает до 39% времени клеточного цикла.
4. Синтеза клеточных компонентов для митоза (фазаG
2
). В частности синтезируется мономеры и
полимер тубулина и т.д. Процесс занимает около 19% времени цикла делящейся клетки.
5. Митоза (фазаM): разделение генетического материала между вновь образующимися дочерними
клетками; клеточное деление. Процесс занимает 2% времени.
Часть химические вещества способны вызывать мутации лишь тех клеток, которые находятся в
определенной фазе цикла, это так называемые цикло-специфичные вещества. Другие действуют
на генетический аппарат не зависимо от того, в каком периоде клеточного цикла находится клетка
(цикло-неспецифичные). Такая особенность в действии веществ определяется механизмом,
посредством которого токсикант повреждает ДНК (см. выше). К числу цикло-неспецифичных
принадлежат мутагены, способные вызывать химическое повреждение нуклеотидов
(алкилирующие агенты и химические модификаторы нуклеотидов). Все остальные мутагены
являются цикло-специфичными.
4. Изучение мутагенной активности
Изучение мутагенной активности химических веществ осуществляется в опытахin vitro на
прокариотических и эукариотических клетках, путем непосредственного изучения степени
повреждения ДНК, и выявления хромосомных аберраций у животных, подвергшихся действию
токсикантов.
4.1. Исследования в опытах на прокариотах. Тест Эймса
В основе теста, разработанного Брюсом Эймсом, лежит способность мутагенов вызывать
обратную мутацию измененного штаммаSalmonella typhimurium, неспособного к биосинтезу
гистидина. Микроорганизмы данного штамма не растут в среде, не содержащей гистидин, однако
под влиянием мутагенов вновь приобретают эту способность, свойственную исходному штамму
сальмонелл (обратная мутация). В настоящее время созданы специальные штаммы, позволяющие
выявлять мутации типа "замещение основания" (штамм ТА-1531) и типа "сдвиг цепи нуклеотдидов"
(штамм ТА-1537, ТА-1538).
Тест осуществляется на суспензии бактериальных клеток в расплавленном при 45
0
агаре. В
инкубационную среду (не содержащую гистидин) добавляют токсикант. К части проб добавляют
также фракцию микросом, выделенных из гепатоцитов крыс, предварительно обработанных
полихлорированными бифенилами, с целью индукции цитохромовР-450 (фракцияS-9). Смеси
разливают по чашкам Петри. Число бактерий, приобретших вследствие обратной мутации
способность синтезировать гистидин, оценивают путем подсчета колоний, развившихся в
инкубате. Исследуемое вещество оценивается в нескольких концентрациях (установление дозовой
зависимости эффекта). В итоге получается информация о наличии мутагенности у исходного
вещества (среды без фракцииS-9) и его метаболитов (среды, содержащие фракциюS-9).
Недостатком метода является сложность получения количественных характеристик мутагенной
активности обследуемых веществ для млекопитающих и человека.
В настоящее время тестирование проводят и на других биологических объектах (прямая и
обратная мутацияEscherichia coli,прямая мутация сальмонелл).
4.2. Исследования в опытах на клетках млекопитающих
Первоначально считалось, что культуры клеток млекопитающих будут идеальным объектом для
изучения мутагенной активности токсикантов. Однако в процессе работы, вскрылись
обстоятельства поколебавшие эти представления. Прежде всего клетки многих тканей трудно
культивировать, у многих из них практически отсутствует способность к клонированию,
метаболическая активность клеток недостаточна. В настоящее время в исследованиях
предпочтение отдают культурам клеток перевиваемых линий (например, овариальные клетки
китайского хомячка, клетки мышиной лимфомы и т.д.). Однако чувствительность этих клеток к
ксенобиотикам уже отличается от чувствительности клеток первичных тканевых культур.
Исследования по оценке мутагенности обычно проводят, изучая изменения резистентности клеток
к: 8-азагуанину или 6-тиогуанину (определяется активностью гипоксантин-гуанин-
фосфорибозилтрансферазы - ГГФРТ); бромдезоксиуридину или трифтортимидину (определяется
активностью тимидинкиназы - ТК); оуабаину (определяется активностьюNa/К-АТФазы).
ГГФРТ регулирует инкорпорацию пуринов из среды в клетку. Мутация локуса ДНК, ответственного
за синтез энзима, приводит к угнетению ферментативной активности, прекращению транспорта
пуринов в клетку, в том числе и их токсичных аналогов. Мутировавшие клетки выживают в среде,
содержащей аза- и тиогуанины.
ТК активирует транспорт пиримидинов. Мутация лкуса ДНК, ответственного за синтез ТК, делает
клетку не чувствительной к токсическому действию токсичных аналогов пиримидина.
Оуабаин убивает клетки, взаимодействуя сNa/К-АТФазой. Мутация локуса, ответственного за
синтез этого энзима изменяет его сродство к токсиканту, увеличивает резистентность клетки к яду.
Наиболее часто используется модель мутации ТК локуса в опытах с культурой клеток мышиной
лимфомы (иногда с добавлением в инкубационную средуS-9 фракции гепатоцитов). После
воздействия исследуемого токсиканта оценивается количество клеток, способных образовывать
колонии в среде, содержащей бромдезоксиуридин.
В настоящее время описано множество других тест-объектов, на которых можно проводить
подобные исследования.
