Кац Н.Г., Стариков В.П., Парфенова С.Н. Химическое сопротивление материалов и защита оборудования нефтегазопереработки от коррозии
Подождите немного. Документ загружается.


9
рий нефтегазовых сооружений свидетельствует о превалирующем
влиянии коррозионного фактора. Так, в нефтеперерабатывающей
промышленности и на транспорте нефти и газа 70% отказов происхо-
дит по причине коррозионных повреждений [7, 24-28] (табл. 1).
Из общего количества отказов промысловых трубопроводов
(см. табл. 1) свыше 70% аварий приходится на так называемую ру-
чейковую (канавочную) коррозию (рис. 1).
Рис. 1. Дефект в трубе при ручейковой коррозии
По данным Ростехнадзора, протяженность промысловых трубо-
проводов в Российской Федерации превысила 350000 км, а протяжен-
ность магистральных трубопроводов составляет свыше 150000 км, из
которых:
– 25% служат более 40 лет;
– 33% служат более 27 лет;
– 27% выработало нормативный срок.
В результате в РФ ежегодно происходит более 20000 порывов,
свищей и других аварий при максимальной скорости коррозии
12-16 мм/год.
10
В новых экономических условиях предприятия зачастую экс-
плуатируют оборудование и трубопроводы до их полного выхода из
строя. Поэтому знание причин отказов наряду с изучением коррози-
онных процессов, методов защиты от коррозии и своевременным мо-
ниторингом позволит минимизировать потери от коррозии.
2. Определение понятия «коррозия металлов».
Термины и стандарты
Коррозией металлов называют самопроизвольное разрушение
металлических материалов вследствие химического или электрохи-
мического взаимодействия их с окружающей средой.
Коррозионный процесс протекает на границе раздела двух сред
металла и окружающей среды, т.е. является гетерогенным процессом
взаимодействия жидкой или газообразной среды с металлом
(рис. 2) [1, 2, 4].
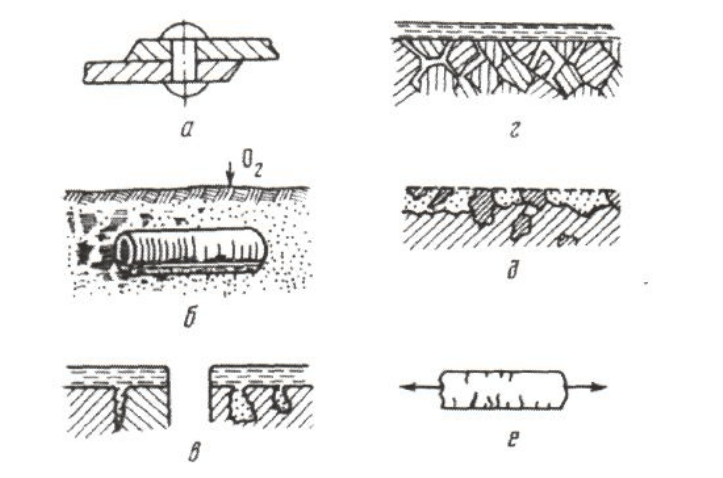
Рис. 2. Некоторые типы гетерогенности поверхности
корродирующего металла:
а – контакт разнородных металлов; б – дифференциальная аэрация;
в – образование щелей и питтингов; г – межкристаллитная коррозия;
д – структурно-избирательное разрушение; е – коррозионное растрескивание,
или коррозионная усталость, при приложении нагрузки
11
Способность металлов сопротивляться воздействию среды назы-
вается коррозионной стойкостью, или химическим сопротивлением
материала. Металл, подвергающийся коррозии, называют корроди-
рующим металлом, а среда, в которой протекает коррозионный про-
цесс, – коррозионной средой. В результате коррозии изменяются
свойства металла и зачастую происходит ухудшение его функцио-
нальных характеристик.
Металл при коррозии может частично или полностью разрушать-
ся. Химические соединения, образующиеся в результате взаимодей-
ствия металла и коррозионной среды, называют продуктами корро-
зии. Продукты коррозии могут оставаться на поверхности металла в
виде оксидных пленок, окалины или ржавчины. В зависимости от
степени адгезии их к поверхности металла наблюдаются различные
случаи. Например, ржавчина на поверхности железных сплавов обра-
зует рыхлый слой, процесс коррозии распространяется далеко в ме-
талл и может привести к образованию сквозных язв и свищей. Напро-
тив, при окислении алюминия на поверхности образуется плотная
сплошная пленка оксидов, которая предохраняет металл от дальней-
шего разрушения [1-5, 9, 15, 24].
Коррозия является физико-химическим процессом, и закономер-
ности ее протекания определяются общими законами термодинамики
и кинетики гетерогенных систем. Различают внутренние и внешние
факторы коррозии. Внутренние факторы характеризуют влияние на
вид и скорость коррозии природы металла (состав, структура и т.д.).
Внешние факторы включают влияние состава коррозионной среды и
условий протекания коррозии (температура, давление и т.д.).
Противокоррозионной защитой называют процессы или средства,
применяемые для уменьшения или прекращения коррозии металла.
Основные понятия, термины и определения в области коррозии стан-
дартизированы (ГОСТ 5272-68*). В системе государственных стан-
12
дартов единой системы защиты от коррозии, старения и биоповреж-
дений (ЕСЗКС) вопросы коррозии выделены в класс под номером
«9». Следующая цифра, отделенная точкой от цифры «9», соответст-
вует определенной классификационной группе стандарта [24]:
0 – Методы испытаний;
1 – Организационно-методические правила и нормы;
2 – Общие требования к выбору конструкционных материалов и
комплексной защите;
3 – Металлические и неметаллические неорганические покрытия;
4 – Лакокрасочные, полимерные покрытия;
5 – Временная противокоррозионная защита;
6 – Электрохимическая защита;
7 – Защита от старения;
8 – Защита от биоповреждений;
9 – Общие вопросы коррозии и защиты металлов.
Чем же занимается наука о коррозии, каковы ее задачи и научные
основы курса? Наука о коррозии изучает взаимодействие материалов
с коррозионной средой, устанавливает механизм этого взаимодейст-
вия и его общие закономерности. Практическая цель учения – защита
материалов от коррозии и разрушения при их обработке и эксплуата-
ции конструкций из них в различных агрессивных средах.
Для установления механизма и общих закономерностей этого
взаимодействия и разработки методов борьбы необходимо знание
свойств материалов и коррозионной среды, а также основные зако-
номерности химических и электрохимических процессов, т.е. науч-
ной базой учения о коррозии и защите являются материаловедение и
физическая химия, в первую очередь такие ее разделы, как термоди-
намика и кинетика гетерогенных химических и электрохимических
процессов.
13
3. Общие сведения о коррозионной стойкости металлов
Первопричиной коррозии металлов является их термодинамиче-
ская неустойчивость в различных средах при данных внешних усло-
виях, т.е. самопроизвольный переход металла в более устойчивое
окисленное состояние за счет уменьшения термодинамического по-
тенциала системы, которое достигается в результате реакции:
металл +
окислительный
компонент среды
=
продукт
коррозии
Термодинамика дает исчерпывающие сведения о возможности
или невозможности самопроизвольного протекания коррозионного
процесса при определенных условиях.
Термодинамические потенциалы могут быть использованы для
количественной оценки движущих сил химических или электрохими-
ческих коррозионных процессов, а также для расчета скоростей этих
процессов и практических методов защиты от коррозии, т.е. создания
условий, уменьшающих или полностью исключающих возможность
протекания коррозионного процесса.
Однако термодинамика не дает ответа на вопрос, с какой скоро-
стью будет протекать термодинамически возможный коррозионный
процесс. Рассмотрением этого вопроса, а также установлением влия-
ния различных факторов на скорость коррозии и характер коррозион-
ного разрушения металлов занимается кинетика (учение о скоростях)
коррозионных процессов.
Отличительной особенностью коррозионных процессов является
их сложность и многостадийность. Обычно коррозионный процесс
состоит из трех основных стадий [1-5, 7, 9, 15, 24]:
1) перенос реагирующих веществ к поверхности раздела фаз;
2) собственно гетерогенная реакция;
3) отвод продуктов реакции из реакционной зоны.
14
Каждая из этих стадий может протекать последовательно или па-
раллельно с образованием на поверхности металла продуктов корро-
зии.
Реакция окисления происходит, когда металл соединяется с ато-
мом или группой молекул, теряя при этом электроны, либо когда он
переходит из одной степени окисления в другую, более высокую.
Суммарная реакция окисления этого типа может быть представ-
лена как две реакции, протекающие одновременно [1]:
окисление
n
Me
Me
n
электронов;
восстановление nO
2
электронов
2
)2/( On ;
суммарная реакция
2/2 n
MeOOMe
.
Одновалентный металл будет образовывать один оксид, многова-
лентный может формировать, как правило, несколько различных ок-
сидов, число которых определяется валентностью металла. Оксиды
электрически нейтральны, имеют определенную кристаллическую
структуру, состоят из зерен (кристаллов), свойства которых подобны
свойствам металлов. Оксид способен к рекристаллизации, росту зе-
рен и может подвергаться пластической деформации, особенно при
высоких температурах.
4. Классификация коррозионных процессов
Процессы коррозии можно классифицировать по различным при-
знакам [1-4, 7, 20]:
1. По механизму протекания коррозии.
2. По условиям процесса.
3. По характеру разрушения поверхности.
В зависимости от механизма различают химическую, электрохи-
мическую и биохимическую коррозию металлов [47].
Химическая коррозия – это взаимодействие металла с коррози-
онной средой, при котором окисление металла и восстановление
15
окислительного компонента коррозионной среды протекают в одном
акте. Продукты коррозии при этом процессе возникают непосредст-
венно на корродирующих участках.
Электрохимическая коррозия – это взаимодействие металла с
коррозионной средой (раствором электролита), при котором иониза-
ция атомов металла и восстановление окислительного компонента
коррозионной среды протекают не в одном акте и их скорости зави-
сят от электродного потенциала металла. При этом виде коррозии
протекают две реакции – анодная и катодная, локализованные на оп-
ределенных участках поверхности корродирующего металла.
Биохимическая коррозия – это процесс, связанный с воздейст-
вием на материал микроорганизмов, выделяющих вещества, которые
ускоряют процесс коррозии. При этом металл может разрушаться из-
за того, что он служит для этих микроорганизмов питательной сре-
дой, или из-за воздействия на металл продуктов жизнедеятельности
этих микроорганизмов. В чистом виде такой процесс встречается
редко, поэтому при анализе причин разрушения различных конструк-
ций, связанных с биохимической коррозией, их обычно относят к
разрушениям, связанным с электрохимической коррозией.
По условиям протекания процессов коррозии выделяются [1-4]:
– газовая коррозия – коррозия металлов в газах при высоких тем-
пературах и минимальном содержании влаги (как правило, не более
0,1%). В химической, нефтехимической и нефтеперерабатывающей
промышленности такой вид коррозии встречается при получении
серной кислоты на стадии окисления диоксида серы, при синтезе ам-
миака, получении азотной кислоты и хлористого водорода, в процес-
сах синтеза органических спиртов, крекинга нефти и т.д.;
– атмосферная коррозия – коррозия металлов в атмосфере воз-
духа или влажного газа (например, ржавление стальных конструкций
на открытом воздухе);
– жидкостная коррозия – коррозия металла в жидкой среде, как в
неэлектролите, так и в растворах электролита. Различают жидкост-
16
ную коррозию металла при полном, неполном и переменном погру-
жении, погружении по ватерлинии, в неперемешиваемой (спокойной)
и перемешиваемой (движущейся) коррозионной среде;
– подземная коррозия – коррозия металла в почвах и грунтах (на-
пример, коррозия подземных стальных трубопроводов);
– структурная коррозия – коррозия, связанная со структурной
неоднородностью металла. Например, ускорение коррозионного про-
цесса в растворах серной и соляной кислот катодными включениями:
карбидами в стали, графитом в чугуне, интерметаллидом CuAl
2
в дю-
ралюминии;
– коррозия внешним током – электрохимическая коррозия метал-
ла под воздействием тока от внешнего источника. Может наблюдать-
ся в процессе растворения стального анодного заземлителя катодной
защиты подземного трубопровода;
– коррозия блуждающим током – электрохимическая коррозия
под воздействием блуждающих токов (например, коррозия подземно-
го трубопровода);
– контактная коррозия – электрохимическая коррозия, вызванная
контактом металлов, имеющих разные стационарные потенциалы в
данном электролите (например, коррозия в морской воде деталей из
алюминиевых сплавов, находящихся в контакте с медными изделиями);
– щелевая коррозия – коррозия в щелях и зазорах между поверх-
ностями различных конструктивных элементов, а также в местах не-
плотного контакта металла с неметаллическими материалами (на-
пример, в резьбовых и фланцевых соединениях стальных конструк-
ций, находящихся в агрессивной среде);
– коррозия под напряжением – коррозия металла при одновре-
менном воздействии коррозионной среды и механических напряже-
ний. В зависимости от характера нагрузок может иметь место корро-
зия при постоянной и переменной нагрузках. При одновременном
воздействии коррозионной среды и знакопеременных или цикличе-
ских растягивающих нагрузок наблюдается коррозионная усталость –
понижение предела усталости металла;
17
– коррозионная кавитация – коррозия, вызванная одновремен-
ным коррозионным и ударным воздействием внешней среды;
– коррозия при трении – разрушение металлической поверхно-
сти, вызванное одновременным воздействием коррозионной среды и
трения поверхностей, часто этот вид коррозии называют коррозион-
ной эрозией;
– фреттинг-коррозия – коррозия металла при колебательном пе-
ремещении двух поверхностей друг относительно друга в условиях
воздействия коррозионной среды (например, разрушение двух метал-
лических поверхностей, плотно соединенных болтами, в результате
вибрации в атмосфере, содержащей кислород).
По характеру коррозионных разрушений различают следующие
виды коррозии [1-4, 7, 14].
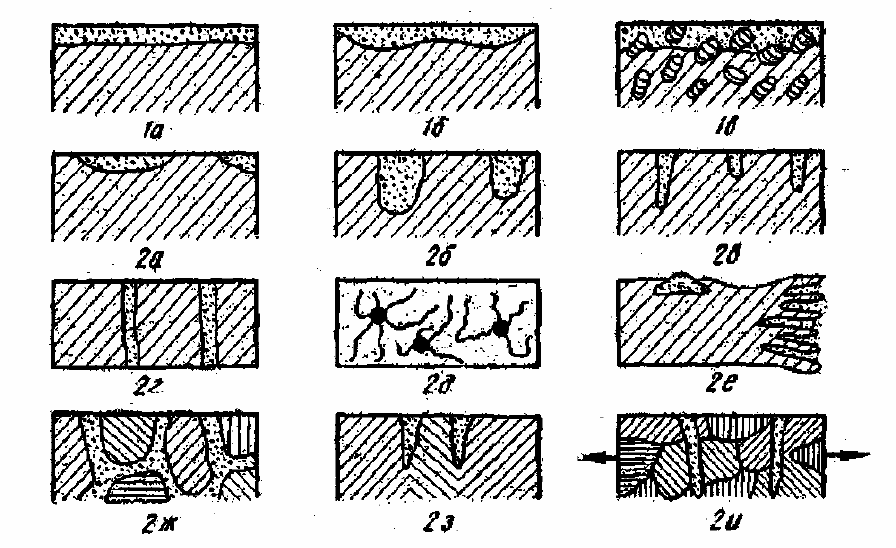
1. Сплошная, или общая коррозия, охватывающая всю поверх-
ность металла (рис. 3), которая также подразделяется на равномерную
(1а) и рис. 4 а, неравномерную (1б) и избирательную (1в), когда раз-
рушается одна структурная составляющая сплава или один его ком-
понент.
Рис. 3. Виды коррозии

18
а б
Рис. 4. Равномерная (а) и местная (б) коррозия
2. Местная коррозия (рис. 4, б), включающая следующие виды
(см. рис. 3):
пятнами (2а) – в виде отдельных пятен;
язвами (2б) – коррозионное разрушение, имеющее вид ра-
ковины. Язвенная коррозия сопровождается образованием неглу-
боких, но широких язв. Обычно ее причиной является нарушение
целостности защитного покрытия;
точечная (2в) – в виде отдельных точечных поражений;
сквозная (2г) – вызывающая разрушение металла насквозь;
нитевидная (2д) – распространяется в виде нитей преимущест-
венно под неметаллическими защитными покрытиями. Является спе-
цифической формой щелевой коррозии. Процесс может происходить
в условиях атмосферной коррозии при относительной влажности
воздуха более 65%. Нить – это самораспространяющаяся щель, в го-
ловке которой преобладает анодный процесс и образуется темный
осадок
2
)(OHFe , а в канале выше кислорода
2
)(OHFe переходит в
более светлый осадок
3
)(OHFe ;
подповерхностная (2е) – начинается с поверхности, но распро-
страняется преимущественно под поверхностью металла таким обра-
зом, что разрушение и продукты коррозии оказываются сосредото-
ченными в некоторых областях внутри металла. Подповерхностная
коррозия часто вызывает вспучивание металла и его расслоение;
