Запорожан В.М., Цегельський М.Р. Гінекологічна патологія: Атлас
Подождите немного. Документ загружается.

9. Плацента
289
фобласта звичайно є більш фокальною і виражена в
меншому ступені, ніж при повному міхуровому заносі,
хоча також може бути надмірною. Домінуючим є син-
цитіотрофобласт, часто з маленькими сосочковими ви-
ростами або ніжками. Фетальні тканини в більшості
випадків відсутні. Характер цих тканин залежить від
гестаційного віку і часу загибелі плода. Інколи живий,
але нежиттєздатний плід з вадами розвитку може на-
родитися в терміні пологів.
Від міхурового заносу слід відрізняти окремий стан,
який дістав назву гідропічного аборту. В цьому разі
тканина, яка евакуюється з матки, звичайно представ-
лена в обмеженій кількості. Гідропічні ворсинки при
макро- і мікроскопічному дослідженні можуть бути
подібними за розмірами до таких при повному міхуро-
вому заносі, але вони поодинокі, їхній середній діаметр
є меншим, ніж при повному або частковому міхурово-
му заносі (рис. 9.15, 9.16). Цистерн немає або вони є
випадковими і не перевищують 3 мм в діаметрі. Деякі
ворсинки можуть бути аваскулярними або фібротизо-
ваними або містити судини з фетальними еритроцита-
ми. На відміну від міхурового заносу, трофобласт при
гідропічному аборті звичайно дифузно розріджений і
має менше атипових рис. Проте гіперплазія ворсинок
трофобласта є типовою для абортів з аномальним ка-
ріотипом, особливо триплоїдних абортусів. Близько 4–
14 % плодів при гідропічних абортах є триплоїдними
внаслідок зайвого материнського набору хромосом.
Гіперплазія, подібна до такої при повному міхурово-
му заносі, спостерігається у разі трисомії 7, 15, 21 або
22. Гіперплазія трофобласта частіше трапляється при
абортах у терміні понад 8,5 тижнів гестаційного віку
за відсутності уніформних гідропічних ворсинок і фе-
тальних тканин.
Диференційний діагноз проводять між повним, част-
ковим міхуровим заносом і гідропічним абортом (табл.
9.1).
Лікування. Відразу після встановлення діагнозу
міхурового заносу слід виконати евакуацію порожни-
ни матки (механічний кюретаж, вакуум-аспірація і зно-
ву гострий кюретаж). Перед операцією проводять рент-
генографію легень і визначають рівень ХГ у сироватці
крові. Евакуацію вмісту матки починають від шийки
і поступово переходять до дна матки. Інфузія оксито-
цину проводиться після спорожнення матки. У пацієн-
ток старшого віку з завершеною репродуктивною фун-
кцією можливо виконання гістеректомії. Потрібно
мати запас крові і кровозамінників, оскільки може ви-
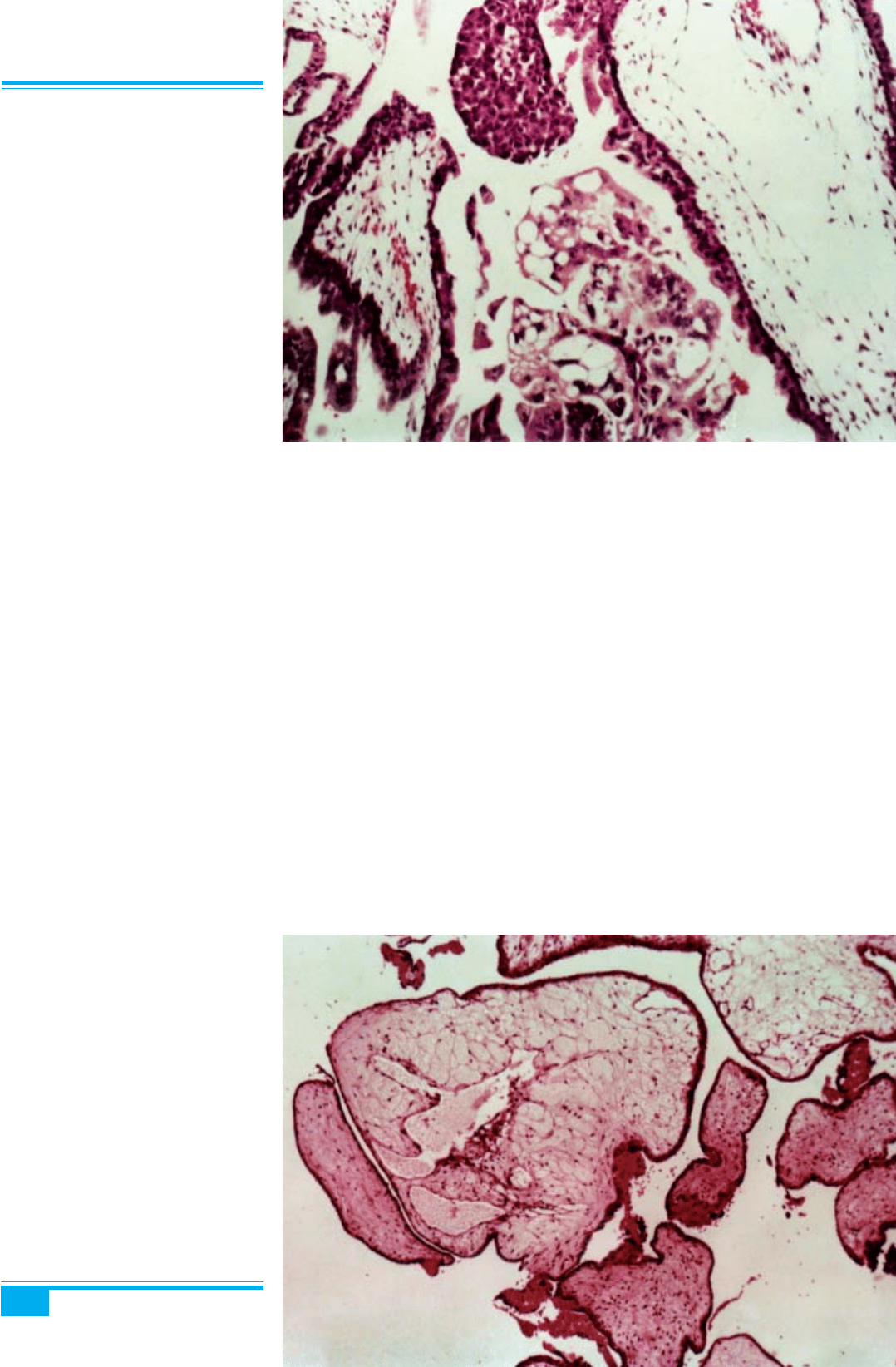
Рис. 9.14. Повний міхуровий занос.
Ядерний детрит у стромі
Рис. 9.15. Гідатиформна трансфор-
мація ворсинок при гідропічному
аборті. Дифузне розрідження тро-
фобласта

Гінекологічна патологія
290
Характерні риси
Найвищий рівень ХГ, МО/мл
Гестаційний вік під час аборту
або евакуації, тиж
Кількість плацентарної тканини порівняно
з нормою для даного терміну
Максимальний діаметр ворсинки, мм
Популяції ворсинок
Поліпоїдні виступи ворсинок
Фестончасті контури ворсинок і круглі
включення в трофобласті
Трофобласт ворсинок
Атипія трофобласта
Цистерни
Каріорексис в судинах ворсинок
Розширені анастомози судин
Фетальні тканини
Вміст ДНК
Хромосомний набір
Нормалізація рівня ХГ після евакуації без
хіміотерапії, днів
Таблиця 9.1
Типові риси міхурового заносу і гідропічного аборту
повний
185 000
12
Надмірна (в 5–10
разів більше)
70
Широкий спектр
Часто
Рідко
Дифузна гіперпла-
зія
Виразна
Часто
Інтенсивний
Рідко
Звичайно відсутні
Диплоїдний/тетра-
плоїдний
46, ХХ; 46, XY
78,3
частковий
66 000
15
Помірно збільшена
(в 2 рази)
50
Дві популяції
Рідко
Часто
Локальна гіпер-
плазія
Рідко
Трапляються
Невиразний
У 20 %
Наявні, аномальні
Триплоїдний
69, ХХХ;
69, XXY;
69, XYY
62,8
Гідропічний
аборт
8000
11
Менше, ніж у нормі
30
Широкий спектр
Рідко
Рідко
Розріджений
Відсутня
Мінімальні
Невиразний
Рідко
Звичайно відсутні
Диплоїдний
46 ± декілька
46,7
Міхуровий занос
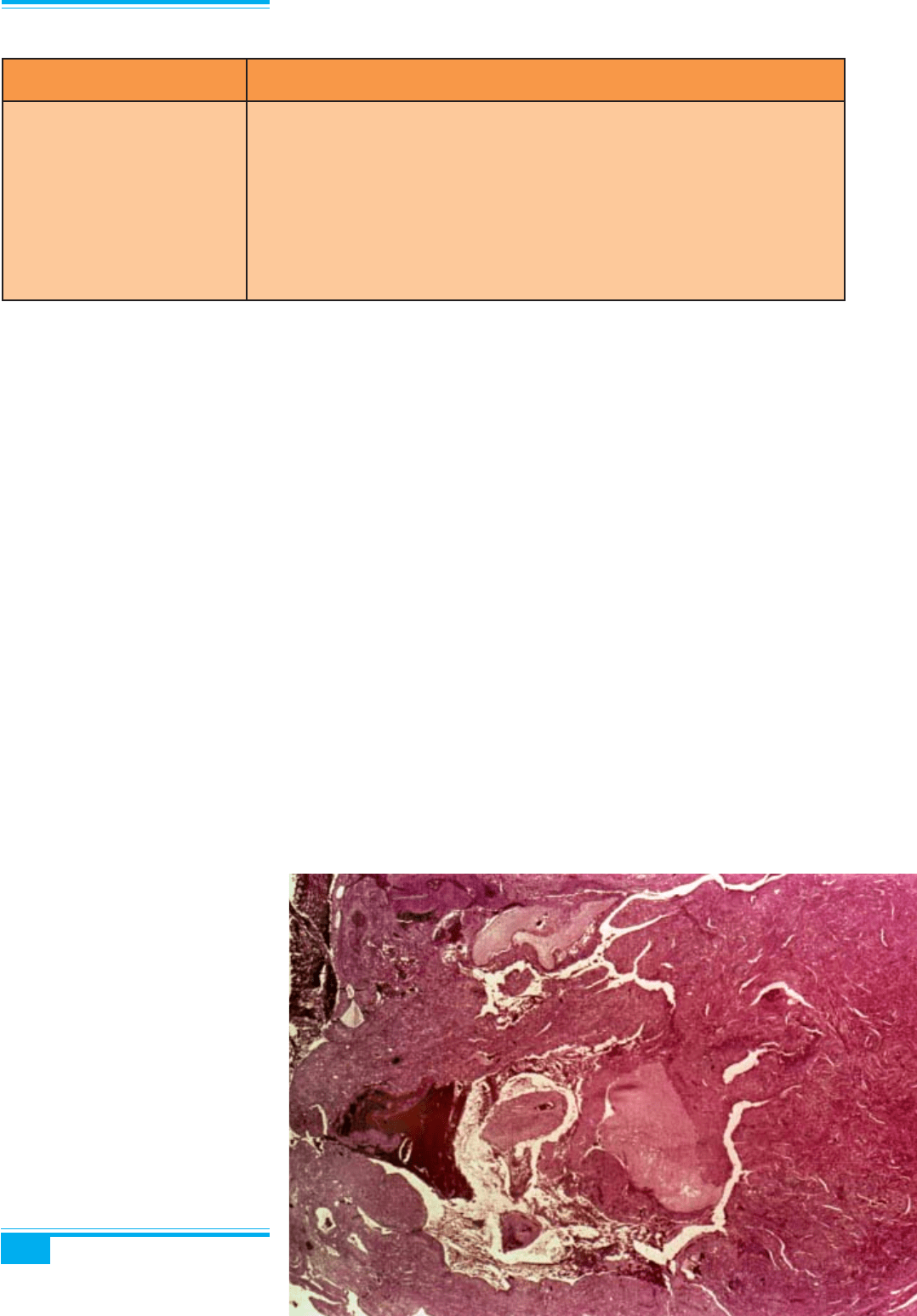
Рис. 9.16. Гідатиформна трансфор-
мація ворсинок при гідропічному
аборті. Аваскулярні ворсинки, набряк
строми, кістозні простори, слабка
проліферація трофобласта
никнути масивна кровотеча з розвитком синдрому дисе-
мінованої внутрішньосудинної коагуляції (ДВК), легене-
вої недостатності. Текалютеїнові кісти звичайно регре-
сують спонтанно протягом 2 місяців.
Після евакуації міхурового заносу щотижня визна-
чають сироватковий рівень ХГ; після його нормалі-
зації контрольні дослідження проводять через 6 і 12
місяців (табл. 9.2).
Персистуючий міхуровий занос виникає у 8–20 %
випадків повного міхурового заносу.
Факторами ризику персистуючої гестаційної тро-
фобластичної хвороби є: попередній міхуровий занос,
рівень ХГ > 100 000 МО/мл, розмір матки перевищує
гестаційний вік, текалютеїнові кісти > 6 см, вік матері.
Клінічними симптомами персистуючого міхурово-
го заносу можуть бути відсутність нормалізації рівня
9. Плацента
291
ХГ після евакуації заносу, початковий рівень ХГ по-
над 100 000 МО/мл, великі розміри матки, наявність
hyperreactio luteinalis, прееклампсія, гіпертиреоїдизм
або трофобластичні емболи. Ведення хворих включає
хіміотерапію та (або) гістеректомію залежно від стадії,
рівня ХГ, бажання зберегти репродуктивну функцію.
Близько 15 % пацієнток з повним міхуровим заносом
потребують проведення хіміотерапії (монохіміотерапія
актиноміцином D, або дактиноміцином).
Інвазивний міхуровий занос (chorioadenoma
destruens) розвивається в 5–10 % випадків повного
міхурового заносу, його можна запідозрити при пер-
систуючому підвищенні рівня ХГ після евакуації зано-
су та відсутності ворсинок при повторному кюретажі
матки. Діагноз інвазивного міхурового заносу підтвер-
джується наявністю міометріальної і судинної інвазії
ворсинок заносу (рис. 9.17–9.19), що потребує гістер-
ектомії, або віддалених метастазів (у легенях, піхві,
вульві, широкій зв’язці матки), які містять ворсинки за-
носу. Ведення пацієнток аналогічно такому при пер-
систуючому міхуровому заносі.
Рецидивна гестаційна трофобластична хвороба
(новий епізод гестаційної трофобластичної хвороби
після повної постхіміотерапевтичної ремісії) діагнос-
тується при підвищенні рівня ХГ після трьох нормаль-
них щотижневих його значень. При відсутності леге-
невих або вагінальних метастазів, рівні ХГ менше
40 000 МО/мл, нетривалому захворюванні ефек-
Заходи, що вживаються
Дослідження рівня ХГ
до нормалізації
після нормалізації
Рентгенограма грудної клітки
Контрацепція
Гінекологічне обстеження
Хіміотерапія
Таблиця 9.2
Ведення пацієнток з міхуровим заносом
Терміни і умови проведення
Щотижня (до його нормалізації)
Щомісяця (6–12 місяців)
До операції і після (при аномальних результатах або підвищенні рівня ХГ)
Протягом 1 року
Кожні 2 тижні до нормальних результатів, потім кожні 3 місяці
Збільшення або персистенція рівня ХГ; наявність метастазів або хоріокар-
циноми; підвищення рівня ХГ через 6 місяців після евакуації заносу; підви-
щення рівня ХГ після його нормалізації
тивність лікування дорівнює 100 %; тимчасом як при
наявності віддалених метастазів (мозок, печінка, нир-
ки), рівні ХГ понад 40 000 МО/мл, розвитку пухлини
після доношеної вагітності — лише 83 %. Ускладнен-
ня міхурового заносу (персистуючий, інвазивний, ме-
тастазуючий, хоріокарцинома) є більш частими після
повного, ніж після часткового міхурового заносу. Ли-
ше близько 5 % пацієнток із частковим міхуровим за-
носом мають персистуючу або метастазуючу хворобу.
Хоріокарцинома
Хоріокарцинома (гестаційна трофобластична пух-
лина, злоякісна гестаційна трофобластична хвороба)
ускладнює 1:20 000–1:25 000 вагітностей. Пухлина
розвивається з епітелію трофобласта, який не має хорі-
альних ворсинок і звичайно локалізується в матці. В
країнах Азії, Африки і Латинської Америки її частота
в 20–40 раз вища, ніж у Західній Європі і США. У 20–
50 % випадків хоріокарцинома виникає після повного
міхурового заносу (хоріокарцинома ускладнює 1 з 40
міхурових заносів); 25 % — після абортів (1:15 000);
22,5 % — після нормальної вагітності (1:160 000) і 2,5 %
— після позаматкової вагітності (1: 5300). Іншими фак-
торами ризику є старший вік матері; чорна раса; гру-
па крові матері А(II), батька — 0(I) і навпаки. Рідко
хоріокарциному виявляють у доношеній плаценті.
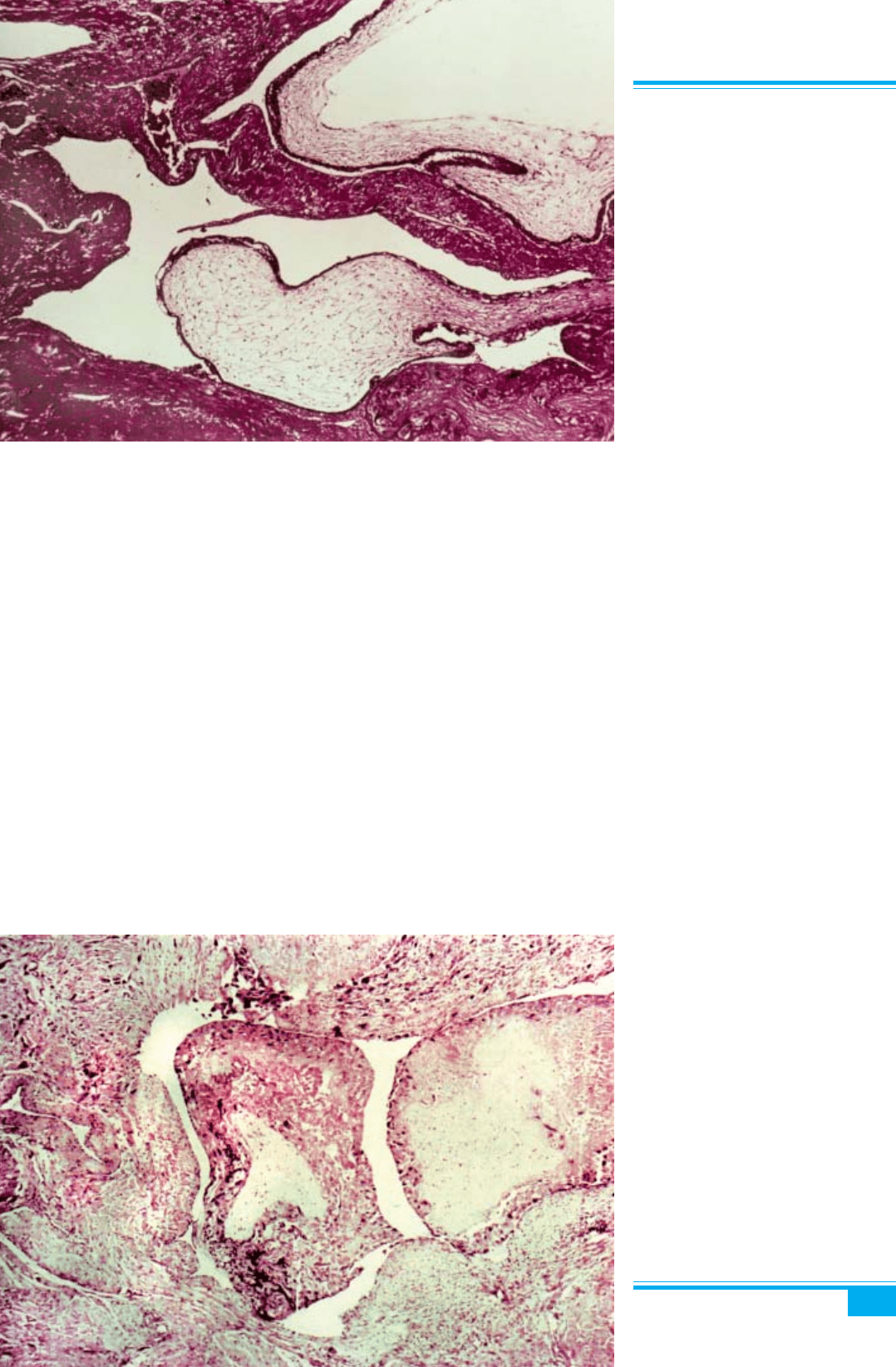
Рис. 9.17. Інвазивний міхуровий за-
нос. Екстенсивна, глибока пенетрація
міометрія ворсинками заносу
Гінекологічна патологія
292
Рис. 9.18. Інвазивний міхуровий
занос. Помірне збільшення гідропіч-
них ворсинок, які локалізуються в
міометрії
Рис. 9.19. Інвазивний міхуровий за-
нос. Інвазивні ворсинки в судинних
просторах, частково оточені фібри-
ном
Клініка і діагностика. Пацієнткам, у яких трива-
ють вагінальні кровотечі після завершення будь-якої
вагітності, обов’язково проводять дослідження рівня
β-субодиниці хоріонічного гонадотропіну (β-ХГ).
Якщо хоріокарцинома обмежена міометрієм, захворю-
вання звичайно є безсимптомним. Найвищі значення
ХГ відмічаються при наявності метастазів (метастазу-
юча гестаційна трофобластична пухлина). У цих ви-
падках скарги хворих пов’язані з локалізацією мета-
стазів (легені, мозок, печінка, нирки, кишки, шкіра).
Найчастіше метастази виявляються в легенях (80–
90 % випадків), рідше — у печінці, мозку, яєчниках і
піхві. З метою діагностики віддалених метастазів ви-
користовують рентгенологічне, ультразвукове дослі-
дження, комп’ютерну томографію і ядерний магнітний
резонанс.
Залежно від локалізації захворювання, тривалості
його симптомів, рівня ХГ, наявності попередньої хіміо-
терапії виділяють групи високого, помірного і низького
ризику гестаційної трофобластичної пухлини (табл. 9.3).
Класифікація гестаційних трофобластичних пухлин
(відповідає класифікації FIGO) використовується для
хоріокарциноми, інвазивного міхурового заносу та
трофобластичних пухлин плаценти. При цих пухлинах
не застосовується класифікація за категорією N (регіо-
нарні лімфатичні вузли). При оцінці стадії хвороби
враховується попередня хіміотерапія, наявність пухли-
ни плацентарної площини. Гістологічна верифікація
пухлини не є конче необхідною.
Стадії I–IV підрозділяються на підгрупи: А (відсутні
фактори ризику); В (один фактор ризику); С (два фак-
тори ризику). Факторами ризику є сироватковий рівень
ХГ понад 100 000 МО/мл і тривалість захворювання
більше 6 місяців після закінчення попередньої вагіт-
ності.
Макроскопічне дослідження: хоріокарцинома мат-
ки звичайно червоного або коричневого кольору, м’я-
систа, з виразними некрозами та геморагіями і деструк-
тивною міометріальною інвазією (рис. 9.20). Поверх-
нева частина пухлини може бути поліпоїдною. Рідко
первинна пухлина розвивається в шийці матки (рис.
9.21). Хоріокарцинома нерідко супроводжується утво-
ренням текалютеїнових кіст яєчників (рис. 9.22). В де-
яких випадках при метастатичній хоріокарциномі пер-
винна пухлина в матці не виявляється, що може свідчи-
ти про її регресію.

9. Плацента
293
Таблиця 9.3
Прогностичні фактори гестаційної трофобластичної хвороби
Фактори
Вік
Попередня вагітність
Інтервал між попередньою вагітні-
стю і початком хіміотерапії, міс
Рівень ХГ, МО/л
Найбільша пухлина, включаючи
матку, см
Місця метастазів
Кількість метастазів
Попередня хіміотерапія
0
< 39 років
Міхуровий занос
<4
<10
3
< 3
1
≥ 39 років
Викидень
4–6
10
3
–10
4
3–4
Селезінка, нирки
1–3
2
Доношена
7–12
10
4
–10
5
≥ 5
Шлунок,
печінка, кишки
4–8
1 препарат
4
>12
>10
5
Мозок
> 8
≥ 2 препаратів
* < 4 балів — низький ризик; 5–7 балів — помірний ризик; > 8 балів — високий ризик
Оцінка, бали*
Гістопатологічне дослідження: основою гістоло-
гічного діагнозу хоріокарциноми є наявність зміша-
ного злоякісного цитотрофобласта і синцитіотрофо-
бласта (рис. 9.23, 9.24). Часто спостерігається пере-
плетена структура пухлини, утворення широких смуг
цитотрофобласта, які перериваються синцитіотрофо-
бластом або проміжним трофобластом. Синцитіотро-
фобласт може вистилати простори, які містять ерит-
роцити.
КЛАСИФІКАЦІЯ ГЕСТАЦІЙНИХ ТРОФОБЛАСТИЧНИХ ПУХЛИН
ЗА СИСТЕМОЮ ТNМ I FIGO
TNM- FIGO-
категорії стадії
Т Первинна пухлина
Тx Не досить даних для оцінки первинної пухлини
Т0 Первинна пухлина не визначається
T1 I Пухлина обмежена маткою
Т2IIПухлина метастазує або безпосередньо розповсюджується на інші геніталії: піхву,
яєчники, широку зв’язку або маткові труби
M1a III Метастази в легені
M1b IV Інші віддалені метастази, з ураженням або без ураження легенів
М — Метастази*
Mx Не досить даних для визначення
віддалених метастазів
М0 Немає ознак віддалених метастазів
М1 Наявні віддалені метастази
М1а Метастази в легеню (легені)
М1b Інші віддалені метастази, з або
без ураження легенів
*Метастази в геніталії розцінюються як Т2.
рТМ Патоморфологічна класифікація
Категорії рТ та рМ відповідають категоріям Т і М
Групування за стадіями
Стадія Т М Фактори
ризику
ІА Т 1 М0 Немає
IВТ1 М0 Один
ІС Т1 М0 Обидва
IIA Т2 М0 Немає
IIB Т2 М0 Один
ІІС Т2 М0 Обидва
ІІІА Будь-яке ТМ1а Немає
IIIB Будь-яке ТМ1а Один
IIIC Будь-яке ТМ1а Обидва
IVA Будь-яке ТМ1b Немає
IVB Будь-яке ТМ1b Один
IVC Будь-яке ТМ1b Обидва
Синцитіотрофобласт має інтенсивну еозинофільну
цитоплазму і численні великі везикулярні ядра зі скуп-
ченим хроматином. Цитотрофобласт складається з дис-
кретних, мононуклеарних, овальних чи полігональних
клітин зі світлою цитоплазмою, скрученими ядрами та
збільшеними ядерцями. Спостерігаються численні, в
тому числі атипові мітози. Проміжний трофобласт має
мікроскопічні риси пухлини плацентарної площини, у
тому числі виразну клітинну атипію.
Гінекологічна патологія
294
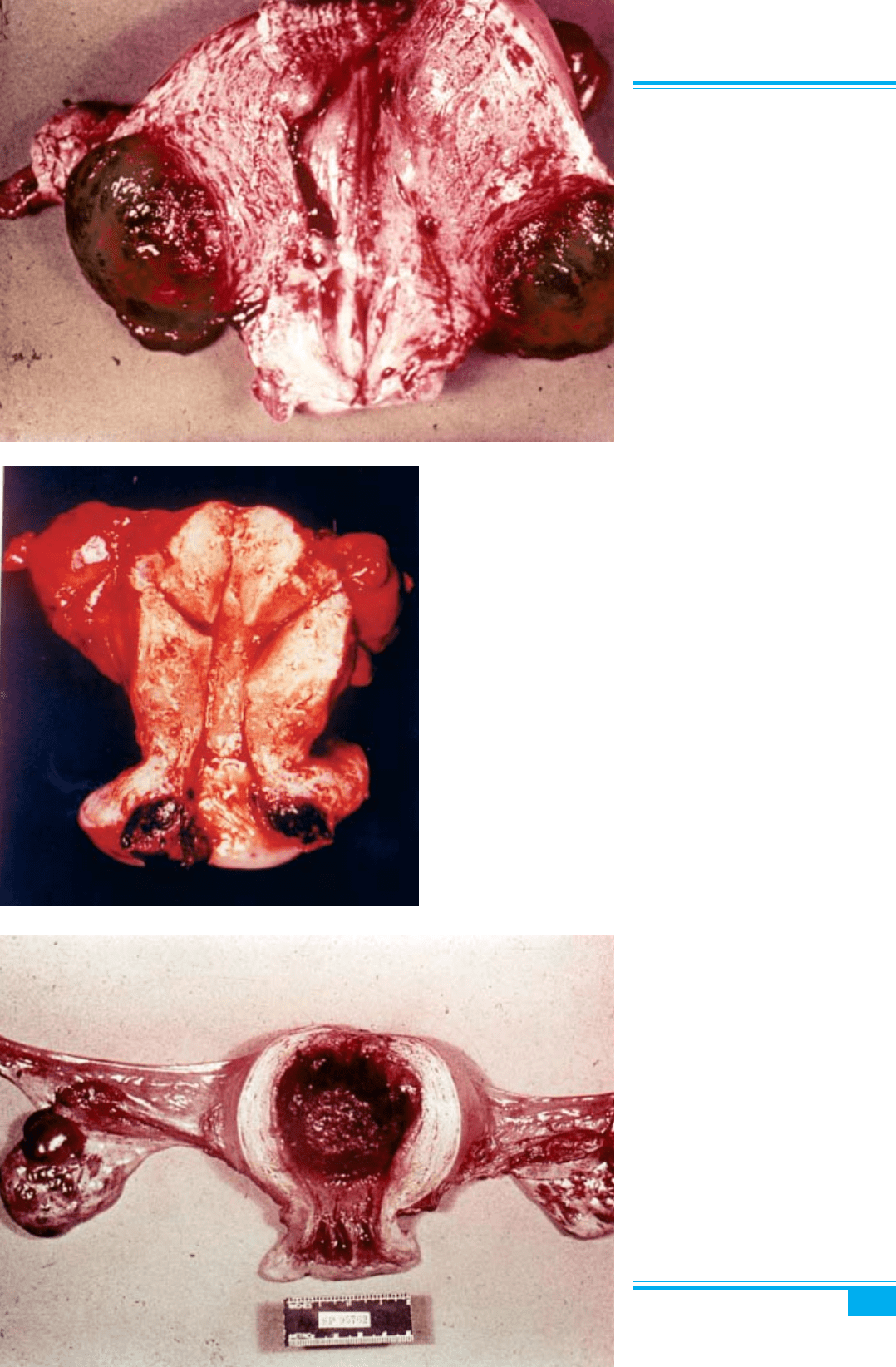
Рис. 9.20. Хоріокарцинома матки.
Сферичні геморагічні фокуси пухлин-
ної тканини в міометрії
Рис. 9.21. Первинна хоріокарцино-
ма шийки матки
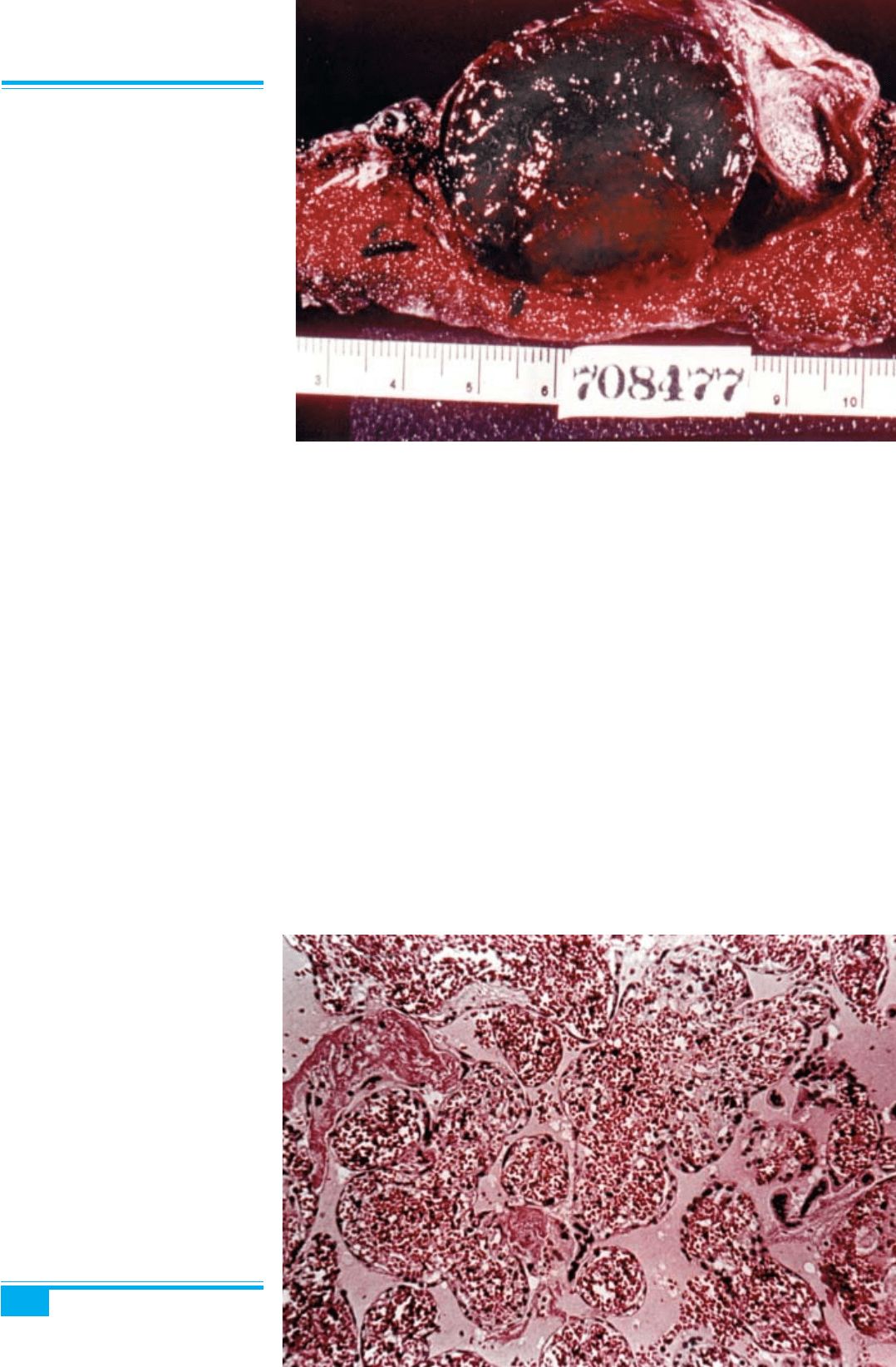
Рис. 9.22. Хоріокарцинома матки
і текалютеїнові кісти яєчників. Гемо-
рагічна некротична пухлина випов-
нює порожнину матки
9. Плацента
295
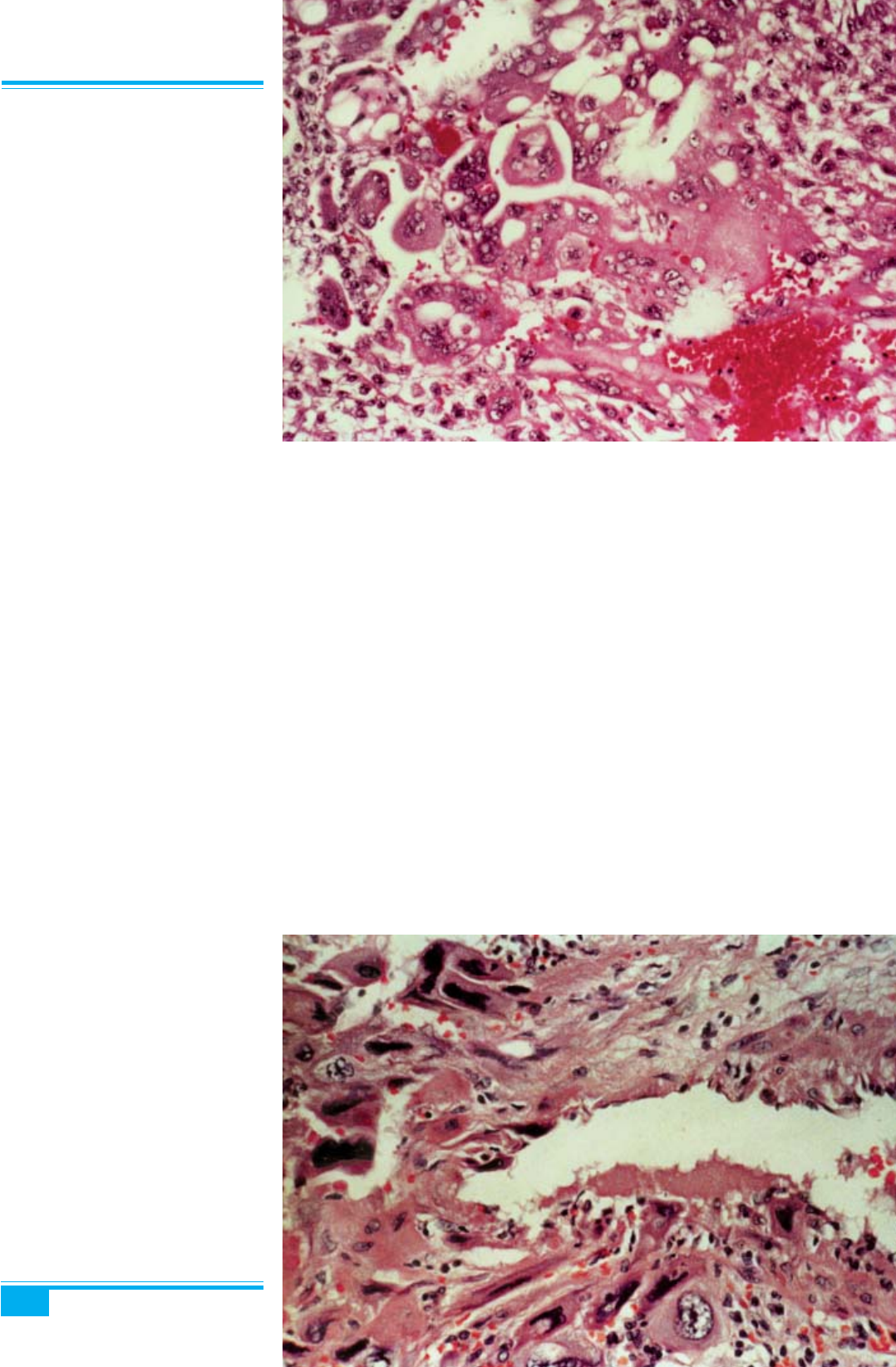
Рис. 9.24. Хоріокарцинома матки.
Атиповий цитотрофобласт і синци-
тіотрофобласт, крововиливи. Великі
ядра в клітинах синцитіотрофоблас-
та
Рис. 9.23. Хоріокарцинома матки.
Примітивні стовпи трофобластних
епітеліальних клітин. Стовпи цито-
трофобласта оточені синцитіотрофо-
бластом, який вистилає кістозні про-
стори, виповнені кров’ю
Термін атипова хоріокарцинома застосовується в
рідкісних випадках хоріокарциноми, коли деякі або всі
пухлини складаються переважно з цитотрофобласта,
проміжного трофобласта і ріденького синцитіотро-
фобласта. Ця структура може виявлятися в первинних
або метастатичних пухлинах і, в деяких випадках, після
хіміотерапії. Деякі або всі ці пухлини можуть бути іден-
тичними епітеліоїдній трофобластичній пухлині.
Хоріокарцинома звичайно інвазує міометрій і міо-
метріальні судини. Хоріокарцинома з виразними інфарк-
тами може бути складною для гістологічної інтерпре-
тації (часто вона представлена лише периферичною зо-
ною пухлини, яка оточує великі зони некрозів).
Диференційний діагноз проводять з простим (неди-
ференційованим) трофобластом, нормальним трофо-
бластом ворсинок, проміжним трофобластом, вузлами
плацентарної площини; негестаційною (зародковоклі-
тинною) метастатичною хоріокарциномою; аденокарци-
номою ендометрія з трофобластичною диференціацією,
хоріоангіокарциномою, іншими злоякісними епітеліаль-
ними і мезенхімальними пухлинами (можуть симулюва-
ти атипову хоріокарциному). Диференційний діагноз
базується на даних анамнезу (попередня вагітність,
міхуровий занос), серологічній та імуногістохімічній
ідентифікації ХГ, інгібіну і плацентарного лактогену.
Лікування. Хірургічне лікування при хоріокарци-
номі проводиться лише за життєвими показаннями (за-
гроза кровотечі) або при резистентності пухлини до
хіміотерапії. Планова гістеректомія виправдана у хво-
рих віком понад 40 років, за відсутності метастазів
або у разі резистентності до хіміотерапії.
У хворих з неметастазуючою гестаційною трофо-
бластичною пухлиною, а також з метастазуючою, але
низького ризику (зі сприятливим прогнозом) проводять
монохіміотерапію (метотрексат або актиноміцин D —
дактиноміцин). Лікування триває до нормалізації рівня
ХГ; після цього призначають ще 1–2 додаткових кур-
си хіміотерапії. Рецидиви можливі в 5 % випадків і зви-
чайно не спостерігаються пізніше ніж через 6–12
місяців після лікування. Щотижневе дослідження рівня
β-ХГ проводять до трьох послідовних нормальних його
значень, потім — щомісячне дослідження рівня ХГ про-
тягом 6–12 місяців, після чого дозволяють вагітність.
Навіть за наявності рецидивів хіміотерапія є ефектив-
ною в 100 % хворих при неметастазуючій гестаційній
трофобластичній хворобі низького ризику.
З метою лікування гестаційної трофобластичної
пухлини з поганим прогнозом використовують полі-

Гінекологічна патологія
296
хіміотерапію (схема МАС: метотрексат, актиноміцин
D і хлорамбуцил або циклофосфамід; СНАМОСА
(гідроксисечовина, вінкристин, метотрексат, цикло-
фосфамід, актиноміцин D, доксорубіцин, кальцію фо-
лінат); VP-16 (етопозид); ЕМА/СО (етопозид, метотрек-
сат, актиноміцин D, циклофосфамід, вінкристин (он-
ковін)) на фоні моніторингу рівня ХГ у сироватці
крові. Цикли повторюють кожні 9–14 днів, залежно
від переносимості. Додаткові два курси хіміотерапії
проводять після нормалізації рівня ХГ. Рецидиви мож-
ливі в 20 % випадків. При метастазах у мозок засто-
совують променеву терапію.
Після нормалізації рівня ХГ протягом 3 циклів його
рівень визначають кожні 2 тижні протягом 3 місяців і
потім щомісяця протягом 1 року; потім кожні 6 місяців
протягом 5 років з метою виявлення пізніх рецидивів.
Рентгенологічне дослідження грудної клітки повторю-
ють кожні три місяці протягом першого року спосте-
реження. Через 1 рік після досягнення нормалізації по-
казників ХГ дозволяють вагітність. Наступна вагіт-
ність звичайно є нормальною. Пацієнтки, які одержу-
вали лікування актиноміцином D (дактиноміцином),
мають збільшений ризик аномалій розвитку плода,
тому обов’язковим є ранній ультразвуковий моніто-
ринг. Після пологів контролюють рівень ХГ (мож-
ливість рецидивів). Плаценту піддають ретельному
гістологічному дослідженню.
Прогноз. П’ятирічне виживання хворих після хіміо-
терапії для всіх стадій хоріокарциноми без метастазів
дорівнює 80 %, з метастазами — 70 %. Несприятливи-
ми прогностичними факторами є рівень ХГ до лікуван-
ня понад 100 000 МО/мл, метастази в печінку або в
мозок, відстрочення хіміотерапії внаслідок запізнілої
діагностики; інтервал понад 4 місяці після завершен-
ня попередньої вагітності.
Смерть настає від кровотечі, пов’язаної з метаста-
зами, легеневої недостатності або несприятливих
ефектів хіміотерапії.
Хоріоангіокарцинома — рідкісна пухлина, яка
складається з негідропічних ворсинок, вистелених зло-
якісним трофобластом, асоційованим з судинною про-
ліферацією ворсинок. Пухлина не має малігнізуючих
наслідків для матері і новонародженого.
Нормальний проміжний трофобласт поділяється на
3 різні морфологічні та імуногістохімічні субтипи: про-
міжний трофобласт ворсинок (клітини проміжного тро-
фобласта у трофобластичних стовпах) і 2 інших типи,
які походять від першого: проміжний трофобласт місця
імплантації і проміжний трофобласт хоріального типу.
До уражень проміжного трофобласта (змішаних
трофобластичних уражень) належать збільшення пла-
центарної площини (синцитіальний ендометрит), а та-
кож вузли і диски плацентарної площини, які потребу-
ють диференціації з так званою трофобластичною пух-
линою плацентарної площини.
Трофобластична пухлина
плацентарної площини
Це рідкісна форма гестаційної трофобластичної хво-
роби. Виникає переважно в репродуктивному віці (се-
редній вік — 28 років), хоча можливі випадки розвит-
ку хвороби і в постменопаузі.
Клініка і діагностика. Можуть спостерігатися аме-
норея, мено- і метрорагії, збільшення розмірів матки
(до 8–16 тижнів вагітності). Нерідко захворювання
може симулювати звичайну або завмерлу вагітність
(missed abortion). При вишкрібанні матки часто трап-
ляється її перфорація. В анамнезі хворих звичайно на-
явна попередня нормальна вагітність або, рідше, спон-
танний аборт. Сироватковий рівень ХГ злегка підви-
щений у 45 % хворих, помірно підвищений — у 30 %
пацієнток; у решті випадків рівень ХГ є нормальним.
Менш часті симптоми можуть включати вірилізацію
під впливом стромального гіпертекозу (дія підвищено-
го рівня ХГ), еритроцитоз або гіперпролактинемію, не-
фротичний синдром внаслідок хронічного синдрому
ДВК (дисемінованої внутрішньосудинної коагуляції).
Макроскопічне дослідження: пухлинна маса зви-
чайно поліпоїдна, інколи виповнює порожнину матки
або інфільтрує міометрій; можливі випадки перфорації
міометрія. Поліпоїдні маси часом розповсюджуються
на шийку матки. Пухлина може бути чітко окресле-
ною, але межу пухлини в міометрії звичайно тяжко роз-
пізнати внаслідок дифузного збільшення матки. Рідко
спостерігається кістозна трансформація пухлини та її
розповсюдження на яєчники.
Мікроскопічне дослідження: трофобластична пух-
лина плацентарної площини складається переважно з
багатогранних, круглих або, інколи, веретеноподібних
клітин проміжного трофобласта. Клітини можуть бути
одно- або багатоядерними. Інколи багатоядерні кліти-
ни нагадують синцитіотрофобластні. Цитоплазма зви-
чайно рясна, амфофільна, але може бути еозинофіль-
ною або світлою. Ядра варіюють від маленьких до ве-
ликих, скручених, гіперхромних і брудних. Ядерця мо-
жуть бути виразними. Інколи помітні внутрішньоядерні
включення. Мітотична активність звичайно не переви-
щує 2 мітотичних фігур у 10 полях зору, але інколи бу-
ває вище 5 мітозів у 10 полях зору. Типовими є ано-
мальні мітотичні фігури.
Трофобластична пухлина плацентарної площини
часто супроводжується міоінвазією. Міометральна
Прогностична класифікація злоякісної гестаційної
трофобластичної хвороби
I. Неметастазуюча гестаційна
трофобластична пухлина
II. Метастазуюча гестаційна трофобластична
пухлина: хвороба за межами матки
А. Сприятливий прогноз:
1. Захворювання персистує менш ніж
4 місяці (короткотривале).
2. Рівень β-ХГ до лікування менше
40 000 МО/мл.
3. Відсутність попередньої хіміотерапії.
Б. Несприятливий прогноз:
1. Захворювання персистує понад 4 місяці
(довготривале).
2. Рівень β-ХГ до лікування понад
40 000 МО/мл.
3. Виявлення позалегеневих і позапіхвових
метастазів (печінка, мозок).
4. Незадовільні результати попередньої
хіміотерапії.
9. Плацента
297
інвазія представлена клітинними агрегатами або по-
одинокими клітинами, які локалізуються між м’язови-
ми волокнами. Інколи пухлина має інвазивні краї і су-
проводжується гіалінізацією, як і типовий вузол пла-
центарної площини. Пухлина в 1/3 випадків досягає
серозної оболонки матки і, інколи, ендоцервіксу. Не-
рідко виявляється судинна інвазія пухлинними кліти-
нами з відкладенням фібрину в судинній стінці та
просвіті кровоносних судин. У прилеглому до пухли-
ни ендометрії може спостерігатися децидуальна реак-
ція та (або) Аріас–Стелли феномен. Ворсинки хоріона
трапляються дуже рідко.
Імуногістохімічне дослідження: трофобластична
пухлина плацентарної площини є імунореактивною до
цитокератину, плацентарного лактогену та інгібіну і,
лише фокально, до хоріонічного гонадотропіну. Про-
ліферативний індекс Кі-67 є високим у 90 % хворих.
Диференційний діагноз проводять зі збільшенням
плацентарної площини (відсутня інвазія міометрія,
низький проліферативний індекс Кі-67); з хоріокарци-
номою (геморагічні та некротичні маси, висока реак-
тивність до ХГ, вищий проліферативний індекс Кі-67);
епітеліоїдною лейоміосаркомою (гістоструктура, іму-
нореактивність до десміну); світлоклітинною карцино-
мою ендометрія і плоскоклітинною карциномою ший-
ки матки з некрозами і гіалінізацією (за клінічними і
лабораторними показниками, рівнем ХГ і плацентар-
ного лактогену, типовою міоінвазією та судинною
інвазією, імунореактивністю).
Прогноз. У 15–20 % пацієнток трофобластична пух-
лина плацентарної площини має злоякісну поведінку з
метастазуванням у легені, печінку, центральну нерво-
ву систему. Злоякісні пухлини звичайно виявляють ви-
соку мітотичну активність (понад 4 мітози в 10 полях
зору) і значно рідше — менший мітотичний індекс.
Більш злоякісні пухлини характеризуються наявністю
великих некрозів і збільшенням кількості клітин зі
світлою цитоплазмою.
Лікування полягає в екстирпації матки. Трофоблас-
тичні пухлини плацентарної площини звичайно є резис-
тентними до хіміотерапії. При наявності метастазів за-
стосовуються хіміотерапевтичні агенти.
Епітеліоїдна трофобластична пухлина (вузли про-
міжного трофобласта) — рідкісна трофобластична пух-
лина, яка утворюється проміжним трофобластом хорі-
ального типу і має риси, відмінні від хоріокарциноми
і трофобластичної пухлини плацентарної площини.
Рис. 9.25. Хоріоангіома. Темно-чер-
воні м’які пухлинні маси
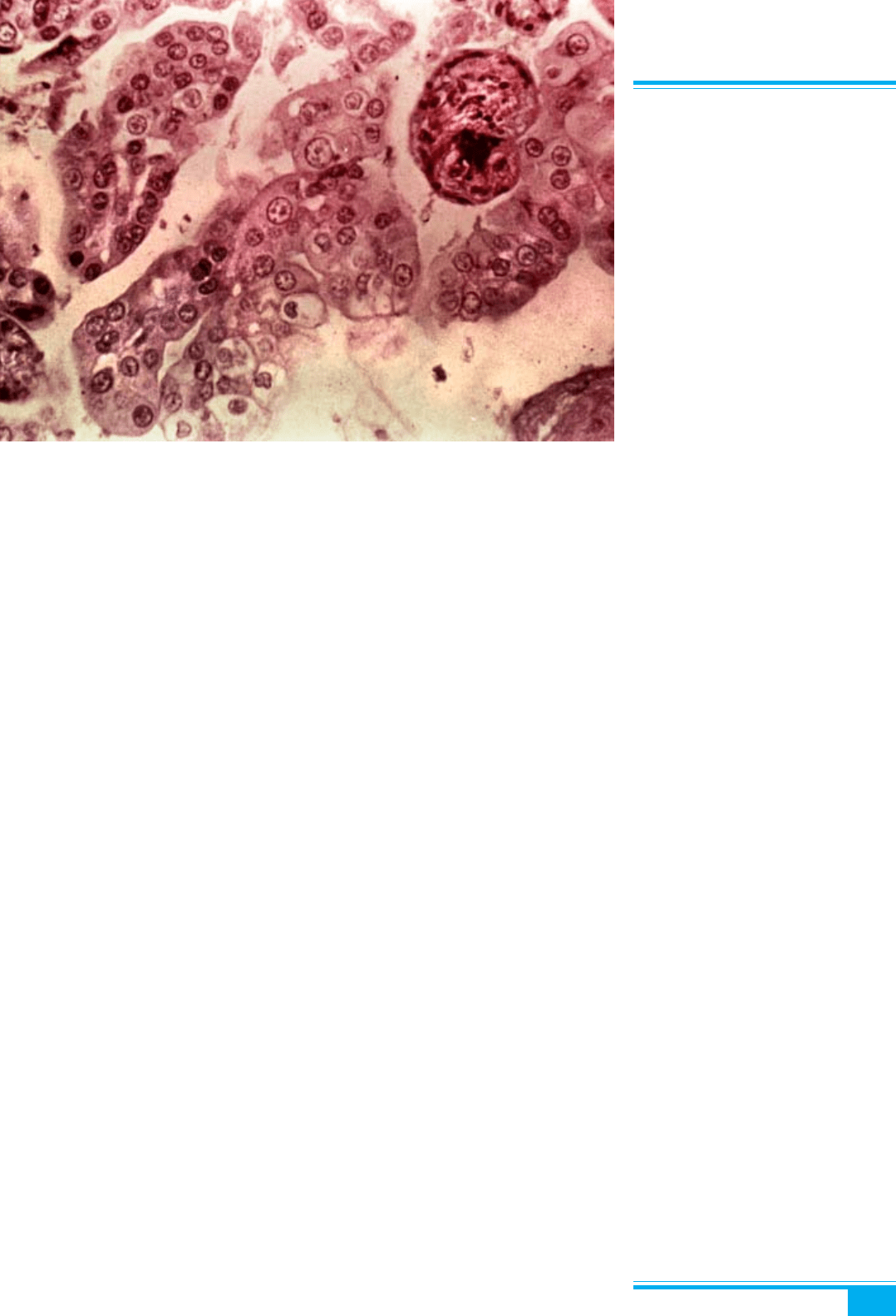
Рис. 9.26. Інфаркт у хоріоангіомі.
Виразні капіляри серед фіброзної тка-
нини з хоріальними стромальними
клітинами
Гінекологічна патологія
298
Клінічними симптомами можуть бути аномальні вагінальні
кровотечі, підвищений рівень ХГ. В анамнезі більшості
пацієнток є свідчення про недавню вагітність.
Макроскопічне дослідження: пухлина є солідною або
кістозною, геморагічною, може локалізуватися в будь-
якій частині матки і характеризується глибокою інвазією.
Мікроскопічне дослідження: пухлина нагадує низь-
кодиференційовану карциному і має вузлові експан-
сивні краї, оточені лімфоцитним інфільтратом. Уні-
формні круглі одноядерні клітини утворюють «гнізда»
та смуги і містять еозинофільний гіаліновий матеріал.
Некрози є частими. Мітотична активність становить
2 мітози в 10 полях зору. Пухлинні клітини звичайно є
імунореактивними до цитокератину, ЕМА й α-інгібіну
і лише фокально — до плацентарного лактогену і ХГ.
Диференційний діагноз проводять з трофобластич-
ною пухлиною плацентарної площини (інфільтративна
смугоподібна структура, виразна судинна інвазія,
більший ступінь плеоморфізму); плоскоклітинною кар-
циномою шийки матки (містить кератин, відсутня іму-
нореактивність до інгібіну і цитокератину 18); епіте-
ліоїдною гладком’язовою пухлиною (містить компо-
нент гладком’язових клітин; відсутня імунна реак-
тивність до α-інгібіну, плацентарного лактогену і хо-
ріонічного гонадотропіну).
Епітеліоїдна трофобластична пухлина здатна до
метастазування.
Лікування включає кюретаж, гістеректомію, хіміо-
терапію, або їх комбінацію.
Плацентарний поліп — поліпоїдний фрагмент за-
триманої в матці плацентарної тканини, який звичай-
но виявляється при вишкрібанні матки після пологів.
Головним клінічним симптомом є аномальні маткові
кровотечі. Затримка частин плаценти в матці виникає,
можливо, внаслідок локального порушення або
відстрочення інволюції плацентарного ложа.
При мікроскопічному дослідженні виявляють вор-
синки, змішані зі згустками крові, фібрином і матко-
во-плацентарними судинами.
Хоріоангіома — найчастіша доброякісна пухлина
плаценти (трапляється в 1 % усіх пологів).
Клініка і діагностика. Під час вагітності хоріоан-
гіома може проявлятись ознаками плацентарної недо-
статності, багатоводдям, аномаліями розвитку плода,
передчасними пологами.
Макроскопічне дослідження: пухлина є круглою,
твердою або м’якою, геморагічною, інкапсульованою,
червоно-пурпурного кольору, діаметром 5–6 см (рис.
9.25).
Гістологічне дослідження: виявляється високоди-
ференційована капілярна структура доброякісного ен-
дотелію і фіброзна тканина з хоріальними стромаль-
ними клітинами; нерідко спостерігаються інфаркти
(рис. 9.26). Капіляри містять фетальні ядерні еритро-
цити. Асоційованою аномалією може бути одна арте-
рія пуповини.
Плацентарні метастази материнських пухлин є
дуже рідкісними вторинними пухлинами. Вони розпов-
сюджуються гематогенним шляхом і виникають лише
у разі дисемінованих злоякісних пухлин. Відповідно до
частоти, метастази можуть бути представлені злоякіс-
ною меланомою, раком молочної залози або бронхів
(рис. 9.27).
При метастазах злоякісної меланоми ураження
плаценти є видимим, має вигляд чорних або темно-
коричневих вузлів різного розміру в тканині пла-
центи.
Мікроскопічне дослідження: виявляються широкі
смуги клітин злоякісної меланоми в міжворсинковому
просторі.
Плацентарні метастази пухлин плода є дуже
рідкісними і спостерігаються при нейробластомі.
Макроскопічне дослідження: пухлина розміщуєть-
ся у великій блідій плаценті, маса якої досягає 1 кг.
При гістологічному дослідженні виявляються проб-
ки нейробластоматозних клітин у фетальних судинах
ворсинок.
Рис. 9.27. Метастатична карцино-
ма плаценти (можливо, метастаз раку
молочної залози)
