Менделевич В.Д. (ред) Руководство по аддиктологии
Подождите немного. Документ загружается.

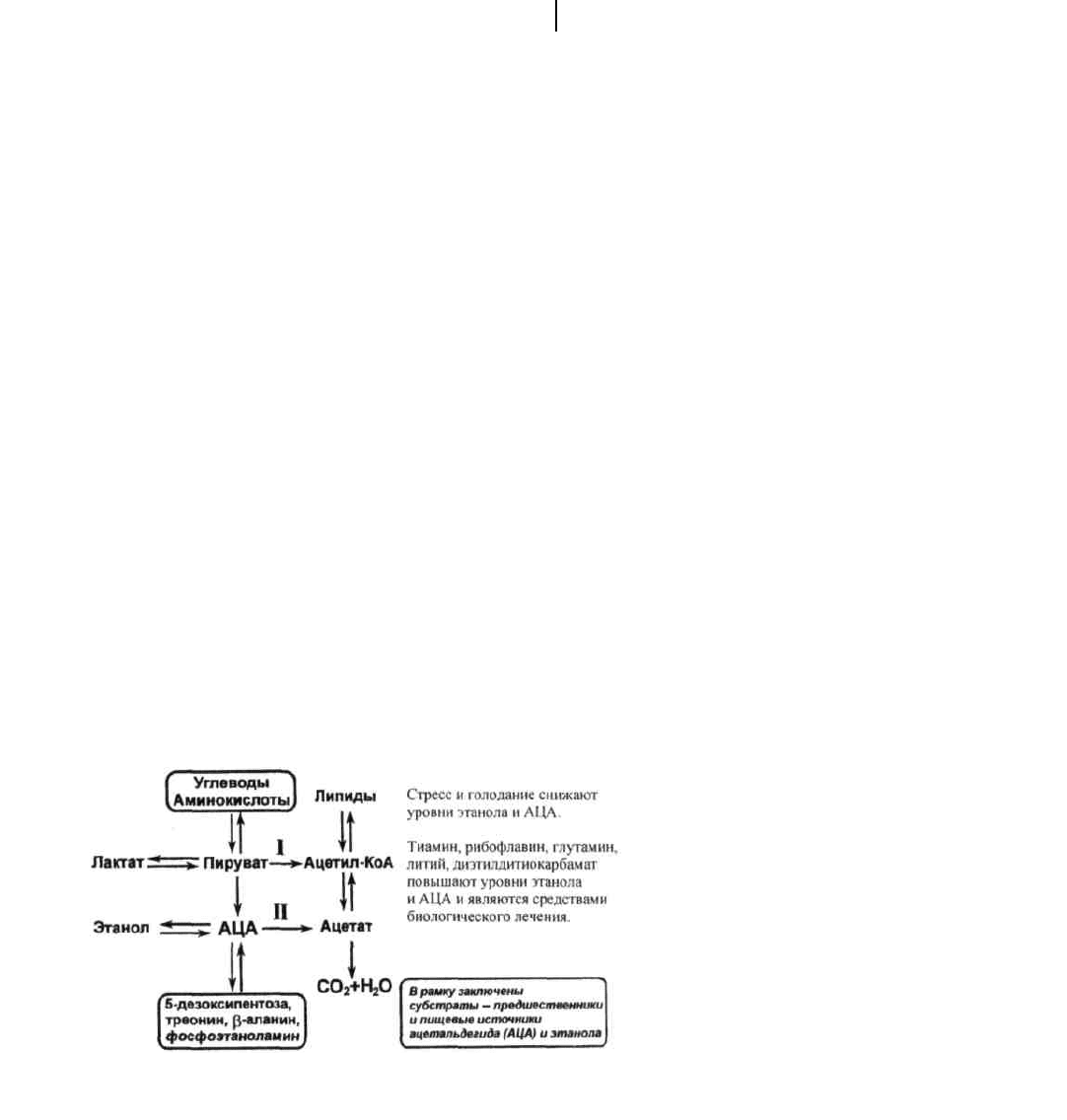
Подходы к метаболитной и энзимной терапии в наркологии
251
• ароматические аминокислоты — источники катехоламиновых нейромедиато-ров: тирозин (предшественник ДОФА и
дофамина с участием ферментов; тирозин-3-гидроксилазы и ДОФА-декарбоксилазы); триптофан (предшественник серотонина с уча-
стием триптофан-5-гидроксилазы); гистидин (предшественник синтеза гистамина с участием специфической и неспецифической
декарбоксилаз);
• серосодержащие аминокислоты: таурин (слабый Р-адренергический агонист, активирует высвобождение норадреналина,
повышает синтез дофамина, подавляет захват и освобождение Са 1+ синаптосомами мозга);
• монокарбоновые аминокислоты: глицин функционирует как ингибиторный медиатор, главным образом в спинном мозге;
предшественник этаноламина и эндогенного этанола; синтезируется в мозге из глюкозы и серина с участием оксиметилтрансферазы;
• пептиды выполняют регуляторную роль, участвуя в синаптической и дистантной передаче нервных импульсов, выступают как
модуляторы других медиаторов; обеспечивают психосоматические взаимодействия (Ашмарин, 1999): опиоидные пептиды; хо-
лецистокинин; ангиотензин; брадикинин; окситоцин; тиролиберин; кортиколиберин; бомбезин; ангиотензин; вазопрессин; субстанция
Р; соматостатин; люлиберин; нейро-пептид Y и другие;
• пуриновые нукпеотиды: АТФ — медиатор в синапсах вегетативных нервов гладких мышц, функционирует через Са1+-каналы;
аденозин—тормозящий нейромодулятор, действует через метаботропные рецепторы, опосредованно через К+- и Са1+-ионные каналы.
Помимо собственной нейромедиаторной активности самих аминокислот, известна также их опосредующая роль в поддержании
функционального состояния (тонуса) звеньев вегетативной нервной системы. Так, уровень ароматической аминокислоты триптофана
влияет на процессы синтеза серотонина и мелатонина в организме, что, в свою очередь, во многом определяет аффективную
симптоматику у алкогользависимых пациентов.
Аминокислоты рассматривают также в качестве источников лактата и пирувата — предшественников эндогенных ацетальдегида и
этанола, которые служат альтернативным медикаментозному способом подавления или предотвращения влечения к алкоголю.
Все вышесказанное позволяет заключить, что, вероятно, качественная и количественная адекватность питания, характер
используемой пищи по составу белков, углеводов может влиять на интенсивность синтеза и транспорт необходимых аминокислот в
мозг и, соответственно, определять психоневрологические расстройства в отдельных клинических состояниях.
Рис. 7. Пути (
I
и
II
) восполнения и формирования резерва 2
-
углеродных эквивалентов
(по Ю. Островскому) как альтернатива потреблению алкоголя или снятию влечения
к алкоголю медикаментозными ме
тодами

252 Алкоголизм (алкогольная зависимость и алкогольная болезнь)
Показано также, что введение липоевой кислоты — эффективное метаболитное средство на всех этапах лечебно-
реабилитационного процесса (Дудко, Панченко. Пирожков, 2004). Введение глутамата смягчает симптомы аммонийной комы при
функциональной недостаточности печени.
Известно, что витамины (аскорбиновая кислота, группы В) участвуют как кофер-менты в реакциях синтеза нейроактивных
аминокислот и метаболитов. Поэтому их адекватная поставка в организм во многом определяет полноценное функционирование
отделов нервной системы. Таурин рассматривают как наиважнейший гармонизатор выведенной из равновесия нервной системы.
Нетрудно видеть, что все перечисленные методы и средства представляют собой, по сути, разновидность заместительной терапии и
малозатратный путь вторичной профилактики. Фармацевтические формы биологически активных добавок и композитных смесей,
потенциально эффективных при алкогольной и других видах химической зависимости, приведены в таблице. Необходимо добавить
также, что многие из вышеперечисленных метаболитных и энзимных средств рекомендованы как эффективные лечебные и
протекторные препараты органопатоло-гических осложнений при химической зависимости.
11.15.3. Ограничения применения метаболитной и энзимной терапии
Воплощение в практику метаболитной и ферментной диеты неоднозначно просто и требует строго дифференцированного подхода
и в плане индивидуального подбора биокорректоров, и в плане их дозировки. Какие предупредительные мотивы и ограничения
известны на сегодня? Некоторые из них приведены ниже.
Обоснование дифференцированного применения метаболитной терапии и биокоррекции:
I. Особенности биохимической конституции:
I) ацетиляторный тип (скорость окислительного метаболизма); 2) метаболическая и функциональная толерантность к алкоголю
(активность АДГ, АльДГ, ГГТ); 3) биоритмологическая организация (сбой или отсутствие у наркозависимых индивидуальной
фенотипической категоризации: спринтеры—стайеры, ритмоводители—ритмоведомые, совы—жаворонки и нарушенный внутренний
контроль индивидуального «чувства времени». Это обусловливает нарушение фармакокинетики, сбой функционирования т. н.
метаболических часов и неспособность фазовой синхронизации при доставке биокорректора к цели).
II. Нарушение эндогенной биорегуляции поддержания субстратного баланса «депо—антидепо» и системы «метаболитных
качелей» в конкретный момент времени.
III. Существование принципа гомеопатической доктрины, подразумевающего возможность высокой токсичности даже
физиологических субстратов-метаболитов (например, дофамина, гистамина, гамма-оксибутирата и др.).
ГУ Существование принципа функциональной архитектоники (компартментализа-ции депо аминокислот), которая изменяется у
людей, зависимых от ПАВ, из-за нарушения барьерных, транспортных и рецепторных функций биологических мембран.
V Измененная реактивность у зависимых от ПАВ (вследствие нарушения питания, всасывания, свойств константности
биохимических систем и других. См. пункт I. Например, отмечено, что кишечник алкогользависимого НЕ СПОСОВЕН усваивать
пищевые источники фолатов, тиамина и втгамина В,.

Подходы к метаболитной и энзимной терапии в наркологии
253
VI. Способность некоторых метаболитов, компонентов биодобавок образовывать высокотоксичные и иммунореактивные
комплексы с низкомолекулярными соединениями.
Важно: все перечисленные выше обоснования (I—VI) связаны между собой причинно-следственными взаимоотношениями,
игнорировать которые нельзя.
Во-первых, известно, что толерантность к алкоголю, как и, вероятно, к другим ПАВ. определяется соотношением активности
участвующих в метаболических превращениях ПАВ ферментных систем: в первую очередь — алкоголь- и альдегиддегидрогеназ.
мик-росомальной этанолокисляющей системы с цитохромом Р-450, а также каталазы, гамма-глутамилтрансферазы и других. Во-
вторых, соответственно конституциональным типам (т. н. быстрым или медленным ацетиляторам, спринтерам и стайерам) в
норме существует несколько вариантов сочетаний функциональных мощностей этих ферментных систем, что необходимо
учитывать и у наркозависимых пациентов. Индивиды —быстрые и медленные ацетиляторы — различаются по скорости
метаболизма ПАВ и продолжительности их эффектов, например, по длительности наркотического обезболивающего эффекта,
времени сна. А лица с дефицитарной или ригидной формой фермента ГГГ характеризуются низкой толерантностью к алкоголю
ибыстропрогредиентным алкоголизмом с тяжелой и многообразной органопатологией, а также — повышенной аллергической
готовностью. Поскольку существенный вклад в избирательную органопатоло-гию при алкоголизме обеспечивается
функциональной мощностью полифункциональной ферментной системы ГГТ, небезынтересен перечень средств
медикаментозной терапии и факторов среды, модулирующих ее активность. В-третьих, известно о биоритмологическом режиме
работы «метаболитных клеточных часов», который в норме поддерживается функцией не одного, а целого содружества
ферментов и, следовательно, нарушается у больных с зависимостями. С этим невозможно не считаться при назначении
энзимо- и метаболитной терапии. В-четвертых, надо принимать во внимание, что избыточные концентрации физиологических
метаболитов (дофамина, гистамина) высокотоксичны. Токсичность показана и для других нейроактивных метаболитов: глутами-
на, глицина. Известна также зависимость нейро- и психоэффективности последнего от состояния гипер- или гипокортизолизма
алкогользависимых пациентов. То есть на фоне гипер- или гипофункционального состояния надпочечников у разных пациентов
одна и та же доза глицина может вызывать в двух крайних случаях прямо противоположный (тормозящий, успокаивающий или
возбуждающий до агрессивности и провоцирующий алкогольную мотивацию) эффект. Следовательно, применяя
модификаторы обмена биогенных аминов, необходимо рассчитывать на сохранные регуляторные механизмы поддержания
гомеостаза и эндоэкологического баланса. В-пятых, следует принимать во внимание компартментализацию аминокислот в зонах
головного мозга, а также специфичность транспортных систем, что определяет, по выражению И. П. Ашмарина с соавт. (2004),
принцип «химических адресатов» в технологиях метаболитной терапии. Понятно, что у больных с алкогольной энцефалопатией
наверняка нарушены процессы компартментализации и сама архитектоника депо и рецепторного аппарата, отчего может
исказиться или вовсе не состояться ожидаемый эффект энзимотерапии.
Таким образом нам представляется, что существование временных и пространственных особенностей передачи сигналов в
нейромедиаторных постсинаптических эффектах и функционировании системы «химических адресов» в организме выдвигает
ряд очень важных требований и ограничений в вопросе использования метаболитных смесей и биологически активных добавок к
пище (БАД). БАД (или композит) не могут утилизироваться организмом со 100-процентной эффективностью, действовать сразу и
непосредственно на органы-мишени, они должны быть «узнаваемы» и пройти иммуноло-
254 Алкоголизм (алкогольная зависимость и алкогольная болезнь)
гическую «таможню». В то же время понятно, что у большинства наркозависимых больных с сопутствующими функциональными
нарушениями печени и почек, других внутренних органов и защитных систем организма «таможенный контроль» снижен или от-
сутствует. Для прогнозирования эффективности лечения необходимо предусматривать целостность регуляции, осуществляемой
гормонами, секретирующихся в кровь, спинномозговую или межклеточную жидкость и циркулируют в них, модулируют состояние
клеток-мишеней, на которые направлена энзимная терапия.
Галоперидол ТАД
Антиконвульсанты Оральные контрацептивы
Нестероидные противовоспалительные средства
Антиритмики, антикоагулянты
Г ГГТ Ноксирон
Дексаметазон
Эстрадиол
Мембранотропные и мембраностабилизирующие средства
Цитостатики: актиномицин D, циклогексимид
Глюкокортикоиды
Инсулин
Г ГГТ Антигипертензивные средства
а-метилдофа Резерпин-азатиоприн
Примечание. ТАД — трициклические антидепрессанты; f 4- —двухфазное действие (сначала
повышает Т. а затем снижает 4 активность ГГТ) оказывает цитостатик и иммуномодулятор
азатиоприн.
Избыточное углеводное питание и жиры снижают, а высокобелковая диета — способствует
повышению акгивности ГГТ.
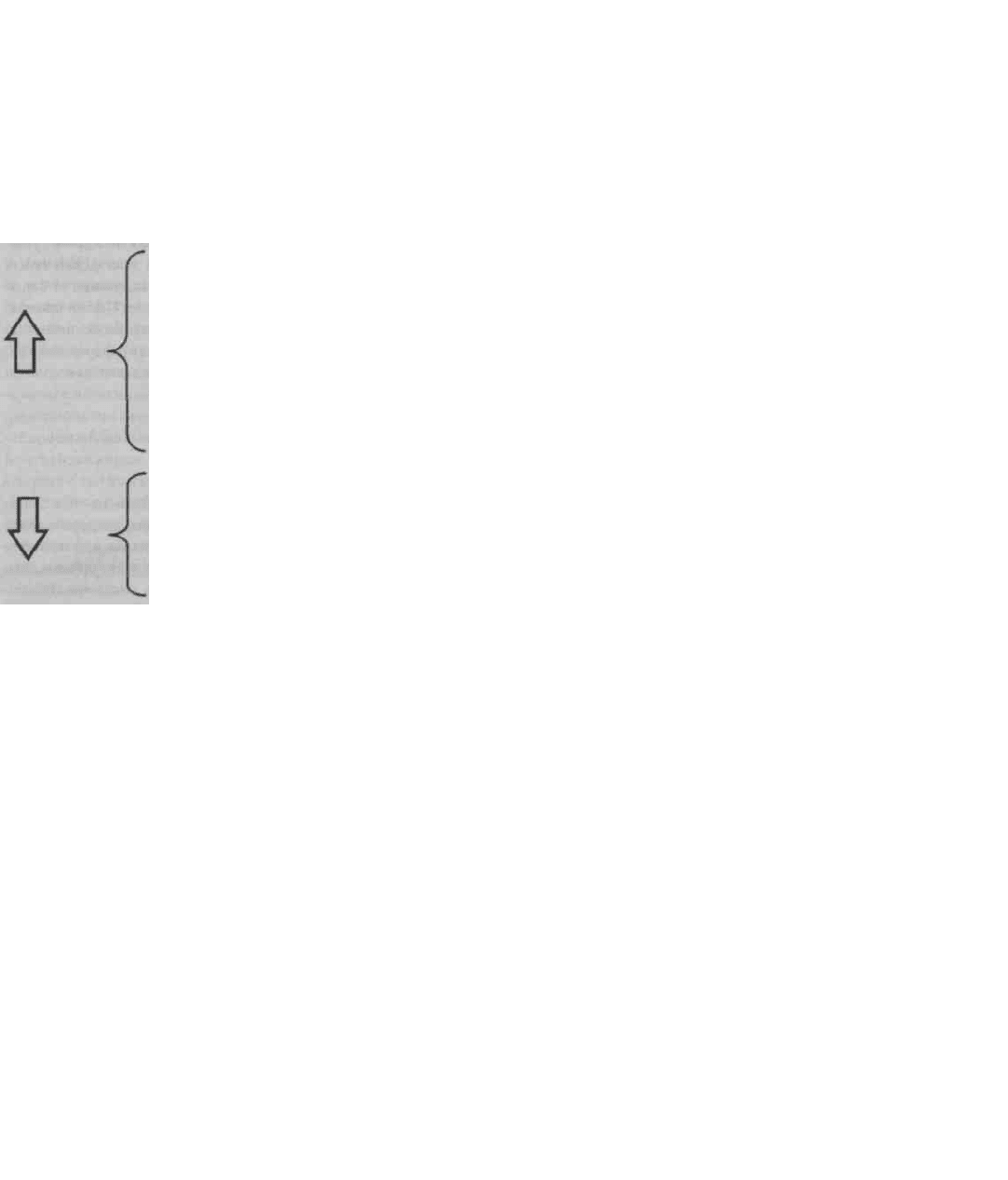
Рис. 8. Влияние некоторых лекарственных препаратов и особенностей питания на активность гамма-глутамилтрансферазы (ГГТ) в
крови
11.15.4. Концепция рационального питания и метаболитная терапия
Биохимики и биофизики подчеркивают, что как сложный метаболизм клетки может быть упрощен и сведен к интегральным
моделям, так и молекулярный патогенез алкоголизма, любой другой патологии, может быть упрощен, сведен к интегральным форму-
лам. Эти формулы возможно составить для самоорганизующейся системы организма человека, т. к. вся его регуляторная
деятельность построена на контроле за движением и распределением интегральных метаболитных потоков.
В науке о питании давно существует идея и разрабатывается концепция рационального питания с учетом феномена
адаптивного роста клеток, тканей и органов. Значительная роль в потребностях организма принадлежит регулирующим системам,
способ-
Подходы к метаболитной и энзимной терапии в наркологии 255
ным получать, накапливать, перерабатывать и направлять информацию для регулирования адаптивного роста. Предполагается
наличие взаимосвязи питания и регулирующих систем, получающих информацию о точках депо и направлениях метаболического
потока, и существование интегративных показателей метаболического статуса организма — т. н. метаболитов с интегрирующей
ролью и класса биомопекуп-переносчжов информации. То есть допускается возможность некоего дискриминантного образа
жизни и питания с доминирующей ролью в алгоритме последнего основных компонентов регуляции гомеостаза, поддержания
метаболического статуса организма и его адаптивности. При этом подчеркивается, что адаптивный рост тканей нуждается в
избирательной информации о метаболитах с интегральной ролью в организме. В этой структурно-функциональной цепи именно
ферментам может принадлежать ведущая роль. Поэтому и сами ферменты, как информаторы, медиаторы и модуляторы
ферментов (витамины и микроэлементы с коферментной ролью) могут быть целенаправленно использованы в лечебно-
реабилитационной наркологической практике.
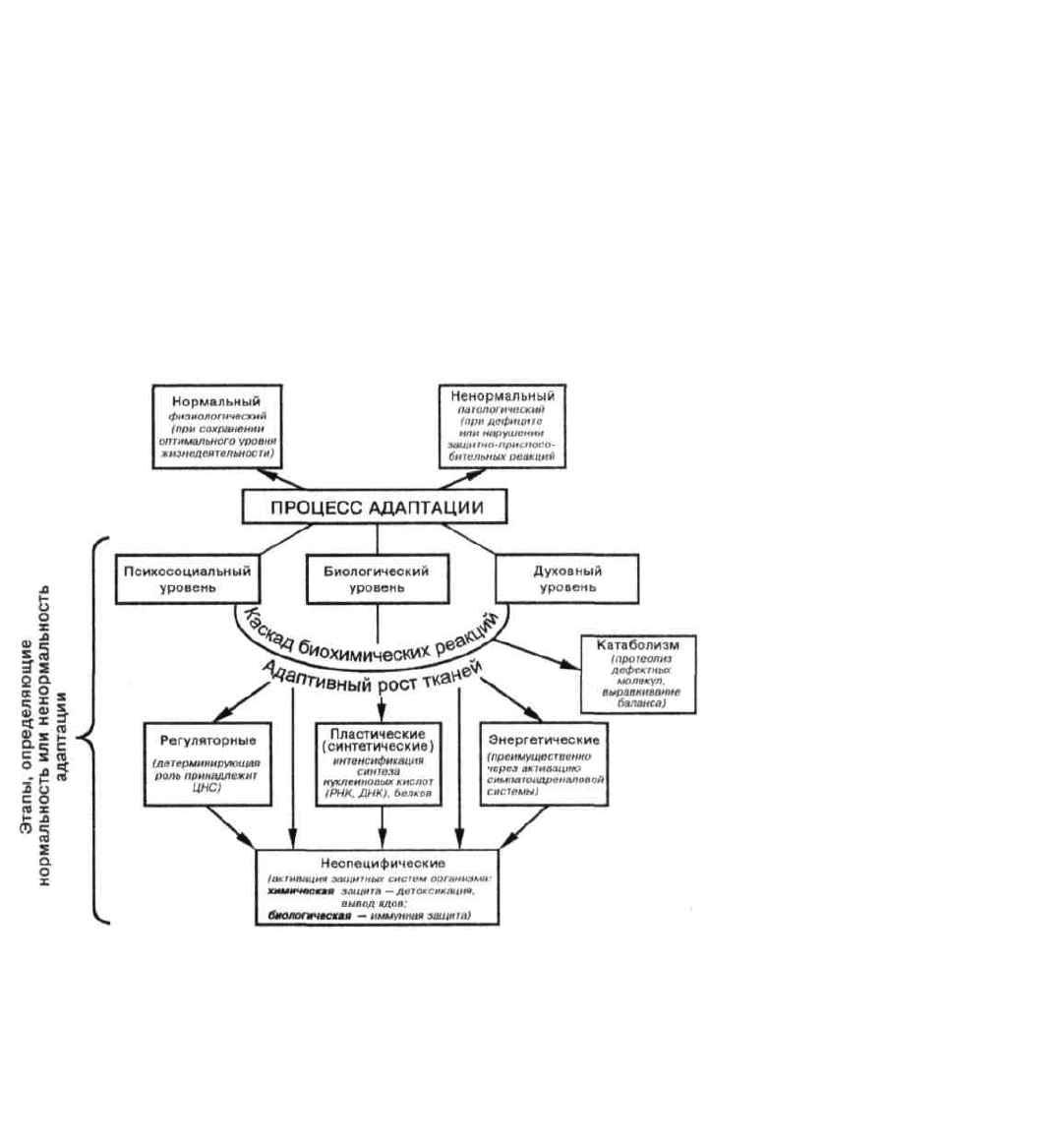
Примечание. Разделение специфического и неспецифического механизмов весьма условно — они почти всегда протекают сочетание
Принципиальная регуляция тех и других одинакова и сводится к оптимальному функционированию с учетом потока информации от факторов
воздействия.
Рис. 9. Общие пути и механизмы адаптации
256
Алкоголизм (алкогольная зависимость и алкогольная болезнь)
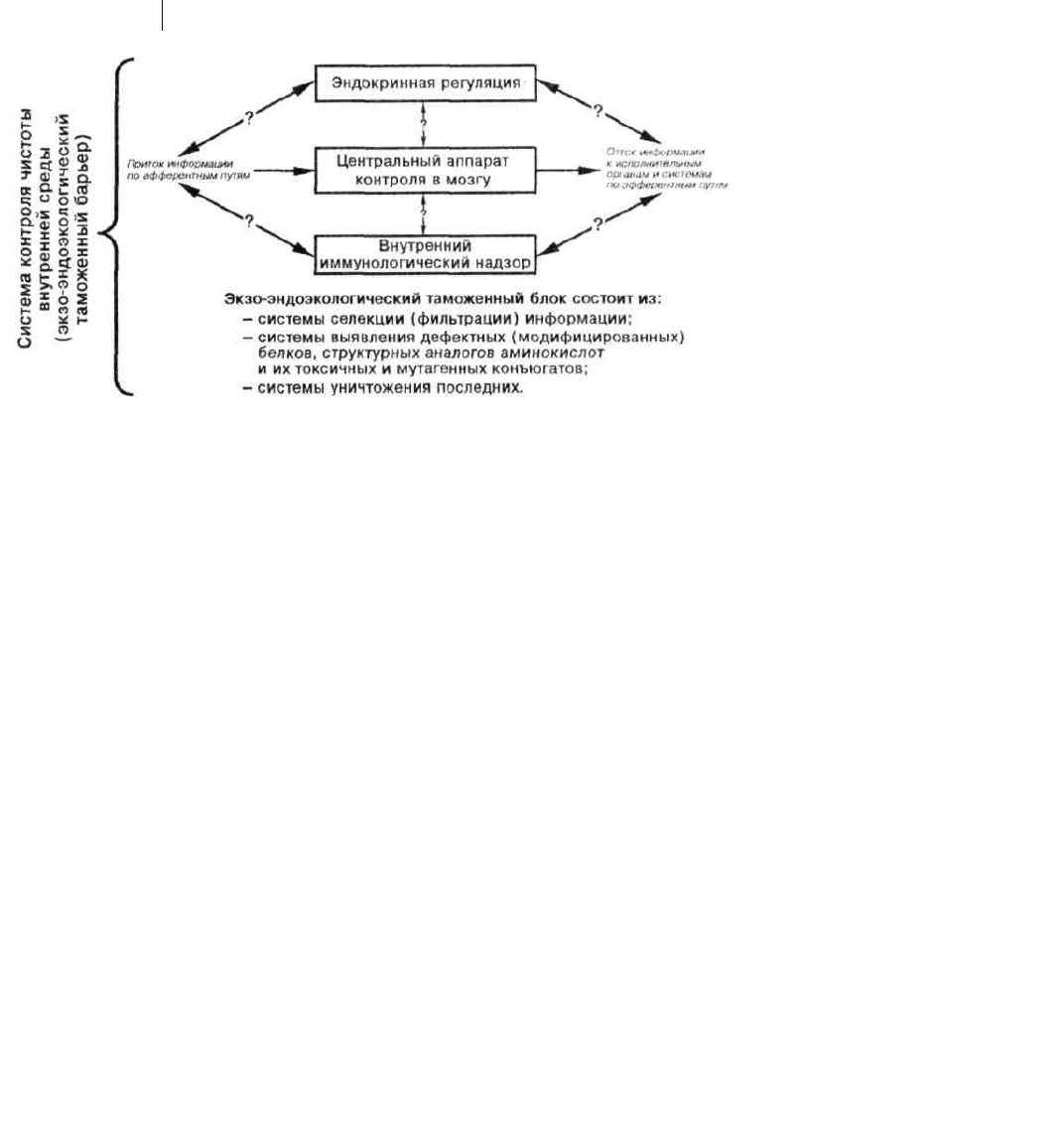
Примечание. Практически все методы рефлексотерапии, а также метаболитная, энзимотерапия и даже психотерапия действуют на
перечисленные выше биохимические и биофизические пути и механизмы адаптации.
Рис. 10. Система контроля чистоты внутренней среды
Интегративность, интегративная роль метаболитов, интегральная информация. В настоящее время требуется
содержательная расшифровка этих понятий в прикладном (лечебно-диагностическом) аспекте. Откуда и какую информацию
получают регулирующие питание системы организма? Только ли от продуктов питания, плодов и растений? Или и от других
источников информационно-волновой природы, способных влиять на системы регуляции гомеостаза изнутри и извне? Что
заключают в себе понятия «метабо-литный голод», «метаболические болезни», «метаболитная терапия»? Концепции «мо-
лекулярных болезней», «энергетических болезней» существовали уже в 1960-е гг. Известно даже понятие «уход за
метаболизмом». «Расшифровка» смысла этих терминов и механизмов позволила бы разработать, с одной стороны,
математическую модель питания как потребностного поведения организма и с другой — алгоритм коррекции нарушенного
питания и управления им, в том числе выправления алкогольного наркомани-ческого гомеостаза и снятия (или погашения)
потребностной доминанты — влечения к алкоголю. Вероятно, ошибочная диета может сделать человека алкоголиком: это экспе-
риментально доказано на крысах. Например, известно, что высокий уровень рафинированных углеводов на фоне дефицита
витаминов, минеральных солей и белков могут индуцировать тягу к спиртному.
В работах А. А. Артемчука показано, что дисбаланс минеральных компонентов сопровождает алкогольную болезнь и
особенно обостряется в периоды предрецидивов и после запоев. Американские диетологи даже рекомендуют
противоалкогольную диету, что не лишено оснований, учитывая накопленный экспериментальный и практический опыт в
области изучения обменных нарушений при хронической алкогольной интоксикации, в медицинской генетике и медицинской
энзимологии. Особенности питания, обеспечивающие индукцию метаболитной тяги к спиртному и усугубляющие эффекты
алкогольной интоксикации, таковы: богатая рафинированными углеводами диета на фоне дефицита белков и минеральных
солей (один из возможных механизмов — снижение уровня тиамина и активности транскетолазы, вызываемые глюкозой);

Подходы к метаболитной и энзимной терапии в наркологии
257
дефицит селена повышает нейротоксические эффекты алкоголя и других психоактивных веществ; ацетачьдегид, ацетат
ингибируют транспорт тиамина с участием Na,K-АТФазы и синтез пиридоксаль 5-фосфата; гамма-оксибутират как
нейроактивный субстрат и метаболит очень опасен, т. к. может вызывать кому с остановкой дыхания и летальным исходом,
гипотермию; /3-аланин.
Необходимо подчеркнуть, что энзимотерапия и метаболитная терапия входят в т. н. базисную терапию наркологических
заболеваний. Базисная терапия в основном пред-стаагсена методами и средствами, направленными на повышение качества
жизни и оптимизацию (восстановление) саногенетических механизмов и естественных процессов саморегуляции организма
больного, поэтому имеет решающее влияние на этапах ремиссии и реабилитации. Особенное значение метаболитная и энзимная
терапия приобретают в случаях коморбидно отягощенной алкогольной или наркотической зависимости соматическими и
неврологическими заболеваниями и осложнениями. Показано, что своевременное назначение необходимых (что выявляется
путем клинико-лабораторного исследования по паттернам диагностических и прогностических показателей) метаболитов в виде
композитных смесей в составе комплексного лечения больных алкоголизмом ускоряет редукцию большинства клинических
симптомов заболевания, повышает адаптационный потенциал и качество ремиссии наркозависимых по сравнению с лечением
только традиционными методами патогенетической терапии (Артемчук, 2002-2005). Особую ценность применение
комплексной метаболитной терапии имеет у больных с тяжелым коморбидным сопровождением и в состояниях декомпенсации,
когда традиционная детоксикационная терапия и медикаментозная интервенция не только малоэффективны, но иногда и
противопоказаны из-за нарушения фармакокинетики, развития феноменов синергизма, летального синтеза и
парадоксальности эффектов.
Исходя из основополагающих принципов неотложной помощи в наркологии ферменты и метаболиты могут применяться с
целью уменьшения вреда. В число приемов такого применения входят: детоксикация путем ферментативного ускорения
выведения ядов и метаболитов; восстановление гомеостаза; лечение (снятия симптомов и синдромов) и предупреждение
осложнений интоксикации ПАВ.
В качестве теоретической основы для прикладной энзимотерапии перспективна разработка следующих направлений:
ферменты и метаболиты в детоксикации при острых и хронических отравлениях ПАВ; ферментная и метаболитная регуляция
толерантности; ферментная и метаболитная регуляция влечения; ферменты и метаболиты в поддерживающей и
противорецидивной терапии наркозависимостей; ферментная и метаболитная терапия и профилактика
соматоневрологических осложнений наркотизации; аминокислоты в качестве метаболитной терапии (купирования) синдромов
влечения и отмены.
11.15.5. Примеры практического применения метаболитной и энзимной терапии в наркологии
В качестве практического примера можно привести ранее описанное нами эффективное использование терапевтических
доз гистамина(1,0 мл 0,1% внутрикожно, ежедневно в течение трех дней) в качестве противорецидивного средства у больных с
алкогольной зависимостью.
Недавно полученные данные (Кржечковская, Желтухина, Небольсин, 2003) об антиаллергических свойствах гамма-
глутамилгистамина в опытах на морских свинках и мышах подтверждают предполагаемое нами ранее участие фермента
гамма-глутамил-
9 Зак. .1806
258
Алкоголизм (алкогольная зависимость и алкогольная болезнь)
трансферазы крови и тканей в гистаминообезвреживающей функции организма и в обеспечении индивидуальной толерантности к
алкоголю путем дезактивации высвобождающегося при алкогольных эксцессах гистамина. Эти работы открывают новые воз-
можности энзимной терапии, во-первых, острых отравлений (алкогольной, гистамино-вой интоксикации) как у зависимых от алкоголя,
так и у не злоупотребляющих алкоголем лиц и, во-вторых, в управлении толерантностью у алкогользависимых больных с целью
провокации у них аверсивных реакций на прием алкоголя и разрушения потребностной алкогольной доминанты.
Существует достаточно много примеров успешного использования природных источников (грибов, морепродуктов,
лекарственных трав и растений) и приготовленных на их основе БАД в условно-рефлекторной аверсионной терапии алкоголизма.
Изучением механизма их антитоксического и противорецидивного эффектов интенсивно занимается лаборатория токсикологии
национального научного центра наркологии и Институт здоровья в Москве (Нужный с соавт., 2002-2004).
Так, одним из путей частичной реализации энзимотерапии алкогольной зависимости можно рассматривать действующее начало
грибов-копринусов — коприн, который гидролизуется в организме с образованием 1-аминоциклопропанола, мощного ингибитора
АльДГ и обусловливает дисульфирам-подобную реакцию на прием этилового алкоголя (Нужный, Ефремов, Рожанец, 2002).
Показана также способность экстракта гребней винограда (препарат Вега-плюс) изменять фармакокинетику и фармакотокси-
кологию алкоголя. Действующее начало экстракта — флавоноиды, обладающие антиок-сидантной активностью. Клинико-
токсикологическая картина эффектов этого препарата проявляется в снижении скорости элиминации алкоголя и усилении его
опьяняющего действия наряду с ослаблением выраженности алкогольных постинтоксикационных расстройств (похмелья) и
алкогольных осложнений со стороны сердечно-сосудистой системы (Нужный, Пометов, Ковалева и др., 2002).
Чрезвычайный интерес с точки зрения возможной модуляции ферментов метаболизма алкоголя в организме человека
представляет изучение механизмов некоторых видов фитотерапии алкоголизма (с помощью приготовленных по народным
рецептам тимьяна, чабреца, копытня, баранца, корня солодки) с эффектом выработки эмоционально-негативной реакции на
алкоголь. БАД отечественного и импортного производства (такие, как Алкогал, Алкостоп, Вега-плюс и другие) представляют собой
наглядный пример сложных метаболитных и лекарственных растительных смесей, обладающих отрезвляющим и
органопротекторными свойствами при алкогольной интоксикации. Эффективный противовирусный иммуномодулятор ЭПСОРИН,
приготовленный из натив-ных источников животного происхождения, заслуживает пристального изучения как вероятный адаптоген-
энзимный и метаболитный регулятор.
Вопросы ограничения применения, специфичности и неспецифичности в энзимотерапии заслуживают дальнейшего изучения на
основе глубокого системного анализа имеющихся практических наработок, теоретических обоснований и экспериментальных
исследований.

ГЛАВА 12
ОПИОИДНАЯ ЗАВИСИМОСТЬ И ПОСЛЕДСТВИЯ ЗЛОУПОТРЕБЛЕНИЯ ОПИОИДАМИ
Опиоидами называется группа психоактивных веществ, родственных специфическим (опиоидным) рецепторам и оказывающих
многообразное влияние на центральную нервную систему (ЦНС) и физиологические функции.
Подобно алкоголю и лекарственным препаратам снотворно-седативного спектра (например, производным бензодиазепина),
опиоиды преимущественно угнетающе действуют на мозговые функции и относятся, таким образом, к категории супрессоров ЦНС.
В разграничении понятий опиаты и опиоиды есть определенные трудности. I (смятие опиатов в узком смысле подразумевает
наркотические вещества, непосредственно полученные из растительного сырья (снотворного мака) и имеющие, таким образом,
полностью природное происхождение. Категория опиатов наряду с отдельными алкалоидами снотворного мака включает первично
обработанные растительные продукты, содержащие смесь алкалоидов (например, ацетилированный опий).
Под опиоидами традиционно понимают вещества сходного с опиатами фармакологического действия, но полученные
искусственным — полусинтетическим или синтетическим — путем. Для отечественной клинической наркологии более привычен
термин «опиаты», в зарубежной (особенно англоязычной) литературе преимущественно используется термин «опиоиды». В
соответствии с современной систематикой ПАВ, все лиганды опиоидных рецепторов, вне зависимости от их происхождения, носят
название апиоидов.
Примечательно, что в начале 1990-х гг. в России больные опийной наркоманией преимущественно употребляли
ацетилированные препараты снотворного мака (опиаты), а в настоящее время основной употребляемый наркотик этого ряда — героин
(полусинтетический опиоид).
Несомненно, при определенных различиях в степени наркогенности, симптоматике интоксикации, динамике фазных состояний,
связанных со злоупотреблением природными, полусинтетическими или синтетическими веществами, в основе зависимости от них
лежат универсальные механизмы. Эти механизмы при систематическом употреблении наркотиков и выявлении признаков зависимости
от них позволяют констатировать наличие единого заболевания — опиоидной зависимости в ее различных клинических вариантах
(героиновая наркомания, злоупотребление трамадолом или кодеином и т. д.). Равноправным (хотя и менее корректным) синонимом
опиоидной зависимости можно считать традиционный для отечественной наркологии термин «опийная наркомания».
Мы считаем более предпочтительным использование понятия «опиоиды» взамен понятия «опиаты» как термина более общего
порядка и обозначающего все вещества, родственные опиоидным рецепторам.
Терминологические трудности усугубляются тем, что к категории опиоидов относятся не только агонисты опиоидных рецепторов
(т. е. вещества, обладающие морфино-

260 Опиоидная зависимость и последствия злоупотребления опиоидами
подобными свойствами), но и препараты смешанного — агонист-антагонистическо-го — действия, а также антагонисты опиоидных
рецепторов, проявляющие противоположные морфину фармакологические эффекты.
Уникальный спектр фармакологического действия опиоидов обусловливает их широкое использование в медицине в качестве
наркотических анальгетиков. Главное предназначение этих препаратов — обезболивание в послеоперационном периоде в хирур-
гической клинике, а также смягчение хронических болей, вызванных злокачественными опухолями.
Опиоиды находят применение в урологии для купирования почечной колики. Они также используются в реанимационной
практике в качестве противошоковых препаратов и средств, купирующих кардиогенный отек легких. Кроме того, препараты этого
класса применяются в качестве противокашлевых средств (кодеин) и средств, подавляющих перистальтику кишечника (лоперамид).
Наконец, во многих странах официальные опиоиды употребляются в заместительной терапии опиоидной зависимости (метадон,
LAAM, бупренорфин).
При интенсивных (и особенно хронических) болях применению опиоидов нет альтернативы. Средства для наркоза могут их
заменить лишь временно и только в ограниченном круге клинических ситуаций, например в ходе хирургической операции. Ненар-
котические анальгетики (нестероидные противовоспалительные средства) не обладают сравнимой с опиоидами способностью
устранять очень сильные боли.
Постоянный поиск возможности синтеза принципиально новых веществ, альтернативных опиоидам по силе обезболивающего
действия, но не обладающих нарко генным и свойствами, ведущийся в течение многих десятилетий, к сожалению, пока не увенчался
успехом. Более того, с точки зрения современных представлений о механизмах регуляции боли правомерность постановки вопроса о
принципиальной возможности существования лекарственных средств, способных оказывать сопоставимое с опиоидами бо-
леутоляющее действие, но не участвующих в опиоидергических нейрофизиологических процессах, представляется сомнительной.
Следует упомянуть, что в процессе поиска мощных анальгетиков, не обладающих наркогенными свойствами, были в разное
время синтезированы героин, метадон и некоторые другие опиоиды с выраженной способностью вызывать зависимость. Примеча-
тельно, что героин, синтезированный из морфина в расчете на возможность его применения в лечении морфинизма, по
наркогенному потенциалу значительно превзошел исходное вещество.
Наркогенные свойства — облигатная характеристика ПАВ опиоидного ряда. Мощное болеутоляющее действие опиоидов, их
способность устранять любой психофизический дискомфорт в сочетании со специфическим и крайне притягательным для пред-
расположенных лиц психотропным действием, а также быстро развивающийся синдром отмены при повторном употреблении создают
почву для формирования тяжелых форм наркотической зависимости от этих веществ.
Героиновая наркомания и другие формы опиоидной зависимости представляют наряду с алкоголизмом одну из наиболее
распространенных и социально значимых болезней аддиктивного круга. В России и сопредельных государствах, а также во многих
других странах Европы и Азии героиновая (опийная) наркомания преобладает в структуре наркоманий. Сходная ситуация до 1980-х гг.
наблюдалась в США. Но в настоящее время преобладающим запрещенным наркотиком в странах американского континента стал
кокаин (Менделевич, 2005; O'Brien etal., 1999; Brust, 2004).
