Луцкий Д.Л., Николаев А.А. Координационные соединения
Подождите немного. Документ загружается.


11
Хелат, приведенный ниже, содержит два бидентатных хела-
тобразующих лиганда.
Не все хелатные комплексы обладают одинаковой устойчиво-
стью. Согласно правилу циклов Чугаева, максимальной устойчиво-
стью обладают только те комплексные соединения, хелатобра-
зующие лиганды которых образуют совместно с комплексообра-
зователем пяти или шестичленные циклы. Все приведенные выше
хелатные комплексы подтверждают правило циклов Чугаева. Приве-
дем ещё один пример, подтверждающий это правило.
Ni
O
N
N
O
C
N
C
CH
3
HO
CH
3
C
OH
N
C
H
3
C
H
3
C
Na
O O
OO
H
3
C
CH
3
CH
3
O
CH
3
O
HOOC
CH
3
O O
CH
2
CH
2
H
3
C
H
3
C
CH
3
CH
3
H
3
C
OH
N
N
N
N
N
N
Fe
2+
12
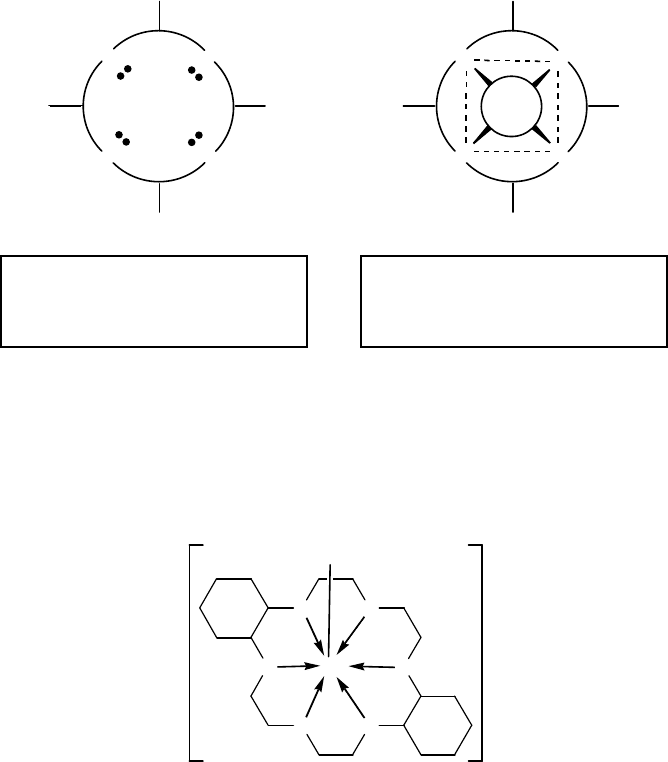
Полидентатные хелатобразующие лиганды, донорные атомы
которых связаны в цикл и жестко скоординированы в пространстве,
называются макроциклическими. Схематичное изображение подоб-
ных лигандов приводится на рисунках 3 и 4.
Примеры:
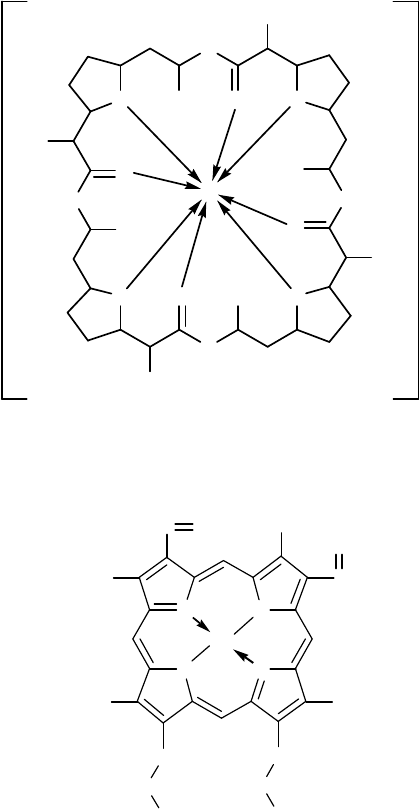
Типичным представителем макроциклов являются полиэфиры
(«краун»-эфиры). Ниже представлено комплексное соединение, со-
держащее один гексадентатный макроциклический лиганд (образо-
ванный «краун»-эфиром) и один монодентатный лиганд SCN
.
O O
O
O
O
O
Rb
SCN
N
N
N
N
R
4
R
3
R
2
R
1
N
N
N
N
R
4
R
3
R
2
R
1
Fe
2+
Рис. 3. Схема строения
макроцикла порфирина.
Рис. 4. Схема строения
макроцикла порфирина в ком-
плексе с ионом железа.
13
В следующем примере роль октадентатного лиганда играет
макролид нонактин, являющийся типичным ионофором, то есть хи-
мическим соединением, которое обладает способностью переносить
ионы через биологические мембраны.
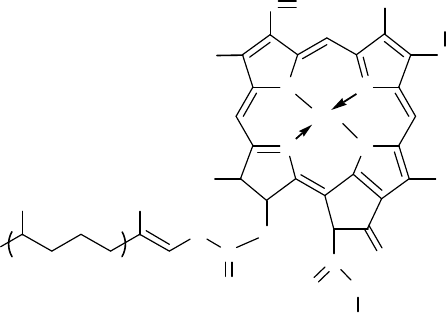
Гем гемоглобина, приведенный ниже, является примером тет-
радентатного макроциклического лиганда, в основе которого лежит
порфирин.
+
O
O O
O
O
O
O
O
O
CH
3
CH
3
H
3
C
O
CH
3
CH
3
O CH
3
CH
3
O
H
3
C
K
N N
NN
HC
CH
3
CH
2
CH
CH
3
H
3
C
H
3
C
CH
2
CH
2
H
2
C
COOH
H
2
C
COOH
CH
2
Fe
2+
14
Порфирин лежит в основе многих биологически важных мак-
роциклов, например, в основе тетрадентатного макроциклического
лиганда хлорофилла а и b, формулы которых приведены ниже.
Существует еще один тип лигандов, получивший название ам-
бидентатных. Амбидентатными лигандами называют многоэлемент-
ные лиганды, способные координироваться различными своими ато-
мами. То есть, в разных комплексах такие лиганды могут образовы-
вать связь с комплексообразователем через разные атомы, входящие в
состав лиганда.
К амбидентатным относятся такие лиганды, как SO
3
2
, NO
2
,
NCS
, CN
и другие. Сравните в приведенных ниже примерах ком-
плексных соединений строение лигандов. Атом, через который осу-
ществляется связь амбидентатного лиганда с комплексообразовате-
лем, в формуле отмечается с помощью валентного штриха.
Примеры: [V(-NCS)
6
]
3
[Hg(-SCN)
4
]
2
,
K
3
[Co(-ONO)
6
] Na
3
[Co(-NO
2
)
6
],
K
3
[Fe(-NCS)
6
] [Cr
2
(NH
3
)
3
(-SCN)
3
],
[Fe(-CN)
6
]
4
[Fe(-NC)
6
]
3
.
В многоядерных комплексах могут встречаться лиганды, кото-
рые координированы двумя или более комплексообразователями, по-
N N
NN
HC
R
CH
2
CH
2
CH
3
H
3
C
H
3
C
CH
3
Mg
2+
O
C
O O
CH
3
CH
2
O
H
3
C
3
CH
3
CH
3
Хлорофилл
a R =
CH
3
Хлорофилл
b R
= CHO
C
O
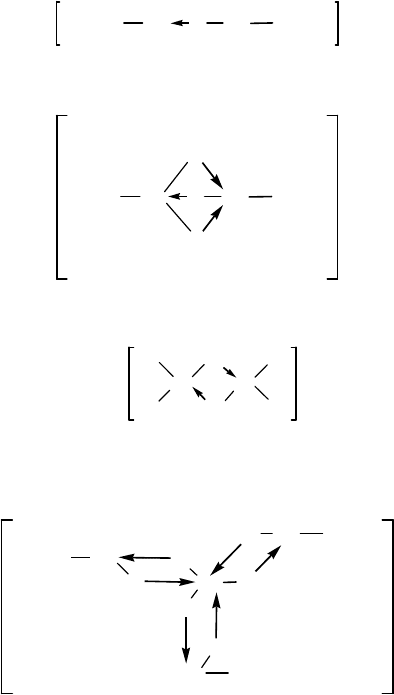
15
добные лиганды называют мостиковыми лигандами (
-лигандами),
поскольку они как настоящие мосты соединяют комплексообразова-
тели между собой.
Примеры:
Лиганд OH
в приведенном ниже двухядерном комплексном
соединении является -лигандом.
В кординационном соединении может быть два и более мости-
ковых лигандов, что показано на приведенном ниже примере.
В ниже приведенном двухядерном комплексе содержатся че-
тыре монодентатных лиганда Cl
и два бидентатных -лиганда Cl
.
В качестве ещё одного примера приведём четырехядерный
комплекс, содержащий шесть бидентатных -лигандов OH
.
Многоядерные комплексы, в которых комплексообразователи
связаны непосредственно друг с другом, называются кластеры.
Co(H
3
N)
5
H
O
Co (NH
3
)
5
Cl
5
Al
Cl
Cl
Al
Cl
Cl
Cl
Cl
Co(H
3
N)
3
H
O
Co (NH
3
)
3
Cl
3
O
H
H
2
N
Co
Co
Co
Co
(H
3
N)
4
O
H
HO
OH
HO
OH
(NH
3
)
4
(NH
3
)
4
OH
Cl
6

16
Примеры:
Важной характеристикой комплексообразователя в комплекс-
ных соединениях является координационное число. Различают ха-
рактеристическое и максимальное координационные числа ком-
плексообразователя. Характеристическим координационным числом
комплексообразователя называют общее число
-связей, образую-
щихся между комплексообразователем и лигандами в конкретном
комплексном соединении. Характеристическое координационное
число (КЧ) зависит от природы лигандов. Максимальное координаци-
онное число (МКЧ) определяет максимально возможное число свя-
зей, которое может предоставить комплексообразователь. Мак-
симальное координационное число не зависит от природы лигандов,
оно полностью определяется электронным строением самого ком-
плексообразователя.
В комплексных соединениях, содержащих только монодентат-
ные лиганды, характеристическое координационное число совпадает с
количеством лигандов.
Примеры: [Co(H
2
O)(NH
3
)
4
Cl]Cl
2
, КЧ=6;
[Pt(NH
3
)
5
(OH)]Br
3
, КЧ=6;
K[Ag(CN)
2
], КЧ=2;
K
2
[TaF
7
], КЧ=7.
В комплексных соединениях, которые содержат полидентат-
ные лиганды, характеристическое координационное число с количест-
вом лигандов не совпадает.
Примеры: [Co(NH
3
)
2
(NH
2
CH
2
CH
2
NH
2
)Cl
2
]Cl, КЧ=6;
[Cu(NH
2
CH
2
COO)
2
], КЧ=4;
Na
2
[Cu(C
2
O
4
)
2
], КЧ=4;
[Cu(NH
2
CH
2
CH
2
NHCH
2
CH
2
NH
2
)(H
2
O)]
2+
, КЧ=4.
Mn Mn (CO)
5
(OC)
5
Re
Re
ReCl
Cl
Cl
(Cl)
3
Cs
3
(Cl)
3
(Cl)
3
MoMo (Cl)
4
(Cl)
4
4
-
W W
Cl
Cl
Cl
Cl
Cl
Cl
Cl
Cl
Cl
3
-
17
НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
Правила, по которым составляются названия комплексных со-
единений, являются систематическими, то есть однозначными. Кроме
того, эти правила являются универсальными.
В формулах комплексных соединений в квадратных скобках
на первом месте ставят комплексообразователь, затем по порядку рас-
полагают лиганды, сначала катионные, после них нейтральные, а в
конце анионные: [М(L
+
)(L
0
)(L
)]. Частицы внешней сферы располага-
ют за пределами квадратных скобок. Если частица внешней сферы
является катионом, её записывают перед квадратными скобками:
X
+
[МL
n
]
. Если частица внешней сферы является анионом, её записы-
вают после квадратных скобок: [МL
n
]
+
X
.
Формулы многих органических лигандов, при записи коорди-
национного соединения, заменяют для краткости общепринятыми бу-
квенными обозначениями (см. табл. 1).
Название комплексного соединения строится из названия ли-
ганда с числовой приставкой n равной количеству лигандных групп и
названия комплексообразователя. Используют следующие числовые
приставки:
1 – моно 4 – тетра 7 – гепта 10 – дека
2 – ди 5 – пента 8 – окта 11 – ундека
3 – три 6 – гекса 9 – нона 12 – додека
Если в названии самого лиганда уже используется числовая
приставка или если при использовании числовой приставки возможно
разночтение, то применяют умножающие приставки:
2 – бис 4 – тетракис
3 – трис 5 – пентакис
Названия катионных лигандов (L
+
) оканчиваются на -ий (ис-
ключение: Н
+
– гидро).
Примеры: N
2
H
5
+
– гидразиний, NO
+
– нитрозилий.
Названия нейтральных лигандов (L
0
) соответствуют названиям
веществ.
Примеры: N
2
– диазот, N
2
H
4
– гидразин,
С
2
H
4
– этилен, (NH
2
)
2
CO – карбамид.
18
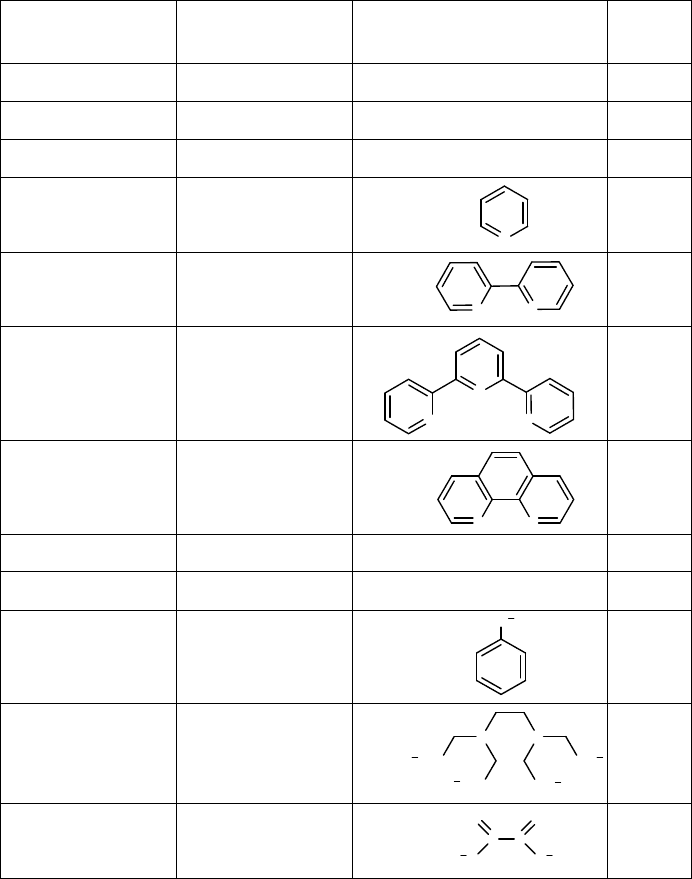
Таблица 1.
ОБЩЕПРИНЯТЫЕ СОКРАЩЕНИЯ НЕКОТОРЫХ СЛОЖНЫХ ЛИГАНДОВ
Название
свободного
лиганда
Название
координированного
лиганда
Формула лиганда
Сокра-
щение
1,2-диаминоэтан
(этилендиамин)
1,2-диаминоэтан
(этилендиамин)
NH
2
CH
2
CH
2
NH
2
en
1,4,7-триазагептан
(диэтилентриамин)
1,4,7-триазагептан
(диэтилентриамин)
NH
2
CH
2
CH
2
NHCH
2
CH
2
NH
2
dien
глицинат-ион глицинато-
NH
2
CH
2
COO
(gly)
пиридин пиридил
py
2,2-дипиридин 2,2-дипиридил
bpy
2,26,2-терпиридин 2,26,2-терпиридил
tpy
1,10-фенантролин 1,10-фенантролин
phen
карбамид
(мочевина)
карбамид
(NH
2
)
2
CO ur
триэтилфосфин триэтилфосфин
P(C
2
H
5
)
3
PEt
3
фенил фенил
(Ph)
N,N,N,N-
этилендиаминтетра-
ацетат-ион
N,N,N,N-
этилендиаминтетра-
ацетато-
(edta)
4
оксалат-ион оксалато-
(ox)
2
N
N
N
N
N
N
N
N
O
O
2
C
O
2
C
N N
CO
2
CO
2
C C
O
O
O
O
19
Исключение составляют следующие нейтральные лиганды:
Н
2
О – аква NH
3
– аммин
CO – карбонил NO – нитрозил
Названия анионных лигандов (L
) оканчиваются на соедини-
тельную гласную -о (за исключением углеводородных радикалов).
Некоторые анионные лиганды имеют специальные названия.
Примеры:
F
– фторо, СN
– циано,
Сl
– хлоро, NCS
– тиоцианато,
O
2
– оксо, CO
3
2
– карбонато,
S
2
– тио, C
2
O
4
2
– оксалато,
N
3
– азидо, SO
3
2
– сульфито,
NO
2
– нитро, SO
3
S
2
– тиосульфато,
OH
– гидроксо, C
5
H
5
– циклопентадиенил.
В названиях катионных ([МL
n
]
+
) и нейтральных ([МL
n
]
0
) ком-
плексов комплексообразователи имеют русские названия соответст-
вующих химических элементов. Русские названия используются и для
большинства комплексообразователей, входящих в состав анионных
комплексов ([МL
n
]
), но, следует отметить, что традиционно, для не-
которых элементов, используют корни их латинских названий:
Ag – аргенат Fe – ферр Pb – плюмб
As – арс, арсен Hg – меркур S – сульф
Au – аур Mn – манган Sb – стиб
С – карб, карбон N – нитр Si – сил, силик
Cu – купр Ni – никкол Sn – станн
Названия нейтральных комплексов ([МL
n
]
0
) состоят из одного
слова, лиганды перечисляются в следующем порядке: сначала ани-
онные, затем нейтральные и после них катионные.
Примеры:
[Cr(H
2
O)
4
(OH)
2
] – дигидроксотетрааквахром
[Fe
2
(C
5
H
5
)
2
] – бис(циклопентадиенил)дижелезо
[Os
3
(CO)
12
] – додекакарбонилтриосмий
[Zn(py)
2
Cl
2
] – дихлоробис(пиридин)цинк
20
[Fe
2
(CO)
9
] – нонакарбонилдижелезо
[Rh(PEt
3
)
3
Cl] – хлоротрис(триэтилфосфин)родий
Названия комплексных соединений имеющих внешнюю сферу
([МL
n
]
+
X
, X
+
[МL
n
]
, [МL
n
]
+
[МL
n
]
-
) состоят из двух слов, с обяза-
тельным указанием степени окисления комплексообразователя.
Если представить в общем виде, то получится «анион катиона».
Примеры:
[Co(NH
3
)
4
(NO
2
)
2
]NO
3
– нитрат динитротетраамминкобальта(III)
[Al(H
2
O)
6
]Cl
3
– хлорид гексаакваалюминия(III)
[Fe(H
2
O)
5
(NO)]SO
4
– сульфат нитрозилпентаакважелеза(II)
[Pt(en)
2
](OH)
2
– гидроксид бис(этилендиамин)платины(II)
[Ru(N
2
)(NH
3
)
5
]Cl
2
– хлорид пентааммин(диазот)рутения(II)
Na
3
[Ag(SO
3
S)
2
] – бис(тиосульфато)аргенат(I) натрия
Н
3
O[AuCl
4
] – тетрахлороаурат(III) оксония
K
3
[Fe(ox)
3
] – триоксалатоферрат(III) калия
Cs[I(I)
2
] – дийодйодат(I) цезия
Na
3
[SbS
3
] – тритиостибат(III) натрия
Na
2
[Sn(OH)
6
] – гексагидроксостанат(IV) натрия
K
2
[Re
2
Cl
8
] – октахлородиренат(III) калия
K
3
[Fe(NCS)
6
] – гексакис(тиоцианато)феррат(III) калия
[XeF
5
][As
V
F
6
] – гексафтороарсенат(V) пентафтороксенона(IV)
Если многоядерные комплексные соединения даны в виде раз-
вернутой формулы, то их названия записывают с учетом мостиковых
лигандов и образующихся кластеров.
Примеры:
[Br
2
AlBr
2
AlBr
2
] – ди(-бромо)бис(дибромоалюминий)
[Cl
2
Pt(N
2
H
2
)
2
PtCl
2
] – ди(-гидразин)бис(дихлорплатина)
[(CO)
5
Mn-Mn(CO)
5
] – бис(пентакарбонилмарганец)
K
2
[Cl
4
Re-ReCl
4
] – бис(тетрахлороренат(III)) калия
Если в комплексном соединении содержатся амбидентатные
лиганды с указанием атома, через который лиганд координирован
комплексообразователем, то это отражается в названии лиганда через
указание символа этого атома.
