Карюхина Т.А., Чурбанова И.Н. Химия воды и микробиология
Подождите немного. Документ загружается.


но
дестабилизировать,
понизить
ее
агрегативную
ус
тойчивость.
Воздействие
на
систему
в
нужном
направ
лении
-
снижение
.~
-потенциала,
ассоцизЦW[
частиц
и
их
седиментация
-
достигается
применением
коагулянтов
и
ФЛОКУЛSlНТОВ.
В
качестве
коагулsmтов
чаще
всего
используют
соли
алюминия
и
железа:
сульфат
алюминия
А12(SО4)э·18Н20,
алюминат
натрия
NaAl02,
сульфат железа
(11)
FeS04"7H20
(железный
купорос),
хлорид
железа
(111)
FеСlз·6Н20.-
В
воде
эти
оали
подверга~я
ступенчатому
гидролизу
по
схеме:
Ме3+
+
Н20
~
Ме(он)2+
Ме<он)2+
+
Н20
~
Ме<ОН)2
+
.н+
Me(OH)~
+
Н20
~
Ме(ОН)э
+
н+
+
Ме(ОН)з
+
ЗН
.
(31)
Полнота
процесса
гидролиза
коагулянта
достигается
только
при
условии
связывания
образующихся
ионов
во
дорода.
В
при
родных
водах
ионы
НСОЭ
в
совокупности
с
растворенной
угольной
кислотой
образуют
буферную
систе-
u u
му,
емкость котороя
определяеТС51
концентрациеи
ИОНОВ
НСОЗ.
Участвуя
в
реакции
·н+
+
НСОз
~
Н2СОз,
ионы
НСОз
обеспечивают
полный
гидролиз
коагулянта.
Однако
в
ряде
случаев
прироДна~
буФерность
воды
оказывается
недостаточной
для
нейтрализации
всех
ионов
и
приходится
прибегать
к
предварительному
подщелачиванию
воды
изве
стью
или
кальцинированной
содой.
Степень
гидролиза
повышается
при
разбавлении
раст-
воров
и
повышении
температуры.
.
Гидролиз
хлорного
железа
по
схеме
(31)
приводит
к
образованию
Fе(ОН)з.
выдлениеe
твердого
гид
роке
ида
же
леза
-
первая
стадия
образования
коллоидной
частицы
(СМ.
16).
Хлопья
Fе(ОН)з
интенсивно
образуются
при
зна
чении
рН
=
5-7
с
оптимумом
в
диапазоне
рН
==
6,1-6,5.
Минимальная
растворимость
гидроксида
железа
(111)
на
блюдается
в
изоэлектрической
точке,
соответствующей
зна
чению
рН
==
6,5.
Гидролиз
солей
алюминия
по
схеме
(31)
приводит
к
образованию
Al(ОН)з
-
типичного
ам<Ix>терноro
со-
160

единения,
способного
раl.'7ВОРЯТЬСЯ
как
в
кислои,
так
и
в
щелочной
среде:
Аl(ОН)з
+
зн+
_.:~
AI
3
+ +
ЗН20;
AIOi +
2Н20.
Аl(ОН)з
+
он-
._--
.,.-
..
Минимальную
растворимость
гидроксид
алюминия
име-
ет
при
рН
-
6,5-7,5.
Мицелла
золя
Al<ОН)з
имеет
сле
дующее
строение:
КОЛЛОИДНАЯ
ЧА~
ТИЦА
/ ,
{
m[AZ
(ОН),]
А
Z
Jr
3
(n
-х)
с
г-}
+ . .J
х
С
z-
, J
Т
ЯДРО
~
_____________________________________
~)
т
У~ЦЕ.ЛnА
Гидрозоли
алюминия
и
железа
образуют
пространст
венные
структуры,
напоминающие
сетку,
в
ячейках
кото
рой
находится
вода.
Формирующиеся
структуры
имеют
очень
развитую
высокопористую
поверхность,
поэтому
обладают
большой
адсорбционной
способностью.
Коллоидные
примеси
воды,
-
оБУСЛОВ-!lивающие
ее
цвет
ность,
адсорбируются
на
хлопьях
гидроксидов,
и
вслеДствие
разноименности
зарядов
гидроксидов
и
частиц
примесей
последние
прочно
фиксируются
на
поверхности
адсорбента.
Собственно
коагуляции
подвергаются
гидрозоли
алюминия
и
железа.
Коагуляция
их
происходит
ПОД
действием
электролитов,
присутствующих
в
воде.
Посколь
ку
коллоидные
частицы
гидроксидов
алюминия
и
железа
заряжены
положительно,
коагулирующими
ионами
для
них
являются
анионы
(s02-, Cl-,
нсоз).
Агломерация
коллоидных
частиц,
обусловливающих
мутность
воды,
происходит
в
результате
сжатия
однова
лентных
катионов
диффузного
слоя
на
более
активные
трехвалентные
катионы
алюминия
или
железа,
всегда
присутствующие
в
растворе
при
введении
коагулянта.
Это
приводит
к
снижению
!
-потенциала
частиц
прим:есей
и
их
коагуляции
~см.рис.
4).
Осветление
воды
происходит
также
в
результате
прилипания
частиц
взвеси
к
хлопьям
гидроксида.
Большое
значение
имеет
ортокинетическая
ко
агуляция
вследствие
захватывания
частиц
сеткой
оседа
ющих
хлопьев
гидроксидов
алюминия
или
железа.
161

Процесс
коагуляции
з~канчиваеТС$I
выведением
из
очищенной
воды
отработанного
сорбента.
Для
определения
оптимальной
дозы
коагулянта
прово
дят
пробное
коагулирование~
по
результатам
которого
строят
коагуляционную
кривую
-
зависимость
остаточной
мутности
или
цветности
от
дозы
коагулянта.
Доза,
соот
ветствующая
минимальной
концентрации
остаточных
за
грязнений~
считается
оптимальной.
для
ускорения
осаждения
хлопьев
необходимо
:их
укруп
нение,
что
достиrnегся/
использованием
Флокулянтов.
Из
не
органических
флокулянтов
чаще
Bcero
применяют
активированный
кремнезем
(Н:zSiОз)4.
Растворы
кремниевой
кислоты
нестабильны,
и
поэтому
'их
готовят
непосредственно
перед
использованием.
Из
органических
флокулянтов
наиболь
шее
распространение
в
нашей
стране
получили
полиакриламид
(ПАА)
~
ПOJIифункционалъные
полимеры
амфотерноro
типа
К-4
и
K-6~
катионный ФЛокулянт
ВА-2.
/./0
Полиакриламид
-
сополимер
акриламида
CHi=:CH-С
'tJH.
u
u:l
И
аммониевых,
натриевых
или
кальциевых
солеи
акриловои
кислоты
СН?=СН-СООН.
Карбоксильные
ГРУППЫ
придают
мо
лекуле
ПАА
свойства
анионноro
полиэлектрОлита,
диссоциирующеro
в
воде
с
ооразованием
полимерного
аниона
и
ПJX>CТЫХ
катионов.
Молекулы
ПАА
образуют
ассоциаты
в
виде
длинных
цепочек.
Вследствие
адсорбционноro
взаимо
действия
молекулы
ПАА
одновременно
с
несколькими
частицами
mдроксида
алюминия
и
железа
ot5разуются
тяже
лые,
крупные
и
прочныe
агрегаты,
легко
оседающие.
Флокулянты
типа
К
получают
ОМhIЛением
полиакрилнитрила
[-CH2-CH-CN
]n,
в
результате
чего
в
составе
полимера
оказываются
карбоксильные,
аминные
и
другие
группы,
обусловливающие
амфотерный
характер
полиэлектролита.
Катионные
флокулянты
представляют
собой
чет
вертичные
аммониевые
соли
на
основе
полистирола
и
поливинилтолуола.
К
их
числу
относится
Флокулянт
ВА-2,
макроионы
которого
имеют
положительный
заряд.
Адсорбируясь
на
отрицательно
заряженных
коллоидных
примесях
воды,
он
образует
крупные
агрегаты.
В
опреде
ленных
условиях
ВА-2
может
быть
использован
без
мине
ральных
коагулянтов.
Дозы
Флокулянтов~
требуемые
для
удовлетворительного
осаждения, очень
малы
-
обычно
менее
1
мг/
л;
если
же
162

реагент
используется
в
роли
не
только.
флокулянта,
но
и
собственно
коагулянта,
то
ДОЗЫ
повышаются.
Въщеление
взвешенных
веществ
из
сточных
вод
обычно
осуществляется
безреагентным
путем,
по
крайней
мере,
на
первых
стадиях
их
обработки.
Однако
в
последние,
годы
была
разработана
схема
физика-химической
очистки
го
родских
сточных
ВОД,
когда
уже
на
первой
стадии
обработки
к
воде
добавляют
peaгeHTы
-
сульфат
алЮl.IИНИЯ
или
хлор
ное
.железо
и
известь,
после
чеro
смесь
направляют
в
первичныe
отстойники
ДЛЯ
отделения
взвешенных
частиц
от
воды.
В
этом
случае
происходит
несколько
процессов
-
коагуляция,
Флокуляция,
соосаждение,
сорбция
примесеЙ.
Дозы
реагентов
в
несколько
раз
выше,
чем
требуемые
ДЛЯ
обработки
природных
вод.
При
очистке
производственныx
сточных
вод
большой
Иdтерес
представляет
применение
в
качестве
коагулянтов
отходов
производства
-
шламов
и
отработанных
растворов.
Так,
при
производстве
этилбензола
в
качестве
отхода
полу
чается
хлорид
алюминия,
при
травлении
металлов
-
суль
фат
двухвалентноro
железа
и
т
.д.
40.
ОТСТАИВАНИЕ
в
технологии
проце~сов
очистки
природных
и
сточных
вод
рассматривается
осаждение
частиц
двух
типов
--
гра
нулированных
и
флокулированных.
Гранулированные
частицы
осаждаются
независимо
друг
от
друга
и
с
пос
тоянной
скоростью,
а
флокулированные,
Koтopыe
могут
быть
естественного
происхождения
или
искусственно
полу
ченными
вследствие
агломерации
коллоидных
веществ,
осаждаются
по-разному
в
зависимости
от
исходной
кон
центрации
частиц.
Если
их
концентрация
мала,
то
в
верхних
слоях
воды
осаждение
каждого
хлопка
происходит
индивидуально,
но
затем
при
столкновении
и
слипании
частиц
~J{oPOCТb
осаждения
увеличиваетсSl.
Это
явление
носит
название
стесненного
или
Флокулянтноro
осаждения.
При
высокой
концентрации
происходит
совместное
осаж
дение
хлопьев
с
четко
выраженной
границей
раздела
фаз
.
между
вер}{ним
слоем
ЖИДКОСТИ
и
ocaд~,?M.,..
Такое
осаж
дение
называют
зонным.
Теория
осаждения
гранулированных
частиц
агрегативно
устойчивой
взвеси,
частицы
которой
в
процессе
осаждения
не
меняют
своей
формы
и
размера,
основана
на
следующих
163

представлениях.
На
частицу
действует
гравитационная
сила,
вследствие
чего
она
двигается
вниз.
Осаждению
частицы
препятствуют
СИЛЫ
сопротивления,
обусловленные
вязкостью
cpeды.
Для
процесса
осаждения
таких
частиц
при
условии
их
малого
размера
и
малой
скорости
осаж
дения
справедливо
уравнение
Стокса:
uo
-
1/18[(Рч
-
...Рж)/fi]gd
2
,
(32)
где
uo
-
скорость
осаждеНИ51,
ИЛИ
гидравлическаJJ
:крупность
части~,
M/C;'p1.4
И
.Р*
-
соответственно
плотность
частиц
и
жидкости,
И/м
;jL{-
ко
эффициент
дин~ической
вязкости
ЖИДКОСТИ,
Па.
с;
g -
ускорение
свободно
го
падеНИfl,
м/с;
d -
диаметр
шарообразной
частицы,
М.
ИЗ
cтpyKTypы
формулы
(32)
ВИДНО,
что
на
скорость
седиментации
влияют
размер
частиц,
разность
nлотностей
частиц
и
жидкости,
температура,
от
КОТОРОЙ
зависит
вяз
кость
среды.
Повышение
температуры
приводит
к
умень
шению
вязкости
и
соответствующему
увеличению
скорости
осаждения
частиц.
Взвешенные
вещества
СТОЧНЫХ
вод
и
взвесь,
образую
щаяся
в
результате
обработки
воды
коагулянтами,
недно
родны
ПО
фОрме
частиц,
их
размеру
и
плотности,
более
TOro,
частицы
в
процессе
осаждения
агломерируются,
вследствие
чего
изменяется
и
скорость
их
осаждения.
Такая
взвесь
называется
nолuдu
сnеРСIl
ой
,
агрегативно
не
устойчивой.
Закономерности
осаждения
частиц
полидиспер
сной
взвеси
оказываются
более
сложными.
Строгого
мате
матическогО
описания
для
осаждения
такой
взвеси
нет,
и
кинетические
зависимости
получают
опытным
путем.
Для
решения
задач
проектирования
отстойных
соору
жений
изучают
зависимость
Э
=
f(l)
,
при
этом
высота
столба
воды
в
отстойном
сосуде
h
должна
быть
не
менее
500
мм,
в
диаметр
сосуда
не
менее
100
ММ.
ЭТИ
условия
обеспечивают
возможность
фиксирования
эффекта
слипания
частиц
и
ускорения
их
падения
при
одновремен
ном
сведении
к
минимуму
искажающего
картину
явления
налипания
частичек
на
стенки
сосуда.
Для
агрегативно
устойчивых
взвесей
необходимое
ДЛЯ
их
осаждения
время
Т
в
сооружении
с
глубиной
н
при
заданном
эффекте
(3)
отстаивания
определится
из
соот
ношения:
Т/Н
= t/h.
(33)
Если
частицы
взвеси
в
процессе
осаждения
образуют
агломераты,
зависимость
(33)
принимает
вид:
164

т
==
t(H
/
h)ll,
где
n -
показатель
степени,
отражающий
влияние
агломерации.
Для
хорошо
сформированных
скоагулированных
хлопьев
n - 0,5;
для
взвешенных
веществ
roРОДСКИХ
СТОЧНЫХ
вод
n-О,2-0,3.
.
Д.п:я
зонноro
осаждения,
которое
наблюдается
при
исходной
концентрации
взвешенных
веществ
более
1000
мг/л,
закономерности
осаждения
описываются
также
эмпирическими
формулами.
В
расчетах
зонного
осаждения
(активного
ила)
иногда
пользуются
понятием
"индекс".
Объемный
индекс
1
-это
объем
(мл)
,
занимаемый
1
г
осадка
после
30
мин
отстаивания.
процессы
отстаивания
-
наиболее
широко
применяе
мые
процессы
в
любой
очистке
природных
вод
ИЛИ
бытовых
и
производственных
отходов.
41.
ФЛОТАЦИЯ
Флотация
(всплывание)
основана
на
разности
удель
ных
масс
взвешенных
частиц
(или
капель
жидкости)
и
жидкости,
в
которой
они
суспензированы.
Флотация
осу
ществима
в
том
случае,
если
примеси
способны
образовы
вать
!'омплекс
"частица-воздух"
с
плотностью,
меньшей
плотности
воды.
В
результате
действия
сил
всплывания,
..
"
гравитации
и
сопротивления
комплексы.
частица--воздух
флотируют
и
образуют
концентрированный
слой
на
сво
бодной
поверхности
ЖИДКОСТИ,
откуда
этот
слой
затем
уда
ляется.
Плотность
примесей
обычно
больше
плотности
во
ДЫ,
поэтому
для
осуществления
флотации
нужно,
чтобы
адгезия
(т.е.
слипание)
МИКроПу3ЫрЬКов
воздуха
и
частиц
БЬL'Iа
выше
смачивающего
действия
воды
на
частицы.
Смачивание
твердого
вещества
ЖИДКОСТЬЮ
определяется
величиной
краевого
угла
контакта
8
между
поверхностью
твердого
вещества
и
пузырьком
газа
(рис.
25)
.
Если
()
-
(),
то
твердое
тело
смачивается
водой
и
адгезия
его
с
воздухом
невозможна.
Если
е
=
1800,
то
твердое
тело
не
смачивается,
а
контакт
его
с
воздухом
максимален.
На
практике
этот
случай
не
встречается,
наибольший
угол
()
==
1100
наблюдается
при
смачивании
сРтути.
Все
обычные
примеси
воды
дают
{)
между
О
и
11
О
,
и
чем
этот
угол
больше,
т.е.
чем
более
rnдрофобна
поверхность
частицы,
тем
выше
прочность
прилипания
частицы
к
пузырьку
воз
духа.
165

.идкость
Рис.
25.
Угол
смачиванИJI
.8
~,
~
;:hФ~т':;;;;
ТВЕРАОЕ
ТЕЛО
Основные
ОТЛИЧIISl
способов
флотации
связаны
с
ВИДОМ
насыщения
жидкости
пузырьками
воздуха.
По
этому
прииципу
различают:
пенную,
наиорную
флотацию
и
элек
трофлотацию.
При
пенной
флотации
воздух
подается
в
систему
через
ПОРИСТЫС
материалы;
при
напорной
-
воду
насыщают
воздухом
под
давлением,
после
снятия
котороro
начинается
выдлениеe
пузырьков
воздуха;
при
алектрофло
тации
пузырьки
газа
образуются
в
результате
электролиза
воды.
Метод
флотации
нашел
широкое
применение
в
практике
ОЧИСТКИ
сточных
ВОД,
особенно
производственных.
Из
воды
удаляются
взвешенные
вещества,
а
TaKx~e
частично
коллоидные
и
растворенные.
Флотация
применяется
и
при
очистке
природных
вод
С
мутностью
до
150
мг/
л
и
цветностью
ДО
200
град.
42.
ФИЛЬТРОВАНИЕ
Фильтрование
-
процесс
процеживания
суспензии.
че-
и
v
рез
пори
стыи
материал,
задерживающии
твердые
~римеси
·И
пропускающий
воду.
Если
размеры
частиц
больше
раз
меров
пор
фильтрующей
загрузки,
ТО
частицы
останутся
на поверхности
загрузки.
Этот
тип
фильтрования
называ
ется
поверхностным,
осадочным
или
ОПОРНЫМ.
Если
частицы
проходят
внутрь
материала
загрузки,
то
процесс
называется
фИЛЬ'l'рованием
в
объеме,
или
объемным
фильтрованием~
С
поверхностным
фильтрованием
мы
встречаемся
при
движении
воды
через
фильтры
из
пористой
керамики,
при
фильтровании
под
давлением
или
вакуумом
через
сетчатые
и
тканевые
переroродки
и
.т.д.
При
ЭТОМ
на
фильтре
за
держиваются
все
частицы,
размеры
которых
превышают
размеры
пор
фильтрующей
ocHoBы.
В
результате
на
ней
формируется
слой
осадка,
ИВЛЯЮЩИЙСЯ
дополнительным
фильтрующим
слоем.
Процесс
поверхностного
фильтрования
подчиняется
за
кону
дарен)
по
которому
скорость
фильтрования
v
166

пропорциональна
потерям
напора
р,
коэффициент
пропорциональности
J(
зависит
от
динамической
вяз
кости
~
и
вмичины,
определяющей
сопротив:ление
среды
R:
v -
Кр;
К
==
1/
<J'R>;
V
..
р/
~R.
(34)
В
свою
очередь,
сопротивление
среды
R
складывается
из
начального
сопротивления
фильтрующей
ocHoBы
R
H
И
сопротивления
образовавшеrocя
СЛОЯ
осадка
R
oc
:
R
=-=
R
и
+ R
oc
•
(35)
Сопротивление
слоя
осадка:
R
oc
-=
гМ/
Р,
(36)
где
r -
удельное
сопротивление
осадка
фильтрованию;
М
-
масса
отложивwеr:ocя:
осадка;
F -
площадь
фильтра.
После
подстановки
(35)
и
(36)
в
(34)
и
преобразования
получаем
выражение
ДЛЯ
скорости
фильтрования
v:
v
..
р/
[jI(rM/
F + R
H
].
При
фильтровании
воды
со
взвешенными
веществами
через
слой
песка
или
другие
зернистые
материалы,
т.е.
при
объемном
фильтровании,
наблюдаются
следующие
про
цессы:
извлечение
взвешенных
частиц
из
воды
и
их
за
крепление
на
зернах
фильтрующей
загрузки
ПОД действием
. .
сил
адгезии;
отрыв
части
задержанных
частиц
от
зерен
загрузки
и
переное
их
в
последующие
слои,
где
они
снова
задерживаются
в
порах
загрузочного
материала.
До
тех
пор
пока
интенсивность
первого
процесса
пре
выlаet
интенсивность
второго,
происходит
очистка
ВОДЫ
от
взвешенных
частиц.
С
течением
времени
в
загрузке
накаnливаегся
осадок,
при
этом
объем
свободного
поровоro
пространства
уменьшается,
а
гидравлическое
сопротивлеlШе
загрузки
возрастает.
это
про
является
в
увеличении
потери
напора
в
фильтрующей
~груз
ке,
повышении
концентрации
взвеси
в
фильтрате.
Время,
в
течение
которого
слой
загрузочноro
материала
обеспечивает
очистку
вoды
до
требуемой
концентрации,
называется
време
нем
защитного
действия
заrpУЗКИ
1'3
:са
l/K·bIa(x
-
ХО/Ь)
,
где
Ки
Х
О
-
KOHcraHTbl,
зависящие
только
от
требуемого
эффекта
очистки
и
определяемые
по
номограммам
Д.М.
Минца;
Ы
а
и
Ь
-
кинетические
парамет
ры
процесса
фильтрования,
характеризующие
соответственно
скорость
проникновения
взвести
В
rnубь
загрузки
и
интенсивность
прилипания
частиц
к
зернам
загрузки.
167

Продолжительность
работы
фильтра
tu
ДО
момента
достижения
предельной
потери
напора
определяется
из
вы
раж.ения:
tH
-
[(Н
пр
-
Ho)ioJx/
НоТ,
где
НО
и
Н
пр
-
соответственно
начальная
и
предельно
допустимая
потеря
на
пора
в.загрузке
фильтра;
io
-
темп
ПрИJ>OCта
потери
напора;
х
-
толщина
СЛОЯ
загрузки.
Отношение
tз/
tH
характеризует
надежность
работы
фильтра
и
при
ta/t
H
l
гарантирует
высокое
качество
фильтрата.
Чем
больше
это
отношение,
тем
выше
степень
санитарной
надежности
фильтра.
Процесс
фильтрования
-
ОДИН
ИЗ
основных
приемов
в
водоподгот\)вке,
обеспечивающий
удаление
из
природной
воды
как
взвешенных,
так
и
КОЛЛОИДНЫХ
примесеЙ.
Этот
метод
широко
применяетс'я
также
ДЛЯ
доочистки
СТОЧНЫХ
ВОД,
прошедших
сооружение
биологической
или
физико
химической
очистки.
Особенность
фильтрования
биологически
очищенных
сточных
вод
заключается
в
том,
что
наряду
с
процессом
задержания
яерастворенныx
приме
сей
в
фильтрах
достаточно
интенсивно
идут
биохимические
процессы
окисления
остаточных
органических
веществ.
43.
МЕМБРАННАЯ
СЕПАРАЦИЯ
Под
термином
мембранная
сепарация
понимают
проц
ессы
разделения
истинных
растворов
с
помощью
различного
рода
мембран.
Этот
термин
объединяет
процессы
гunерфu..льmрацuu
или
обратного
осмоса,
ульm-
рафильтрацuu
и
элеJCтродuШLUЗа.
Панятие
обратный
осмос
показывает
обратимость
про
цесса
естественного
осмоса,
paCCMOTpeHHOro
в
з.
Известно,
что
прямой
(или
естественный)
ОСМОС
(рис.
26,
а)
наблюдается,
если
чистая
вода
А
и
водныи
раствор
Б
разделены
полуп
роницаемой
мембраной
В,
через
которую
вода
устреМi'lЯется
v
В
C'fOJЮНУ
раствора.
Эrот
процесс
продолжается
до
тех
пор,
пока уровень
раствора
не
поднимается
на
высоту
Н,
равную
осмотическому
давлению
раствора
(рис.
26,
б).
При
этом
достигается
осмотическое
равновесие.
для
того,
чтобы
за
ставить
молекулы
воды
двигаться
в
противоположном
прямому
осмосу
направлеШlИ
к
раствору
Б,
нужно
при.д:ожить
ГИДIЮ-
.статическое
давление
Р,
величина
которого
должна
быть
боль
ше
осмотического
давления
Н
(рис.
26,
в).
Упрощенная
схема
обратноro
осмоса
показана
на
рис.
26,
г.
Очищаемая
вода
J
168
а)
б)
8.
-.~-
~
-.'
.
~--=-
---=-
А ..
~
Б
6)
р
г}
~~
2
f
:В·.
-=---
~--=
..
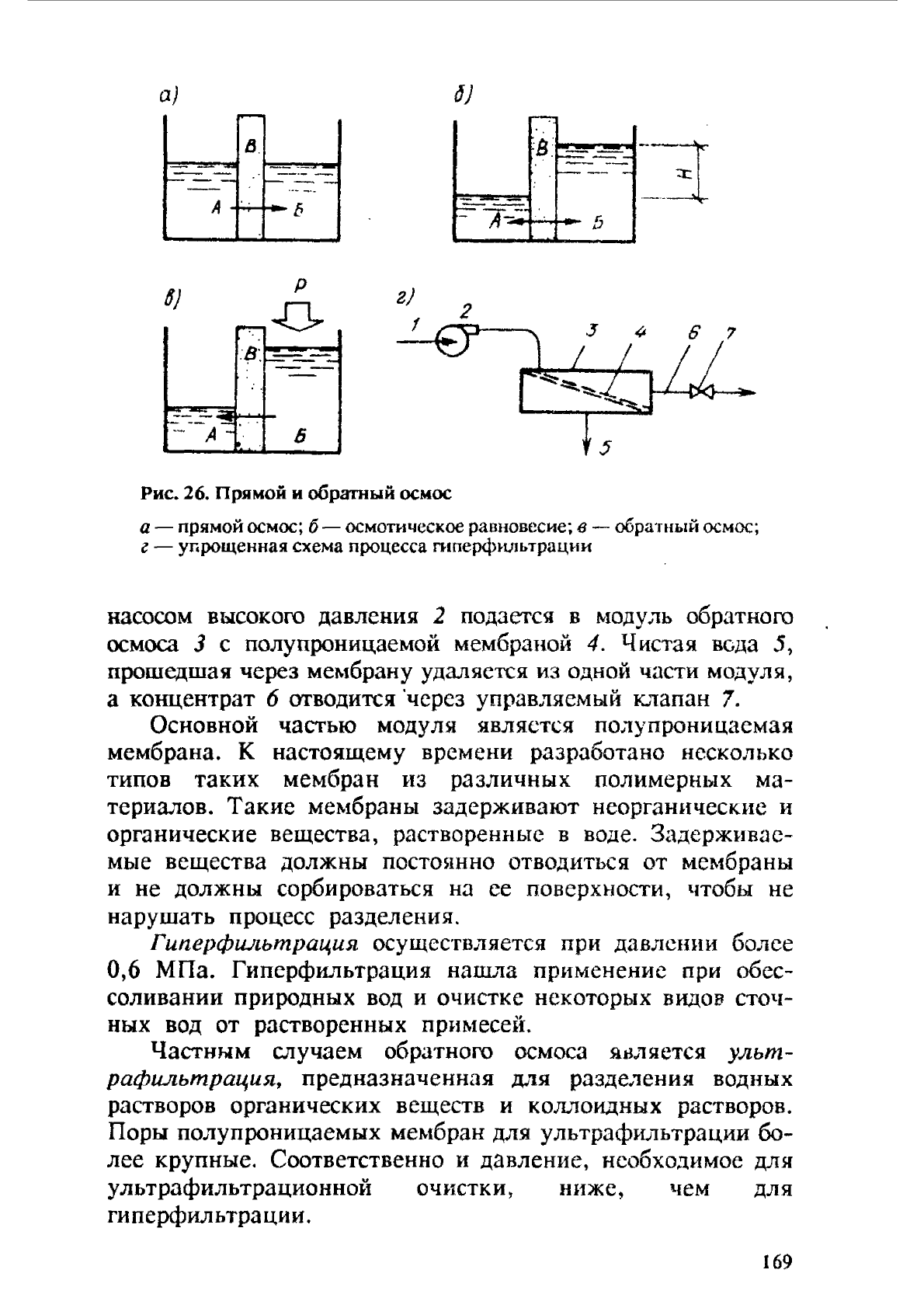
Рис.
26.
Прямой
и
обратный
ОСМОС
а
-
прямой
осмос;
6 -
осмотическое
равновесие;
в
-
обратный
осмос;
г
-
упрощенная
схема
процесса
гиперфИJIьтрацни
насосом
высокого
давления
2
подается
в
~IОДУЛЬ
обратного
осмоса
3
с
полупроницаемой
мембраной
4.
Чистая
веда
5,
прошедшая
через
меr..lбрану
удаляется
из
одной
чисти
модуля,
а
концентрат
6
отводится
'через
управляемый
KTranaH
7
..
ОСНОВНОЙ
частью
модуля
ЯВJIЯСТ(Я
полупроницаемая
мембрана.
к
настоящему
времени
разработано
несколько
типов
таких
мембран
из
различных
полимеРНI)IХ
ма
териалов.
Такие
ме~lбраны
задерживают
неорганические
и
органические
вещества,
растворенные
в
воде.
Задерживае
мые
вещества
ДОЛЖНЫ
постоянно
ОТВОДИТЬСЯ
от
ме~fбраны
и
не
ДОЛЖНЫ
сорбироваться
на
ее
поверхности,
чтобы
не
нарушать
процесс
разделения.
ГunерФuльmрацuя
осуществляется
при
давлении
более
0,6
МПа.
Гиперфильтрация
нашпа
применение
при
обес
соливании
природных
вод
И
очистке
некоторых
ВИДОВ
сточ
ных
ВОД
от
растворенных
ПРИ~fесеЙ.
Частным
случаем
обратного
осмоса
я.gляется
ульт
раФuльmрацuя,
предназначенная
ДJ1Я
разделения
ВОДНЫХ
растворов
органических
веществ
и
комондных
растворов.
Поры
полупроницаемых
ме"'Iбран
ДЛЯ
ультрафильтрации
бо
лее
крупные.
Соответственно
и
давление,
необходимое
ДЛЯ
ультрафильтрационной
ОЧИСТКИ,
ниже,
чем
для
гиперфильтрации.
169
