Чиркина Т.Ф., Битуева Э.Б. (сост.) Методические указания к выполнению лабораторного практикума по курсу Пищевая химия для студентов пищевых специальностей
Подождите немного. Документ загружается.

Подтверждения наличия БК и СК.
Объем NaOH, израсходованный на титрование (V), мл
Молярная концентрация раствора NaOH (C), моль/дм
3
Молекулярная масса бензойной кислоты (M), г/моль
Общий объем приготовленного раствора (V
1
), мл
Объем фильтрата, взятый для экстракции хлороформом (V
2
), мл
Масса навески продукта (m), г
Массовая доля бензойной кислоты (X), %
7.4. Контрольные вопросы
1. Сущность метода определения бензойной и сорбиновойкислот.
2. Растворы используемые для осаждения белковых веществ
3. Чем экстрагируют бензойную кислоту из водной вытяжки
4. Для чего используется раствор НСL.
5. В чем растворяют остаток бензойной кислоты.
6. Понятие пищевые добавки .
7. Классификация пищевых добавок.
8. Чем отличаются биологически активные добавки от пищевых добавок.
9. Классификация биологически активных добавок.
10. Принцип действия консервантов.
11. Цель введения консервантов в пищевые продукты.
12. Различия красителей и цветокорректоров.
13. Положительные и отрицательные стороны использования пищевых добавок.
14. Опасность отдаленных последствий при использовании пищевой добавки.
15. Сахарозаменители, требования предъявляемые к ним.
16. Приведите примеры природных антиокислителей.
17. Приведите примеры пищевых добавок, ускоряющих технологические процессы.
18. Пищевые добавки, запрещенные в России.
19. Главное свойство пищевых добавок.
20. Роль БАД в питании.
Раздел III.
БЕЗОПАСНОСТЬ ПИЩИ
Лабораторная работа №8
Определение нитратов
Цель: ознакомиться с методами определения нитратов в пищевых продуктах.
Интенсификация производства овощей приводит к применению азотистых удобрений.
Это влечет за собой повышение содержания в сырье и, следовательно, в продуктах питания
нитратов, которые могут восстанавливаться в нитриты в верхних отделах пищеварительного
тракта и оказывать вредное влияние на организм человека.
На концентрацию нитратов в растениях влияет недостаток света, сроки уборки уро-
жая. Так увеличение продолжительности вегетации в весенний период положительно сказы-
вается на снижение содержания нитратов в овощах. В молодых растениях нитратов на
50÷70% больше чем в зрелых.
При хранении овощей может происходить микробиологическое восстановление нит-
ратов под действием ферментов нитратредуктаз. Поэтому для продуктов содержащие нитра-
ты опасны высокие температуры в течение длительного времени.
Установлено, что нитраты могут угнетать активность иммунной системы организма,
снижать устойчивость организма к отрицательному воздействию факторов окружающей сре-
ды. Нитраты и нитриты также способны изменять активность обменных процессов в орга-
низме. Допустимая суточная доза поступления нитратов с пищей составляет 300÷350 мг.
8.1. Ионометрический метод
Наиболее простым и экспрессным методом определения нитратов является иономет-
рический, но его можно применять только при контроле свежей растительной продукции.
Более универсальным методом, пригодным при анализе нитратов как в сырье, так и в гото-
вой продукции, является фотометрический метод.
Сущность ионометрического метода состоит в извлечении нитратов из анализируемо-
го материала раствором алюмокалиевых квасцов с последующим измерением их концентра-
ции, в полученной вытяжке, с помощью ионоселективного электрода. Для ускорения анализа
вместо вытяжки может быть использован сок продукции, разбавленный раствором алюмока-
лиевых квасцов. При анализе капусты, для разрушения примесей, мешающих определению
нитратов, дополнительно проводят их окисление марганцевокислым калием.
Нижний предел обнаружения нитратов – 6 мг на 1 л анализируемого раствора. Предел
надежного определения нитратов в анализируемой пробе – 30 мг/кг.
Техника выполнения. 10 г измельченного материала взвешивают с точностью до вто-
рого десятичного знака, помещают стакан гомогенизатора или измельчителя, наливают 50 мл
1%-ного раствора алюмокалиевых квасцов и гомогенизируют в течение 1 минуты при часто-
те вращения 6000мин
-1
. При отсутствии гомогенизатора пробу с квасцами перемешивают в
стакане с помощью мешалки в течение 3-х минут. В полученной суспензии определяют кон-
центрацию нитрат-ионов. Гомогенизацию можно заменить растиранием массы в ступке с
прокаленным песком или битым стеклом, или 15-минутным нагреванием суспензии в кипя-
щей водяной бане с последующим охлаждением.
При анализе капусты 10 г измельченного сырья помещают в стакан на 100 мл, нали-
вают 50 мл экстрагирующего раствора, перемешивают с помощью мешалки в течение 3-х
минут. Не прекращая перемешивания, добавляют (2-3) капли 33%-ного раствора перекиси
водорода до обесцвечивания раствора. В полученной суспензии измеряют концентрацию
нитрат-ионов.
При использовании для анализа сока отбирают пипеткой 10 мл сока, прибавляют 50
мл 1%-ного раствора алюмокалиевых квасцов, перемешивают и в полученном растворе оп-
ределяют концентрацию нитрат-ионов.
Измерение концентрации нитрат-ионов проводят непосредственно в логарифмиче-
ских единицах pC
NO3
(pC
NO3
= -log C
NO3
) по шкале иономера, предварительно отградуирован-
ного по растворам сравнения, или в милливольтах с последующим определением наличия
pC
NO3
по градуировочному графику, построенному по результатам измерения ЭДС элек-
тродной пары в растворах сравнения или в единицах концентрации, в соответствии с инст-
рукцией к прибору.
Перед началом работы измеряют показания растворов сравнения в порядке возраста-
ния концентрации, начиная с меньшей: с (NO
3
) = 0,0001 моль/дм
3
.
Перед погружением электродов (ионоселективного нитратного и электрода сравнения
– хлорсеребрянного) исследуемые суспензии взбалтывают. Показания прибора считывают не
ранее, чем через 1 минуту после прекращения дрейфа показания прибора. Температура ис-
пытуемых проб и растворов сравнения должна быть одинаковой.
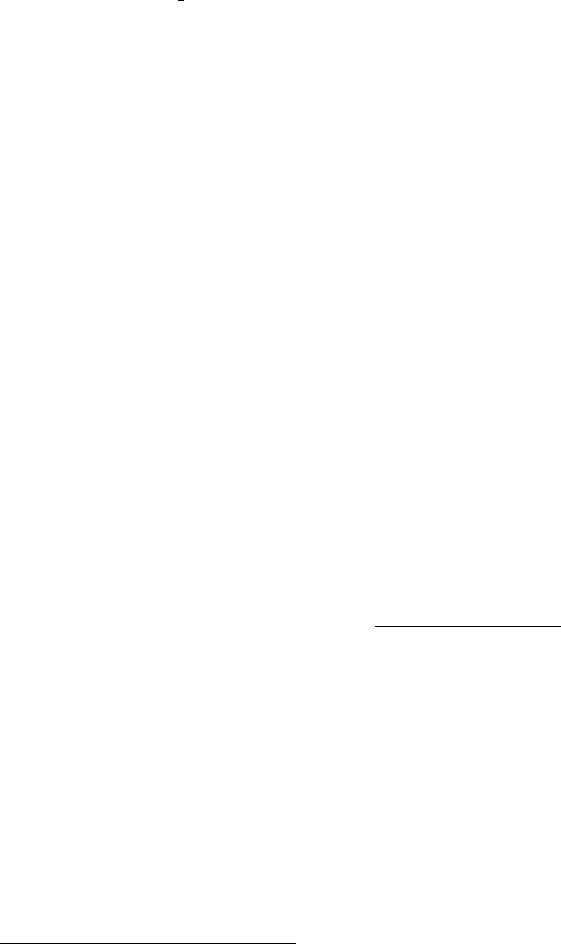
После каждого измерения электроды ополаскивают дистиллированной водой и про-
мокают фильтровальной бумагой.
По полученному значению величины pC
NO3
– определяют содержание нитрат-ионов в
мг/кг в исследуемом продукте.
Оценку качества продукции проводят в соответствии с допустимыми уровнями со-
держания нитратов в растительных продуктах. Допустимые отклонения от ПДК при содер-
жании нитратов до 100 мг/кг – 20%, свыше 100 мг/кг – 24%.
8.2. Спектрофотометрический метод
Принцип метода. Определение нитратов основано на образовании бесцветного ком-
плекса нитротолуола. Метод обладает большой чувствительностью по сравнению с сущест-
вующими, т.к. нитраты определяются непосредственно, без предварительного их восстанов-
ления из нитритов. Чувствительность метода – 0,016 мг/кг.
Техника выполнения. 25 г измельченного продукта (овощи – на терке, зерновые – на
кофемолке, мясные изделия – в мясорубке) помещают в колбу Эрленмейера на 250 мл с
притертой пробкой, извлекают присутствующие токсические вещества 50-100 мл дистилли-
рованной водой из овощей, зерновых (плюс 5 мл – концентрированной уксусной кислоты в
случае мясных изделий) при взбалтывании на встряхивателе в течение 15 минут. Затем экс-
тракт фильтруют через ватный фильтр и прибавляют к нему 25-50 мл суспензии гидроокиси
алюминия. После 30-минутного контакта, когда осадок гидроокиси алюминия станет серого
цвета, его отфильтровывают через беззольный складчатый фильтр (синяя, красная, желта
лента), а в фильтрате определяют нитраты.
Для определения нитратов к 5 мл анализируемого раствора, помещенного в кониче-
скую колбу на 100 мл с притертой пробкой, прибавляют 5 мл толуола и 15 мл серной кисло-
ты (3:1). Раствор встряхивают в течении 5 минут в делительной воронке и после охлаждения
до 20
0
С отделяют бесцветный органический слой и измеряют оптическую плотность на спек-
трофотометре при λ = 284 нм, в кювете l = 1 см против дистиллированной воды.
Содержание нитрата определяется по соответствующему калибровочному графику,
для построения которого используется стандартный раствор нитрата калия.
При определении нитратов раствором сравнения служит дистиллированная вода.
Содержание нитратов в пробе рассчитывают по формуле:
1
1000001,0
Vm
VA
X
⋅
⋅
⋅
⋅
=
,
где: A - содержание определяемых веществ в мкг, рассчитываемое по калибровочно-
му графику;
V - общий объем фильтрата, мл;
V
1
- анализируемый объем, мл;
0,001 - коэффициент пересчета мкг в мг;
1000 - коэффициент пересчета г в кг;
m - навеска продукта, г.
Регистрируемые показатели:
Общий объем фильтрата (V), мл;
Анализируемый объем (V
1
), мл;
Масса навески (m), г;
Содержание нитратов в пробе (X), кг.

Лабораторная работа №9
Обнаружение антибиотиков в молоке
Цель работы: ознакомиться с методикой определения антибиотиков в молоке.
Антибиотики в молоке являются чужеродными веществами, могут попасть в него при
непосредственном лечении вымени или опосредованно, через корма или при лечении самого
животного. Методы обнаружения антибиотиков в молоке основаны на восстановлении реза-
зурина или метиленового голубого при развитии в молоке чувствительного к антибиотикам
микроорганизмам вида Streptoccocus thermofilus. Метод позволяет обнаружить пенициллин
более 0,01 МЕ/мл, стрептомицин более 30 мкг/мл, тетрациклин – от 1 МЕ/мл, олендомицин –
от 10 МЕ/мл.
9.1. Алгоритм работы
Сформулировать этапы выполнения лабораторной работы.
Подготовить рабочую тест-культуру.
9.2. Определение антибиотиков
Техника выполнения. В чистую пробирку наливают 10 мл исследуемого молока, за-
крывают резиновой пробкой и нагревают на водяной бане до 85÷90
0
С с выдержкой 10 минут,
затем охлаждают до 42÷45
0
С. После этого в пробирку вносят стерильной пипеткой 0,3 мл
рабочей тест-культуры. Содержимое пробирки тщательно перемешивают путем 3-кратного
перевертывания, после чего пробирку выдерживают в водяной бане при температуре
42÷43
0
С в течении 1 час. 40 мин – 2 час. 20 мин. Затем в пробирку вносят 1 мл 0,05%-ного
раствора резазурина с температурой не ниже 18÷20
0
С и тщательно перемешивают, перевер-
тывая пробирку. Пробирку с молоком и резазурином выдерживают при 42÷43
0
С в течение 15
минут.
В случае использования метиленового голубого его вносят одновременно с рабочей
тест-культурой в количестве 0,1 мл 0,5%-ного раствора.
Примечание:
растворы резазурина и метиленового голубого готовятся на дистиллиро-
ванной кипяченой воде.
9.3. Чтение результатов
При отсутствии в молоке антибиотиков, ферменты, выделяемые термофильным
стрептококком, восстанавливают краситель, и молоко будет иметь белый или розовый цвет.
При наличии антибиотиков, они ингибируют развитие тест-культуры, в результате че-
го она не вырабатывает ферменты, и красители не восстанавливаются, при этом молоко ок-
рашено в их цвет: в случае с резазурином – сине-стальной, сине-фиолетовый, в случае с ме-
тиленовым голубым – голубой. Голубое кольцо, образующееся в пробирке на поверхности
молока высотой 1 см, не учитывают.
Регистрируемые показатели:
Окраска исследуемых проб.
9.4. Контрольные вопросы
1. Что такое нитраты?
2. Почему говорят об опасности нитратов для людей?
3. Допустимая суточная доза нитратов для человека?
4. Основные источники попадания нитратов в пищу?
5. Как уменьшить содержание нитратов в процессе технологической переработки ?
6. Сущность ионометрического метода определения нитратов.
7. Достоинства и недостатки ионометрического метода.
8. Сущность спектрофотометрического метода.
9. Достоинство спектрофотометрического метода.
10. Объяснить почему контролируется содержание нитратов, если известно, что нит-
раты являются нормальным продуктом обмена азотистых веществ любого организма.
11. Причины возникновения метгемоглобинемии.
12. Понятие ксенобиотиков.
13. Промзагрязнения.
14. Общие свойства ксенобиотиков.
15. Пути загрязнения пищевого сырья и готовых продуктов.
16. Контаменанты, попадающие в пищевые продукты в результате химизации сель-
ского хозяйства
17. Антибиотики, пути их попадания в пищевые продукты.
18. В каких продуктах обнаружено значительное количество нитрозоаминов ?
19. Что происходит с нитратами при хранении овощей ?
20. Вещества, образующиеся в пищевых продуктах в результате технологических
процессов.
ПРИЛОЖЕНИЯ
Приложение 1
Таблица 1
Допустимые уровни содержания нитратов в продуктах
растительного происхождения СанПиН 42-123-469-88 от 30.05.88
Содержание нитратов, мг/кг
Пищевой продукт
из открытого
грунта
из закрытого
грунта
Картофель
Капуста белокочанная:
-ранняя (до 1 сентябрь)
-поздняя
Морковь:
-ранняя (до 1 сентября)
-поздняя
Томаты
Огурцы
Свекла столовая
Лук репчатый
Лук-перо
Зеленые культуры (салаты.,
капуста салатная, петрушка,
сельдерей, укроп и т.д.)
Дыни
Арбузы
Перец сладкий
Кабачки
250
900
500
400
250
150
150
1400
80
600
2000
90
60
200
400
-
-
-
-
-
300
400
-
-
800
3000
-
-
400
400
Тыквы (для изготовления кон-
сервов)
Виноград столовых сортов
Яблоки
Груши
200
60
60
60
-
-
-
-
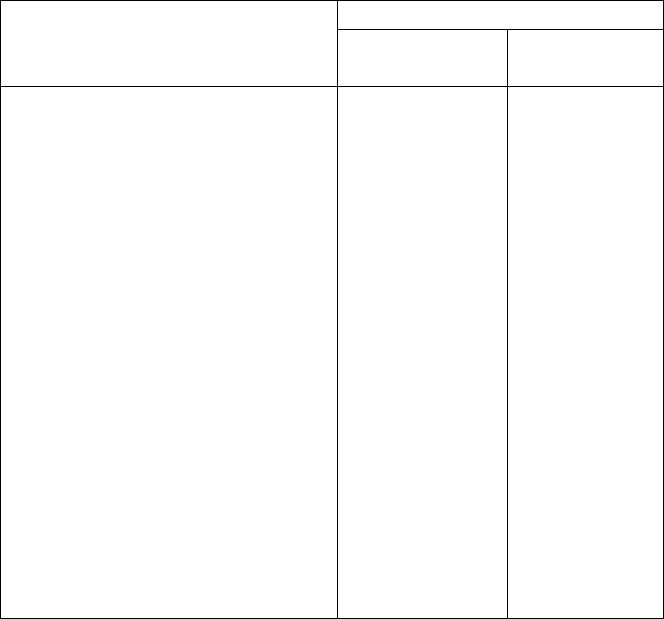
Таблица 2
Перевод значений
3
NO
pC
в массовую долю нитратов в NO
3
-
(млн
-1
, мг/кг) при анализе
вытяжки из картофеля, столовой свеклы, лука-репки, винограда (H:V=1:5)
Сотые доли
−
3
NO
pC
pC
NO3
-
.00 .01 .02 .03 .04 .05 .06 .07 .08 .09
1,6
1,7
1,8
1,9
2,0
2,1
2,2
2,3
2,4
2.5
2.6
2,7
2.8
2,9
3.0
3.1
3,2
3,3
3,4
3,5
3,6
3,7
3,8
3,9
4,0
903
3
717
5
569
9
452
7
359
6
285
6
226
9
180
2
432
113
7
993
717
570
453
366
286
227
180
143
114
90,3
70,7
57,0
45,4
36,0
882
770
12
557
0
442
4
351
4
279
1
221
7
176
1
139
9
111
1
863
702
557
442
351
279
222
176
140
111
88,3
70,1
55,7
44,2
35,1
862
668
52
544
3
432
3
343
4
272
8
216
1
172
1
133
7
108
6
853
686
554
423
343
273
217
172
137
109
86,3
68,5
54,4
43.2
34,3
843
0
696
531
9
422
5
335
6
266
6
211
7
166
2
133
6
106
1
843
570
532
422
335
267
212
166
134
106
84,3
70,0
53,2
42,2
33,6
823
8
654
4
519
8
419
8
328
0
260
5
206
9
164
4
130
6
103
7
824
554
520
413
328
261
207
164
131
104
82,4
65,4
52,0
41,3
32,8
805
0
637
5
507
9
403
5
320
5
254
6
202
2
160
5
127
6
101
3
805
639
508
403
320
255
202
161
128
101
80,5
63,9
50,8
40,3
32,0
786
7
824
9
498
4
394
3
313
2
248
8
197
6
157
0
124
7
990
787
625
496
394
313
249
198
158
125
99,0
78,7
62,5
49,6
39,4
31,3
768
8
610
7
485
1
385
3
306
1
243
1
193
1
153
4
121
8
968
761
611
485
385
306
243
193
153
122
97,0
76,9
61,1
48,5
38,5
30,6
751
3
596
8
474
0
376
5
299
1
237
6
188
7
149
9
119
1
946
751
597
474
377
299
238
189
150
119
95,0
75,1
59,6
47,4
37.7
29,9
734
258
32
453
3
368
0
292
3
232
2
184
4
146
5
116
4
924
734
583
463
368
292
232
184
146
116
92,0
73,4
58,3
46,3
36,8
29,2
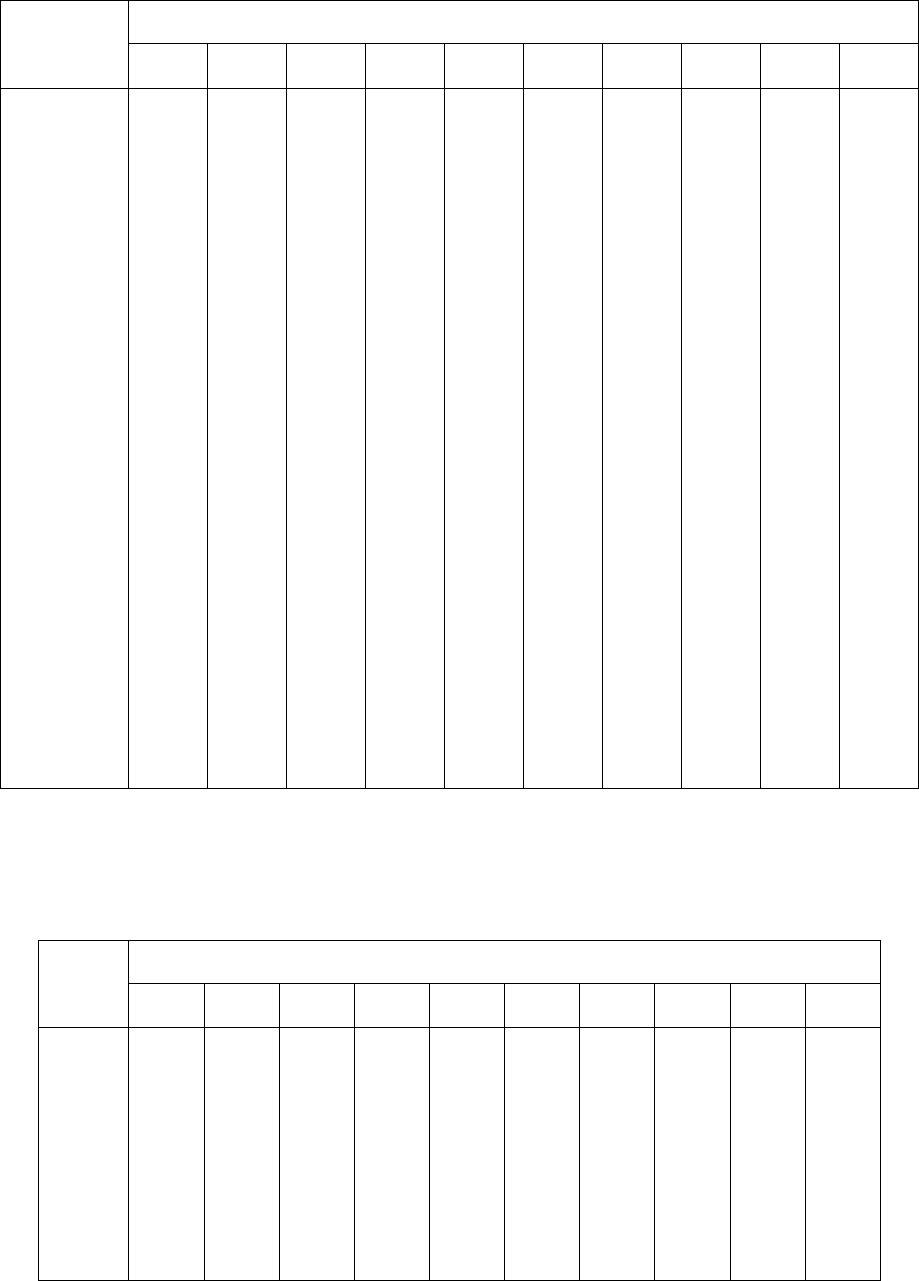
Таблица 3
Перевод значений
3
NO
pC
в массовую долю нитратов в NO
3
-
(млн
-1
, мг/кг) при анализе
вытяжки из капусты белокочанной, моркови, томатов, огурцов, лука-перо, дыни, арбузов,
тыквы, перца сладкого, кабачков, зеленых культур, яблок, груш (H:V=1:5)
Сотые доли
−
3
NO
pC
pC
NO3
-
.00 .01 .02 .03 .04 .05 .06 .07 .08 .09
1,6
1,7
1,8
1,9
2,0
2,1
2,2
2,3
2,4
2.5
2.6
2,7
2.8
2,9
3.0
3.1
3,2
3,3
3,4
3,5
3,6
3,7
3,8
3,9
4,0
9188
7299
5798
4606
3653
2906
2308
1833
1456
1157
919
730
580
461
336
291
231
183
146
116
91,9
73,0
58,0
46,1
36,6
8979
7138
5669
4500
3576
2840
2256
1792
1423
1130
898
713
576
450
357
284
226
170
142
113
89,8
71,3
56,7
45,0
35,7
8775
6970
5537
4398
3493
2775
2204
1751
1391
1105
877
697
554
440
349
277
220
175
139
110
87,7
69,7
55,4
44,0
34,9
8575
6812
5411
4298
3414
2712
2154
1711
1350
1080
858
681
541
430
341
271
215
171
136
108
85,8
68,1
54,1
43,0
34,1
8380
6656
5287
4200
3336
2650
2105
1672
1328
1055
838
666
529
420
334
265
210
167
133
106
83,8
66,6
52,9
42,0
33,4
8189
6505
5167
4101
3260
2590
2057
1634
1298
1031
819
650
517
410
326
259
206
163
130
103
81,9
65,0
51,7
41,0
32,6
8003
6357
5049
4011
3186
2531
2010
1597
1268
1007
800
636
505
401
319
253
201
166
127
101
80,0
63,6
50,5
40,1
31,9
7821
6212
4935
3920
3113
2473
1964
1560
1239
985
782
621
439
392
311
247
196
156
124
98
78,2
62,1
49,3
39,2
31,1
7643
6071
4822
3830
3043
2417
1920
1525
1211
962
764
607
482
383
304
242
192
152
121
96
76,4
60,7
48,2
38,3
30,4
7460
5933
4712
3743
2973
2362
1876
1490
1184
940
747
593
471
374
297
236
186
149
118
94
74,7
59,3
47,9
37,4
29,7
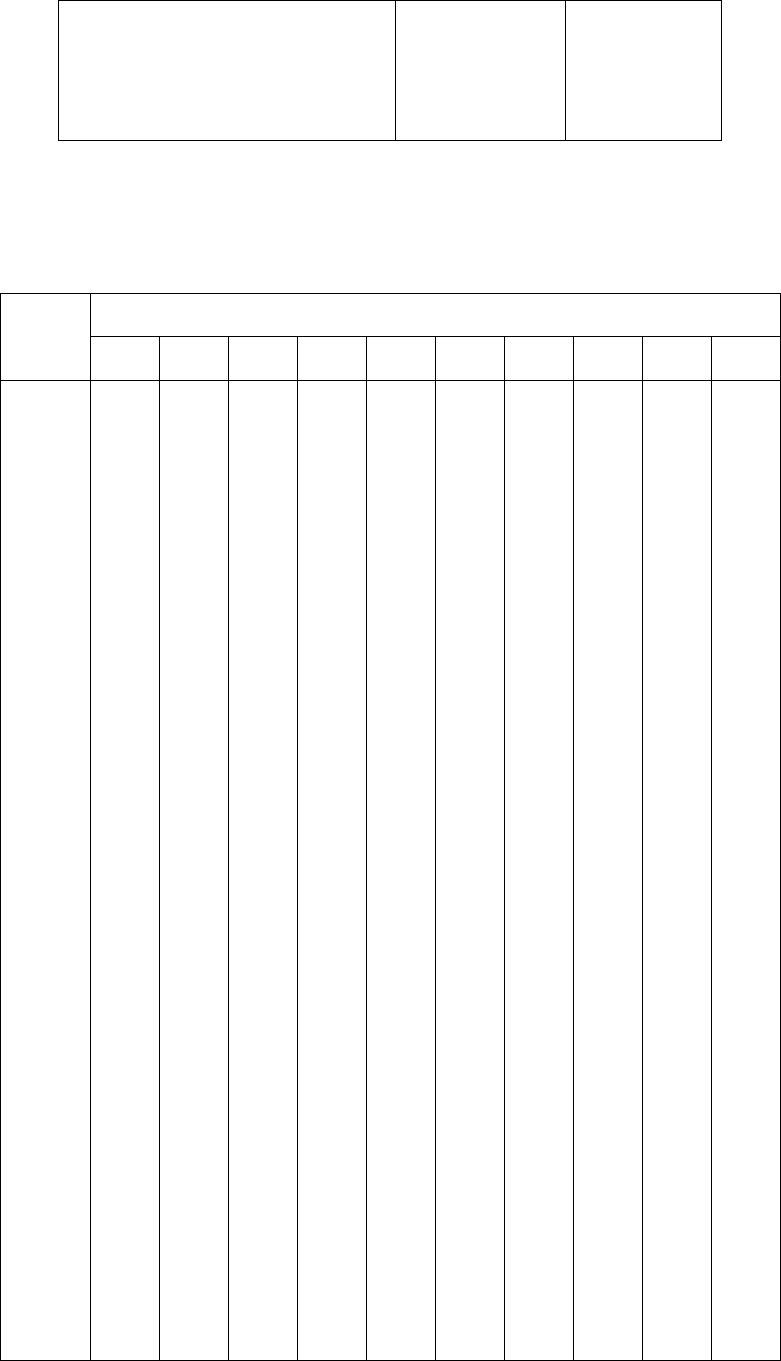
Таблица 4
Перевод значений
3
NO
pC
в массовую долю нитратов в NO
3
-
(млн
-1
, мг/кг) при анализе
сока свеклы и моркови (V
сока
:V
экстрагир.р-ра
=1:5)
Сотые доли
−
3
NO
pC
pC
NO3
-
.00 .01 .02 .03 .04 .05 .06 .07 .08 .09
1,6
1,7
1,8
1,9
2,0
2,1
2,2
2,3
2,4
7943
6309
5011
3981
3162
2512
1995
1585
1259
7762
6165
4897
3890
3090
2454
1950
1549
1230
7585
6025
4786
3802
3020
2399
1905
1515
1200
7412
5888
4677
3715
2951
2344
1862
1479
1175
7244
5754
4570
3630
2884
2291
1820
1445
1148
7079
5623
4466
3548
2818
2239
1778
1412
1122
6918
5495
4346
3467
2754
2188
1738
1380
1096
6760
5370
4265
3388
2691
2138
1698
1349
1071
6606
5248
4168
3311
2630
2089
1659
1318
1047
6456
5128
4073
3236
2570
2042
1622
1288
1023

2.5
2.6
2,7
2.8
2,9
3.0
3.1
3,2
3,3
3,4
3,5
3,6
3,7
3,8
3,9
4,0
1000
794
631
501
398
316
251
200
158
126
100
79
63
50
40
32
977
776
617
490
389
309
245
195
155
123
98
78
62
49
39
31
966
759
603
479
380
302
240
191
151
120
95
76
60
48
38
30
933
741
589
458
372
295
234
186
148
117
93
74
59
47
37
30
912
724
575
457
363
288
229
182
145
115
91
72
58
46
36
29
891
708
562
447
355
282
224
178
141
112
89
71
56
45
35
28
871
692
549
436
347
275
219
174
138
110
87
69
55
44
35
28
851
676
537
427
339
269
214
170
135
107
85
68
54
43
34
27
832
661
525
417
331
263
209
166
132
105
83
66
52
42
33
26
813
646
513
407
324
257
204
162
129
102
81
65
51
41
32
26
Приложение 2
ПРИГОТОВЛЕНИЕ РАСТВОРОВ
Лабораторная работа № 2
Реактивы (2.2.1): уксусный натрий; едкий натрий; пепсин; трипсин; 0,1 н раствор
серной кислоты; индикатор Таширо (смешанный); 0,1 н раствор едкого натрия; 0,1 н раствор
соляной кислоты; 20% трихлоруксусная кислота; фосфатный буфер рН 8,0.
Лабораторная работа № 3
Реактивы (3.2):1,25 % раствор серной кислоты; 1,25 % раствор едкого натрия; спирт;
эфир.
Определение пектиновых веществ:
Реактивы (3.3): 0,3 моль/дм
3
раствор соляной кислоты; 1 % раствор лимоннокислого
аммония; 10 % раствор едкого натрия; 0,4 % раствор едкого натрия; 1 моль/дм
3
раствор ук-
сусной кислоты; 2 моль/дм
3
хлорида кальция.
Лабораторная работа № 4
Реактивы (4.2): 0,5 М раствор хлорида калия; биуретовый реактив.
Приготовление биуретового раствора. 1,5 г сульфата меди (CuSO
4
·5H
2
O) и 6,0 г
виннокислого натрия-калия (NaKC
4
H
4
O
6
·4H
2
O) растворяют в 500 мл воды. К этому раствору
при хорошем помешивании добавляют 300 мл 10%-ного раствора NaOH
3
свободного от
Na
2
CO
3
, и 2 г KI для предотвращения самопроизвольного восстановления. Раствор доводят
до 2 мл и хранят в полиэтиленовой склянке.
Примечание.
Биуретовую реакцию нельзя проводить в присутствии солей аммония в
виду образования медноаммиачных комплексов.
Лабораторная работа № 5
Реактивы (5.3): смесь эфира и этанола (2:1); 1% спиртовой раствор фенолфталеина;
0,1н раствор едкого калия или натрия.
Реактивы (5.4): хролоформ; ледяная уксусная кислота; 10% раствор йодистого калия;
1% раствор крахмала; 0,01н раствор Na
2
S
2
O
3
.
Лабораторная работа № 6
Реактивы (6.3): 0,5 моль/дм
3
, 1моль/дм
3
, 2 моль/дм
3
, 2,5 моль/дм
3
растворы соляной
кислоты; 30% раствор едкого натрия; 10% раствор желтой кровяной соли; 15% раствор суль-
фата цинка; медный окислительный реактив; 10% раствор йодида калия; 25% раствор
соляной кислоты; 20% раствор роданистого калия или аммония; 0,1 моль/дм
3
раствор тио-
сульфата натрия.
Раствор А: 25 г CuSO
4
⋅5H
2
O растворяют в 100 см
3
дистиллированной воды.
Раствор Б: 144 г Na
2
CO
3
безводного растворяют в 300-400 см
3
воды при температуре
50
0
С.
Раствор В: 50 г лимонной кислоты растворяют в 50 см
3
воды.
Соединяют растворы А и Б и перемешивают до образования диоксида углерода. К
полученной смеси добавляют раствор В и оставляют смесь для охлаждения до комнатной
температуры. Затем объем доводят дистиллированной водой до 1 дм
3
и через сутки фильт-
руют. После 50-кратного разбавления дистиллированной водой рН раствора должен состав-
лять 10±0,1.
Лабораторная работа № 7
Раствор 1.
Отвешивают 100 мг бензойной кислоты, переносят в мерную колбу на 25
см
3
и доводят до метки этилацетатом (концентрация полученного раствора 4 мг/ см
3
).
Раствор 2.
Отвешивают 40 мг сорбиновой кислоты, переносят в мерную колбу на 100
см
3
и доводят до метки этилацетатом (концентрация полученного раствора 0,4 мг/ см
3
).
Раствор 3.
Смешивают равные объемы растворов 1 и 2. Концентрация БК в получен-
ном растворе 2.0 мг/ см
3
, СК - 0,2 мг/ см
3
.
Реактивы (7.3): 15% раствор железистосинеродистого калия; 30% раствор сернокис-
лого цинка; 10% раствор соляной кислоты; хлороформ; 95% этиловый спирт; фенолфталеин;
0,05 моль/дм
3
раствор едкого натрия; 10% раствор едкого натрия.
Лабораторная работа № 8
Реактивы (8.2). 1% раствор алюмокалиевых квасцов; 33% раствор перекиси водоро-
да.
Лабораторная работа № 9
Приготовление рабочей тест-культуры (9.2):
Рабочую тест-культуру готовят из коллекционной. В пробирку с 10 мл стерильного
обезжиренного молока вносят 1 петлю культуры Streptoccocus thermofilus и выдерживают в
термостате при 42÷43
0
С в течение 16÷18 час. Коллекционную тест-культуру хранят при
6÷8
0
С и перевивают через 10÷14 суток. Из этой культуры берут 1 петлю в пробирку с 10 мл
стерильного обезжиренного молока и выдерживают в термостате 16÷18 час. при 42÷43
0
С.
Для проведения анализа используют 1-2- суточную культуру при условии хранения ее в хо-
лодильнике при 6÷8
0
С.
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
1. Скурихин И.М., Нечаев А.П. "Все о пище с точки зрения химика" - М.: Высшая
школа, 1991г.
2. Голубев В.Н. Основы пищевой химии. Курс лекций для студентов высших учеб-
ных заведений. /М., МГЗИПП, 1997. – 224 с.
3. Нечаев А.П. Пищевая химия: Курс лекций/ МГУПП.- М.: Издательский комплекс
МГУП, 1998.- ч. I и ч. II.
4. Павлоцкая А.Ф., Дуденко Н.М., Эльман М.М. "Физиология питания " - М.: Выс-
шая школа, - 1989 г.
5. "Безвредность пищевых продуктов" под редакцией Говарда Р. Робертса (перевод с
английского) - М.: –Агропромиздат, - 1986г.
6. Росивал Д., Эгест Р., Соколай А. "Посторонние вещества и пищевые добавки в
продуктах " - М.: Легкая и пищевая промышленность, 1982 г.
7. Уголев А.М. "Естественные технологии биологических систем" - Л.: Наука, -
1987 г.
8. Чиркина Т.Ф., Хлебников В.И. "Роль пищевых добавок в повышении качества
мясных консервов" – М. – 1986 г.(Обзор. инф. ЦНИИТЭИ мясомолпром сер. мясн. промыш-
ленность)
9. Денис В., Парк Н. "Биохимия чужеродных соединений" - М.: Медицина, - 1973 г.
10. Методы определения микроколичеств пестицидов в продуктах питания, кормах,
внешней среде. Справочное издание./Под редакцией М.А.Клисенко. - М.: Колос, - 1983 г.
11. Крутошикова А., Угер М. "Подслащивающие вещества в пищевой промышленно-
сти " - М.: "Агропромиздат", - 1988 г.
12. Эмануэль Н.М., Зайков Г.Е. "Химия и пища " - М.: Наука, - 1986 г.
13. Чиркина Т.Ф., Чебунина Е.И., Думнова Т.Г. "Методические указания по опреде-
лению биологической ценности белков расчетным методом КЭБ" - Улан-Удэ, - 1987 г.
14. Эйхлер В. "Яды в нашей пище" (перевод с немецкого – М.: Мир, 1993 г.
15. Булдаков А.С. "Пищевые добавки" Справочник- Санкт-Петербург."Иt", 1996. –
240 с.
16. Люк Э., Ягер М. Консерванты в пищевой промышленности: Свойства и примене-
ние. 1998.–256 с.
17. Донченко Л.В., Надыкта В.Д. Безопасность пищевого сырья и продуктов питания.
– М.:Пищепромиздат, 1999.–352 с.
