Задачи 42-ой Международной Химической олимпиады по химии
Подождите немного. Документ загружается.

42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 20
b) Если такую же процедуру провести в присутствии сульфида серебра, образу-
ется сплав серебра и свинца. Запишите
уравнения химических реакций между
сульфидом серебра и теми промежуточными соединениями, которые вы пред-
ложили в пункте (a). В общем случае сплав нельзя описать стехиометрическим
составом, но для ответа используйте формулу AgPb
2
.
c) Напишите уравнение реакции, протекающей со свинцом на воздухе при 800 ºC.
d) Укажите причину, по которой соединение свинца отделяется от сплава. Выбе-
рите один из предложенных вариантов ответа.
A: Соединение свинца реагирует с керамической поверхностью.
B: Соединение свинца смачивает поверхность и впитывается в керамику благо-
даря капиллярным силам.
C: Соединение свинца испаряется.
D: Соединение свинца отделяется от сплава из-за своей низкой плотности.
E: Соединение свинца отделяется от сплава из-за своей высокой плотности.
e) Что произойдет, если руда будет содержать золото? Выберите
один из пред-
ложенных вариантов ответа.
A: Серебро окисляется при осаждении золота.
B: Золото осаждается на дне под сплавом и может быть отделено от серебра.
C: Золото покрывает поверхность сплава и может быть отделено от серебра.
D: Золото осаждается внутри сплава и может быть отделено от серебра.
E: Золото образует однородный сплав с серебром и не может быть отделено от
него.
Задача 17: Комплексы кобальта(II)
Хлорид кобальта (II) широко используют как индикатор влажности силикагелей. В
сухом силикагеле индикатор синий, во влажном – красный. Чистый безводный хло-
рид кобальта имеет синий цвет, а его шестиводный гидрат окрашен в красный цвет.
Водные растворы обоих соединений – красные, тогда как спиртовой раствор без-
водной соли имеет синюю окраску. При добавлении воды спиртовой раствор стано-
вится красным.
42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 21
a) Определите координационное число кобальта и координационную структуру
комплекса в спиртовом растворе безводного хлорида кобальта (II).
b) Синий цвет раствора сохраняется, если количество добавленной воды в два
раза превышает количество безводной соли. Напишите формулу комплекса
кобальта в полученном растворе.
c) Напишите
уравнение реакции, протекающей при добавлении избытка воды к
спиртовому раствору.
d) Определите
координационное число кобальта и координационную структуру
комплекса в водном растворе.
e) При добавлении некоторого количества воды к спиртовому раствору последний
становится фиолетовым. Объясните, почему изменяется цвет, если к фиоле-
товому раствору добавить небольшое количество концентрированной соляной
кислоты.
f) Объясните, почему изменится цвет при понижении температуры фиолетового
раствора.
g) Запишите
формулу комплекса в гексагидрате хлорида кобальта (II).
Задача 18: Окислительно-восстановительное титрование
Содержание хрома в образце нержавеющей стали (сплава Fe-Cr) анализировали по
следующей методике.
i) 0.1000 г образца растворили в 20 мл горячей серной кислоты (1.8 М).
ii) К раствору добавили 4 мл концентрированной азотной кислоты и нагревали
его в течение 10 мин, пока цвет раствора не изменился с голубого на зеленый.
iii) К раствору добавили одновременно 10 мл 0.5% водного раствора нитрата
серебра и 6 г персульфата аммония (NH
4
)
2
S
2
O
8
. Раствор нагревали в течение 20
мин до полного разложения персульфата аммония и образования оранжевого рас-
твора.
iv) Добавили 10 мл 5% водного раствора NaCl.
42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 22
v) С помощью бюретки прилили 20 мл 1.00x10
–1
М раствора соли Мора
(FeSO
4
·(NH
4
)
2
SO
4
).
vi) Раствор титруют 2.00x10
–2
М раствором перманганата калия (KMnO
4
). Ко-
нечная точка определяется по переходу цвета раствора в светло-красный.
Ответьте на вопросы a) - f), считая атомную массу хрома равной 52.00.
a) Опишите процесс, происходящий в п. ii).
b) После процесса ii) в растворе содержится трехвалентный хром. В каком виде
хром будет в растворе после процесса iii)?
c) Напишите
уравнение реакции, происходящей в п. iv). Укажите цель этого этапа.
d) Напишите ионное уравнение реакции, происходящей между ионами тяжелых
металлов в п. v). Каков будет цвет раствора после этой реакции?
e) Напишите уравнение реакции в п. vi).
f) Объем титранта в п. vi) составил 12.00 мл. Определите содержание хрома в
исходном образце.
Задача 19: Производство и кристаллическая структура
железа
Общий способ получения железа из руды – восстановление углеродом. Основной
процесс происходит в доменной печи и конвертере. Железную руду, флюс (CaO) и
кокс загружают в печь сверху, а снизу подают горячий воздух. В результате восста-
новления руды при нагревании образуется расплавленный чугун. Из него в конвер-
тере получают расплавленную сталь, удаляя углерод и примеси путем их окисления.
Ответьте на приведенные ниже вопросы, считая, что содержание углерода в чугуне
составляет 4.50 мас.%, кокс содержит 90.0 мас.% C, 7 мас.% SiO
2
, 3 мас.% Al
2
O
3
.
Атомные массы C, O, Ca и Fe равны, соответственно 12.0, 16.0, 40.1 и 55.8. Плот-
ность железа при комнатной температуре 7.90 г/см
–3
.
a) Основной компонент железной руды – Fe
2
O
3
– восстанавливается до Fe и CO
2
(i) оксидом углерода CO, который образуется в реакции между коксом и горячим
воздухом, (ii) углеродом в составе кокса. Напишите
уравнения всех перечис-
ленных реакций.
42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 23
b) Железная руда также содержит примеси – 7 мас.%SiO
2
и 3 мас.%Al
2
O
3
, ос-
тальное – Fe
2
O
3
. Они реагируют с примесями в коксе и с флюсом CaO, образуя
оксидный плав, который превращается в шлак. Сколько
килограммов шлака
образуется при получении 1 кг чугуна? Считайте, что масса CaO равна массе
SiO
2
.
c) В конвертерном процессе углерод удаляют, продувая O
2
через расплавленный
чугун. Считая, что образуются равные количества CO и CO
2
, рассчитайте, какой
объем O
2
(в литрах) потребуется для полного окисления углерода в 1.00 кг чу-
гуна при 27
o
C и 2.026×10
5
Па?
d) Сколько
килограммов CO
2
выделяется при получении 1.00 кг железа в доменной
печи и в конвертере с помощью процесса (i) в вопросе a)? Считайте, что CO,
выходящий из конвертера, окисляется до CO
2
. В расчете учтите также CO
2
, об-
разующийся при получении CaO из CaCO
3
.
e) Железо имеет объемноцентрированную кубическую решетку. Рассчитайте
ра-
диус атома железа при комнатной температуре.
Задача 20: Энергия Гиббса реакций окисления
a) Заполните
пропуски в предложениях словами или химическими формулами.
Уравнение реакции окисления металла M одним молем кислорода с образованием
оксида M
m
O
n
(m, n – целые) можно записать в виде ( ). Изменение стан-
дартной энергии Гиббса при абсолютной температуре T в этой реакции, ΔG
o
, можно
выразить следующим образом ( ) через изменение стандартной
( ), ΔH
o
, и изменение стандартной ( ), ΔS
o
. С другой стороны, если
чистый металл M и чистый оксид M
m
O
n
находятся в равновесии при температуре T,
парциальное давление кислорода p
O2
можно выразить через ΔG
o
и газовую посто-
янную R следующим образом: ( ). Диаграмму, на которой значения ΔG
o
различных реакций окисления изображены как функции абсолютной температуры,
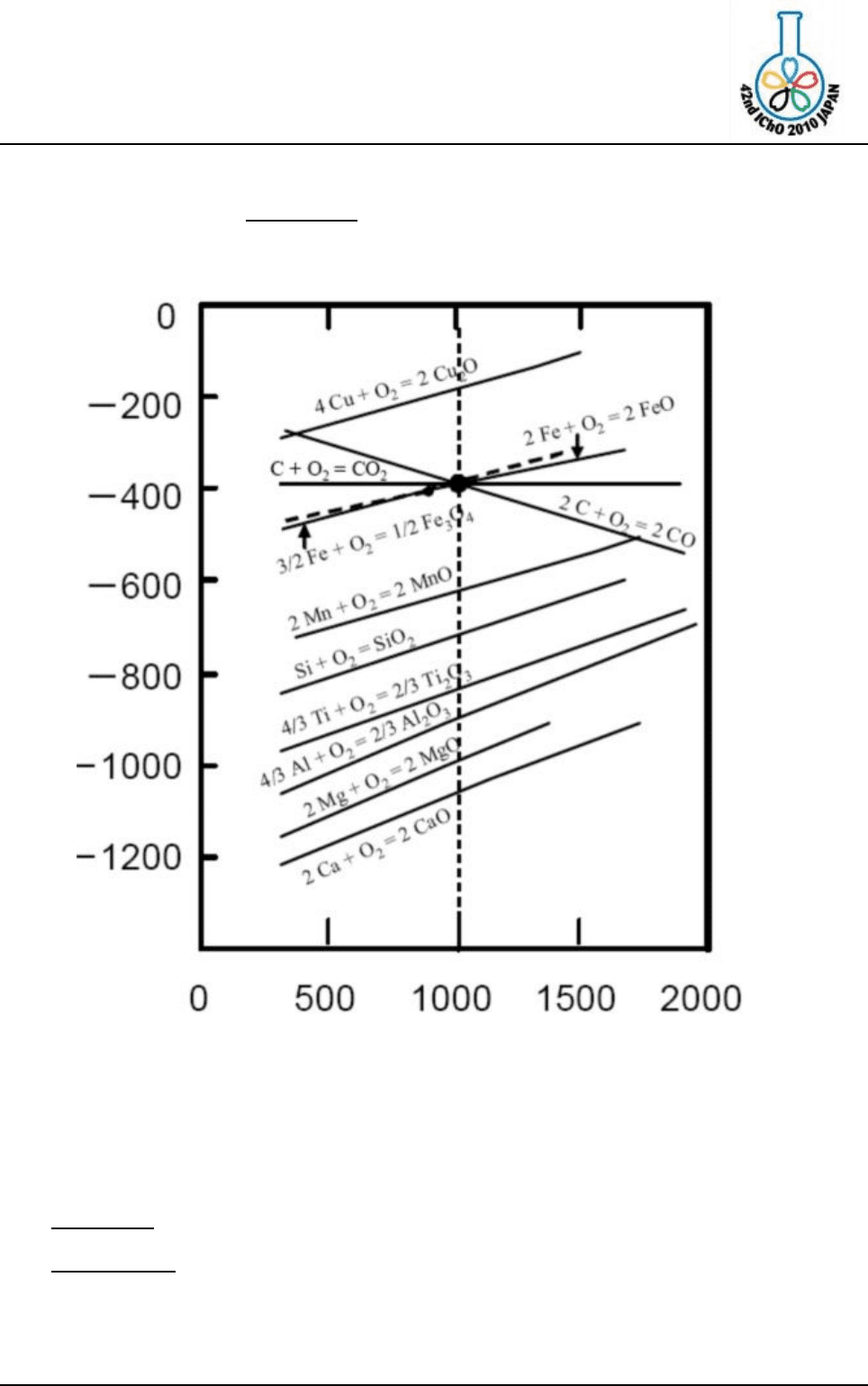
называют “диаграммой Эллингема” (рис. 1). Как видно из рисунка, большинство
функций изображены прямыми линиями, а металлы в нижней части рисунка легче
( ), чем металлы в верхней части.
b) Когда и реагенты, и продукты находятся в конденсированном состоянии (жидком
или твердом), прямые на рис. 1 имеют почти одинаковый наклон. Прямая почти
горизонтальна в случае газообразного CO
2
и имеет противоположный по знаку,
42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 24
но одинаковый по абсолютной величине с остальными реакциями наклон для
газообразного CO. Объясните, почему.
Температура (К)
Рис. 1. Зависимость энергии Гиббса реакций окисления от температуры
(Диаграмма Эллингема)
c) Напишите
уравнение реакции восстановления Cu
2
O с помощью Al.
d) Определите теплоту реакции в п. c) в расчете на один моль Al.
Энергия Гиббса реакций окисления, кДж / моль O
2

42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 25
e) Укажите на рис. 1 точки, через которые проходят любые линии постоянного
парциального давления кислорода p
O2
, и точки, через которые проходят линии
постоянного отношения парциальных давлений p
CO
/p
CO2
.
f) Какая доля (%) CO вступит в реакцию при восстановлении им твердого FeO до
Fe при 1000 K в равновесных условиях?
Задача 21: Количественный анализ состава вулканических
газов
Ответьте на вопросы a) – c) о составе фумарольных газов.
В шприц поместили 20 мл 5 М раствора NaOH и вытеснили из него воздух. В фума-
ролу вставили титановую трубку и дождались, пока она заполнится горячими газами.
Трубку соединили со шприцом резиновым переходником и шприц медленно запол-
нили фумарольными газами, охлаждая его мокрой тряпкой. После сбора газов шприц
привели к нормальным условиям (0 °C, 101.3 кПа), при этом объемы газовой и жид-
кой фаз оказались равны 50.0 мл и 38.0 мл, соответственно.
Из 38.0 мл раствора в шприце отобрали аликвоту 10 мл, и все серосодержащие со-
единения окислили до сульфат-иона. К раствору добавили разбавленную HCl до
слабокислотной среды и прилили 20 мл 10%-ного раствора BaCl
2
. Образовавшийся
осадок высушили и взвесили, его масса составила 0.30 г.
a) Рассчитайте
объемную долю (в %) водяных паров в фумарольных газах, считая,
что объем раствора NaOH изменяется только при поглощении паров воды.
Плотность раствора NaOH в условиях анализа не менялась и составляла 1.0
г/мл.
b) Рассчитайте
количество серы (в моль) в фумарольных газах в шприце. Опре-
делите общий объем (в мл) H
2
S и SO
2
в пересчете на нормальные условия.
Ответ дайте с двумя значащими цифрами.
c) Для оценки молярного отношения H
2
S к SO
2
используют различие в их реакци-
онной способности в газовой фазе. Фумарольный газ пропустили через 30 мл
0.03 М раствора KIO
3
-KI и 3 мл 4 M раствора HCl. Напишите уравнения химиче-
ских реакций, происходящих с H
2
S и SO
2
.
42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 26
Задача 22: Колебательные и вращательные спектры
вулканических газов
Состав фумарольных газов можно определять не только химическим анализом, но и
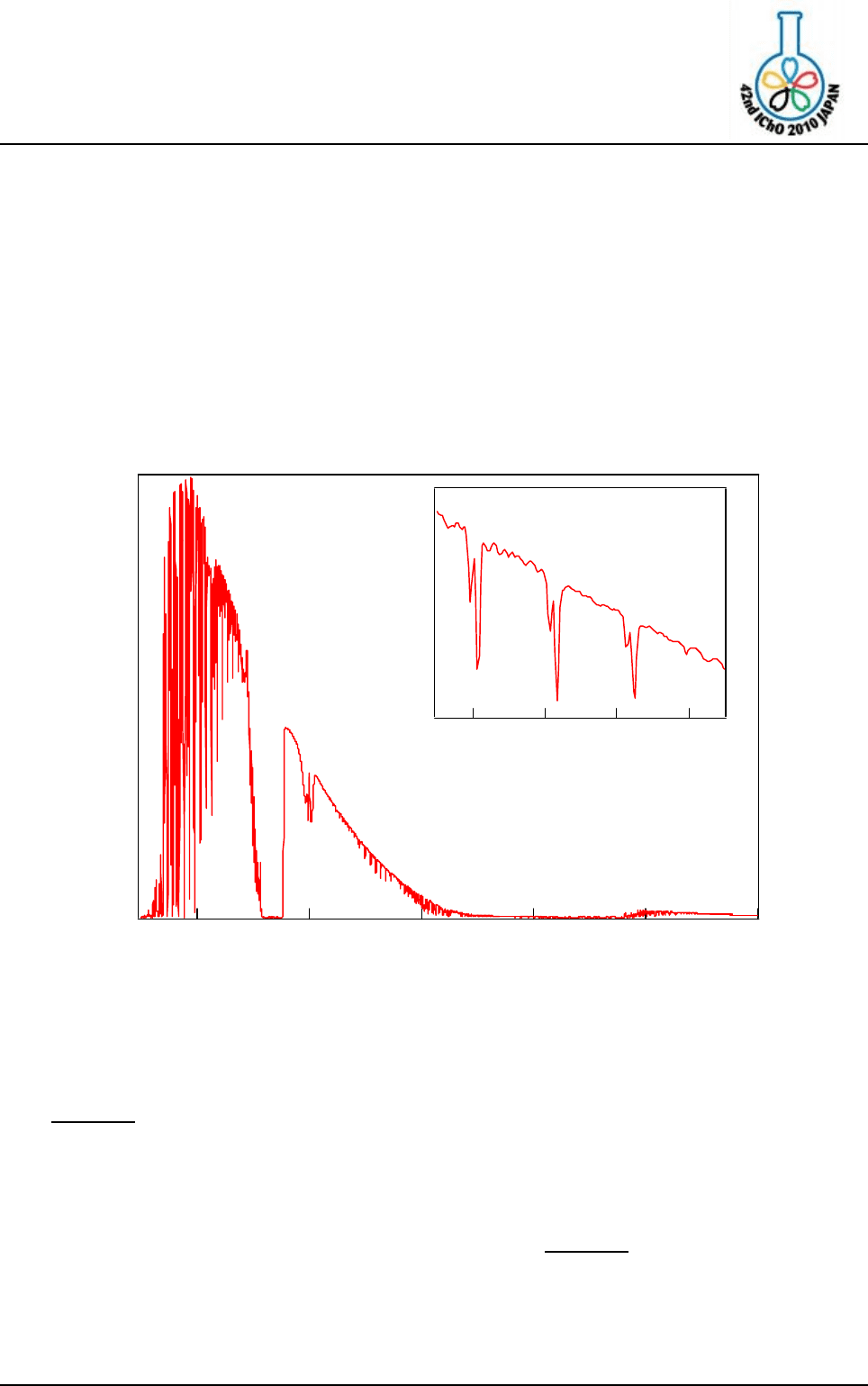
с помощью спектроскопических методов. На рисунке приведен ИК спектр поглощения
(колебательно-вращательный спектр) фумарольного газа. Вещества X и Y на рисунке
– галогеноводороды, Y растворяет силикаты.
Transmittance
2880286028402820
Wavenumber (cm
-1
)
Transmittance
450040003500300025002000
Wavenumber (cm
-1
)
a) Укажите формулы веществ X и Y.
b) Как видно на вставке, полосы поглощения вещества X расщеплены. Это рас-
щепление связано с изотопным составом галогена в “X”. У этого галогена два
природных изотопа, соотношение которых 3 :1. Укажите
эти изотопы в порядке
уменьшения распространенности.
Рис.
ИК спектр поглощения фумарольного газа, полученный дистанционно, с
помощью ИК Фурье-спектрометра.
X
X
Y
Пропускание
Пропускание
Волновое число (см
-1
)
Волновое число (см
-1
)

42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 27
Задача 23: Введение в химию макромолекул
Концепция макромолекул (полимеров), представленная в 1925 году лауреатом Но-
белевской премии по химии Штаудингером, открыла мир новых полимерных мате-
риалов, которые широко используются как пластики, волокна, каучуки и т.д. Поли-
меры можно разделить на две большие группы: виниловые и не-виниловые полиме-
ров. Первые обычно получают из соответствующих виниловых мономеров
(-олефинов) методами цепной полимеризации в присутствии подходящих инициа-
торов или катализаторов. В отличие от них, не-виниловые мономеры синтезируются
поликонденсацией (ступенчатой полимеризацией) из мономеров или смеси моно-
меров, несущих две функциональные группы, способные вступать в реакции кон-
денсации. Примерами могут служить H
2
N-R-COOH (при конденсации образуются
полиамиды), HO-R-COOH (сложные полиэфиры), H
2
N-R-NH
2
+ HOOC-R’-COOH (по-
лиамиды), HO-R-OH + HOOC-R’-COOH (сложные полиэфиры) и т.д. Очевидно, что
стехиометрия (соотношение компонентов) в случаях поликонденсации смеси моно-
меров (сополиконденсации) является одним из ключевых факторов, определяющих
молекулярную массу образующегося продукта.
Если элементарные стадии ступенчатой полимеризации обратимы, как, например,
реакция этерификации, то для получения высокомолекулярного продукта важно
смещать равновесие реакции вправо. В задаче обсуждается взаимосвязь равновес-
ного состояния элементарных стадий поликонденсации и длины цепи полимера, по-
лученного из стехиометрической смеси бифункциональных мономеров. Реакция
этерификации (1) – типичный пример реакции со сравнительно низкой константой
равновесия (K = 4.20 при 78
o
C – температуре кипения этанола).
K
¾ ¾®
3 25 3 252
CH COOH + C H OH CH COOC H + H O
(1)
a) Рассчитайте массу этилацетата в равновесной смеси, образующейся по урав-
нению (1) из смеси, содержащей по 1.00 моль спирта и кислоты.

42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 28
Если вместо монофункциональных молекул использовать дикарбоновую кислоту и
диол, то по реакции, аналогичной (1), можно получить линейные сложные полиэфи-
ры.
Хотя процесс поликонденсации происходит через многочисленные равновесные
стадии, его часто упрощенно представляют в виде уравнения (2), предполагая, что
константы равновесия на каждой стадии одинаковы.
n HOOC-R
1
-COOH + n HO-R
2
-OH ® HO-[COR
1
CO-OR
2
O]
n
-H + (2n-1)H
2
O (2)
Длина полимерной цепи – очень важная характеристика полимеров. Из механически
прочных длинноцепных полимеров можно изготавливать ткани и тонкие пленки. На-
оборот, короткоцепные молекулы используются в качестве адгезивов, детергентов,
для изготовления различных покрытий. Длину цепи полимера нам будет удобнее
выражать через степень полимеризации (X)
*1)
, чем через молекулярную массу,
которая зависит от структур R
1
и R
2
исходных молекул. Например, в уравнении (2) X =
1 для дикарбоновой кислоты и диола, и X = 2n для полиэфира (отметим, что струк-
тура повторяющегося звена полимера уже представляет собой «димер»)
*2)
. Так как
полимер состоит из смеси молекул различной длины, его степень полимеризации –
усредненная величина
*1)
. Группы HO- и –H, в структуре полиэфира называют кон-
цевыми группами, а структура в скобках -COR
1
CO-OR
2
O- есть повторяющееся звено,
в данном случае представляющее собой «димер» спирта и кислоты. Поэтому моле-
кулярная масса мономерного звена, M
u
, в случае (2) может быть представлена как
M
u
= «молекулярная масса повторяющегося звена) / 2 (3)
Если M
*3)
– средняя молекулярная масса полимера, то X, M и M
u
связаны следующим
соотношением:
X = (M – «молек. масса концевых групп») / M
u
(4)
Как легко понять из вычислений при ответе на вопрос a), если константа равновесия
использованной реакции сравнительно мала, значительные количества исходных
42-ая Международная химическая олимпиада 2010, Япония
Химия: ключ к нашему будущему
Подготовительные задачи 29
веществ в состоянии равновесия остаются непрореагировавшими. Количество об-
разовавшегося продукта можно определить, рассматривая расход функциональных
групп. Определим “глубину (степень) протекания реакции“, p, как;
p = [число прореагировавших функциональных групп] / [исходное число
функциональных групп] (5)
Например, по уравнению (1), после достижения глубины превращения p = 0.80 из
1.00 моль исходных бифункциональных компонентов, образуется 0.80 моль сложного
эфира.
В органическом синтезе величину p × 100 называют выходом реакции (%). Если вы-
ход реакции p = 0.80, обычно это считается хорошим. Однако, в случае синтеза по-
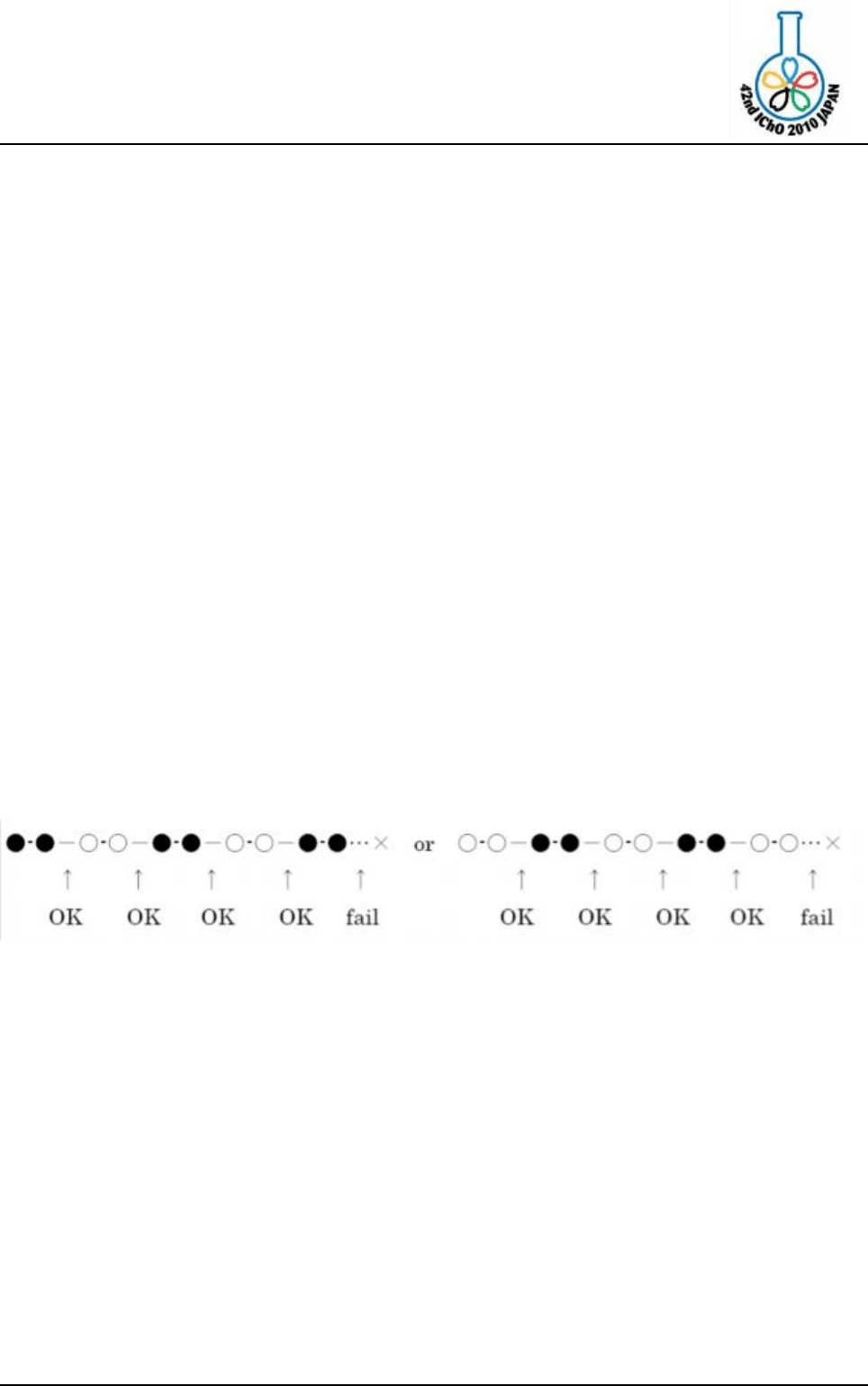
лимера методом поликонденсации значение p = 0.80 недостаточно велико. Как
представлено ниже, p = 0.80 означает успешное прохождение 4 последовательных
реакций конденсации (●-● и ○-○ обозначают соответственно дикарбоновую кислоту и
диол). В этом случае X равняется 5.0.
Соответственно, для получения высокомолекулярного продукта глубина протекания
реакции должна быть как можно ближе к единице, p ® 1. Американский исследова-
тель Карозерс вывел соотношение (6), связывающее среднюю степень полимериза-
ции продукта и глубину протекания реакции поликонденсации:
X = 1 / (1 – p) (уравнение Карозерса) (6)
Хотя приготовить полимеры винилового ряда, например, полистирол, с молекулярной
массой M ≥ 10
6
(что соответствует X ≥ 10
4
) методом цепной полимеризации олефи-
новых мономеров легко может даже начинающий экспериментатор, получаемые в
